-
Medical journals
- Career
Komplexní léčba difuzních nízkostupňových gliomů – technika operování a onkologická léčba rezidua
Authors: R. Bartoš 1,2; M. Sameš 1; A. Malucelli 1; A. Hejčl 1; D. Ospalík 3; F. Třebický 4; V. Němcová 2
Authors‘ workplace: Neurochirurgická klinika Univerzity J. E. Purkyně, Masarykova nemocnice v Ústí nad Labem 1; Anatomický ústav, 1. LF UK, Praha 2; Neurologické oddělení, Masarykova nemocnice v Ústí nad Labem 3; Ústav radiační onkologie, Nemocnice Na Bulovce, Praha 4
Published in: Cesk Slov Neurol N 2021; 84/117(1): 72-78
Category: Original Paper
doi: https://doi.org/10.48095/cccsnn202172Overview
Cíl: Cílem naší práce bylo zpětné vyhodnocení možné a skutečně dosažené radikality resekcí nízkostupňových gliomů (low-grade glioma; LGG). Dále jsme hodnotili chování definovaných reziduálních tumorů po následující onkologické léčbě u parciálních a subtotálních resekcí.
Soubor a metodika: Hodnocení souboru našich 37 pacientů operovaných v letech 2010–2019 na Neurochirurgické klinice Masarykovy nemocnice v Ústí nad Labem. Anatomické elokventní hranice byly definovány striktně primárním motorickým a zrakovým kortexem (g. precentralis a gyri přilehlé k sulcus calcarinus), vč. jejich drah, dále p. triangularis a p. opercularis dolního frontálního gyru jako expresivní řečové oblasti a strukturami centrálního jádra (central core). Nikoli absolutní elokventní oblastí byl perisylvijský kortex dominantní hemisféry. Parciální resekci jsme definovali jako přítomnost lemu tumoru > 1 cm hodnoceného v T2 vážené MR za 2–4 měsíce po operaci. Subtotální resekce byla definována identicky jako lem reziduálního tumoru ≤ 1 cm.
Výsledky: Pro potenciálně možnou radikální (ANO) resekci jsme vyhodnotili v našem souboru celkem 25 pacientů (68 %), a to: 1) 6 pacientů (16 %) s bezpečným odstupem k elokventní oblasti (ANO Safe) – zde jsme dosáhli ve všech případech radikální resekce; 2) 19 pacientů (51 %) vyžadujících dosažení hranice k elokventní oblasti (ANO Risk) – v této skupině jsme dosáhli radikální/subtotální/parciální resekce u 7/6/6 pacientů. Jako nutně parciálně operabilní (NE) jsme vyhodnotili 12 pacientů (32 %), u všech těchto pacientů byla operace skutečně parciální. Reziduum pozitivně reagovalo na onkologickou léčbu v 90 % případů, přičemž nejkratší doba sledování byla 13 měsíců. Vážná komplikace chirurgického výkonu nastala u jedné pacientky (2,7 %). Další komplikace (5,4 %) byly mírné, v jednom případě hemianopsie a v druhém léze suplementární motorické oblasti.
Závěr: Definice anatomických hranic LGG a pozice elokventních oblastí korespondují s predikcí rozsahu dosažené resekce. Alfou a omegou úspěchu je však respektování mozkových arterií a žil v operačním poli. Pokud se neurochirurg subjektivně během operace pohybuje na hraně bezpečnosti stran elokventního kortexu a jeho drah a ponechá malé reziduum, je radiochemoterapie po operaci indikována a je účinná.
Klíčová slova:
nízkostupňový difuzní gliom – operace – radioterapie – anatomie
Úvod
V návaznosti na recentní souhrnné práce domácí literatury o managementu nízkostupňových gliomů (low-grade glioma; LGG) [1,2] bychom toto zajímavé téma rádi doplnili naším pohledem na technickou stránku operace a předoperační úvahu. Vycházíme z našeho 10letého souboru pacientů s difuzním LGG operovaných mezi lety 2010 a 2019 se snahou o maximální možnou resekci. Navazujeme na náš předchozí soubor z let 2002–2009 [3]. Hlavním přínosem práce je dle našeho názoru zpětné vyhodnocení potenciální operability zhodnocením T2 vážených obrazů a sekvencí FLAIR (fluid attenuated inversion recovery) MR s ohledem na jasně definované elokventní anatomické struktury a také vyhodnocení dynamiky grafického nálezu po onkologické léčbě.
Materiál a metodika
Soubor čítá 37 pacientů (22 mužů) s histologicky verifikovaným hemisferálním LGG, který byl primárně operován se snahou o maximální resekci. Vyloučili jsme jednoho pacienta s cystickým hemisferálním LGG a čtyři pacienty po biopsii, u kterých nebyl resekční výkon ani zvažován. Průměrný věk pacientů v době operace byl 43 (20–69) let. Celkem 8 LGG bylo lokalizováno v insule, 19 frontálně či parietálně, 5 temporálně nebo mediotemporálně, 1 paraspleniálně a 4 jsme rozsahem nazvali komplexními, tzn. insulární, ale přesahující Yaşargilův typ 5B, zejména směrem do cingula a bazálních ganglií. Celkem 26 operací bylo provedeno za použití nějaké formy mapování nebo monitorace neurologických funkcí (4× awake, 5× elektrická stimulace, 3× elektrická stimulace v kombinaci s motorickými evokovanými potenciály [MEP] a 14 operací za monitorace MEP, 11 operací bylo provedeno bez mapování/monitorace funkcí [30 %]). Celkem 28 pacientů bylo histologicky hodnoceno jako LGG WHO (World Health Organization) II, 9 pacientů bylo hodnoceno jako WHO II–III, což bylo dáno např. vyšším proliferačním indexem Ki67 nebo přítomností gemistocytární komponenty. Mutační status IDH1 a přítomnost oligodendrogliální složky jsou uvedeny v souhrnné tab. 1.
Table 1. Charakteristika souboru 37 pacientů s nízkostupňovými gliomy. 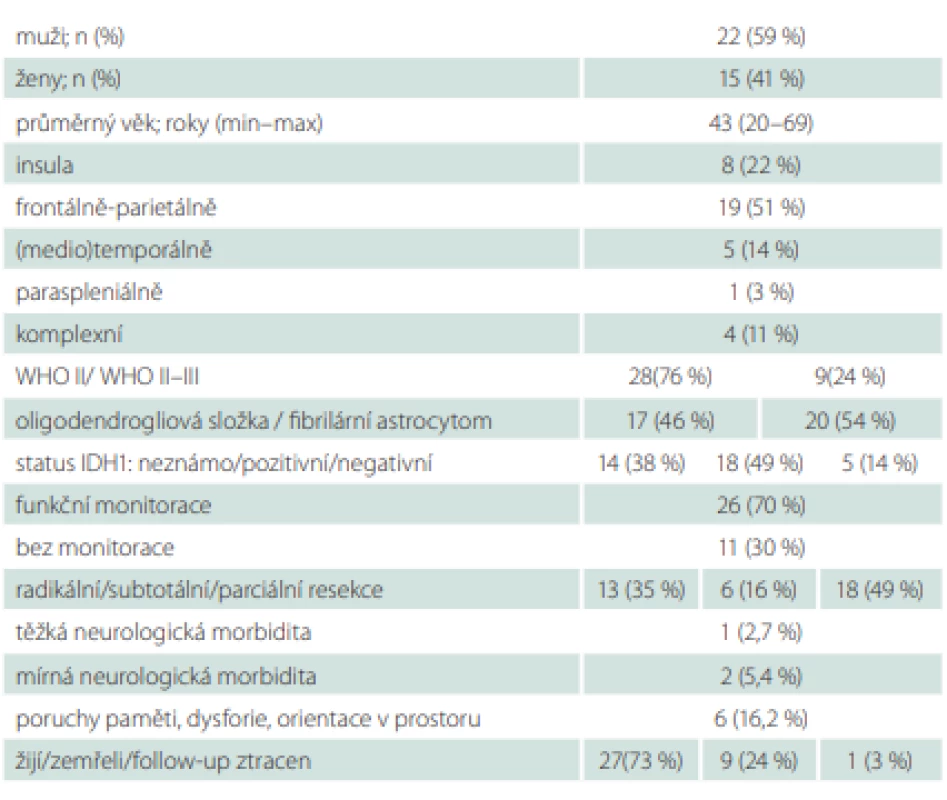
WHO – Světová zdravotnická organizace V rámci retrospektivního hodnocení operability společně zařadili vždy dva neurochirurgové, kteří však pacienta neoperovali, podle T2 vážených obrazů a sekvencí FLAIR daného pacienta do jedné ze skupin:
- radikálně inoperabilní (NE);
- radikálně operabilní, avšak hranice nádoru dosahují k elokventním anatomickým strukturám (ANO Risk);
- radikálně operabilní s bezpečným lemem k elokventním anatomickým strukturám ≥ 1 cm (ANO Safe).
Radikalita operací byla následně vyhodnocena neurochirurgem (první autor) a nezainteresovaným neurologem (studentem doktorského programu „zobrazovací metody v lékařství“) v sekvenci T2 MR. Hodnoceny byly snímky za 2–4 měsíce po operaci, nikoli časná kontrola do 72 h. Za radikální resekci byla považována situace, kdy graficky došlo k dosažení gyrálních hranic nádoru dle anatomických znaků, a dále absence jasné T2 hyperintenzity značící reziduální tumor. Jako subtotální resekce byla hodnocena resekce, kdy šíře lemu rezidua musela být v jeho antero-posteriorním (lokalizace zejména v oblasti motorické), kaudo-kraniálním (lokalizace zejména v oblasti mediotemporální) a latero-mediálním (lokalizace zejména v insule) rozměru ≤ 1 cm. Průměrná šířka lemu u 6 pacientů po subtotální resekci byla 8 mm (5–10 mm). Jako parciální resekce bylo vyhodnoceno částečné odstranění nádoru ve vztahu k naší definici subtotální resekce, tedy lem rezidua byl > 1 cm. Vývoj rezidua byl hodnocen stejnou metodikou na sekvencích T2 a FLAIR, přičemž hodnocen byl rozsah definovaného rezidua v sérii MR s nejvýraznější odpovědí po radiochemoterapii v sekvencích T2 a FLAIR, hodnotili jsme i vznik poléčebných drobných pseudocyst. Onkologická léčba zahrnovala zevní frakcionovanou radioterapii a adjuvantní léčbu temozolomidem (dávka 150–200 mg/m2 p. o. D1–5 à 28 dní, 6 cyklů dle klinické a grafické odpovědi, s event. prodloužením na 10 cyklů).
Výsledky
Skupina pacientů, u kterých jsme konstatovali, že operace nemůže být radikální (NE), čítala 12 pacientů. Zde jsme dosáhli opravdu ve všech případech parciální resekce (100 %), byť v jednom případě mediotemporálního nádoru jsme zprvu i zvažovali nález hodnotit jako subtotální resekci, lem však byl v rozsahu 15 mm kaudo-kraniálně v oblasti bazálních ganglií. Skupina pacientů, u kterých jsme konstatovali, že hranice nádorů se dotýká neresekabilních elokventních oblastí (ANO Risk) byla nejpočetnější, čítala 19 pacientů. Zde jsme dosáhli parciální resekce u 6 pacientů (32 %), u dalších 6 pacientů (32 %) subtotální resekce a u 7 pacientů (37 %) radikální resekce. Skupina pacientů, u kterých jsme konstatovali, že lze dosáhnout bezpečně okrajů nádoru (ANO Safe), byla bohužel nejmenší, čítala 6 pacientů, nicméně zde jsme ve všech případech (100 %) dosáhli radikální resekce (obr. 1). Při 26 mapovaných/monitorovaných operacích u 16 (62 %) z nich neurochirurg funkční oblasti lokalizoval nebo došlo k poklesu MEP, u zbylých 10 operací (38 %) bylo mapování negativní nebo MEP nepoklesly. V této skupině bylo dosaženo subtotální/radikální resekce pouze ve 40 % (4/10) a naopak ve skupině, kde byly „hranice funkčně definovány“, v 69 % (11/16).
Image 1. Dosažená radikalita vzhledem k anatomickému předpokladu v počtech pacientů.
Fig. 1. Achieved radical measures towards the anatomical assumption in a number of patients.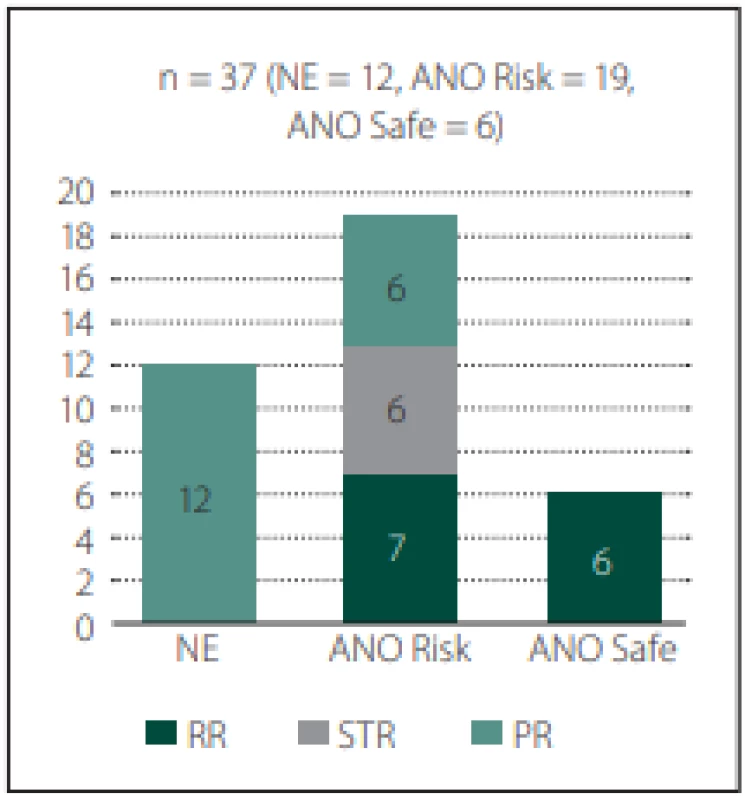
ANO Risk – radikálně operabilní, avšak hranice nádoru dosahují k elokventním anatomickým strukturám; ANO Safe – radikálně operabilní s bezpečným lemem k elokventním anatomickým strukturám ≥ 1 cm; n – počet; NE – radikálně inoperabilní; PR – parciální resekce; RR – radikální resekce; STR – subtotální resekce
ANO Risk – radically operable, however, the border of the tumor reaches eloquent anatomical structures; ANO Safe – radically operable with a safe distance towards eloquent anatomical structures ≥ 1 cm; n – number; NE – radically inoperable; PR – partial resection; RR – radical resection; STR – subtotal resectionMěli jsme jednu vážnou komplikaci u 60leté pacientky s progredujícím komplexním gliomem zahrnujícím mediotemporální a temporální kortex a insulu vč. bazálních ganglií. Po temporální a mediotemporální resekci bez alterace MEP došlo k prokrvácení rezidua, což rezultovalo v hemiplegii a časné úmrtí pacientky na přidružené infekční komplikace. Těžká morbidita souboru byla tedy 2,7 %. Další pacientka měla hemianopsii po zadním interhemisférickém přístupu, danou zřejmě retrakcí hemisféry, reagovali jsme na ni prováděním disekce parietookcipitálního sulku v podobných případech. Jedné pacientce jsme způsobili poměrně těžkou lézi suplementární motorické oblasti, která se za 2 měsíce majoritně upravila, avšak přetrvává u ní porucha jemné motoriky a paměti. Obě pacientky však byly soběstačné (skóre modifikované Rankinovy škály bylo 2). Mírná morbidita byla 5,4 %. Dalších 6 pacientů (16,2 %) si aktivně během ambulantních kontrol stěžovalo na poruchy paměti, změny nálady či poruchu orientace v prostoru. K 13. 1. 2021 žije 27 pacientů (73 %), zemřelo 9 pacientů (24 %) a u jednoho pacienta se podařilo dohledat follow-up pouze 4,5 roku, tzn. do roku 2019. Osm z devíti pacientů, kteří již zemřeli (pacientka se závažnou komplikací nezahrnuta), mělo celkovou dobu přežití v průměru 3,3 roku. Z 22 pacientů, u kterých můžeme sledovat > 5leté přežití, jich žije 15 (68 %), všichni z 10 pacientů, kteří byli operováni v posledních 3 letech souboru (tedy od roku 2017 vč.) žijí.
Dále jsme hodnotili vývoj rezidua po onkologické léčbě. U 24 pacientů po parciální nebo subtotální resekci, u kterých byla po operaci aplikována radiochemoterapie (20/24), došlo k alespoň dočasné regresi reziduálního tumoru u 18 pacientů (90 %). U jednoho pacienta jsme pozorovali stacionární reziduum po subtotální resekci, které po 3,5 letech bohužel ztransformovalo do vysokostupňového gliomu (high-grade glioma; HGG), u další pacientky po parciální resekci LGG po ozáření protony (na vlastní žádost pacientky) došlo k rozvoji symptomatické radionekrózy mimo reziduum nádoru (obr. 2).
Image 2. Komplikace protonové radioterapie u 60leté pacientky po parciální resekci fibrilárního astrocytomu středního frontálního gyru v roce 2017 (ANO Risk), pacientka nebyla náladou zcela komponovaná k awake resekci, operace byla prováděna v celkové anestezii, poté pacientka sama konzultovala ozáření v Protonovém centru.
Fig. 2. Complication of proton therapy in a 60-year old female patient after partial resection of the middle frontal gyrus fi brillary aytrocytoma in 2017 (ANO Risk); initially the patient was not in agreement for undergoing non-anesthetic surgery, so the surgery was done under general anaesthesia; afterwards, the patient consulted the Proton Therapy Center about radiotherapy on her own.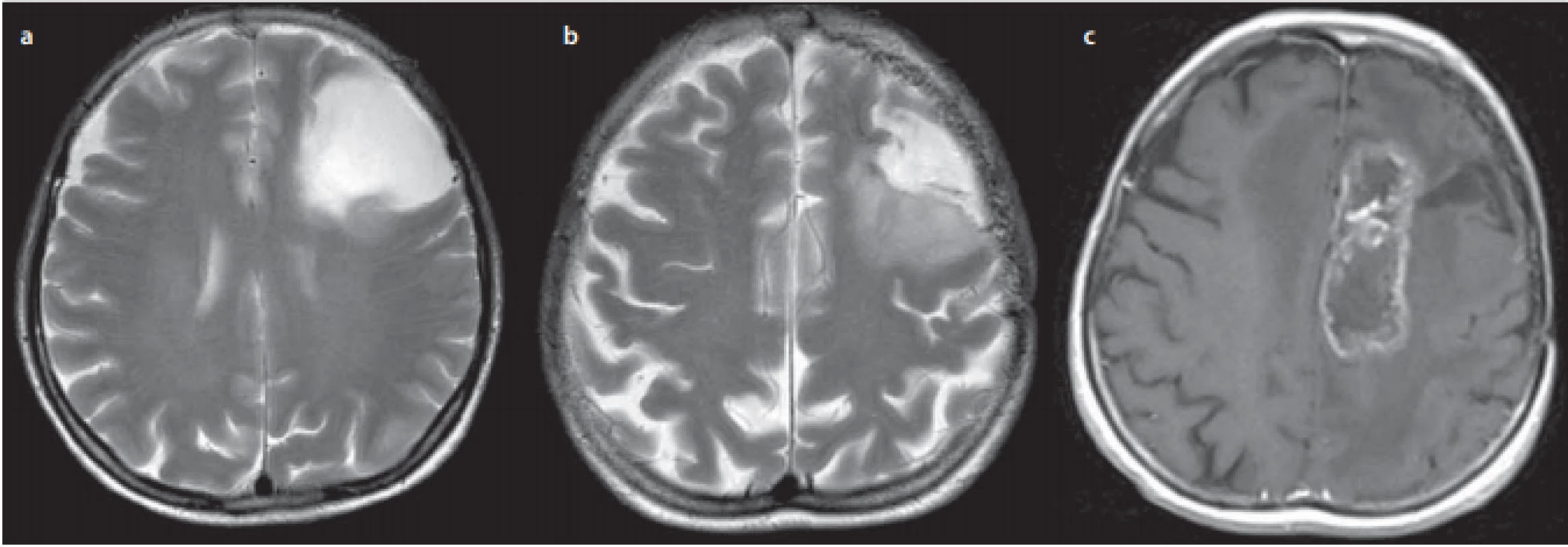
(a) sken T2 MR před operací;
(b) sken T2 MR 4 měsíce po operaci, pacientka bez neurologického deficitu;
(c) sken T1 MR s kontrastní látkou 18 měsíců po dokončení ozáření protony (54 Gy) – radionekróza verifi kována FDG PET, nyní na kortikoterapii, komunikuje s fatickou poruchou, na vozíku pro hemiparézu. FDG – fludeoxyglukóza
(a) T2WI MRI scan before surgery;
(b) T2WI MRI scan 4 months after surgery; patient without neurological deficit;
(c) T1WI MRI scan with contrast matter 18 months after completion of proton radiotherapy (54 Gy) – radionecrosis was confi rmed by FDG
PET; patient is nowadays on corticotherapy, communicates with a phatic disorder, and is wheelchaired due to hemiparesis.
FDG – fluorodeoxyglucoseDiskuze
Dlouhodobě existují dvě základní školy operování intrinsických mozkových lézí: jedna ctí disekci arachnoidálních hranic – tu zastupují např. „otec mikroneurochirurgie“ Yaşargil et al [4,5] nebo Türe et al [6,7] – a na druhé straně existují zastánci transkortikálního přístupu, např. Duffau et al [8] a další [9–11]. Tato situace připomíná známou „bitvu proudů“ Thomase Alvy Edisona a Nikoly Tesly. Edison údajně řekl o Teslově střídavém proudu: „Stejnosměrný proud je jako klidná řeka, která plyne do moře. Naopak střídavý proud můžeme přirovnat k divoké řece, která se žene přes sráz do propasti.“ Naopak taktéž Tesla o Edisonovi: „Kdyby měl hledat jehlu v kupce slámy, nezastaví se, aby nejdříve zvážil, kde se jehla může s největší pravděpodobností nacházet. Pustí se do hledání jako pilná včelička.“ [12].
Kdo je kdo v neurochirurgickém souboji, nechám na laskavém čtenáři. Osobně bych si to vysvětloval tak, že transkortikální přístup může být „méně citlivý“ a transcisternální přístup „zdlouhavější“. Pokud bychom chtěli tuto historickou paralelu dotáhnout do konce, Tesla nakonec s využitím střídavého proudu vyhrál, tedy vítězem by byl transkortikální přístup. To koreluje i s vhodností dosažení a identifikací funkčních oblastí, pokud jsou v okolí gliomu přítomny, a skutečně – kupodivu, i v našem souboru jsme dosáhli větší radikality v případě lokalizace funkčních hranic nádoru (69 vs. 40 %). To potvrzuje metaanalýza právě zastánců transkortikálního přístupu (H. Duffau, M. Berger) [13] čítající 8 091 dospělých pacientů s mozkovými gliomy, operovaných v letech 1990–2010, kdy „gross total“ resekce bylo během mapovaných operací dosaženo v 75 % a naopak během operací bez použití intraoperativní elektrické stimulace pouze v 58 %. Asi nejlepší je pohled určitého kompromisu a „čisté“ operační techniky, ať již neurochirurg preferuje jakýkoli přístup, identifikace a zachování důležitých struktur, jako jsou elokventní korové struktury a hemisférální dráhy, dále kortikální (obr. 3a–c) a hluboké žíly, arterie vč. těch traverzujících nádor (obr 3d–f), hlavové nervy a struktury mozkového kmene.
Image 3. Zachování důležitých cévních struktur během operace nízkostupňového gliomu.
Fig. 3. Sparing of important vascular structures during low grade glioma surgery.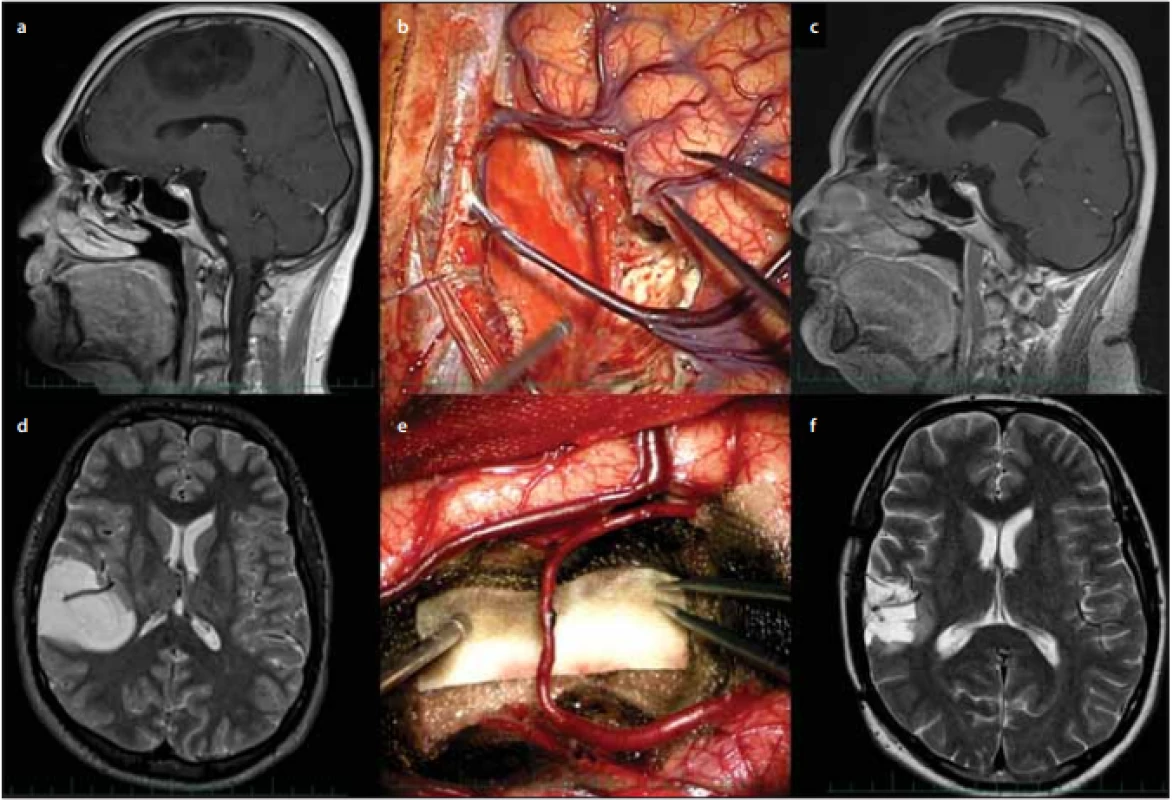
(a–c) 54letá pacientka po radikální resekci fi brilárního astrocytomu frontálně-parietálně vpravo (ANO Risk) v roce 2011, během operace byly monitorovány motorické evokované potenciály a prováděna elektrická stimulace, po operaci bez neurologického defi citu – (a) sagitální sken T1 MR s kontrastní látkou, lze předpokládat zasahování tumoru k precentrálnímu gyru; (b) intraoperační fotografi e s postresekční dutinou a zachováním přemosťujícíh žil do horního sagitálního splavu; (c) sagitální sken T1 MR s kontrastní látkou 3 měsíce po operaci; (d–f) 26letý pacient po parciální resekci oligodendrogliomu gyrus supramarginalis vpravo (ANO Risk) v roce 2019, po operaci bez neurologického defi citu, vč. perimetru – (d) axiální sken T2 MR, tumor zasahuje k optické radiaci; (e) intraoperační fotografi e s postresekční dutinou a zachováním traverzující větve a. cerebri media; (f) axiální sken T2 MR 10 měsíců po operaci, již po dokončení radioterapie s mírně regredujícím reziduem.
(a–c) 54-year-old female patient after the radical resection of a right frontal-parietal fi brillary astrocytoma (ANO Risk) in 2011; during the surgery, motor evoked potentials were monitored and electric stimulation was performed; after the procedure, no neurological defi cit was detected – (a) T1WI MRI sagittal scan with contrast matter, where the proximity of the tumor to the precentral gyrus is predictable; (b) intraperative photograph with post-resection cavity and spared draining veins to the superior sagittal sinus; (c) T1WI MRI sagittal scan 3 months after surgery. (d–f) 26-year-old male patient after partial resection of the right supramarginal gyrus oligodendroglioma (ANO Risk) in 2019; after surgery, there was no neurological defi cit including visual fi elds – (d) T2WI MRI axial scan, tumor is proximal to the optic radiation; (e) intraoperative photograph with post-resection cavity and spared traversing branch of the middle cerebral artery; (f) T2WI MRI axial scan 10 months after surgery; after completion of radiotherapy with slight regression of the residual tumor.Recentně to dokladuje práce z Barrow Neurological Institute srovnávající transsylvijský a transkortikální přístup v souboru 100 insulárních gliomů (LGG i HGG). Klinické výsledky obou přístupů jsou podobné, ale s preferencí transkortikálního přístupu k hornímu zadnímu kvadrantu insuly, kdy rozvoj pooperační ischemie byl přítomen pouze po transsylvijském přístupu (46 vs. 0 %) [14]. My jsme se snažili využívat spíše transcisterální a sulkální přístupy, bez využívání non-elokventních přístupových koridorů a subpiální resekce [15]. U jedné pacientky jsme využili transtentoriální přístup k mediotemporální oblasti, u další zadní interhemisférický přístup, bohužel komplikovaný hemianopsií. V případě insulárních a mediotemporálních gliomů používáme transsylvijský přístup.
Každopádně je praktické si definovat:
a) anatomickou operabilitu nádoru – kdy resekce musí vynechat primární funkční oblasti, tzn. motorický, zrakový kortex a primární řečové oblasti – zejména motorickou (p. triangularis a p. opercularis dolního frontálního gyru) a dráhy vycházející z těchto oblastí a taktéž většinu oblastí tzv. mozkového jádra (central core) [16], s výjimkou části caput ncl. caudati a talamu. Nikoli absolutní anatomicky inoperabilní oblastí jsou senzorické řečové oblasti v oblasti planum temporale, g. temporalis superior a medius, g. angularis a g. supramarginalis, kde je popsána velká funkční variabilita [17]. Anatomickou operabilitu intraoperačně kontrolujeme především vlastní znalostí anatomie, dále neuronavigací, UZ nebo někteří intraoperační MR. My jsme intraoperační MR s převozem pacienta na pracoviště MR během operace použili pouze u našeho nejmladšího pacienta s nevelkým gliomem předního dolního kvadrantu insuly, kde si operatér nebyl jist rozsahem resekce i lokalizací patologické tkáně. Intraoperační zobrazovací metody však musí vždy být mentálně fúzovány s vlastní znalostí anatomie a během operace dosaženými orientačními body, jako jsou tvar jednotlivých gyrů, mozkové cévy a jejich průběh vzhledem ke gyrifikaci, dále pak komorový systém, cisterny a durální hranice;
b) funkční operabilitu nádoru, kterou lze odhadnout předoperačně podle anatomických struktur a dále za použití pomocných metod, jako jsou funkční MR [18] a zobrazení tenzorů difuze [19]. Dále ji verifikujeme pomocí intraoperativního mapování a monitorace (kortikální a subkortikální stimulace, evokované potenciály).
U 20 pacientů, u kterých byla následně aplikována radiochemoterapie a měli pozorovatelné reziduum, bylo možno u 90 % z nich pozorovat grafickou regresi nálezu (obr. 4). Tento nález koreluje jak s našimi předchozími výsledky [20], tak i s dalšími onkologickými publikacemi ve světě i u nás [21,22].
Image 4. MR, T2 axiální skeny – 45letá pacientka operovaná v roce 2010 pro difuzní infiltrativní fibrilární astrocytom (skupina NE), původně neindikovaný k operaci, pacientka měla několikrát denně generalizovaný epileptický záchvat.
Fig. 4. T2WI MRI, axial scans – 45-year-old female patient operated on in 2010 for diffuse infi trative fibrillary astrocytoma (group NE); initially not indicated for surgery, but the patient had several generalized epileptic seizures daily.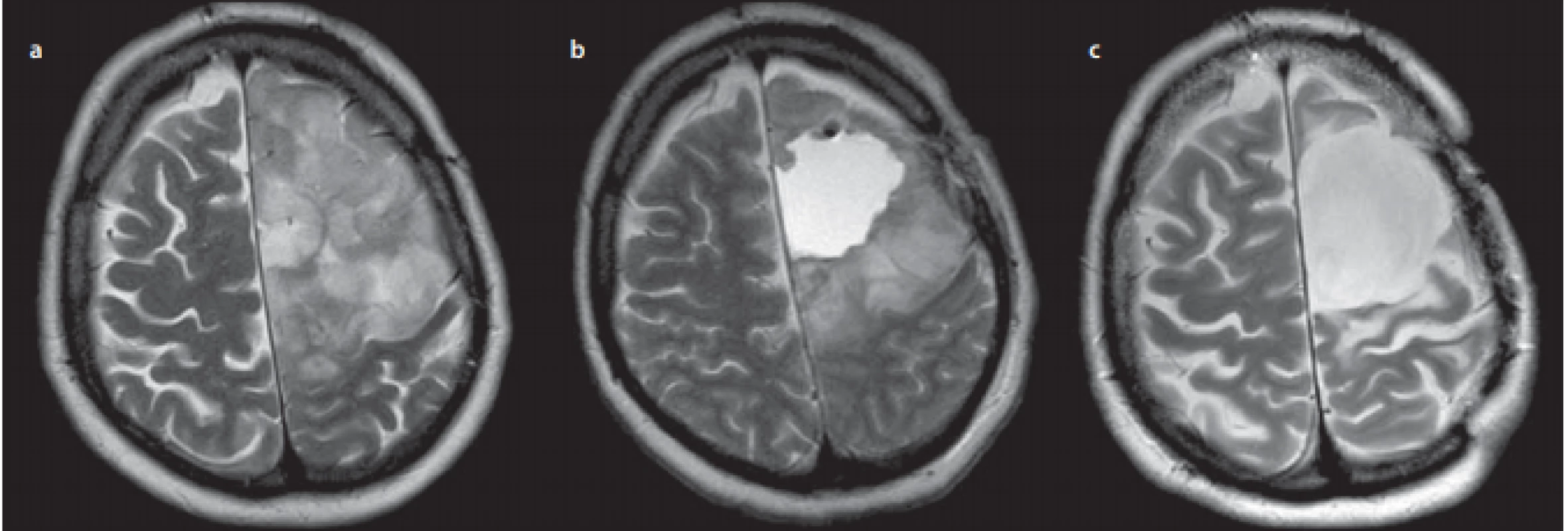
(a) před operací – infiltrace primární motorické kůry gliomem;
(b) reziduum 3 měsíce po operaci před zahájením onkologické léčby;
(c) 10 let po dokončení radiochemoterapie s regresí reziduálního nádoru, pacientka je samostatně mobilní s oporou hole, jemná motorika pravé horní končetiny je horší zejména při psaní a má pouze ojedinělé Jacksonské epileptické záchvaty.
(a) before the surgery – infi ltration of the primary motor cortex by glioma;
(b) residual tumor 3 months after surgery before starting oncological treatment;
(c) 10 years after completion of radiochemotherapy with residual tumor regression; the patient is unaidedly mobile with walking stick for support, fine finger movements of the right hand are worse especially when writing, and she has only sporadic Jacksonian epileptic seizures.Závěr
Před operací a během ní si musíme postupně jasně anatomicky pojmenovat oblasti, ve kterých je resekce ještě smysluplná a nepřináší pacientovi enormní riziko. Difuzní LGG můžeme tedy rozdělit na:
- radikálně operabilní (ANO) – v našem souboru 68 %:
- a) s bezpečným odstupem k elokventní oblasti (ANO Safe) – v našem souboru 16 %;
- b) vyžadující dosažení hranice k elokventní oblasti (ANO Risk) – v našem souboru 51 %,
- nutně parciálně operabilní (NE) – v našem souboru 32 %.
Naše resekční výsledky potvrzují logičnost takovéto klasifikace operability LGG na základě předoperačního snímku: ANO Safe – radikální resekce ve 100 %; ANO Risk – radikální resekce v 37 % a subtotální resekce v 32 %, tzn. celkem v 69 %, neúspěšní jsme byli v 21 %; NE – parciální resekce ve 100 % případů.
Ve skupině ANO Risk, pokud se subjektivně během operace pohybujeme na hraně bezpečnosti (obr. 5), je nutné mít na paměti, že u pacienta staršího 40 let je radiochemoterapie po operaci indikována a je účinná. Mějme tedy na mysli, že bychom pacientovi neměli způsobit motorický, řečový a pokud možno ani kognitivní deficit. Dobrá znalost anatomie a stanovení jasných anatomických hranic před operací nám v tom může pomoci, doporučujeme si před každou operací LGG načrtnout skicu anatomického obrazu, který se nám naskytne po provedení durotomie.
Image 5. Pooperační MR pacientů po resekcích nízkostupňových gliomů skupiny ANO Risk, kde operatér dosáhl maximální možné resekce.
Fig. 5. Postoperative MRI of patients with low grade gliomas in the group ANO Risk, when the surgeon was able to achieve maximal possible radical resection.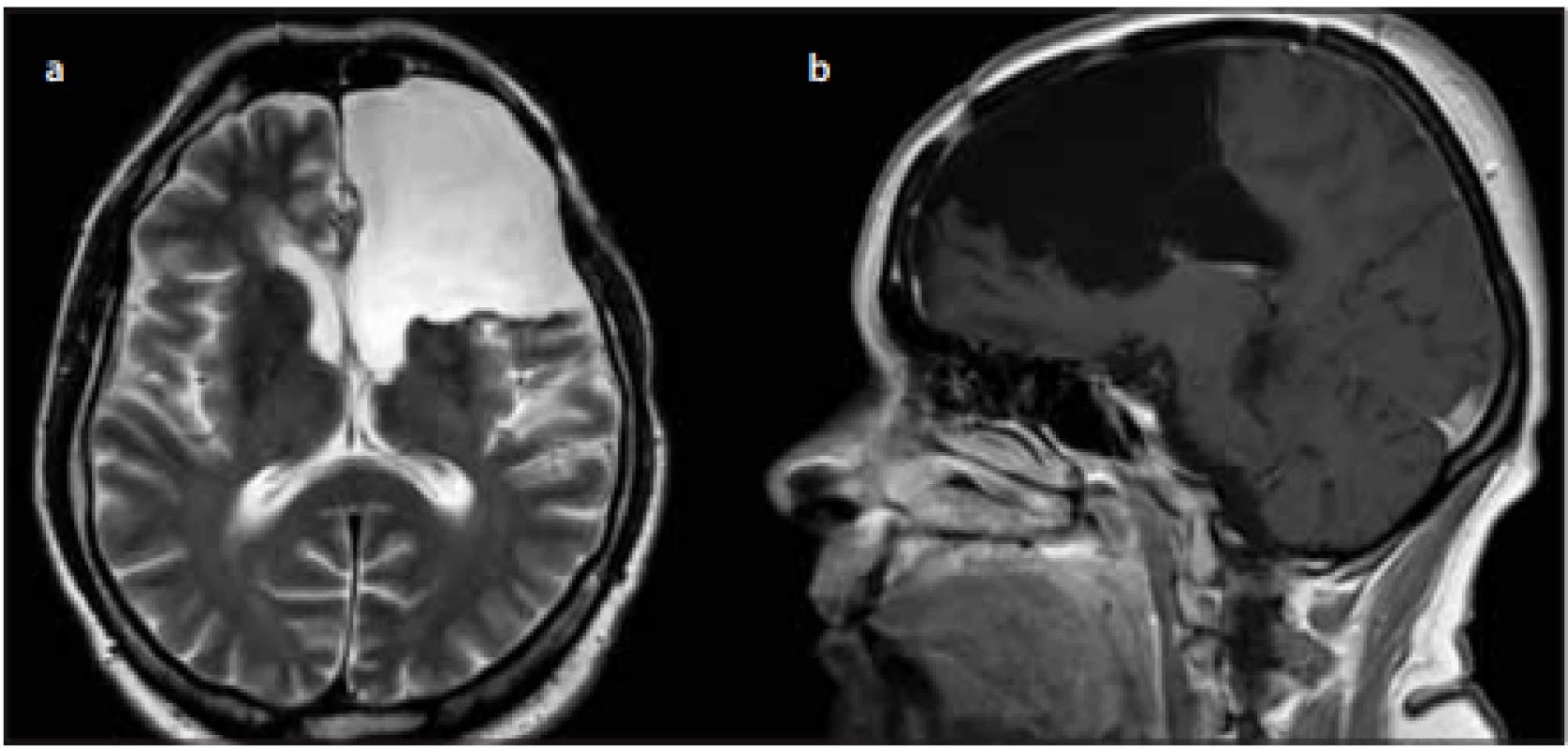
(a) T2 MR axiální sken – 44letý muž operovaný v roce 2013 pro oligodendrogliom WHO grade II–III, provedena frontální lobektomie, vč. resekce části caput ncl. caudati; (b) T1 MR sagitální sken – 44letá žena operovaná v roce 2016 pro oligodendrogliom WHO grade II, provedena resekce horního frontálního gyru, g. cinguli a infi ltrovaného corpus callosum. WHO – Světová zdravotnická organizace
(a) T2WI MRI axial scan – 44-year-old male patient operated on in 2013 for oligodendroglioma WHO grade II–III; frontal lobectomy was performed including resection of the part of the caput nuclei caudati; (b) T1WI MRI sagittal scan – 44-year-old female patient operated on in 2016 for oligodendroglioma WHO grade II; resection of the superior frontal gyrus, g. cinguli and infi ltrated corpus callosum was performed. WHO – World Health OrganizationEtická aspekty
Autoři prohlašují, že operace pacientů byla provedena po jjich předchozím informování v souladu s etickými standardy Etické komise Masarykovy nemocnice odpovědné za provádění klinických studií a Helsinskou deklarací z roku 1974, revidovanou v roce 2000.
Grantová podpora
Tato práce byla částečně podpořena vnitřním grantem KZ. a. s. (IGA-KZ-2020-1-20).
Konflikt zájmů
Autoři deklarují, že v souvislosti s předmětem studie nemají žádný konflikt zájmů.
MUDr. Robert Bartoš, Ph.D.
Neurochirurgická klinika Univerzity
J. E. Purkyně
Masarykova nemocnice,
Krajská zdravotní, a.s.
Sociální péče 3316/12A
400 11 Ústí nad Labem
e-mail: Robert.Bartos@kzcr.eu
Přijato k recenzi: 9. 12. 2020
Přijato do tisku: 20. 1. 2021
Sources
1. Polívka J Jr., Polívka J, Rohan V et al. Aktuální pohled na management nízkostupňových gliových nádorů centrálního nervového systému. Cesk Slov Neurol N 2016; 79/112 (5): 534–540.
2. Konečná D, Netuka D. Difuzní nízkostupňové gliomy. Cesk Slov Neurol N 2020; 83/116 (5): 467–490. doi: 10.14735/amcsnn2020467.
3. Bartoš R, Vachata P, Hejčl A et al. Vliv funkčního mapování na výsledky operací nízkostupňových gliomů WHO grade II. Cesk Slov Neurol N 2011; 74/107 (3): 292–298.
4. Yaşargil MG, Krisht AF, Tűre U et al. Microsurgery of insular gliomas: part II – opening of the sylvian fissure. Contempor Neurosurg 2017; 39 (14): 1–6. doi: 10.1097/000 29679-200206150-00001.
5. Yaşargil MG, Krisht AF, Tűre U et al. Microsurgery of insular gliomas: part IV – surgical treatement and outcome. Contempor Neurosurg 2017; 39 (18): 1–8. doi: 10.1097/01.CNE.0000527944.73058.a6.
6.Tűre U, Harupt MV, Kaya AH et al. The paramedian supracerebellar-transtentorial approach to the entire lenght of the mediobasal temporal region: an anatomical and clinical study. J Neurosurg 2012; 116 (4): 773–791. doi: 10.3171/2011.12.JNS11791.
7. Serra C, Türe U, Krayenbühl N et al. Topographic classification of the thalamus surfaces related to microneurosurgery: a white matter fiber microdissection study. World Neurosurg 2017; 97 : 438–452. doi: 10.1016/ j.wneu.2016.09.101.
8. Duffau H, Khalil I, Gatignol P et al. Surgical removal of corpus callosum infiltrated by low-grade glioma: functional outcome and oncological considerations. J Neurosurg 2004; 100 (3): 431–437. 10.3171/jns.2004.100.3. 0431.
9. Morshed RA, Young JS, Han SJ et al. The transcortical equatorial approach for gliomas of the mesial temporal lobe: techniques and functional outcomes. J Neurosurg 2019; 130 (3): 822–830. doi: 10.3171/2017.10.JNS172055.
10. Mishra A, Shetty P, Singh V et al. Microsurgical subpial resections for diffuse gliomas – old wine in a new bottle. Acta Neurochirurgica 2020; 162 (12): 3031–3035. doi: 10.1007/s00701-020-04524-1.
11. Roux A, Dezamis E, Trancart B et al. How I do it: trans-cortical approach for insular diffuse glioma. Acta Neurochirurgica 2020; 162 (12): 3025–3030. doi: 10.1007/s00701-020-04553-w.
12. National Geographic. Edison and Tesla‘s cutthroat ‚Current War‘ ushered in the electric age. [online]. Available form URL: https: //www.nationalgeographic.com/history/magazine/2016/07-08/edison-tesla-current-war-ushered-electric-age/.
13. De Witt Hamer PC, Robles SG, Zwinderman AH et al. Impact of intraoperative stimulation brain mapping on glioma surgery outcome: a meta-analysis. J Clin Oncol 2012; 30 (20): 2559–2565. doi: 10.1200/JCO.2011.38.4818.
14. Przybylowski CJ, Baranoski JF, So VM et al. Surgical morbidity of transsylvian versus transcortical approaches to insular gliomas. J Neurosurg 2019; 5 : 1–8. doi: 10.3171/2018.12.JNS183075.
15. Bartoš R, Němcová V, Radovnický T et al. Gliomy limbického a paralimbického systému, technika a výsledky resekcí. Cesk Slov Neurol N 2016; 79/112 (2): 131–147. doi: 10.14735/amcsnn2016131.
16. Ribas EC, Yağmurlu K, de Oliveira E et al. Microsurgical anatomy of the central core of the brain. J Neurosurg 2017; 129 (3): 752–769. doi: 10.3171/2017.5.JNS162897.
17. Ojemann G, Ojemann J, Lettich E et al. Cortical language localization in left, dominant hemisphere. An electrical stimulation mapping investigation in 117 patients. 1989. J Neurosurg 2008; 108 (2): 411–421. doi: 10.3171/JNS/2008/108/2/0411.
18. Bartoš R, Jech R, Vymazal J et al. Validity of primary motor area localization with fMRI versus electric cortical stimulation: a comparative study. Acta Neurochir (Wien) 2009; 151 (9): 1071–1080. doi: 10.1007/s00701-009-0368-4.
19. Zolal A, Hejčl A, Vachata P et al. The use of diffusion tensor images of the corticospinal tract in intrinsic brain tumor surgery: a comparison with direct subcortical stimulation. Neurosurgery 2012; 71 (2): 331–340. doi: 10.1227/NEU.0b013e31825b1c18.
20. Třebický F, Kubeš J, Bartoš R et al. Léčba nízkostupňového gliomu supratentoriální oblasti mozku po neurochirurgické subtotální resekci s projevy objemového up-gradingu. Klin Onkol 2012; 25 (4): 294–298. doi: 10.14735/amko2012294.
21. Bell EH, Zhang P, Shaw EG et al. Comprehensive genomic analysis in NRG oncology/RTOG 9802: a phase III trial of radiation versus radiation plus procarbazine, lomustine (CCNU), and vincristine in high-risk low-grade glioma. J Clin Oncol 2020; 38 (29): 3407–3417. doi: 10.1200/JCO.19.02983.
22. Lakomý R, Kazda T, Poprach A et al. Postavení chemoterapie v pooperační léčbě low-grade gliomů. Klin Onkol 2017; 30 (5): 343–348. doi: 10.14735/amko2017343.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2021 Issue 1-
All articles in this issue
- Editorial
- Poděkování recenzentům
- Frontotemporální demence
- COVID-19 a iktus
- Vizuální hodnocení a digitální analýza ultrazvukového obrazu u stabilního a progredujícího aterosklerotického plátu v karotické tepně
- Karotická endarterektómia po intranevóznej trombolýze a mechanickej trombektómii
- Validace české verze škály NPCS pro hodnocení potřeb pacientů s progresivním neurologickým onemocněním
- Encefalokéla v České republice – incidence, prenatální diagnostika a mezinárodní srovnání
- Komplexní léčba difuzních nízkostupňových gliomů – technika operování a onkologická léčba rezidua
- Komentář k článku autorů Bartoš et al Komplexní léčba difuzních nízkostupňových gliomů – technika operování a onkologická léčba rezidua
- Bowing třetí komory jako radiologický ukazatel obstrukčního hydrocefalu a úspěšnosti endoskopické ventrikulocisternostomie
- Vliv první vlny pandemie COVID-19 na počty hospitalizovaných pacientů s ischemickou cévní mozkovou příhodou, na jejich diagnostiku a terapii
- Kazuistika relabující infekce COVID-19 u pacientky s roztroušenou sklerózou léčenou ocrelizumabem
- Komentář k článku autorů Sejkorová et al Hemodynamic changes in four aneurysms leading to their rupture at follow-up periods
- Informace vedoucího redaktora
- Prof. MUDr. Vladimír Beneš, DrSc. – 100 let
- Epiglotopexe v léčbě obstrukční spánkové apnoe
- Prognostická úloha poměru neutrofilů k lymfocytům u dětského typu cystického adamantinomatózního kraniofaringeomu
- „Nový normál“ pro adjuvantní léčbu glioblastomu v podmínkách pandemie COVID-19
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Frontotemporální demence
- Encefalokéla v České republice – incidence, prenatální diagnostika a mezinárodní srovnání
- COVID-19 a iktus
- Karotická endarterektómia po intranevóznej trombolýze a mechanickej trombektómii
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

