-
Medical journals
- Career
Komplikace kranioplastik po dekompresivní kraniektomii
Authors: D. Hrabovský 1; R. Jančálek 1,2; I. Říha 1,3; J. Chrastina 1,3
Authors‘ workplace: Neurochirurgická klinika LF MU a FN U sv. Anny v Brně 1; ICRC – Mezinárodní centrum klinického výzkumu, FN u sv. Anny v Brně 2; CEITEC – Středoevropský technologický institut, MU, Brno 3
Published in: Cesk Slov Neurol N 2016; 79/112(1): 77-81
Category: Short Communication
Overview
Cíl:
Podle literatury dosahuje četnost komplikací kranioplastiky po dekompresivní kraniektomii i více než 30 %. Cílem studie je hodnocení četnosti, příčin a léčby komplikací kranioplastik po dekompresivní kraniektomii pro expanzivně se chovající supratentoriální ischemii nebo kraniocerebrální poranění a analýza důvodů neprovedení kranioplastiky u části nemocných po dekompresivní kraniektomii.Soubor a metodika:
V retrospektivní studii nemocných po dekompresivní kraniektomii (2006 – 2014) byla kranioplastika provedena u 25 z 35 nemocných s expanzivní malacií (71,4 %) a u 33 z 68 zraněných s poúrazovou nitrolební hypertenzí (48,5 %).Výsledky:
Nejčastější příčinou neprovedení kranioplastiky bylo úmrtí. U 20 % nemocných s mozkovou ischemií a 61,3 % zraněných byla kranioplastika provedena časně (do 10 týdnů). Četnost neurochirurgických komplikací byla u kranioplastik u nemocných s expanzivní malacií 12 % (explantace plastiky u 8 %) a u kranioplastik po kraniocerebrálním poranění dosahovala 9,1 % (explantace plastiky u 3 %). Hydrocefalus a subdurální kolekce byly před kranioplastikou přítomny u 6 a 9,1 % zraněných. Četnost hydrocefalu po kranioplastice byla u kraniotraumat 6 % a u mozkové ischemie 4 %.Závěry:
Četnost komplikací kranioplastik, byť nižší než uvádí literatura, převyšuje hodnoty očekávané u elektivních operací. Subdurální kolekce a hydrocefalus nelze jednoznačně hodnotit jako komplikaci kranioplastiky, protože mohou být přítomny již před kranioplastikou v důsledku základního onemocnění.Klíčová slova:
kranioplastika – dekompresivní kraniektomie – mozková ischemie – kraniocerebrální poranění – hydrocefalus – neurochirurgická komplikaceÚvod
Cílem dekompresivní kraniektomie (DK) je rychlá kontrola refrakterní nitrolební hypertenze především po kraniocerebrálním poranění, expanzivně se chovající malacii, subarachnoidálním nebo intracerebrálním krvácení a u zánětlivých onemocnění mozku [1 – 5]. Po odeznění otoku mozku je nutné uzavření defektu lebky – kranioplastika. Mimo obnovení integrity kostního krytu mozku a kosmetického efektu je důležitým výsledkem kranioplastiky pozitivní ovlivnění příznaků zahrnovaných do termínu ,,syndrome of the trephined“ (syndrom trepanovaných) [6]. Technicky relativně jednoduchá kranioplastika je ovšem spojena s několika problémy. Prvním je porovnání výhodnosti různých kranioplastických materiálů, kdy je mimo vlastní kostní ploténky (autoplastika) možné použít náhradu umělou, např. PEEK (polyetheretherketon), Palacos (metylmetakrylát) a titan, což je spojeno s možností využití počítačově modelovaných náhrad [7,8]. Další otázkou je podíl nemocných po DK, kteří se kranioplastiky dožijí a jejichž stav operaci umožňuje [9]. Zásadní problém kranioplastik po DK je překvapivě vysoká četnost komplikací, dosahující 30 – 40 % [10,11]. Četnost komplikací může být ovlivněna řadou faktorů, např. načasováním plastiky, kdy rozlišujeme kranioplastiky časné a pozdní (hranice např. 10 týdnů po DK) [12]. Příčinou rozvoje hydrocefalu nebo subdurálních kolekcí po DK nemusí být pouze provedená DK, ale také onemocnění, které vyžadovalo provedení DK (např. poúrazový hydrocefalus) [13,14]. Oba problémy mohou komplikovat realizaci kranioplastiky. Dojde-li k rozvoji hydrocefalu nebo subdurální kolekce po kranioplastice, mohou být považovány za její komplikaci.
V předložené retrospektivní studii se výše uvedenými problémy zabýváme z pohledu vlastních zkušeností s kranioplastikou po DK pro expanzivně se chovající supratentoriální mozkovou malacii a poúrazovou nitrolební hypertenzi. Funkční výsledky DK pro účely studie zjednodušeně hodnotíme podle počtu nemocných, kteří se kranioplastiky dožijí ve stavu, jenž operaci umožňuje. Hlavní náplní práce je analýza komplikací kranioplastiky, jejich příčin, četnosti a možností léčby s porovnáním výsledků s literárními daty. Práce navazuje na domácí písemnictví zabývající se problematikou DK a některými specifickými problémy kranioplastik [7,15,16].
Soubor a metodika
V nemocničním informačním systému bylo vyhledáno 35 nemocných s DK pro expanzivně se chovající supratentoriální mozkovou malacii (17 mužů, 18 žen, medián věku 59 let, SD 10,6 roku) operovaných v letech 2006 – 2014. Do souboru byli zařazeni i čtyři nemocní s expanzivní malacií po kardiochirurgické operaci nebo endovaskulárním výkonu. Medián Glasgow Coma Scale (GCS) před operací byl 10 (SD 2,4) a medián intervalu iktus – DK 1 den (SD 1,8 dne, průměr 2,02 dne). Kranioplastika byla provedena u 25 nemocných (71,4 %) ze souboru (medián věku 54,5 roku, SD 11,2 roku), u nichž jsme hodnotili interval mezi DK a kranioplastikou, podíl časných a pozdních kranioplastik (hranice 10 týdnů) a především problém komplikací.
Do souboru DK pro kraniocerebrální poranění bylo zařazeno 68 zraněných (11 žen, 57 mužů, medián věku 58 let, SD 16,9 roku, medián GCS 7, SD 3,6) operovaných ve stejném období. U 38 zraněných byla DK součástí primární operace a u 30 se jednalo o výkon sekundární (medián odstupu po primooperaci 20 hod, SD 20,4 hod). Indikací k sekundárnímu výkonu byla trvající nitrolební hypertenze po primární operaci podle hodnot nitrolebního tlaku (ICP) a nálezu na kontrolním CT. Zranění po DK indikované na základě monitorace ICP po implantaci čidla bez jiného výkonu byli hodnoceni jako sekundární DK. Bilaterální DK byla indikovaná u dvou zraněných, bifrontální DK u žádného. Kranioplastika byla provedena u 33 (48,5 %) z 68 zraněných s DK (medián věku 51 roku, SD 17,1 roku), u kterých byl sledován interval DK – kranioplastika, podíl časných a pozdních kranioplastik a problematika komplikací kranioplastik.
Kranioplastika byla prováděna především pomocí kostní ploténky odstraněné při DK, jež byla uchovávána v mrazicím boxu kliniky ( – 83 °C – teplota jako v tkáňové bance, technika uskladnění a manipulace standardní – dva obaly, řádné označení). Umělé náhrady byly primárně použity při devastaci kalvy tříštivými zlomeninami a při kontaminovaném poranění. Základními podmínkami k provedení kranioplastiky bylo zhojení operační rány, vyloučení infekčního fokusu, celkový stav nemocného umožňující výkon v celkové anestezii a předpoklad přínosu kranioplastiky pro nemocného.
Intervaly pooperačních klinických kontrol byly stanoveny v závislosti na stavu nemocného nebo zraněného a vzdálenosti spádové nemocnice, kam byl po kranioplastice překládán. Odstup od operace byl u všech zařazených pacientů delší než 12 měsíců.
Výsledky
DK pro expanzivně se chovající malacii
Nejčastější důvod neprovedené kranioplastiky bylo úmrtí (osm nemocných). U dvou nemocných neproběhla konzultace klinického stavu a výsledku CT doporučená při překladu na spádové pracoviště, ale vzhledem k jejich stavu lze předpokládat úmrtí. Pro zdůvodnění mortality uvádíme, že 20 % nemocných bylo před DK v kómatu. Celková četnost infekčních komplikací po DK byla 40 %, ovšem četnost infekčních komplikací postihujících ránu byla 0 %.
U všech nemocných byla primárně provedena autoplastika. Medián intervalu kraniektomie–kranioplastika byl tři měsíce (SD 1,8 měsíce). Časná kranioplastika byla provedena u 20 % nemocných. Komplikace kranioplastiky byly řešeny ve třech případech (12 %). U jednoho nemocného byla povrchová infekce zvládnuta konzervativně (DK–kranioplastika čtyři měsíce). U dalšího (DK–kranioplastika šest měsíců) bylo nutné kranioplastiku odstranit pro epidurální empyém a po čtyřech měsících následovala plastika Palacosem. U těchto nemocných nebyl v předchorobí nebo během hospitalizace identifikován žádný faktor potenciálně zvyšující riziko komplikace. U nemocného s expanzivně se chovající mozkovou ischemií po disekci aorty vyžadující akutní operaci byla dlouhodobá hospitalizace po DK komplikována řadou infekčních problémů (DK–kranioplastika šest měsíců). Ovšem již za měsíc po kranioplastice bylo nutné zavést ventrikuloperitoneální shunt pro hydrocefalus a explantovat dislokovanou ploténku pro infekci. Nová plastika Palacosem byla provedena za čtyři měsíce, ale infekční komplikace si vynutila také její odstranění. Explantace kranioplastiky byla tedy indikována u dvou nemocných (8 %) a u jednoho nemocného bylo nutné řešit hydrocefalus (4 %). Všechny popisované komplikace postihovaly pozdní kranioplastiky.
Nemocní s DK pro kraniocerebrální poranění
U 27 zraněných (39,3 %) nebyla kranioplastika provedena pro úmrtí. Zde uvádíme, že 37 zraněných ze souboru (54,4 %) bylo po úrazu v kómatu (GCS < 8). Stav čtyř zraněných přijatých, tlumených na řízené ventilaci nebyl hodnotitelný pro nedostatečnou dokumentaci z odesílajícího pracoviště nebo RZP. U dalších šesti zraněných po DK neproběhla konzultace klinického stavu a výsledku CT doporučená při překladu na spádové pracoviště. S výjimkou jediného zraněného repatriovaného v dobrém stavu do zahraničí lze předpokládat, že příčinou byl špatný celkový stav nebo úmrtí. U dvou zraněných dlouhodobě ve vegetativním stavu s infekčními komplikacemi jsme kranioplastiku neindikovali. Dva zranění byli po DK reoperováni pro hematom a u jednoho byla kranioplastika odkládána pro lokální infekci. Četnost infekčních komplikací mimo oblast DK dosahovala 33 %.
U 31 zraněných po DK (11 sekundárních, 20 primárních – 93,9 %) byla provedena autoplastika. Primární plastika Palacosem byla indikována u dvou zraněných s kominutivními otevřenými zlomeninami. Medián intervalu DK–kranioplastika byl dva měsíce (SD 1,88; 0,5 – 10 měsíců). U 63,6 % zraněných se jednalo o kranioplastiku časnou. Komplikace postihly tři zraněné (9,1 %). U dvou (jeden primární, druhý sekundární DK) dostačovalo lokální ošetření kožní dehiscence (DK–kranioplastika tři měsíce oba). U jedné zraněné (DK–kranioplastika 1,5 měsíce) byla s odstupem jednoho roku po autoplastice prokázána její výrazná resorpce, což vyžadovalo metylmetakrylátovou rekranioplastiku. Četnost komplikací kranioplastik po primárních (10 %) a sekundárních DK (9,1 %) je tedy prakticky totožná. I zde je četnost komplikací u kranioplastik pozdních (16,7 %) vyšší než u časných (4,8 %).
Subdurální kolekce byla před kranioplastikou popsána u tří nemocných (9,1 %). Ve dvou případech byla kranioplastika s evakuací kolekce provedena během jedné operace. U nemocného s extrakraniálními infekčními problémy byla trepanace k vyloučení subdurálního empyému provedena tři dny před kranioplastikou. U dvou nemocných (6 %) byla před vlastní kranioplastikou nutná implantace shuntu (v jednom případě lumboperitoneálního při dobrém efektu lumbální drenáže) pro dlouhotrvající hydrocefalus s nápadnou protruzí mozkové tkáně. Součástí původního poranění u obou nemocných bylo významné subarachnoidální krvácení a rozsáhlá kontuzně hemoragická ložiska, což mohlo vést malresorpci mozkomíšního moku. U dvou nemocných bylo nutné s odstupem čtyř a sedmi měsíců po kranioplastice zavést shunt pro hydrocefalus.
Diskuze
Nejobvyklejší příčinou neprovedené kranioplastiky u některých nemocných po DK je úmrtí nebo závažný celkový stav. Výsledky Movassaghiho et al (kranioplastika u 81,5 % nemocných po DK) [9] a El Ghoula et al (kranioplastika u 96,2 % zraněných po DK) [17] výrazně převyšují vlastní četnost kranioplastik po DK pro kraniocerebrální poranění (48,5 %). Za příčinu považujeme a vysoký podíl zraněných s GCS < 8 (54,4 %) a vysoký medián věku (51,1 roku) ve srovnání s 37,7 roku [17], což znamená vyšší mortalitu i v důsledku interních komplikací. U nemocných s DK pro expanzivně se chovající malacii je nižší podíl provedených kranioplastik méně výrazný (71,4 %).
V tab. 1 shrnujeme počty nemocných a indikace DK ve vybraných studiích zabývajících se komplikacemi kranioplastik. V souboru 348 nemocných s DK pro nitrolební hypertenzi při subarachnoidálním krvácení, expanzivní ischemii mozku a kraniocerebrálním poranění dosahovala četnost komplikací 31,32 % [11]. Coulter et al řešili alespoň jednu pooperační komplikaci u 40,4 % nemocných s kranioplastikou. Dominovaly infekční komplikace (21,7 %), které byly nejčastější příčinou odstranění kranioplastiky (16,3 % nemocných) [10]. Vysokou četností reoperací (25,4 %) při srovnatelné četnosti komplikací (34 %) je zatížen soubor zraněných s kranioplastikou po kraniocerebrálním poranění publikovaný Goochem et al [18].
Table 1. Přehled studií zabývajících se problematikou komplikací kranioplastik po DK z různých indikací. 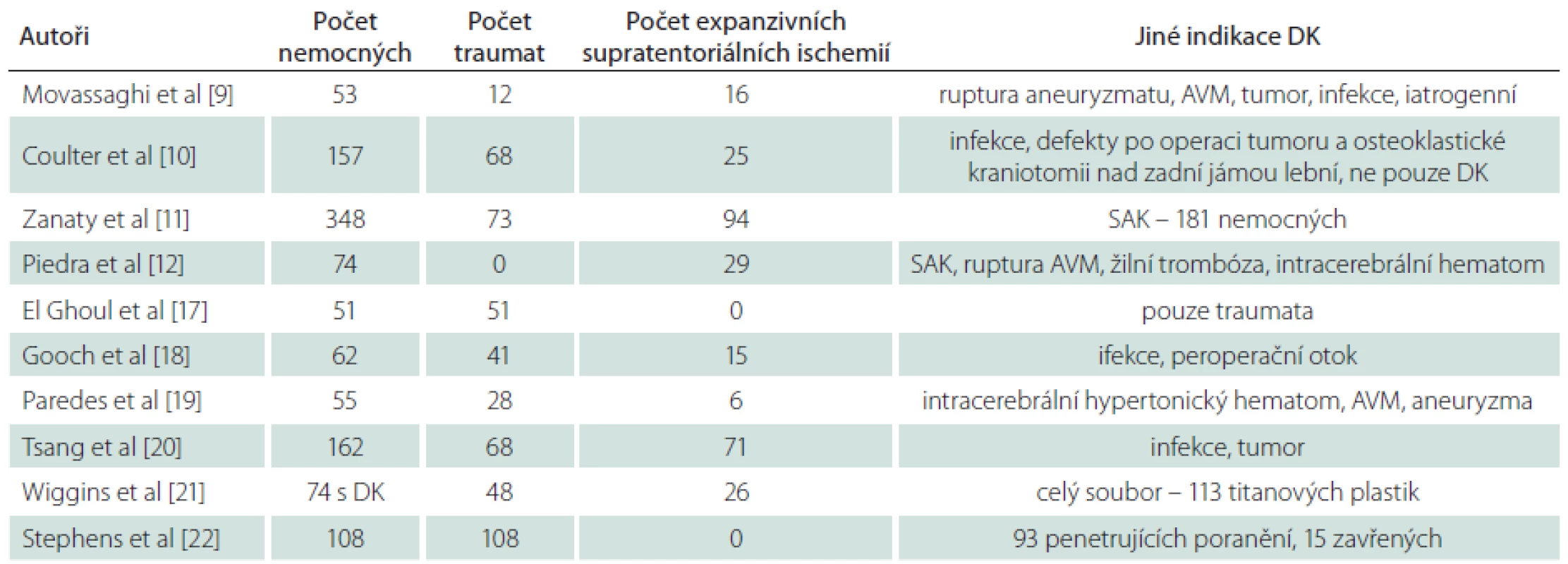
AVM – arteriovenózní malformace, DK – dekompresivní kraniektomie, SAK – subarachnoidální krvácení. Nižším počty komplikací uvádějí Paredes et al (18,2 %) a Tsang et al (16,7 %) [19,20]. Tato data jsou srovnatelná s našimi vlastními výsledky, i když spektrum zařazených nemocných je odlišné (tab. 1). Zmínku zasluhuje studie Wigginse et al hodnotící titanové kranioplastiky „na míru“, prováděné především u rizikových nemocných s kostními infekcemi po primární operaci nebo kranioplastice (61,5 %) a u infikovaných poranění (16,1 %). Ze 113 kranioplastik ale pouze 74 řešilo rozsáhlý defekt po DK. Četnost komplikací dosahovala 33 % a polovina byla infekčního původu [21]. Závěrem uvádíme data z Walter Reed Center a National Naval Medical Center, kam byli repatriováni zranění z Iráku a Afghánistánu. U těchto válečných poranění nebyly prováděny ,,jednoduché“ kranioplastiky, ale komplexní výkony s rekonstrukcí spodiny lební, paranazálních dutin a orbitofaciálního skeletu. Četnost komplikací dosahovala 24 % (12 % infekce, 11 % odstraněných náhrad), což je srovnatelné s výše uvedenými mírovými daty [22].
Cílem citovaných studií byla také identifikace příčin vysoké četnosti komplikací kranioplastik. Podle některých autorů je kranioplastika po bifrontální kraniektomii zatížena vyšším rizikem komplikací než plastika jednostranné DK [10,11,18,19]. Coulter et al uvádějí četnost reoperací po bifrontální kranioplastice 36,0 % (16,4 % po jednostranné) [10]. Příčinou vyšší četnosti komplikací u bifrontálních kranioplastik je vztah defektu k paranazálním dutinám s potenciální kontaminací operačního pole. Ovšem Wiggins et al významně vyšší četnost komplikací u bifrontálních kranioplastik ve srovnání s jednostrannými neprokázali [21]. Jiným faktorem zvyšujícím četnost komplikací je zavedený ventrikuloperitoneální shunt [20]. Při hodnocení vztahu materiálu kranioplastiky a četnosti komplikací citujeme přehledovou práci Yadla et al, kde autoři po vyhodnocení celkem 18 publikovaných sdělení uvádějí, že typ materiálu nemá vliv na četnost komplikací kranioplastiky [23]. Z dalších rizikových faktorů uvádíme vyšší věk, horší celkový stav, hypertenzi a diabetes [11,19].
Vztah načasování kranioplastiky a četnosti komplikací není jednoznačný. Časná kranioplastika může znamenat vyšší riziko infekce především u nemocných v závažném stavu, dlouhodobě hospitalizovaných na JIP s invazivními vstupy a možnými infekčními fokusy. Ovšem časná plastika může díky zlepšení perfuze mozku jeho oddělením od působení atmosférického tlaku napomoci zlepšení stavu [24]. Pro časnou kranioplastiku hovoří i jednodušší preparace jednotlivých vrstev [18]. Důležitým argumentem pro časnou kranioplastiku je zabránění rozvoji „syndrome of the trephined“ (syndromu trepanovaných), zahrnujícímu ortostatickou cefaleu a horšící se motorické a kognitivní funkce. U pozdních kranioplastik také dochází k výraznější resorpci kosti [25].
K preferenci pozdních kranioplastik přispěla historická práce Rishe et al, jejíž autoři prokázali, že kranioplastiky provedené s odstupem méně než šest měsíců po DK jsou zatíženy vyšším rizikem komplikací. Ovšem tato práce se zabývala rizikovými penetrujícími kraniocerebrálními poraněními [26]. Yadla et al vliv načasování kranioplastiky na četnost infekčních komplikací neprokázali [23]. Podobně Piedra et al (hranice časná–pozdní kranioplastika 10 týdnů) neprokázali statisticky významný rozdíl mezi četností komplikací časných (22 %) a pozdních kranioplastik (16 %) [12].
Ve vlastním souboru nemocných s DK pro expanzivní supratentoriální ischemii je četnost chirurgických komplikací kranioplastik 12 % a z toho četnost odstraněných náhrad 8 %, což je méně, než uvádějí citovaná sdělení. Podobná situace je i u kranioplastik po DK pro kraniocerebrální poranění, kdy četnost chirurgických komplikací kranioplastiky dosahovala 9,1 % a explantace kranioplastiky byla nutná u jediného nemocného (3,1 %). V obou skupinách byla vyšší četnost komplikací u kranioplastik pozdních.
U některých nemocných dochází po DK k rozvoji hydrocefalu, často spojeného s výrazným vyklenováním mozku kostním defektem. Tento problém může být dočasný, protože provedení kranioplastiky vytváří podmínky k úpravě mokové cirkulace. Tsang et al to dokládají změnami dynamických studií mozkomíšního moku po kranioplastice u nemocných se „syndrome of the trephined“ [20]. Proto někdy může dostačovat peroperační punkce komory nebo předoperační lumbální drenáž. Ovšem při výrazném hydrocefalu a prominenci mozkové tkáně kraniektomií a delším odstupu mezi DK a kranioplastikou lze předpokládat trvalou poruchu cirkulace moku (zvláště po masivním subarachnoidálním krvácení nebo infekci). K redukci prominence mozkové tkáně komplikující kranioplastiku může být zaveden shunt, ovšem po jeho implantaci bez kranioplastiky dochází k propadnutí („sinkingu“) kraniektomie [27]. Možným řešením je kranioplastika a zavedení shuntu v jedné době, ale tento postup může být zatížen vyšším rizikem komplikací než výkon dvoudobý [13]. Oh et al sice popisují lepší výsledky, pokud je shunt implantován po kranioplastice, ovšem pouze u nemocných s hydrocefalem a velmi mírnou prominencí mozku. Při výrazné prominenci mozku dané hydrocefalem citovaní autoři primárně implantují shunt [28].
Považovat rozvoj hydrocefalu po kranioplastice za její komplikaci je velmi diskutabilní především u nemocných s kraniocerebrálními poraněními. Podle Kammersgarda et al dosahuje četnost hydrocefalu po těžkém kraniocerebrálním poranění 14,3 % a u 75 % zraněných dochází k rozvoji hydrocefalu s odstupem od operace, tedy i v období po kranioplastice [29].
Jiným problémem, který může být nutné řešit při kranioplastice, jsou subdurální kolekce pozorované u některých nemocných kontralaterálně k DK. Jejich příčinou jsou trhliny arachnoidey a porucha vstřebávání mozkomíšního moku při blokádě arachnoidálních klků. Symptomatické jsou přibližně u poloviny nemocných [30]. Řešením může být časná kranioplastika, která napomůže úpravě mokové cirkulace [14]. Jinou možností je provedení kranioplastiky s následnou trepanací a evakuací kolekce. Efekt trepanace bez kranioplastiky je pouze dočasný [30]. Především u rozsáhlých symptomatických kolekcí je nutné zvážit provedení trepanace a kranioplastiky v jedné době.
Pro snížení vysoké četnosti komplikací kranioplastiky je třeba zhodnotit stav nemocného s důrazem na vyloučení infekčních fokusů a stav nutrice (hojení operační rány). Časnou kranioplastiku považujeme za výhodnou pro možnost zlepšení mozkové perfuze po uzavření lebečního defektu. Navíc literární data vyšší četnost komplikací časných kranioplastik neprokázala. Přesný odstup mezi DK a kranioplastikou je nutné zvážit individuálně. Kranioplastiku neindikujeme u nemocných se stacionární dlouhodobou poruchou vědomí a závažným neurologickým deficitem při prokázané strukturální lézi mozku. Autoplastiku považujeme za metodu první volby při nemožnosti autoplastiky. Při sekundární plastice po infektu jsou na místě umělé náhrady s možným použitím individuálně připravovaných náhrad např. u složitých defektů postihujících i bazi lební. Co se týče řešení komplikací, infekce kranioplastiky znamená indikaci k jejímu odstranění. Rekranioplastiku lze provést po sanaci infekce většinou s odstupem několika měsíců. Problematiku hydrocefalu a subdurálních kolekcí shrnujeme výše.
Za limitaci studie je možné považovat její retrospektivní charakter, i když výsledky léčby byly k dispozici u všech nemocných s kranioplastikou. Důvod neprovedení kranioplastiky nebyl jasný pouze u ojedinělých nemocných. Doba sledování v rozmezí jednoho až dvou let je pro záchyt některých komplikací hraniční (kostní resorpce nebo pozdní infekce), ovšem při vzniku komplikace postihující operovanou oblast jsou neurochirurgičtí nemocní odesíláni na pracoviště, kde byl proveden primární výkon.
Závěry
Analýza výsledků kranioplastik po DK pro kraniocerebrální poranění nebo expanzivně se chovající malacii ukazuje nižší počet komplikací, než odpovídá literárním datům. Ovšem i tato čísla převyšují četnost očekávanou u elektivních neurochirurgických operací. Vyšší riziko komplikací u časných kranioplastik nebylo prokázáno. Specifický problém kranioplastik představují hydrocefalus a subdurální kolekce vznikající v důsledku narušení mokové cirkulace.
Prohlášení
Autoři prohlašují, že studie na lidských subjektech popsaná v manuskriptu byla provedena v souladu s etickými standardy příslušné komise (institucionální a národní) odpovědné za provádění klinických studií a Helsinskou deklarací z roku 1975, revidovanou v roce 2000.
Podpořeno projektem CEITEC CZ.1.05/ 1.1.00/ 02.0068.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Přijato k recenzi: 1. 10. 2015
Přijato do tisku: 24. 11. 2015
doc. MUDr. Jan Chrastina, Ph.D.
Neurochirurgická klinika
LF MU a FN u sv. Anny v Brně
Pekařská 53
656 91 Brno
e-mail: jan.chrastina@fnusa.cz
Sources
1. Hofmeijer J, Kapelle LJ, Algra A, Amelink GJ, van Gijn J, van der Worp HB. Surgical decompression for space occupying cerebral infarction (the Hemicraniectomy After Middle Cerebral Artery Inferction with Lifethreatening Edema Trial [HAMLET]): a multicentre, open, randomized trial. Lancet Neurol 2009; 8(4): 326 – 333. doi: 10.1016/ S1474-4422(09)70047-X.
2. Juráň V, Smrčka M, Svoboda K, Fadrus P, Šprláková A, Gál R. Indikace dekompresivní kraniektomie u traumat mozku. Cesk Slov Neurol N 2009; 72/ 105(5): 439 – 445.
3. Mak C, Lu ZZ, Wong GK. Review and recommendations on management of refractory raised intracranial pressure in aneurysmal subarachnoid hemorrhage. Vasc Health Risk Manag 2013; 9 : 353 – 359. doi: 10.2147/ VHRM.S34046.
4. Esquenazi Y, Savitz SI, ElKhoury R, McIntosh MA, Grotta JC, Tandon N. Decompressive hemicraniectomy with or without clot evacuation for large spontanenous supratentorial intracerebral hemorrhages. Clin Neurol Neurosurg 2015; 128(1): 117 – 122.
5. Pérez-Bovet J, Garcia-Armengol R, Buxo-Pujolras M, Lorite-Díaz N, Narváez-Martínez Y, Caro-Cardera JL et al. Decompressive craniectomy for encephalitis with brain herniation: case report and review of the literature. Acta Neurochir (Wien) 2012; 154(9): 1717 – 1724. doi: 10.1007/ s00701-012-1323-3.
6. Bender A, Heulin S, Rohrer S, Mehrkens JH, Heidecke V, Straube A et al. Early cranioplasty may improve functional outcome in neurological patients with decompressive craniectomy. Brain Injury 2013; 27(9): 1073 – 1079. doi: 10.3109/ 02699052.2013.794972.
7. Buchvald P, Čapek L, Suchomel P. Počítačem modelované náhrady kostních defektů lební klenby. Cesk Slov Neurol N 2009; 72/ 105(2): 169 – 172.
8. Homolková H, Prchlík M. Náhrada defektu kalvy u dítěte po úrazu CNS biokompatibilním materiálem na míru – kazuistika. Cesk Slov Neurol N 2012; 75/ 108(2): 617 – 620.
9. Movassaghi K, Ver Halen J, Ganchi P, Amin-Hanjani S, Mesa J, Yaremchuk MJ. Cranioplasty with subcutaneously preserved autologous bone grafts. Plast Reconstr Surg 2006; 117(1): 202 – 206.
10. Coulter IC, Pesic-Smith JD, Cato-Addison WB, Khan SA, Thompson D, Jenkins AJ et al. Routine but risky: a multi-centre analysis of the outcomes of cranioplasty in the Northeast of England. Acta Neurochir (Wien) 2014; 156(7): 1361 – 1368. doi: 10.1007/ s00701-014-2081-1.
11. Zanaty M, Chalouhi N, Starke RM, Clark SW, Bovenzi CD, Saigh M et al. Complications following cranioplasty: incidence and predictors in 348 cases. J Neurosurg 2015; 123(1): 182 – 188. doi: 10.3171/ 2014.9.JNS14405.
12. Piedra MP, Ragel BT, Dogan A, Coppa ND, Delashaw JB. Timing of cranioplasty after decompressive craniectomy for ischemic or hemorrhagic stroke. J Neurosurg 2013; 118(1): 109 – 114. doi: 10.3171/ 2012.10.JNS121037.
13. Heo J, Park SQ, Cho SJ, Chang JC, Park HK. Evaluation of simultaneous cranioplasty and ventriculoperitoneal shunt procedures. J Neurosurg 2014; 121(2): 313 – 318. doi: 10.3171/ 2014.2.JNS131480.
14. Nalbach SV, Ropper AE, Dunn IF, Gormley WB. Craniectomy-associated Progressive Extra-Axial Collections with Treated Hydrocephalus (CAPECTH): redefining a common complication of decompressive craniectomy. J Clin Neurosci 2012; 19(9): 1222 – 1227. doi: 10.1016/ j.jocn.2012.01.016.
15. Mraček J, Choc M., Mraček Z. Osteoplastická dekompresivní kraniektomie – indikace a operační technika. Rozhl Chir 2010; 89(2): 109 – 112.
16. Mracek J, Hommerova J, Mork J, Richtr P, Priban V. Complications of cranioplasty using a bone flap sterilized by autoclaving following decompressive craniectomy. Acta Neurochir (Wien) 2015; 157(3): 501 – 506. doi: 10.1007/ s00701-014-2333-0.
17. El Ghoul W, Harrisson S, Belli A. Autologous cranioplasty following decompressive craniectomy in the trauma setting. Br J Neurosurg 2014; 29(1): 64 – 69.
18. Gooch MR, Gin GE, Kenning TJ, German JW. Complications of cranioplasty following decompressive craniectomy: analysis of 62 cases. Neurosurg Focus 2009; 26(6): E9. doi: 10.3171/ 2009.3.FOCUS0962.
19. Paredes I, Castaño-León AM, Munarriz PM, Martínez-Perez R, Cepeda S, Sanz R et al. Cranioplasty after decompressive craniectomy. A prospective series analyzing complications and clinical improvement. Neurocirugia (Astur) 2015; 26(3): 115 – 125. doi: 10.1016/ j.neucir.2014.10.001.
20. Tsang AC, Hui VK, Lui WM, Leung GK. Complications of post-craniectomy cranioplasty: risk factor analysis and implications for treatment planning. J Clin Neurosci 2015; 22(5): 834 – 837. doi: 10.1016/ j.jocn.2014.11.021.
21. Wiggins A, Austerberry R, Morrison D, Ho KM, Honeybul S. Cranioplasty with custom-made titanium plates – 14 years experience. Neurosurgery 2013; 72(2): 248 – 256. doi: 10.1227/ NEU.0b013e31827b98f3.
22. Stephens FL, Mossop CM, Bell RS, Tigno T jr, Rosner MK, Kumar A et al. Cranioplasty complications following wartime decompressive craniectomy. NeurosurgFocus 2010; 28(5): E3. doi: 10.3171/ 2010.2.FOCUS1026.
23. Yadla S, Campbell PG, Chitale R, Maltenfort MG, Jabbour P, Sharan AD. Effect of early surgery, material and method of flap preservation on cranioplasty infection: a systematic review. Neurosurgery 2011; 68(4): 1124 – 1129. doi: 10.1227/ NEU.0b013e31820a5470.
24. Chibbaro S, Vallee F, Beccaria K, Poczos P, Makiese O, Fricia M et al. The impact of early cranioplasty on cerebral blood flow and its correlation with neurological and cognitive outcome. Prospective multi-centre study on 24 patients. Rev Neurol (Paris) 2013; 169(3): 240 – 248. doi: 10.1016/ j.neurol.2012.06.016.
25. Jelcic N, della Puppa A, Mottaran R, Cecchin D, Manara R, Dam M et al. Case series evidence for improvement of executive functions after late cranioplasty. Brain Inj 2013; 27(13 – 14): 1723 – 1726. doi: 10.3109/ 02699052.2013.844857.
26. Rish BL, Dillon JD, Meirowsky AM, Caveness WF, Mohr JP, Kistler JP et al. Cranioplasty: a review of 1,030 cases of penetrating head injury. Neurosurgery 1979; 4(5): 381 – 385.
27. Sarov M, Guichard JP, Chibarro S, Guettard E, Godin O, Yelnik A et al. DECIMAL investigators. Sinking skin flap syndrome and paradoxical herniation after hemicraniectomy for malignant hemispheric infarction. Stroke 2010; 41(3): 560 – 562. doi: 10.1161/ STROKEAHA.109.568543.
28. Oh CH, Park CO, Hyun DK, Park HC, Yoon SH. Comparative study of outcomes between shunting after cranioplasty and in cranioplasty after shunting in large concave flaccid cranial defect with hydrocephalus. J Korean Neurosurg Soc 2008; 44(4): 211 – 216. doi: 10.3340/ jkns.2008.44.4.211.
29. Kammersgaard LP, Linnemann M, Tibaek M. Hydrocephalus following severe traumatic brain injury in adults. Incidence, timing and clinical predictors during rehabilitation. NeuroRehabilitation 2013; 33(3): 473 – 480. doi: 10.3233/ NRE-130980.
30. Salunke P, Garg R, Kapoor A, Chhabra R, Mukherjee KK. Symptomatic contralateral subdural hygromas after decompressive craniectomy: plausible causes and management protocols. J Neurosurg 2015; 122(3): 602 – 609. doi: 10.3171/ 2014.10.JNS14780.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2016 Issue 1-
All articles in this issue
- Dynamické metody kvantitativního testování senzitivity
- Komplikace kranioplastik po dekompresivní kraniektomii
- Možnosti terapie pacientů s meningeomem grade III
- Promptní resorpce traumatického akutního subdurálního hematomu – kazuistika
- Neobvyklá příčina spánkové apnoe – kazuistika
- Spinální epidurální lipomatóza – tři kazuistiky
- Konsenzus a návrh k algoritmu léčby – mechanická trombektomie u akutního mozkového infarktu
- Indikace dekompresivní kraniektomie
- Psychické poruchy a kardiovaskulární onemocnění
- Použití optické koherenční tomografie u roztroušené sklerózy
- Pozorovanie hrúbky vrstvy nervových vlákien sietnice u pacientov so sklerózou multiplex pomocou optickej koherentnej tomografie
- Sympatická kožní odpověď v diagnostice neuropatie tenkých vláken
- Kardioembolizace je nejčastější příčinou akutní ischemické cévní mozkové příhody u pacientů přijatých do Komplexního cerebrovaskulárního centra do 12 hodin od začátku příznaků – výsledky studie HISTORY
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Sympatická kožní odpověď v diagnostice neuropatie tenkých vláken
- Pozorovanie hrúbky vrstvy nervových vlákien sietnice u pacientov so sklerózou multiplex pomocou optickej koherentnej tomografie
- Komplikace kranioplastik po dekompresivní kraniektomii
- Indikace dekompresivní kraniektomie
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

