-
Medical journals
- Career
Skrat u karotických endarterektomií zvyšuje riziko ischemického iktu
Authors: M. Orlický 1,2; P. Vachata 1,2; R. Bartoš 1,2; M. Sameš 1
Authors‘ workplace: Neurochirurgická klinika Masarykovy nemocnice a Univerzity J. E. Purkyně, Ústí nad Labem 1; ICRC – Mezinárodní centrum klinického výzkumu, FN u sv. Anny v Brně 2
Published in: Cesk Slov Neurol N 2015; 78/111(2): 163-166
Category: Original Paper
doi: https://doi.org/10.14735/amcsnn2015163Overview
Cieľ:
Rozsiahla prospektívna štúdia porovnávala výskyt nových ischemických lézií zobrazených na magnetickej rezonancii mozgu (difúzne vážený obraz, MR DW) pri karotických endarterektómiách s použitím intraluminálneho skratu a bez neho.Súbor a metodika:
Do prospektívnej štúdie bolo na Neurochirurgické klinice Masarykovy nemocnice v Ústí nad Labem v období od roku 2005 do roku 2013 zaradených 1 019 karotických endarterektomií. Všetky operácie boli v lokálnej anestézii so selektívnym použitím skratu v závislosti na vývoji neurologického stavu po nasadení klipov na karotídu. Vyšetrenie mozgu pomocou MR DW bolo uskutočnené v deň príjmu pacienta k operácii a 24 hod po výkone. Pri hodnotení výskytu a charakteru akútnych ischemickým lézií na MR DW sme používali klasifikáciu publikovanú Szabo et al (Stroke, 2001).Výsledky:
Výskyt významných komplikácií (mozgová príhoda, infarkt myokardu, smrť) bol v skupine symptomatických pacientov 3,2 %, v skupine asymptomatických 1,7 %. Intraluminálny skrat musel byť použitý u 73 zo 1 019 prípadov (7,1 %). Nová ischemická lézia bola detekovaná u 78 pacientov z celej skupiny (7,7 %). Až 80 % týchto lézií bolo klinicky nemých. V podskupine pacientov s použitím skratu sme novú ischemickú léziu zaznamenali v 25 prípadoch (34,3 %), v skupine bez použitia skratu len v 53 prípadoch (5,6 %) – štatisticky významný rozdiel. Väčšina nových lézií bola charakteru embolizačných či hypoperfúznych.Záver:
Použitie intraluminálneho skratu pri CEA zvyšuje výskyt nových ischemických lézií na MR DW mozgu až sedemkrát. Tento výsledok významne podporuje našu stratégiu selektívneho používania intraluminálneho skratu pri CEA.Klíčová slova:
karotická endarterektómia – použitie intraluminálneho skratu – cievná mozgová príhodaÚvod
Prínos karotickej endarterektómie (CEA) v znížení rizika ischemickej cievnej mozgovej príhody bol už overený v známych veľkých štúdiách [1 – 5].
Vlastný chirurgický výkon s uzavretím karotídy nasadením dočasných klipov v oblasti bifurkácie na druhej strane vnáša do výkonu riziko periprocedurálnej ischemickej mozgovej príhody. Trombo ‑ embolické príhody pri vlastnej preparácii cievy a nedostatočná perfúzia mozgu pri nasadení dočasných klipov sú považované za hlavné príčiny tejto komplikácie. Premostenie svorkami uzavretých častí karotídy skratom (shuntom) s minimalizovaním času prerušeného zásobenia mozgu z danej cievy na jednej strane znižuje riziko inadekvátnej perfúzie, na strane druhej nie je bezrizikové. Poškodenie cievnej steny pri zavádzaní skratu, drobné krvné zrazeniny v priebehu skratu a embolizácia poškodenej cievnej steny či zmienených koagúl hrozia opäť vznikom ischemickej mozgovej príhody [6,7].
Nejednoduchej otázke indikovania a používania karotického skratu sa venuje nemálo článkov a štúdií. Niektoré podporujú stratégiu rutinného zavádzania skratu, iné nepoužívajú skrat vôbec, v ďalších je dôraz na selektívne používanie skratu [8 – 14]. Jednotný názor na rutinné alebo selektívne skratovanie zatiaľ ale žiadna štúdia neobhájila.
V článku na našom rozsiahlom súbore pacientov, ktorí podstúpili CEA, hodnotíme riziko vzniku periprocedurálnej ischemickej mozgovej príhody pri použití skratu a bez neho a na základe získaných výsledkov doporučujeme selektívne používanie karotického skratu pri karotických endarterektomiách.
Súbor a metodika
V období rokov 2005 – 2013 bolo na Neurochirurgické klinice Masarykovy nemocnice v Ústí nad Labem prevedených 1 080 CEA. Indikácie boli v súlade s aktuálnymi odporučeniami štúdií NACSET, ACST, ECST [1 – 5].
Do štúdie bolo zaradených 1 019 endarterektomií. Do štúdie nebolo zaradených 61 ostatných prípadov s kontraindikáciou k vyšetreniu MR alebo klaustrofóbiou.
Všetky výkony prebiehali v regionálnej anestézii (blok cervikálneho plexu) so selektívnym použitím karotického skratu na základe vývoja neurologického stavu hodnoteného v priebehu uzavretia karotídy svorkami (podľa postupnosti: arteria thyroidea superior, arterial carotis externa (ACE), communis (ACC) a interna (ACI)). Magnetickú rezonancia mozgu (v sekvenciách T2, DW b0, b500, b1000, ADC) podstúpil každý pacient približne 24 hod pred výkonom a po ňom a prítomnosť akútnych ischemických ložisiek bola hodnotená podľa klasifikácie autorov Szabo et al [15]. Grafický nález hodnotili nezávisle rentgenológ a neurochirurg (prvý autor). Pri ich nezhode hodnotenie doplnil ďalší neurochirurg (druhý autor).
Vývoj neurologického stavu hodnotil anestéziológ podľa predefinovanej schémy, v priebehu a po uzavretí karotídy svorkami. Hodnotil sa vývoj kvali - i kvantitatívneho stavu vedomia, reč, motorika kontralaterárnych končatín. Akékoľvek zhoršenie uvedených viedlo k okamžitému zavedeniu skratu.
Výsledky sme hodnotili štatisticky využitím chí kvadrát analýzy. Štúdiu sme viedli prospektívne, nerandomizovane, zaslepene.
Výsledky
- Z 1 019 endarterektomií zahrnutých do štúdie bolo 584 prípadov (57 %) asymptomatických, 435 (43 %) symptomatických.
- Intraluminálny skrat musel byť použitý u 73 z 1 019 prípadov (7,1 %).
- Nová ischemická lézia bola detekovaná v 78 prípadoch z celej skupiny (7,7 %).
- Až 80 % týchto lézii bolo klinicky nemých. V podskupine pacientov s použitím skratu sme novú ischemickú léziu zaznamenali v 25 prípadoch (34,3 %), v skupine bez použitia skratu len v 53 prípadoch (5,6 %). Rozdiel je štatisticky významný (p < 0,001).
- Z 25 spomenutých nových ischemických lézií v podskupine so skratom, 13 (52 %) spadalo do kategórie 4 podľa Szabo – embolizačná etiológia, a sedem (28 %) do kategórie 5 podľa Szabo et al – hypoperfúzna etiológia využitím klasifikácie podľa Szaboa et al; tab. 1 [15].
Table 1. Zastúpenie nových ischemických lézií na MR DW mozgu v skupine endarterektomií so skratom, podľa Szabo et al [15], n = 25. ![Zastúpenie nových ischemických lézií na MR DW mozgu v skupine endarterektomií so skratom, podľa Szabo et al [15], n = 25.](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/4808fccc1d19fffc0aae777d02ebee65.png)
- Z 53 nových ischemických lézií v podskupine bez skratu sme rovnakou klasifikáciou do kategórie 4 – embolizačná etiológia – zaradili 24 prípadov (45,3 %), do kategórie 5 – hypoperfúzna etiológia – 20 prípadov (37,7 %); tab. 2 [15].
Table 2. Zastúpenie nových ischemických lézií na MR DW mozgu v skupine endarterektomií bez skratu, podľa Szabo et al [15], n = 53. ![Zastúpenie nových ischemických lézií na MR DW mozgu v skupine endarterektomií bez skratu, podľa Szabo et al [15], n = 53.](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/6402ce67b2632d0364936b790b698503.png)
- Výskyt závažných komplikácií (mozgová príhoda, infarkt myokardu, smrť) bol v skupine so skratom až 7,3 %, v skupine bez skratu 2,6 %. Výskyt menej závažných komplikácií bol v skupine so skratom 7,3 %, bez skratu 4,9 %; tab. 3.
Table 3. Zastúpenie komplikácii v skupinách s a bez použitia skratu. 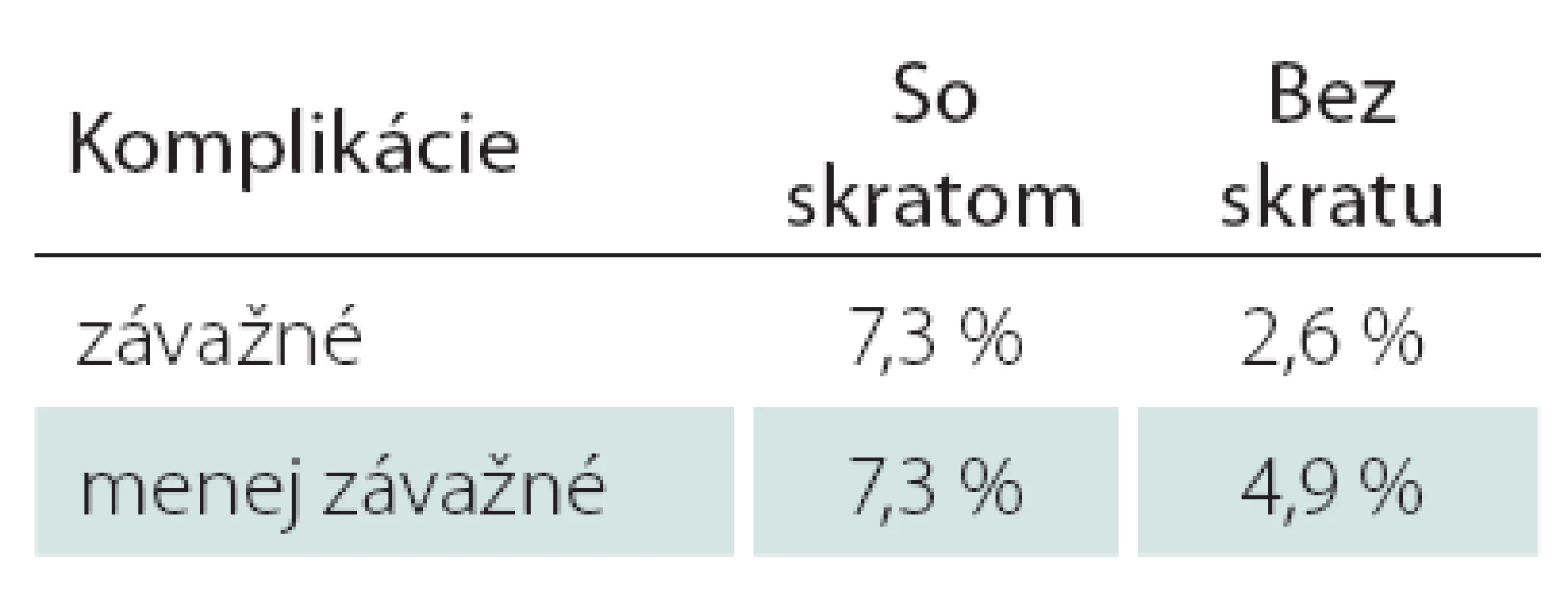
- Podiel závažných komplikácií bol u symptomatických pacientov 3,2 %, v skupine asymptomatických 1,7 %.
Diskusia
Od roku 1953, keď doktor Michael DeBakey previedol v Houstone prvú karotickú endarterektómiu [16], stále nie sú vyriešené niektoré dôležité otázky. V článku riešená indikácia použitia karotického skratu je jednou z nich. Prístupy s rutinným používaním či naopak striktným nepoužívaním, tak aj selektívne používanie skratu sú všeobecne akceptované a v literatúre popisované ich výhody a nevýhody. Všetky prístupy majú spoločnú myšlienku – minimalizovať periprocedurálne komplikácie. Jednou z najvýznamnejších periprocedurálnych komplikácií CEA je ischemická mozgová príhoda. Tejto problematike sa recentne venovala subštúdia v rámci International Carotid Stenting Study (ICSS), ktorá porovnávaním pred ‑ a pooperačných nálezov na MR DW mozgu ukázala až 17% podiel nových ischemických lézií po CEA u symptomatických pacientov [17]. Etiológia periprocedurálnej ischemickej mozgovej príhody je hypoperfúzna alebo embolizačná.
Riziko hypoperfúzie znížime použitím karotického skratu, ktorý obnoví prietok distálnou vnútornou karotídou krátko po jej uzavretí svorkou. Na druhej strane tento proces má inú potencionálnu komplikáciu – periprocedurálnu ischemickú mozgovú príhodu embolizačnej etiológie.
Ak sa zameriame na indikácie zavedenia skratu v skupine jeho selektívneho používania, zistíme, že pre operácie vedené v celkovej anestézií je v literatúre popísaných niekoľko monitorovacích metód a im odpovedajúce indikácie. Pre operácie vedené v regionálnej anestézii s precíznym sledovaním neurologického stavu je jeho relevantné zhoršenie indikáciou pre použitie skratu. V literatúre sa spomína i prebudenie pacientov z celkovej anestézie k zhodnoteniu neurologického stavu po uzavretí karotídy s opätovným uvedením do celkovej anestézie pre ďalšiu časť výkonu [9].
Či už otázku okrajovo zmienenej celkovej vs regionálnej anestézie, tak i aktuálnu otázku použitia skratu zatiaľ nevyriešili ani veľké multicentrické štúdie, resp. ich metaanalýzy [8].
V článku preto prezentujeme náš názor na používanie skratu pri karotických endarterektomiách opierajúci sa o naše výsledky veľkej prospektívnej štúdie.
Ako už bolo zmienené, všetky operácie – CEA – boli vedené v regionálnej anestézii, rozhodnutie o použití skratu záviselo na vývoji neurologického stavu po uzavretí karotídy svorkou. Z 1 019 CEA vyžadovalo 73 (7,16 %) použitie skratu. Po operácii vyšetrenie neurologického stavu a MR mozgu mali odhaliť nové čerstvé ischemické ložiská. Samostatné hodnotenie neurologického stavu odhalilo len 20 % zo 78 prípadov novej ischemickej lézie zistenej na MR mozgu. Inak povedané, len 20 % nových ischemických lézií bolo symptomatických.
Zo všetkých nových ischemických lézií (78), zistený rozdiel – 25 prípadov (34,3 %) v podskupine so skratom a 53 prípadov (5,6 %) v neskratovanej skupine je štatisticky významný pri p < 0,001.
Tieto výsledky presvedčivo ukazujú, že použitie skratu pri operácii zvyšuje riziko novej ischemickej lézie až sedemkrát. Môžeme si tiež všimnúť, že počet všetkých závažných komplikácií v skupine so skratom je daný hlavne podielom nových klinických ischemických príhod v tejto skupine – 7,3 % vs 6,8%.
Ďalej, v podskupine endarterektomií so skratom sme napočítali 13 (52 %) lézií embolizačného charakteru (kategória Szabo 4) proti siedmim (28 %) hypoperfúzneho charakteru (kategória Szabo 5). V podskupine bez použitia skratu bol počet prípadov v kategórii Szabo 4 a 5 prakticky rovnaký (24 a 20 prípadov).
Tieto výsledky naznačujú, že poškodenie aterosklerotickej cievnej steny a embolizácia odlúčenej intimy alebo trombu je najčastejšou príčinou nových ischemických lézií pri použití skratu.
Zaujímavým zistením v podskupine bez skratu je nález 20 prípadov novej ischemickej lézie hypoperfúzneho charakteru (kategória Szabo 5) na MR DW mozgu (2 % zo všetkých CEA). Všetci títo pacienti boli klinicky asymptomatickí v priebehu operácie i následne. Môžeme odvodiť, že ani precízne sledovanie neurologického stavu po uzavretí karotídy nie je 100% senzitívne. Na druhej strane počet týchto falošne negatívnych prípadov je veľmi nízky v porovnaní so senzitivitou iných metód používaných v indikáciách skratu [7,12 – 14].
Ďalším zaujímavým zistením je, že i v podskupine so skratom nájdeme hypoperfúzny charakter nových ischemických lézií (28 %, sedem prípadov). Šiesti z týchto pacientov sa neurologicky zhoršili po uzavretí karotídy v rámci sekúnd s časným a plným obnovením stavu po zavedení skratu. Zavádzanie skratu bolo nekomplikované. V jednom prípade bol test pri uzavretí karotídy negatívny a operácia začala bez skratu. Niekoľko minút po arterotomii viedol prudší pokles krvného tlaku (veľmi pravdepodobne farmakologického pôvodu) k strate vedomia. Zavedenie skratu a obnovenie krvného tlaku nezlepšilo stav vedomia a operácia sa dokončila v endotracheálnej anestézii. Časne po operácii sa pacient prebudil bez neurologického deficitu.
Po prehodnotení tejto skupiny pacientov usudzujeme, že i časné a nekomplikované zavedenie skratu môže viesť k hypoperfúzii mozgu – v našom prípade našťastie klinicky asymptomatickej. V etiológii predpokladáme insuficientné kolaterálne riečište; tab. 4.
Table 4. Skupina endarterektomií so skratom a novou léziou hypoperfúznej etiologie. 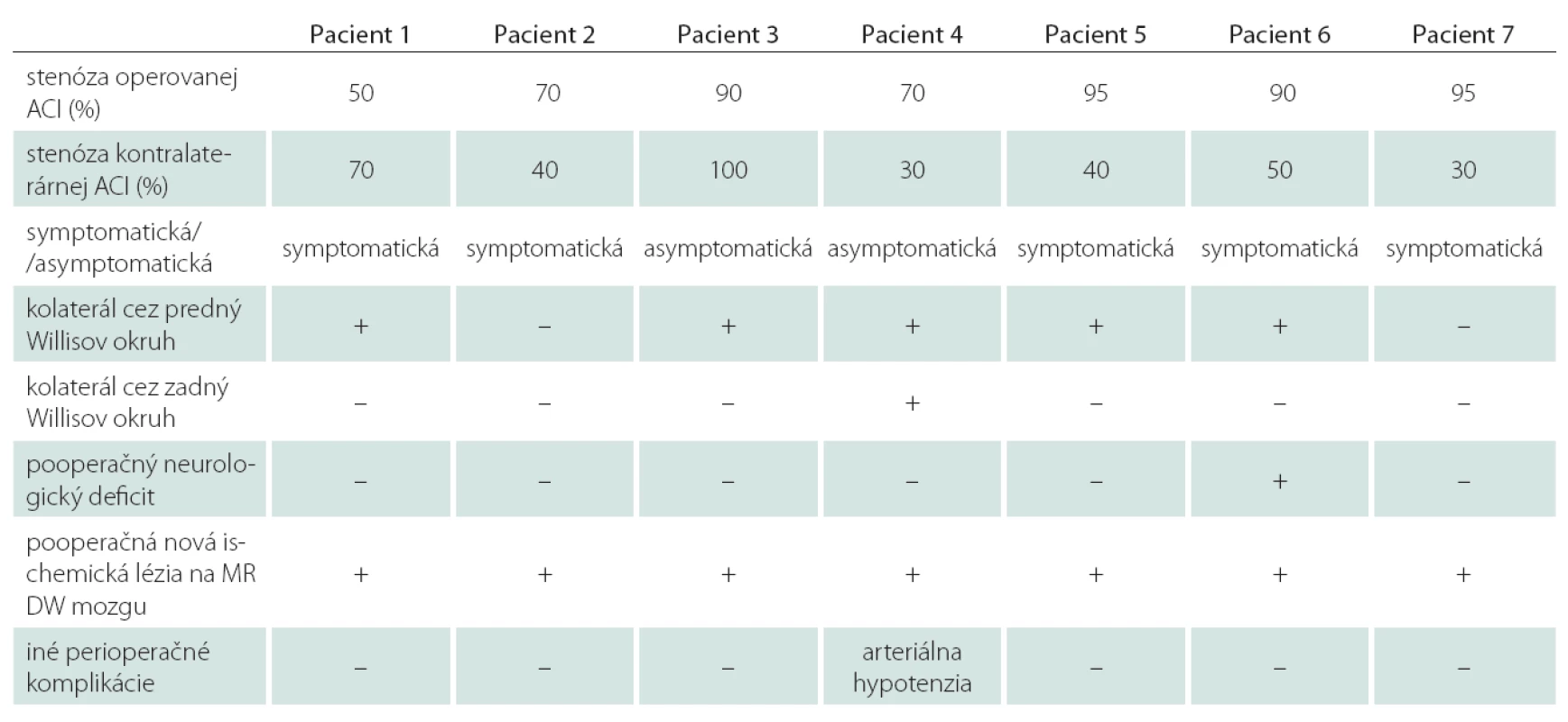
Záver
Použitie intraluminálneho skratu pri CEA zvyšuje riziko nových ischemických lézií mozgu až sedemkrát. Tento výsledok významne podporuje našu stratégiu selektívneho používania intraluminálneho skratu pri CEA.
Práca nebola podporená grantom.
Prijaté k recenzii: 1. 10. 2014
Prijaté do tlače: 13. 1. 2015
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Michal Orlický
Neurochirurgická klinika
Masarykova nemocnice
Sociální péče 12A
401 13 Ústí nad Labem
e-mail: orlicky@gmail.com
Sources
1. Arazi HC, Capparelli FJ, Linetzky B. Carotid endarterectomy in asymptomatic carotid stenosis: a decision analysis. Clin Neurol Neurosurg 2008; 110(5): 472 – 479. doi: 10.1016/ j.clineuro.2008.02.012.
2. Rothwell PM, Goldstein LB. Carotid endarterectomy for asymptomatic carotid stenosis asymptomatic carotid surgery trial. Stroke 2004; 35(10): 2425 – 2427.
3. Endarterectomy for asymptomatic carotid artery stenosis. Executive committee for the asymptomatic carotid atherosclerosis study. JAMA 1995; 273(18): 1421 – 1428.
4. Randomised trial of endarterectomy for recently symptomatic carotid stenosis: final results of the MRC European Carotid Surgery Trial (ECST). Lancet 1998; 351(9113): 1379 – 1387.
5. Ferguson GG, Eliasziw M, Barr HW, Clagett GP, Barnes RW,Wallace MC et al. The North American Symptomatic Carotid Endarterectomy Trial: surgical results in 1,415 patients. Stroke 1999; 30(9): 1751 – 1758.
6. Gumerlock MK, Neuwelt EA. Carotid endarterectomy: to shunt or not to shunt. Stroke 1988; 19(12): 1485 – 1490.
7. Michaelides C, Nguyen TN, Chiappa KH. Cerebral embolism during elective carotid endarterectomy treated with tissue plasminogen activator: utility of intraoperative EEG monitoring. Clin Neurol Neurosurg 2010; 112(5): 446 – 449. doi: 10.1016/ j.clineuro.2010.01.009.
8. Rerkasem K, Rothwell PM. Routine or selective carotid artery shunting for carotid endarterectomy (and different methods of monitoring in selective shunting). Cochrane Database Syst Rev 2009; 7(4): CD000190. doi: 10.1002/ 14651858.CD000190.pub2.
9. Cho J, Lee KK, Yun WS. Selective shunt during carotid endarterectomy using routine awake test with respect to a lower shunt rate. J Korean Surg Soc 2013; 84(4): 238 – 244. doi: 10.4174/ jkss.2013.84.4.238.
10. Rerkasem K, Rothwell PM. Routine or selective carotid artery shunting for carotid endarterectomy and different methods of monitoring in selective shunting. Stroke 2010; 41 : 53 – 54.
11. Evans WE, Hayes JP, Waltke EA. Optimal cerebral monitoring during carotid endarterectomy: neurologic response under local anesthesia. Journal of Vascular Surgery 1985; 2 : 775 – 777.
12. Cao P, Giordano G, Zannetti S, De Rango P, Maghini M,Parente B et al. Transcranial Doppler monitoring during carotid endarterectomy: is it appropriate for selecting patients in need of a shunt? J Vasc Surg 1997; 26(6): 973 – 980.
13. Ali AM, Green D, Zayed H. Cerebral monitoring in patients undergoing carotid endarterectomy using a triple assessment technique. Interact CardioVasc Thorac Surg 2011; 12(3): 454 – 457. doi: 10.1510/ icvts.2010.235598.
14. Ricotta JJ, Charlton MH, DeWeese JA. Determining criteria for shunt placement during carotid endarterectomy. EEG versus back pressure. Ann Surg 1983; 198(5): 642 – 645.
15. Szabo K, Kern R, Gass A, Hirsch J, Hennerici M. Acute stroke patterns in patients with internal carotid artery disease: a diffusion ‑ weighted magnetic resonance imaging study. Stroke 2001; 32(6): 1323 – 1329.
16. DeBakey ME. Successful carotid endarterectomy for cerebrovascular insufficiency. Nineteen-year follow-up. JAMA 1975; 2233(10): 1083–1085.
17. Bonati LH, Jongen LM, Haller S, Flach HZ, Dobson J,Nedorkoorn PJ et al. New ischaemic brain lesions on MRI after stenting or endarterectomy for symptomatic carotid stenosis: a substudy of the International Carotid Stenting Study (ICSS). Lancet Neurol 2010; 9 : 353 – 362. doi: 10.1016/ S1474 ‑ 4422(10)70057 ‑ 0.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2015 Issue 2-
All articles in this issue
- Progredující demence s parkinsonizmem a poruchami chování – od prvních příznaků k neuropatologické diagnóze (kazuistika)
- Kongenitální centrální hypoventilační syndrom (Ondinina kletba)
- Neurologická komplikace hepatitidy E – kazuistika
- Neurologické projevy Behçetovy nemoci – kazuistika
- Úspešne liečená depresia u pacienta s epilepsiou – kazuistika
- Zánětlivý pseudotumor imitující intrakraniální, konvexitární meningeom – kazuistika
- Neuromyelitis optica
- Radiologické hodnocení lumbální spinální stenózy a jeho klinická korelace
- Agresivní hemangiom obratle
- Použití antipsychotik u nemocných s demencí
- Skrat u karotických endarterektomií zvyšuje riziko ischemického iktu
- Chirurgická léčba laterální bederní stenózy perkutánně zavedeným interspinózním implantátem
- Chirurgický přístup k tumorům thalamu
- Možnosti ovlivnění diplopie při paralytickém strabizmu konzervativní léčbou
- Dotazník funkcionální komunikace (DFK) – validace originálního českého testu
- Penilní vibrostimulace u pacientů s míšním poraněním
- Registr mechanických rekanalizací u akutního iktu – pilotní výsledky multicentrického registru
- Rozdiely medzi pohlaviami v klinických prejavoch a výskyte porúch spánku u pacientov s Parkinsonovou chorobou – populačná štúdia
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Agresivní hemangiom obratle
- Neuromyelitis optica
- Kongenitální centrální hypoventilační syndrom (Ondinina kletba)
- Radiologické hodnocení lumbální spinální stenózy a jeho klinická korelace
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

