-
Medical journals
- Career
Úloha predoperačného časového intervalu pri liečbe diskogenného syndrómu caudae equinae
Authors: I. Lukáč; I. J. Šulla
Authors‘ workplace: Neurochirurgická klinika LF UPJŠ a FNLP Košice
Published in: Cesk Slov Neurol N 2010; 73/106(5): 523-528
Category: Original Paper
Overview
Syndroma caudae equinae (SCE) je ochorenie prevažne produktívneho veku, často s vážnymi následkami. Autori prehodnotili súbor 101 pacientov liečených pre SCE za obdobie 12 rokov (1996–2007) a sledovali u nich dynamiku rozvoja príznakov podľa etiológie. Pacientov s diskogénnym SCE minimálne rok po skončení liečenia, kedy ich zdravotný stav už bol ustálený, pozvali na kontrolné vyšetrenie a skúmali u nich vplyv predoperačného časového intervalu, t.j. doby od vzniku ťažkostí po chirurgické uvoľnenie nervových štruktúr na nasledujúce ukazovatele: pretrvávanie bolesti, úpravu citlivosti, sfinkterových porúch a motorických funkcií. Na základe získaných poznatkov zo súboru 68 pacientov s diskogénnym SCE, ktorí sa podrobili kontrolnému vyšetreniu alebo odpovedali dotazníkom z celkového počtu 101 pacientov, po štatistickom spracovaní χ2 (chí kvadrát) testom a v prípade, kde boli hodnoty menšie alebo rovné 5, bol použitý Fisherov exaktný test, autori konštatujú, že predoperačný časový interval v skúmanom súbore u diskogénnych SCE nemal vplyv na konečný výsledok liečby. Naopak predoperačný časový interval závisel od príčiny vzniku SCE, najkratší je u pacientov s voľným sekvestrom a veľkými herniami intervertebrálnych diskov v spinálnom kanáli. Pomalšie sa SCE rozvíja pri stenózach spinálneho kanála a najpomalšie pri nádoroch.
Kľúčové slová:
syndrom caudae equinae – timing operácieÚvod
Syndróm konského chvosta (syndroma caudae equinae, SCE) je charakterizovaný poruchou taktilnej citlivosti v oblasti pohlavných orgánov, okolia konečníka, vnútorných plôch stehien, lýtok a nôh (hypestéza až anestéza typu jazdeckých nohavíc), pálčivými bolesťami v inervačných zónach postihnutých miechových koreňov, slabosťou až ochrnutím dolných končatín, oslabením až vymiznutím príslušných reflexov, neschopnosťou ovládať vyprázdňovanie močového mechúra, stolice a poruchou sexuálnych funkcií. Sfinkterové poruchy sa môžu prejaviť v zmysle retencie moču alebo inkontinencie, resp. vo forme ischuria paradoxa. Asi v 60–80 % býva znížený až vymiznutý tonus análneho sfinktera. Klinický stav sa podobá stavu pri poškodení conus medullaris. Príznaky môžu byť asymetrické, nemusia sa vyvinúť v úplnej popísanej podobe u každého pacienta [1].
Syndróm miechoveho konu a epikonu je veľmi podobný, ľahko môže dôjsť k zámene. Klinický obraz obsahuje chabú paraparézu s postihnutím sfinkterov, senzitívne postihnutie je variabilné, perianogenitálna citlivosť môže byť čiastočne zachovaná. V chronickej faze dochádza k spasticite a atrofii svalov, môže sa vyvinúť aj autonomný mechúr. Naopak, SCE má jednostrannú prevahu postihnutia, zatiaľ čo syndróm epikonu a konu má príznaky symetrické.
Materiál a metóda
Súbor tvorí 101 pacientov (38 žien a 63 mužov), ktorí boli operovaní a liečení na Neurochirurgickej klinike UPJŠ LF a FNLP Košice za obdobie 12 rokov (1996–2007). Opakovane boli prehodnotené písomné záznamy vrátane dostupnej rtg, CT a MR dokumentácie, ďalej operačné nálezy, klinický stav pri prijatí a po prepustení z neurochirurgickej kliniky. Členovia sledovaného súboru sa podrobili kontrolnému vyšetreniu minimálne rok od operácie, kedy ich zdravotný stav bol už stabilizovaný. V prípade, že sa na vyšetrenie nedostavili, odpovedali na priložený dotazník. Zisťovali sme u nich:
- predoperačný časový interval v závislosti od etiológie SCE
- výskyt bolesti
- poruchy taktilnej citlivosti perianogenitálne a na dolných končatinách
- motorickú funkciu na DK – mobilitu
- sfinkterové poruchy:
a) močenie
b) stolica - následky SCE v sexuálnej oblasti.
Absolútne početnosti výskytu jednotlivých parametrov sme hodnotili χ2 (chí kvadrát) testom a v prípade, kde boli výskyty menšie alebo rovné 5, bol použitý Fisherov exaktný test. Za významné považujeme rozdiely na hladine významnosti p < 0,05.
Výsledky
Súbor pozostáva zo 101 pacientov operovaných pre SCE rôznej etiológie za uvedené obdobie 12 rokov. Z toho bolo 63 mužov vo veku od 26 do 83 rokov, priemerný vek 47,6 roka. Vekové rozpätie 38 žien bolo od 29 do 75 rokov, priemerný vek 47,9 rokov.
Okrem najčastejšej – diskogénnej, príčiny vzniku SCE sme našli aj SCE zriedkavej etiológie (tab. 1). Pri podrobnejšej analýze súboru podľa etiológie sme okrem počtu pacientov sledovali aj priemerný čas, ktorý uplynul od začiatku ťažkostí po samotnú operáciu, t.j. predoperačný časový interval. Ukazuje sa, že sa príznaky SCE najrýchlejšie rozvíjali v prípadoch, kde kompresia nervových štruktúr bola zapríčinená voľným sekvestrom intervertebrálneho disku v spinálnom kanáli alebo veľkou herniou intervertebrálneho disku. Naopak najpomalší vývoj príznakov bol u pacientov s nádorom alebo so stenózou spinálneho kanála.
Table 1. Dynamika rozvoja SCE v závislosti od etiológie SCE. 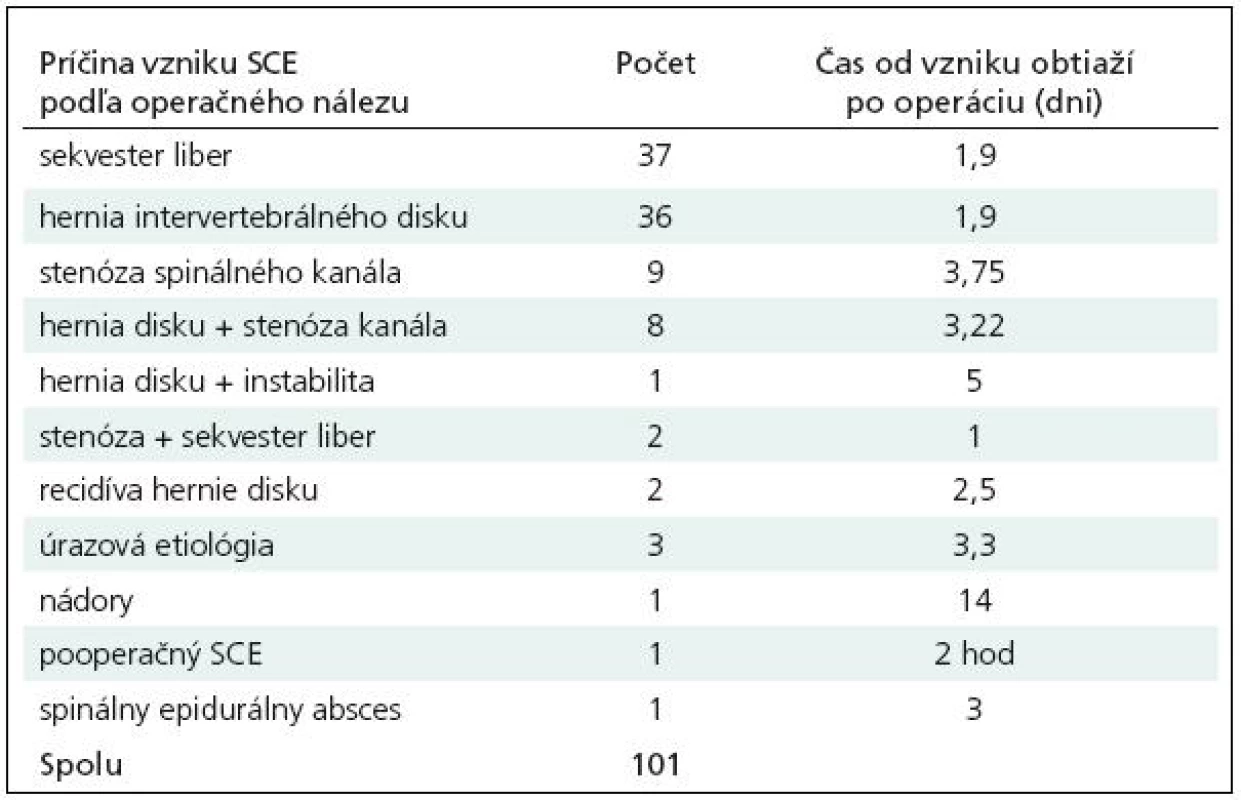
SCE zriedkavej etiológie neboli pre malý počet ďalej hodnotené. V ďalšom sme skúmali len diskogénne SCE.
Na kontrolné vyšetrenie z celého súboru 95 pacientov operovaných pre SCE diskogénneho, resp. vertebrogéneho pôvodu zozbieraného za 12 rokov prišlo celkove 31 pacientov. Všetci ostatní mali zaslaný priložený dotazník, v ňom na položené otázky odpovedali zakrúžkovaním najvhodnejšej odpovede. Vrátilo sa nám 32 vyplnených dotazníkov. Dodatočne prišlo na kontrolné vyšetrenie päť pacientov. Celkove sme teda získali údaje o zdravotnom stave od 68 pacientov. U nich sme sledovali vplyv predoperačného časového intervalu na úpravu už spomínaných ukazovateľov.
1. Úprava citlivosti v závislosti od predoperačného časového intervalu
Pri kontrolnom vyšetrení sme sledovali úpravu, resp. pretrvávanie porúch taktilnej citlivosti perianogenitálne a na DK. Získané poznatky uvádza graf 1.
Graph 1. Obnova citlivosti v závislosti od trvania ťažkosti pred operáciou. 
Záver: Nepotvrdil sa štatisticky významný rozdiel medzi trvaním ťažkostí a úpravou citlivosti.
2. Pretrvávanie bolesti v závislosti od predoperačného časového intervalu
Pacienti boli rozdelení podľa toho, či pociťujú bolesti niekedy, stále alebo bolesti nemajú (graf 2).
Graph 2. Vzťah medzi ústupom bolesti a trvaním ťažkostí pred operáciou. 
Záver: Nepotvrdil sa štatisticky významný rozdiel medzi pretrvávaním bolesti a trvaním ťažkostí pred operáciou. Hodnotenie bolo urobené pomocou Fisherovho exaktného testu.
3. Úprava motoriky v závislosti od predoperačného časového intervalu
Pacienti boli delení do nasledujúcich skupín (graf 3):
- motorický nález bol v norme
- ľahký deficit, nepostojí na špičke alebo päte, chodí bez pomoci
- stredný motorický deficit: chodí s pomocou barlí
- ťažký motorický deficit: neschopný chôdze.
Graph 3. Vzťah medzi trvaním ťažkostí pred operáciou a obnovou motoriky. 
Záver: Vzhľadom k malým počtom pacientov v jednotlivých skupinách sa nepotvrdil štatisticky významný vplyv trvania ťažkostí na úpravu motoriky.
4. Úprava močenia a stolice v závislosti od predoperačného časového intervalu
Získané poznatky udávajú grafy 4 a 5.
Graph 4. Úprava močenia v závislosti od trvania ťažkostí pred operáciou. 
Graph 5. Ovládanie stolice v závislosti od trvania obtiaží pred operáciou. 
Záver: Trvanie ťažkostí nemá štatisticky významný vplyv na obnovu močenia a stolice.
5. Úprava sexuálnych funkcií v závislosti od predoperačného časového intervalu
Pacientov sme rozdelili do troch skupín:
- bez následkov v sexuálnej oblasti
- zhoršenie, ale nie strata sexuálnych funkcií
- strata sexuálnych funkcií.
Úpravu sexuálnych funkcií u mužov a žien v závislosti od trvania ťažkostí pred operáciou ukazuje tab. 2.
Table 2. Obnova sexuálnych funkcií v závislosti od trvania ťažkostí pred operáciou. 
Záver: Štatisticky sa nepotvrdil vplyv trvania ťažkostí na obnovu sexuálnych funkcií u mužov a žien spolu. Pre celkove malý počet pacientov nebolo možné urobiť štatistické analýzy osobitne v podskupinách mužov a žien.
Na základe vyššie uvedených zistení možno konštatovať, že akútnosť stavu pri SCE vo všeobecnosti závisí od príčiny. Najakútnejší priebeh má pri voľných sekvestroch v spinálnom kanáli a pri veľkých herniách intervertebrálnych diskov, teda pri diskogénnych SCE, naopak najpomalší pri výrazných stenózach spinálneho kanála a pri nádoroch.
Získané štatistické spracovanie výsledkov poukazuje na to, že predoperačný časový interval u diskogénneho SCE nemá vplyv na výsledok liečby. Treba však pripomenúť, že sledovaní pacienti boli operovaní 16 a viac hodín od začiatku ťažkostí. Príčinu tejto skutočnosti vidíme v relatívnej ťažšej dostupnosti CT a MR vyšetrenia v minulosti, časovou stratou pri transporte chorého, podceňovaním prvých príznakov ochorenia zo strany pacienta i v neskorom odosielaní chorého na špecializované pracovisko.
Diskusia
Vo všeobecnosti syndróm konského chvosta (SCE) môže začať náhle z plného zdravia ako SCE I typu (podľa Tandoma a Sankarana), častejšie vzniká po predchádzajúcich epizódach bolestí v krížoch, resp. lumboischiadického syndrómu. Stav sa však môže náhle zmeniť a v priebehu niekoľkých minút sa vyvinie SCE typu II. Inokedy začína postupne v priebehu dní až týždňov – SCE typ III [2–4].
Podľa našich skúseností urgentnosť príznakov, ktoré nútia pacienta vyhľadať lekára, závisí vo veľkej miere od etiológie SCE. Práve závažnosť ťažkostí je rozhodujúcim faktorom, ktorý najviac ovplyvňuje predoperačný časový interval, teda dobu od vzniku ťažkostí po operáciu. Pri jeho posudzovaní musíme pamätať na to, že okrem akútnosti stavu, ktorý je rozhodujúcim činiteľom, sú tu aj ďalšie objektívne príčiny, napr. vzdialenosť pacienta od špecializovaného pracoviska, dostupnosť CT, resp. MR vyšetrenia a podobne. Subjektívne príčiny, podceňovanie príznakov, rozličný prah bolesti, môžu tiež predĺžiť predoperačný časový interval.
V skúmanom súbore najkratší predoperačný časový interval okrem pooperačného syndrómu kaudy bol u pacientov s voľným sekvestrom v spinálnom kanáli a pri veľkých herniách intervertebrálnych diskov. Najdlhší bol u pacienta s nádorom ossis sacri, o niečo kratší pri stenózach spinálneho kanála. Je pozoruhodné, že u ďalších štyroch pacientov s rozsiahlymi tumormi v oblasti ossis sacri sa príznaky SCE nevyvinuli.
Uvedené fakty stoja za zamyslenie. V experimentálnych prácach sa uvádza, že epidurálna aplikácia štepu z autologného nucleus pulposus má negatívny vplyv na nervové tkanivo v zmysle morfologických a funkčných zmien, ako napr. intracelulárny edém, edém axónov, signifikantné štrukturálne zmeny, spomalenie rýchlosti vedenia vzruchov a podobne [5,6]. Je teda možné, že práve tieto skutočnosti spolu so samotnou kompresiou koreňov vysvetľujú, prečo voľné sekvestre v spinálnom kanáli alebo veľké hernie intervertebrálnych diskov nútia pacienta vyhľadať pomoc skôr.
Stenóza spinálneho kanála môže byť tiež príčinou vzniku SCE. Experimentálne práce na zvieratách ukázali, že pri zužovaní priečneho priemeru spinálneho kanála dochádza k stúpaniu tlaku medzi koreňmi konského chvosta. Pritom sa pozoroval rozvoj neurologickej symptomatológie v podobe slabosti zadných končatín, inkontinencie, paralýzy chvosta. Zaznamenali aj zmeny až vymiznutie evokovaných potenciálov. U týchto zvierat ďalej zistili blokádu axonového prúdenia, Walerovu degeneráciu motorických koreňov distálne od miesta konstrikcie, senzitívnych dráh proximálne od miesta poškodenia. Stenóza sa negatívne prejavila aj v cirkulácii. Udáva sa zúženie ciev v mieste kompresie a rozširovanie žíl [7].
Príznaky boli tým výraznejšie, čím bola stenóza väčšia, stupeň poškodenia tiež závisel na rýchlosti rozvoja stenózy. Akútne navodená stenóza je menej priaznivá, podobne sa javila aj stenóza na viacerých úrovniach [8,9].
Naopak pri tumoroch majú korene konského chvosta čas prispôsobiť sa novým podmienkam a príznaky SCE sa vyvíjajú pomaly alebo až veľmi neskoro.
V literatúre pokračuje polemika týkajúca sa urgentnosti operácie (timing). Názory sa značne líšia. Hoci logická úvaha vedie k záveru, že výsledky by mali byť priaznivejšie pri včasnejšom zrušení tlaku na LS miechové korene, skúsenosti niektorých autorov ukazujú, že čas operácie pravdepodobne výrazne neovplyvní výsledok liečby [10–12]. Experimentálne práce hovoria o nutnosti operovať do štyroch hodín [13,14], iní lekári do šiestich hodín [15], ďalší nevidia rozdiel medzi urgentnou a odloženou operáciou [11,12]. Tolerovanou hranicou je 48 hodín [16]. V literatúre nechýba ani taký optimistický názor, že pri operáciach do 48 hodín od vzniku ťažkostí dochádza k úprave neurologického deficitu skoro až u 100 % pacientov [17]. Naopak pri operácii po 48 hodinách úprava neurologických príznakov klesá až o 70 %.
V našom súbore sme vplyv predoperačného časového intervalu, teda času od vzniku ťažkostí po operáciu na pretrvávanie bolesti, úpravu citlivosti, sfinkterových porúch a sexuálnych funkcií v pooperačnom období nezistili. Treba však pripomenúť, že naši pacienti boli operovaní pri predoperačnom časovom intervale prevažne 16 a viac hodín, iba ojedinele pod touto hranicou. Ukazuje sa, že za uvedených okolností predoperačný časový faktor nehrá podstatnú úlohu. Naopak je možné predpokladať, že pred operáciou už zrejme prebehli patofyziologické zmeny, ktoré už v značnej miere ireverzibilne poškodili nervové štruktúry.
Za povšimnutie stoja poznatky získané v experimentoch na zvieratách. Pri vzniku SCE okrem už spomínaného vzostupu tlaku v spinálnom kanáli, ku ktorému môže dôjsť okrem stenózy aj pri veľkej herniácii intervertebráneho disku či voľnom sekvestri v spinálnom kanáli, uvádza sa aj kompresia ciev, následkom toho je znížená výživa a hypoxia nervových štruktúr. Je sťažený aj venózny odtok, v dôsledku rozšírenia žíl venózne chlopne sú nefunkčné, žíly nadobudajú varikózny charakter. Poruší sa bariéra medzi stenou kapilár a nervovým tkanivom, čo vedie k rozvoju edému koreňa [6,9,18].
Uvádza sa aj negatívny účinok fragmentov medzistavcovej platničky, ktoré majú zápalový účinok na okolie. Sekvestre z poškodeného disku majú vyššiu hladinu fosfolipázy A2 než kúsky zdravej medzistavcovej platničky. Práve táto okolnosť ako príčina zápalových a funkčných zmien môže posúvať vývoj ďalej negatívnym smerom [19].
Pri rozvoji SCE v experimente dochádza k zmenám v hladine neurotransmiterov. Hladina substancie P a somatostatinu klesá, serotonín a norepinefrin stúpa. Neuromodulátor NO, resp. aktivita NOS (syntáza oxidu dusnatého) klesá v sivej hmote kraniálne od kompresie, stúpa kaudálne od kompresie, v bielej hmote sa nemení. Stresový proteín HSP 72, ktorý je vo všeobecnosti považovaný za odpoveď bunky na poškodenie a má pre ňu protektívny účinok, stúpa [6,20,21].
Pri niektorých chorobách, ako napr. morbus Bechterev, sa pri rozvoji príznakov môžu podieľať aj meningeálne zápalové zmeny, ktoré sa šíria ďalej, dochádza k arachnoiditíde, neuritíde, vaskulitíde a k tvorbe adhézií medzi štruktúrami konského chvosta [6].
Tieto zmeny spôsobujú už uvádzané morfologické zmeny. Sú to Walerova degenerácia motorických koreňov distálne od miesta konstrikcie a senzitívnych dráh proximálne od miesta poškodenia.
V experimente sa v liečbe SCE osvedčila chirurgická dekompresia, vazodilatačná liečba a protizápalová liečba. Z vazodilatačných prostriedkov sa ako sľubné ukazuje podávanie lipoprostaglandínu E1 (lipo-PGE1). Skúša sa podávanie steroidov epidurálne a intratekálne. Skúša sa aj použitie stimulácie, mechanizmus nie je jasný, pozitívny efekt sa dáva do súvisu s uvoľnením inhibičných neurotrasmiterov GABA a glycin [6].
Výsledky liečby SCE v experimente sú pomerne optimistické. Často sa udáva kompletná, resp. skoro úplná úprava neurologického stavu, nemusí sa však normalizovať nález na SEP. Timing operácie sa nejaví ako rozhodujúci faktor, predsa však hrá určitú úlohu. Pri včasnejších dekompresiach dochádza rýchlejšie k úprave SEP [6]. Berúc na zreteľ patofyziologické zmeny aj napriek nejednoznačným skúsenostiam z klinickej praxe sa viacerí autori klonia k včasným operáciam [6,22–24].
V klinickej praxi SCE prináša aj riziko vzniku flebotrombózy. Z uvedeného dôvodu dávame dôraz na preventívne opatrenia počínajúce bandážou a polohovaním končatín, včasnou rehabilitáciou i podávaním LMWH. To snáď bolo príčinou, že sa spomínaná komplikácia u žiadneho pacienta sledovaného súboru nevyskytla.
SCE často zanecháva trvalé následky. V našom súbore to boli hlavne bolesti (bolesť stála 22 %, občasná 59 %), poruchy citlivosti perianogenitálne (hypestéza 31 %, anestéza 10 %), motorický deficit (ľahký 23 %, stredný 24 %, ťažký 28 %). Vyprázdňovanie močového mechúra sa tiež neupravilo úplne (brušný lis musí použiť 31 %, katéter potrebuje 12 %), podobne vyprázdňovanie stolice (občasný únik vetrov a stolice 38 %, preháňadlá 10 %, kolostómia 2 %). Sexuálne funkcie neostávajú ušetrené (zhoršenie 38 %, strata 17 %). Pre malý počet nebolo možné hodnotiť mužov a ženy samostatne [23].
Podľa našich poznatkov závažnosť a dynamika progresie ťažkostí pri SCE v značnej miere závisí od etiológie. Pacienti najrýchlejšie vyhľadávajú lekára v prípadoch voľných sekvestrov a veľkých hernií intervertebrálnych diskov v spinálnom kanáli, naopak progresia ťažkosti je pomalšia pri výrazných stenózach spinálneho kanála a nádoroch.
Vplyv predoperačného časového intervalu (timing operácie) na pretrvávanie bolesti, úpravu citlivosti, motoriky, sfinkterových porúch a sexuálnych funkcií nebol štatisticky potvrdený. Tu je však treba pripomenúť fakt, že pacienti boli operovaní s časovým odstupom cca 16 hodín a viac od začiatku ochorenia. Experimentálne práce však poukazujú na rýchlejšiu úpravu SEP pri včasnejšej dekompresii. Uvádzaná patofyziológia SCE logicky tiež podporuje užitočnosť včasnej dekompresie.
Pre zlepšenie výsledkov liečby SCE je potrebné hľadať aj iné možnosti, napr. účinnú neuroprotekciu, a prísľub prináša aj možnosť využitia kmeňových buniek.
doc. MUDr. Imrich Lukáč, CSc.
Neurochirurgická klinika
LF UPJŠ a FNLP Košice
Trieda SNP č. 1
040 11 Košice
e-mail: ilukac@inmail.skPrijato k recenzii: 10. 3. 2010
Prijato do tlače: 10. 5. 2010
Sources
1. Šulla I, Balík V, Výrostko J. Platničkový syndrom cauda equina a jeho vplyv na pracovnú schopnosť. Praktická medicína 2008; 2(3): 32–34.
2. Tandon PN, Sankaran B. Caudae equina syndrome due to lumbar disc prolapse. Indian J Orthop l967; l: 112–119.
3. Spännare BJ. Prolapsed lumbar intervertebral disc with partial or total occlusion of the spinal canal. A study of 30 patients with and 28 without cauda equina symptoms. Acta Neurochir (Wien) 1978; 65(3–4): 189–198.
4. Šulla IJ, Lukáč I, Šulla I jr. Syndroma caudae equinae discogenes. 1st ed. Košice: UPJŠ 2009.
5. Olmarker K, Rydevik B, Nordborg C. Autologous nucleus pulposus induces neurophysiologic and histologic changes in porcine cauda equina nerve roots. Spine 1993; 18(11): 1425–1432.
6. Orendácová J, Cízková D, Kafka J, Lukácová N, Marsala M, Sulla I et al. Cauda equina syndrome. Prog Neurobiol 2001; 64(6): 613–637.
7. Delamarter RB, Bohlmann HH, Bodner D, Biro C. Neurologic function after experimental cauda equina compression: cystometrograms versus cortical evoked potentials. Spine 1990; 15(9): 864–870.
8. Olmarker K, Rydevik B. Single - versus double-level nerve root compression. An experimental study on the porcine cauda equina with analyses of nerve impulse conduction properties. Clin Orthop 1992; 279 : 35–39.
9. Mao GP, Konno S, Arai I, Olmarker K, Kukusi S. Chronic double-level cauda equina compression. An experimental study on the dog cauda equina with analyses of nerve conduction velocity. Spine 1998; 23(15): 1641–1644.
10. Kafka J, Lukáčová N, Čížková D, Maršala J. Zmeny v aktifite syntázy oxidu dusnatého v mieche po ligácii koreňov cauda equina v experimente. Cesk Slov Neurol N 2007; 70/103(5): 505–511.
11. Šulla I jr, Vanický I, Danko J. An attempt at an explanation of unsatisfactory outcomes after operation for cauda equina syndrome. Experimental study. Acta Spondylologica 2004; 2 : 44–48.
12. Todd NV. Cauda equina syndrome: the timing of surgery probably does influence outcome. Br J Neurosurg 2005; 19(4): 301–306.
13. Sayegh FE, Kapetanos GA, Symeonides PP, Anogiannakis G, Madentzidis M. Functional outcome after experimental cauda equina compression. J Bone Joint Surg 1997; 79(4): 670–674.
14. Stephenson GC, Gibson RM, Sontag VKH. Who is to blame for the morbidity of acute cauda equina compression? J Neurol Neurosurg Psychiatry 1994; 57 : 388.
15. Dyck POJ, Thomas PK, Lambert EH, Bunge R. Peripheral neuropathy. 2nd ed. Philadelphia: WB Saunders 1984.
16. Greenberg MS. Handbook of Neurosurgery. 5th ed. New York: Thieme 2001.
17. Caputo LA, Cusimano MD. Atypical presentation of cauda equina syndrome. J Can Chiropr Assoc 2002; 46(1): 36–38.
18. Olmarker K, Rydevik B, Holm S, Bagge U. Effects of experimental graded compresion on blood flow in spinal nerve roots. A vital microscopic study on the porcine cauda equina. J Orthop Res 1989; 7(6): 817–823.
19. Franson RC, Saal JS, Saal JF. Human disc phospholipase A2 is inflamatory. Spine 1992; 17 (Suppl 6): S129–S132.
20. Kawakami M, Tamaki T. Morphlologic and quantitative changes in neurotransmitters in the lumbar spinal cord after acute or chronic mechanical compression of the cauda equina. Spine 1992; 17 (Suppl 3): S13–S17.
21. Marsala J, Sulla I, Santa M, Marsala M, Mechírová E, Jalc P. Early neurohistological changes of canine lumbosacral spinal cord segments in ischemia-reperfusion induced paraplegia. Neurosci Lett 1989; 106(1–2): 83–88.
22. DeLong WB, Polissar N, Neradilek B. Timing of surgery in cauda equina syndrome with Urinary retention: meta analysis of observational studies. J Neurosurg Spine 2008; 8(4): 305–320.
23. Lukáč I. Syndroma caudae equinae. Košice: LF UPJŠ 2009.
24. Gajdoš M, Leško J, Cicholesová T. Ochorenia driekovej chrbtice – 1. časť: všeobecné poznámky, klinika, diagnostika, konzervatívna liečba. Praktická medicína 2008; 2(3): 30–31.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2010 Issue 5-
All articles in this issue
- Cievna mozgová príhoda a ischemická choroba srdca
- Konkomitantní chemoradioterapie a cílená biologická léčba u glioblastoma multiforme
- Syndrom útlaku ulnárního nervu v oblasti lokte – přehled operačních technik a srovnání jejich výsledků
- Analýza „default mode“ sítě u zdravých dobrovolníků
- Úloha predoperačného časového intervalu pri liečbe diskogenného syndrómu caudae equinae
- Výskyt psychogénnych porúch v neurológii
- Behaviorálne poruchy u pacientov s Parkinsonovou chorobou – anamnestický skríning za pomoci špecializovaného dotazníka
- Přítomnost tzv. typických MR nálezů u multisystémové atrofie a progresivní supranukleární paralýzy – retrospektivní pilotní studie
- Endoskopická transnazální chirurgie hypofýzy – výhody spolupráce otorinolaryngologa a neurochirurga
- Střelná poranění hlavy a mozku
- Hemangioblastom kaudy – kazuistika
- Neuralgie nervus pudendalis – kazuistika
- Bodná poranění míchy a míšních kořenů – kazuistiky
- Morbus Lhermitte-Duclos – kazuistika
- Vývoj Národní sady klinických standardů a ukazatelů zdravotní péče a první výsledky v oboru neurologie
- Standard pro léčbu pacientů s autoimunitními nervosvalovými onemocněními intravenózním lidským imunoglobulinem a plazmaferézou
- Antikoagulační terapie v prevenci a léčbě ischemických iktů
- Vývoj technik PLIF a TLIF
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Neuralgie nervus pudendalis – kazuistika
- Vývoj technik PLIF a TLIF
- Syndrom útlaku ulnárního nervu v oblasti lokte – přehled operačních technik a srovnání jejich výsledků
- Střelná poranění hlavy a mozku
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

