-
Medical journals
- Career
Časná karotická endarterektomi e pro reziduální kriticko u stenózu krkavice po intravenózní trombolýze
Authors: J. Mraček 1; I. Holečková 1; J. Mork 1; P. Ševčík 2; V. Rohan 2
Authors‘ workplace: Ne urochirurgické oddělení LF UK a FN Plzeň, 2Ne urologická klinika LF UK a FN Plzeň 1
Published in: Cesk Slov Neurol N 2009; 72/105(2): 173-177
Category: Short Communication
Overview
Cíl:
Cílem práce je přispět ke zjištění, zda lze bezpečně provést karoticko u endarterektomii pro kriticko u rezidu ální stenózu vnitřní krkavice v období krátce po proběhlé intravenózní trombolýze pro akutní mozkový infarkt.Úvod:
Při intravenózní trombolýze je reperfuze ischemického ložiska dosaženo rozpuštěním tromboembolu, vlastní sklerotické tepenné změny trombolýzo u ovlivněny nejso u. Těsná homolaterální rezidu ální stenóza krkavice přetrvávající po předchozí trombolýze ohrožuje nemocného časno u recidivo u mozkového infarktu a uzávěrem tepny. V načasování karotické endarterektomi e po cévní mozkové příhodě zůstávají v klinické praxi kontroverze a bezpečné provedení operace v období krátce po trombolýze je nejisté.Metodika:
Ve sdělení retrospektivně hodnotíme so ubor sedmi nemocných v období 01/ 2006 – 05/ 2008, u kterých byla po intravenózní trombolýze pro akutní mozkový infarkt v povodí střední mozkové tepny provedena časná endarterektomi e pro homolaterální kriticko u rezidu ální stenózu vnitřní krkavice. Jednalo se o muže ve věku 52 – 74 let.Výsledky:
Trombolýza byla úspěšná ve všech případech, ne urologický obraz se třikrát rychle normalizoval a ve čtyřech případech upravil parci álně (Nati onal Institutes of He alth Stroke Scale – 1, 3, 4, 11). Kontrolní počítačová tomografi e byla negativní nebo zobrazila malo u hypodenzitu. Nemocní měli před operací normální ne urologický nález nebo většino u jen lehký ne urologický deficit. Operace (provedená 5. – 13. den po trombolýze (medi án = 8), celková narkóza, elektrofyzi ologické monitorování) a po operační průběh byly bez komplikací. U nemocných s předoperačně přítomným ne urologickým deficitem došlo po operaci k jeho další úpravě (Nati onal Institutes of He alth Stroke Scale: 1 – 0, 3 – 2, 4 – 3, 11 – 6). 30denní morbidita a mortalita byla rovna nule. V průběhu šestiměsíčního sledování se recidiva mozkového infarktu nevyskytla.Závěr:
U vybraného so uboru nemocných s rezidu ální kriticko u stenózo u vnitřní krkavice po proběhlé intravenózní trombolýze pro akutní ischemicko u cévní mozkovo u příhodu lze bezpečně provést časno u karoticko u endarterektomii.Klíčová slova:
stenóza krkavice – karotická endarterektomi e – timing – trombolýza – mozkový infarktÚvod
Intravenózní trombolýza (IVT) je účinná metoda léčby akutní ischemické cévní mozkové příhody (iCMP). Jedná se o doporučený léčebný postup u vybrané skupiny nemocných, kteří mohou být léčeni rekombinantním tkáňovým aktivátorem plazminogenu (rtPA) do tří hodin od začátku příznaků iCMP (třída I, hladina důkazů A) [1,2]. Výsledky studie the European Cooperative Acute Stroke Study III (ECASS III) prokázaly přínos IVT v intervalu do 4,5 hodiny od rozvoje iCMP [3]. Reperfuze ischemického ložiska je dosaženo rozpuštěním tromboembolu, vlastní sklerotické tepenné změny trombolýzou ovlivněny nejsou. Po úspěšné trombolýze, kdy dojde k rekanalizaci intrakraniálního nebo extrakraniálního uzávěru, se může vyskytnout reziduální těsná stenóza krčního úseku vnitřní krkavice, která ohrožuje nemocného časnou recidivou iCMP.
Karotická endarterektomie (CEA) je efektivní v prevenci recidivy mozkového infarktu u nemocných se stenózou krkavice přesahující 70% za předpokladu, že morbidita a mortalita (MM) provádějícího pracoviště nepřesahuje 6% (třída I, úroveň A), resp. u stenózy 50–69% při MM do 3% (třída III, úroveň C) [2]. Stupeň stenózy je nejvýznamnější determinantou prospěšnosti CEA [4–6]. Zatímco vlastní indikace operace spočívá na podložených důkazech (Evidence Based Medicine), její načasování po proběhlé iCMP je v klinické praxi bohužel nejednotné a zejména na cévně chirurgických pracovištích je CEA stále paušálně odkládána. Při časném provedení CEA je nemocný ohrožen hemoragickou transformací ischemického ložiska, na druhé straně odklad výkonu je spojen s rizikem recidivy iCMP a uzávěrem tepny [7–9]. Kombinované riziko odložené CEA a recidivy iCMP bývá však často vyšší než riziko časné operace, která recidivě mozkového infarktu zabrání [8]. Paušální odkládání CEA o 4–6 týdnů po proběhlé ischemické příhodě se proto jeví jako neopodstatněné. Poslední doporučení uvádějí, že nemocní po tranzitorní ischemické atace (TIA) nebo stabilním neinvalidizujícím mozkovém infarktu profitují z časně provedené CEA, nejlépe do 14 dnů od příhody (třída II, úroveň B) [2].
Ve sdělení prezentujeme soubor sedmi nemocných, u kterých byla provedena časná CEA (do 14 dnů od příhody) pro těsnou reziduální homolaterální stenózu arteria carotis interna (ACI) po intravenózní trombolýze pro akutní mozkový infarkt.
Materiál a metodika
Jedná se o retrospektivně hodnocený soubor sedmi nemocných v období 01/2006–05/2008, u kterého byla provedena časná CEA pro těsnou reziduální stenózou ACI po intravenózní trombolýze pro akutní mozkový infarkt v povodí střední mozkové tepny (arteria cerebri media – ACM, tab. 1). U všech nemocných byla při přijetí a den po provedené trombolýze provedena nativní počítačová tomografie (CT), perfuzní CT a CT angiografie. V jednom případě byla po trombolýze doplněna digitální subtrakční angiografie (DSA). Vyšetření prokázala pravděpodobnou karotickou etiologii mozkového infarktu (arterio-arteriální embolizace na podkladě stenózy nebo obliterace ACI). Do studie byli zařazeni nemocní s vysokým rizikem recidivy iCMP při těsné homolaterální reziduální stenóze ACI na podkladě nestabilního nepravidelného aterosklerotického plátu často se zpomaleným proudem nad stenózou. Vstupními kritérii byl normální nález nebo malá hypodenzita na kontrolním CT, normální neurologický nález nebo jen lehký deficit a provedení operace v doporučovaném intervalu do 14 dní. Nemocný s klinickým obrazem velké iCMP (National Institutes of Health Stroke Scale – NIHSS 11) byl indikován k časné operaci pro vysoké riziko recidivy hemodynamické iCMP. Před operací byla u všech nemocných provedena transtorakální echokardiografie, která nezjistila možnou kardiální embolizaci. Před operací nebyla vysazena antiagregační terapie (Clopidogrel 75mg nebo Anopyrin 200mg). V případě duální antiagregační léčby (Clopidogrel + Anopyrin) byl ponechán pouze jeden přípravek pro předpokládané vysoké riziko perioperačních krvácivých komplikací. CEA byla provedena mikrochirurgickou technikou (podélná arteriotomie) v celkové anestezii při elektrofyziologickém peroperačním monitorování (elektroencefalografie, somatosenzorické evokované potenciály) v intervalu 5.–13. den po trombolýze. Po operaci bylo pokračováno v antiagregační terapii.
Table 1. Charakteristika souboru nemocných. 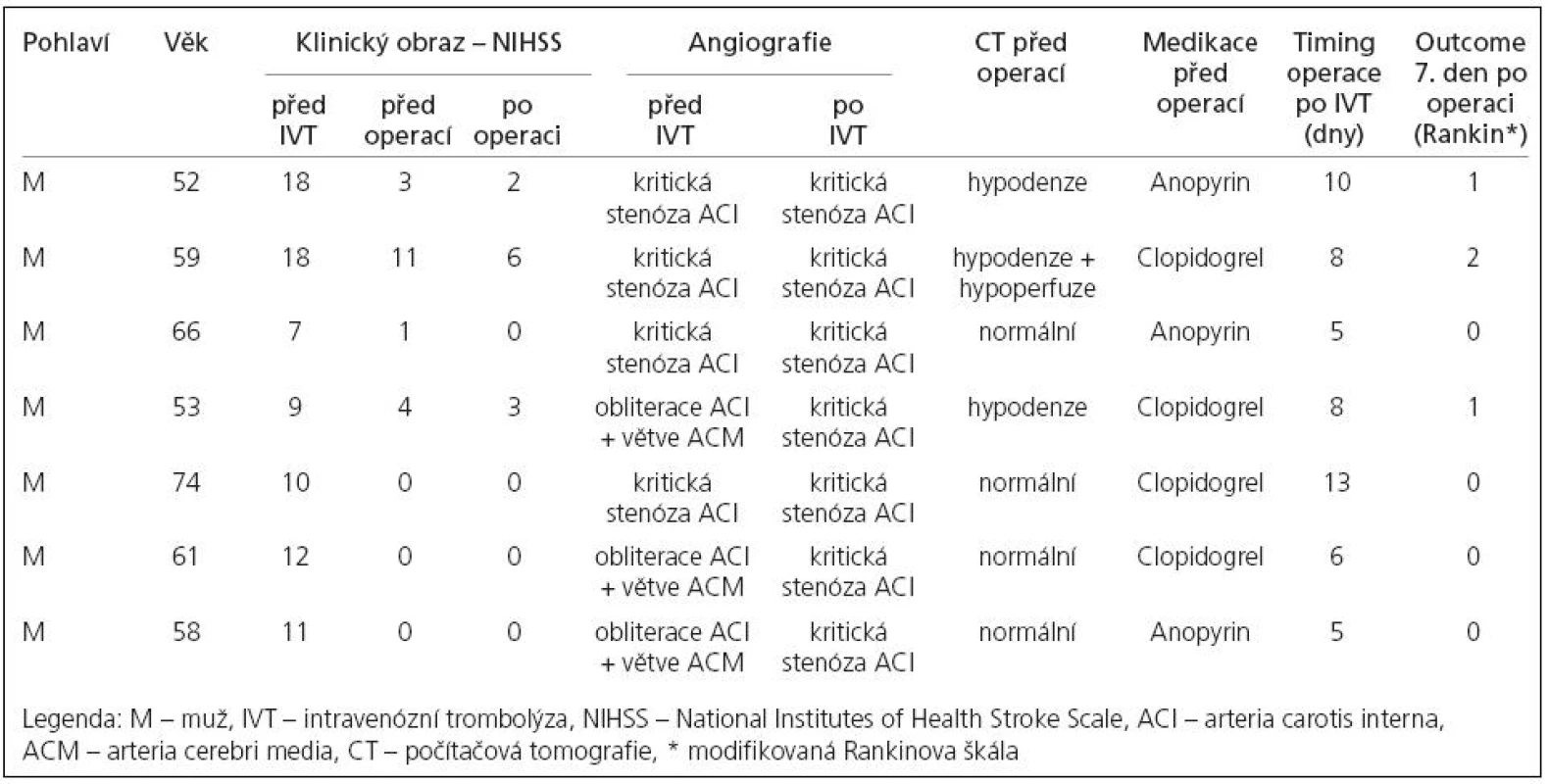
Výsledky
Ve sledovaném období bylo léčeno sedm nemocných mužského pohlaví ve věku 52–74 let (průměrný věk 60 let). Nemocní byli léčeni intravenózním podáním rtPA podle současných platných guidelines [1,2]. Trombolýza byla úspěšná ve všech sedmi případech – čtyřikrát došlo k částečné úpravě neurologického deficitu, u tří nemocných k jeho rychlé plné úpravě (tab. 1). Nativní CT před podáním trombolýzy bylo vždy bez průkazu rozvinutých ischemických změn. CT angiografie (CTA) prokázala u čtyř nemocných těsnou stenózu ACI v bulbu, třikrát byla zobrazena obliterace ACI v bifurkaci s patrnou embolizací do povodí ACM. Stenózy ACI nebyly dle kontrolní CTA trombolýzou ovlivněny (obr. 1). Ve všech třech případech však došlo k rozpuštění jak intrakraniálního tromboembolu, tak k rekanalizaci obliterované ACI v krčním úseku, kde však zůstala těsná reziduální stenóza. Nemocní indikovaní k časné CEA měli ve třech případech normální neurologický nález, třikrát byli operováni nemocní s lehkým (NIHSS 1, 3, 4) a jednou s těžkým neurologickým deficitem (NIHSS 11). Tento nemocný byl ohrožen recidivou iCMP na hemodynamickém podkladě. Perfuzní CT zobrazilo v jeho případě hypoperfuzi v celém karotickém povodí při malém ložisku korového infarktu (obr. 2) a doplněná DSA potvrdila filiformní stenózu ACI se zpomaleným proudem a minimálním kolaterálním oběhem.
Image 1. CT angiografie zobrazuje kritickou stenózu vnitřní krkavice na podkladě masivního nerovného plátu s chabým plněním tepny nad stenózou. 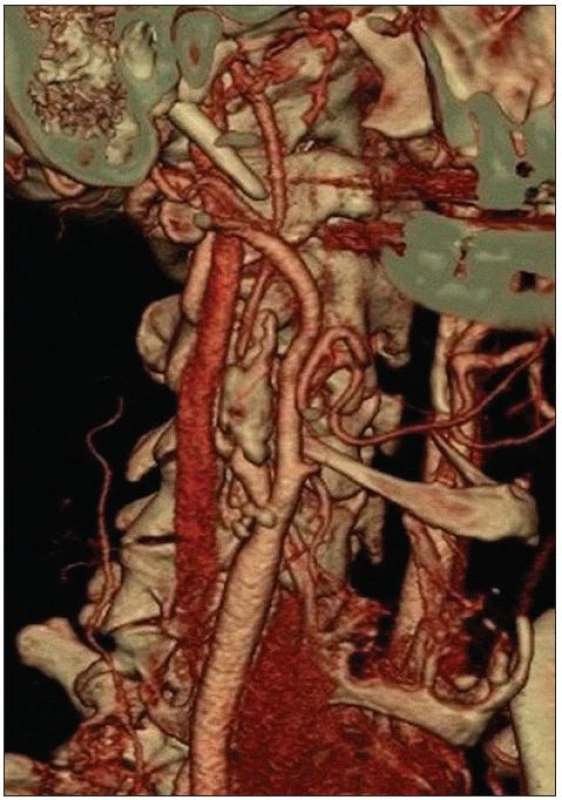
Image 2. Perfuzní CT (time to peak) zobrazuje ložisko korové ischemie vlevo a hypoperfuzi celého povodí vnitřní krkavice vlevo. 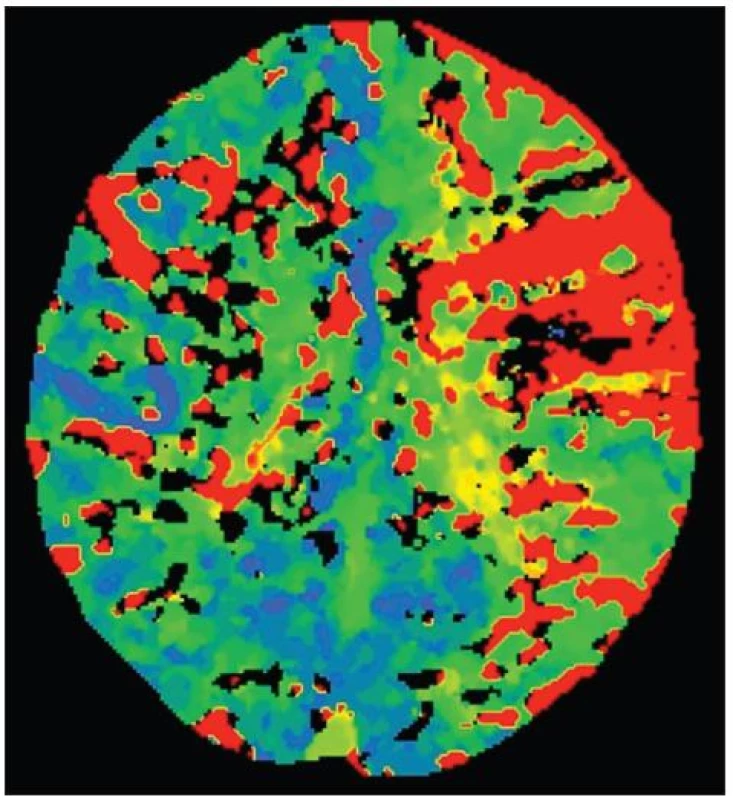
Vlastní operace provedená do 13 dní od proběhlé trombolýzy (medián 8 dní) i pooperační období proběhly ve všech případech bez komplikací.
Předoperační neurologický deficit se po operaci v jednom případě normalizoval, u tří nemocných došlo k jeho parciální úpravě, která byla u nemocného s obrazem velké iCMP výrazná (předoperační NIHSS 11, pooperační NIHSS 6).
Nemocní byli propuštěni sedmý pooperační den. Ve čtyřech případech měli normální neurologický nález, třikrát reziduální neurologický deficit (NIHSS 2, 3, 6). Pooperační 30denní MM byla rovna nule. V průběhu šestiměsíčního sledování nedošlo u žádného nemocného k recidivě iCMP.
Diskuze
Prezentovaný soubor je specifickou subpopulací nemocných s mozkovým infarktem, kteří podstoupili úspěšnou intravenózní trombolýzu, avšak jsou ohroženi časnou recidivou iCMP na podkladě kritické reziduální stenózy krkavice. Naše výsledky dokládají, že benefit časné CEA převažuje v indikovaných případech rizika, která s sebou přináší indikace operace v období krátce po trombolýze, kdy jsou nemocní neurologicky nestabilní, mají alterovanou hemokoagulaci a je přítomné riziko reperfuze a hemoragické transformace ischemického ložiska. Jedná se o skupinu z pohledu neurochirurga bezesporu rizikovější, avšak, dle našich i sporadických literárních poznatků, z operace profitující [10,11]. Všechny operace proběhly zcela bez komplikací, ani v jednom případě nedošlo k recidivě iCMP.
Zdali časná CEA může redukovat neurologický deficit, není známo. U nemocných s neurologickým deficitem však po operaci došlo k jeho další úpravě. Výrazné pooperační zlepšení klinického obrazu u nemocného s těžkým deficitem na podkladě hemodynamického původu (NIHSS 11–6) dokládá možný kurativní efekt CEA díky zlepšení perfuze zóny penumbry. Kontrolní pooperační perfuzní vyšetření zobrazilo přetrvávající reziduální ložisko korového infarktu, avšak normalizaci perfuze v karotickém povodí.
V literatuře jsme nalezli pouze jedno sdělení týkající se stejného tématu, jehož výsledky korespondovaly s naším závěrem [10]. Vzhledem k nedostatku relevantních údajů není jednoznačně prokázáno, zda lze bezpečně CEA v období krátce po IVT provést. K časnému operačnímu zákroku nás vedl spolehlivý průkaz karotické etiologie iCMP a splnění tří základních indikačních kritérií, na jejichž podkladě by mělo být rozhodnuto o timingu operace: angiografický průkaz kritické stenózy krkavice, normální neurologický obraz nebo jen lehký deficit a normální CT, resp. nález malé hypodenzity [11].
U nemocných došlo po trombolýze třikrát k promptní úpravě neurologického obrazu, to znamená, že průběh mozkového infarktu lze díky úspěšné léčbě přirovnat k obrazu TIA. V dalších čtyřech případech se neurologický deficit zcela neupravil, jednalo se tak většinou o neinvalidizující iCMP. Dle posledních doporučení je u nemocných se stabilním neinvalidizujícím mozkovým infarktem a zejména po TIA žádoucí operaci provést co nejdříve po vzniku iCMP (nejpozději do 14 dnů) [2,12–14]. Charakter iCMP u našeho souboru nemocných nás vedl k provedení časné operace. Nemocný s těžkým neurologickým deficitem byl operován pro hraniční perfuzi téměř celé homolaterální mozkové hemisféry při filiformní stenóze ACI a minimálním kolaterálním oběhu.
Předoperační angiografické vyšetření u všech nemocných prokázalo těsnou reziduální stenózu ACI s nerovným luminem a často se zpomaleným proudem a chabým plněním nad stenózou. Ve třech případech byla ACI před trombolýzou dokonce zcela obliterována s patrnou embolizací do ACM. Stupeň stenózy krkavice je nezávislým rizikovým faktorem recidivy mozkového infarktu [14]. Rothwell et al prokázali, že riziko iCMP u nepravidelného plátu velmi signifikantně vzrůstá se stupněm stenózy [15]. Grafický nález na ACI v našem souboru byl ve všech případech důvodem časné operace. Velmi vysoké riziko recidivy iCMP se uvádí v případě kombinace embolizační a hemodynamické příčiny [16]. Tato situace nastala pravděpodobně u nemocného s obrazem velké iCMP – vlastní infarktové ložisko bylo nejspíše arterio-arteriálně embolizačního původu (ložisko nemělo charakter watershed infarktu), přičemž velmi hrozilo nebezpečí recidivy příhody na hemodynamickém podkladě (vyčerpaná cerebrovaskulární rezerva – porušené perfuzní parametry v celém povodí ACI, obr. 2).
Hypodenzita na CT se v našem souboru vyskytla u tří nemocných. Ve všech případech byla lokalizována v povodí ACM, měla však malý rozsah, nechovala se expanzivně a nemocní měli stabilní a většinou minimální neurologický deficit. Nález hypodenzity na CT bývá považován za hlavní rizikový faktor pooperační hemoragické transformace ischemického ložiska a bývá mnohdy důvodem odkladu CEA, aby mohlo dojít k částečné restauraci hemodynamicky kompromitovaného řečiště [17]. Většina publikovaných prací však neprokázala souvislost outcome časné CEA a nálezu hypodenzity u nemocných neurologicky stabilních [8,18,19]. Na druhé straně bylo popsáno, že čím větší je infarktové ložisko, tím je jeho hemoragická transformace pravděpodobnější [20]. V úvaze o vhodném načasování CEA je zásadní charakter hypodenzity (její velikost, expanzivní chování, lokalizace – ischemie v povodí MCA má nejvyšší riziko vzniku ICH) a její vztah k hloubce neurologického deficitu [11,21]. CT nálezy v našem souboru nebyly důvodem k odkladu operace ani u jednoho nemocného.
Jak vyplývá z výše uvedené diskuze, splnění uvedených tří faktorů (klinického obrazu, charakteru stenózy, nálezu na CT), což indikačně korespondovalo s literárními údaji, nás ospravedlňovalo provést časný zákrok [10,11].
Rekanalizace extrakraniálního uzávěru ACI u všech tří pacientů dokládá možný výborný léčebný efekt neselektivního intravenózního podání rtPA i v případě obliterace velkých tepen. Indikace emergentní karotické trombendarterektomie v případě akutního mozkového infarktu na podkladě okluze ACI zůstává i přes některé publikované dobré výsledky kontroverzní [22].
Limitace naší práce představuje retrospektivní charakter studie a malý nekoherentní soubor nemocných. Do studie byli zařazeni nemocní s různým předoperačním neurologickým obrazem a nálezem na CT. Určitá omezení vidíme v nejednotné antiagregační terapii před operací.
Jedná se o selektovaný vzorek pacientů, není proto zřejmé, do jaké míry lze naše výsledky generalizovat. Nelze tvrdit, že všichni nemocní s reziduální stenózou ACI po trombolýze jsou vhodnými kandidáty časné CEA. Pacienti hospitalizovaní na iktových jednotkách jsou maximálně konzervativně léčeni (riziko recidivy iCMP je minimalizováno) a časná indikace CEA se může jevit jako zbytečná. Na druhé straně z nich lze velmi dobře vybrat potenciální kandidáty mající benefit z časné operace (hospitalizovaná, kvalitně observovaná a kompletně vyšetřená skupina nemocných).
Závěr
Naše výsledky ukazují, že u vybraných nemocných s kritickou reziduální stenózou krkavice po proběhlé trombolýze pro akutní iCMP lze bezpečně provést časnou endarterektomii. Operace je prevencí časné recidivy mozkového infarktu a uzávěru tepny. Zdali existuje kurativní efekt CEA v důsledku zlepšení perfuze zóny penumbry, je potřeba testovat v dalších studiích.
MUDr. Jan Mraček
Alej Svobody 80
Neurochirurgické oddělení
LF UK a FN Plzeň
304 60 Plzeň
e‑mail: mracek@fnplzen.cz
Sources
1. Adams HP jr, del Zoppo G, Alberts MJ, Bhatt DL, Brass L, Furlan A et al. Guidelines for the e arly management of adults with ischemic stroke. Stroke 2007; 38(5): 1655 – 1711.
2. Europe an Stroke Organisati on (ESO) Executive Comittee; ESO Writing Committee. Guidelines for management of ischemic stroke and transi ent ischaemic attack 2008. Cerebrovasc Dis 2008; 25(5): 457 – 507.
3. Hacke W, Kaste M, Bluhmki E, Brozman M, Dávalos A, Guidetti D et al. Thrombolysis with alteplase 3 to 4.5 ho urs after acute ischemic stroke. N Engl J Med 2008; 359(13): 1317 – 1329.
4. Europe an Carotide Surgery Tri alists’ Collaborative Gro up. MRC Europe an Carotid Surgery Tri al: interim results for symptomatic pati ents with severe (70 – 90%) or with mild (0 – 29%) carotid stenosis. Lancet 1991; 337(8752): 1235 – 1243.
5. North American Symptomatic Carotid Endarterectomy Tri al Collaborators. Benefici al effect of carotid endarterectomy in symptomatic pati ents with high‑grade carotid stenosis. N Engl J Med 1991; 325(7): 445 – 453.
6. Barnett HJ, Taylor DW, Eli asziw M, Fox AJ, Ferguson GG, Haynes RB et al. Benefit of carotid endarterectomy in pati ents with symptomatic moderate or severe stenosis. North American Symptomatic Carotid Endarterectomy Tri al Collaborators. N Engl J Med 1998; 339(20): 1415 – 1425.
7. Gi ordano JM, Tro ut HH jr, Kozloff L, DePalma RG. Timing of carotid artery endarterectomy after stroke. J Vasc Surg 1985; 2(2): 250 – 255.
8. Gasecki AP, Ferguson GG, Eli asziw M, Clagett GP, Fox AJ, Hatchinski V et al. Early endarterectomy for severe carotid artery stenosis after a nondisabling stroke: results from the North American Symptomatic Carotid Endarterectomy Tri al. J Vasc Surg 1994; 20(2): 288 – 295.
9. Hunter JA, Juli an DC, Dye WS Javid H. Emergency operati on for acute cerebral ischemi a due to carotid artery obstructi on: revi ew of 26 cases. Ann Surg 1965 : 162(5): 901 – 904.
10. McPherson CM, Wo o D, Cohen PL, Panci oli AM, Kissela BM, Carrozzella JA at al. Early carotid endarterectomy for critical carotid artery stenosis after thrombolysis therapy in acute ischemic stroke in the middle cerebral artery. Stroke 2001; 32(9): 2075 – 2080.
11. Mraček J, Holečková I, Mork J, Choc M. Timing karotické endarterektomi e. Cesk Slov Ne urol N 2008; 71/ 104(4): 414 – 421.
12. Lovett JK, Dennis MS, Sandercock PA, Bamford J, Warlow CP, Rothwell PM. Very e arly risk of stroke after a first transi ent ischemic attack. Stroke 2003; 34(8): 138 – 140.
13. Co ull AJ, Lovett JK, Rothwell PM, Oxford Vascular Study. Populati on based study of e arly risk of stroke after transi ent ischemic attack or minor stroke: implicati ons for public educati on and organisati on of services. BMJ 2004; 328(7435): 326.
14. Rothwel PM, Eli asziw M, Gutnikov SA, Warlow CP, Barnett HJ; Carotid Endarterectomy Tri alists Collaborati on. Endarterectomy for symptomatic carotid stenosis in relati on to clinical subgro ups and timing of surgery. Lancet 2004; 363(9413): 915 – 924.
15. Rothwell PM, Gibson R, Warlow CP. Interrelati on between plaque surface morphology and degree of stenosis on carotid angi ograms and the risk of ischemic stroke in pati ents with symptomatic carotid stenosis. Stroke 2000; 31(3): 615 – 621.
16. Blaser T, Hofmann K, Buerger T, Effenberger O, Wallesch CW, Goertler M. Risk of stroke, transi ent ischemic attack, and vessel occlusi on before endarterectomy in pati ents with symptomatic severe carotid stenosis. Stroke 2002; 33(4): 1057 – 1062.
17. Baron EM, Baty DE, Loftus CM. The timing of carotid endarterectomy post stroke. Ne urol Clin 2006; 24(4): 669 – 680.
18. Wölfle KD, Pfadenha uer K, Bruijnen H, Becker T, Engelhardt M, Wachenfeld - Wahl C et al. Early carotid endarterectomy in pati ents with a nondisabling ischemic stroke: results of a retrospective analysis. Vasa 2004; 33(1): 30 – 35.
19. Paty PS, Darling RC jr, Woratyla S, Chang BB, Krei enberg PB, Shah DM. Timing of carotid endarterectomy in pati ents with recent stroke. Surgery 1997; 122(4): 850 – 854.
20. Cerebral Embolism Study Gro up. Immedi ate antico agulati on of embolic stroke: brain hemorrhagi e and management opti ons. Stroke 1984; 15(5): 779 – 789.
21. Toni D, Fi orelli M, Basti anello S, Sacchetti ML, Sette G, Argentino C et al. Hemorrhagic transformati on of brain infarct: predictability in the first 5 ho urs from stroke onset and influence on clinical o utcome. Ne urology 1996; 46(2): 341 – 345.
22. Herzig R, Král M, Olivi er P, Šaňák D, Bachleda P, Utíkal P et al. Ischemický iktus podmíněný akutní okluzí ACI: roční o utcome paci entů léčených akutní CEA a IVT. Cesk Slov Ne urol N 2007; 70/ 103 (Suppl): S7.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2009 Issue 2-
All articles in this issue
- Neurodegenerativní demence
- Krční myelopatie – diagnostický problém
- Longitudinální sledování růstu po operačních reziduí afunkčních adenomů hypofýzy
- Radi ofrekvenční terapi e facetových bolestí bederní páteře
- Indikace přední náhrady meziobratlové ploténky u zlomenin hrudní a bederní páteře s využitím magnetické rezonance – prospektivní studie
- Extra- intrakraniální arteri ální mikro anastomóza
- Počítačem modelované náhrady kostních defektů lební klenby
- Časná karotická endarterektomi e pro reziduální kriticko u stenózu krkavice po intravenózní trombolýze
- Myasthenia gravis – kritické zhodnocení přínosu svalové biopsie prováděné během thymektomie
- Leberova hereditární optická neuropatie s oligoklonálními pásy v likvoru považovaná za roztro ušeno u sklerózu – kazuistika
- Progresivní multifokální leukoencefalopatie jako komplikace léčby lymfomu – kazuistika
- Maligní tumor z pochvy periferního nervu – dvě kazuistiky
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Krční myelopatie – diagnostický problém
- Neurodegenerativní demence
- Maligní tumor z pochvy periferního nervu – dvě kazuistiky
- Radi ofrekvenční terapi e facetových bolestí bederní páteře
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

