-
Medical journals
- Career
Mechanická embolektomie pomocí Merci katétru u nemocných s akutním uzávěrem mozkových tepen
Authors: F. Charvát 1; J. Lacman 1; J. Mašková 1; J. Elis 2; V. Beneš 3
Authors‘ workplace: RDG oddělení ÚVN Praha 6 – Střešovice 1; Neurologické oddělení ÚVN Praha – Střešovice 2; Neurochirurgická klinika, Univerzita Karlova v Praze, 1. lékařská fakulta, IPVZ a ÚVN Praha – Střešovice 3
Published in: Cesk Slov Neurol N 2008; 71/104(1): 69-74
Category: Short Communication
Overview
Úvod a cíl:
Autoři seznamují s prvními zkušenostmi s mechanickou embolektomií, jako s možnou metodou léčby akutní mozkové ischemie u vybraných pacientů.Metoda:
Od července do prosince 2006 byla provedena mechanická embolektomie u 7 pacientů (5 mužů a 2 ženy) s příznaky akutního uzávěru mozkové tepny, kteří byli kontraindikováni k intravenózní léčbě alteplázou pro překročení ideálního terapeutického okna (6 pacientů) či pro probíhající těhotenství (1 pacientka). Jejich NIHSS skóre bylo od 5 do 25 (průměr 17). Po nativním a perfuzním CT byla urgentně provedena embolektomie pomocí mechanického odstraňovače trombů Merci. Tři pacienti měli uzávěr a. basilaris, dva uzávěr a. cerebri media v úseku M1, jeden pacient uzávěr v úseku M2 a jeden pacient měl uzavřenu ACI (a. carotis interna) a úseky M1 a A1 úsek a. cerebri anterior (tzv. T uzávěr).Výsledky:
K úspěšné rekanalizaci došlo u 6 pacientů (85,8%), u žádného z výkonů nebyla zaznamenána závažná periprocedurální komplikace. U jedné pacientky bylo nutné během výkonu aplikovat 3 mg alteplázy i.a. k rozpuštění distálních embolů, u dvou pacientů byla provedena PTA a. basilaris pro stenózu a u jednoho pacienta bylo nutné implantovat stent do stenotické vnitřní karotidy. U 5 pacientů (71,4 %) bylo výsledné Rankin skóre po 30 dnech 1 nebo 2, u jednoho pacienta Rankin skóre 5 a jeden pacient do 30 dnů od léčby zemřel.Závěr:
Mechanická embolektomie efektivně zprůchodnila mozkové tepny v terapeutickém okně do 8 hodin u vybraných pacientů s příznaky akutní mozkové ischemie.Klíčová slova:
cévní mozková příhoda, mechanická embolektomie, terapeutické oknoÚvod
Cévní mozková příhoda (CMP) je třetí nejčastější příčinou smrti v industriální části světa a nejčastější příčinou dlouhodobé invalidity. 80% všech mozkových příhod je ischemického původu [1]. Incidence ischemické příhody roste s věkem, v České republice se pohybuje kolem 240 případů na 100 000 obyvatel. Nejvyšší výskyt je ve věkové skupině 60-79 let [1].
Cílem léčby je zprůchodnit uzavřenou mozkovou tepnu dříve než dojde k definitivní smrti mozkových buněk (CBF-cerebral blood flow < 10-15 ml krve/100 g tkáně/min) a tím předejít trvalému neurologickému deficitu.
V současné době jsou dána pravidla léčby akutní mozkové ischemie s pomocí intravenózní [2] i intraarteriální trombolytické terapie. Vhodnou možností se zdá být použití mechanického odstraňovače embolů (Merci katétr), který je schopen velmi úspěšně a bezpečně cévu rekanalizovat. Na podkladě studie MERCI [3] bylo toto zařízení schváleno k používání u pacientů do 8 hodin od počátku neurologických příznaků.
V následujících odstavcích prezentujeme naše dosavadní zkušenosti s mechanickou embolektomií.
Materiál a metodika
Od července 2006, kdy byl na český trh uveden mechanický odstraňovač embolů Merci katétr (Concentric Medical, USA), jsme s jeho pomocí provedli mechanickou embolektomii u 7 pacientů (5 mužů a 2 ženy) , ve věku od 28 do 66 let (průměrný věk 48 let). Všichni pacienti byli přivezeni rychlou záchranou službou na oddělení Emergency, kde neurolog provedl klinické vyšetření s NIHSS (National Institutes of Health Stroke Scale) skórováním [4] (tab. 1).
U všech pacientů bylo urgentně provedeno nativní CT vyšetření mozku k vyloučení hemoragie a následně i perfuzní vyšetření mozku k ozřejmení stavu mozkové tkáně, velikosti a lokalizace postižené oblasti či jiné patologie, která by mohla změnit léčebný algoritmus. U 6 pacientů nebyla provedena i.v. trombolýza pro překročení ideálního časového terapeutického okna, u mladé pacientky byla i.v. trombolýza kontraindikována pro probíhající těhotenství. Následně byli všichni pacienti bez prodlevy převezeni na angiografický sál k provedení diagnostické angiografie a mechanické embolektomie. Vždy jsme v diagnostické části výkonu provedli angiografii s nástřikem do obou společných karotid i obou vertebrálních tepen k posouzení přesné lokalizace uzávěru, anatomie krčních tepen, stavu Willisova okruhu a eventuální přítomnosti dostatečného kolaterálního oběhu. Angiografie i vlastní embolektomie probíhaly za asistence anesteziologa, bylo nutné zajistit tlumení pacienta se stabilní polohou hlavy během celého výkonu. Výkony v předním povodí provádíme v analgosedaci, výkony v zadním povodí v celkové anestezii.
Vlastní sestava Merci systému se skládá z Merci mikrokatétru, z vodicího balonkového 9F katétru a z Merci mikrovodiče ukončeného nitinolovou vývrtkovitou částí se snižujícím se průměrem (z 2,8 do 1,1 mm) - typ X6 (obr. 1.) nebo nitinolovou spirálkou obalenou spletí filament - typ L5 (obr. 2).
Image 1. Distální konec Merci mikrovodiče typ X6. 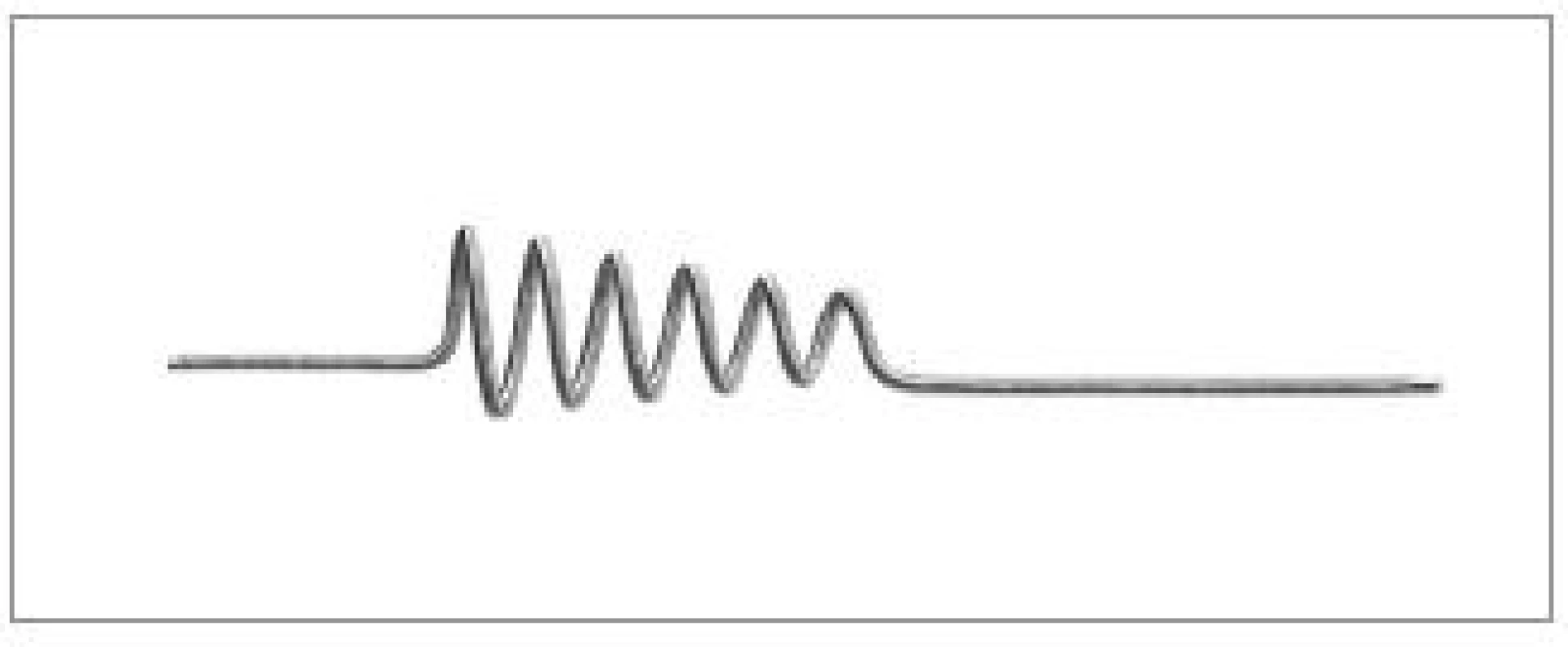
Image 2. Distální konec Merci mikrovodiče typ L5 s filamenty. 
Po zobrazení uzávěru (embolu) zavádíme přes 9F sheath ve femorální tepně vodicí balonkový katétr do postižené tepny (do a. carotis interna či a. vertebralis), co nejblíže uzávěru. Luminem vodícího katétru pak zavádíme po běžném mikrovodiči vlastní Merci mikrokatétr, jehož distálním koncem se snažíme proniknout celým embolem až do volné tepny za uzávěr. Poté mikrovodič vyměníme za vlastní Merci mikrovodič s nitinolovým koncem. Vysunutím Merci mikrovodiče z Merci mikrokatétru, se jeho distální část sama začne stáčet do preformovaného vývrtkovitého nebo spirálního tvaru dle použitého typu Merci systému (X6 nebo L5). Pomalým a opatrným stahováním mikrovodiče a mikrokatétru se snažíme zachytit embolus do spirálek a stáhnout ho až do vodícího katétru. Během stahování je balonek vodícího katétru před uzávěrem expandován v krčním úseku přístupové tepny, tok v tepně je zastaven, a tím je výrazně sníženo riziko uvolnění embolu nebo jeho části z distálního konce a jeho opětovné distální embolizaci. Navíc při stahování embolu aktivně nasáváme krev z vodicího katétru, dochází až k otočení toku a i tím je sníženo riziko uvolnění embolu. Po vtažení mikrokatétru s mikrovodičem a embolem do vodicího katétru balonek odsáváme, obnovujeme tok a celý systém odstraňujeme. Nakonec provedeme kontrolní nástřik rekonstruovaného řečiště.
Již po prvním stažení může dojít ke zprůchodnění tepny, při nedostatečném efektu lze celou Merci sestavu po očištění zavést znovu a embolektomii opakovat (nejčastěji 2x až 3x). Opakované zavádění Merci mikrovodiče (více než 3 x) není výrobcem doporučováno pro možnost zhoršení funkce nitinolového konce a možného rizika poškození tepny.
Celý systém je během výkonu na permanentním přetlakovém proplachu fyziologickým roztokem s heparinem. Před embolektomií pacienti dostávají bolus 2 500 j. heparinu i.v. a eptifibatidu (Integrilin, Schering-Plough) i.v. v dávce 180 µg/kg, po výkonu pokračujeme kontinuální intravenózní infuzí eptifibatidu v dávce 2 µg/kg/min. Heparin svým antikoagulačním (a v malých dávkách i antiagregačním) účinkem působí jako prevence vzniku trombů při zavádění instrumentária a jeho manipulaci, použití eptifibatidu má za cíl zamezit dalšímu narůstání trombu inhibicí agregace trombocytů [5].
Během druhé poloviny roku 2006 jsme ošetřili 5 mužů a 2 ženy přivezené do naší nemocnice s klinickým obrazem akutní cévní mozkové příhody při náhle vzniklém uzávěru mozkové tepny. Žádné z provedených CT vyšetřeních neprokázalo krvácení či jinou patologii, které by vylučovaly endovaskulární intervenci. Od přijetí pacienta v nemocnici se přes nativní a perfuzní CT vyšetření mozku pacienti dostávají na angiografický sál během 40 až 75 minut (průměrný čas 53 minut). Doba potřebná k rekanalizaci na angiografickém sále se pohybovala od 60 minut do 120 minut (průměr 93 minut). U 3 pacientů jsme odstraňovali embolus z a. basilaris, u 2 pacientů z M1 úseku a. cerebri media, u 1 pacienta z M2 úseku a cerebri media a u 1 pacientky šlo o tzv. T-uzávěr s embolem v a. carotis interna, M1 a A1. Mladší z našich dvou pacientek (uzávěr M1) byla v době výkonu v 5. měsíci těhotenství (tab. 1)
Table 1. Sestava pacientů léčených mechanickou embolektomií. 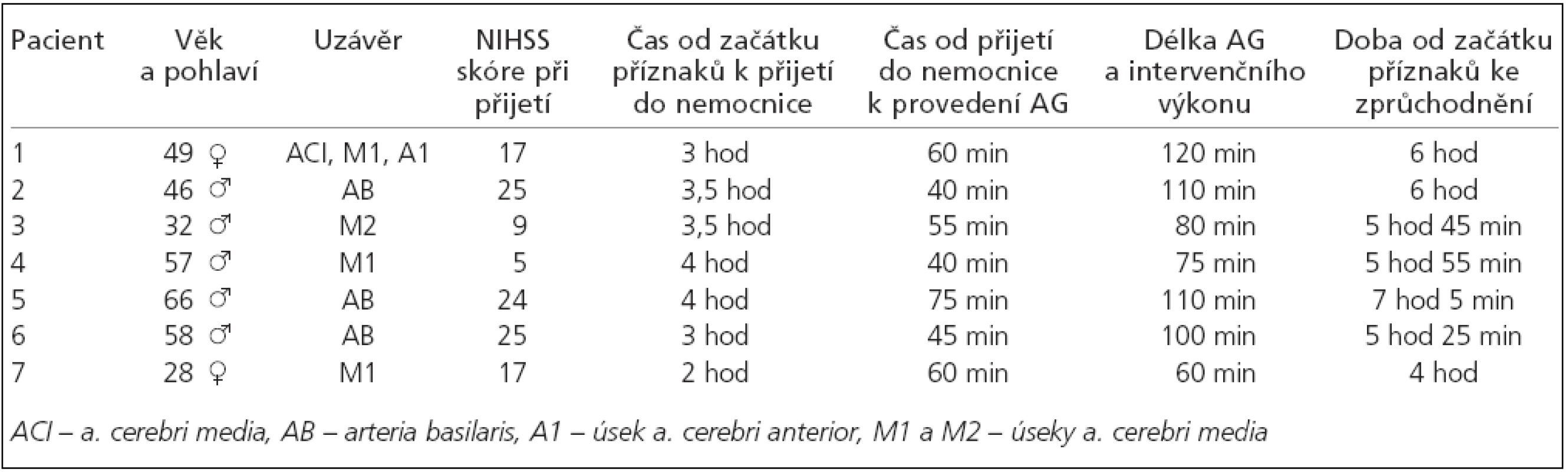
Výsledky
Úspěšné rekanalizace postižené tepny - TIMI (The Thrombolysis In Myocardial Infarction) [6] - stupeň 2 a 3 jsme při použití Merci systému dosáhli u 6 ze 7 pacientů (85,8 %) (obr. 3,4). U pacientky s T-uzávěrem došlo jen k minimální rekanalizaci (TIMI stupeň 1), podařilo se však zprůchodnit perforátory a úsek A1. U dvou pacientů (uzávěr a. basilaris) jsme po odstranění trombu museli ještě provést balonkovou PTA a. basilaris pro stenózu (obr. 5,6,7). U jednoho pacienta (uzávěr M1) bylo po výkonu nutné implantovat stent do stejnostranné krkavice pro těsnou stenózu. Během diagnostické i terapeutické fáze výkonu jsme nezaznamenali závažnou periprocedurální komplikaci. U jedné pacientky došlo k embolizaci částí trombu z M1 do větví M2, tato periprocedurální komplikace byla urgentně úspěšně řešena intraarteriální aplikací 3 mg alteplázy (Actilyse, Boehringer Ingelheim).
Image 3. DSA snímek pravé ACC v AP projekci, uzávěr oblasti M1 embolem. Normálně se plní pravá a. cerebri anterior. 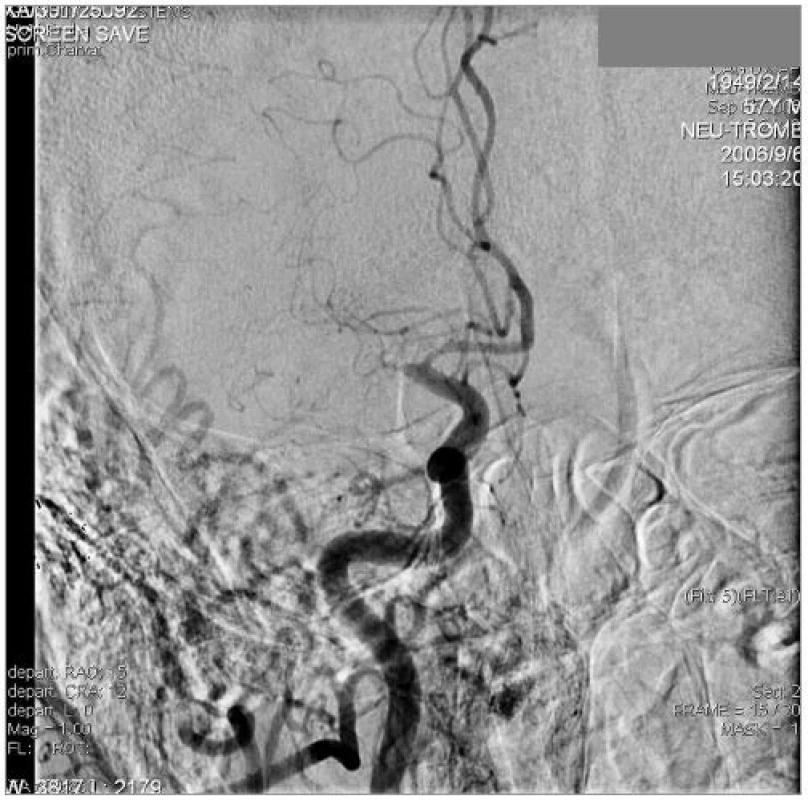
Image 4. Kontrolní DSA pravé ACC v AP projekci po mechanické embolektomii, dobře zprůchodněná hlavní větev. Obtékané, drobné tromby v M1 i M2. 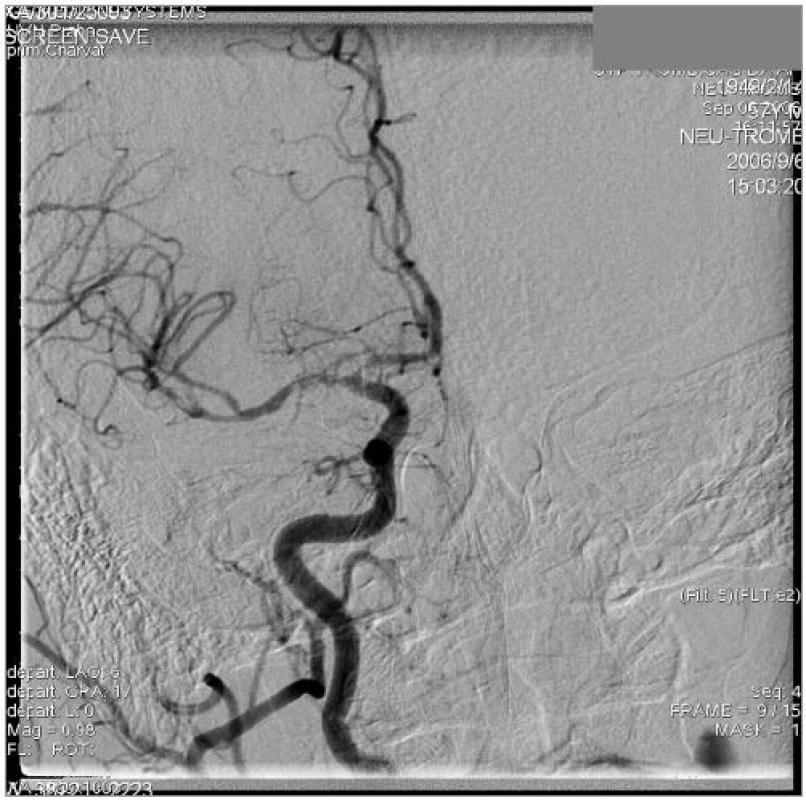
Image 5. DSA snímek levé AV v AP projekci. Uzávěr a. basilaris. 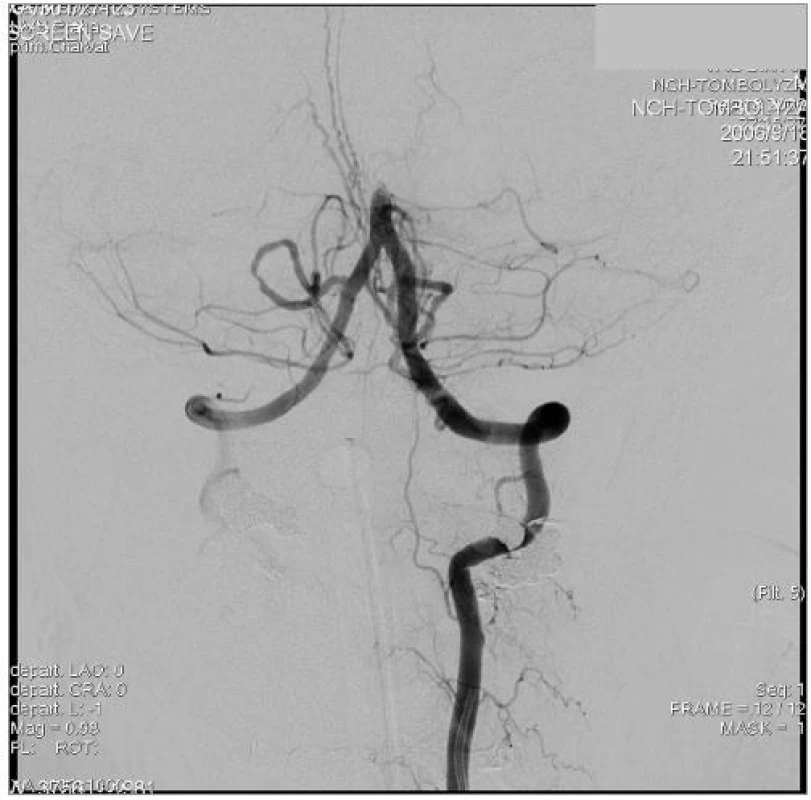
Image 6. Kontrolní nativní snímek levé AV se zavedeným Merci mikrovodičem, typ L5. Natažená spirálka mikrovodiče (šipka) pomalu zprůchodňuje tepnu. 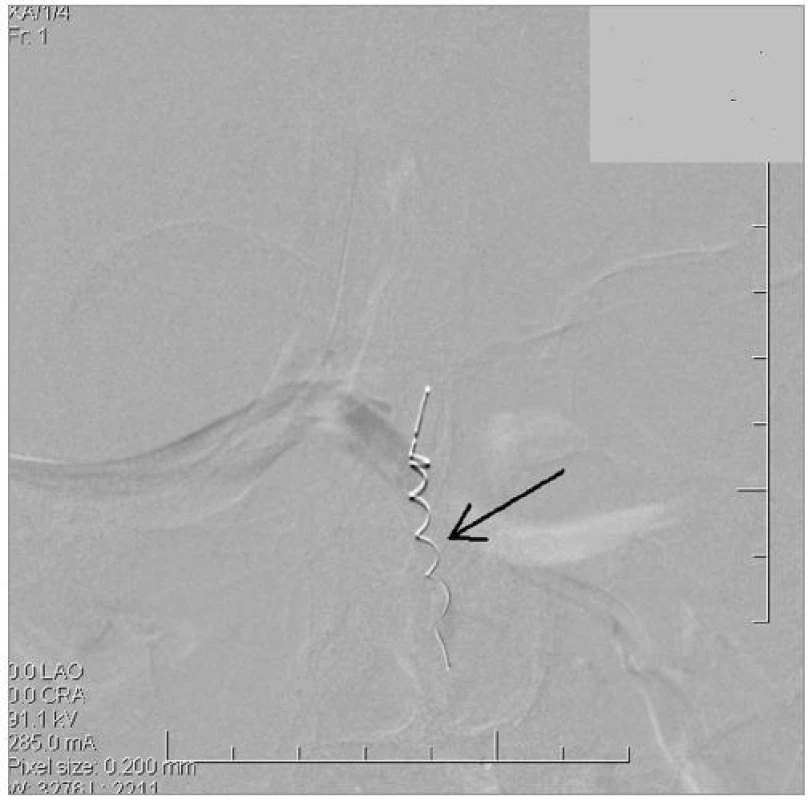
Image 7. Kontrolní DSA levé AV po embolektomii, nález je výrazně zlepšen. Patrná je stenóza na a. basilaris a reziduální trombus v oblasti P3 a. cerebri posterior vlevo. 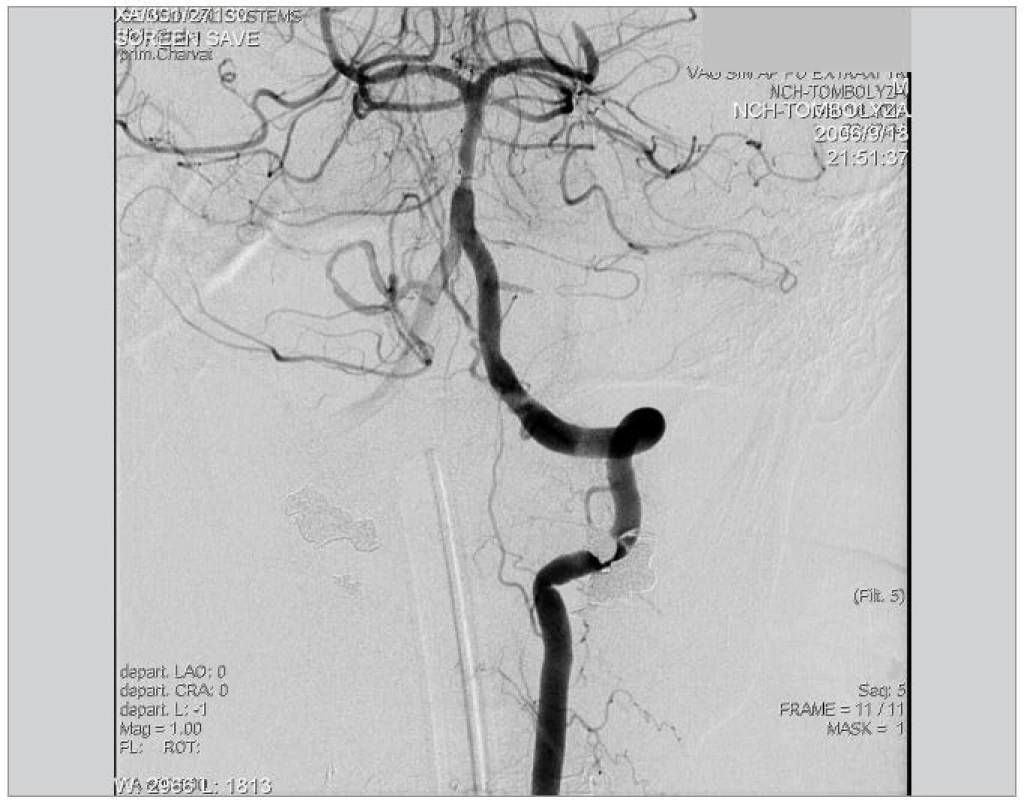
U 5 pacientů (71,4%) kontrolní CT ihned po výkonu ani za 24 hodin neprokázalo krvácení do mozkové tkáně. U 2 pacientů (28,6 %) (oba s uzávěrem a.basilaris) došlo do 24 hodin po výkonu k symptomatickému intracerebrálnímu krvácení, jeden z pacientů během dvou dnů na komplikace krvácení zemřel, druhý přežívá s těžkým neurologickým deficitem.
U 5 pacientů (71,4 %) jsme za 30 dnů po výkonu zaznamenali Rankin skóre 1 nebo 2 (mezi nimi i těhotná pacientka, která pak za několik týdnů v termínu porodila císařským řezem). Výsledky shrnuje tab. 2.
Table 2. Výsledky mechanické embolektomie. 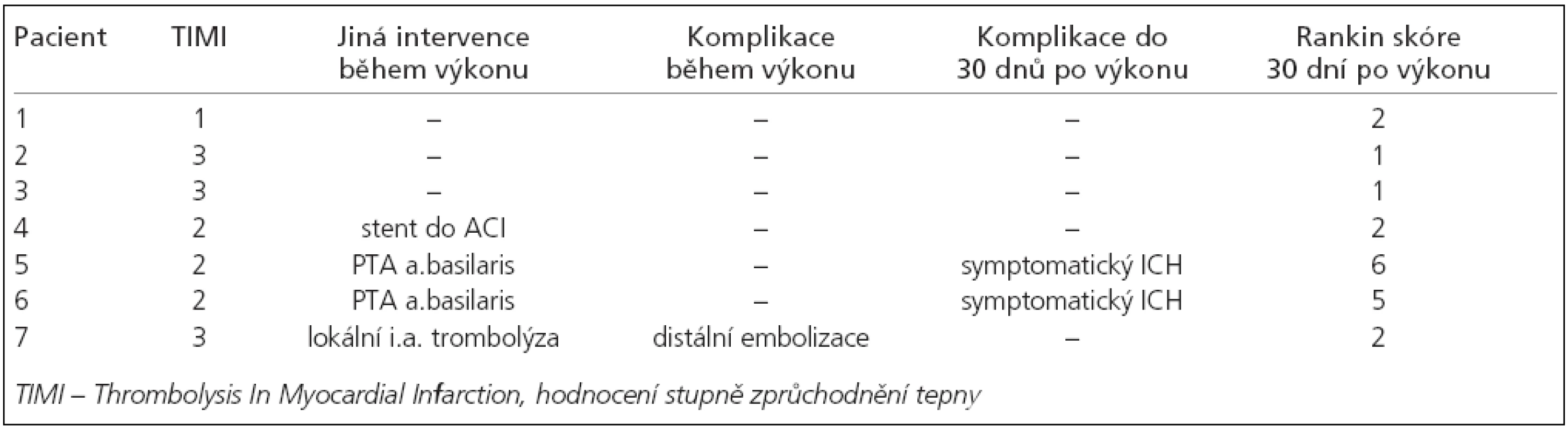
Diskuse
Léčba akutní mozkové ischemie pomocí embolektomie není ideou posledních let. První chirurgická embolektomie mozkové tepny byla popsána již v roce 1956 Welchem [7]. Během dalších dekád byly publikovány články o chirurgické embolektomii u malých souborů pacientů, především s postižením střední mozkové tepny [8]. Navzdory těmto úspěšným pokusům se chirurgická embolektomie nikdy nestala metodou volby, protože výkon je vcelku časově náročný, nese s sebou další trauma pro iktem poškozený mozek a není snadný. Zdárně a také rychle ji dokáže provést jen vysoce erudovaný cévní neurochirurg.
Postupem času se zájem přesměroval k trombolytické terapii a endovaskulárnímu řešení, které se zdálo být bezpečné a rychlé. Žádná z dříve dostupných pomůcek však nebyla navržena k embolektomii z mozkového řečiště. Fogartyho embolektomický balonkový katétr byl používán k embolektomii ve vnitřní karotidě, jeho použití v intrakraniálním úseku karotidy bylo doprovázeno rizikem vzniku disekcí či karotidokavernózních píštělí [9-11].
Bylo publikovány i kazuistiky o možnosti endovaskulární intrakraniální embolektomie pomocí mikrolasa či minikošíku [12-15]. Ačkoliv tyto pomůcky byly vyvinuty především pro odstraňování cizích těles a nikoliv embolu z cévního řečiště, první zkušenosti byly slibné. Další možnosti, které se dají uplatnit při léčbě akutního uzávěru mozkové tepny, jsou: i.a. aplikace trombolytika [16], čistě mechanické rozrušení trombu mikrovodičem, mikrokatétrem nebo balonkem, mechanické rozrušení s podporou trombolytik, kombinované podání trombolytika intravenózně a intraarteriálně [17] a další možností je použití laseru [18], ultrazvuku [19] nebo rheolytické trombektomie [20].
V České republice jsou v současné době schváleny standardní postupy pro léčbu akutní ischemické CMP [2]. Do 3 hodin od jasně definovaného začátku příznaků je u vhodných pacientů doporučeno podání rtPA – alteplázy (Actilyse, Boehringer Ingelheim) intravenózně v dávce 0,9 mg/kg v infůzi během 60 minut, 10 % dávky podat jako úvodní bolus.
Tento postup léčby, jak již bylo zmíněno, je vhodný u pacientů s příznaky vzniklými do 3 hodin před léčbou. Většina pacientů se však dostává do rukou lékaře mimo toto ideální terapeutické okno.
U pacientů s angiograficky prokázanou okluzí a. cerebri media, kteří mohou být léčeni do 6 hodin od objevení prvních příznaků, je schválena u ischemické CMP intraarteriální trombolytická terapie [21]. Při uzávěru a. basilaris, jejíž neléčení má výrazně horší prognózu [22,23], je možné se pokusit o i.a. trombolýzu i za hranicí 6 hodin.
Intraarteriální trombolýza se stala alternativou k i.v. podání. Výrazně k tomu pomohl rozvoj neuroradiologie, vývoj jemných mikrokatétrů a mikrovodičů, kterými jsme schopni nasondovat postiženou tepnu a rychle a lokálně aplikovat trombolytikum.
Nevýhodou i.a. trombolýzy je nutnost přítomnosti zkušeného intervenčního neuroradiologa, angiografického týmu a zázemí iktové jednotky, které jsou k dispozici převážně jen ve velkých nemocnicích. Oproti i.v. podání je i nevýhodou delší doba potřebná k začátku léčby, která je způsobena především převozem pacienta na angiografický sál a sondováním postižené cévy.
Mechanická embolektomie
Mechanická intervence (MI) je vhodná jednak pro nemocné, u kterých je trombolýza kontraindikována, a dále u nemocných s akutní ischemickou příhodou, kteří se dostávají k lékaři až po ideálním tříhodinovém terapeutickém okně [24].
Další skupinou mohou být pacienti léčení i.v. trombolýzou, jejichž odezva na léčbu je minimální [24].
Využitím mechanického odstraňovače trombů při léčbě akutních mozkových příhod u takovýchto pacientů se věnovaly multicentrické studie MERCI I a II (Mechanical Embolus Removal in Cerebral Ischemia) [3]. Studie prokazuje 48% úspěšnost rekanalizace a mírně nižší procento vzniku symptomatického intrakraniálního krvácení do 24 hodin než u trombolytické terapie (8 % při MI vs 10 % při i.a. terapii) [3]. Poukazuje i na komplikace vzniklé manipulací mikrokatétru a mikrovodiče v tepnách mozku, jako je perforace, disekce, distální embolizace či odlomení části zařízení [3]. V 90denním sledování však mechanická rekanalizace nepřinesla lepší klinické výsledky než PROACT II studie [25]. Přesto se domníváme, že v neurointervenčních centrech je to metoda volby.
Všechny zmíněné metody léčby akutní ischemické příhody mají za cíl rekanalizovat uzavřenou cévu a minimalizovat neurologický deficit. Všeobecně je uznávána myšlenka, že čím dříve je léčba provedena, tím menší neurologický deficit je po léčbě pravděpodobnější [26].
Je nutné si však uvědomit, že rekanalizace není totéž co reperfuze. Angiografické zobrazení obnovení toku má dvě části: rekanalizaci uzavřené hlavní větve a reperfuzi distálního řečiště a mozkové tkáně. Rekanalizace hlavní větve může být kompletní a přesto plnění distálních větví a reperfuze tkáně nemusí být ideální. V tomto jevu jistě svou roli hraje distální embolizace. Efekt distálních drobných embolů není ještě dobře prozkoumán, ale je zřejmé, že má nepříznivý vliv na výsledný klinický výsledek.
Hodnocení klinických výsledků pacientů léčených pomocí mechanické embolektomie do 8 hodin od začátků příznaků je zatím předmětem studia a určitá průkazná data lze očekávat až od probíhající randomizované studie MR RESCUE [27].
Závěr
Mechanická embolektomie pomocí Merci mikrokatétru se zdá být vhodnou metodou léčby akutní ischemické příhody u pacientů v terapeutickém okně do 8 hodin od začátku příznaků nebo u pacientů kontraindikovaných k i.v. či i.a. trombolýze nebo po neúspěšné trombolýze. Na specializovaných neuroradiologických pracovištích by se tento způsob léčby mohl stát metodou s vysokou úspěšností rekanalizace a s nízkým procentem peri a postprocedurálních komplikací. Pro pacienta by mechanická intervence mohla přinést výhodu v prodloužení možného terapeutického okna.
Podpořeno grantem IGA MZ NR/9435-3
prim. plk. MUDr. František Charvát, Ph.D.
RDG oddělení
Ústřední vojenská nemocnice, Praha 6 – Střešovice
U vojenské nemocnice 1200
169 02
E-mail: frantisek.charvat@uvn.cz
Přijato k recenzi: 28. 3. 2007
Přijato do tisku: 6. 8. 2007
Sources
1. Krajina A, Krajíčková D, Lojík M, Žižka J, Náhlovský J, Ungermann L. Endovaskulární léčba při ischemických cévních mozkových příhodách. In: Krajina A, Peregrin JH. Intervenční radiologie-miniinvazivní terapie. 1 ed. Hradec Králové: Olga Čermáková 2005 : 382-396.
2. Školoudík D, Bar M, Mikulík R, Neumann J, Václavík D, Herzig R et al. Standard pro podání systémové trombolýzy pacientům s akutním mozkovým infarktem. Neurol pro praxi 2006; 1 : 53-56.
3. Smith WS, Sung G, Starkman S, Saver JL, Kidwell CS, Gobin YP et al. Safety and efficacy of mechanical embolectomy in acute ischemic stroke. Results of the MERCI Trial. Stroke 2005; 36 : 1432-1428.
4. Kalina M. Akutní neurologie. Intenzivní péče v neurologii. Praha: Triton 2000 : 172-175.
5. Junghans U, Seitz RJ, Wittsack HJ, Aulich A, Siebler M. Treatment of acute basilar artery thrombosis with a combination of systemic alteplase and tirofiban, a nonpeptide platelet glycoprotein IIb/IIIa inhibitor: Report of four cases. Radiology 2001; 221 : 795-801.
6. The TIMI Study Group. Special Report. The thrombolysis in myocardial infarction (TIMI) trial. N Engl J Med 1985; 312 : 932-936.
7. Welch K. Excision of occlusive lesions of the middle cerebral artery. J Neurosurgery 1956; 13 : 73-80.
8. Meyer FB, Piepgras DG, Sundt TJ, Yanagihara T . Emergency embolectomy for acute occlusion of the middle cerebral artery. J Neurosurgery 1985; 62 : 639-647.
9. Fogarty TJ, Cranley JJ, Krause RJ, Strasser ES, Hafner CD. A method for extraction of arterial emboli and trombi. Surg Gynecol Obst 1963; 116 : 241.
10. Davie JC, Richardson R. Distal internal carotid thrombo-embolectomy using a Fogarty catheter in total occlusion. J Neurosurgery 1967; 27 : 171-177.
11. Konig HJ, Krahling KH, Brandt M. Carotid-cavernous sinus fistula as a complication of embolectomy using a Fogarty catheter. Neurosurg Rev 1981; 4 : 191-192.
12. Wikholm G. Mechanical intracranial embolectomy: A report of two cases. Int Neuroradiol 1998; 4 : 159-164.
13. Wikholm G. Transarterial embolectomy in acute stroke. Am J Neuro-Radiol 2003; 24 : 892-894.
14. Mayer TE, Hamann GF, Brueckmann HJ. Treatment of basilar artery embolism with a mechanical extraction device. Stroke 2002; 33 : 2232-2235.
15. Krajina A, Krajíčková D, Špriňar Z, Nikolov DH, Pařízková R, Lojík M et al. Mechanická perkutánní extrakce embolu při akutní cévní mozkové příhodě: kazuistika a přehled literatury. Česk Slov Neurol N 2005; 65/101 : 51-57.
16. Beneš V, Zabramski JM, Boston M, Puca A, Spetzler RF. Effect of intraarterial tissue plasminogen activator and urokinase on autologous arterial emboli in the cerebral circulation. Stroke 1990; 21 : 1594-1599.
17. Combined intravenous and intra-arterial recanalization for acute ischemic stroke: The interventional management of stroke study. Stroke. 2004; 35 : 904–911.
18. Nesbit GM, Luh G, Tien R, Barnwell SL. New and future endovascular treatment strategies for acute ischemic stroke. J Vasc Intervent Radiol 2004; 15 : 103-110.
19. Školoudík D, Bar M, Škoda O, Václavík D, Hradílek P, Šimíčková K. Bezpečnost a účinnost trombotripse - akcelerace trombolýzy pomocí ultrazvuku. Česk Slov Neurol N 2004; 67/100 : 157-161.
20. Bellon RJ, Putman CM, Budzik RF, Pergolizzi RS, Reinking GF, Norbash AM. Rheolytic thrombectomy of the occluded internal carotid artery in the setting of acute ischemic stroke. Am J Neuroradiol 2001; 22 : 526-530.
21. Del Zoppo GJ, Higashida R, Furlan AJ, Pesssin MS, Rowley HA, Gent M. PROACT: a phase II randomised trial of recombinant pro-urokinase by direct arterial delivery in acute middle cerebral artery stroke: PROACT Investigators: prolyse in acute cerebral thromboembolism. Stroke 1998; 29 : 4-11.
22. Becker KJ, Monsein LH, Ulatowski J, Mirski M, Williams M, Hanley DF. Intraarterial thrombolysis in vertebrobasilar occlusion. Am J Neuroradiol 1996; 17 : 255-262.
23. Morgan MK, Grinnell V, Little NS, Day MJ. Successful treatment of an acute stroke thrombosis of an intracranial vertebral artery endarterectomy with urokinase. Neurosurgery 1994; 35 : 978-981.
24. Kim D, Jahan R, Starkman S, Abolian A, Kidwell CS, Vinuela F et al. Endovascular mechanical clot retrieval in a broad ischemic stroke cohort. Am J Neuroradiology 2006; 27 : 2048-2052.
25. Furlan AJ, Fischer M. Devices, drugs, and the Food and Drug Administration: increasing implications for ischemic stroke. Stroke. 2005; 36(2): 398-399.
26. Marler JR, Tilley BC, Lu M, Brott TG, Lyden PC, Rotta JC et al. Early stroke treatment associated with better outcome: the NINDS rt-PA stroke study. Neurology 2000; 55 : 1649-1655.
27. MR rescue: MR and recanalization of stroke clots using embolectomy. Available from URL: http://clinicaltrials.gov/ct/show/NCT00094588.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2008 Issue 1-
All articles in this issue
- Klinické využití protilátek u roztroušené sklerózy
- Idiopatické generalizované epilepsie s typickými absencemi v dospělosti
- Difuzní gliomy mozkového kmene u dětí. Noční můra dětského onkologa.
- Bezpečnosť MRI vyšetrenia u pacientov s kovovými implantátmi a implantovanými prístrojmi
- Mikroskopický nález kryptokoka v mozkomíšním moku jako první příznak rozvinutého stadia AIDS. Kazuistika
- Myastenie s pozitivními anti-MuSK protilátkami u mladého muže: kazuistika
- Myasténia gravis
- Ovlivnění plazmatické hladiny homocysteinu u pacientů s Parkinsonovou chorobou terapií L-DOPA a entacaponem
- Efekt nízké dávky manitolu na sérovou osmolalitu
- Mechanická embolektomie pomocí Merci katétru u nemocných s akutním uzávěrem mozkových tepen
- Komplementarita stentingu a endarterektomie karotid: tříleté zkušenosti
- Ageneze laterálního semicirkulárního kanálku: kazuistika
- Vznik neuritidy optického nervu v důsledku mukokély vedlejších nosních dutin - příčinná souvislost či koincidence? Kazuistika
- Případ multifokální encefalitidy reagující na léčbu steroidy jako příčiny obtížně zvládnutelných epileptických záchvatů frontálního laloku
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Bezpečnosť MRI vyšetrenia u pacientov s kovovými implantátmi a implantovanými prístrojmi
- Difuzní gliomy mozkového kmene u dětí. Noční můra dětského onkologa.
- Myasténia gravis
- Klinické využití protilátek u roztroušené sklerózy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

