-
Medical journals
- Career
Komplikace operací z předního přístupu pro degenerativní onemocnění krční páteře
Authors: L. Hrabálek 1; M. Vaverka 1; B. Kupka 2; M. Houdek 1
Authors‘ workplace: Neurochirurgická klinika FN a LF UP Olomouc 1; Neurologická klinika FN a LF UP Olomouc 2
Published in: Cesk Slov Neurol N 2007; 70/103(2): 201-206
Category: Short Communication
Overview
Přední přístup ke krční páteři považujeme za šetrný a bezpečný, a proto bývá provázen výskytem malého množství komplikací. Přesto i zdánlivě menší pooperační obtíže z operačního přístupu nebo po odběru kostního štěpu z lopaty kosti kyčelní někdy ruší jinak pozitivní efekt operačního zákroku. Cílem této práce je zhodnocení charakteru a frekvence výskytu těchto obtíží.
Retrospektivně jsme hodnotili výsledky 255 operací s minimální dobou sledování 2 roky. Nejčastější komplikací operačního přístupu ke krční páteři byla dysfagie. Vyskytla se u 23,7 % pacientů a prokázali jsme závislost na počtu operovaných etáží. Statisticky signifikantně častější byla dysfagie u víceetážových výkonů a souvisela tedy s rozsahem expozice přední plochy páteře. Dysfonie se objevila celkem u 13,9 % pacientů, vymizela do 6 měsíců u 12,7 % nemocných a jen u 1,2 % pacientů trvala déle. Komplikace z odběrového místa kostního štěpu se vyskytly u 41,5 % pacientů, byly malé u 31,2 % nemocných a velké (bolest v odběrovém místě trvající déle jak 6 měsíců, trvalá meralgia paresthetica, fraktura hřebene kosti kyčelní nebo absces v odběrovém místě) u 10,3 % pacientů.Klíčová slova:
krční páteř – degenerativní onemocnění páteře – operace – přední přístup – odběr kostního štěpu – komplikaceÚvod
Degenerativní onemocnění krční páteře může vést ke kompresi nervových struktur s projevy radikulopatie, myelopatie nebo ke kombinaci obou postižení. Příčinou je buď hernie disku, stenóza způsobená spondylózou nebo nestabilita v páteřním segmentu. K operaci se přistupuje u nemocných s ložiskovými neurologickými příznaky při adekvátním nálezu na zobrazovacích metodách, a to po selhání komplexní konzervativní terapie nebo při rychle progredujícím neurologickém deficitu.
Příčina patologického stavu je v naprosté většině případů degenerativní onemocnění meziobratlové ploténky, proto se základní operací stala disektomie vyžadující přední operační přístup. Metodiku operace zavedli Smith a Robinson v roce 1955. K náhradě meziobratlové ploténky používali trikortikální štěp [1]. Tato metoda byla dále dopracována dalšími autory [2]. Vývoj této metody završil Caspar zavedením sofistikovaného instrumentária pro operační přístup i vlastní výkon na krční páteři [3]. V současnosti je již běžné ošetření degenerativního onemocnění krční páteře předním výkonem vysoce efektivní a je všeobecně považováno za šetrné, s výskytem malého množství nezávažných komplikací. Často se pak do popředí dostávají obtíže způsobené přístupovou cestou ke krční páteři a v místě odběru kostního štěpu.
Cílem této práce je zhodnocení komplikací předního operačního přístupu ke krční páteři a komplikací vztažených k odběrovému místu kostního štěpu.
Materiál a metodika
V rozmezí let 1993 až 2003 jsme operovali z předního přístupu 244 pacientů s degenerativním onemocněním krční páteře. Pro selhání štěpu nebo rozvoj syndromu sousedního segmentu (adjacent segment syndrome) bylo 11 nemocných reoperováno, takže celkem se jednalo o 255 operačních výkonů provedených předním přístupem.
K operaci jsme indikovali 144 pacientů pro radikulopatii, 22 pacientů pro myelopatii, 69 pacientů pro myeloradikulopatii a 11 pro cervikalgii a cefaleu nereagující na konzervativní léčbu.
Patologicko anatomickou příčinou klinického obrazu těchto pacientů bylo degenerativní onemocnění krční páteře, a to v jednom prostoru u 142 nemocných, ve dvou prostorech u 78 nemocných a ve třech prostorech u 24 pacientů.
Standardní náhradou meziobratlové ploténky byl autogenní trikortikální štěp odebíraný z hřebene kosti kyčelní, který byl použit u 150 operací. Harmsův košík byl náhradou ve 3 případech, 15 operací v počátečním období bylo provedeno bez náhrady disku. Od roku 1997 jsme používali výhradně náhradní materiály, resp. bioaktivní sklokeramický implantát BAS-0, který jsme implantovali 87 pacientům.
Ve 150 případech byla stabilita operovaného segmentu zajištěna trapézovou dlahou s bikortikálním nebo unikortikálním zavrtáním fixačních šroubů. Od roku 1995 jsme používali pouze titanový materiál. K fixaci segmentu jsme přistupovali u všech operací ve více prostorech nebo u jednoprostorových operací s předpokládanou mimořádnou zátěží segmentu v pooperačním období.
Průměrný věk 244 nemocných byl 49,8 roku, z toho bylo 150 mužů ve věku 29-74 let s průměrným věkem 50,3 roku a 94 žen ve věku 32-72 let s průměrným věkem 49,0 let.
Operační technika předního operačního přístupu ke krční páteři
Asi 30 minut před incizí dostal každý pacient intravenózně první dávku antibiotické profylaxe. Intubace byla vždy orotracheální.
Operovaný byl na operačním sále připraven v supinační poloze s mírným záklonem hlavy, podložením krku a se stažením ramen kaudálně. Tím byla dána možnost provést bočnou rentgenovou kontrolu během operace. Operovali jsme z pravé strany, jen v případech výkonů na prostorech C6/7 nebo C7/Th1 jsme zpravidla přistupovali ze strany levé pro menší pravděpodobnost poranění n. laryngeus recurrens (NLR). Kožní řez jsme zaměřovali na operovanou etáž pomocí RTG (C-rameno).
Incize byla vedena horizontálně ve směru kožních řas, začínala ve střední čáře a byla 3-5 cm dlouhá. Kratší incize byla u žen s operací v jednom prostoru. Následovala discize m. platysma a povrchové krční fascie podél vnitřního okraje m. sternocleidomastoideus. M. omohyoideus jsme zachovali vždy u operací v jednom prostoru a zpravidla jsme jej přerušovali u operací ve více prostorech. Preparace do hloubky byla převážně tupá, a. carotis communis se přitom odsouvala laterálně a středočárové krční struktury kontralaterálně (hrtan, průdušnice, štítná žláza, hltan a jícen). Často bylo nutné podvázat přemosťující tyreoideální cévy, tedy vas thyroideale superius et inferius. Nervové struktury, zejména n. vagus a jeho větve NLR a n. laryngeus superior (NLS) jsme šetřili, ale byli jsme nuceni přerušit některá vlákna z ansa n. hypoglossus a plexus pharyngeus. V podélném směru jsme incidovali hlubokou krční resp. prevertebrální fascii a preparovali přední plochu páteře. Ostře jsme oddělovali mediální okraje obou mm. longi colli a odsouvali je laterálně. Pomocí bočného rtg jsme si ověřovali vypreparovanou etáž a dokončili preparaci segmentu. Casparovy rozvěrače opřené o okraje m. longus colli nám následně zajistily retrakci středočárových krčních struktur mediálně. Opět pod boční rtg-kontrolou jsme zavrtali distrakční šrouby do obratlových těl a následně použitý distraktor nám umožnil zvýšit meziobratlový prostor o 1-3 milimetry.
Po této makroskopické fázi následovala mikroskopická část výkonu za použití operačního mikroskopu Zeiss NC 4 nebo Olympus 5000. Odstranili jsme meziobratlovou ploténku včetně krycích chrupavčitých desek a současně i hernii disku, popřípadě dorzální nebo unkovertebrální osteofyty. Použili jsme k tomu lžičky a klíšťky a při výraznější spondylóze i elektrické nebo vzduchové mikrofrézy. K dokonalému přehledu o epidurálním prostoru jsme protínali současně i zadní podélný vaz a definitivně tak dekomprimovali durální vak míšní a kořeny.
Poté jsme pokračovali již bez operačního mikroskopu a další fází operace byla náhrada meziobratlové ploténky s cílem provedení fúze. K tomu jsme použili trikortikální kostní štěp nebo Harmsův titanový košík vyplněný spongiózní kostí (autotransplantáty) nebo sklokeramický implantát BAS-0. Odběr kostního štěpu jsme prováděli z hřebene lopaty kosti kyčelní pomocí vibrační pily a originálních Casparových štípacích kleští. Odběr štěpu byl přísně subperiostální, periost byl rekonstruován přímou suturou. Defekt v kosti nebyl vyplňován, spongióza byla ošetřena zavoskováním a ve všech případech bylo standardně použito Redonovo sání.
Redonův drén jsme vkládali také na přední plochu páteře a operační ránu uzavírali suturou m. platysma a podkoží. Kůži jsme šili intradermálně.
Nemocní po operaci byli standardně vertikalizováni první pooperační den nebo výjimečně již ve večerních hodinách po výkonu. Fixaci ortopedickým límcem typu Philadelphia jsme u nemocných po výkonu, zabezpečeném dlahou, snímali po převazu rány první pooperační den. Nemocní ošetření bez dlahy nosili límec šest týdnů. Délka hospitalizace byla maximálně 7denní.
Hodnocení pooperačních komplikací
Během hospitalizace jsme provedli první pooperační hodnocení neurologického stavu a případných operačních komplikací. V případech chrapotu trvajícího déle než 3 dny jsme nechali provést na ORL-klinice laryngoskopické vyšetření. Po propuštění chodili pacienti na kontroly ambulantně, vždy včetně RTG-kontroly (bočního a předozadního snímku krční páteře) v intervalech 6 týdnů, 3 měsíců, 6 měsíců a l rok po operaci. Ke zhodnocení stavu po více než 1 roce od operace jsme vytvořili dotazník, který byl zaslán všem pacientům. Dotazník zahrnoval m.j. otázku, zda přetrvávají případné polykací obtíže, chrapot a bolest v jizvě po odběru kostního štěpu. Odpovědělo 151 pacientů, tedy 62 % dotázaných.
Hodnocení pooperačních komplikací jsme prováděli retrospektivně z chorobopisů, z ambulantní dokumentace a vyhodnocením dotazníků.
Komplikace jsme rozdělili na 2 skupiny. První tvořily problémy přímo vztažené k operačnímu přístupu na přední plochu páteře, druhou potíže v místě odebraného kostního štěpu.
Obtíže pacienta charakterizované chrapotem, tichým hlasem nebo zvýšenou únavností hlasu jsme popsali jako dysfonii. Stížnosti pacientů na váznutí či ztížení prostupu sousta při polykání nebo pocit tlaku, sevření a překážky v krku jsme hodnotili jako dysfagii.
Komplikace z odběrového místa kostního štěpu (vždy se jednalo o hřeben lopaty kosti kyčelní) jsme sledovali u pacientů po odběrech trikortikálního kostního štěpu (takto bylo operováno 144 pacientů) a nebo při odběru spongiózy do Harmsovy klícky (takto byli operováni 3 pacienti), potenciálně bylo tedy ohroženo 147 pacientů.
Dysfonii, dysfagii a bolesti v místě odběru kostního štěpu jsem hodnotili jako krátkodobé, pokud netrvaly déle než 6 měsíců, a dlouhodobé v případě trvání delším než 6 měsíců.
Při statistickém zpracování dat jsme použili Studentův T-test a χ2 analýzu.
Výsledky
Typ operační komplikace z předního přístupu, počty a procenta postižených pacientů a eventuálně délku trvání obtíží uvedádí tab 1.
Table 1. Komplikace z předního operačního přístupu. 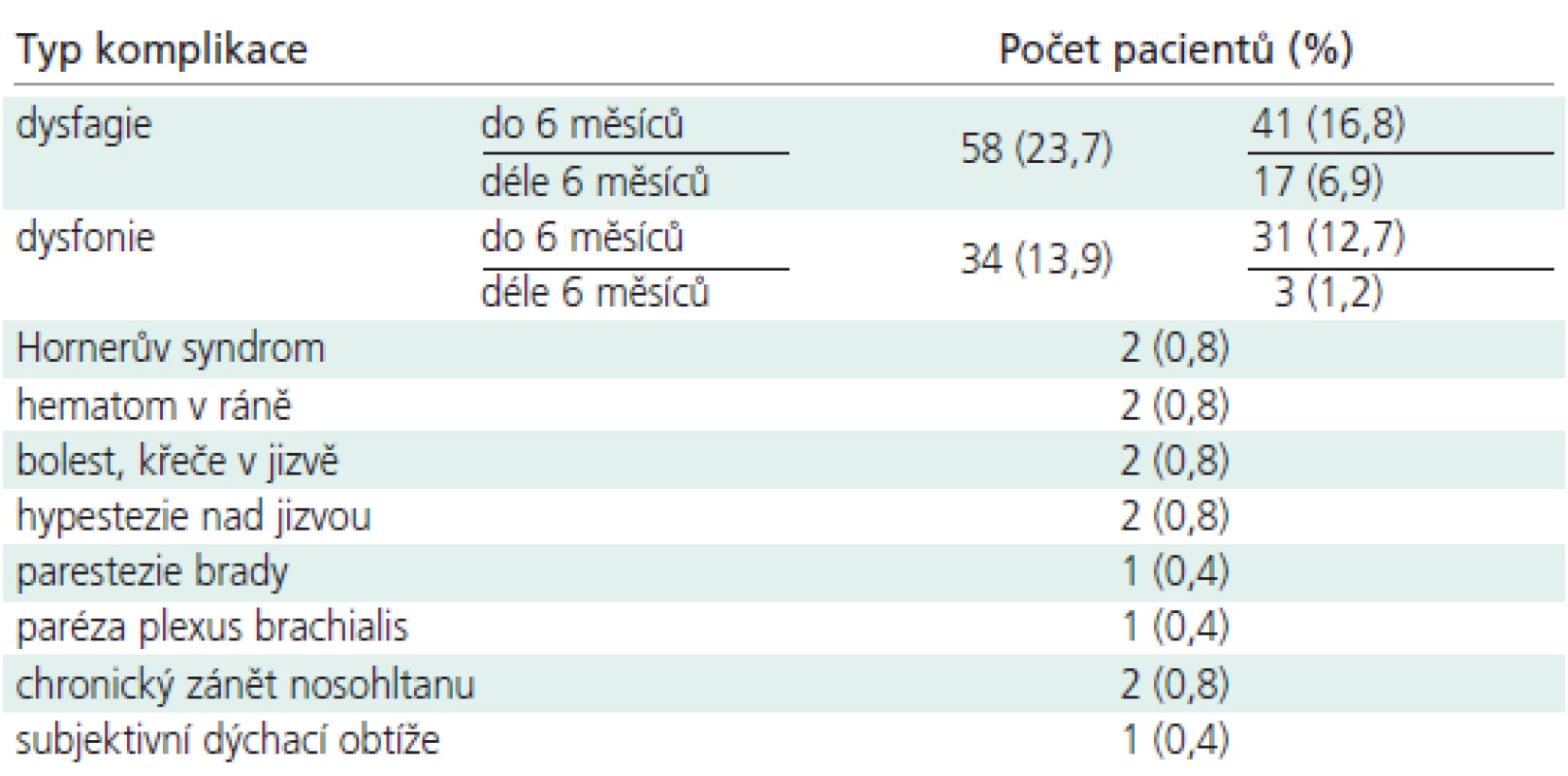
Výskyt dysfagie v závislosti na množství a úrovni operovaných prostor rozebírá tab. 2. Zjištěné rozdíly byly statisticky signifikantní při 5% hladině významnosti. Při podrobnějším rozboru dat byla významně častější dysfagie po operacích ve 3 prostorech v etáži C4-7 ve srovnání se všemi výkony 2 - a 1prostorovými. U 3prostorových operací v etáži C3-6 jsme totéž prokázali pouze ve srovnání s výkony v segmentu C4/5. Dysfagie byly dlouhodobé po operacích ve 3 prostorech u 5 z 24 pacientů (20,8 %), u výkonu ve 2 prostorech u 8 ze 78 pacientů (10,2 %) a u 1prostorových operací u 4 ze 142 pacientů (2,8 %).
Table 2. Počet nemocných s dysfagií v závislosti na počtu a úrovni operovaných meziobratlových prostorů. 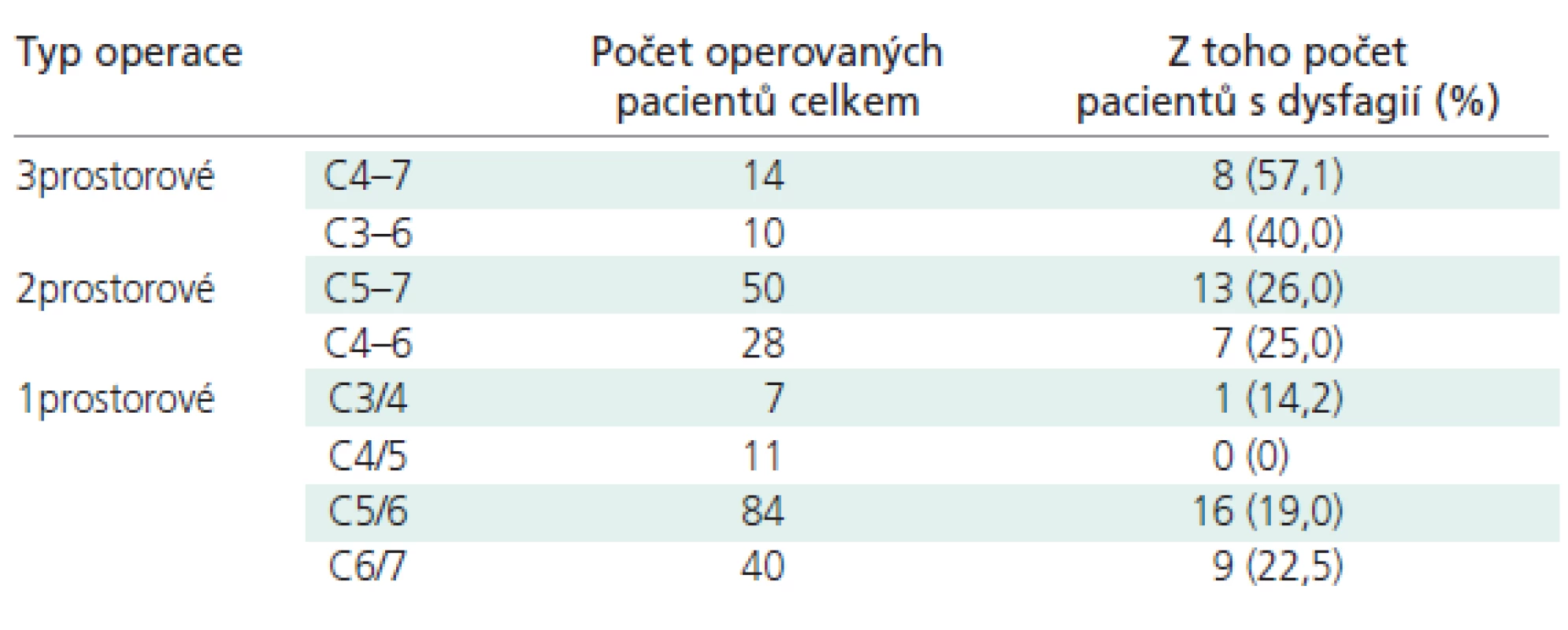
K laryngoskopicky jasně prokázané paréze NLR došlo ve 2 případech (0,8 %). Operován byl vždy prostor C6/7 zprava a k úpravě došlo do 6 měsíců od operace. U 3 pacientů s dlouhodobou dysfonií přitom nebyla známka poranění NLR. K transcizi NLS došlo u 1 pacienta při operaci v prostoru C4/5 zprava a nerv byl ošetřen mikrosuturou. Paréza se projevila nenápadnou změnou barvy hlasu a k ústupu dysfonie došlo během 6 měsíců.
Ze 34 pacientů s dysfonií mělo současně dysfagii 19 nemocných, tedy plných 56 % (dysfagie byla dočasná u 15 a dlouhodobá u 4 pacientů). Naopak u 58 operovaných s dysfagií mělo současně dysfonii 21 z nich, tedy 36 % (dysfonie byla dočasná u 20 a dlouhodobá u 1 pacienta). Pouze jeden pacient měl dlouhodobou dysfonii i dysfagii současně.
Další komplikace z předního přístupu byly výrazně méně časté. V případě Hornerova syndromu, který vznikl po 1prostorových operacích na C5/6 a na C6/7 poraněním plexus sympaticus cervicalis, resp. jeho pleteně v m. longus colli, bylo postižení u obou pacientů trvalé.
Hematom v ráně způsobil kompresi a otok hrtanu s následnou dušností ve 2 případech. Byl tak důvodem k urgentní revizi rány s evakuací krevních koagul. Významný zdroj krvácení zjištěn nebyl a příčinou bylo ucpání Redonova sání.
Hypestezie nad jizvou, parestezie brady a bolest v jizvě ustoupily do 6 měsíců u všech pacientů.
Příčinou parézy plexus brachialis u 1 nemocného byla komprese plexus brachialis při stažení ramen a záklonu hlavy a současném náhodném výskytu costa cervicalis. Paréza trvala 1 týden a byla jednostranná.
Nebyla zcela jasná závislost na operačním přístupu u pacientů, kteří měli zánět nosohltanu nebo udávali dýchací potíže bez zjevné objektivní příčiny.
Typ komplikace v místě odběru kostního štěpu, počty a procenta postižených pacientů a eventuálně délku trvání obtíží uvádí tab. 3.
Table 3. Komplikace v místě odběru kostního štěpu. 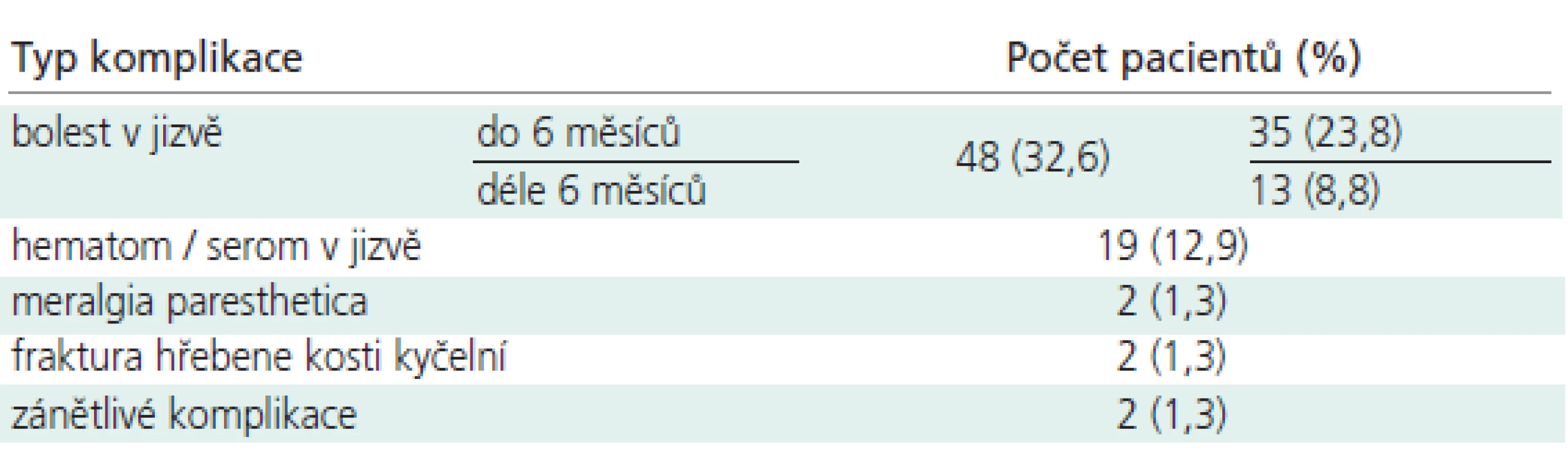
Celkem se komplikace z odběru kostního štěpu vyskytly u 61 ze 147 pacientů (41,5 %), z toho 12 pacientů mělo dva typy komplikací. Malé komplikace, jako krátkodobou bolest nebo hematom v místě po odběru štěpu, mělo 46 pacientů (31,2 %). Velké komplikace, jako dlouhodobou bolest v místě odběru štěpu, trvalou meralgia paresthetica, frakturu hřebene lopaty kosti kyčelní nebo absces v odběrovém místě mělo 15 pacientů (10,3 %).
Bolesti v místě odběru kostního štěpu byly nejčastějším steskem. V pátrání po příčině bolesti jsme zjistili, že ze 48 pacientů s pooperační bolestí mělo jen 8 hematom či serom v odběrovém místě (16,6 %). Hematom nebo serom nikdy nebyly dlouhodobým problémem. Vyřešily se zpravidla během 2-3 týdnů spontánní resorpcí nebo opakovanými punkcemi podkoží a nevyžádaly si reoperaci.
Meralgia paresthetica z tupého poranění n. cutaneus femoris lateralis byla v 1 případě trvalého rázu, bez reakce na lokální obstřiky a pacient odmítl operační revizi.
K fraktuře hřebene lopaty kosti kyčelní došlo následkem nesprávného odběru štěpu příliš ventrálně při spina iliaca anterior superior s jejím částečným odlomením. Ke zhojení bez komplikací došlo v obou případech.
Povrchový kožní zánět u jednoho pacienta se rychle zhojil při antibiotické terapii. Hluboký absces v odběrovém místě u dalšího pacienta si vyžádal operační revizi s lokální sanací a následným zhojením.
Diskuse
Za příčinu polykacích obtíží se všeobecně považuje částečná denervace hltanu přerušením vláken z plexus pharyngeus nebo rami pharyngei z n. vagus a při oboustranném přístupu může vést až k těžké dysfagii s nutností provedení gastrostomie [4]. Výjimečně může dojít i k poranění hypofaryngu při přístupu na horní etáže krční páteře. Bertalanffy to ve svém souboru udává v 0,2 % případů [5]. Příčinou snazšího poranění hypofaryngu je tenčí svalová stěna ve srovnání s jícnem. Dočasné polykací obtíže vznikají také často následkem lokálního otoku hltanu a jícnu po operaci [5]. Dysfagie je udávána v rozmezí 7-35 % [4-7]. V našem souboru to bylo průměrných 23,7 % a nikdy nedošlo k perforaci hltanu nebo jícnu, u žádného z pacientů nebyla dysfagie natolik závažná, aby si vyžádala zavedení žaludeční sondy.
U dysfonie je příčinou lokální otok hrtanu nebo paréza NLR [5,8,9]. V případech parézy NLR většinou nedochází k anatomickému přerušení nervu, ale k jeho kompresi z vnitřní strany hrtanu balonkem endotracheální kanyly nebo z vnější strany hrtanu rozvěračem, nejčastěji zřejmě kombinací obou faktorů. Apfelbaum kontrolou a snižováním tlaku v balonku endotracheální kanyly během operace snížil frekvenci výskytu parézy NLR ze 6,4 % na 1,69 % [8].
Komprese a trakce nervu rozvěračem z vnější strany hrtanu hrozí zvláště při přístupu na dolní etáže krční páteře zprava. Je to dáno odlišnými anatomickými poměry v průběhu NLR vpravo a vlevo. Vpravo odstupuje NLR pod a. subclavia dextra, zatímco odstup levého NLR se nachází kaudálněji, pod arcus aortae. Odtud vystupují rami tracheales, rami oesophagei a n. laryngeus inferior (NLI) inervující hlasivky [10]. Ebraheim popsal průběh NLR, který probíhá v superomediálním směru v sagitální rovině na pravé straně pod úhlem 25° ± 4,7°a vlevo 4,7° ± 3,7° [9]. NLR se nachází na etáži C7 ve žlábku mezi průdušnicí a jícnem vpravo povrchověji než vlevo (ventrálněji o 6,5 mm ± 1,2 mm a laterálněji o 7,3 mm ± 0,8 mm) a snadněji se tak vpravo poraní, zejména nestandardně umístěným rozvěračem [9]. To je hlavní důvod, proč jsme přestali prostory C6-Th1 operovat z pravé strany a nyní volíme přístup levostranný.
Méně často dochází k poranění NLR při příliš mediálním podvazu vas thyreoideum inferius. Abnormální odstup NLI může být příčinou jeho přerušení během preparace. Přibližně v 1 % případů není totiž pravý NLI rekurentní a vede přímo z n. vagus do hrtanu. Naproti tomu vlevo je nerekurentní NLI vzácný [9]. Dysfonie, kdy je příčinou paréza NLR, je popisována až v 16 % případů [4-6,8,11,12] a je dočasná, jen v 1-2 % případů je trvalého charakteru [5,13]. Apfelbaum považuje dysfonii za trvalou, trvá-li déle než jeden rok [8]. V našem souboru mělo prokazatelnou parézu NLR jen 0,8 % pacientů a vymizela do 6 měsíců. Nízké procento výskytu je pravděpodobně způsobeno tím, že na dolní etáže páteře volíme již jen levostranný přístup.
Výskyt Hornerova syndromu bývá uváděn v sestavách v 0,2-4 %. V našem souboru jsme jej zaznamenali ve srovnatelném počtu (0,8 %). Příčinou je poranění truncus sympaticus v m. longus colli [4,5,14]. Zranitelnější je truncus sympaticus v dolních etážích, protože sympatická pleteň v m. longus colli leží mediálněji v etáži C6 [14]. Tyto nálezy odpovídají našim zkušenostem, protože oba případy Hornerova syndromu vznikly po operacích v dolních segmentech páteře.
Respirační insuficience se v literatuře vyskytuje v 1 % [5]. V našem souboru jsme zaznamenali subjektivní dýchací potíže v 1 případě, avšak bez objektivních příznaků ventilační nedostatečnosti.
Hematom v ráně se nachází v 1 % případů [5,6] a tomu odpovídal i výskyt v našem souboru (0,8 %). Epidurální hematom popsal Bertalanffy v 0,9 % [5].
Infekční komplikace charakteru povrchové nebo hluboké infekce, subdurálního empyému nebo spondylodiscitidy se většinou nevyskytují, ale ve velkém souboru Bertalanffyho byly popsány ve 2 % [5]. Johnston udal 2 % septických komplikací [4]. Poranění dura mater s likvorovou píštělí udávají autoři do 2,5 % [5,9,14]. Žádná z těchto komplikací se v našem souboru nevyskytla.
V žádném z našich případů nedošlo k poranění velkých cév jako a. carotis communis, a. vertebralis nebo v. jugularis interna, nedošlo k poranění hrtanu, průdušnice, hltanu nebo jícnu. Neměli jsme komplikaci, která by vedla k úmrtí pacienta (mortalita 0 %).
Všem uvedeným komplikacím se dá předejít pouze šetrnou preparací, regulérním naložením rozvěračů při adekvátním uvolnění okrajů m.longus colli, pečlivou hemostázou, zkrácením operačního času a podáním kortikoidů k potlačení lokální otoku. V prevenci infekčních komplikací lze jen zdůraznit pečlivou přípravu operačního pole s použitím incizních folií. Peroperační antibiotická profylaxe je standardně používána na všech pracovištích. Musí respektovat aktuální mikrobiologickou situaci v operujícím zařízení a měla by mít odpovídající průnik do tkáně disku [16,17].
Významnou skupinu problémů tvoří komplikace v místě po odběru štěpu. Vyskytují se v 5-49 % [11,18-20] a v našem souboru je mělo 41,5 % pacientů. Tyto obtíže mohou rušit pozitivní efekt operačního zákroku na krční páteři a bývají často jediným steskem pacienta i příčinou prodloužené hospitalizace. Dle našich zkušeností lze mnoha těmto komplikacím, zejména meralgii, fraktuře hřebene kyčelní kosti, zánětu nebo hematomu účinně předejít šetrným odběrem a podáním antibiotik. Ale i přes pečlivě provedený subperiostální odběr, ať už je proveden vibrační pilou nebo dlátem, se nelze vždy vyvarovat zejména následné bolesti. Bolest se může stát trvalou a pacienta výrazně obtěžuje. Toto je také hlavní důvod, proč se většina autorů snaží kostnímu odběru vyhnout, a proto používají k náhradě disku alogenní kostní štěp [21], bioaktivní sklokeramické materiály [22-25] nebo syntetické, např. titanové náhrady [26].
Dle Youngera a Chapmana se komplikace z odběru štěpu dělí na malé (bolest, sepse, necitlivost v odběrovém místě) a vyskytují se ve více než 20 % a na velké komplikace (zlomenina os ilium, heterotopní kostní formace, pánevní nestabilita), které jsou v dalších 5 % [27]. V našem souboru se vyskytly malé komplikace v 31,2 % a velké v 10,2 %. Mezi velké komplikace jsme ale zařadili i dlouhodobé bolesti v odběrovém místě (bez nich by se vyskytly velké komplikace jen ve 2,5 % případů).
Závěr
Dysfagie a dysfonie nepatří mezi velké komplikace, přesto jsou vnímané nemocným velmi negativně a často překryjí jinak příznivý výsledek operace. Výskyt dysfagie přímo souvisí s rozsahem expozice přední plochy krční páteře, a tím způsobené denervaci jícnu a hltanu. Důraz klademe na maximálně šetrný přístup s korektní polohou retraktorů zvláště u víceetážových výkonů. Dokonalá znalost anatomických poměrů v operačním poli sníží četnost výskytu poranění důležitých struktur. V případě výkonů na etážích C6/7 a C7/Th1 se lze vyhnout poranění NLR volbou levostranného přístupu pro jeho stranově příznivější anatomickou polohu.
Vzhledem k nástupu používání umělých náhrad meziobratlových plotének mizí problémy s odběrovým místem štěpu. V případě nutnosti použít autologní kostní štěp doporučují autoři přísně subperiostální odběr s dokonalou hemostázou.
MUDr. Lumír Hrabálek, Ph.D.
Neurochirurgická klinika FN a LF UP
I.P. Pavlova 6,
775 20 Olomouc
e-mail: lumir.hrabalek@seznam.cz
Přijato k recenzi: 16. 2. 2006
Přijato do tisku: 10. 8. 2006
Sources
1. Smith GW, Robinson RA. Anterolateral cervical disc removal and interbody fusion for cervical disc syndrome. Bull Johns Hopkins Med Soc 1955; 96 : 223-4.
2. Bailey RW, Badgley CE. Stabilisation of the cervical spine by anterior fusion. J Bone Point Surg Am 1960; 42 : 565-94.
3. Caspar W. Die ventrale intercorporale stabilisierung mit der HWS-Trapez-Osteosyntheseplatte: Indikation, Technik, Ergebnisse. Z Orthop 1981; 119 : 809-10.
4. Johnston FG, Crockard HA. One – stage internal fixation and anterior fusion in complex cervical spinal disorders. J Neurosurgery 1995; 82 : 234-8.
5. Bertalanffy H, Eggert HR. Complications of anterior cervical discectomy without fusion in 450 consecutive patients. Acta Neurochirurgica 1989; 99 : 41-50.
6. Heidecke V, Rainov NG, Burkert W. Anterior cervical fusion with the Orion locking plate system. Spine 1998; 23(16): 1796-1803.
7. Kostuik JP, Conolly PJ, Esses SI, Suh P. Anterior cervical plate fixation with the titanium hollow screw plate system. Spine 1993; 18(10): 1273-8.
8. Apfelbaum RI, Kriskovich MD, Halley JR. On the incidence, cause and prevention of recurrent laryngeal nerve palsies during anterior cervical spine surgery. Spine 2000; 25(22):2906-2912.
9. Ebraheim N, Lu J, Skie M, Heck BE, Yeasting RA. Vulnerability of the recurrent laryngeal nerve in the anterior approach to the lower cervical spine. Spine 1997 : 22(22): 2664-7.
10. Kos J. Periferní nervstvo. Systema nervosum periphericum. In: Borovanský L et al. Soustavná anatomie člověka II. 5th ed. Praha: Avicenum: 1976 : 950.
11. Gore DR, Sepic SB. Anterior discectomy and fusion for painful cervical disc disease. Spine 1998; 23(19): 2047-51.
12. Grisoli F, Graziani N, Fabrizi AP, Peragut JC, Vincentelli F, Diaz – Vasques P. Anterior discectomy without fusion for treatment of cervical lateral soft disc extrusion: a follow – up of 120 cases. Neurosurgery 1989; 24(6): 853–9.
13. Cuatico W. Anterior cervical discectomy without interbody fusion. An analysis of 81 cases. Acta Neurochirurgica 1981; 57 : 269-74.
14. Ebraheim NA, Lu J, Heck BE, Yeasting RA. Vulnerability of the sympathetic trunk during the anterior approach to the lower cervical spine. Spine 2000; 25(13):1603-1.
15. Dubuisson A, Lenelle J, Stevenaert. Soft cervical disc herniation: a retrospective study od l00 cases. Acta Neurochirurgica 1993; 125 : 115-9.
16. Rhoten RL, Murphy MA, Kalfas LH, Hahn JF, Washington JA. Antibiotic penetration into cervical discs. Neurosurgery l995; 37(3): 418-421.
17. Vaverka M, Petrželová J. Penetrace antibiotika do intervertebrálního disku. Acta chirurgie orthopaedicae et traumatologie Čechoslovaca 1991; 58(1-2): 98-103.
18. Banwart JCh, Aster MA, Hassanein RS. Iliac crest bone graft harvest donor site morbidity. Spine 1995; 20(9): 1055-60.
19. Kurz LT, Gardin SR, Booth RE. Harvesting autogenous iliac bone grafts: A review of complications and techniques. Spine 1989; 14 : 1324-31.
20. Thalgott JS, Fritts K, Giuffre JM, Timlin M. Anterior interbody fusion of the cervical spine with coralline hydroxyapatite. Spine 1999; 24(13): 1296-9.
21. Suchomel P, Barsa P, Buchvald P, Svobodník A, Vaníčková E. Autologous versus allogenic bone grafts in instrumented anterior cervical discectomy and fusion: a prospective study with respect to bone union pattern. Eur Spine J 2004; 13(6): 510-5.
22. Fuller DA, Stevenson S, Emery SE. The effects of internal fixation on calcium carbonate. Spine 1996; 21 (18): 2131-6.
23. Ibanez J, Carreno A, Garcia-Amorena C, Caral J, Gaston F, Ferrer E. Results of the biocompatible osteoconductive polymer (BOP) as an intersomatic graft in anterior cervical surgery. Acta Neurochirurgica 1998; 140 : 126-33.
24. Lozes G, Fawas A, Cama A, Krivosic I, Devos P at al. Discectomies of the lower cervical spine using interbody biopolymer (BOP) implants. Acta Neurochirurgica 1989; 96 : 88-93.
25. Rudinský B, Hill R. Intervertebrálna fúzia po použití biokeramickej náhrady NZ 2000 ( hydroxyapatit ) pri jeho dvojúrovňovej mikrodisektómii cervikálnej chrbtice. Acta Spondylologica 2002; 1(1): 16-20.
26. Suchomel P, Barsa P. Náhrada krční meziobratlové ploténky vložkou Cespace bez použití kosti či její náhrady. Prospektivní studie. Acta Spondylologica 2004; 3(1): 5-9.
27. Younger EM, Chapman MW. Morbidity at bone graft donor sites. J Orthop Trauma 1989; 3 : 192-5.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2007 Issue 2-
All articles in this issue
- Súčasný pohľad na diagnostiku a terapiu afázie
- Jednorázové intratékální podání baklofenu a následné zavedení pumpového systému v léčbě těžké spasticity u osob s roztroušenou sklerózou
- Chirurgická léčba ependymomů krční a horní hrudní míchy
- Komplikace operací z předního přístupu pro degenerativní onemocnění krční páteře
- Solitární fibrózní tumor mening
- Epilepsie a cyklus spánku a bdění
- Zhoršování epileptických záchvatů a epilepsií antiepileptiky - je to možné?
- Význam MR v indikaci systémové trombolýzy – analýza prvních 30 pacientů
- Specifické protilátky proti beta-tubulinu v diferenciální diagnostice demencí
- Riziko vzniku vaskulární příhody při léčbě fluvastatinem a fenofibrátem
- Korelace ptiO2 a apoptózy u fokální mozkové ischemie a vliv systémové hypertenze
- Radiochirurgická léčba schwannomu trojklaného nervu pomocí Leksellova gama nože
- Abnormální mikrostruktura spánku a autonomní odpověď u narkolepsie
- Turbulence srdeční frekvence v posouzení kardiální autonomní funkce u migreniků
- Bazaliom s propagací do mostomozečkového koutu asociovaný s ipsilaterálním neurinomem akustiku – kazuistika
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Epilepsie a cyklus spánku a bdění
- Súčasný pohľad na diagnostiku a terapiu afázie
- Komplikace operací z předního přístupu pro degenerativní onemocnění krční páteře
- Zhoršování epileptických záchvatů a epilepsií antiepileptiky - je to možné?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

