-
Medical journals
- Career
CT kolonografie – přehled vývoje metodiky a indikací
: P. Opletal; M. Standara
: Masarykův onkologický ústav, Brno
: Klin Onkol 2012; 25(4): 241-245
: Reviews
Východiska:
Technologický pokrok ve vývoji CT přístrojů a výpočetní techniky v polovině 90. let 20. století umožnil vizuální rekonstrukci vnitřního lumen dutých orgánů. Metoda, využívaná zejména pro zobrazení tračníku, se od počátku potýkala s mnoha obtížemi a limity způsobenými především nedostatečně propracovanou metodikou přípravy a distenze střeva a vysokou radiační zátěží pacienta na soudobých přístrojích.Cíl:
Cílem práce je poskytnout přehled o inovacích technického i metodického charakteru, které zmíněné nedostatky částečně či úplně řeší. Díky těmto změnám CT kolonografie získala své místo v algoritmu diagnostiky kolorektálního karcinomu jako vyšetření po nekompletní nebo neproveditelné optické kolonoskopii. Jsou jmenovány specifické skupiny pacientů, kteří z nové metody mají zvláštní prospěch. Stručně je nastíněna i problematika dosud nevyjasněné pozice CT kolonografie v rámci screeningu kolorektálního karcinomu.Závěr:
CT kolonografie je relativně novou metodou, která nemůže beze zbytku nahradit optickou kolonoskopii. Díky pokrokům v technologiích se nicméně stává platným diagnostickým nástrojem s určitými výhodami oproti jiným zobrazovacím nebo intervenčním metodám, jež lze při vhodné indikaci přenášet na pacienta.Klíčová slova:
radiologie – tomografie spirální počítačová – kolonografie počítačovou tomografií – kolonoskopie – kolorektální nádory – plošný screeningÚvod
Pokrok ve vývoji technologií a výzkum nových diagnostických postupů jdou v radiologii vždy ruku v ruce v takřka dokonalé synergii, nelze si představit nové sofistikované vyšetřovací metody bez podpory výkonného přístrojového a softwarového vybavení, a zároveň naopak nové poznatky vědeckých týmů udávají směr technologického pokroku a stimulují přenášení pokročilých technologií do každodenní praxe. Tento synergizmus lze sledovat i na příkladu relativně nové aplikace – CT kolonografie (CTC). Vývoj počítačové techniky a softwarového vybavení umožnil z naskenovaných dat spirálního CT přístroje rekonstruovat detailní trojrozměrné zobrazení vnitřního povrchu tělních dutin připomínající endoskopický pohled (obr. 1). Takto pojatá „virtuální endoskopie“ byla poprvé prezentována Viningem a Gelfandem v roce 1994 na endoskopii bronchů a střeva [1]. Nový přístup k zobrazení získaných objemových dat podnítil další výzkum a upozornil na tehdejší limity přístrojového vybavení [2]. Následné studie [3,4] se pokusily stanovit místo CTC ve vyšetřovacím algoritmu a poskytly praktické informace k provedení výkonu [5]. Přesto ve svých počátcích metoda do klinické praxe významněji nevstoupila, a to kvůli radiační zátěži pacientů na soudobých CT přístrojích, vysokým finančním nákladům [6] a problematické očistě střeva před vyšetřením [7].
1. Multiplanární a 3D rekonstrukce vnitřního povrchu tračníku s polypem. 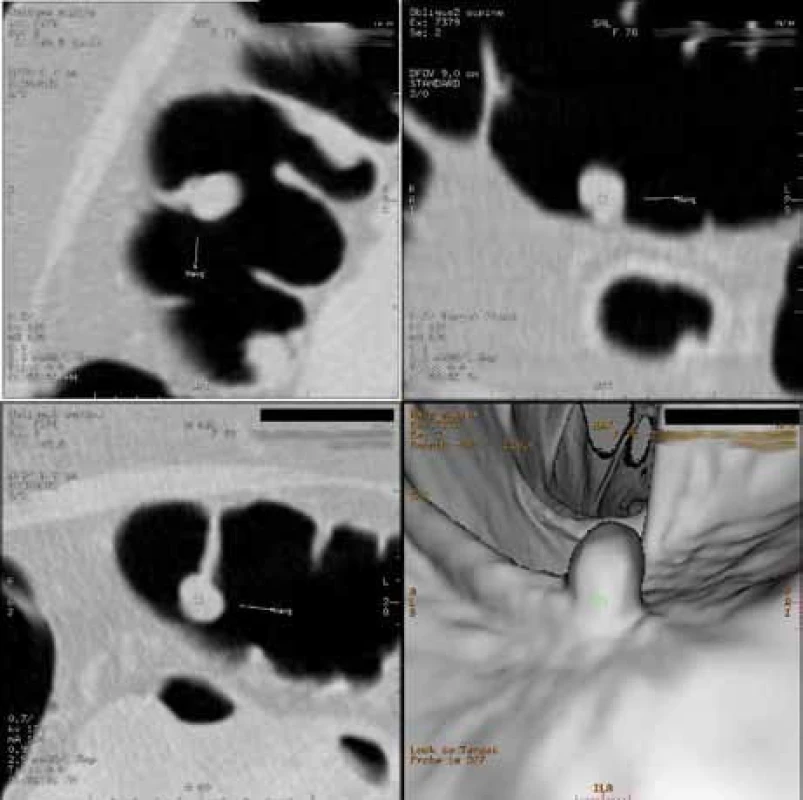
V současné době již díky technologickému i medicínskému vývoji lze CT kolonografii považovat za zavedenou radiologickou techniku zobrazení tlustého střeva, bylo publikováno množství vylepšení, zejména v oblasti přípravy střevního lumen a jeho distenze, akvizice a zpracování dat, což nepochybně přispělo ke zlepšení diagnostické síly metody a rozšířilo její indikace.
Současné standardy a indikace
Příprava a distenze střeva
Z technického pohledu první podstatný krok představuje příprava pacienta. V současné době je jako alternativa ke kompletní očistě střeva laxativy, obdobně jako před optickou kolonoskopií, uváděna minimálně invazivní příprava střeva s malým množstvím nebo i bez nutnosti podání laxativ [8]. Tento pro pacienta komfortní postup však současně vyžaduje k označení reziduí tekutiny a stolice ve střevě perorální podání pozitivní kontrastní látky, využít lze baryové nebo jodové kontrastní látky. Toto „značení stolice“ zvyšuje senzitivitu vyšetření na úroveň odpovídající postupu s kompletní střevní přípravou [9].
Bezprostředně před vyšetřením je nutné střevo distendovat, toto provádíme pomocí manuální nebo automatické insuflace střeva vzduchem nebo CO2 po intravenózním podání spasmolytika. Preferována je automatická aplikace CO2, některé studie [10] uvádějí vyšší komfort pro pacienta, protože dochází k rychlejší resorbci plynu po vyšetření, udávána je rovněž kvalitnější distenze střevní stěny pomocí CO2, nicméně subjektivní efekt pro pacienta je hodnocen jako nevýrazný [11]. Užití spasmolytika (N-butyl-scopolaminu, Buscopanu) zabraňuje spasmům tlustého střeva, jinak častým zejména v oblasti sigmoidea a při výskytu divertiklů [12].
CT vyšetření
Ke standardnímu postupu nadále patří vyšetření pacienta v poloze na zádech a na břiše (obr. 2, 3). Díky pokrokům ve vývoji CT přístrojů jsou nyní skenovací protokoly extrémně rychlé, což snižuje množství pohybových artefaktů a umožňuje významné snížení radiační zátěže pacienta. Nyní jsou již rutinně užívány nízkodávkové protokoly s dávkou okolo 5–6 mSv, což představuje přibližně 2,5násobek dávky obdržené při klasickém vyšetření dvoukontrastní irigografií [13] a dvojnásobek průměrné roční efektivní dávky z přírodních zdrojů, odhadované na přibližně 2,4 mSv [14]. S novými rekonstrukčními algoritmy lze dosáhnout dalšího snížení efektivní dávky přibližně na polovinu, a to při zachované diagnostické hodnotě obrazových dat [15].
2. Polohově nedependentní léze – polyp. 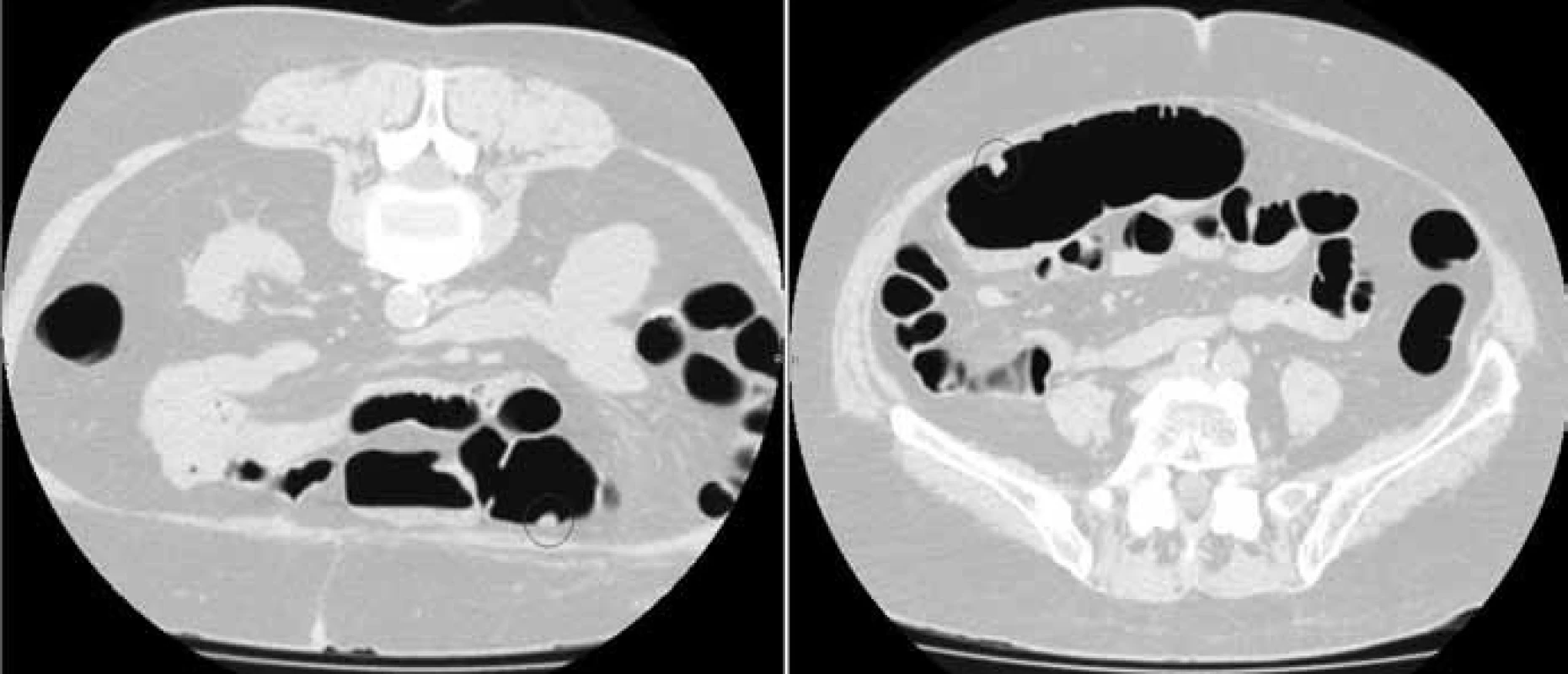
3. Polohově dependentní léze – fekální zbytky. 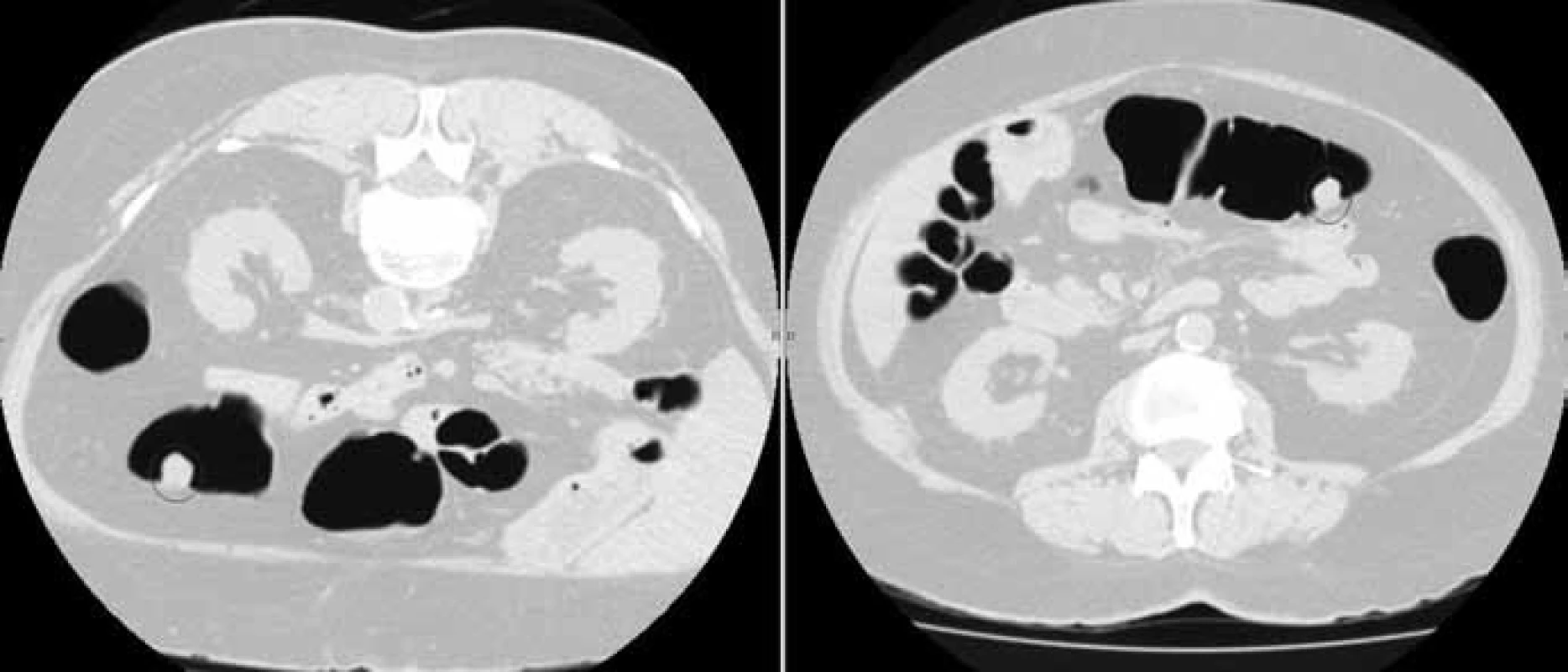
Vyhodnocení nálezu
Pokročilé softwarové nástroje jako virtuální disekce nebo počítačově asistovaná diagnóza (CAD) jsou schopné zvyšovat výkon hodnotícího radiologa [16], doporučována je aplikace CAD pro obě části vyšetření, v poloze na zádech i na břiše (obr. 4–6) [17]. Přesto nelze roli CAD přeceňovat, v prospektivní studii [18] nebyl přínos CAD na základě zvýšení senzitivity vyšetření statisticky významný, CAD rovněž nemůže nahradit zkušenosti radiologa [19]. Jako podklad ke stanovení optimálního postupu při aplikaci CAD mohou sloužit pouze jednotlivé studie, metaanalýza [20] dosvědčuje nemožnost shrnutí současných publikovaných dat týkajících se využití CAD do kvalifikovaného závěru pro jejich nehomogenitu.
4. Porovnání obrazu z CT kolonografie s konvenční kolonoskopií. 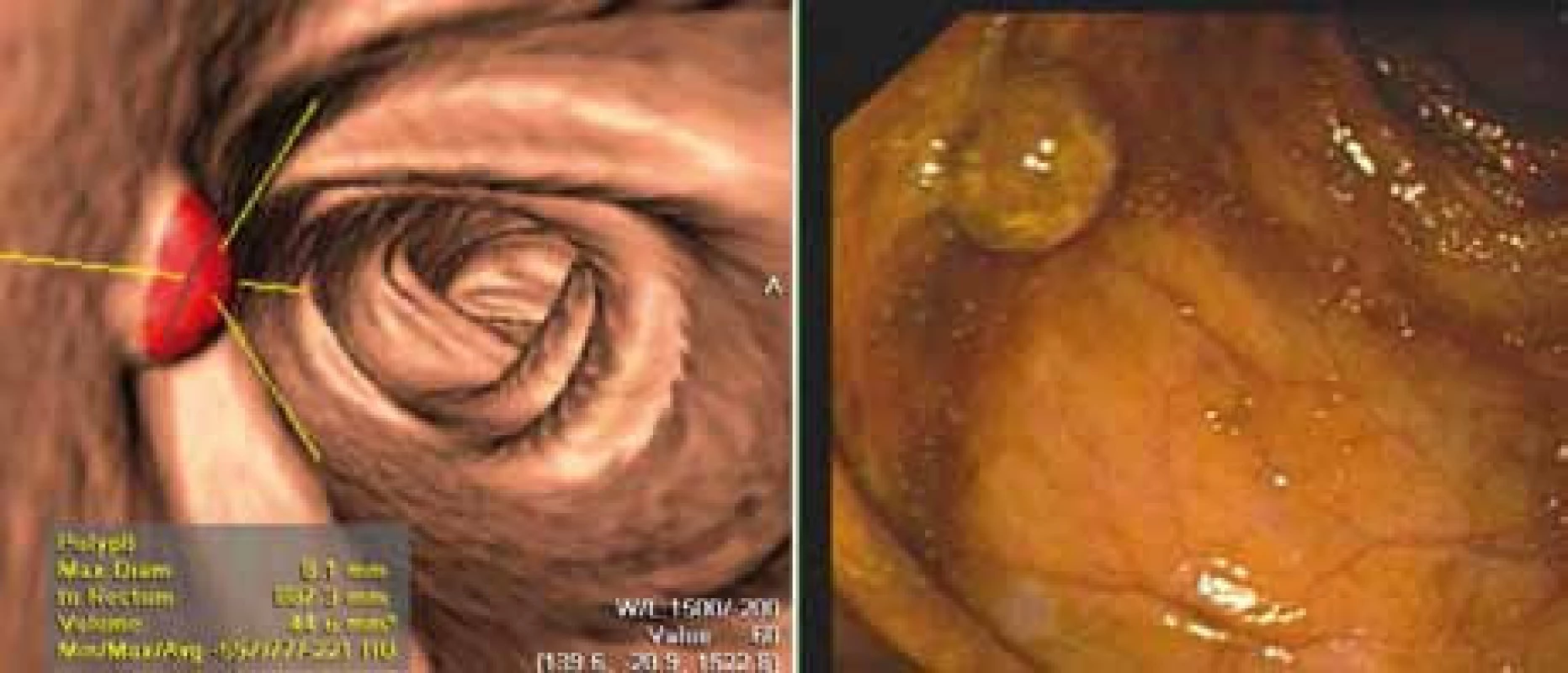
5. Porovnání obrazu z CT kolonografie s konvenční kolonoskopií. 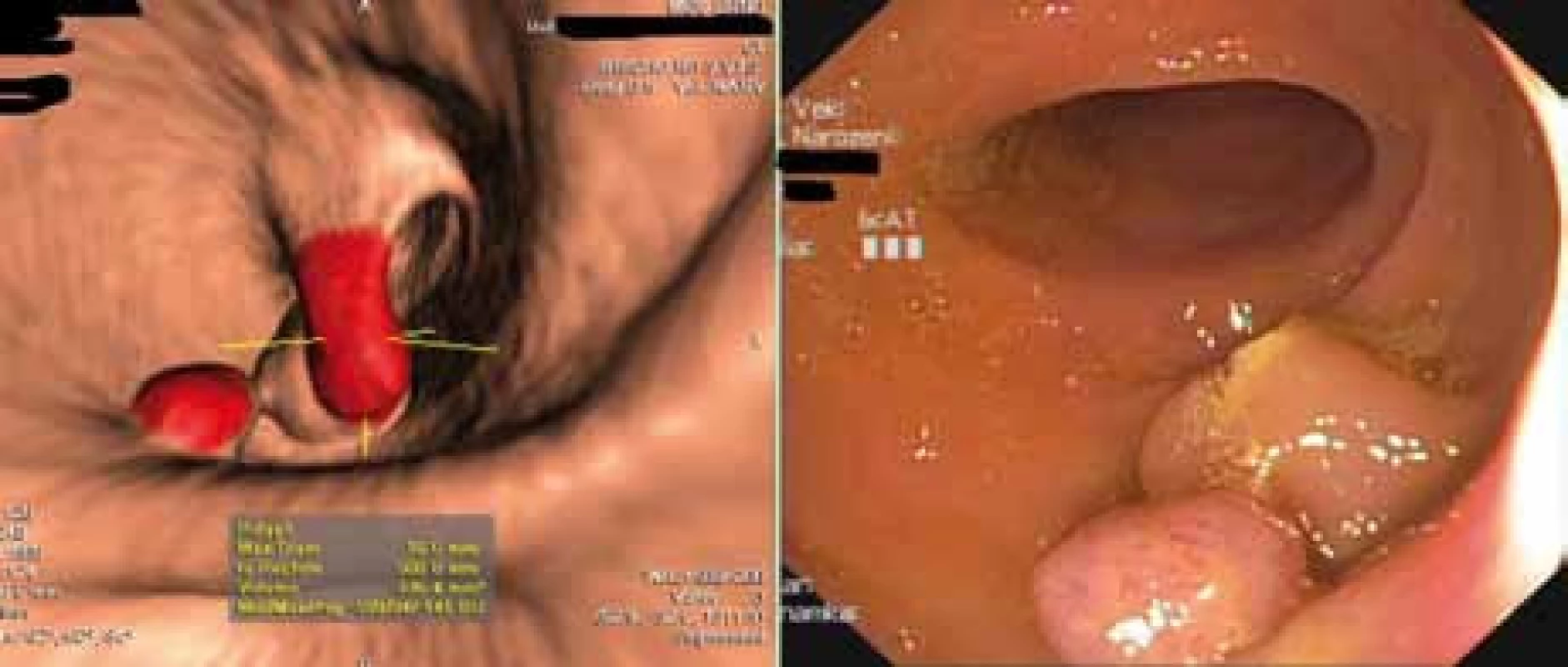
6. Segmentace tračníku (volume rendering). 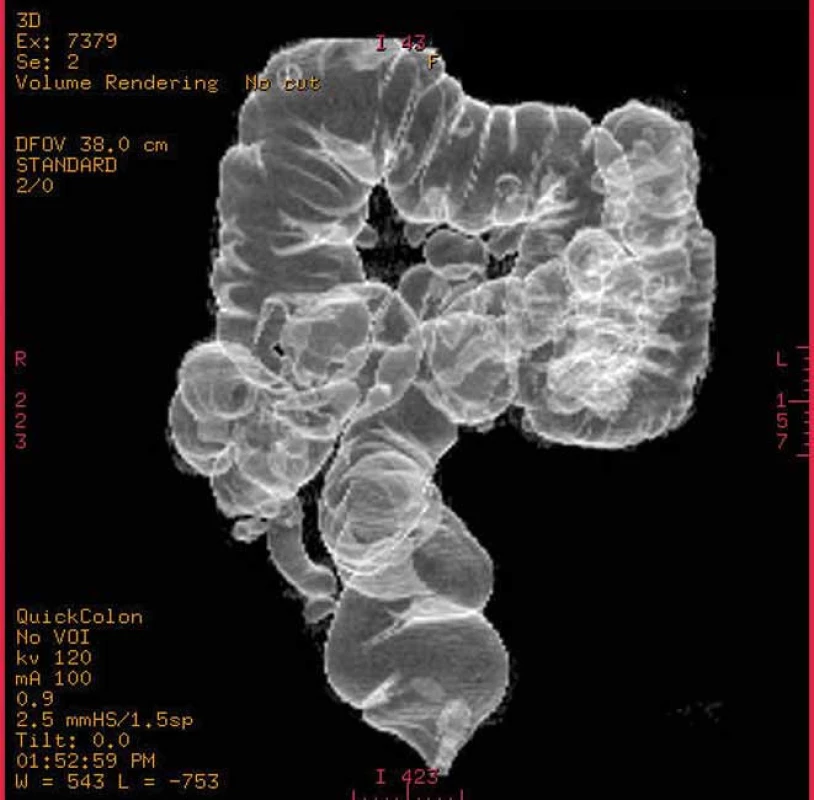
Indikace
V současné době je CT kolonografie jednoznačně uznávanou metodou volby po nekompletní kolonoskopii namísto dříve užívané irigografie [21]. Metoda je často užívána k detekci nádorů u starších pacientů, a to z důvodu vyššího podílu inkompletních kolonoskopií v této populaci a nižší invazivity ve srovnání s optickou kolonoskopií, což významně snižuje riziko komplikací [22,23]. Další skupinou pacientů, která může těžit z výhod CTC, jsou nemocní s divertikulární chorobou tračníku, rovněž v tomto případě bývá klasická kolonoskopie často nedokončena, terén mnohočetných divertiklů nesnižuje diagnostickou hodnotu CT kolonografie [24].
Nejdiskutovanější indikací CTC zůstává screening kolorektálního karcinomu [25,26]. Panuje shoda o pozici CTC ve screeningu v již zmíněné indikaci po nekompletní kolonoskopii namísto dříve užívané dvoukontrastní irigografie, naopak v případě zařazení CT vyšetření tračníku do první linie screeningového vyšetření se názory odborných společností liší, v současné době není screeningová CT kolonografie např. v USA hrazena z programu Medicare [27]. Největší rozpaky nadále vzbuzuje relativně vysoká expozice ionizačnímu záření a v pozadí nezůstává ani problém nestejnorodé kvality vyšetření v běžné praxi [28].
V budoucnu k širšímu uplatnění metody CTC v rámci onkologické prevence bude potřebné učinit z ní metodu obecně přijímanou v populaci, zlepšit efektivitu a snížit radiační zátěž z ní plynoucí.
Komplikace
Mezi závažné komplikace vyšetření patří zejména střevní perforace, ostatní v literatuře popisované události zahrnují jednotlivé případy bolestí na hrudi nebo akutního renálního selhání v souvislosti s přípravou k vyšetření [29].
Incidence perforace se pohybuje dle jednotlivých studií mezi 0,005 % a 0,06 % u diagnostických vyšetření, výskyt perforace při optické kolonoskopii je popisován okolo 0,1–0,2 % [29]. Perforace vznikala téměř výhradně u vysoce rizikových pacientů, u nichž optická kolonoskopie nebyla dokončena, nebo byla kontraindikována [29–31]. U screeningových pacientů byl výskyt perforace ojedinělý [31], někteří autoři rovněž upozorňují na skutečnost, že střevní perforace nebyly popisovány v případech, kdy se pro distenzi lumen použilo automatické insuflace CO2 [29].
Závěr
Radiologická vyšetřovací metoda CT kolonografie je známa laické veřejnosti i části lékařů – neradiologů jako virtuální kolonoskopie. Tento název, přestože již není v současném odborném názvosloví, nejspíše zůstane s metodou i nadále spjat, zřejmě díky pocitu odlehčení, které slovo „virtuální“ přináší k nepříjemné a často neopodstatněně odmítané „kolonoskopii“. Ona virtuálnost slibuje počítačovou futuristickou dokonalost a bezbolestné vyšetření, které v očích pacientů probíhá vlastně pouze na obrazovce.
Pokud přijmeme laické zjednodušení popisované v předchozím odstavci, lze skutečně tuto mladou metodu přijmout jako platný diagnostický nástroj s nepominutelnými přednostmi, přestože metoda k dokonalosti ještě zdaleka nedospěla.
Technika výkonu je skutečně pro pacienta příjemnější než optická kolonoskopie nebo dvoukontrastní irigografické vyšetření a metoda je principiálně bezpečná, udávané počty komplikací souvisejících s výkonem jsou mnohem nižší než při optické kolonoskopii. Za velkou výhodu této techniky lze považovat současné CT zobrazení i ostatních břišních struktur včetně orientačního posouzení spádových lymfatických uzlin, což lze v praxi využít pro sledování pacientů v průběhu léčby maligního onemocnění tlustého střeva (tab. 1).
1. CT kolonografie – srovnání s optickou kolonoskopií. 
Práce byla podpořena výzkumným záměrem MZ ČR: FUNDIN MZ0MOU2005. Práce byla podpořena Evropským fondem pro regionální rozvoj a státním rozpočtem České republiky (OP VaVpI – RECAMO, CZ.1.05/2.1.00/03.0101).
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Michal Standara
Masarykův onkologický ústav
Žlutý kopec 7
656 53 Brno
e-mail: standara@mou.cz
Obdrženo: 21. 12. 2011
Přijato: 18. 3. 2012
Sources
1. Vining DJ, Gelfand DW. Non-invasive colonoscopy using helical CT scanning, 3D reconstruction, and virtual reality. Hawaii, Maui: 23rd annual meeting, SGR Scientific Program 1994: Abstract 70.
2. Johnson CD, Hara AK, Reed JE. Computed tomographic colonography (Virtual colonoscopy): a new method for detecting colorectal neoplasms. Endoscopy 1997; 29(6): 454–461.
3. Fletcher JG, Johnson CD, Welch TJ et al. Optimization of CT colonography technique: prospective trial in 180 patients. Radiology 2000; 216(3): 704–711.
4. Royster AP, Fenlon HM, Clarke PD et al. CT colonoscopy of colorectal neoplasms: two-dimensional and three-dimensional virtual-reality techniques with colonoscopic correlation. AJR Am J Roentgenol 1997; 169(5): 1237–1242.
5. Valev V, Wang G, Vannier MW. Techniques of CT colonography (virtual colonoscopy). Crit Rev Biomed Eng 1999; 27(1–2): 1–25.
6. Sonnenberg A, Delcò F, Bauerfeind P. Is virtual colonoscopy a cost-effective option to screen for colorectal cancer? Am J Gastroenterol 1999; 94(8): 2268–2274.
7. McFarland EG, Brink JA. Helical CT colonography (virtual colonoscopy): the challenge that exists between advancing technology and generalizability. Am J Roentgenol 1999; 173(3): 549–559.
8. Liedenbaum MH, Denters MJ, de Vries AH et al. Low-fiber diet in limited bowel preparation for CT colonography: influence on image quality and patient acceptance. AJR Am J Roentgenol 2010; 195(1): W31–W37.
9. Mahgerefteh S, Fraifeld S, Blachar A et al. CT Colonography with decreased purgation: balancing preparation, performance, and patient acceptance. Am J Roentgenol 2009; 193(6): 1531–1539.
10. Church J, Delaney C. Randomized, controlled trial of carbon dioxide insufflation during colonoscopy. Dis Colon Rectum 2003; 46(3): 322–326.
11. Burling D, Taylor SA, Halligan S et al. Automated insufflation of carbon dioxide for MDCT colonography: distension and patient experience compared with manual insufflation. AJR Am J Roentgenol 2006; 186(1): 96–103.
12. Behrens C, Stevenson G, Eddy R et al. Effect of intravenous Buscopan on colonic distention during computed tomography colonography. Can Assoc Radiol J 2008; 59(4): 183–190.
13. Hirofuji Y, Aoyama T, Koyama S et al. Evaluation of patient dose for barium enemas and CT colonography in Japan. Br J Radiol 2009; 82(975): 219–227.
14. United Nations Scientific Committee on the Sources and Effects of Ionising Radiation. Report on the effects of atomic radiation to the general assembly, 2000. Medical radiation exposures. New York: UN 2001.
15. Flicek KT, Hara AK, Silva AC et al. Reducing the radiation dose for CT colonography using adaptive statistical iterative reconstruction: a pilot study. Am J Roentgenol 2010; 195(1): 126–131.
16. Dachman AH, Obuchowski NA, Hoffmeister JW et al. Effect of computer-aided detection for CT colonography in a multireader, multicase trial. Radiology 2010; 256(3): 827–835.
17. Robinson C, Halligan S, Iinuma G et al. CT colonography: computer-assisted detection of colorectal cancer. Br J Radiol 2011; 84(1001): 435–440.
18. de Vries AH, Jensch S, Liedenbaum MH et al. Does a computer-aided detection algorithm in a second read paradigm enhance the performance of experienced computed tomography colonography readers in a population of increased risk? Eur Radiol 2009; 19(4): 941–950.
19. Fisichella VA, Jäderling F, Horvath S et al. Computer-aided detection (CAD) as a second reader using perspective filet view at CT colonography: effect on performance of inexperienced readers. Clin Radiol 2009; 64(10): 972–982.
20. Robinson C, Halligan S, Taylor SA et al. CT colonography: a systematic review of standard of reporting for studies of computer-aided detection. Radiology 2008; 246(2): 426–433.
21. AGA Clinical Practice and Economics Committee. Position of the American Gastroenterological Association (AGA) Institute on computed tomographic colonography. Gastroenterology 2006; 131(5): 1627–1628.
22. Iafrate F, Hassan C, Zullo A et al. CT colonography with reduced bowel preparation after incomplete colonoscopy in the elderly. Eur Radiol 2008; 18(7): 1385–1395.
23. Yucel C, Lev-Toaff AS, Moussa N et al. CT colonography for incomplete or contraindicated optical colonoscopy in older patients. AJR Am J Roentgenol 2008; 190(1): 145–150.
24. Sanford MF, Pickhardt PJ. Diagnostic performance of primary 3-dimensional computed tomography colonography in the setting of colonic diverticular disease. Clin Gastroenterol Hepatol 2006; 4(8): 1039–1047.
25. Levin B, Lieberman DA, McFarland B et al. Screening and surveillance for the early detection of colorectal cancer and adenomatous polyps, 2008: a joint guideline from the American Cancer Society, the US Multi-Society Task Force on Colorectal Cancer, and the American College of Radiology. CA Cancer J Clin 2008; 58(3): 130–160.
26. Laghi A, Iafrate F, Rengo M et al. Colorectal cancer screening: the role of CT colonography. World J Gastroenterol 2010; 16(32): 3987–3994.
27. Mitka M. Virtual colonoscopy dealt setback with rejection for coverage by Medicare. JAMA 2009; 301(13): 1327–1328.
28. Whitlock EP, Lin JS, Liles E et al. Screening for colorectal cancer: a targeted, updated systematic review for the U.S. Preventive Services Task Force. Ann Intern Med 2008; 149(9): 638–658.
29. Pickhardt PJ. Incidence of colonic perforation at CT colonography: review of existing data and implications for screening of asymptomatic adults. Radiology 2006; 239(2): 313–316.
30. Burling D, Halligan S, Slater A et al. Potentially serious adverse events at CT colonography in symptomatic patients: national survey of the United Kingdom. Radiology 2006; 239(2): 464–471.
31. Sosna J, Blachar A, Amitai M et al. Colonic perforation at CT colonography: assessment of risk in a multicenter large cohort. Radiology 2006; 239(2): 457–463.
Labels
Paediatric clinical oncology Surgery Clinical oncology
Article was published inClinical Oncology

2012 Issue 4-
All articles in this issue
- Implication of Bone Marrow Microenvironment in Pathogenesis of Multiple Myeloma
- CT Colonography – Evolution of Methodology and Indications
- Long Non-Coding RNAs And Their Relevance in Cancer
- Treatment of Langerhans Cells Histiocytosis by Cladribin Reached Long-Term Complete Remission in 9 out of 10 Adult Patients
- EGFR Mutations in Patients with Advanced NSCLC
- HARDROCK Project: Parametric Data Collection and Analysis of Patients with Head and Neck Cancer in the Comprehensive Cancer Centre of Ostrava – Role of Fractionation and Target Volume Definition in Radiotherapy
- What is the Prognostic Importance of Molecular Genetic Factors in Endometrial Carcinoma?
- Hepatocellular Carcinoma – Long-Term Treatable Disease
- Treatment For Volume Upgrading of the Low-Grade Supratentorial Glioma After the Subtotal Neurosurgical Resection
- Comparision of Histological Types of Primary and Subsequent Relapsing Basal Cell Carcinomas of the Skin
- Paratesticular Mesothelioma in Young Age. Case Report
- Clinical Oncology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Hepatocellular Carcinoma – Long-Term Treatable Disease
- Treatment For Volume Upgrading of the Low-Grade Supratentorial Glioma After the Subtotal Neurosurgical Resection
- EGFR Mutations in Patients with Advanced NSCLC
- CT Colonography – Evolution of Methodology and Indications
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

