-
Medical journals
- Career
Novinky ve farmakoterapii srdečního selhání se zachovalou ejekční frakcí
Authors: Andreasová T.; Málek F.
Authors‘ workplace: Nemocnice Na Homolce, Praha
Published in: Kardiol Rev Int Med 2020, 22(1): 29-32
Overview
Srdeční selhání se zachovalou ejekční frakcí (EF) se vyskytuje v populaci pacientů s tímto klinickým syndromem často a léčba je obtížná. Léky modifikující průběh onemocnění u nemocných se srdečním selháním a sníženou EF se ukázaly být u pacientů se zachovalou EF neefektivní. Doporučena je léčba ischemické choroby srdeční, arteriální hypertenze a kontrola rytmu nebo frekvence u fibrilace síní jako hlavní principy terapie této populace nemocných. Naděje byla vkládána do duální inhibice systému renin-angiotenzin na úrovni receptoru pro angiotenzin II a inhibitoru neprilysinu. Výsledky randomizované studie sakubitril-valsartanu u srdečního selhání se zachovalou EF nedopadly jednoznačně příznivě. Ve stadiu klinického výzkumu jsou nové léky, jejichž efekt vychází ze zcela odlišných mechanizmů.
Klíčová slova:
srdeční selhání – zachovalá ejekční frakce – farmakoterapie – nové léky
Úvod
Evropská kardiologická společnost klasifikuje srdeční selhání (SS) podle ejekční frakce (EF) levé komory do tří skupin: SS se sníženou EF (heart failure with reduced ejection fiction – HFrEF) s EF levé komory (LK) < 40 %, s mírně sníženou EF (heart failure with midrange ejection fraction – HFmrEF) s EF LK 41 – 50 % a SS se zachovalou EF (heart failure with preserved ejection fraction – HFpEF) s EF LK > 50 % [1,2]. HFpEF je klinický syndrom charakterizovaný normální nebo téměř normální systolickou funkcí LK. Tato jednotka představuje zásadní a narůstající medicínský problém především díky vzestupu prevalence. Významná část nemocných s klinickým syndromem SS má normální nebo zachovalou EF LK. Prevalence SS s normální nebo se zachovalou EF LK se v populaci pacientů se syndromem chronického SS (CHSS) odhaduje až na 50 %. Prognóza nemocných s HFpEF je po hospitalizaci pro akutní SS stejná jako u pacientů s HFrEF. Riziko úmrtí je 65% během 5 let [3 – 6]. HFpEF je odpovědné za 50 % hospitalizací pro SS, incidence HFpEF ve světě stoupá [4,7]. Léčebné strategie, které byly u pacientů s HFrEF spojeny se snížením nemocnosti a se zlepšením prognózy, se ukázaly být u nemocných s HFpEF neúspěšné. V dosud provedených studiích u pacientů s HFpEF se ukázalo, že léky modifikující průběh onemocnění u HFrEF, mají u pacientů s HFpEF dopad na snížení mortality a morbidity ve srovnání s placebem neutrální [8]. Například terapie pomocí léků, které inhibují renin-angiotenzin-aldosteronový systém (RAAS), nebyla u pacientů s HFpEF spojená s očekávaným snížením rizika úmrtí a hospitalizace [9 – 11]. Na základě těchto výsledků se doporučení odborných společností zaměřují na léčbu komorbidit – arteriální hypertenze, ischemické choroby srdeční a fibrilace síní, které jsou nejčastějšími komorbiditami HFpEF [1,2]. Selhání principů neurohumorální blokády, zejména inhibice RAAS u HFpEF, by mohlo být vysvětleno odlišnou patofyziologií HFrEF a HFpEF.
Terapie HFpEF
Současná doporučení pro diagnostiku a léčbu SS se v případě terapie HFpEF již několik let nemění. Hlavními principy léčby jsou nadále – agresivní kontrola krevního tlaku u pacientů s arteriální hypertenzí v prevenci nebo k zábraně progrese srdeční hypertrofie, koronární revaskularizace u pacientů s prokázanou ischemií myokardu s cílem zlepšit relaxaci komor, kontrola tepové frekvence u pacientů s chronickými formami fibrilace síní s cílem zpomalit komorovou odpověď a zlepšit diastolické plnění komor a koronární perfuzi a těsná kontrola retence tekutin pomocí diuretik k odstranění kongesce s plným vědomím toho, že výrazné snížení preloadu při nadměrné diuretické terapii je spojeno s rizikem symptomatické hypotenze. Žádná farmakologická léčba dosud jednoznačně neprokázala schopnost snížit morbiditu a mortalitu pacientů s HFpEF. Vzhledem k tomu, že typicky se jedná o starší nemocné s řadou komorbidit a pokročilými symptomy, je důležitým léčebným cílem i zlepšení kvality života.
Farmakoterapie HFpEF spojená se zlepšením symptomů a snížením hospitalizace pro SS
Diuretika zlepšují symptomy srdečního selhání s plicní nebo systémovou kongescí jak u nemocných s HFrEF, tak i u pacientů s HFpEF. Vliv na zlepšení symptomů je nezávislý na EF LK. Je nutné mít na mysli, že u pacientů s HFpEF může být příliš agresivní diuretická terapie spojená s významným poklesem žilního návratu a rozvojem symptomatické hypotenze. Chybí důkazy o zlepšení příznaků při léčbě betablokátory (BB) a antagonisty mineralokortikoidních receptorů (MRA). Existují důkazy pro zlepšení symptomatologie u pacientů s HFpEF léčených antagonistou AT1 receptoru angiotenzinu II (ARB) kandesartanem a inhibitorem enzymu konvertující angiotenzin (ACEI) perindoprilem [12,13].
Snížení rizika hospitalizace pro SS je důležitým klinickým cílem, jedná se o hlavní parametr morbidity. V případě pacientů s HFpEF existují důkazy o snížení rizika hospitalizace pro nebivolol, digoxin, spironolakton a kandesartan [12,14 – 16]. Tyto závěry ovšem platí pouze pro pacienty se sinusovým rytmem. U pacientů s fibrilací síní důkazy pro BB, digoxin, ACEI a ARB chybí.
Farmakoterapie HFpEF s účinkem na snížení mortality
Studie s ACEI, ARB, BB a MRA neprokázaly jednoznačné snížení mortality. Pouze ve studii SENIORS nebivolol u starších pacientů snížil riziko úmrtí a hospitalizace z kardiovaskulárních (KV) příčin bez ohledu na EF LK [14]. Subanalýza studie SENIORS si položila za úkol zjistit, zda je efekt nebivololu na snížení rizika úmrtí a KV hospitalizace nezávislý na EF LK. Do subanalýzy bylo zahrnuto 2 111 pacientů, z nichž 1 359 (64 %) mělo sníženou EF LK ≤ 35 % a 752 (36 %) mělo mírně sníženou nebo zachovalou EF LK > 35 %. Průměrná EF LK první skupiny byla 28,7 % a u druhé skupiny 49,2 %. Pacienti s HpEF byli častěji ženy, měli méně pokročilé symptomy, častěji hypertenzi a méně často byli po infarktu myokardu. Primární kombinovaný sledovaný ukazatel úmrtí a hospitalizace z KV příčin se vyskytl u 34,2 % pacientů s HFrEF a u 31,2 % pacientů s HFpEF. Efekt nebivololu na snížení rizika primárního sledovaného ukazatele ve srovnání s placebem nebyl mezi oběma skupinami rozdílný, snížení rizika (HR = hazard ratio) bylo u HFrEF 0,86 a u HFpEF 0,81. Stejně tak nebyl rozdíl ve snížení rizika sekundárního ukazatele – úmrtí z jakékoli příčiny mezi oběma skupinami. Efekt betablokády pomocí nebivololu u starších nemocných se SS byl pozitivní jak u nemocných se sníženou, tak u pacientů se zachovalou EF LK [17]. Doplňující post-hoc analýza této studie ukázala, že efekt nebivololu na snížení rizika byl patrný i u pacientů s EF LK ≥ 40 % (n = 643) a nelišil se od pacientů s EF LK ≥ 35 %. Přehled farmakoterapie HFpEF ukazuje tab. 1.
Table 1. Efekt farmakoterapie HFpEF na defi nované klinické cíle. 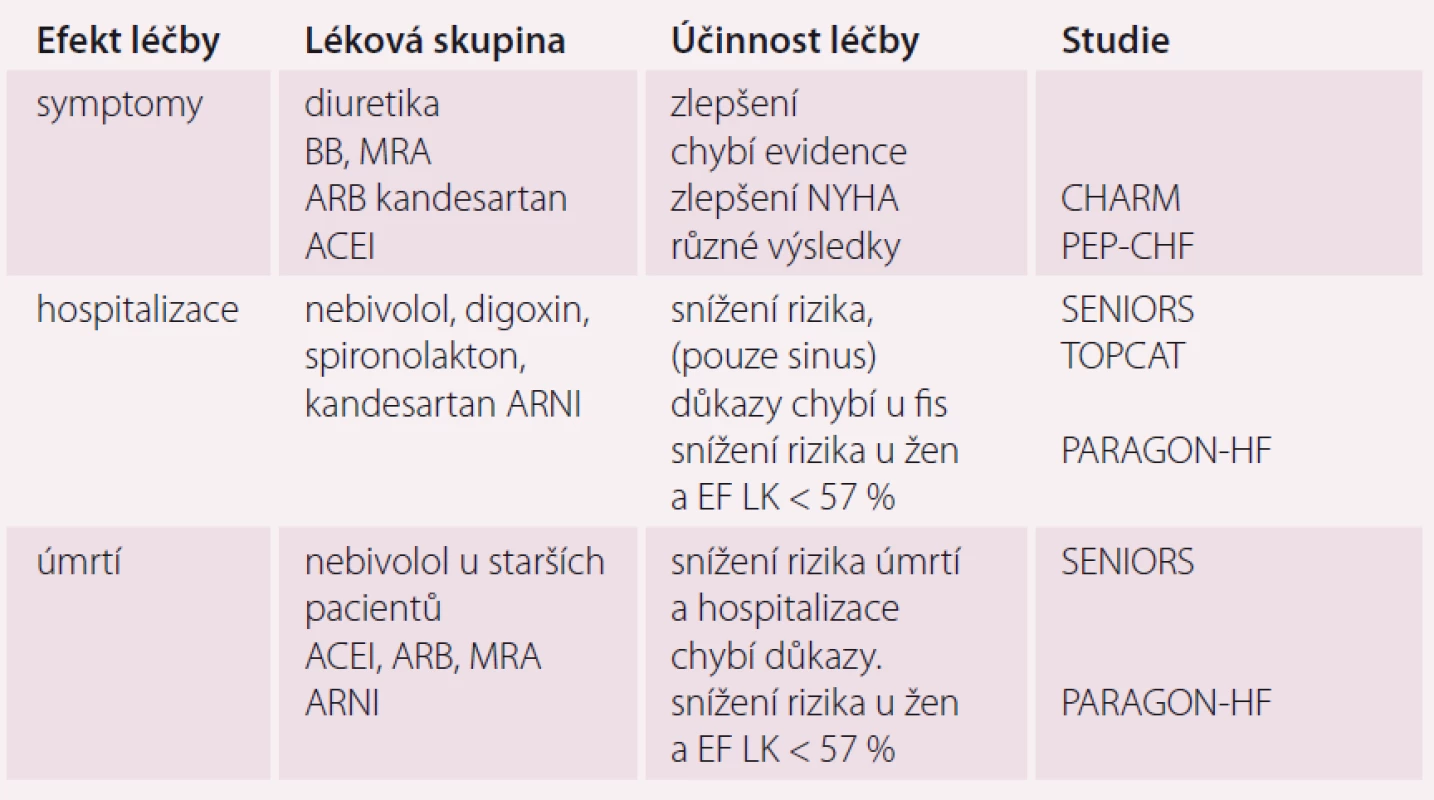
HFpEF – srdeční selhání se zachovalou ejekční frakcí; BB – betablokátory; MRA – antagonisté mineralokortikoidních receptorů; ARB – antagonisté AT1 receptoru angiotenzinu II; ACEI – inhibitor enzymu konvertující angiotenzin; ARNI – inhibitory receptoru angiotenzinu a neprilysinu; EF LK – ejekční frakce levé komory Novinky ve farmakoterapii HFpEF
V indikaci HFpEF se testovala řada léků s různým mechanizmem účinku, např. donátory oxidu dusnatého NO (např. Nitroprusid), nitráty a hydralazin [18]. Dále aktivátory a stimulátory guanylátcyklázy (sGC), které mají silný vazodilatační a antihypertenzní potenciál při zachování kardioprotektivních i nefroprotektivních účinků. Riociguat je prvním orálním stimulátorem sGC, byl testován u pacientů s HFpEF s plicní hypertenzí. Zlepšil srdeční výdej a snížil dotížení komor, ale neměl vliv na tlak v plicnici, ani na plicní vaskulární rezistenci [19]. V rámci programu SOCRATES (Soluble Guanylate Cyclase stimulator Heart Failure Studies, ClinicalTrials.gov NCT101951638) ve studii SOCRATES-PRESERVED – randomizované, dvojitě slepé studii – byla hodnocena účinnost a bezpečnost vericiguatu (BAY1021189), stimulátoru sGC u hospitalizovaných pacientů s HFpEF (EF LK ≥ 45 %) [17]. V této studii nedošlo k významnému snížení koncentrace NT-proBNP, ale ke zlepšení kvality života pacientů s HFpEF. Aktivita cGMP může být ovlivněna inhibitory fosfodiesterázy-5 (PDE-5). Testovaným lékem byl v několika studiích u pacientů s HFpEF sildenafil, který má selektivní vazodilatační efekt na plicní cirkulaci. V menší studii pacientů s HFpEF a plicní hypertenzí vedl sildenafil ke snížení tlaku v plicnici, tlaku v plicnici v zaklínění a došlo ke zlepšení funkce levé i pravé komory. Tyto příznivé výsledky však nebyly ve studii fáze III RELAX (Phosphodiesterase-5 Inhibition to Improve Clinical Status and Exercise Capacity in Heart Failure with Preserved Ejection Fraction) potvrzeny [20]. Naděje byla vkládána do možnosti ovlivnění degradace natriuretických peptidů, a tím využití jejich fyziologické vlastnosti také v populaci pacientů s HFpEF. Sakubitril-valsartan je zatím jediným představitelem lékové skupiny inhibitorů receptoru angiotenzinu a neprilysinu (angiotensin receptor and neprilysin inhibitors – ARNI). U pacientů s HFrEF bylo prokázáno, že duální inhibice neprilysinu a receptoru angiotenzinu II je mnohem efektivnější na snížení rizika úmrtí a hospitalizace pro SS než konvenční léčba inhibitorem ACE enalaprilem. Randomizovaná srovnávací studie PARAMOUNT II. fáze klinického výzkumu ukázala, že sakubitril-valsartan 97/ 103 mg 2× denně, ve srovnání s valsartanem 160 mg 2× denně, významně snížil průměrnou koncentraci NT-proBNP o 23 % (p = 0,005) u 283 pacientů s CHSS NYHA II a III a EF LK ≥ 45 % [21]. Cílem studie PARAGON-HF bylo zjistit dopad sakubitril-valsartanu na riziko úmrtí z KV příčin a hospitalizace pro SS ve srovnání s valsartanem u pacientů s HFpEF (NYHA II a III a EF LK ≥ 45 %) [22]. Sakubitril-valsartan 97/ 103 mg 2× denně ve srovnání s valsartanem 160 mg 2× denně snížil riziko KV úmrtí a hospitalizace pro SS o 13 % (HR 0,87), tento rozdíl však nedosáhl statistické významnosti (p = 0,059). Při analýze podskupin pak bylo zjištěno, že snížení primárního sledovaného výsledku bylo statisticky významné u žen a u pacientů s EF LK < medián 57 %. Sakubitril-valsartan tak tedy zůstává nadějí pro pacienty se HFmrEF. Dalším zajímavým přístupem k léčbě pacientů se SS jsou léky ze skupiny antidiabetik, které blokádou reabsorpce glukózy v proximálním tubulu vedou ke snížení glykemie navozením glykosurie. Tyto tzv. inhibitory sodíkoglukózového ko-transporteru 2 (iSGLT2) – glifloziny – byly testovány v několika studiích u pacientů s diabetes mellitus 2. typu (DM2) a vysokým KV rizikem. V první z těchto studií EMPA-REG OUTCOME vedl empagliflozin nejen ke zlepšení kompenzace diabetu, ale i k významnému snížení rizika KV úmrtí a ke snížení rizika hospitalizace pro SS [23]. A na Evropském kardiologickém kongresu v Paříži v srpnu 2019 byly prezentovány pozitivní výsledky studie DAPA-HF, ve které byl testován další ze skupiny iSGLT2 dapagliflozin u pacientů s HFrEF (EF LK ≤ 40 %) NYHA II – IV bez ohledu na přítomnost DM2. Dapagliflozin ve srovnání s placebem snížil u pacientů s HFrEF riziko KV úmrtí a zhoršení průběhu SS (hospitalizace nebo mimořádné návštěvy ambulance) o 26 % a tento rozdíl byl velmi významný (p < 0,001) [24]. Tento efekt nebyl ovlivněn přítomností DM2, tzn. že byl příznivý efekt dapagliflozinu pozorován jak u diabetiků, tak u nediabetiků s HFrEF. Přesný mechanizmus účinku iSGLT2 u pacientů se SS není znám a nelze jej vysvětlit pouze diuretickým účinkem, příznivým ovlivněním krevního tlaku a kompenzace diabetu. Zřejmě dochází k pozitivnímu ovlivnění metabolizmu kardiomyocytů a intersticiálních buněk, což dává naději na úspěšnost této léčby i u pacientů s HFpEF. Rozsáhlý klinický výzkum v této oblasti probíhá (studie EMEROR-PRESERVED a DELIVER) [25,26].
Závěr
Farmakoterapie HFpEF se zatím nemůže opřít o tak průkazné výsledky klinických studií zaměřených na ovlivnění mortality a morbidity, které známe z výzkumu léčby HFrEF. Studie se sakubitril-valsartanem nepřinesla jednoznačně pozitivní výsledky, nicméně zůstává naděje pro pacienty s HFmrEF (EF LK 40 – 50 %). Ovlivnění dalších patofyziologických procesů v této populaci pacientů pokračuje i s hledáním nových cest, vyčkáme výsledků studií s glifloziny. Důvod pokračujícího zájmu o tuto populaci nemocných je nasnadě – prevalence a incidence tohoto syndromu stoupá a dlouhodobá prognóza se příliš od osudu nemocných s HFrEF neliší.
Podpořeno MZ ČR – RVO (Nemocnice Na Homolce – NNH, 00023884), IG160502
Doručeno do redakce: 11. 11. 2019
Přijato po recenzi: 22. 11. 2019
doc. MUDr. Filip Málek, Ph.D.,MBA
Sources
1. Ponikowski P, Voors AA, Anker SD et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Eur Heart J 2016; 37(27): 2129 – 2200. doi: 10.1093/ eurheartj/ ehw128.
2. Špinar J, Hradec J, Špinarová L et al. Souhrn Doporučených postupů ESC pro diagnostiku a léčbu akutního a chronického srdečního selhání z roku 2016. Cor Vasa 2016; 58(5): e530 – e568.
3. Yancy CW, Lopatin M, Stevenson LW et al. Clinical presentation, management, and in-hospital outcomes of patients admitted with acute decompensated heart failure with preserved systolic function: a report from the Acute Decompensated Heart Failure National Registry (AD-HERE) Database. J Am Coll Cardiol 2006; 47(1): 76 – 84. doi: 10.1016/ j.jacc.2005.09.022.
4. Lam CS, Donal E, Kraigher-Krainer E et al. Epidemiology and clinical course of heart failure with preserved ejection fraction. Eur J Heart Fail 2011; 13(1): 18 – 28. doi: 10.1093/ eurjhf/ hfq121.
5. Bhatia RS, Tu JV, Lee DS, et al. Outcome of heart failure with preserved ejection fraction in a population-based study. N Engl J Med 2006; 355(3): 260 – 269. doi: 10.1056/ NEJMoa051530.
6. Steinberg BA, Zhao X, Heidenreich PA et al. Trends in patients hospitalized with heart failure and preserved left ventricular ejection fraction: prevalence, therapies, and outcomes. Circulation 2012; 126(1): 65 – 75. doi: 10.1161/ CIRCULATIONAHA.111.080770.
7. Solomon SD, Dobson J, Pocock S et al. Influence of nonfatal hospitalization for heart failure on subsequent mortality in patients with chronic heart failure. Circulation 2007; 116(13): 1482 – 1487. doi: 10.1161/ CIRCULATIONAHA.107.696906.
8. Paulus WJ, van Ballegoij JJ. Treatment of heart failure with normal ejection fraction: an inconvenient truth! J Am Coll Cardiol 2010; 55(6): 526 – 537. doi: 10.1016/ j.jacc.2009.06.067.
9. Massie BM, Carson PE, McMurray JJ et al. Irbesartan in patients with heart failure and preserved ejection fraction. N Engl J Med 2008; 359(23): 2456 – 2467. doi: 10.1056/ NEJMoa0805450.
10. Campbell RT, Jhund PS, Castagno D et al. What have we learned about patients with heart failure and preserved ejection fraction from DIG-PEF, CHARM-Preserved, and I-PRESERVE? J Am Coll Cardiol 2012; 60(23): 2349 – 2356. doi: 10.1016/ j.jacc.2012.04.064.
11. Pitt B, Pffefer MA, Assman SF et al. The TOPCAT Investigators Spironolactone for Heart Failure with Preserved Ejection Fraction. N Engl J Med 2014, 370(15): 1383 – 1392. doi: 10.1056/ NEJMoa1313731.
12. Yusuf S, Pfeffer MA, Swedberg K, et al. for the CHARM Investigators and Committees. Effects of candesartan in patients with chronic heart failure and preserved left-ventricular ejection fraction: the CHARM-Preserved Trial. Lancet 2003; 362(9386): 777 – 781. doi: 10.1016/ S0140-6736(03)14285-7.
13. Cleland JG, Tendera M, Adamus J et al. The PEP-CHF Investigators. The perindopril in elderly people with chronic heart failure (PEP-CHF) study. Eur Heart J 2006; 27(19): 2338 – 2345. doi: 10.1093/ eurheartj/ ehl250.
14. Flather MD, Shibata MC, Coats AJ et al. The SENIORS Investigators. Randomised trial to determine the effect of nebivolol on mortality and hospital admission in elderly patients with heart failure (SENIORS). Eur Heart J 2005; 26(3): 215 – 225. doi: 10.1093/ eurheartj/ ehi115.
15. Ahmed A, Rich MW, Fleg JL et al. The Ancillary Digitalis Investigation Group. Effect of digoxin on morbidity and mortality in diastolic heart failure Trial. Circulation 2006; 114(5): 397 – 403. doi: 10.1161/ CIRCULATIONAHA.106.628347.
16. Van Veldhuisen DJ, Cohen-Solal A, Bohm M et al. The SENIORS Investigators Beta-blockade with nebivolol in elderly heart failure patients with impaired and preserved left ventricular ejection fraction. J Am J Cardiol 2009; 53(23): 2150 – 2158. doi: 10.1016/ j.jacc.2009.02.046.
17. Bonderman D, Pretsch I, Steringer-Mascherbauer R et al. Acute hemodynamic effects of riociguat in patients with pulmonary hypertension associated with diastolic heart failure (DILATE-1): a randomized, double-blind, placebo-controlled, single-dose study. Chest 2014; 146(5): 1274 – 1285. doi: 10.1378/ chest.14-0106.
18. Zamani P, Rawat D, Shiva-Kumar P et al. Effect of inorganic nitrate on exercise capacity in heart failure with preserved ejection fraction. Circulation 2015; 131(4): 371 – 380. doi: 10.1161/ CIRCULATIONAHA.114.012957.
19. Pieske B, Maggioni AP, Lam CS et al. Vericiguat in patients with worsening chronic heart failure and preserved ejection fraction: results of the SOluble guanylate Cyclase stimulatoR in heArT failurE patientS with PRESERVED EF (SOCRATES-PRESERVED) study. Eur Heart J 2017 : 38(15): 1119 – 1127. doi: 10.1093/ eurheartj/ ehw593.
20. Redfield MM, Chen HH, Borlaug BA et al. Effect of phosphodiesterase-5 inhibition on exercise capacity and clinical status in heart failure with preserved ejection fraction: a randomized clinical trial. JAMA 2013; 309(12): 1268 – 1277. doi: 10.1001/ jama.2013.2024.
21. Solomon SD, Ziele M, Pieske B et al. The Prospective comparison of ARNI with ARB on Management Of heart failUre with preserved ejectioN fracTion (PARAMOUNT) Investigators. The angiotensin receptor neprilysin inhibitor LCZ696 in heart failure with preserved ejection fraction: a phase 2 double-blind randomised controlled trial. Lancet 2012; 380(9851): 1387 – 1395. doi: 10.1016/ S0140-6736(12)61227-6.
22. Solomon SD, McMurray JJ, Anand IS et al. The PARAGON-HF Investigators and Committees. Angiotensin-neprilysin inhibition in heart failure with preserved ejection fraction. N Engl J Med 2019; 381(17): 1609 – 1620. doi: 10.1056/ NEJMoa1908655.
23. Zinman B, Lachin JM, Inzucchi. Empagliflozin, cardiovascular outcomes and mortality in type 2 diabetes. N Engl J Med 2016; 374(11): 1094. doi: 10.1056/ NEJMc1600827.
24. McMurray JJ, Solomon SD, Inzucchi SE et al. The DAPA-HF Trial Investigators.Dapagliflozin in patients with heart failure and reduced ejection fraction. N Engl J Med 2019; 381(21): 1995 – 2008. doi: 10.1056/ NEJMoa1911303.
25. EMPagliflozin outcomE tRial in Patients With chrOnic heaRt Failure With Preserved Ejection Fraction (EMPEROR-Preserved). Available at: https:/ / clinicaltrials.gov/ ct2/ show/ NCT03057951.
26. Dapagliflozin Evaluation to Improve the LIVEs of Patients With PReserved Ejection Fraction Heart Failure. (DELIVER). Available at: https:/ / clinicaltrials.gov/ ct2/ show/ NCT03619213.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2020 Issue 1-
All articles in this issue
- Doba kardiokoronarovirová – jak moc v tom lítáme?
- Co je to komplexní kardiovaskulární rehabilitace?
- Kardiorehabilitace v klinické praxi
- Vliv pohybové aktivity na snížení hodnot krevního tlaku u pacientů s arteriální hypertenzí
- Možnosti kardiovaskulární prevence v nutričním kontextu
- Kardiovaskulární rehabilitace pacientů po chirurgické korekci chlopenních a vrozených srdečních vad
- Nové vzorce pro výpočet maximální spotřeby kyslíku při zátěžových testech podle registru FRIEND
- Nikotin, kouření a kardiovaskulární rizika – základní pojmy
- Novinky ve farmakoterapii srdečního selhání se zachovalou ejekční frakcí
- EKG diagnostika prvního kontaktu v osmi krocích
- Doporučená očkování pro osoby s kardiovaskulárním onemocněním
- Doporučená vyšetření v infekční sérologii u pacientů s kardiovaskulárním onemocněním
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- EKG diagnostika prvního kontaktu v osmi krocích
- Nikotin, kouření a kardiovaskulární rizika – základní pojmy
- Doporučená vyšetření v infekční sérologii u pacientů s kardiovaskulárním onemocněním
- Vliv pohybové aktivity na snížení hodnot krevního tlaku u pacientů s arteriální hypertenzí
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career
