-
Medical journals
- Career
Chronické onemocnění ledvin – novinky v klasifikaci a terapii
Authors: O. Zakiyanov 1,2; J. Vachek 1,3; V. Tesař 1
Authors‘ workplace: Klinika nefrologie VFN a 1. LF UK v Praze 1; Ústav lékařské biochemie a laboratorní diagnostiky VFN a 1. LF UK v Praze 2; Farmakologický ústav 1. LF UK v Praze 3
Published in: Kardiol Rev Int Med 2014, 16(1): 49-52
Category: Internal Medicine
Overview
Chronické onemocnění ledvin je nejnověji definováno jako abnormality ledvinné struktury nebo funkce přítomné po více než tři měsíce a ovlivňující zdraví. Jde o patologický stav se stále vzrůstající prevalencí, která způsobuje mimo jiné enormní zátěž pro zdravotní systém. Při včasném záchytu a odpovídající léčbě lze rozvoj chronického onemocnění ledvin zpomalit, a pacienta tak uchránit konečného stadia selhání ledvin spojeného s nutností náhrady funkce ledvin. S chronickým onemocněním ledvin se nesetkávají již jen nefrologové, ale lékaři ze všech oborů. Toto sdělení pojednává o epidemiologii, rizikových faktorech, klasifikaci a možnostech léčby, cílem je podat stručný přehled aktuálních informací o tomto závažném onemocnění.
Klíčová slova:
chronické onemocnění ledvin – CKD – dialýza – transplantace – náhrada funkce ledvin – RRTDefinice
Chronické onemocnění ledvin (CKD) je nejnověji definováno podle doporučení skupiny KDIGO nazvaného Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease jako abnormality ledvinné struktury nebo funkce přítomné po více než tři měsíce a ovlivňující zdraví [1]. Nepatří sem tedy poměrně časté situace, kdy je funkce ledvin snížena, avšak neprogreduje a neovlivňuje zdravotní stav, např. fyziologický pokles renální funkce bez dalšího orgánového poškození ve vyšším věku – dle starších definic tyto změny dosud vedly k diagnóze nefropatie.
Ke stanovení diagnózy CKD je nutná přítomnost jednoho nebo více markerů poškození ledvin (albuminurie, patologicky močový sediment, elektrolytové abnormality vznikající v důsledku tubulárního postižení, histologické abnormality, strukturní abnormality prokázané užitím zobrazovacích metod nebo stav po transplantaci ledviny) a/ nebo snížení glomerulární filtrace (GFR pod 60 ml/ min/ 1,73 m2), pokud trvá déle než tři měsíce a ovlivňuje zdraví.
Epidemiologie
Prevalence a incidence CKD se v populaci neustále zvyšuje, což souvisí především s nárůstem civilizačních chorob (arteriální hypertenze, diabetes mellitus, kardiovaskulární choroby), takže se užívá termínu epidemie chronického onemocnění ledvin. Incidence CKD se v rozvinutých zemích západní Evropy odhaduje na 10/ 100 000 ročně, prevalence CKD definovaného jako pokles GFR pod 60 ml/ min/ 1,73 m2 je okolo 12 % [1,2]. Prudký nárůst výskytu CKD v populaci vede k závažným zdravotním následkům pro jednotlivce, přičemž nejde jen o progresi do konečného stadia selhání ledvin, ale především o zvýšení kardiovaskulární morbidity a mortality a k enormní zátěži zdravotního systému.
Klasifikace
Od roku 2002 se užívá rozdělení do pěti stadií poškození ledvin (CKD 1 – CKD 5). Nová klasifikace je založena na příčině onemocnění, kategorii GFR a kategorii albuminurie a je také označována jako stupeň CGA (cause, GFR, albuminuria) [1]. Dle doporučení KDIGO z roku 2013 [1] nyní CKD rozdělujeme do šesti stadií (tab. 1).
Table 1. Klasifikace chronického onemocnění ledvin dle GFR. 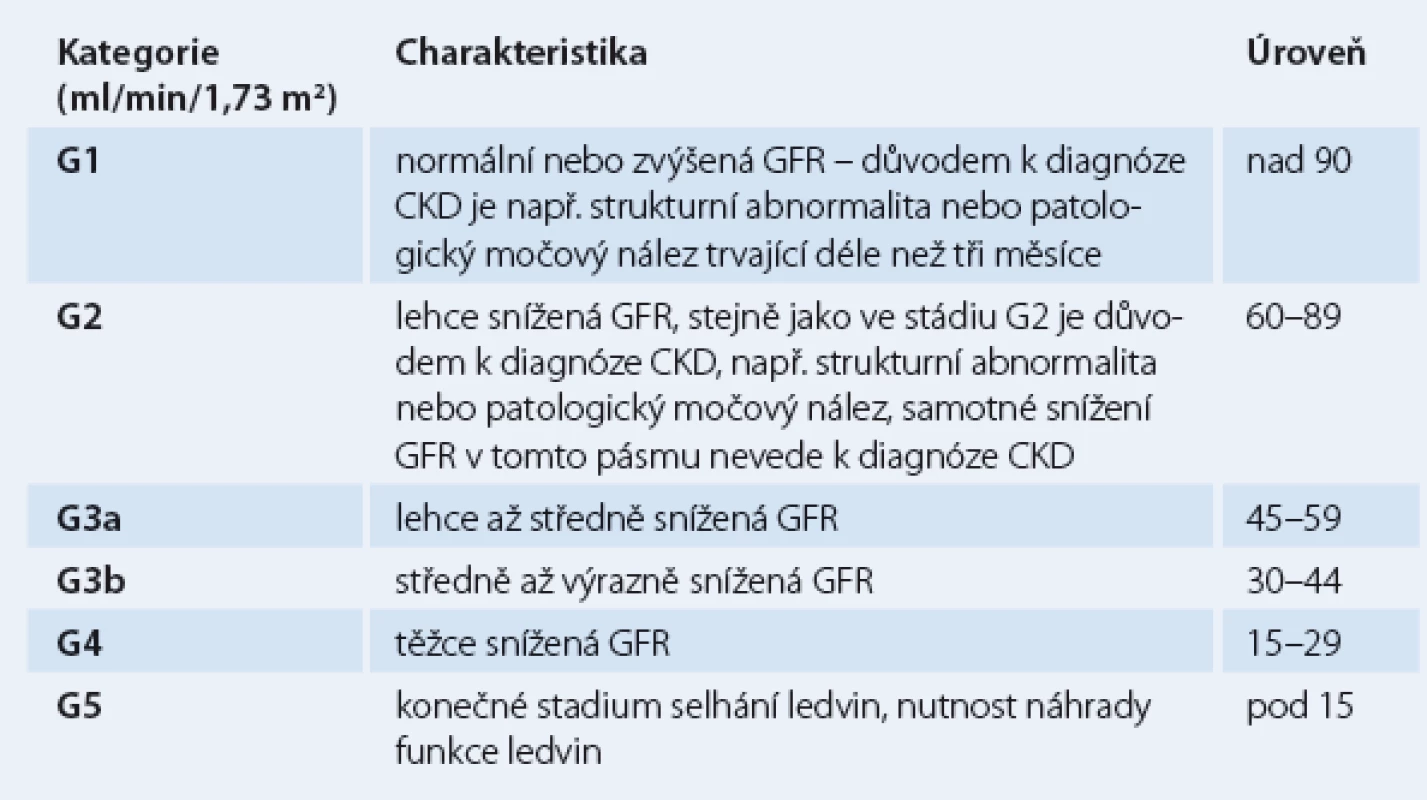
Hlavní rozdíl oproti předchozí klasifikaci GFR z roku 2002 spočívá v rozdělení někdejšího stadia CKD 3 do dvou pásem (G3a, G3b). K správnému určení stadia CKD je však vždy nutné ještě uvést příčinu a přítomnost albuminurie (≥ 30 mg/ 24 hod trvající déle než tři měsíce), jejíž přítomnost má prognostický význam ve vztahu ke kardiovaskulární mortalitě [3,4]. Rozdělení tíže albuminurie uvádí tab. 2.
Table 2. Klasifikace chronického onemocnění ledvin dle albuminurie. 
Vyšetření glomerulární filtrace a albuminurie
Jako zlatý standard stanovení očišťovací schopnosti ledvin je dosud mnohdy uváděno vyšetření clearance kreatininu pomocí 24hodinového sběru moči, od něhož se však postupně upouští pro časté zatížení chybou na straně pacienta nebo ošetřujícího personálu. V současnosti se doporučuje odhad glomerulární filtrace (eGFR – estimated Glomerular Filtration Rate) s užitím některého ze vzorců, např. MDRD, CKD ‑ EPI nebo Lund ‑ Malmö. Pro evropské pacienty s již předpokládaným snížením funkce ledvin se jeví jako nejvhodnější vzorec Lund ‑ Malmö se zohledněním výšky a hmotnosti pacienta [5]. K vyšetření albuminurie lze užít testační proužky na močový albumin nebo vyšetření poměru albumin/ kreatinin ve vzorku moči. Protože je vyšetření albuminurie senzitivnějším ukazatelem glomerulárního poškození než proteinurie, má se mu dávat přednost [1]. Vyšetření GFR a albuminurie by mělo být u nemocných s CKD prováděno alespoň jednou ročně.
Etiologie
Nejčastěji ke vzniku a rozvoji CKD vedou diabetes mellitus (cca 30 %) a arteriální hypertenze (cca 22 %), glomerulopatie (cca 12 %), intersticiální nefritidy (8 %), dědičné nefropatie (zejména polycystické onemocnění ledvin (5 %) a systémová onemocnění (4 %), v méně než 10 % není příčina chronického selhání ledvin zjištěna [6].
Hlavní rizikové faktory ovlivňující progresi chronického selhání ledvin uvádí tab. 3.
Table 3. Rizikové faktory chronického onemocnění ledvin [1,6]. ![Rizikové faktory chronického onemocnění ledvin [1,6].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/07206d81d702ca344cc3e19197bf86ac.png)
Patofyziologie
CKD vede k postupné ztrátě funkčních glomerulů. Ve zbývajících glomerulech dochází ke zvýšení intraglomerulárního tlaku s hyperfiltrací, kterou dále zvyšuje současně přítomná arteriální hypertenze. Hyperfiltrace je do značné míry zprostředkována angiotenzinem II, který působí zvýšenou produkci cytokinů a růstových faktorů, čímž dochází ke glomerulární hypertrofii a hyperplazii. Současně dochází ke zvýšení glomerulární permeability s následnou ztrátou glomerulární funkce. Důsledkem je albuminurie a proteinurie, která vede k dalšímu poškození renální funkce. U nemocných s CKD je dále zvýšená koncentrace hormonu regulujícího sérový fosfát (FGF 23 – Fibroblast Growth Factor 23), který snižuje zvýšením fosfaturie sérové koncentrace fosforu. Míra zvýšení FGF 23 signifikantně koreluje s morbiditou a mortalitou pacientů s CKD [7]. CKD vede k progresivnímu poklesu exkretorické renální funkce, k poruše vodní, elektrolytové a acidobazické rovnováhy, k poklesu endokrinní funkce (např. snížená sekrece erytropoetinu, reninu, aktivního vitaminu D a prostaglandinů) a k toxickému orgánovému poškození následkem retence nefrotoxinů.
Terapie
Každý pacient s CKD by měl být odeslán nejpozději ve stadiu G3a k nefrologické dispenzarizaci. Od okamžiku stanovení diagnózy CKD je indikována konzervativní terapie, při jejímž selhání je třeba funkci ledvin nahradit (RRT). Vhodná léčba chronického onemocněn ledvin může oddálit nutnost náhrady funkce ledvin o řadu let. I pokud není příčina onemocnění ledvin ovlivnitelná, lze při dobrém vedení pacienta optimálně načasovat náhradu funkce ledvin, do níž nemocný vstupuje připraven (pacientovi je umožněn výběr metody náhrady funkce ledvin; je provedeno očkování proti hepatitidě B; je zajištěn cévní přístup – event. katetr pro peritoneální dialýzu; proběhl kontakt s transplantačním centrem – zařazení do čekací listiny k transplantaci ledviny, ideálně pak je možná preemptivní transplantace od žijícího dárce ještě před nutností zahájení dialýzy). Neplánované akutní zahájení dialyzační léčby znamená pro nemocného větší zátěž a potenciálně větší množství komplikací [8].
Konzervativní terapie zahrnuje:
Léčbu základního onemocnění, je‑li to možné, např. těsnou kompenzaci diabetu v případě diabetického onemocnění ledvin (nový nález pro diabetickou nefropatii), terapii glomerulopatie nebo např. experimentální terapii hereditárních renálních chorob.
Úpravu stávající a nové farmakoterapie, především eliminaci lékových nefrotoxinů (např. aminoglykosidy, analgetika, nesteroidní antiflogistika a selektivní COX2 inhibitory), opatrné užití rentgenových kontrastních látek, prevence kontrastové nefropatie. Před nasazením nové lékové terapie je zapotřebí ověřit případné kontraindikace vyplývající z deteriorace renální funkce.
Kompenzaci arteriální hypertenze – důsledná kontrola hypertenze má zásadní význam v zabránění progrese renální insuficience, cílové hodnoty u nemocných s albuminurií jsou pod 130/ 80 mmHg a u nemocných bez albuminurie pod 140/ 90 mmHg. Preferovaným antihypertenzivem jsou ACE ‑ I nebo sartany, kombinace obou je vyhrazena jen pro zvláštní případy [9,10].
Dieta s omezením bílkovin se již nedoporučuje paušálně všem nemocným, o jejím doporučení by mělo být rozhodnuto individuálně. Vhodná jsou ketoanaloga esenciálních aminokyselin. Význam diety s omezením bílkovin poklesl v éře bezproblémové dostupnosti metod náhrady funkce ledvin, v každém případě musí být dieta energeticky hodnotná a nesmí vést k malnutrici. Při hypertenzi a přítomnosti otoků se doporučuje omezení soli, naopak v případě excesivních ztrát soli je někdy nutné sůl substituovat [11].
Zvýšený obrat tekutin s cílem dosáhnout diurézy kolem 2,5 l/ den napomáhá poklesu sérové močoviny. Při progresi renální insuficience je třeba zavést do medikace kličková diuretika, z nichž se v tuzemsku užívá dosud jen furosemid, ve světě je k dispozici účinnější torasemid [11].
Nutností je pravidelná kontrola vodní, elektrolytové a acidobazické rovnováhy. Pro nemocného je největším bezprostředním rizikem hyperkalemie, kterou lze ovlivnit omezením potravin bohatých na draslík (ovoce, zelenina), nutná je také kontrola užívané medikace a léčba event. současně přítomné metabolické acidózy. Acidózu je třeba korigovat substitucí bikarbonátu, čímž se snižuje progrese sekundárního hyperparatyreoidizmu [11].
Součástí léčby chronického onemocnění ledvin je i profylaxe a léčba renální osteopatie (substituce vitaminu D3 po normalizaci hladiny sérového fosfátu, normalizace hladiny sérového kalcia).
Terapie renální anemie je indikována při poklesu Hb pod 100 g/ l, cílovou hodnotou Hb je 110 – 120 g/ l [12].
Náhrada funkce ledvin (RRT) je možná hemodialýzou, peritoneální dialýzou a transplantací ledviny. RRT je indikována při poklesu renální funkce do stadia G5, při nekontrolovatelné hypertenzi, nezvládnutelné hyperhydrataci, symptomech uremie (perikarditida, encefalopatie, krvácení, gastritida), konzervativně neovlivnitelných poruchách acidobazické rovnováhy a výrazné hyperkalemii. Většina nemocných v České republice je léčena hemodialýzou. Rovnocennou alternativou hemodialýzy je peritoneální dialýza, která má oproti hemodialýze některé výhody (větší autonomie pacienta, flexibilnější rozvržení času, nezávislost na dialyzačním středisku, nižší výkyvy objemu tělních tekutin a nižší alterace renální perfuze a s tím spojené delší přetrvávání reziduální funkce ledvin, menší kardiovaskulární zátěž – není nutný cévní přístup, zahájení je možné v krátké době po zavedení katetru, očišťování krve probíhá plynule a nikoli skokově jako při hemodialýze, déle je zachována reziduální diuréza). Peritoneální dialýza též představuje nejvhodnější metodu k překlenutí období mezi selháním ledvin a transplantací. Má některé kontraindikace, např. nekooperativní pacient, těžká obezita, střevní vývod a srůsty po břišních operacích [13].
Transplantace ledviny je optimální léčebná varianta u konečného selhání ledvin. Jde již o rutinní chirurgický zákrok používaný více než 60 let. Ve srovnání s dialýzou je transplantace spojena s lepší prognózou, kvalitou života a s významně nižšími náklady pro zdravotní systém. S lepšími výsledky je spojena transplantace ledviny od žijícího dárce. V rozporu s obecným přesvědčením již není kompatibilita krevních skupin dárců nezbytným předpokladem. V České republice je možné provést tzv. cross ‑ over transplantaci mezi dvěma páry s inkompatibilní krevní skupinou, rozvíjí se i program transplantace od AB0 inkompatibilního žijícího dárce – díky pokrokům v imunosupresivní léčbě a po přípravě imunoabsorpcí, jíž se odstraní protilátky proti příjemcově krevní skupině [13].
Závěr
Chronické onemocnění ledvin je závažný, progredující stav, který vede k závažným komplikacím, především ke zvýšení kardiovaskulární morbidity a mortality a k nutnosti náhrady funkce ledvin i k velmi vysoké finanční zátěži celého zdravotního systému. Počet nemocných s CKD se nadále zvyšuje. Chronické onemocnění ledvin by mělo být aktivně vyhledáváno zejména v rizikových skupinách (diabetiků, hypertoniků). K nemocnému s CKD je nutný komplexní přístup, každý pacient s onemocněním ledvin v jakémkoli stadiu by měl být vyšetřen nefrologem, od stadia G3a je nutná nefrologická dispenzarizace. Vzhledem ke zvýšenému kardiovaskulárnímu riziku a riziku progrese chronické renální insuficience by u pacientů s CKD měla být včas zavedena preventivní opatření. Optimální metodou náhrady funkce ledvin je transplantace ledviny od žijícího dárce. Při pečlivé dispenzarizaci a odpovídající spolupráci je možné dosáhnout dobré kvality života.
Doručeno do redakce 13. 2. 2014
Přijato po recenzi 17. 2. 2014
MU Dr. PhDr. Oskar Zakiyanov
www.vfn.cz
zoskar@post.cz
Sources
1. Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Inter Suppl 2013; 3 : 1 – 150.
2. US Renal Data System (USRDS). 2010 Annual Data Report: Atlas of Chronic Kidney Disease and Atlas of End‑Stage Renal Disease in the United States. Bethesda, Md: National Institutes of Health, National Institute of Diabetes and Digestive and Kidney Diseases; 2010.
3. Chronic Kidney Disease Prognosis Consortium, Matsushita K, van der Velde M, Astor BC et al. Association of estimated glomerular filtration rate and albuminuria with all‑cause and cardiovascular mortality in general population cohorts: a collaborative meta‑analysis. Lancet 2010; 375 : 2073 – 2081. doi: 10.1016/ S0140 – 6736(10)60674 – 5.
4. Hallan S, Astor B, Romundstad S et al. Association of kidney function and albuminuria with cardiovascular mortality in older vs younger individuals:The HUNT II Study. Arch Intern Med 2007; 167 : 2490 – 2496.
5. Björk J, Jones I, Nyman U et al. Validation of the Lund ‑ Malmö, Chronic Kidney Disease Epidemiology (CKD ‑ EPI) and Modification of Diet in Renal Disease (MDRD) equations to estimate glomerular filtration rate in a large Swedish clinical population. Scand J Urol Nephrol 2012; 46 : 212 – 222. doi: 10.3109/ 00365599.2011.644859.
6. Trivedi HS, Pang MM, Campbell A et al. Slowing the progression of chronic renal failure: economic benefits and patients’ perspectives. Am J Kidney Dis 2002; 39 : 721 – 729.
7. Wahl P, Wolf M. FGF23 in chronic kidney disease. Adv Exp Med Biol 2012; 728 : 107 – 125. doi: 10.1007/ 978 - 1 - 4614 - 0887 - 1_8.
8. Tiefenthaler M, Gritsch B, Zotter K et al. Reduced costs of hospitalization at the start of hemodialysis by previous creation of an AV ‑ fistula. Investigation of the Austrian system of financing data of incident patients from 1999 to October 2000 at the Landeskrankenhaus Innsbruck University Clinic. Acta Med Austriaca 2003; 30 : 121 – 126.
9. Upadhyay A, Earley A, Haynes SM et al. Systematic review: blood pressure target in chronic kidney disease and proteinuria as an effect modifier. Ann Intern Med 2011; 154 : 541 – 548. doi: 10.7326/ 0003 - 4819 - 154 - 8 - 201104190 – 00335.
10. Brenner BM, Cooper ME, De Zeeuw D et al. Effects of losartan on renal and cardiovascular outcomes in type 2 diabetes and nephropathy. N Engl J Med 2001; 345 : 861 – 869.
11. Abboud H, Henrich WL. Clinical practice. Stage IV chronic kidney disease. N Engl J Med 2010; 362 : 56 – 65. doi: 10.1056/ NEJMcp0906797.
12. Locatelli F, Covic A, Eckardt KU et al. Anaemia management in patients with chronic kidney disease: a position statement by the Anaemia Working Group of European Renal Best Practice (ERBP). Nephrol Dial Transplant 2009; 24 : 348 – 354. doi: 10.1093/ ndt/ gfn653.
13. Sinnakirouchenan R, Holley JL. Peritoneal dialysis versus hemodialysis: risks, benefits, and access issues. Adv Chronic Kidney Dis 2011; 18 : 428 – 432.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2014 Issue 1-
All articles in this issue
- Invazivní léčba karotických stenóz a možnosti její optimalizace transkraniální dopplerovskou ultrasonografií
- Trvalá kardiostimulace z pohledu nových evropských doporučení roku 2013
- Kardiohepatální syndrom u chronického srdečního selhání
- Prognostický význam elevace funkčních jaterních testů u akutních koronárních syndromů s manifestním srdečním selháním
- Vývoj renálních parametrů u pacientů s pokročilým srdečním selháním léčených levosimendanem – retrospektivní analýza
- Renální denervace – budoucnost nebo zklamání
- Hluboká žilní trombóza a plicní embolie při užívání hormonální antikoncepce
- Argumenty pro konzervativní léčbu chronické formy ischemické choroby srdeční přibývají
- Komplexní ošetřovatelská dokumentace při krátkodobé hospitalizaci pacientů indikovaných k trvalé kardiostimulaci
- Chronické onemocnění ledvin – novinky v klasifikaci a terapii
- Farmakoterapie při chronickém onemocnění ledvin
- Akutní poškození ledvin
- Rychle progredující glomerulonefritidy (srpkovité glomerulonefritidy)
- Vybrané choroby ledvin v těhotenství
- Infekce dolních a horních močových cest
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Akutní poškození ledvin
- Vybrané choroby ledvin v těhotenství
- Rychle progredující glomerulonefritidy (srpkovité glomerulonefritidy)
- Farmakoterapie při chronickém onemocnění ledvin
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

