-
Medical journals
- Career
Ticagrelor u pacientů s akutním koronárním syndromem
: J. Špinar; J. Vítovec
: Kardiol Rev Int Med 2012, 14(3): 194-199
:
Ticagrelor je orální, reverzibilní, přímý inhibitor receptoru pro adenozindifosfát (ADP) typu P2Y12, má rychlejší nástup účinku a více vyjádřenou antiagregační aktivitu než clopidogrel a nepatří do skupiny thienopyridinů. Ve velké multicentrické studii PLATO (180 mg úvodní dávka, 90 mg dvakrát denně udržovací dávka) byl zkoušen proti clopidogrelu (300–600 mg úvodní dávka, 75 mg udržovací dávka) u 18 624 nemocných s akutním koronárním syndromem s ST elevacemi i bez nich. Po 12 měsících se kombinovaný cíl úmrtí z kardiovaskulárních příčin, infarkt myokardu či cévní mozková příhoda vyskytl u 9,8 % nemocných léčených ticagrelorem vs 11,7 % u nemocných léčených clopidogrelem (p < 0,001). Nebyl pozorován rozdíl ve výskytu velkých krvácení (11,6 % vs 11,2 %, p = 0,43). V prosinci 2010 byl ticagrelor pod názvem Brilique registrován i v České republice, od června 2012 má schválenou úhradu a některá pracoviště s ním mají již první klinické zkušenosti.
Klíčová slova:
ticagrelor – akutní koronární syndrom – duální antiagregace – mortalita – krvácení
Ticagrelor je nové perorálně účinné protidestičkové léčivo; chemickou strukturou patří mezi cyklopentyl-triazolo-pyrimidiny (CPTP) (není tedy thienopyridin!) (obr. 1). Mechanizmus jeho antiagregačního účinku spočívá stejně jako u thienopyridinů (clopidogrel, prasugrel) ve vazbě na destičkový receptor P2Y12 pro ADP s následnou blokádou aktivace trombocytů zprostředkované ADP (obr. 2). Na rozdíl od thienopyridinů působí ticagrelor přímo, bez nutnosti konverze na aktivní metabolit, a blokáda aktivace destiček vyvolaná ticagrelorem je reverzibilní [1]. Ticagrelor má rychlý nástup účinku, po perorálním podání iniciální dávky 180 mg pacientům se stabilizovanou ICHS léčeným ASA dochází po 30 min k průměrné inhibici agregace krevních destiček v rozsahu přibližně 41 %, maxima (asi 89 %) je dosaženo za 2–4 hod, účinek přetrvává 2–8 hod [2–3].
1. Chemické složení inhibitorů P2Y<sub>12</sub> blokátorů. 
2. Mechanizmus účinku léků s antiagregačním působením. 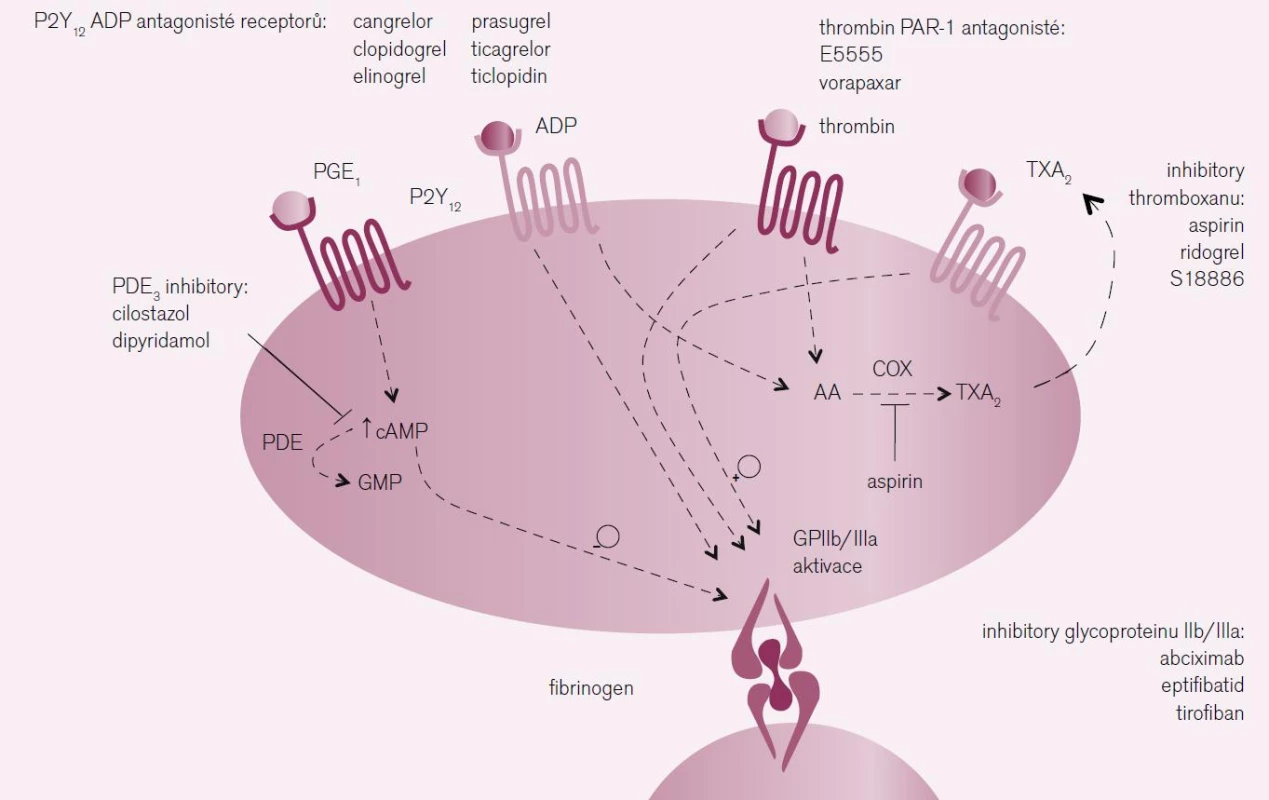
Ticagrelor se po perorálním podání rychle absorbuje. Příjem stravy významně neovlivňuje Cmax ani AUC ticagreloru ani aktivního metabolitu. Obě látky se silně vážou na plazmatické proteiny (> 99,7 %). Po podání radioaktivního ticagreloru se větší část aktivity z organizmu vylučuje stolicí, menší část močí. Průměrný eliminační poločas je asi 7 hod pro ticagrelor a 8,5 hod pro aktivní metabolit.
Ticagrelor je indikován v kombinaci s kyselinou acetylsalicylovou (ASA) k prevenci aterotrombotických příhod u dospělých pacientů s akutním koronárním syndromem (nestabilní angina pectoris, infarkt myokardu bez elevace segmentu ST nebo infarkt myokardu s elevací segmentu ST, včetně pacientů léčených konzervativně a pacientů, kteří byli ošetřeni perkutánní koronární intervencí (PCI) nebo jsou po koronárním arteriálním bypassu (CABG)).
Mezi kontraindikace podání ticagreloru patří přecitlivělost na složky přípravku, aktivní patologické krvácení, anamnéza nitrolebního krvácení, střední až závažné poškození jater, souběžné podávání se silnými inhibitory CYP3A4 (např. s ketokonazolem, klarithromycinem, nefazodonem, ritonavirem a atazanavirem).
Podávání ticagreloru pacientům se zvýšeným rizikem krvácení se má zvažovat, pouze pokud příznivý efekt prevence ischemických příhod převáží nad rizikem závažného krvácení. To se týká zejména pacientů: se sklonem ke krvácení (např. kvůli nedávnému úrazu, nedávno prodělané operaci, nedávnému nebo opakovanému gastrointestinálnímu krvácení nebo aktivnímu peptickému vředu); kteří současně užívají další léčivé přípravky, které mohou zvyšovat riziko krvácení, včetně perorálních antikoagulancií, NSAID atd.
Pokud má pacient podstoupit plánovanou operaci a antiagregační účinek není žádoucí, je vhodné ticagrelor vysadit sedm dní před výkonem. Opatrnost se doporučuje u pacientů s bronchiálním astmatem a/nebo CHOPN, u pacientů se středně závažným a závažným poškozením funkce ledvin a u pacientů s hyperurikemií.
Pacienti se zvýšeným rizikem bradykardie (např. pacienti bez pacemakeru se syndromem nemocného sinu, AV blokádou 2. a 3. stupně nebo synkopou vyvolanou bradykardií) byli vzhledem k výskytu většinou asymptomatických komorových pauz v časných fázích klinického vývoje vyloučeni ze studie PLATO. Vzhledem k omezeným klinickým zkušenostem se u těchto pacientů doporučuje opatrnost.
Podle výsledků studie PLATO se ticagrelor a clopidogrel významně nelišily ve frekvenci velkých fatálních nebo život ohrožujících krvácení (viz níže). U pacientů léčených ticagrelorem byly s vyšší četností než u pacientů léčených clopidogrelem dále hlášeny: dušnost (proto opatrnost u nemocných s CHOPN) a pocit tíže na hrudi, zvýšení sérového kreatininu, zvýšení koncentrace kyseliny močové v séru. Zvýšený výskyt bradyarytmických příhod neměl klinický význam.
Současné podávání silných inhibitorů CYP3A4 je vzhledem k možnosti zvýšení expozice vůči ticagreloru kontraindikováno. Nedoporučuje se ani současné podávání simvastatinu nebo lovastatinu v dávkách nad 40 mg/den, jiné statiny metabolizované CYP3A4 byly v klinické studii podávány bez problémů s bezpečností. Pečlivé klinické sledování se doporučuje při současném podávání léků s nízkým terapeutickým indexem, jejichž metabolizmus je závislý na P-gp (např. digoxin nebo cyklosporin). Opatrnost se doporučuje také při současném podávání s léky, které působí bradykardii; při současném podávání s betablokátory; s blokátory kalciového kanálu diltiazemem a verapamilem ani s digoxinem však nebyly pozorovány žádné klinicky významné nežádoucí účinky.
Počáteční (sytící) dávka je 180 mg (2 tbl), dále se pokračuje dávkou 90 mg dvakrát denně. Podává se v kombinaci s ASA (pokud není kontraindikována) v dávce 75–150 mg/den. Doporučená doba léčby je až 12 měsíců po akutním koronárním syndromu, zkušenosti s delší léčbou jsou omezené. Pokud to není klinicky indikováno, léčba by neměla být přerušena ani předčasně ukončena. S podáváním ticagreloru s antikoagulačními preparáty (warfarin, dabigatran, rivaroxaban) jsou jen omezené zkušenosti. Pacienti dosud léčení clopidogrelem mohou být převedeni na ticagrelor podle potřeby. Přechod z prasugrelu nebyl studován. Současná doporučení po akutním infarktu myokardu doporučují až 12měsíční užívání duální antiagregační léčby – kyselina acetylsalicylová + clopidogrel nebo prasugrel nebo ticagrelor.
U starších pacientů, u pacientů s poruchou funkce ledvin a u pacientů s mírnou poruchou funkce jater není nutná úprava dávky. Tablety se užívají v pravidelnou denní dobu, s jídlem nebo mimo jídlo. Vynechání dávky je nežádoucí.
Ticagrelor byl testován v klinické studii PLATO: Ticagrelor versus clopidogrel in patients with acute coronary syndroms [4–6].
Do studie PLATO bylo zařazeno 18 624 ne-mocných po akutním infarktu myokardu, kteří byli randomizováni na clopidogrel (300–600 mg úvodní dávka, 75 mg udržovací dávka) a ticagrelor (180 mg úvodní dávka, 90 mg dvakrát denně udržovací dávka) a bylo doporučeno, aby současně užívali kyselinu acetylsalicylovou. Studie probíhala v 862 centrech ve 43 zemích a nábor byl zahájen v říjnu 2006 a ukončen v červnu 2008. Sledování nemocných probíhalo do února 2009. Randomizace proběhla do 24 hod od akutního koronárního syndromu, medián podání léku od vzniku bolesti na hrudi byl 11,3 hod. Permanentní ukončení léčby během dvojitě slepé fáze bylo v 23,4 % u nemocných léčených ticagrelorem a v 21,5 % u nemocných léčených clopidogrelem. Průměrná doba užívání léčby byla 277 dní (od 179 do 365 dní). Vstupní charakteristiku souboru ukazuje tab. 1.
1. Charakteristika nemocných ve studii PLATO. 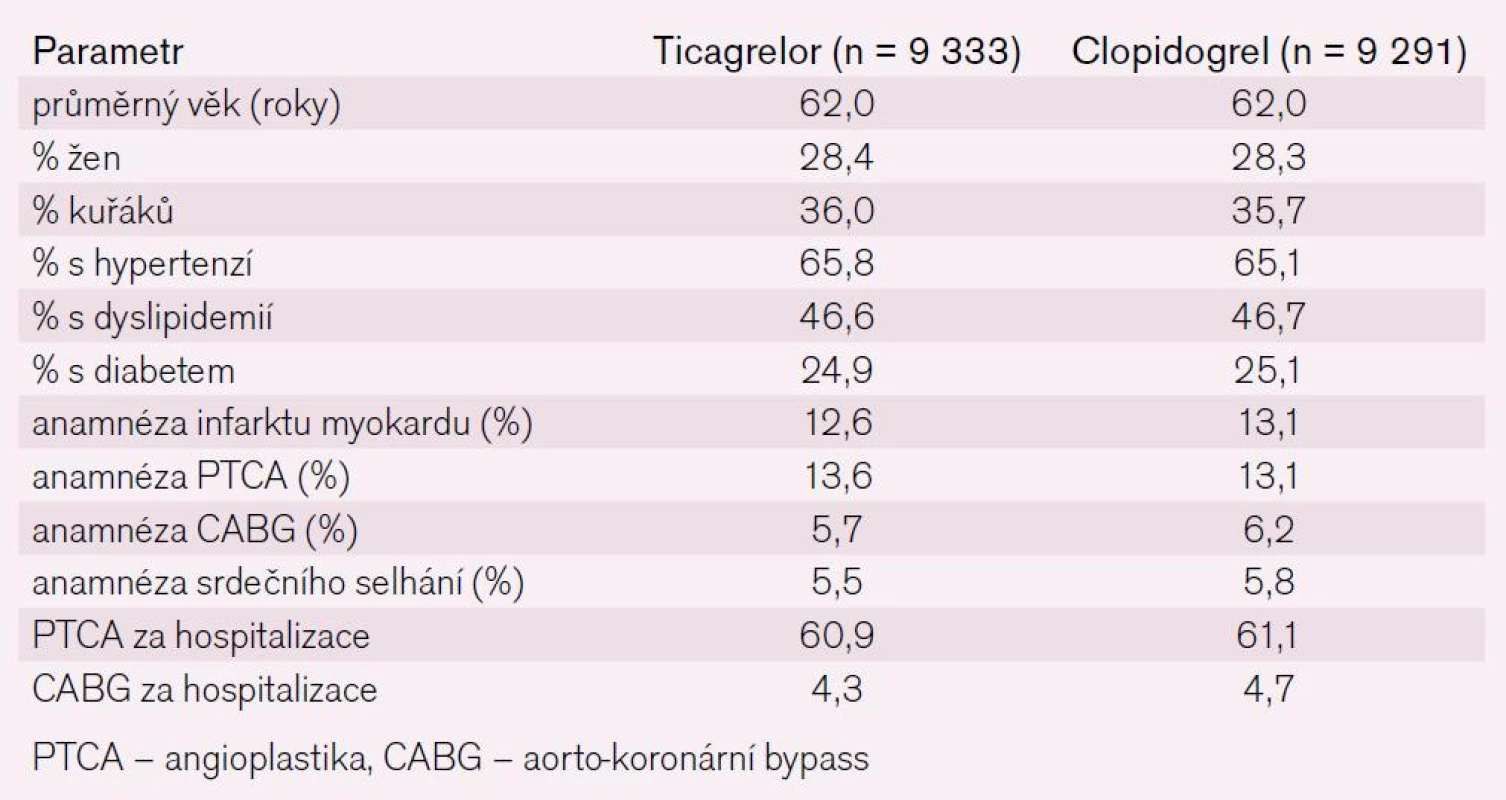
Kyselinu acatylsalicylovou za hospitalizace užívalo 97,4, resp. 97,5 % nemocných, ACE inhibitory nebo sartany 88 % nemocných, betablokátory skoro 90 % nemocných a statiny 89,7, resp. 89,2 % nemocných.
Koronární angiografie za hospitalizace byla provedena u 7 599 (81,4 %) nemocných léčených ticagrelorem a u 7 571 (81,5 %) nemocných léčených clopidogrelem.
Primární cíl – kardiovaskulární úmrtí, infarkt myokardu a cévní mozkovou příhodu ukazuje obr. 3.
3. Primární složený cíl ve studii PLATO. 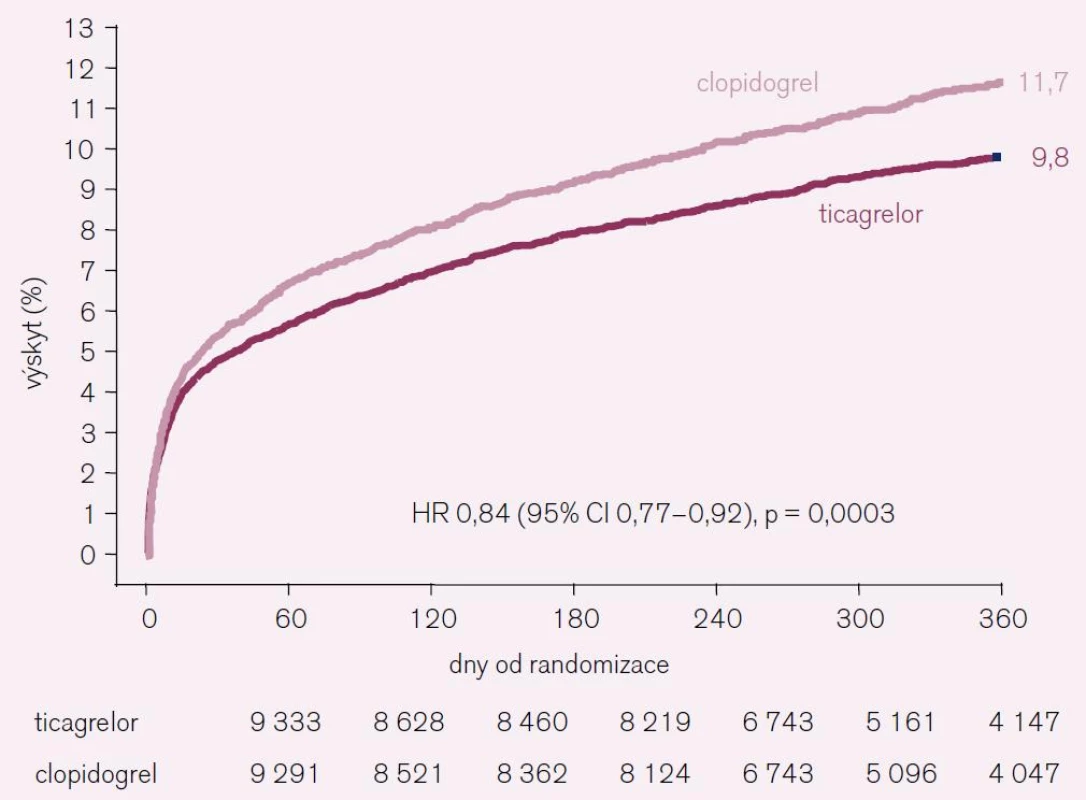
Primární cíl v čase ukazuje obr. 4. Z obrázku je patrné, že rozdíl byl pozorován již během prvních 30 dní (p = 0,045) a že se zvýraznil od 30. do 360. dne (p < 0,001).
4. Primární cíle ve studii PLATO v čase. 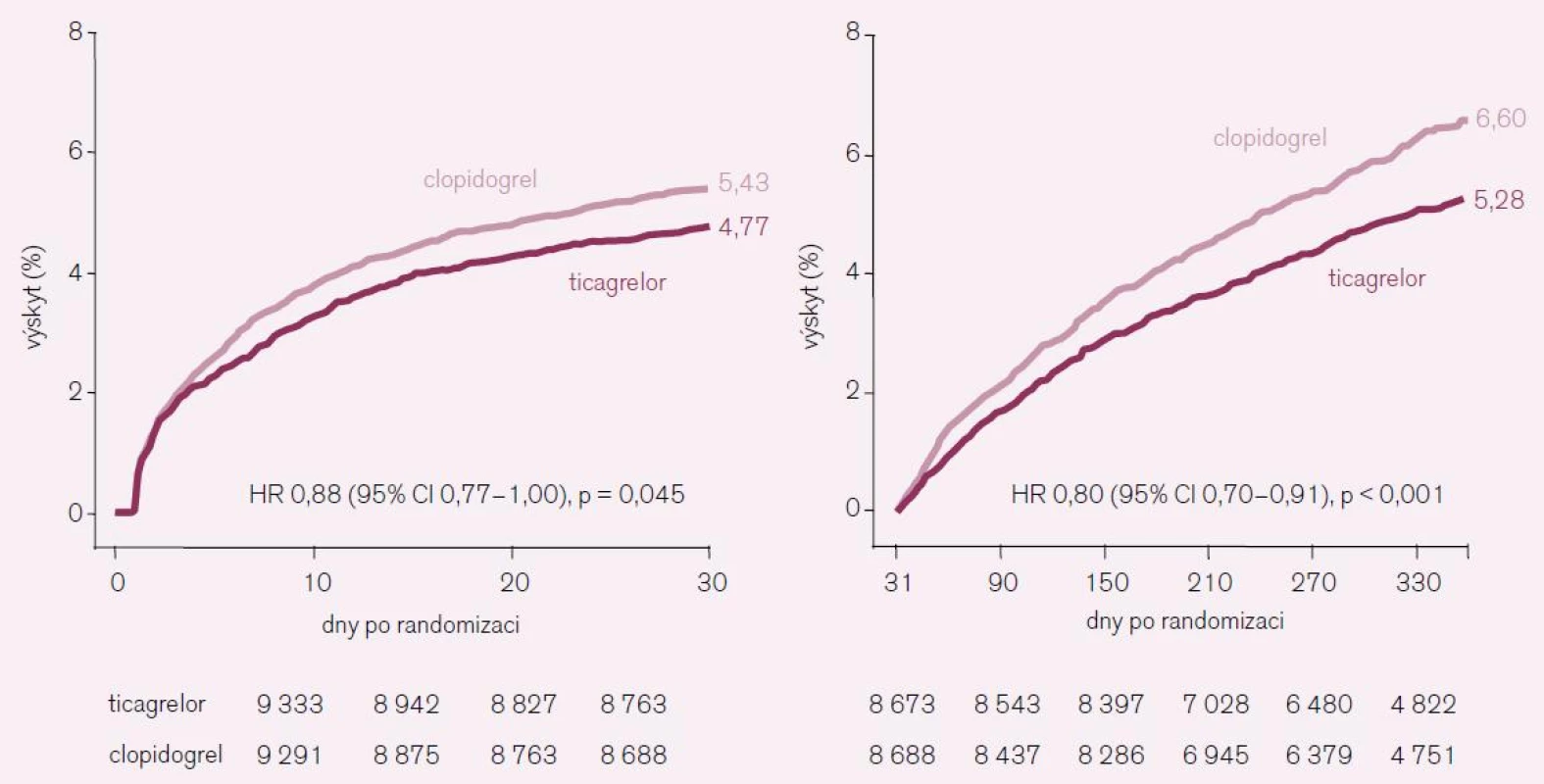
Sekundární cíle – infarkt myokardu a kardiovaskulární úmrtí samostatně ukazuje obr. 5. Oba parametry byly vysoce statisticky významné, pro infarkt myokardu p = 0,005, pro kardiovaskulární úmrtí p = 0,001.
5. Sekundární cíle ve studii PLATO. 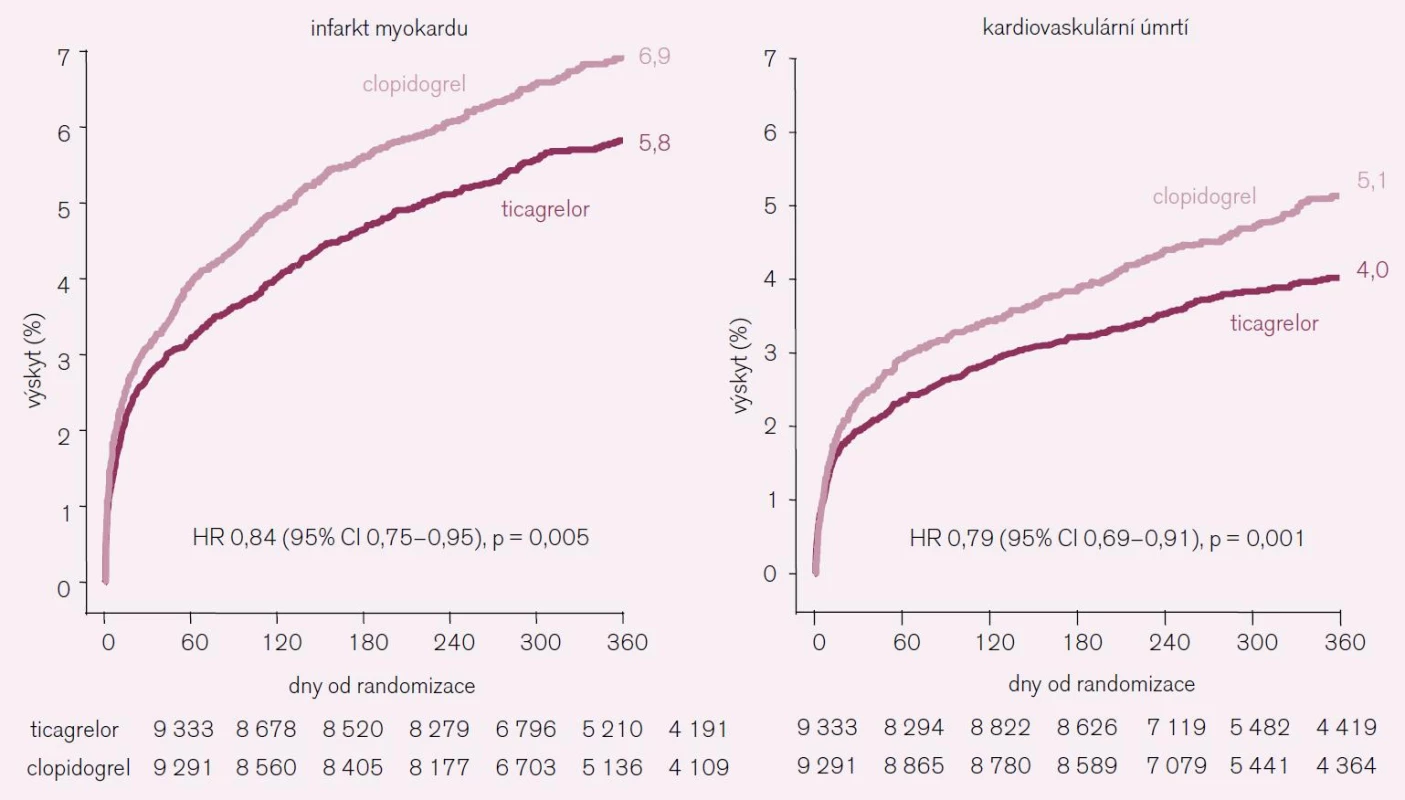
Některé vedlejší nálezy jako trombózu ve stentu, dušnost a malignity ukazuje tab. 2. Trombóza ve stentu byla významně méně přítomna u nemocných léčených ticagrelorem, naopak vyšší výskyt dušnosti u nemocných léčených ticagrelorem doposud nemá jasné vysvětlení [7,8].
2. Vedlejší nálezy ve studii PLATO. 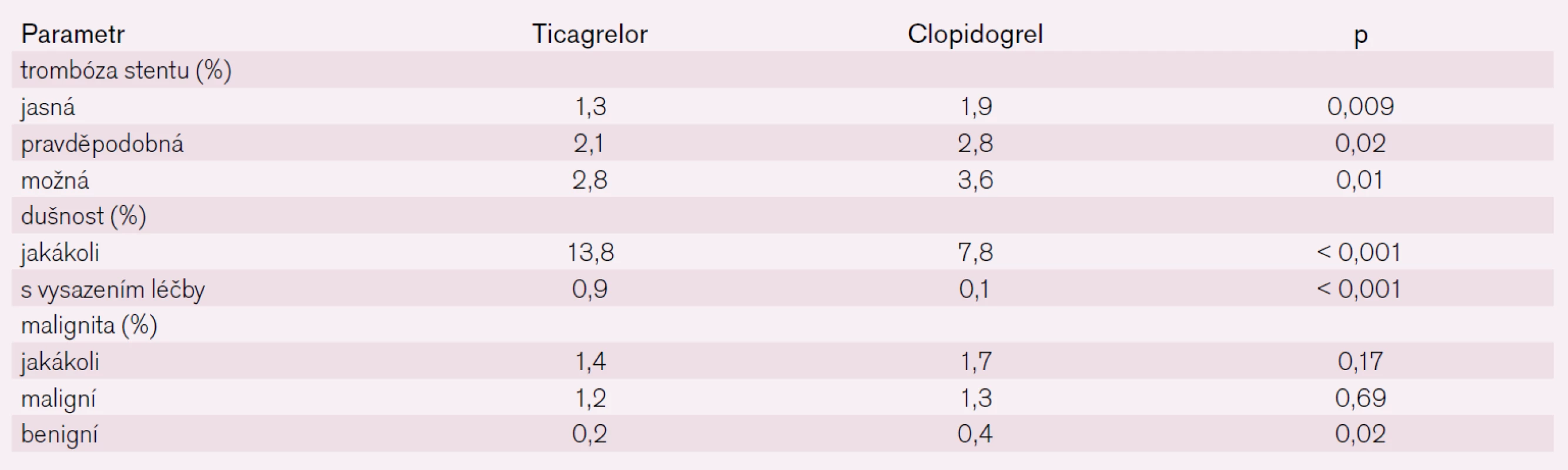
Primární bezpečnostní cíl – velké krvácení ukazují obr. 6 a 7. Je patrné, že nebyl rozdíl v obou léčených větvích. Souhrn primárních a sekundárních cílů podává tab. 3.
6. Krvácení ve studii PLATO v čase. 
7. Krvácení ve studii PLATO podle závažnosti. 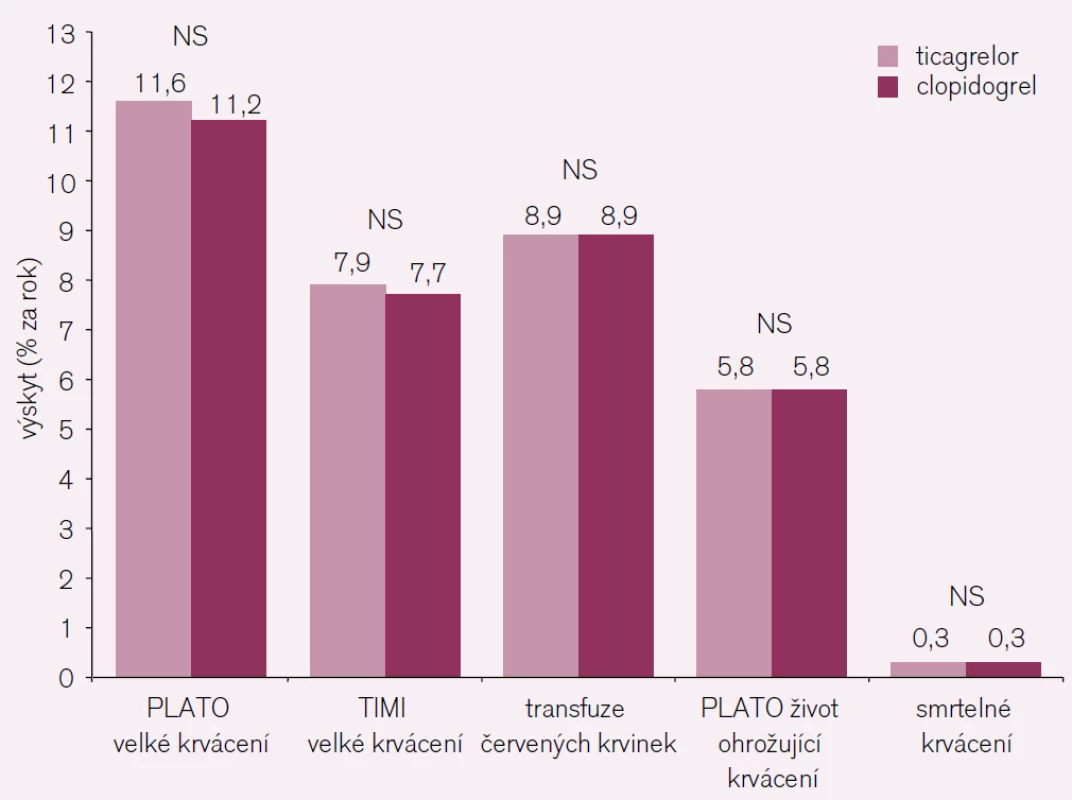
3. Hlavní výsledky studie PLATO. 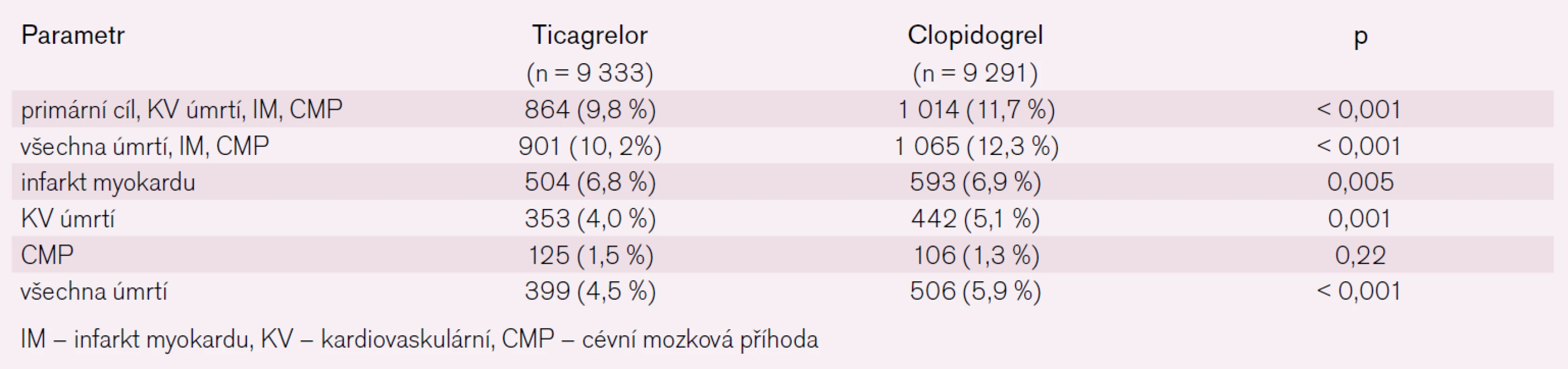
Výsledky studie PLATO můžeme shrnout do následujících bodů:
- Při léčbě 1 000 nemocných s akutním infarktem myokardu ticagrelor oproti clopidogrelu zabrání:
- 14 úmrtím,
- 11 infarktům myokardu,
- 7 trombózám ve stentu.
- Ticagrelor oproti clopidogrelu má statisticky významně nižší celkovou i kardiovaskulární mortalitu.
- Ticagrelor nezvyšuje velké ani malé krvácení.
- Zvýšený výskyt dušnosti nebyl vysvětlen, plicní funkce nebyly po ticagreloru horší než po clopidogrelu.
Americká Food and Drug Administration (FDA) schválila 20. června 2011 Brilique (ticagrelor) pro léčbu akutních koronárních syndromů [9]. V České republice byl Brilique (ticagrelor) registrován 3. 12. 2010 a úhradu má schválenou od 1. 6. 2012 a je indikován 12 měsíců po akutním koronorním syndromu společně s kyselinou acetylsalicylovou [10].
Na studii PLATO volně navazuje studie PEGASUS-TIMI 54, která má za cíl objasnit, zda má smysl dlouhodobé podávání duální antiagregace kyseliny acetylsalicylové s clopidogrelem či ticagrelorem. Randomizováni jsou tentokrát nemocní s chronickou ischemickou chorobou srdeční (1–3 roky po infarktu myokardu) a studie se opět aktivně účastní i Česká republika. Ukončení náboru se očekává ještě v roce 2012, délka sledování bude záležet na výskytu primárních endpointů – kardiovaskulárního úmrtí, infarktu myokardu a cévní mozkové příhody.
Podpořeno projektem (Ministerstva zdravotnictví) koncepčního rozvoje výzkumné organizace 65269705 (FN Brno).
Doručeno do redakce 26. 6. 2012
Přijato po recenzi 16. 7. 2012
prof. MUDr. Jindřich Špinar, CSc., FESC1
prof. MUDr. Jiří Vítovec, CSc., FESC2
1 Interní kardiologická klinika LF MU a FN Brno-Bohunice a ICRC, Brno
2 I. interní kardioangiologická klinika LF MU a FN u sv. Anny v Brně
jspinar@fnbrno.cz
Sources
1. Bultas J. Tikagrelor. Remedia 2011; 21 : 116–125.
2. Penka M. Antikoagulační a antiagregační léčba – základní principy. Kardiol Rev 2012; 14 : 63–67.
3. Penka M. Máme dnes lepší antitrombotika? Kardiol Rev 2012; 14 : 62.
4. Wallentin L, Becker RC, Budaj A et al. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009; 361 : 1045–1057.
5. Špinar J, Vítovec J. Komu zvoní hrana. Kardiol Rev 2009; 11 : 197–199.
6. Špinar J, Vítovec J. Studie RE-LY a PLATO – budeme přepisovat guidelines. Bulletin Hypertenze 2010; 13 : 22–25.
7. Scirica BM, Vannon CHP, Emanuelsson H et al. The incidence or arrhytmias and clinical arrhytmias events in patients with acute coronary syndromes treated with ticagrelor or clopidogrel in the PLATO trial. JACC 2010; 55 (10A): 1100–1274.
8. Storey RF, Bliden KP, Patil SB et al. Incidence of dyspnea and assessment of cardiac and pulmonary function in patients with stable coronary artery disease receiving ticagrelor, clopidogrel, or placebo in the ONSET/OFFSET study. J Am Coll Cardiol 2010; 56 : 185–193.
9. U.S. Food and Drug Administration. BrilintaTM Prescribin Information. http://www.accessdata.fda.gov/drugsatda/label/2011/022433s000lbl.pdf.
10. Štípal R. Perorální protidestičková léčba u pacientů s akutním koronárním syndromem. Kardiol Rev 2012; 14 : 68–71.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2012 Issue 3-
All articles in this issue
- Antidiabetic drugs and cardiovascular risk – before and now
- Importance of determining apolipoproteins B and A-1 in clinical practice
- Residual vascular risk and the possibilities of therapy.
- Lipid-modifying therapies of tomorrow – what will they be like?
- Sudden death in cardiology
- Hypertriglyceridemia and cardiovascular risk
- Troponin as a prognostic risk factor in patients hospitalized for decompensation of chronic systolic heart failure
- The use of levosimendan: up-date 2012
- Ticagrelor in patients with acute coronary syndrome
-
Antithrombotics in the prevention of cerebrovascular accidents.
Part I – Significance of antiplatelet treatment - Renal denervation and its role in the treatment of resistant hypertension
- Mitral stenosis in the terminal phase – a case report
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Importance of determining apolipoproteins B and A-1 in clinical practice
- Ticagrelor in patients with acute coronary syndrome
- Hypertriglyceridemia and cardiovascular risk
- Troponin as a prognostic risk factor in patients hospitalized for decompensation of chronic systolic heart failure
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

