-
Medical journals
- Career
Roboticky asistovaná chirurgie v ČR – aktuální pohled
Authors: J. Schraml 1; M. Broul 1; J. Rejholec 1,2; I. Blšťák 1,3; M. Vančo 1,3; K. Sláma 1,4; V. Kokoška 1
Authors‘ workplace: Klinika urologie a robotické chirurgie, Masarykova nemocnice, Univerzita Jana Evangelisty Purkyně v Ústí nad Labem 1; Chirurgické oddělení, Nemocnice Děčín 2; Gynekologicko-porodnická klinika, Masarykova nemocnice, Univerzita Jana Evangelisty Purkyně v Ústí nad Labem 3; Klinika ORL a chirurgie hlavy a krku, Masarykova nemocnice, Univerzita Jana Evangelisty Purkyně v Ústí nad Labem 4
Published in: Anest. intenziv. Med., 30, 2019, č. 6, s. 288-295
Category:
Overview
Autoři předkládají aktuální pohled na roboticky asistovanou chirurgii v České republice.
Klíčová slova:
robotické operace
Článek přináší přehled současného stavu robotické chirurgie v České republice. Metodika výběru témat a formát zpracování byly ponechány na autorském týmu, případné komentáře vyjadřují názor autorů k dané problematice.
AKTUÁLNÍ STAV V ČESKÉ REPUBLICE
Roboticky asistovaná chirurgie byla zahájena v České republice v roce 2005. Aktuálně u nás pracuje devět center robotické chirurgie, hlavně s přímou návazností na komplexní onkologická centra (KOC) – Masarykova nemocnice v Ústí nad Labem, Ústřední vojenská nemocnice, Nemocnice Na Homolce, Fakultní nemocnice v Motole, Fakultní nemocnice Hradec Králové, Fakultní nemocnice Olomouc, Nemocnice Nový Jičín, Nemocnice České Budějovice, Masarykův onkologický ústav a Nemocnice sv. Zdislavy. Většímu rozvoji robotické chirurgie ve srovnání s vyspělými státy světa nám brání systém úhrad. V minulosti byly rutinně hrazeny pouze onkologické výkony – radikální prostatektomie, radikální hysterektomie, nízká přední resekce rekta a určitou výjimkou jsou cévní a kardiochirurgické výkony v Nemocnici Na Homolce. Před zhruba třemi lety došlo k rozšíření úhrad i o robotickou resekci ledviny pro karcinom a pyeloplastiku.
Z výše uvedeného spektra hrazených výkonů vyplývá hlavní role urologa v naplnění objemu výkonů prováděných v našich jednotlivých centrech. Nosným výkonem se díky narůstající incidenci karcinomu prostaty stala robotická radikální prostatektomie. V USA došlo v posledních letech ke změně a v počtu prováděných výkonů byli urologové vystřídáni gynekology, což je dáno jinými ekonomickými podmínkami a množstvím prováděných hysterektomií i z neonkologické indikace.
ROBOTICKÉ SYSTÉMY A NÁSTROJE
Role chirurga je nadále nezastupitelná, protože robot sám nic neprovede, jedná se v podstatě o telemanipulátor. Na vlastní robotiku je nutno pohlížet jako na vyšší stupeň laparoskopie, kdy využívá všech výhod miniinavizity laparoskopie doplněné o lepší manipulaci s nástroji, u kterých došlo k miniaturizaci. Byl odstraněn třes rukou a díky tomu můžeme rutinně operovat v desetinásobném zvětšení. Dalším posunem dopředu je digitalizace přenášeného obrazu z operačního pole do konzole chirurga a možnost s tím dále pracovat.
Jediné robotické systémy dostupné v ČR jsou systémy amerického výrobce firmy Intuitive Surgical (IS). Tato firma má se svými modely daVinci i nadále 99% podíl na trhu (v ČR 100 %). Na obrázku 1 je vidět robotický systém daVinci S, skládající se z chirurgické konzole, robotických ramen a obslužné věže. Prvním systémem byl daVinci Standard, pak přišla generace daVinci S (S, Si, Sie) a poslední generací je systém daVinci X (Xi a Xs). Systém Xi v plné konfiguraci je schopen synchronního pohybu s operačním stolem (obr. 2). Varianta Xs je ekonomičtější variantou, která má určité limity při extenzivních výkonech v dutině břišní a není možná synchronizace s operačním stolem. V roce 2020 je avizován příchod Xsp, což má být přímo speciální stroj na práci pomocí speciálních nástrojů v tzv. single portu.
Image 1. Systém daVinci S. Pohled na pracujícího operatéra, který je zcela mimo operační pole 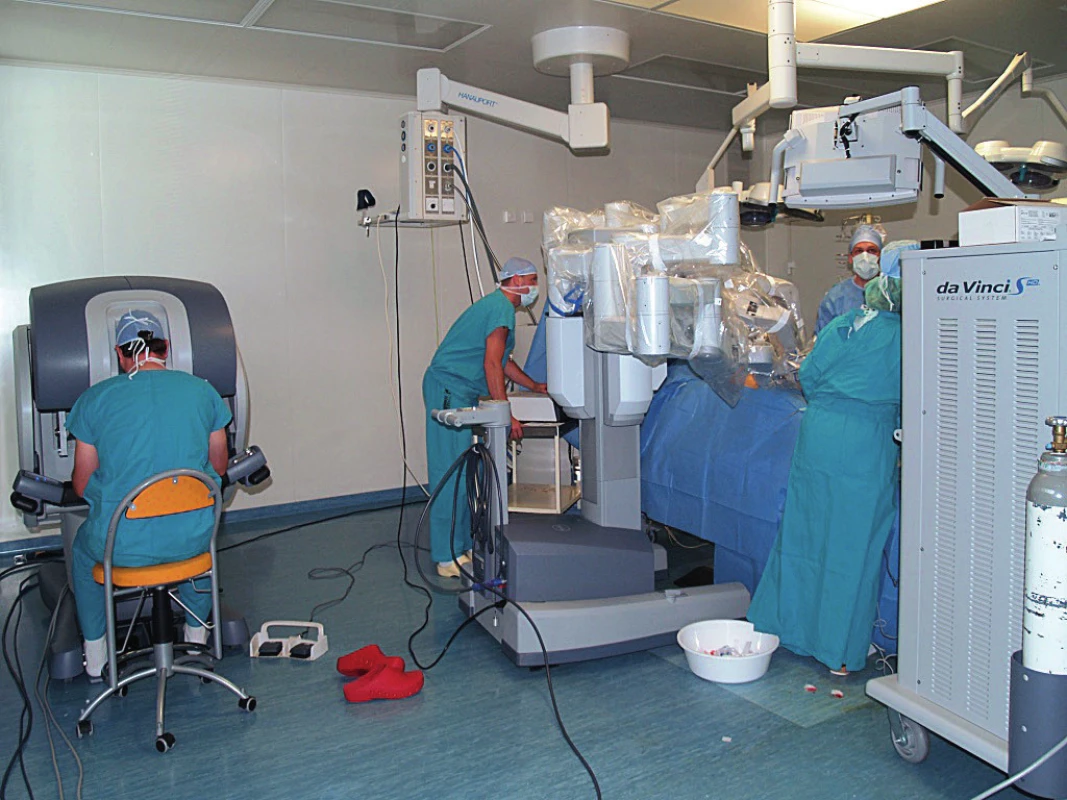
Image 2. Ukázky synchronního pohybu operačního stolu spolu s rameny systému daVinci Xi 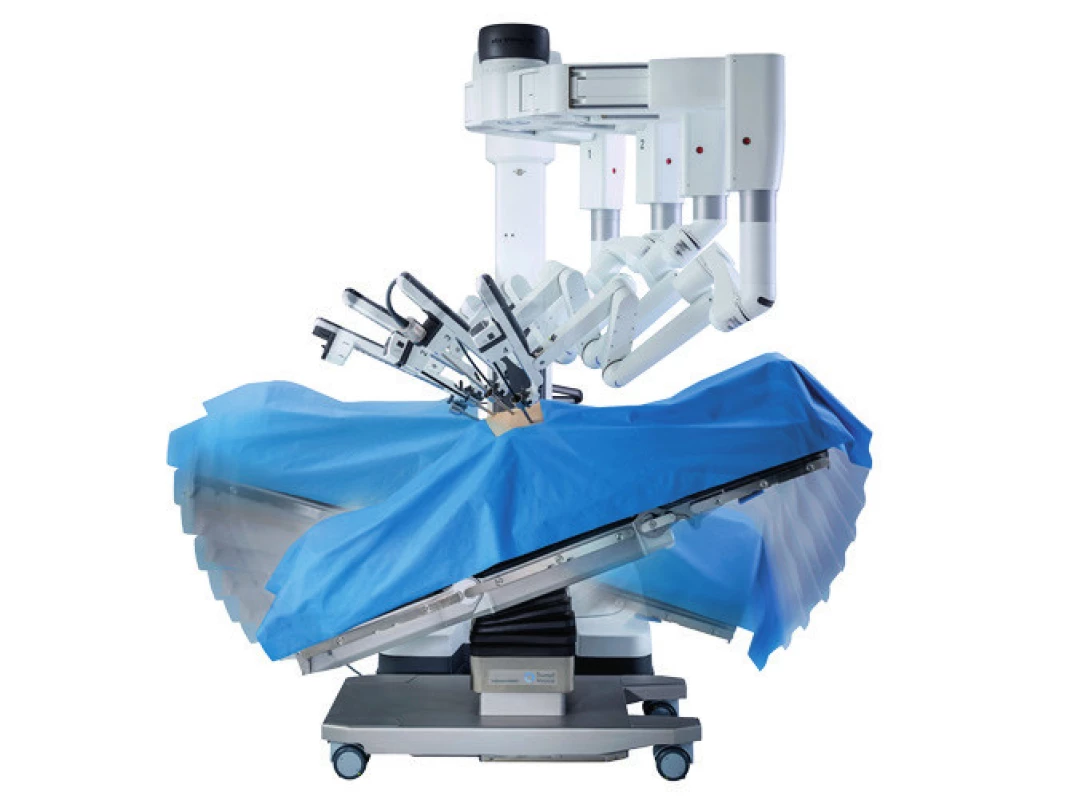
Robotické nástroje jsou schopné pracovat ať v břišní, tak i v hrudní dutině a jsou ovládány přeneseně pomocí elektromechaniky na ramenech robota. Robotické instrumenty využívají pouze 8mm portů, stejně tak i kamera u poslední generace X. To u generace X umožňuje během operace vyměnit kameru za instrument v jakémkoliv rameni. Každý z nástrojů má čipem daný limitní počet použití. Operatér ovládá stroj z chirurgické konzoly mimo operační pole, kde má reálný 3D obraz vysokého rozlišení. Povely z ovládacích zařízení jdou kabelem do věže a odtud do pacientské části, kde jsou sterilně potažená ramena a sterilní nástroje s kamerou přímo procházející do těla pacienta (obr. 1). Kamera je ovládána svépomocí operatérem a kam si ji nastaví, tam zůstane stát. Stejně tak je to s třetím nástrojem, který je úchopový a táhne či fixuje tkáň libovolně dlouho tam, kam si ho operatér postaví. Ve většině případů se využívá tří instrumentačních portů, jednoho kamerového a jednoho asistentského portu, což je běžný laparoskopický port. Určitou novinkou je možnost jednoportové varianty, např. pro cholecystektomie a apendektomie, v ČR zatím nedostupné.
PROVOZ PRACOVIŠŤ ROBOTICKÉ CHIRURGIE
Plně zapracované centrum robotické chirurgie by mělo provádět 300 a více operací za rok na jednom robotickém systému. V začátcích robotiky se udávala hranice 200 a více výkonů na sytém a rok. Nyní je IS doporučováno při dosažení 400 výkonů ročně na jednom stroji uvažovat o pořízení dalšího systému. Udává se, že logistická kapacita jednoho stroje je kolem 500 výkonů za rok. Je nutno kalkulovat, že plně edukované centrum je schopné v běžné pracovní době v průměru provádět 2,5 výkonu denně. Většina zapracovaných center zvládne tři robotické prostatektomie za osmihodinovou směnu [1, 2].
OBLASTI ROBOTICKÉ CHIRURGIE
ROBOTIKA V UROLOGII
Roboticky asistované výkony (RAS) se nyní stávají moderním způsobem léčby a i „zlatým standardem“ pro mnoho urologických operací. Nejvíce rozšířená je roboticky asistovaná radikální prostatektomie (robot-assisted laparoscopic prostatectomy, RALP) [3]. Jako první RALP popsali Menon et al. [4]. RALP nyní nahrazuje i otevřenou retropubickou radikální prostatektomii (RRP) i laparoskopickou prostatektomii (LRP) ve většině moderních nemocnic a robotických centrech [3]. Zatím neexistuje dostatek vysoce kvalitních randomizovaných studií (RCT), které by jasně prokázaly výhodu RALP oproti otevřené RRP [5], ale existuje již velké množství nerandomizovaných studií, které prokázaly jasné výhody robotického systému, a to nižší peroperační krevní ztráty, nižší nutnost krevních transfuzí, dobu nutnosti zavedení permanentního močového katétru, délky hospitalizace, pozitivních okrajů, erektilní funkce a močové kontinence [6, 7].
ROBOTICKY ASISTOVANÁ RESEKCE TUMORŮ LEDVIN (RAPN)
Přináší výhody oproti otevřenému či laparoskopickému výkonu (snížení perioperační ztráty krve, pooperační bolest a kratší dobu hospitalizace) [8]. Systematické přehledy při porovnávání RAPN a laparoskopické resekce tumoru ledvin (LPN) ukázaly, že RAPN prokazuje kratší dobu ischemie a nižší celkovou míru komplikací než LPN [9]. RAPN má také kratší learning curve než LPN a umožňuje operovat i složitější případy a větší tumory (> 4 cm, multifokální, centrální umístěné, solitární ledvina) [10, 11]. Tyto výhody jsou podobné jako u jiných operací horních cest močových, jako je roboticky asistovaná pyeloplastika, kde autoři mnoha kazuistik a malých studií uvádějí, že se RAS v této oblasti stává standardem péče [12, 13].
ROBOTICKY ASISTOVANÁ RADIKÁLNÍ CYSTEKTOMIE (RARC)
První provedli Menon et al. [14] v roce 2003. Nedávné práce porovnávaly RARC (zejména s extrakorporálními typy močových derivací) s otevřenými cystektomiemi a potvrdily, že RARC má méně perioperačních komplikací, větší množství vyňatých lymfatických uzlin, nižší ztráty krve a kratší dobu hospitalizace [15]. V současné době mnoho pracovišť již rutinně provádí cystektomie s intrakorporálními derivacemi moče (ICUD). Dalšími výhodami je postupné zkracování kožních incizí, nižší pooperační bolestivost a menší výskyt střevních komplikací [16].
ROBOTICKY ASISTOVANÁ JEDNODUCHÁ PROSTATEKTOMIE PRO BENIGNÍ HYPERPLAZII PROSTATY (BHP)
Možnosti chirurgického řešení benigní hyperplazie prostaty se za posledních dvacet let výrazně rozšířily. Pro prostatickou žlázu menší než 80 ml je jako zlatý standard doposud považována transuretrální resekce prostaty (TURP). Pro žlázy větší než 80 ml to pak bývala otevřená transvezikální prostatektomie (TVPE) [17]. Vývoj laserových technologií a MIS poskytuje mnoho alternativ léčby BHP a mají i potenciální výhody oproti tradičním způsobům [18, 19]. První laparoskopická prostatektomie pro BHP byla popsána v roce 2008 [20]. Následně vyšlo dalších 18 malých studií a existují tři nerandomizované srovnávací studie [31–38]. V těchto studiích bylo popsáno několik chirurgických technik této prostatektomie. Autoři prováděli excizi adenomů buď prostřednictvím předního transkapsulární řezu (jako u Millenovy TVPE), nebo přední horizontální cystotomii v blízkosti prostaticko-vezikální junkce (jako u Freyerovy TVPE), nebo vertikálním řezem ve vrcholu močového měchýře. Co se týče roboticky asistovaných jednoduchých prostatektomií, existuje pouze minimum randomizovaných studií. Pokud bychom srovnávali literaturu o otevřených versus roboticky asistovaných prostatektomiích, najdeme údaje o delším operačním čase roboticky asistovaných, ale opět jsou výhody MIS (menší krevní ztráta, kratší hospitalizace). Komplikace typu Clavien–Dindo větší než stupeň dva a funkční výsledky bývají popisovány u obou metod ve stejné míře. Tyto závěry byly publikovány v jediné (nerandomizované) porovnávací studii roboticky asistované versus otevření prostatektomii [38]. Existují studie porovnávající laserovou prostatektomii (HoLEP) a roboticky asistovanou jednoduchou prostatektomii [33, 35]. Počty komplikací a funkční výsledky obou metod jsou velmi podobné, ale laserové operace mají kratší dobu hospitalizace a kratší dobu se zavedením permanentním katétrem (což je dáno nutností provedení cystotomie při robotických výkonech). Jako výhodné se jeví roboticky asistované prostatektomie u pacientů, kteří mají prostatickou žlázu větší než 150 ml.
SALVAGE RARP
Salvage radikální, roboticky asistovaná prostatektomie (sRALP) bývá spojena s velkou morbiditou. První studie o roboticky asistované salvage prostatektomii vyšla v roce 2008 [40]. Následně poté proběhlo 9 dalších studií s celkovým počtem 197 zařazených pacientů. Z těchto studií vyplývá, že onkologické výsledky sRALP jsou horší než u mužů, kteří primárně podstoupili RALP. Co se týče funkčních výsledků, dopadá sRALP daleko hůř než primární RALP, a to ve všech ohledech (pozitivní okraje, krevní ztráta, striktury uretry močová inkontinence). sRALP je tedy vhodné nabízet pouze pečlivě vybraným pacientům a počítat s vysokém rizikem perioperačních komplikací, které si, na rozdíl od primární RALP, mohou vyžádat intenzivní pooperační péči.
ROBOTICKY ASISTOVANÉ OPERACE PRO NEFROLITIÁZU
Endoskopické výkony zcela vytlačily otevřenou operativu pro močové kameny. V posledních letech bylo publikováno několik studií o roboticky asistované nefrolitotomii (RNL) a roboticky asistované pyelolitotomii (RPL). RPL a RNL mohou být provedeny transperitoneálně i retroperitoneálně. Dále byly popsány případy použití roboticky asistovaných uretrolitotomií z indikace velkých, impaktovaných ureterálních kamenů. Konzolový čas byl většinou do 20 minut, tzv. stone-free rate byl 100 %, většina kamenů byla vyjmuta v cellu. Ve studii, která sledovala pacienty v dalších 20 měsících [41], nebyly pozorovány žádné následné stenózy močovodu. Roboticky asistované operace pro urolitiázu jsou možné a přínosné, ale pouze pro velice komplikované případy, kde selhala endoskopická léčba.
ROBOTICKY ASISTOVANÁ REKONSTRUKCE DISTÁLNÍHO URETERU
Chirurgické řešení ať už maligní či benigní patologie močovodu vyžaduje zároveň provést i rekonstrukční výkon, který následně zajistí normální drenáž ledviny. Existuje sedmnáct studií [42–58] publikujících zkušenosti s roboticky asistovanými rekonstrukcemi močovodů. Nejčastěji bývá popisována uretero-uretrostomie nebo uretero-neocystostomie (často spojené s metodou Boari flap či Psoas hitch). Standardizovat data těchto studií je těžké, protože data jsou velice heterogenní, co se týká typu patologie močovodu, její lokalizace a délky postižení močovodu, komorbidit pacientů, preoperačním vývojem nemoci a popisované techniky operace. Srovnání s laparoskopickou a otevřenou metodou provedli Baldie et al. [49] a Schiavina et al. [58]. Obě studie jsou nerandomizované a jejich výsledky jsou podobné – RAS má prokazatelně nižší krevní ztráty a dobu hospitalizace. Peri - a postoperační komplikace jsou srovnatelné. Počty restenóz po roboticky asistovaných, laparoskopických i otevřených rekonstrukcí jsou minimální. Současné poznatky ukazují, že roboticky asistované rekonstrukce močovodů jsou možné a doporučované.
ROBOTICKY ASISTOVANÉ RETROPERITONEÁLNÍ LYMFADENEKTOMIE (R-RPLND)
Roboticky asistované retroperitoneální lymfadenektomie (R-RPLND) jsou spojeny s lepším kosmetickým efektem, nižším výskytem komplikací, nižší morbiditou a kratší dobou hospitalizace než otevřené retroperitoneální lymfadenektomie (O-RPLND). Laparoskopické retroperitoneální lymfadenektomie mají velice dlouhou learning curve a horší onkologické výsledky než otevřené lymfadenektomie. První (R-RPLND) byla popsána v roce 2006 [59] a v současné době existuje osm dalších studií. Dvě z nich popisují pouze kazuistiky na méně než třech pacientech. Hranice disekce uzlin jsou stejné jako u otevřených operací. Krevní ztráty jsou většinou do 500 ml krve, doba hospitalizace je většinou 3–4 dny a ve studii s celkem 126 případy byla nutná konverze na otevřený výkon v devíti případech. R-RPLND má popsáno méně komplikací typu pooperační ileus, respirační komplikace a záněty v ráně.
ROBOTIKA V CHIRURGII
Pro chirurgii je v ČR limitací úhrada pouze jednoho výkonu, a to nízké resekce rekta. Z toho vyplývá i nižší využití robotických systémů chirurgem. Je to vidět na celkových číslech provedených operací pro karcinom rekta, i když zveřejňovaná data potvrzují vetší pravděpodobnost provedení kontinentní operace při užití systému daVinci Xi,a to zejména u obézních pacientů, u nízko uložených tumorů a taktéž lepší funkční výsledky z hlediska sexuálních a urologických funkcí. Předpokládáme-li cca 1500 operací pro karcinom rekta ročně, je roboticky provedeno pouze cca 25 %, nicméně i to je stále lepší než celkové číslo miniinvazivně provedené kolorektální chirurgie, které se odhadem prohybuje kolem 20 %. Vedle již výše zmíněných obecných výhod robotické chirurgie je dalším přínosem robotický stapler na střevo. Tento stapler, který chirurg přímo ovládá z operační konzole, je jedním z největších vylepšení i díky přesně definované kompresi tkáně. Robotický stapler pro systém Xi zlepšuje manipulaci v malé pánvi, snižuje počet použitých náplní (cartridge), a tím snižuje riziko anastomotického leaku. Část jeho práce je automatická – sám si měří kompresi tkání střeva, a pokud není dostatečná, neprovede transsekci.
ROBOTIKA V GYNEKOLOGII
Ve světě jsou roboticky operována i benigní onemocnění (myomatózní dělohy, endometrióza), proto kolem roku 2010 ve světě počet robotických výkonů v gynekologii převýšil počty urologických výkonů. U maligních onemocnění dělohy je jasný trend poklesu otevřených operací a vzestup robotických výkonů. V ČR je situace odlišná, zdravotní pojišťovny hradí pouze robotickou operaci pro radikální operace s lymfadenektomií pro diagnózu karcinom děložního hrdla a karcinom endometria. V retrospektivní studii srovnávající robotickou a otevřenou radikální hysterektomii u časných stadií karcinomu děložního čípku vyplynulo, že u robotických výkonů je menší krevní ztráta, o něco delší operační čas, menší množství komplikací a rychlejší rekonvalescence se zkrácením délky hospitalizace, což je ekonomicky výhodné. Rekurence malignity a přežití jsou srovnatelné. [70]. Minimálně invazivní přístup umožňuje také laparoskopie, výkon je obtížnější a méně přehledný, zejména u pacientek s vyšším BMI (body mass index). Pro karcinom endometria je obezita významným rizikovým faktorem a hmotnost pacientek většinou převyšuje 100 kg. Při radikálních operacích otevřenou cestou je nutné provedení dolní a horní střední laparotomie s vysokým rizikem sekundárního hojení a s rizikem hernie v místě laparotomie. Robotický systém umožňuje, díky firefly fluorescence imaging po aplikaci ICG (indocyaninová zeleň), dokonalou detekci sentinelové uzliny. Peroperační vyšetření sentinelové uzliny v indikovaných případech snižuje radikalitu výkonu a tím i riziko následných komplikací, například lymfedému, ke kterému často dochází po systematických lymfadenektomiích.
ROBOTIKA V ORL
Ve srovnání s klasickými chirurgickými postupy v ORL umožňuje roboticky asistovaná chirurgie pomocí zmenšených nástrojů operovat v obtížně dostupných místech dutiny ústní a dolní části hltanu, zvláště pak vchodu do hrtanu a do jícnu. Použití precizních robotických nástrojů o velikosti 5–8 mm, vč. laserového nástroje, umožňuje dosáhnout nedostupných anatomických lokalit tam, kde je možný jen standardní zevní chirurgický přístup. Bez použití robota je lékař v oblasti orofaryngu schopen operovat s klasickými nástroji pouze do určité vzdálenosti. Transorální robotický přístup TORS (trans oral robotic surgery) tuto vzdálenost prodlužuje díky miniaturizaci a ohebnosti robotických nástrojů, zavedených skrze dutinu ústní až do oblasti kořene jazyka, hypofaryngu a supraglottis, kam nelze „rukou“ dosáhnout [60, 61]. Takto je možné cestou dutiny ústní operovat onemocnění bez použití klasických zevních chirurgických přístupů, jakými jsou laterální faryngotomie anebo supraglotická horizontální laryngektomie. Roboticky asistovaná chirurgie v otorinolaryngologii je prováděna především v oblasti kořene jazyka, hypofaryngu a supraglottis a v rozšířené v indikaci mimo dutinu ústní také v oblasti štítné žlázy – transaxilární thyreoidektomie. Nověji jsou robotické výkony zaváděny do chirurgie spodiny lebeční. Transorální robotická chirurgie umožňuje provádět výkony v případech, kdy je klasický endoskopický výkon či zevní chirurgický přístup limitován. Hlavní indikací TORS je léčba dlaždicobuněčných karcinomů tonzily, kořene jazyka, supraglottis a hypofaryngu [62]. Pro robotický přístup jsou vhodné především povrchově uložené, ohraničené primární nádory ve stadiu T1 až T2 [63]. Podle doporučených onkologických schémat se v jedné době se zákrokem TORS provádí ošetření krčních uzlin blokovou krční disekcí [64–66]. Rozsah výkonu na krčních lymfatických uzlinách se neliší od rozsahu voleného při endoskopických nebo zevních onkochirurgických výkonech. Další indikační skupinou vhodnou pro TORS jsou pacienti s těžkým syndromem obstrukční spánkové apnoe (OSAS). Technika umožňuje provádět funkční resekci kořene jazyka u pacientů, kteří jsou inkompatibilní s přístrojem CPAP. Všeobecně vykazují TORS zákroky velmi malé peroperační ztráty krve, dobrou hojivost a rychlý návrat sliznice do původního stavu. Na komfort pacienta v pooperačním období má vliv zejména rychlejší obnovení polykacích funkcí a také lepší snášenlivost bolesti po transorálně provedených operacích [67–69]. To vše se podílí na rychlejší rekonvalescenci pacienta, která umožňuje kratší dobu hospitalizace a rychlejší zotavení.
ZÁVĚR
Roboticky asistovaná chirurgie si našla pevné místo v řadě chirurgických oborů a v nejbližších letech lze očekávat nárůst robotických výkonů.
Seznam použitých zkratek
BHP – benigní hyperplazie prostaty
BMI – body mass index
ČR – Česká republika
ICG – indocyaninová zeleň
ICUD – intracorporeal urinary diversion, intrakorporální derivace moče
IS – Intuitive Surgical
KOC – komplexní onkologické centrum
LPN – laparoscopic partial nephrectomy, laparoskopické resekce tumoru ledvin
MIS – minimálně invazivní chirurgie
O-RPLND – open retroperitoneal lymph node dissection, otevřené retroperitoneální lymfadenektomie
OSAS – syndrom obstrukční spánkové apnoe
R-RPLND – robot-assisted retroperitoneal lymph node dissection, roboticky asistované retroperitoneální lymfadenektomie
RALP – robot-assisted laparoscopic prostatectomy, roboticky asistovaná radikální prostatektomie
RAPN – robot-assisted approach for partial nephrectomy, roboticky asistovaná resekce tumorů ledvin
RARC – robot-assisted radical cystectomy, roboticky asistovaná radikální cystektomie
RAS – robot-assisted surgery, roboticky asistovaná chirurgie
RNL – robot-assisted nephrolithotomy, roboticky asitovaná nefrolitotomie
RPL – robot-assisted pyelothotomy, roboticky asistovaná pyelotomie
sRALP – salvage RALP, salvege roboticky asitovaná prostatektomie
sRRP – salvage radikální prostatektomie
TORS – trans oral robotic surgery
TURP – transuretrální resekce prostaty
TVPE – otevřená transvezikální prostatektomie
Práce je původní, nebyla publikována ani není zaslána k recenznímu řízení do jiného média.
Autoři prohlašují, že nemají střet zájmů v souvislosti s tématem práce.
Všichni autoři rukopis četli, souhlasí s jeho zněním a zasláním do redakce časopisu Anesteziologie a intenzivní medicína.
Podíl autorů na vytvoření článku:
SJ, KV: aktuální stav v ČR, robotické systémy a nástroje, závěr.
BM: robotika v urologii.
RJ: robotika v chirurgii.
BI, VM: robotika v gynekologii.
SK: robotika v ORL.
Do redakce došlo dne 13. 11. 2019.
Do tisku přijato dne 9. 12. 2019.
MUDr. Marek Broul, Ph.D., FECSM
Sources
1. Jiménez-Rodríguez RM. Learning curve in robotic rectal cancer surgery: current state of affairs. Int J Colorectal Dis. 2016;3 : 1807–1815.
2. Panteleimonitis S, Ahmed J, Ramachandra M, Farooq M, et al. Urogenital function in robotic vs laparoscopic rectal cancer surgery: a comparative study. Int J Colorectal Dis. 2017;32 : 241–248.
3. Lowrance WT, Eastham JA, Savage C, et al. Contemporary open and robotic radical prostatectomy practice patterns among urologists in the United States. J Urol. 2012;187 : 2087–2092.
4. Menon M, Shrivastava A, Tewari A, et al. Laparoscopic and robot assisted radical prostatec - tomy: establishment of a structured program and preliminary analysis of outcomes. J Urol. 2002;168 : 945–649.
5. Yaxley JW, Coughlin GD, Chambers SK, et al. Robot-assisted laparoscopic prostatectomy versus open radical retropubic prostatectomy: early outcomes from a randomised controlled phase 3 study. Lancet. 2016;388 : 1057–1066.
6. Tang K, Jiang K, Chen H, et al. Robotic vs. retropubic radical prostatectomy in prostate cancer: a system - atic review and an meta-analysis update. Oncotarget. 2017;8 : 32237–32257.
7. Ramsay C, Pickard R, Robertson C, et al. Systematic review and economic modelling of the relative clinical benefit and cost-effectiveness of laparo - scopic surgery and robotic surgery for removal of the prostate in men with localised prostate cancer. Health Technol Assess. 2012;16 : 1–313.
8. Ghani KR, Sukumar S, Sammon JD, et al. Practice patterns and outcomes of open and minimally invasive partial nephrectomy since the introduction of robotic partial nephrectomy: results from the Nationwide inpatient sample. J Urol. 2014;191 : 907–912.
9. Aboumarzouk OM, Stein RJ, Eyraud R, et al. Robotic versus laparoscopic partial nephrectomy: a systematic review and meta-analysis. Eur Urol. 2012;62 : 1023–1033.
10. Eyraud R, Long JA, Snow-Lisy D, et al. Robot-assisted partial nephrectomy for hilar tumors: perioperative outcomes. Urology. 2013;81 : 1246–1252.
11. Shuch B, Singer EA, Bratslavsky G. The surgical approach to multifocal renal cancers: hereditary syndromes, ipsilateral mul - tifocality, and bilateral tumors. Urol Clin North Am. 2012;39 : 133–148.
12. Autorino R, Eden C, El-Ghoneimi A, et al. Robot-assisted and laparoscopic repair of ureteropelvic junction obstruction: a systematic review and meta-analysis. Eur Urol. 2014;65 : 430–52.
13. Moher D, Liberati A, Tetzlaff J, Altman DG, The PRISMA Group. Preferred Reporting Items for Systematic Reviews and Meta-Analyses: the PRISMA statement. PLoS Med. 2009;6:e1000097.
14. Menon M, Hemal AK, Tewari A, et al. Nerve-sparing robot-assisted radical cysto - prostatectomy and urinary diversion. BJU Int. 2003;92 : 232–236.
15. Menon M, Hemal AK, Tewari A, et al. Nerve-sparing robot-assisted radical cysto - prostatectomy and urinary diversion. BJU Int. 2003;92 : 232–236.
16. Ahmed K, Khan SA, Hayn MH, et al. Analysis of intracorporeal compared with extracorporeal urinary diversion after robot-assisted radical cystectomy: results from the International Robotic Cystectomy Consortium. Eur Urol. 2014;65 : 340–347.
17. Gravas S, Bach T, Drake M, et al. EAU Guidelines Managment of Non-neurogenic Male Lower Urinary Tract Symptoms (LUTS), incl. Benign Prostatic Obstruction (BPO). European Association of Urology, 2017. Available at: https://uroweb.org/wp-content/uploads/13-Non - Neurogenic-Male-LUTS_2017_web.pdf. Accessed June 2018.
18. Humphreys MR, Miller NL, Handa SE, Terry C. Holium laser enucleation of the prostate – outcomes independent of prostate size? J Urol. 2008;180 : 2431–2435.
19. Asimakopoulos AD, Mugnier C, Hoepffner JL, et al. The surgical treatment of a large prostatic adenoma: the laparoscopic approach – a systematic review. J Endourol. 2012;26 : 960–967.
20. Sotelo R, Clavijo R, Carmona O, et al. Robotic simple prostatectomy. J Urol. 2008;179 : 513–515.
21. Yuh B, Laungani R, Perlmutter A, et al. Robot-assisted Millin‘s retropubic prostatectomy: case series. Can J Urol. 2008;15 : 4101–4105.
22. John H, Bucher C, Engel N, et al. Preperitoneal robotic prostate adenomectomy. Urology. 2009;73 : 811–815.
23. Uffort EE, Jensen JC. Robotic-assisted laparoscopic simple prostatectomy: an alternative minimal invasive approach for prostate adenoma. J Robot Surg. 2010;4 : 7–10.
24. Matei DV, Spinelli MG, Nordio A, et al. Robotic simple prostatectomy. Eur Urol Suppl. 2008;9 : 337.
25. Sutherland DE, Perez DS, Weeks DC. Robot-assisted simple prostatectomy for severe benign prostatic hyperplasia. J Endourol. 2011;25 : 641–644.
26. Vora A, Mittal S, Hwang J, Bandi G. Robot-assisted simple prostatectomy: multi-institutional outcomes for glands larger than 100 grams. J Endourol. 2012;26 : 499–502.
27. Matei DV, Brescia A, Mazzoleni F, et al. Robot-assisted simple prostatectomy (RASP): does it make sense? BJU Int. 2012;110 : 972–979.
28. Coelho RF, Chauhan S, Sivaraman A, et al. Modified technique of robotic-assisted simple prostatectomy: advantages of a vesico - urethral anastomosis. BJU Int. 2012;109 : 426–433.
29. Clavijo R, Carmona O, Palmer KJ, et al. Robot-assisted simple prostatectomy: novel technique. J Endourol. 2013;27 : 328–332.
30. Banapour P, Patel N, Kane CJ, et al. Robotic-assisted simple prostatectomy: a systematic review and report of a single institution case series. Prostate Cancer Prostatic Dis. 2014;17 : 1–5.
31. Leslie S, de Castro Abreu AL, Chopra S, et al. Transvesical robotic simple prostatectomy: initial clinical experience. Eur Urol. 2014;66 : 321–329.
32. Pokorny M, Novara G, Geurts N, et al. Robot-assisted simple prostatectomy for treatment of lower urinary tract symptoms secondary to benign prostatic enlargement: surgical technique and outcomes in a high-volume robotic centre. Eur Urol. 2015;68 : 451–457.
33. Autorino R, Zargar H, Mariano MB, et al. Perioperative outcomes of robotic and laparoscopic simple prostatectomy: a European-American multi - institutional analysis. Eur Urol. 2015;68 : 86–94.
34. Patel ND, Parsons JK. Robotic-assisted simple prostatectomy: is there evidence to go beyond the experimental stage? Curr Urol Rep. 2014;15 : 443.
35. Martín Garzón OD, Azhar RA, Brunacci L, et al. One-year outcome comparison of laparoscopic, robotic, and robotic intrafascial simple prostatectomy for benign prostatic hyperplasia. J Endourol. 2016;30 : 312–318.
36. Umari P, Fossati N, Gandaglia G, et al. Robotic assisted simple prostatectomy (RASP) versus holmium laser enucleation of the prostate (HoLEP) for lower urinary tract symptoms in patients with large volume prostates (>100ml): a comparative analysis from a high volume center. J Urol. 2017;197 : 1108–1114.
37. Stolzenburg JU, Kallidonis P, Qazi H, et al. Extraperitoneal approach for robotic - assisted simple prostatectomy. Urology. 2014;84 : 1099–10105.
38. Sorokin I, Sundaram V, Singla N, et al. Robot-assisted versus open simple prosta - tectomy for benign prostatic hyperplasia in large glands: a propensity score-matched comparison of perioperative and short-term outcomes. J Endourol. 2017;31 : 1164–1169.
39. Chade DC, Eastham J, Graefen M, et al. Cancer control and functional outcomes of salvage radical prostatectomy for radiation-recurrent prostate cancer: a systematic review of the literature. Eur Urol. 2012;61 : 961–971.
40. Jamal K, Challacombe B, Elhage O, et al. Successful salvage robotic-assisted radical prosta - tectomy after external beam radiotherapy failure. Urology. 2008;72 : 1356–1358.
41. Dogra PN, Regmi SK, Singh P, et al. Lower ureteral stones revisited: expanding the horizons of robot. Urology. 2013;82 : 95–99.
42. Williams SK, Leveillee RJ. Expanding the horizons: robot - assisted reconstructive surgery of the distal ureter. J Endourol. 2009;23 : 457–461.
43. Schimpf MO, Wagner JR. Robot-assisted laparoscopic distal ureteral surgery. J Soc Laparoscop Soc. 2009;13 : 44–49.
44. Glinianski M, Guru KA, Zimmerman G, et al. Robot-assisted ureterectomy and ureteral reconstruction for urothelial carcinoma. J Endourol. 2009;23 : 97–100.
45. Hemal AK, Nayyar R, Gupta NP, Dorairajan LN. Experience with robot assisted laparoscopic surgery for upper and lower benign and malignant ureteral pathologies. Urology. 2010;76 : 1387–1393.
46. Patil NN, Mottrie A, Sundaram B, Patel VR. Robotic-assisted laparoscopic ureteral reimplantation with psoas hitch: a multi-institutional, multinational evaluation. Urology. 2008;72 : 47–50.
47. McClain PD, Mufarrij PW, Hemal AK. Robot-assisted recon - structive surgery for ureteral malignancy: analysis of efficacy and oncologic outcomes. J Endourol. 2012;26 : 1614–1617.
48. Kozinn SI, Canes D, Sorcini A, Moinzadeh A. Robotic versus open distal ureteral reconstruction and reimplantation for benign stricture disease. J Endourol. 2012;26 : 147–151.
49. Baldie K, Angell J, Ogan K, et al. Robotic management of benign mid and distal ureteral strictures and comparison with laparoscopic approaches at a single institution. Urology. 2012;80 : 596–601.
50. Isac W, Kaouk J, Altunrende F, et al. Robot-assisted ureteroneocystostomy: technique and comparative outcomes. J Endourol. 2013;27 : 318–323.
51. Musch M, Hohenhorst L, Pailliart A, et al. Robot-assisted reconstructive surgery of the distal ureter: single institution experience in 16 patients. BJU Int. 2013;111 : 773–783.
52. Gellhaus PT, Bhandari A, Monn MF, et al. Robotic management of genitourinary injuries from obstetric and gynaecological operations: a multi - institutional report of outcomes. BJU Int. 2015;115 : 430–436.
53. Fifer GL, Raynor MC, Selph P, et al. Robotic ureteral reconstruction distal to the ureteropelvic junction: a large single institution clinical series with short-term follow up. J Endourol. 2014;28 : 1424–1428.
54. Slater RC, Farber NJ, Riley JM, et al. Contempo - rary series of robotic-assisted distal ureteral reconstruction utilizing side docking position. Int Braz J Urol. 2015;41 : 1154–1159.
55. Wason SE, Lance RS, Given RW, Malcolm JB. Robotic-assisted ureteral re-implantation: a case series. J Laparoendosc Adv Surg Tech A. 2015;25 : 503–507.
56. Stolzenburg JU, Rai BP, Do M, et al. Robot-assisted technique for Boari flap ureteric reimplantation: replicating the techniques of open surgery in robotics. BJU Int. 2016;118 : 482–484.
57. Franklin A, Pokala N, Jones C, et al. Is the robotic approach feasible for repair of iatrogenic injuries of the lower ureter? World J Urol. 2016;34 : 1323–1328.
58. Schiavina R, Zaramella S, Chessa F, et al. Laparoscopic and robotic ureteral stenosis repair: a multi-institutional experience with a long-term follow - up. J Robot Surg. 2016;10 : 323–330.
59. Davol P, Sumfest J, Rukstalis D. Robotic-assisted laparoscopic retroperitoneal lymph node dissection. Urology 2006;67(199):e7–e8.
60. Eichel L, Mc Dougall EM, Clayman RV. Fundamentals of laparoscopic and robotic urologic surgery. 10th ed. Philadelphia, PA: Elsevier Saunders, 2011;9.
61. O´Malley BW, Weinstein GS. Transoral Robotic Surgery daVinci Procedure Guide. PN 871671 Rev. 2008;3–17.
62. Aubry K, Yachine M, Perez AF, et al. Transoral robotic surgery for head and neck cancer: a series of 17 cases. Eur Ann Otorhinolaryngol Head Neck Dis. 2011;128 : 290–296.
63. Sobin LH, Gospodarowicz M, Wittekind C. TNM classification of malignant tumours. Hoboken. 2009;22–62.
64. Bradford CR. Selective neck dissection is an option for early node-positive disease. Arch Otolaryngol Head Neck Surg. 2004;42(8):837–841.
65. Pathak KA, Das AK, Agarwal R, et al. Selective neck dissection (I-III) for node negative and positive necks. Oral Oncol. 2006;42 : 837–841.
66. Weistein GS, O’Malley BW Jr, Magnuson JS, et al. Transoral robotic surgery: a multicenter study to assess feasibility, safety, and surgical margins. Laryngoscope. 2012;122 : 1701–1707.
67. Mercante G, Ruscito P, Pellini R, et al. Transoral robotic surgery(TORS) for tongue base tumours. Acta Otorhinolaryngol Ital. 2013;33 : 230–235.
68. Park YM, Kim WS, Byeom HK, et al. Surgical techniques and treatment outcomes of transoral robotic supraglottic partial laryngectomy. Laryngoscope. 2013;123 : 670–677.
69. Moore EJ, Olsen SM, Laborde RR, et al. Long-term functional and oncologic results of transoral robotic surgery for oropharyngeal squamous cell carcioma. Mayo Clin Proc. 2012;87 : 219–225.
Labels
Anaesthesiology, Resuscitation and Inten Intensive Care Medicine
Article was published inAnaesthesiology and Intensive Care Medicine

2019 Issue 6-
All articles in this issue
- Kam směřuje náš časopis?
- Rok v přehledu
- Anesteziologie a intenzivní péče v gynekologii a porodnictví
- Nejvýznamnější publikace v oblasti anesteziologie za rok 2019
- Neuroanestezie a neurointenzivní péče
- Důležité publikace v intenzivní medicíně v roce 2018/2019
- Infekční rizika pro anesteziology
- Etika a paliativní péče v intenzivní péči v roce 2019
- Perioperační neurokognitivní poruchy
- Roboticky asistovaná chirurgie v ČR – aktuální pohled
- Perioperační akutní selhávání funkcí ledvin (AKI)
- Rok 2019 v přehledu – urgentní medicína
- Centrální žilní přístupy – novinky 2020
- Poškození lymfocytární DNA během anestezie: pilotní studie srovnávající celkovou a subarachnoideální anestezii
- Akutní poranění laryngu po prodloužené umělé plicní ventilaci
- Doporučení pro intubaci při vědomí u dospělých pacientů
- Zemřela MUDr. Darina Nábělková (3. 2. 1923 – 10. 11. 2019)
- Anaesthesiology and Intensive Care Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Anesteziologie a intenzivní péče v gynekologii a porodnictví
- Etika a paliativní péče v intenzivní péči v roce 2019
- Neuroanestezie a neurointenzivní péče
- Roboticky asistovaná chirurgie v ČR – aktuální pohled
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

