-
Medical journals
- Career
Vliv videolaryngoskopie na hloubku zavedení tracheální rourky a četnost endobronchiální intubace – prospektivní randomizovaná studie
Authors: V. Dostálová 1; J. Schreiberová 1; L. Kukrálová 1; M. Bartoš 2; P. Dostál 1
Authors‘ workplace: Klinika anesteziologie, resuscitace a intenzivní medicíny, Fakultní nemocnice Hradec Králové, Lékařská fakulta v Hradci Králové, Univerzita Karlova 1; Neurochirurgická klinika, Fakultní nemocnice Hradec Králové, Lékařská fakulta v Hradci Králové, Univerzita Karlova 2
Published in: Anest. intenziv. Med., 30, 2019, č. 3-4, s. 130-136
Category:
Overview
Cíl studie: Obtíže v průběhu přímé laryngoskopie nebo suboptimální vizualizace struktur hrtanu mohou být spojeny s nesprávným umístěním tracheální rourky nebo lokálním poraněním dýchacích cest. Cílem této studie bylo porovnat iniciální hloubku zavedení tracheální rourky, četnost nechtěné endobronchiální intubace a výskyt pooperačního diskomfortu po tracheální intubaci pomocí videolaryngoskopu (GlideScope Titanium) nebo Macintoshova laryngoskopu.
Typ studie: Prospektivní randomizovaná otevřená studie.
Typ pracoviště: Operační sály fakultní nemocnice.
Materiál a metoda: Devadesát dospělých pacientů ASA I–III podstupujících elektivní neurochirurgické výkony bylo randomizováno do skupin konvenční přímé laryngoskopie (skupina C) a videolaryngoskopie (skupina V). Vylučovací kritéria zahrnovala operace krční páteře, plánovanou pooperační ventilaci a anamnézu předchozích výkonů na hrtanu, průdušnici a krční páteři. Byly zaznamenávány: intubační čas, iniciální hloubka zavedení rourky, korekce polohy rourky pro známky endobronchiální intubace a známky pooperačního diskomfortu. Výsledky jsou vyjádřeny jako průměr ± směrodatná odchylka, medián (IQR) nebo jako procenta.
Výsledky: Ve skupině C byla zjištěna vyšší iniciální hloubka zavedení tracheální rourky (22 [21; 23] vs. 21 [20; 22] cm, P = 0,010) a vyšší výskyt známek endobronchiální intubace (15,6 % versus 0,0 %, P = 0,012) ve srovnání se skupinou V. Mezi skupinami C a V nebyly pozorovány rozdíly ve výskytu pooperační bolesti krku (20,0 %, versus 17,8 %, P = 1,000) ani chrapotu (31,1 % versus 24,4 %, P = 0,488). Skupiny se nelišily výškou (172,7 ± 10,3 versus 173,5 ± 8,7 cm, P = 0,692) ani zastoupením žen ve skupině (24/45 versus 19/45, P = 0,165).
Závěr: Použití videolaryngoskopie bylo spojeno s menší iniciální hloubkou zavedení tracheální rourky a nižším výskytem nechtěné endobronchiální intubace.
Klíčová slova:
videolaryngoskopie – přímá laryngoskopie – endobronchiální intubace
ÚVOD
Zajištění dýchacích cest tracheální rourkou je rutinní metodou zajištění dýchacích cest v průběhu celkové anestezie. Pro úspěšnou a nekomplikovanou tracheální intubaci je klíčovým krokem úspěšná vizualizace hrtanu, laryngoskopie [1].
U řady nemocných, včetně nemocných bez známek možné obtížné intubace, může být vizualizace hrtanu při direktní laryngoskopii pomocí Macintoshova laryngoskopu nekompletní a při laryngoskopii může dojít k poranění chrupu nebo měkkých tkání v dutině ústní a hrtanu [1, 2].
Videolaryngoskopie je zavedenou alternativní metodou vizualizace hrtanu, která může jak zlepšit vizualizaci hlasových vazů, tak snížit četnost neúspěšné tracheální intubace, zejména u pacientů s obtížným zajištěním dýchacích cest [3]. Dosud ale neexistují jednoznačné důkazy, že videolaryngoskopie snižuje množství intubačních pokusů, četnost hypoxie či respiračních komplikací, ani že zkracuje celkový čas tracheální intubace [3, 4]. Mezi videolaryngoskopy existují značné rozdíly, přehled komerčně dostupných typů s diskusí jejich předností a nevýhod byl nedávno publikován v tuzemském písemnictví [4]. Jedním z rozšířených typů videolaryngoskopu je GlideScope Video Laryngoscope, patřící mezi videolaryngoskopy se speciálně zakřivenou rigidní lžící bez pracovního kanálu, který existuje v několika vývojových variantách s jednorázovými lžícemi nebo ve verzi se speciální nízkoprofilovou lžící GlideScope Titanium [4, 5]. Použití videolaryngoskopů Glidescope bylo široce zkoumáno u různých populací pacientů jak na operačních sálech, tak i mimo ně [4–9]. Použití videolaryngoskopu GlideScope vyžaduje specifický postup odlišný od postupu při klasické direktní laryngoskopii Macintoshovým laryngoskopem a je spojeno obvykle s lepší vizualizací hrtanu ve srovnání s konvenční direktní laryngoskopií [5].
Nedostatečná vizualizace vchodu do hrtanu a případné obtíže při laryngoskopii a/nebo zavádění tracheální rourky mohou být spojeny s traumatizací vchodu do hrtanu, hlasových vazů, poškození sliznice průdušnice nebo s nesprávným umístěním tracheální rourky s nutností následných korekcí její polohy. Stížnosti pacientů na pointubační bolesti v krku, chrapot a obtíže při polykání jsou poměrně časté [1, 2, 7]. Lze předpokládat, že dosažení lepší vizualizace hrtanu, umožňující za kontroly zraku přesné umístění tracheální rourky, může snížit četnost nechtěné nadměrné hloubky tracheální intubace, počet manipulací s tracheální rourkou a výskyt některých známek poextubačního diskomfortu.
Primárním cílem této studie bylo porovnat iniciální hloubku zavedení tracheální rourky při laryngoskopii prováděné videolaryngoskopem a tradičním Macintoshovým laryngoskopem. Sekundární cíle zahrnovaly četnost výskytu známek nechtěné endobronchiální intubace a výskyt známek pooperačního diskomfortu po tracheální intubaci.
SOUBOR A METODA
Protokol této monocentrické prospektivní randomizované otevřené studie, provedené na Klinice anesteziologie, resuscitace a intenzivní medicíny Univerzity Karlovy, Lékařské fakulty v Hradci Králové a Fakultní nemocnice Hradec Králové, byl schválen Etickou komisí Fakultní nemocnice Hradec Králové (předseda MUDr. Jiří Vortel) pod jednacím číslem 201707 S06P dne 8. 6. 2017. Studie byla registrována na ClinicalTrials.gov pod identifikátorem NCT03184246.
Do studie byli zařazováni nemocní podstupující elektivní neurochirurgický výkon. Od všech nemocných byl získán informovaný souhlas, pacienti byli zařazování od 13. 6. 2017 do 6. 11. 2017.
Vstupní kritéria zahrnovala věk nad 18 let, stanovené riziko podle ASA I–III a absenci kognitivního deficitu. Za vylučovací kritérium byla považována plánovaná pooperační ventilace, tumory hrtanu, stavy po tracheotomii a operacích průdušnice a hrtanu a stavy po operacích krční páteře. Pacienti s anamnézou obtížného zajištění dýchacích cest a nemocní s vysokým rizikem obtížného zajištění dýchacích cest podle předanestetického vyšetření nebyli do studie zařazováni.
Anestezie byla vedena podle striktního protokolu. Úvod do anestezie byl zahájen nitrožilním podáním sufentanilu v dávce 5 ug u pacientů s tělesnou hmotností do 60 kg nebo 10 ug u pacientů s tělesnou hmotností nad 60 kg. Za cca 2 minuty byl titračně nitrožilně podán propofol v dávce 0,8–2 mg/kg do dosažení cílové hodnoty entropie (State Entropy) měřené monitorem anesteziologického přístroje (Aisys, GE Healthcare, Helsinky, Finsko) v rozmezí 40–60 bodů a atracurium v dávce 0,3–0,5 mg/kg.
Při tracheální intubaci bylo doporučeno zavedení tracheální rourky pod zrakovou kontrolou tak, aby těsnící manžeta byla zavedena těsně (cca 0,5 cm) za vazy hlasivek a po nafouknutí manžety (za zrakové kontroly, bylo-li to možné) zůstala za vazy. Pokud vizualizace hrtanu neumožnila zrakovou kontrolu polohy manžety, byla ponechána hloubka zavedení rourky na anesteziologovi. Po zavedení rourky anesteziologem byla odečtena hloubka zavedení v ústním koutku. Po kontrole polohy rourky poslechem byla zaznamenána případně provedena úprava polohy rourky. Intubující anesteziolog byl informován, že cílem studie je zhodnotit výskyt pooperačního diskomfortu.
Intraoperační analgezie byla vedena bolusovým podáváním sufentanilu a individualizována podle hodnot tzv. surgical pleth indexu (SPI), hypnotickou složku zajišťoval desflurane v koncentraci podle cílových hodnot entropie v rozmezí 40–60 bodů a podávaný v nosné směsi kyslíku a vzduchu.
Pacienti byli ventilováni objemově řízenou ventilací s dechovým objemem 6 ml/kg predikované tělesné hmotnosti pacienta, dechovou frekvencí 12–15 dechů/min, hodnotou endexspiračního tlaku (PEEP) 4 cm H2O, hodnota endexspirační koncentrace kyslíku byla automaticky udržována na 40 %. Hodnota endexspirační tenze CO2 (ETCO2) byla udržována v rozmezí 35–45 mmHg.
V průběhu operačního výkonu byl udržován střední arteriální tlak v rozmezí ± 15 % pacientovy předoperační hodnoty. Při poklesu tlaku pod tuto hodnotu bylo zahájeno kontinuální podávání infuze noradrenalinu. Efedrin nebyl používán.
Intraoperační analgezie byla vedena bolusovým podáním sufentanilu (Sufentanil Torrex Chiesi CZ s.r.o.) v dávce 5 nebo 10 ug (podle hmotnosti pacienta obdobně jako při dávce sufentanilu při úvodu) podle hodnoty SPI. Bolusová dávky byla podána po vzestupu nad bazální pointubační hodnotu SPI o více než 10 bodů. Posledních 15 minut anestezie již nebyl sufentanil podáván.
U pacientů ve skupině C byla k vizualizaci hrtanu použita direktní laryngoskopie pomocí Macintoshova laryngoskopu s velikostí laryngoskopické lžíce 3 u žen a 4 u mužů. Ve skupině V byl použit videolaryngoskop GlideScope Titanium se lžící LoPro T 4 pro obě pohlaví.
Tlak v manžetě tracheální rourky byl v průběhu operace kontinuálně monitorován a udržován v rozpětí 25–28 cm H2O.
Sledované ukazatele zahrnovaly předoperační hodnotu Mallampati skóre, intubační čas (definovaný jako čas od přerušení ventilace obličejovou maskou do napojení tracheální rourky na okruh anesteziologického přístroje, případná úprava polohy rourky probíhala následně a není zahrnuta v intubačním času), iniciální hloubku zavedení tracheální rourky, nutnost manipulace s tracheální rourkou pro známky suspektní endobronchiální intubace podle klinického vyšetření poslechem plic a zhodnocením tlaku v dýchacích cestách, počet pokusů o intubaci a poextubační bolest v krku a chrapot první pooperační den, výskyt pooperační nevolnosti a zvracení (tzv. známky poextubačního diskomfortu) a délku hospitalizace.
Hloubka zavedení byla srovnávána s tzv. optimální hloubkou (OH) zavedení tracheální rourky kalkulovanou podle rovnic v závislosti na pohlaví [10]. Pro muže byla optimální hloubka OHM kalkulována podle rovnice:
OHM = 11,413 + (0,072 × výška v cm) – 3,
pro ženy byla pro výpočet optimální hloubky OHŽ použita rovnice:
OHŽ = 13,555 + (0,056 × výška v cm) – 3.
Tzv. power analýza s chybou a 0,05 a chybou b 0,2 byla provedena pro dvojstranný dvojvýběrový t-test pomocí software G*Power verze 3.1.9.2 (Kiel University, Kiel, Německo) s předpokladem rozdílu v průměrné hloubce zavedení tracheální rourky mezi skupinami 0,5 cm a směrodatnou odchylkou 0,8 cm. Tato kalkulace ukázala minimální počet 42 subjektů ve skupině, počet zařazených byl následně zvýšen na 45 nemocných vzhledem k možné nepřesnosti predikcí při provedení analýzy.
Výsledky jsou vyjádřeny jako průměr ± směrodatná odchylka nebo jako medián (mezikvartilové rozpětí) na základě výsledků testu normality distribuce pomocí jednovýběrového Kolmogorova-Smirnovova testu. Kategorická data jsou uváděna jako počet (procento). Rozdíly mezi skupinami byly testovány pomocí dvojvýběrového t-testu, Mannova-Whitneyova U testu nebo Fisherova exaktního testu podle povahy dat. P < 0,05 bylo považováno za statisticky významné. Statistické analýzy byly provedeny na software MedCalc 7.6.0 (Ostende, Belgie).
VÝSLEDKY
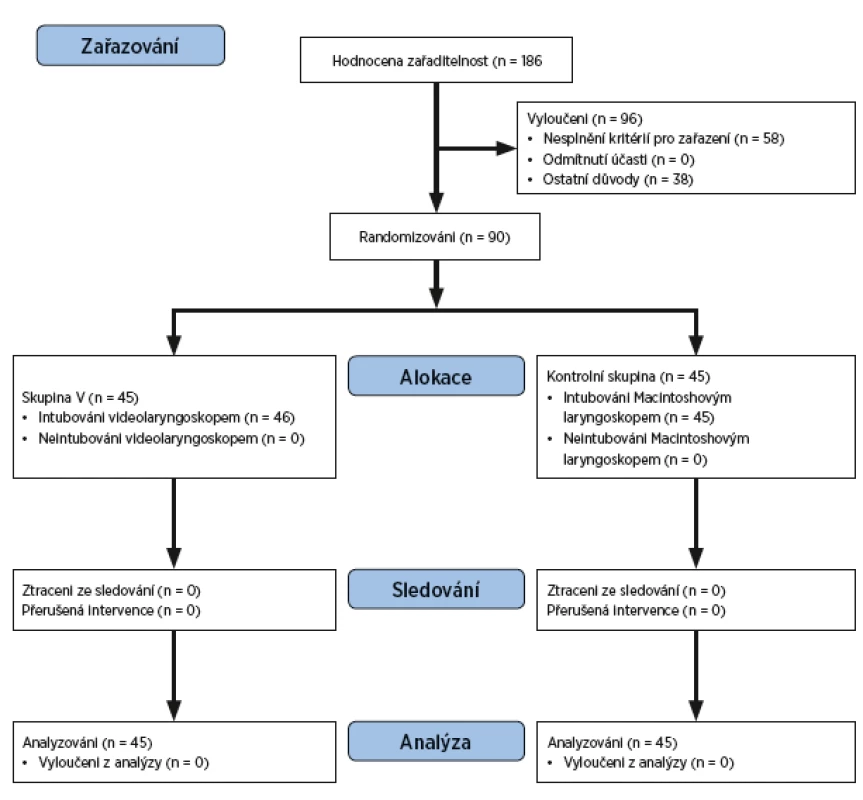
Celkem bylo zvažováno zařazení u 186 nemocných. Po vyloučení nemocných s kontraindikacemi, nemocných zařazených do jiných studií a nemocných nezařazených z logistických důvodů bylo zařazeno 90 nemocných (obr. 1).
Demografická data všech nemocných jsou uvedena v tabulce 1. Předoperační Mallampatiho skóre bylo nižší u nemocných ve skupině C.
Table 1. Charakteristika nemocných 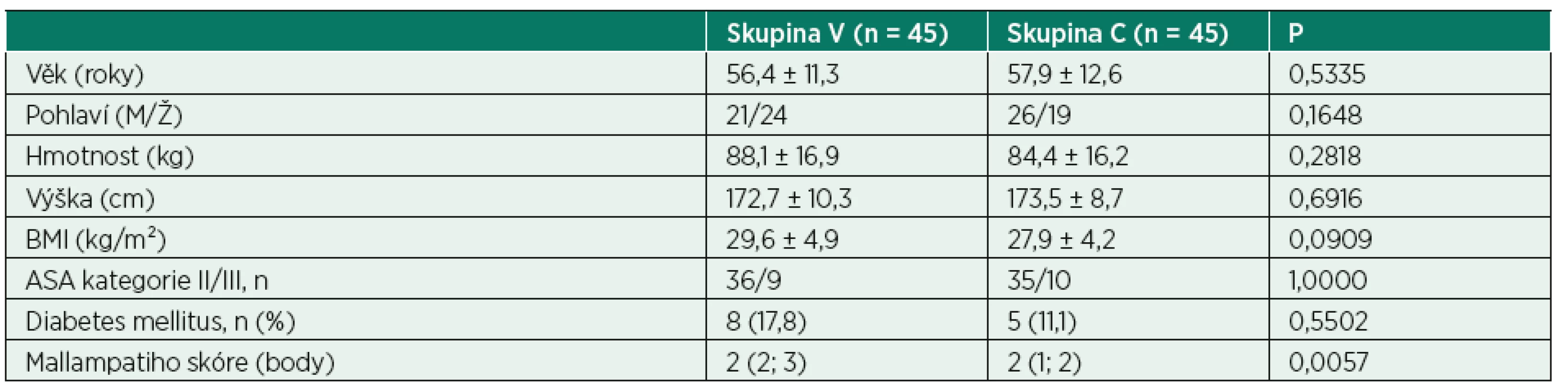
M – muži, Ž – ženy, BMI – body mass index, ASA – American Society of Anesthesiology, n – počet
Spojitá data jsou uváděna jako průměr ± SD nebo jako medián (IQR) na základě výsledků Kolmogorova-Smirnovova testu, kategorická data jsou uváděna jako počet.Ve skupině C byla zjištěna vyšší iniciální hloubka zavedení tracheální rourky, vyšší rozdíl mezi iniciální a kalkulovanou optimální hloubkou zavedení tracheální rourky a vyšší četnost korekcí polohy tracheální rourky pro známky endobronchiální intubace ve srovnání se skupinou V (tab. 2). Výskyt nemocných s Cormack Lehane (CL) skóre větší než 1 bod byl častější ve skupině C (tab. 2). Iniciální hloubka zavedení tracheální rourky u nemocných ve skupině C s CL skóre do 1 bodu a nad 1 bod, 22,0 (21; 23) cm vs. 22 (21; 23) cm, P = 0,9596 ani s hodnotou CL skóre do 2 bodů a nad 2 body, 22,0 (21,0; 23,0) cm vs. 22,0 (21,3; 23,0) cm, P = 0,6662 nebyla rozdílná.
Table 2. Periintubační údaje 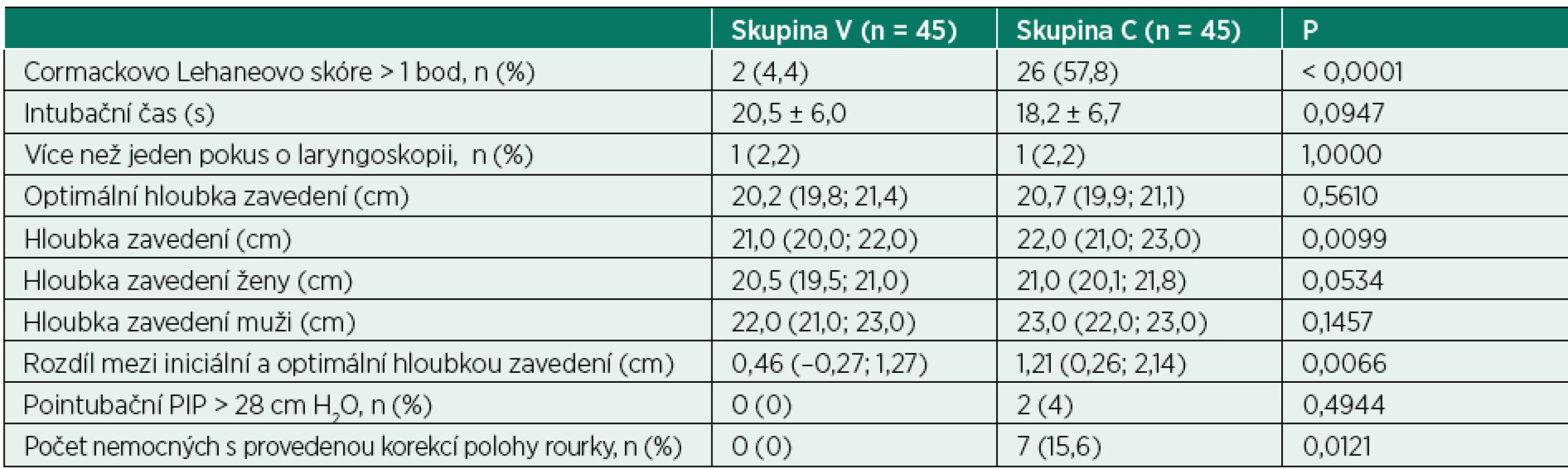
PIP – špičkový inspirační tlak
Spojitá data jsou uváděna jako průměr ± SD nebo jako medián (IQR) na základě výsledků Kolmogorova-Smirnovova testu, kategorická data jsou uváděna jako počet (procento).Mezi skupinami nebyly zjištěny rozdíly v pooperačním výskytu bolestí krku a chrapotu, pooperační nevolnosti nebo zvracení a v délce hospitalizace. Byl pozorován nesignifikantní trend k častějšímu výskytu jakékoliv známky poextubačního diskomfortu ve skupině C (tab. 3).
Table 3. Poextubační průběh 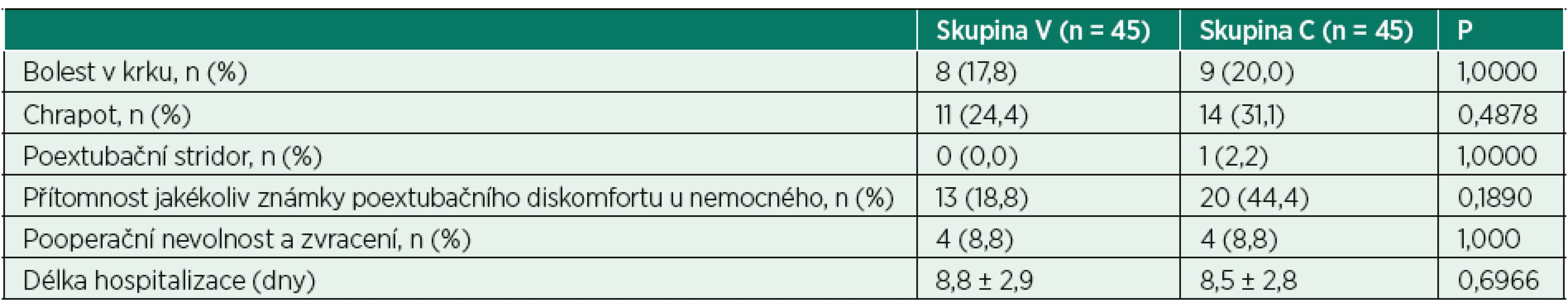
Spojitá data jsou uváděna jako průměr ± SD nebo jako medián (IQR) na základě výsledků Kolmogorova-Smirnovova testu, kategorická data jsou uváděna jako počet (procento). DISKUSE
Hlavním zjištěním této studie je nález větší hloubky iniciálního zavedení tracheální rourky a vyšší četnosti známek endobronchiální intubace vyžadující bezprostřední pointubační korekci polohy tracheální rourky u nemocných intubovaných pomocí Macintoshova laryngoskopu ve srovnání s nemocnými intubovanými pomocí videolaryngoskopu. Výskyt poextubačních bolestí v krku, chrapotu a jakýchkoliv známek diskomfortu nebyl ovlivněn.
Endobronchiální intubace se vyskytuje u 5–28 % intubačních pokusů prováděných pomocí direktní laryngoskopie [11, 12]. Námi pozorovaný výskyt 15,6 % v kontrolní skupině odpovídá těmto údajům, četnost endobronchiální intubace při použití videolaryngoskopu GlideScope Titanium nebyla podle našich znalostí dosud publikována. Vzhledem k potenciálním závažným komplikacím nerozpoznané endobronchiální intubace je prevence této komplikace velmi důležitá [11]. Tradičně je jako prevence a detekce endobronchiální intubace používána kombinace více postupů, obvykle: (a) bilaterální auskultace plic, (b) „pravidlo 21/23“, (c) palpace balónku tracheální rourky v jugulární jamce [13]. Žádný z těchto postupů není zcela spolehlivý. Efektivní auskultace plic je výrazně závislá na dovednostech a zkušenosti a auskultační nález může být zavádějící až ve dvou třetinách případů [14–16]. Tradiční doporučení pro fixaci tracheální rourky na hloubce 21 cm od řezáků pro ženy a 23 cm pro muže [11] bylo nedávno zpochybněno a nyní jsou doporučovány hloubky menší, tj. 20 a 22 cm s tím, že větší hloubky zavedení je třeba používat s extrémní opatrností [17]. Palpace balónku vyžaduje příhodné anatomické poměry a součinnosti dalšího operátora, a přestože recentní data ukazují, že je přesnější než použití fixních pravidel pro hloubku zavedení [18], není na řadě pracovišť standardně používána.
Spolehlivá predikce vzdálenosti mezi hlasovými vazy a karinou je obtížná [11, 19] vzhledem k extrémní variabilitě a vlivem dalších faktorů včetně věku, rasy a pohlaví [19]. Za správnou je u dospělých považována poloha distálního konce tracheální rourky mezi 2,5 až 4 cm nad karinou [17, 18]. Pro kalkulaci optimální hloubky zavedení tracheální rourky byla zvolena studie Gomeze a spolupracovníků [10], která stanovila optimální hloubku zavedení tracheální rourky pomocí měření vzdálenosti od zubů ke karině pomocí fibrobronchoskopického měření a která, na rozdíl od řady jiných kalkulací [19–22] stanovuje hloubku selektivně pro muže a ženy v závislosti na výšce.
Nižší výskyt endobronchiální intubace a nižší hloubka zavedení tracheální rourky ve skupině V byla pravděpodobně umožněna lepší individualizací hloubky zavedení než ve skupině C. Lepší vizualizace hrtanu při použití videolaryngoskopie je považována za hlavní přednost metody [3, 4, 5, 7] a byla pozorována také v této studii. Možnost umístění tracheální rourky pod hlasové vazy za vizuální kontroly proximálního konce manžety tracheální rourky se jeví jako potenciálně efektivní metoda prevence endobronchiální intubace při použití videolaryngoskopu.
Rozdílná hloubka zavedení tracheální rourky by mohla být způsobena odlišným zastoupením mužů a žen ve sledovaných skupinách. Provedená analýza ale ukazuje, že trend k nižší hloubce zavedení tracheální rourky, ačkoliv nesignifikantní, je přítomen bez ohledu na pohlaví.
Použití videolaryngoskopu, přes lepší vizualizaci hrtanu a menší počet manipulací s tracheální rourkou, bylo spojeno pouze s nesignifikantním trendem k nižšímu výskytu chrapotu, bolestí v krku a výskytu jakékoliv známky poextubačního diskomfortu. Tento trend odpovídá výsledkům recentně publikované studie [23], ve které byl zjištěn v souboru 360 nemocných nižší výskyt známek orofaryngeálního poranění (1,1 % versus 5,1 %, P = 0,033) nižší výskyt chrapotu (2,8 % versus 7,9 %, P = 0,035), přestože námi pozorovaná četnost této komplikace byla výrazně vyšší.
Tato studie má také řadu limitací. Vzhledem k povaze studie nebylo možné její zaslepení a zaslepeně byla provedena pouze analýza získaných dat. Detekce endobronchiální intubace byla založena na klinickém zhodnocení příslušného anesteziologa a nebyla použita žádná z metod objektivní validace polohy konce tracheální rourky (fibroskopicky nebo pomocí zobrazovací metody). Použitá metoda umístění balónku tracheální rourky a hodnota peroperačního inflačního tlaku mohla ovlivnit výskyt poextubačního diskomfortu. Počet nemocných zařazených do studie byl relativně nízký a studie neměla dostatečnou sílu ke zjištění rozdílů ve výskytu poextubačních komplikací, jejichž výskyt mohl být také ovlivněn Hawthornským efektem.
ZÁVĚR
V rámci limitací této studie bylo zjištěno, že použití videolaryngoskopu GlideScope Titanium bylo spojeno s nižší iniciální hloubkou zavedení tracheální rourky a nižší četností známek endobronchiální intubace. Výskyt poextubačních bolestí v krku, chrapotu a jakýchkoliv známek diskomfortu nebyl použitím videolaryngoskopu signifikantně ovlivněn.
Práce je původní, nebyla publikována ani není zaslána k recenznímu řízení do jiného média.
Předběžné výsledky byly prezentovány formou posteru na Euroanaesthesia 2019 ve Vídni a jsou přihlášeny jako poster na národní kongres ČSARIM.
Autoři prohlašují, že nemají střet zájmů v souvislosti s tématem studie.
Všichni autoři rukopis četli, souhlasí s jeho zněním a zasláním do redakce časopisu Anesteziologie a intenzivní medicína.
Registrace: studie byla registrována na ClinicalTrials.gov pod identifikátorem NCT03184246.
Podpořeno MZ ČR - RVO (FNHK, 00179906).
Projednání etickou komisí: protokol studie byl schválen Etickou komisí Fakultní nemocnice Hradec Králové (předseda MUDr. Jiří Vortel) pod jednacím číslem 201707 S06P dne 8. 6. 2017.
Podíl autorů na vytvoření článku:
DV: iniciovala vznik studie, podílela se na přípravě protokolu, sběru dat a připravila rukopis studie
SJ, KL a BM: podíleli se na sběru dat a přípravě rukopisu studie.
DP: podílel se na přípravě protokolu studie, provedl statistickou analýzu dat a finalizoval rukopis studie.
Do redakce došlo dne 7. 8. 2019.
Do tisku přijato dne 2. 9. 2019.
Adresa pro korespondenci:
doc. MUDr. Pavel Dostál, Ph.D., MBA
Sources
1. Irefin S, Kopyeva T. Perioperative airway management. In: Sikka P, Beaman S, Street J, eds. Basic Clinical Anesthesia. New York: Springer; 2015 : 23–44.
2. Adnet F, Racine SX, Borron SW, et al. A survey of tracheal intubation difficulty in the operating room: a prospective observational study. Acta Anaesth Scand. 2001;45 : 327–332.
3. Lewis SR, Butler AR, Parker J, et al. Videolaryngoscopy versus direct laryngoscopy for adult patients requiring tracheal intubation. Cochrane Database of Systematic Reviews 2016, Issue 11. Art. No.: CD011136.
4. Brožek T, Michálek P. Role videolaryngoskopie v perioperační medicíně. Anest Intenziv Med. 2018;29 : 96–106.
5. Doyle DJ. The GlideScope video laryngoscope: a narrative review. Open Anesth J. 2017;11 : 48–67.
6. Cooper RM, Pacey JA, Bishop MJ, McCluskey SA. Early clinical experience with a new videolaryngoscope (GlideScope) in 728 patients. Can J Anesth. 2005;52 : 191–198.
7. Cooper RM. Complications associated with the use of the GlideScope® videolaryngoscope. Can J Anesth. 2007;54 : 54–57.
8. Griesdale DEG, Liu D, McKinney J, Choi PT. Glidescope® video-laryngoscopy versus direct laryngoscopy for endotracheal intubation: a systematic review and meta-analysis. J Can Anesth. 2012;59 : 41–52.
9. Tao B, Liu K, Wang D, et al. Comparison of GlideScope video laryngoscopy and direct laryngoscopy for tracheal intubation in neonates. Anesth Analg. 2019;129 : 482–486.
10. Gómez JC, Melo LP, Orozco Y, et al. Estimation of the optimum length of endotracheal tube insertion in adults. Rev Colomb Anestesiol. 2016;44 : 228–234.
11. Owen RL, Cheney FW. Endobronchial intubation: a preventable complication. Anesthesiology. 1987;67 : 255–257.
12. O’Connor CJ, Mansy H, Balk RA, et al. Identification of endotracheal tube malpositions using computerized analysis of breath sounds via electronic stethoscopes. Anesth Analg. 2005;101 : 735–739.
13. Cornelius B, Sakai T. Inadvertent endobronchial intubation in a patient with a short neck length. Anesth Prog. 2015;62 : 66–70.
14. Rudraraju P, Eisen L. Confirmation of endotracheal tube position: a narrative review. J Intensive Care Med. 2009;24 : 283–292.
15. Adriani J, Naraghi M, Ward M. Complications of endotracheal intubation. South Med J. 1988;81 : 739–744.
16. Verghese S, Hannallah R, Slack M, et al. Auscultation of bilateral breath sounds does not rule out endobronchial intubation in children. Anesth Analg. 2004;99 : 56–58.
17. Sitzwohl C, Langheinrich A, Schober A, et al. Endobronchial intubation detected by insertion depth of endotracheal tube, bilateral auscultation, or observation of chest movements: randomised trial. Br Med J. 2010;341:c5943.
18. McKay W, Klonarakis J, Pelivanov V, O’Brien J, Plewes C. Tracheal palpation to assess endotracheal tube depth: an exploratory study. Can J Anaesth. 2014; 61 : 229–234.
19. Pang G, Edwards M, Greenland K. Vocal cord-carina distance in anaesthetised Caucasian adults and its clinical implications for tracheal intubation. Anaesth Intensive Care. 2010; 38 : 1029–1033.
20. Evron S, Weisenberg M, Harow E, et al. Proper insertion depth of endotracheal tubes in adults by topographic landmarks measurements. J Clin Anesth. 2007;19 : 15–19.
21. Goodman LR, Conrardy, Laing F, Singer MM. Radiography evaluation of ETT position. Am J Roentgenol. 1976;127 : 433–434.
22. Schellinger RR. The length of the airway to the bifurcation of the trachea. Anesthesiology. 1964;25 : 169–172.
23. Liu DX, Ye Y, Zhu YH, et al. Intubation of non-difficult airways using video laryngoscope versus direct laryngoscope: a randomized, parallel-group study. BMC Anesthesiol. 2019;19 : 75.
Labels
Anaesthesiology, Resuscitation and Inten Intensive Care Medicine
Article was published inAnaesthesiology and Intensive Care Medicine

2019 Issue 3-4-
All articles in this issue
- Obtížné zajištění dýchacích cest u dospělých a u dětí; nový doporučený postup ČSARIM
- POCT – UZ v diagnostice diafragmatické dysfunkce po torakochirurgických výkonech
- Jak pracovat s Doporučeným postupem ČSARIM pro zajištění obtížných dýchacích cest?
- APACHE a qSOFA ve stratifikaci rizika při sepsi
- Léčba hypotenze po úvodu do celkové anestezie – multicentrická dotazníková studie
- Tako-tsubo syndrom v průběhu spondylochirurgického výkonu
- Vliv videolaryngoskopie na hloubku zavedení tracheální rourky a četnost endobronchiální intubace – prospektivní randomizovaná studie
- ARDS a obézní pacient
- Fasciální prostory na krku pro regionální anestezii
- Deeskalace antibiotické terapie jako součást strategie péče o kriticky nemocné
- TTM – řízená tělesná teplota v současném pojetí
- Základní neuromodulační metody v léčbě chronické bolesti
- Ambulantní kolonoskopie – čas propuštění po výkonu
- Pohled mladých anesteziologů a intenzivistů na specializační vzdělávání v oboru anesteziologie a intenzivní medicína v České republice: dotazníková studie
- Tako-tsubo kardiomyopatie jako perioperační komplikace karotické endarterektomie potvrzená MR zobrazením srdce
- Zajištění obtížných dýchacích cest u dospělých a dětí
- EKG lekce 5
- Farmakologie látek ovlivňujících fluidokoagulační rovnováhu
- Kapilární návrat – klinické vyšetření přítomnosti cirkulační koherence?
- Za primářem MUDr. Vladimírem Kynclem (19. 10. 1930 – 27. 5. 2019)
- Anaesthesiology and Intensive Care Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Kapilární návrat – klinické vyšetření přítomnosti cirkulační koherence?
- Základní neuromodulační metody v léčbě chronické bolesti
- Deeskalace antibiotické terapie jako součást strategie péče o kriticky nemocné
- Zajištění obtížných dýchacích cest u dospělých a dětí
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career