-
Medical journals
- Career
Tako-tsubo syndrom v průběhu spondylochirurgického výkonu
Authors: V. Dostálová 1; T. Hosszú 2; M. Solař 3; P. Dostál 1
Authors‘ workplace: Klinika anesteziologie, resuscitace a intenzivní medicíny, Fakultní nemocnice Hradec Králové, Lékařská fakulta v Hradci Králové, Univerzita Karlova 1; Neurochirurgická klinika, Fakultní nemocnice Hradec Králové, Lékařská fakulta v Hradci Králové, Univerzita Karlova 2; I. interní kardioangiologická klinika, Fakultní nemocnice Hradec Králové, Lékařská fakulta v Hradci Králové, Univerzita Karlova 3
Published in: Anest. intenziv. Med., 30, 2019, č. 3-4, s. 126-129
Category:
Overview
Tako-tsubo kardiomyopatie (syndrom) je akutně vzniklá reverzibilní porucha systolické funkce v oblasti apexu a střední části levé komory s hyperkontraktilitou bazální části komory. Klinický obraz je neodlišitelný od akutní koronární příhody a infarktu myokardu, dochází k elevaci ST úseků a zvýšení hodnot kardiálních enzymů. Postižení je lokalizováno do oblastí bez jasné predilekce ke konkrétní koronární arterii. Koronarografie je negativní. Tako-tsubo kardiomyopatie postihuje zejména postmenopauzální ženy a je vyvolána významným psychologickým stresem. Objevují se ale sporadické kazuistiky popisující vznik tohoto syndromu peroperačně u operací v oblasti hrudní páteře. Tato kazuistika popisuje náhlý vznik ST elevací s výraznou hemodynamickou nestabilitou u 71leté pacientky operované pro hemangiom v oblasti Th6. Pooperační ultrazvuk prokázal poruchu kinetiky spodní a laterální stěny levé komory, koronarografie byla negativní. Ventrikulografie zobrazila typickou hyperkontraktilitu bazální části levé komory a hypokinezi střední a apikální části levé komory s poklesem ejekční frakce levé komory na 36 %. Troponin T dosáhl maximálních hodnot 1. pooperační den (781 ng/l). Za 21 dnů došlo při konzervativní terapii k normalizaci kinetiky levé komory a u pacientky byla dokončena operační stabilizace páteře bez dalších komplikací.
Klíčová slova:
tako-tsubo kardiomypatie – tako-tsubo syndrom – hrudní spondylochirurgický výkon – akutní koronární syndrom
ÚVOD
Stresová kardiomyopatie, původně se preferenčně vyskytující v Asii, byla nazvána v roce 1990 „tako-tsubo“ podle tvaru levé komory na konci systoly na ventrikulogramu, který se podobá japonské nádobě na chytání chobotnic (tako-tsubo) [1] a odpovídá hyperkontraktilní bazální části s minimálně se kontrahující (až balonovitě rozšířenou) střední a apikální částí levé komory. Proto je také nazývaná jako „apical ballooning syndrome“. Pacient má projevy tranzientní dysfunkce levé komory (hypokineze, akineze nebo dyskineze), může být ovlivněna také pravá komora. Tzv. „inverted tako-tsubo“ je stav, kdy je balonovitě rozšířená oblast střední a laterální levé komory, ale apex zasažen není [2]. Poruchy kinetiky většinou neodpovídají vaskulární distribuci a přesahují koronární teritoria.
Tako-tsubo kardiomyopatie byla v nové klasifikaci kardiomyopatií zařazena American Heart Association v roce 2006 do skupiny primárních získaných kardiomyopatií [3]. V současné době je doporučeno používat spíše označení tako-tsubo syndrom (TTS) [4]. Klinické projevy jsou nerozeznatelné od akutního koronárního syndromu (AKS) včetně bolestí na hrudi a elektrokardiografických (EKG) abnormalit. Ze všech případů AKS připadají až 3 % na TTS [4]. TTS nejvíce postihuje postmenopauzální ženy s maximem mezi 67 a 70 lety [4]. V současnosti se zvyšuje výskyt i u mužů po fyzické zátěži, jeho výskyt je popisován i u nedonošených dětí [4]. Příznaky nastupují náhle, jsou často vyvolány psychologickým stresem (strachem, úzkostí), silným spouštěčem je apnoe. TTS je popsán také po podávání chemoterapeutik, 5-fluorouracilu, ergotaminu, při zneužívání kokainu a při vysokých hladinách sympatikomimetik, inotropik a tyreoidních hormonů [5].
POPIS VLASTNÍHO PŘÍPADU
71letá pacientka byla plánována k odstranění agresivně rostoucího hemangiomu obratle Th6 a k laminektomii pro dekompresi míchy v této oblasti. Hlavním příznakem onemocnění byly bolesti zad s propagací do obou dolních končetin, zejména do třísel a stehen. Parézy vyjádřeny nebyly, nebyla diagnostikována myelopatie. Pacientka se léčila pro arteriální hypertenzi, osteoporózu a dyslipidemii, užívala Vigantol, Biomin H, Lozap a Bonvivu. V rámci předanestetického vyšetření byl zjištěn BMI 23,7, krevní tlak 147/99 mmHg a tepová frekvence 111 tepů/min. Před vlastním chirurgickým výkonem byla provedena v lokální anestezii embolizace interkostální tepny Th6 vlevo mikročásticemi, výkon byl bez komplikací. Následující den byl plánován chirurgický výkon, před operací byla pacientka oběhově stabilní, zajištěna čtyřmi periferními žilními katétry, arteriálním katétrem a močovou cévkou. Anestezie byla vedena desfluranem, relaxace intermitentně podávaným atracuriem, analgezie byla vedena pomocí Surgical Pleth Indexu (SPI Aisys GE) bolusovým podáváním sufentanilu. V průběhu anestezie v poloze na břiše byl krevní tlak udržován pomocí noradrenalinu v dávce do 0,15 ug/kg/min k udržení cílového tlaku v rozsahu 70‒75 mmHg středního arteriálního tlaku, průběžná krevní ztráta byla hrazena krví a krevní plasmou, bilance udržována mírně pozitivní v průběhu celého výkonu. Byla provedena laminektomie Th6, byl snesen oblouk a pedikl vlevo, uvolněn kanál páteřní, zleva bylo proniknuto do obratlového těla, kde byl odstraněn hemangiom, po uvolnění levé strany byl snesen oblouk a pedikl vpravo a i zde byla provedena exstirpace tumoru z těla obratle. Natržená dura mater byla ošetřena stehem. V této době (2 hodiny od zahájení operace) dochází náhle na třísvodovém monitoru EKG k elevaci ST úseku až do obrazu Pardeho vlny a následně k poklesu krevního tlaku. Byla zvýšena dávka noradrenalinu na 1 ug/kg/min a pro přetrvávání hypotenze byl podáván kontinuálně adrenalin s rychlou úpravou systémového tlaku k cílové hodnotě. V této fázi po domluvě s operatérem bylo rozhodnuto o ukončení výkonu před provedením stabilizace, pacientka byla po sutuře rány přetočena zpět na záda a bylo natočeno dvanáctisvodové EKG (obr. 1) a odebrána krev na vyšetření krevních plynů, hemoglobinu a mineralogramu k vyloučení některých reverzibilních příčin zhoršení klinického stavu. Následně byla pacientka při vědomí ve stabilizovaném stavu převezena podpůrně ventilovaná na jednotku intenzivní péče a dále do katetrizační laboratoře. Nález na koronarografii a angiografii levé komory a ascendentní aortě byl bez patologického nálezu (obr. 2), ventrikulografie prokázala akineze apikálních segmentů s hyperkontrakcí bazálních segmentů (obr. 3). Nebyla prokázána mitrální insuficience ani aortální vada. Ejekční frakce levé komory byla snížena na 36 %. Po převozu na JIP byla pacientka extubována. V následujících 45 hodinách došlo ke vzestupu hodnot kreatinkinázy (CK) a jejího specifického izoenzymu pro srdeční sval CK-MB (graf 1) a troponinu T (graf 2). ST elevace na EKG se postupně v následujících šesti dnech normalizovala. Kontrolní transtorakální echokardiografie provedená devět dnů od operace prokázala stacionární nález dysfunkce levé komory odpovídající nálezu na pooperační ventrikulografii, kontrolní transtorakální echokardiografie provedená 20. den od operace prokázala zlepšení funkce levé komory s ejekční frakcí levé komory kolem 50 % a přetrvávání mírné hypokineze hrotu a apikálních segmentů přední stěny, septa a laterální stěny levé komory. Čtyřiadvacet dnů od první operace byla pacientce provedena transpedikulární stabilizace páteře v rozsahu Th5‒Th7 bez komplikací a deset dnů od provedení stabilizace byla pacientka přeložena k pooperační rehabilitaci do rehabilitačního ústavu.
Image 1. EKG natočené přímo na operačním sále 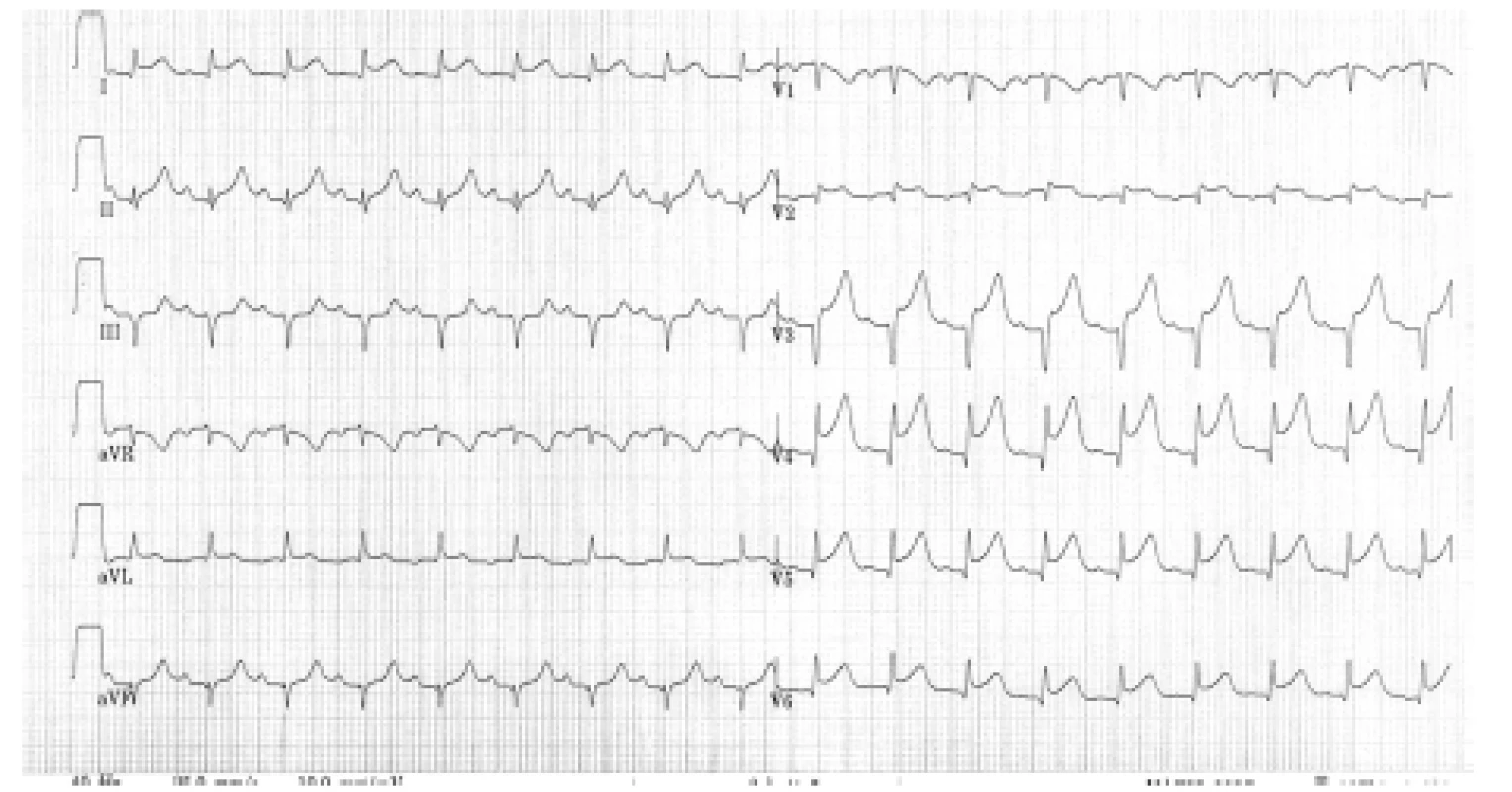
Image 2. Koronarografie jednu hodinu po operaci 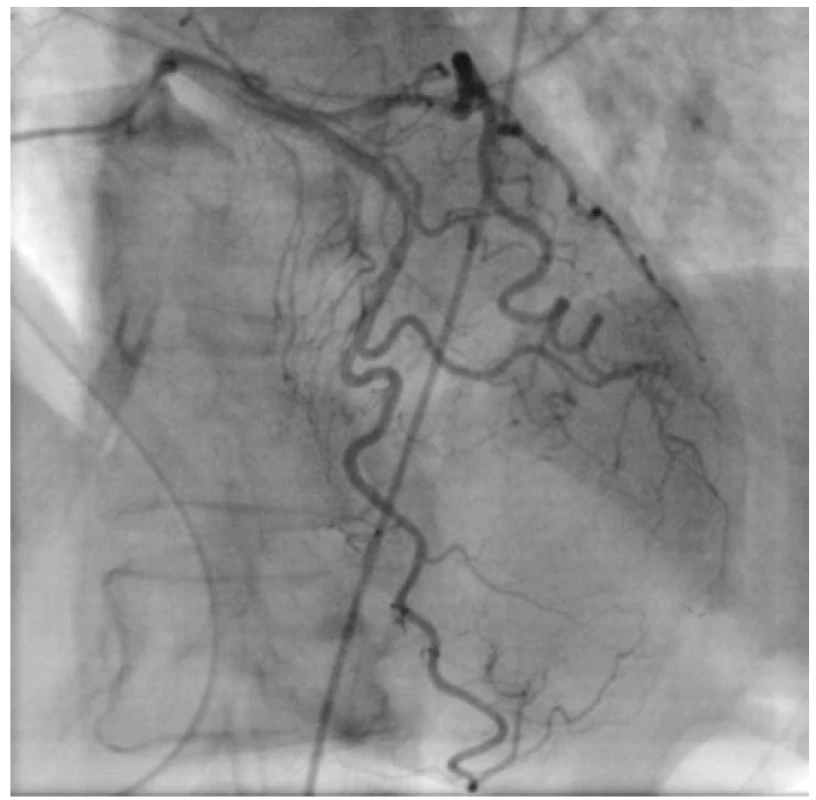
Image 3. Ventrikulografie jednu hodinu od operace. Apex ve tvaru balonu, hyperkontraktilní bazální část levé komory. 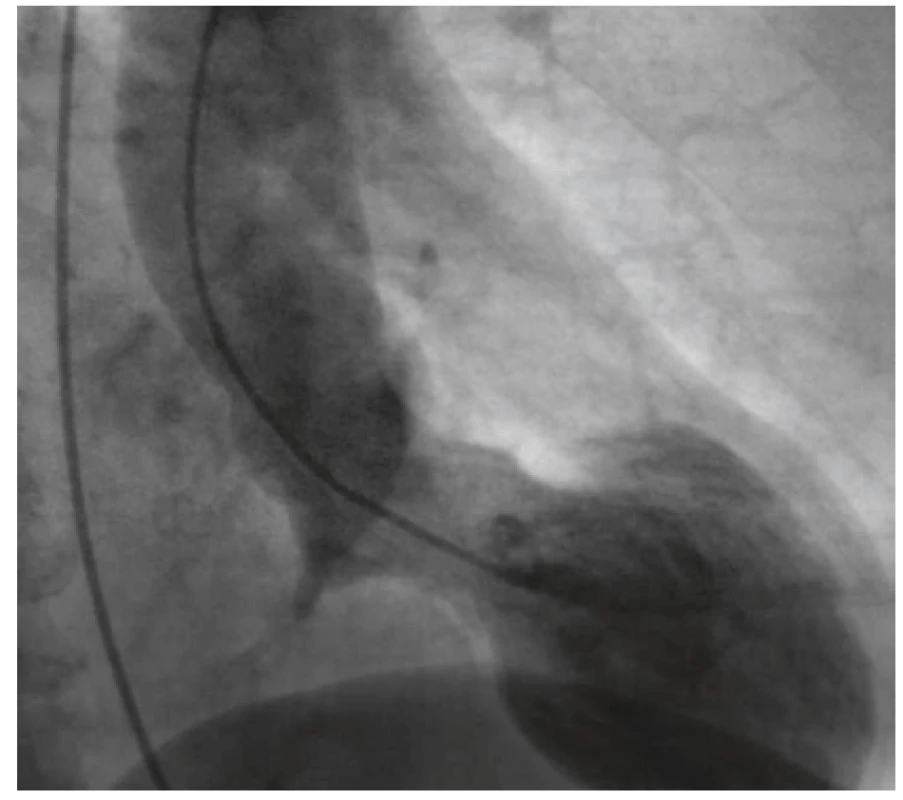
Graph 1. Dynamika kreatinkinázy MB (CK-MB) a jejího poměru k celkové kreatinkináze (CK) 
DISKUSE
Kazuistika popisuje peroperační rozvoj tako-tsubo syndromu u 71leté pacientky podstupující odstranění agresivně rostoucího hemangiomu v oblasti Th6 s invazí do kanálu páteřního, do oblouku, pediklů a těla obratle Th6.
Rozvoj TTS je popisován v perioperačním období u výkonů všeobecné, cévní, hrudní chirurgie a v kardiochirurgii. Ve spondylochirurgii jsou případy TTS raritní [7]. Ačkoli patofyziologie tako-tsubo kardiomyopatie není dosud zcela jasná, za hlavní příčinu je považován nadměrný účinek katecholaminů, zvýšený tonus sympatického nervového systému (SNS) a/nebo přímá stimulace SNS. Spasmus koronárních arterií není pravděpodobná příčina stavu, protože oblast snížené funkce myokardu je u TTS mnohem rozsáhlejší a přesahuje hranice cévního zásobení předpokládanou koronární tepnou [2].
Tako-tsubo kardiomyopatie je doprovázena zvýšením srdečních biomarkerů troponinu T a kreatinkinázy. K poškození kardiomyocytů dochází pravděpodobně přímým účinkem katecholaminů na srdeční buňku a druhotným účinkem katecholaminů na mikrocirkulaci vedoucí k ischemii buněk [6]. Nálezy z biopsií srdečního svalu v průběhu TTS prokazují rozsáhlé plochy srdečních buněk naplněných množstvím glykogenu suspektně po snížení dodávek energie na podkladě ischemie a četnými vakuolami v důsledku poškození metabolismu bílkovin [6]. Katecholaminové toxicitě odpovídá také histologický nález přítomnosti mononukleárů a narušeného specifického uspořádání cytoskeletálních a kontraktilních proteinů s úplnou rekonstitucí za 2‒4 týdny od vzniku onemocnění [6].
Autonomní dysregulace myokardu při TTS souvisí se zvýšením tonu SNS [2]. Převaha tonu levostranného ganglion stellatum v oblasti Th7 je spojena s hypokontraktilitou apexu, převaha pravostranného ganglion stellatum vede k poruše kontraktility ve střední části komory [2]. Levostranné srdeční nervy sympatiku inervují AV uzel a spodní a zadní stěnu levé komory [2]. Ve zvířecím modelu lze vyvolat tako-tsubo kardiomyopatii stimulací jednotlivých ganglií s popsanou predilekcí lokalizace změn [2]. Další příčinou TTS může být zvýšená aktivita sympatiku v situaci zvýšeného množství receptorů SNS v myokardu (i lokalizovaně) [2].
TTS se vyskytuje častěji u žen vyššího věku, důvodem může být zvyšující se tonus sympatiku s vyšším věkem a ukončení působení estrogenů, které tonus sympatiku fyziologicky snižují [6].
Na základě klinického průběhu exstirpace invazivního hemangiomu v oblasti hrudního sympatiku a v blízkosti levého ganglion stellatum nemůžeme vyloučit ani přímou mechanickou aktivaci SNS se vznikem poruchy kinetiky v oblasti apexu levé komory.
Rozvoj tako-tsubo syndromu je možnou závažnou komplikací i elektivních operačních výkonů u rizikových skupin nemocných, především žen v postmenopauzálním věku. Kromě nedostatečně kontrolované stresové odpovědi v perioperačním období může být u vybraných operačních výkonů také vyvolán přímou mechanickou stimulací SNS. Ačkoliv podezření na rozvoj syndromu lze v určitém klinickém kontextu vyslovit při typickém nálezu již na základě ultrazvukového vyšetření srdce, definitivní diagnostika vyžaduje provedení koronarografického vyšetření s ventrikulografií [8].
Práce je původní, nebyla publikována ani není zaslána k recenznímu řízení do jiného média. Práce nebyla prezentována formou přednášky, posteru nebo abstraktu.
Autoři prohlašují, že nemají střet zájmů v souvislosti s tématem práce.
Všichni autoři rukopis četli, souhlasí s jeho zněním a zasláním do redakce časopisu Anesteziologie a intenzivní medicína.
Podíl autorů na přípravě článku:
DV: připravila pracovní verzi rukopisu.
HT: spolupracoval na přípravě rukopisu.
SM: spolupracoval na přípravě rukopisu
DP: finalizoval rukopis
Poznámka: Nebyl získán písemný informovaný souhlas pacienta s publikací z důvodu nemožnosti kontaktu. Z textu a příloh kazuistiky není možné identifikovat pacienta.
Do redakce došlo dne 15. 5. 2019.
Do tisku přijato dne 24. 5. 2019.
Adresa pro korespondenci:
doc. MUDr. Pavel Dostál, Ph.D., MBA
Sources
1. Akashi YJ, Ishihara M. Takotsubo syndrome: insights from Japan. Heart Fail Clin. 2016;12 : 587–595. doi: 10.1016/j.hfc.2016.06.009.
2. Raj SR. Too sympathetic? Role of sympathoexcitation in Takotsubo cardiomyopathy. Heart Rhythm. 2010;7 : 1833–1834. doi: 10.1016/j.hrthm.2010.09.018.
3. Maron BJ, Towbin JA, Thiene G, et al. Contemporary definitions and classification of the cardiomyopathies: an American Heart Association Scientific Statement from the Council on Clinical Cardiology, Heart Failure and Transplantation Committee; Quality of Care and Outcomes Research and Functional Genomics and Translational Biology Interdisciplinary Working Groups; and Council on Epidemiology and Prevention. Circulation. 2006;113 : 1807–1816.
4. Ghadri JR, Wittstein IS, Prasad A. International Expert Consensus Document on Takotsubo Syndrome (Part I): clinical characteristics, diagnostic criteria, and pathophysiology. Eur Heart J. 2018;39 : 2032–2046. doi: 10.1093/eurheartj/ehy076.
5. Ozpelit E, Ozpelit ME, Akdeniz B, Göldeli Ö. Ergotamine-induced takotsubo cardiomyopathy. Am J Ther. 2016;23:e597–600. doi: 10.1097/MJT.0000000000000030.
6. Nef HM, Möllmann H, Kostin S. Tako-Tsubo cardiomyopathy: intraindividual structural analysis in the acute phase and after functional recovery. Eur Heart J. 2007;28 : 2456–2464. doi: 10.1093/eurheartj/ehl570.
7. Hammer N, Kühne C, Meixensberger J. Takotsubo cardiomyopathy – an unexpected complication in spine surgery. Int J Surg Case Rep. 2015;6C:172–174. doi: 10.1016/j.ijscr.2014.10.002.
8. Ghadri JR, Wittstein IS, Prasad A, et al. International expert consensus document on takotsubo syndrome (part II): diagnostic workup, outcome, and management. Eur Heart J. 2018;39 : 2047–2062. doi: 10.1093/eurheartj/ehy077.
Labels
Anaesthesiology, Resuscitation and Inten Intensive Care Medicine
Article was published inAnaesthesiology and Intensive Care Medicine

2019 Issue 3-4-
All articles in this issue
- Obtížné zajištění dýchacích cest u dospělých a u dětí; nový doporučený postup ČSARIM
- POCT – UZ v diagnostice diafragmatické dysfunkce po torakochirurgických výkonech
- Jak pracovat s Doporučeným postupem ČSARIM pro zajištění obtížných dýchacích cest?
- APACHE a qSOFA ve stratifikaci rizika při sepsi
- Léčba hypotenze po úvodu do celkové anestezie – multicentrická dotazníková studie
- Tako-tsubo syndrom v průběhu spondylochirurgického výkonu
- Vliv videolaryngoskopie na hloubku zavedení tracheální rourky a četnost endobronchiální intubace – prospektivní randomizovaná studie
- ARDS a obézní pacient
- Fasciální prostory na krku pro regionální anestezii
- Deeskalace antibiotické terapie jako součást strategie péče o kriticky nemocné
- TTM – řízená tělesná teplota v současném pojetí
- Základní neuromodulační metody v léčbě chronické bolesti
- Ambulantní kolonoskopie – čas propuštění po výkonu
- Pohled mladých anesteziologů a intenzivistů na specializační vzdělávání v oboru anesteziologie a intenzivní medicína v České republice: dotazníková studie
- Tako-tsubo kardiomyopatie jako perioperační komplikace karotické endarterektomie potvrzená MR zobrazením srdce
- Zajištění obtížných dýchacích cest u dospělých a dětí
- EKG lekce 5
- Farmakologie látek ovlivňujících fluidokoagulační rovnováhu
- Kapilární návrat – klinické vyšetření přítomnosti cirkulační koherence?
- Za primářem MUDr. Vladimírem Kynclem (19. 10. 1930 – 27. 5. 2019)
- Anaesthesiology and Intensive Care Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Kapilární návrat – klinické vyšetření přítomnosti cirkulační koherence?
- Základní neuromodulační metody v léčbě chronické bolesti
- Deeskalace antibiotické terapie jako součást strategie péče o kriticky nemocné
- Zajištění obtížných dýchacích cest u dospělých a dětí
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


