-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Hypotyreóza u pacientů se srdečním onemocněním
Hypothyroidism in patients with heart disease
Hypothyroidism is frequently found in patients with heart disease. It is a risk factor for atherosclerosis and ischemic heart disease and has a direct negative effect on both the left and right ventricular functions (hypothyroidism-induced cardiomyopathy). The confirmed manifest hypothyroidism is always a reason for replacement therapy with levothyroxine; regarding patients with heart disease, we always begin treatment with a small dose and increase it gradually. The treatment of subclinical hypothyroidism in patients with heart disease is disputable and its benefits probably depend on age. At a higher age, the therapy-related risks often outweigh its benefits, so we make do with the target levels of the thyroid stimulating hormone being within the upper band of the normal range, or even slightly above it, rather than overdosing the patient. To summarize in a simplified way, the treatment of subclinical hypothyroidism in patients with heart disease is the most effective in younger individuals, mainly those aged below 65, while at a higher age > 80 years the risk usually outweighs the benefit.
Key words:
cardiovascular risk – hypothyroidism – ischemic heart disease – left ventricular dysfunction – right ventricular dysfunction – subclinical hypothyroidism – thyroid peroxidase antibodies
Autoři: Jan Jiskra
Působiště autorů: III. interní klinika 1. LF UK a VFN v Praze
Vyšlo v časopise: Vnitř Lék 2017; 63(9): 566-571
Kategorie: Přehledné referáty
Souhrn
Hypotyreóza je u pacientů se srdečním onemocněním častým nálezem. Je rizikovým faktorem aterosklerózy a ischemické choroby srdeční a má přímý negativní vliv na funkci levé i pravé srdeční komory (hypotyreózní kardiomyopatie). Potvrzená manifestní hypotyreóza je vždy důvodem k substituční léčbě levotyroxinem; u pacientů se srdečním onemocněním vždy začínáme léčbu malou dávku a zvyšujeme postupně. Léčba subklinické hypotyreózy je u pacientů se srdečním onemocněním kontroverzní a její benefity pravděpodobně závisí na věku. Ve vyšším věku často rizika léčby převáží, a proto se raději spokojíme s cílovými hodnotami tyreoidálního stimulačního hormonu v horním pásmu normálního rozmezí, nebo i lehce nad ním, než abychom pacienta předávkovali. Velmi zjednodušeně lze říci, že léčba subklinické hypotyreózy u pacientů se srdečním onemocněním je nejefektivnější u mladších osob, zejména < 65 let, zatímco ve vyšším věku > 80 let již riziko obvykle převyšuje benefit.
Klíčová slova:
dysfunkce levé komory srdeční – dysfunkce pravé komory srdeční – hypotyreóza – ischemická choroba srdeční – kardiovaskulární riziko – protilátky proti tyreoidální peroxidáze – subklinická hypotyreózaÚvod
Hypotyreóza patří mezi onemocnění vyskytující se v masovém měřítku. Prevalence manifestní hypotyreózy, tedy zvýšený tyreoidální stimulační hormon (TSH) a snížený tyroxin v séru, je 3–5 % a asi stejně častá je subklinická hypotyreóza (zvýšený TSH a normální tyroxin v séru). Je zřejmé, že potenciální kardiovaskulární zdravotní rizika s nimi spojená ohrožují významnou část populace. Zatímco u manifestní hypotyreózy není o negativním vlivu na kardiovaskulární systém pochyb, u subklinické jsou význam kardiovaskulárního rizika a možnosti jeho ovlivnění předmětem pokračujících diskusí.
Patofyziologie
Existují 2 hlavní mechanizmy negativního vlivu hypotyreózy na srdce:
- hypotyreóza jako potenciální rizikový faktor aterosklerózy a ischemické choroby srdeční (ICHS)
- přímý negativní vliv hypotyreózy na srdeční funkci (hypotyreózní kardiomyopatie)
Hypotyreóza jako rizikový faktor aterosklerózy a ICHS
Hypotyreóza je příčinou proaterogenní dyslipidemie a snižuje vylučování vody ledvinami, čímž přispívá k diastolické arteriální hypertenzi. Zda je hypotyreóza i nezávislým rizikovým faktorem aterosklerózy, zůstává otevřenou otázkou. Zdá se, že to platí především pro manifestní hypotyreózu a pro subklinickou hypotyreózu u mladších osob (< 65 let). Patofyziologický mechanizmus zůstává neznámý (spekuluje se mimo jiné o roli cytoadhezivních molekul, vlivu na agregaci destiček apod). Naopak subklinická hypotyreóza u starších osob (> 80 let) se zdá být spojena s nižší kardiovaskulární i celkovou mortalitou.
Hypotyreózní kardiomyopatie
Změny srdce u manifestní hypotyreózy jsou dobře známé. Patří k nim perikardiální výpotek a porucha relaxace a kontraktility srdečního svalu s diastolickou a systolickou dysfunkcí. Průvodním jevem jsou nespecifické změny na EKG (negativní vlna T a snížená voltáž v hrudních svodech) a elevace kreatinkinázy v séru. Ty jsou nejednou mylně interpretovány jako ischemické změny (obr. 1). Perikardiální výpotek je způsoben sníženou glomerulární filtrací a sníženou schopností ledvin vylučovat vodu. Při tom dochází k hromadění tekutiny v třetích prostorech a k hyponatremii. To je pro hypotyreózu celkem typický jev. Porucha srdečního svalu se nejprve projeví poruchou relaxace (diastolická dysfunkce). Příčinou je zřejmě změna složení proteoglykanů mezibuněčného prostoru myokardu a vazba vody na ně – podobně jako při změnách kůže. Postupně dochází i ke změně složení bílkovin myokardu a k poruše kontraktility (ke stejným změnám dochází i v příčně pruhovaných svalech – důsledkem je hypotyreózní myopatie). Tyto změny jsou reverzibilní a funkce srdečních komor se po substituční léčbě levotyroxinem normalizuje, i když to může trvat řadu měsíců.
Obr. 1. EKG u hypotyreózy. 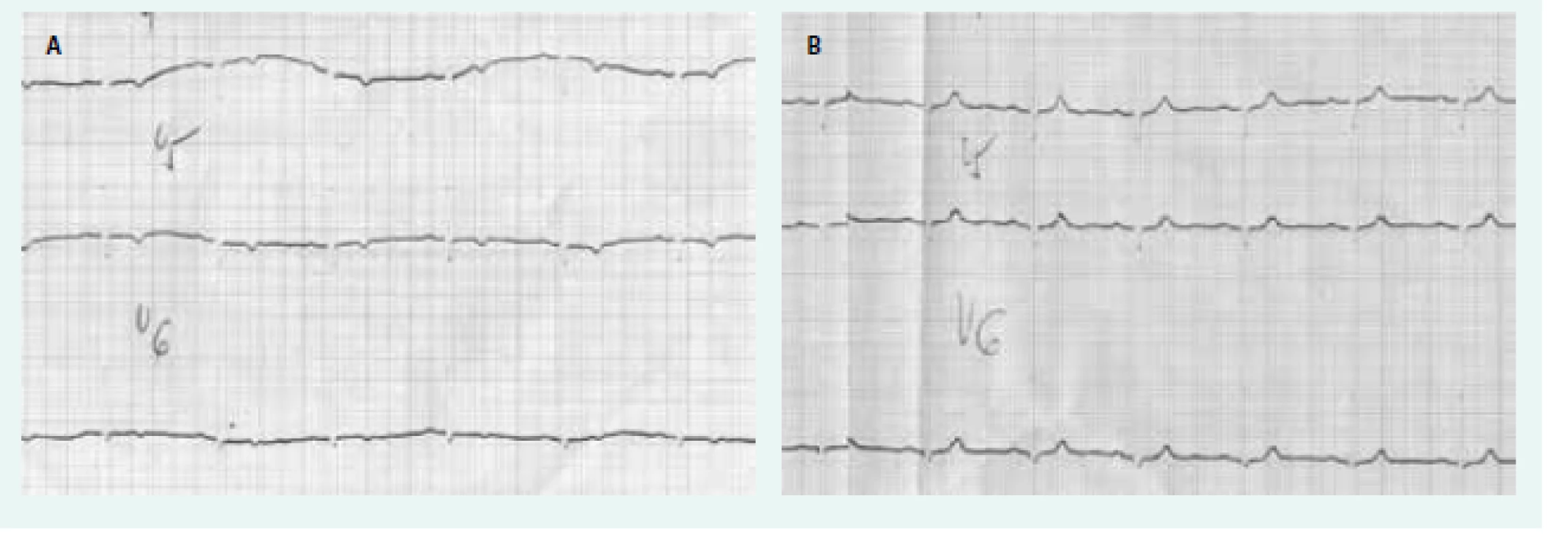
A – negativní vlny T u neléčené hypotyreózy B – normalizace po léčbě levotyroxinem Klinické studie
V posledních 30 letech byla realizována řada studií a metaanalýz, z nichž většina potvrdila manifestní hypotyreózu jako významný rizikový faktor kardiovaskulární morbidity a mortality. Subklinickou hypotyreózu jako rizikový faktor potvrdily jen některé studie a metaanalýzy, a jiné toto spojení naopak zpochybnily. Jednou z hypotéz je, že kardiovaskulární riziko je u subklinické hypotyreózy závislé na věku (graf 1), [12]. Metaanalýzy z posledních let totiž ukázaly, že kardiovaskulární riziko je u subklinické hypotyreózy významně zvýšeno jen u osob mladších 65 let, a to především u postmenopauzálních žen, které jsou ohroženy nejvíce [15]. Naopak ve vyšším věku se subklinická hypotyreóza zdá být naopak protektivním faktorem – příkladem je 2krát nižší mortalita u osob starších 85 let s mírně vyšším TSH (> 4,8 mIU/l) [19].
Graf 1. Hypotetická závislost kardiovaskulárního rizika subklinické hypotyreózy na věku. 
Upraveno podle [12] Dosud nemáme žádné důkazy, že má léčba levotyroxinem u subklinické hypotyreózy pozitivní vliv na kardiovaskulární morbiditu a mortalitu. K dispozici jsou pouze intervenční studie, které ukázaly, že léčba příznivě ovlivňuje rizikové faktory aterosklerózy [2,11], klesala rychlost pulzové vlny jako nezávislého prediktoru koronární aterosklerózy [1], zlepšila se průtokem prostředkovaná vazodilatace [16], došlo k poklesu systolického i diastolického krevního tlaku, zlepšila se glomerulární filtrace, snížila se intimomediální tloušťka a zvětšil se průměr a. carotis a byl pozorován vzestup endoteliálních progenitorových buněk jako nepřímá známka zlepšení endoteliální dysfunkce [18]. Terapie levotyroxinem u subklinické hypotyreózy vedla také ke zlepšení funkční tělesné kapacity (měřené 6minutovým „walk“ testem na běhátku) [7] a ke zlepšení dysfunkce levé [13] i pravé [21] srdeční komory. Na druhou stranu byla kardiovaskulární morbidita zvýšená i u pacientů, kteří měli subklinickou hypotyreózu levotyroxinem léčenou [14]. Řada prací také ukázala, že zejména u starších osob je relativní kardiovaskulární riziko u subklinické hypertyreózy (a tedy i riziko plynoucí z předávkování levotyroxinem!) vyšší než u subklinické hypotyreózy (graf 2) [15]. Recentní retrospektivní kohortová studie neprokázala žádný (ani pozitivní, ani negativní) vliv léčby levotyroxinem u pacientů se subklinickou hypotyreózou na riziko infarktu myokardu a celkovou mortalitu (n = 12 212) [3] ani na další kardiovaskulární příhody či frekvenci hospitalizací (n = 1 192) [4].
Graf 2. Relativní riziko kardiovaskulární morbidity u subklinické hypotyreózy a hypertyreózy u osob starších 80 let. 
RR – relativní riziko Upraveno podle [15] Diagnostika hypotyreózy
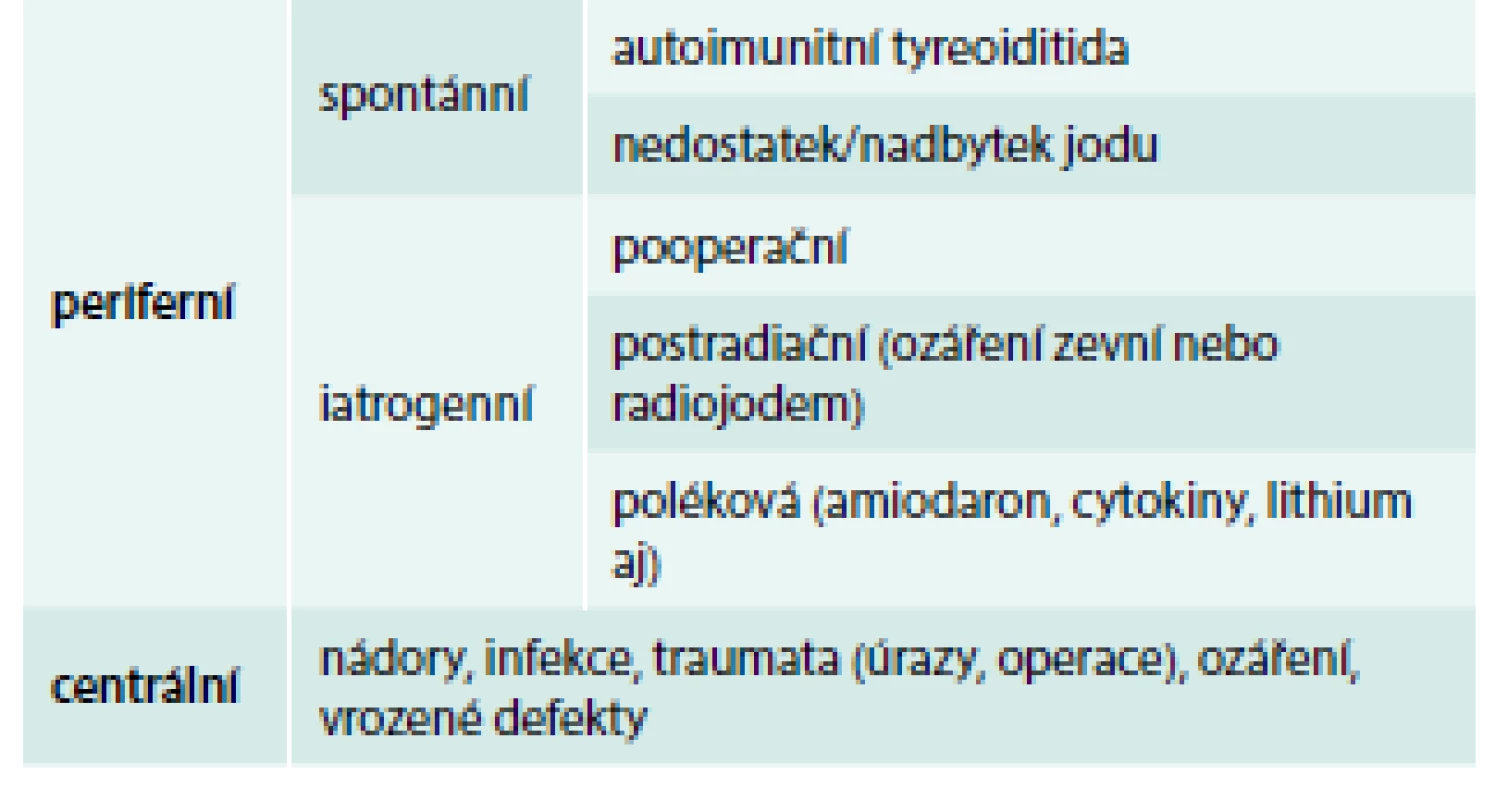
Základem diagnostiky periferní hypotyreózy je vyšetření hladiny TSH v séru. Pokud je normální, lze periferní tyreoidální dysfunkci vyloučit. Pokud jsou hodnoty TSH zvýšené, doplníme volný tyroxin (free thyroxine 4 – fT4) a protilátky proti tyreoidální peroxidáze (TPOAb – anti-thyroid autoantibodies) v séru, ev. zopakujeme vyšetření TSH. Bude-li fT4 snížený, jde o manifestní hypotyreózu, bude-li normální, jde o subklinickou hypotyreózu. Pozitivní TPOAb svědčí pro nejčastější příčinu hypotyreózy – autoimunitní tyreoiditidu. Ostatní příčiny jsou relativně vzácné (tab. 1). Je-li podezření na centrální hypotyreózu (operace nebo onemocnění hypofýzy v anamnéze, úraz hlavy, ozáření CNS, krvácení do CNS apod), je diagnóza naopak založena na vyšetření fT4.
Existují i „netyreoidální“ příčiny mírné elevace TSH (tab. 2), při nichž jsou negativní protilátky a normální nález při ultrasonografickém vyšetření. Tyto stavy nevyžadují léčbu levotyroxinem. Se zvýšeným TSH a sníženým fT4 se setkáme i u iatrogenní hypotyreózy vyvolané podáváním tyreostatik.
Tab. 2. Příčiny netyreoidální elevace TSH v séru 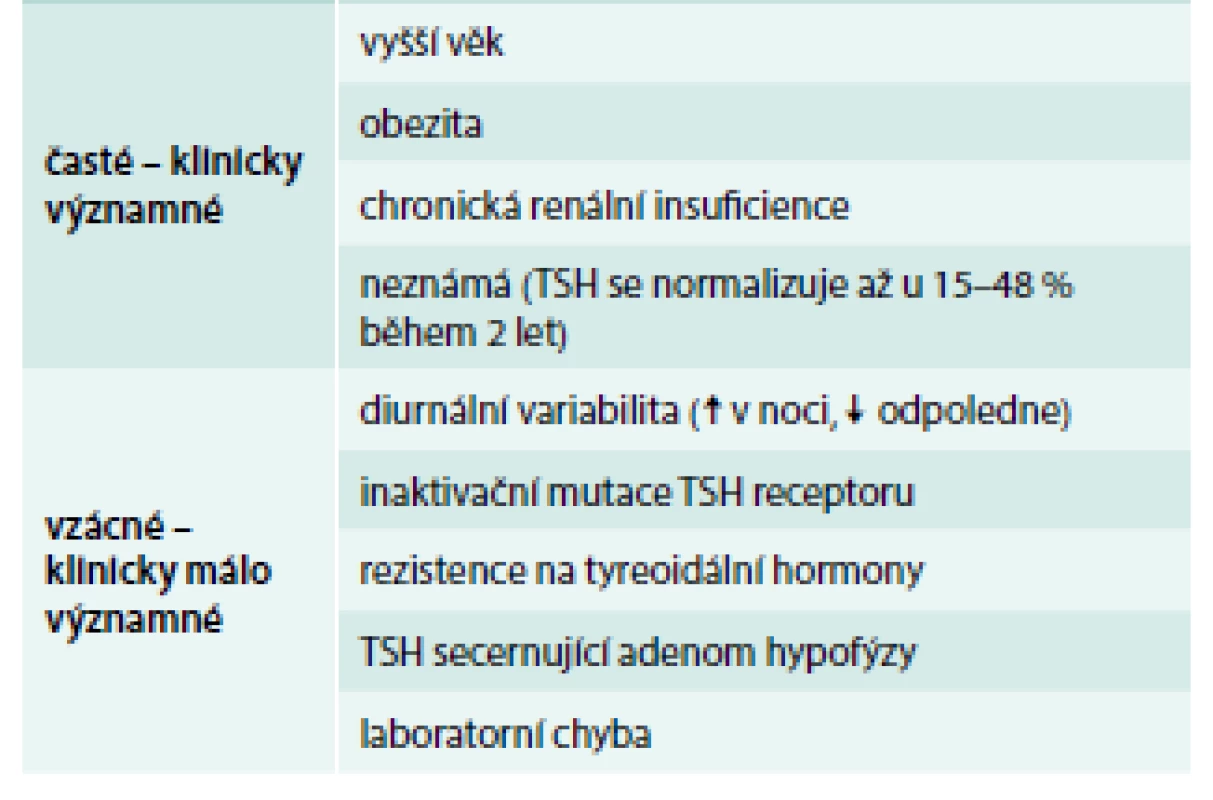
TSH – tyreoidální stimulační hormon Diagnóza subklinické hypotyreózy by měla být potvrzena nejméně 2 patologickými výsledky TSH v odstupu 3–6 měsíců a měly by se doplnit TPOAb v séru nebo ultrasonografické (USG) vyšetření štítné žlázy, aby byla dokumentovaná příčina. Normalizace TSH je totiž častá, zejména ve vyšším věku. Podle studie Somwaru et al z roku 2013 [20] došlo u osob ve věku > 65 let po 2 letech ke spontánní normalizaci TSH u 46 % osob se vstupní hodnotou TSH 4,5–6,9 mIU/l a 10 % osob se vstupní hodnotou TSH 7–9,9 mIU/l; a u 48 % osob se vstupně negativními TPOAb a 15 % osob se vstupně pozitivními TPOAb. Je třeba také mít na paměti, že většina velkých observačních studií ukázala, že hladina TSH v krvi stoupá s věkem [6,10]. Ve studii NHANES u pacientů nad 30–39 let stoupal 97,5 percentil normy pro TSH každých 10 let o 0,3 mIU/l, což nebylo ovlivněno hmotností, tyreoidálními protilátkami ani jodurií [5].
Nejen vyšetření celkového tyroxinu (TT4 – total thyroxine 4) v séru, ale i fT4 může ovlivněno řadou okolností (tab. 3). Proto se jako screeningový test doporučuje TSH a fT4 (eventuálně TT4) se doplňuje pouze, pokud je TSH mimo normu. Celkový či volný trijodtyronin (TT3 či fT3) se vyšetřuje jen v nejasných případech a v běžné praxi jsou tato vyšetření nadbytečná. Jednou z indikací je snížení TSH při normálním fT4 a klinickém podezření na hypertyreózu. Při „syndromu nízkého T3“ je fT3 snížený z důvodu porušené dejodace tyroxinu na trijodtyronin (T3) a preferenční syntézy tzv. reverzního T3, což obvykle provází závažné celkové nemoci (sepse, trauma, multiorgánové selhání, chronická malnutrice, chronické srdeční selhání apod). TSH je při tom obvykle snížený, může však být i normální či zvýšený, stejně jako fT4.
Tab. 3. Faktory, které mohou ovlivnit imunoanalytické stanovení volného tyroxinu v séru 
Platí, že diagnostika hypotyreózy je spolehlivější v ambulantním režimu. Důvodem je to, že TSH je velmi citlivý parametr, který je ovlivněn řadou přidružených akutních i chronických chorob. Uvádí se například, že až třetina hospitalizovaných pacientů má nespecificky suprimovaný (snížený) TSH z netyreoidálních příčin (tab. 4). Pokud je však důvodné klinické podezření na hypotyreózu, provádíme laboratorní testy samozřejmě i za hospitalizace.
Tab. 4. Příčiny netyreoidální suprese TSH 
Terapie hypotyreózy u pacienta se srdečním onemocněním
Podstatou léčby hypotyreózy je hormonální substituce levotyroxinem (LT4). Orientační denní dávka je 1,5 μg LT4 na 1 kg tělesné hmotnosti, závisí však na řadě faktorů. U mladých a jinak zdravých jedinců můžeme ihned podat téměř plnou dávku. U pacientů s ICHS nebo s chronickým srdečním selháním se doporučuje začít léčbu malou dávkou (12,5–25 μg denně), která se zvyšuje postupně (o 50–100 % po 4–6 týdnech). Podobně postupujeme i u starších jinak zdravých osob, i když důkazy pro tento postup chybějí a jsou práce, které ukázaly, že i ve vyšším věku je zahájení substituce plnou dávkou bezpečné [17]. Dávka LT4 se upravuje podle hodnoty TSH v séru – cílové hodnoty jsou rovny pásmu normy příslušné laboratorní metody (obvykle od 0,4–0,5 mIU/l do 4,0–5,0 mIU/l). Při léčbě pacienta se srdečním onemocněním se často raději spokojíme s hodnotami TSH v horní polovině normálního rozmezí (2–4 mIU/l), nebo i lehce nad ni, než abychom pacienta předávkovali. Subklinická hypertyreóza vzniklá předávkováním má totiž prokazatelně větší zdravotní rizika (kardiovaskulární, kostní, depresivní syndrom) než neléčená subklinická hypotyreóza [8,15]. U pacientů se srdečním onemocněním vedou neodůvodněně vysoké dávky LT4 spojené s poklesem TSH pod dolní mez normálního rozmezí (0,4–0,5 mIU/l) prokazatelně ke komplikacím (fibrilace síní, tachykardie, manifestace anginy pectoris, manifestace srdečního selhání, osteoporóza) a jsou spojeny se zvýšenou morbiditou a mortalitou (graf 3). Výjimkou je tzv. supresní léčba po odstranění štítné žlázy pro zhoubný nádor. Jejím cílem je zabránit potlačením produkce TSH růstu případné zbytkové tyreoidální tkáně nebo metastáz. I ta však musí být u pacientů se srdečním onemocněním indikována s rozvahou a s přihlédnutím k poměru rizika a benefitu. U pacientů s karcinomem štítné žlázy s nízkým rizikem se spokojíme se supresí TSH do dolního pásma normálních hodnot (0,5–1,0 mIU/l). Pouze u pacientů s karcinomem štítné žlázy s vysokým rizikem je suprese agresivnější s cílovým TSH pod dolní hranici normálních hodnot, vždy však v závislosti na toleranci pacienta. Po 5 letech se v závislosti na stupni rizika tyreoidálního karcinomu suprese uvolňuje a přechází se na substituční dávku.
Graf 3. Mortalita z kardiovaskulárních příčin v závislosti na TSH. 
TSH – tyreoidální stimulační hormon Upraveno podle [8] Manifestní hypotyreóza by měla být léčena vždy a o příznivém efektu léčby nemůže být pochyb. Indikace k léčbě subklinické hypotyreózy u pacientů se srdečním onemocněním však zůstávají nejasné a kontroverzní. Jak bylo uvedeno výše, léčba sice redukuje rizikové faktory aterosklerózy, zlepšuje srdeční funkci a možná zlepšuje tělesnou zdatnost nemocných, nemá však významný vliv na mortalitu ani morbiditu nemocných. Naopak, při předávkování levotyroxinem může být pacient léčbou i poškozen. U subklinické hypotyreózy u pacienta se srdečním onemocněním by se o léčbě mělo rozhodnout individuálně s přihlédnutím k věku, přidruženým chorobám, komplianci pacienta a laboratorním nálezům (tab. 5).
Tab. 5. Rámcové doporučení pro léčbu hypotyreózy u pacientů s onemocněním srdce 
TSH – tyreoidální stimulační hormon fT4 – volný tyroxin LT4 by se měl užívat nalačno alespoň 30 min před požitím potravy a jiných léků, jinak se snižuje resorpce. Tu snižují nejvíce preparáty železa, léky snižující žaludeční aciditu (omeprazol, antacida) a iontoměniče (pryskyřice při hypolipidemické léčbě). Resorpce se také snižuje u pacientů s chronickým městnavým srdečním selháním. K monitoraci léčby periferní hypotyreózy LT4 se používá výhradně TSH. Vyšetřování fT4 nebo dokonce TPOAb za tímto účelem je zbytečné a imunoanalytické vyšetření fT4 je navíc u polymorbidních pacientů užívajících řadu léků značně nespolehlivé. Než dojde ke stabilizaci stavu a optimalizaci dávky, kontroluje se TSH po 4–6 týdnech od poslední úpravy. Častější kontroly nemají velký význam, změna dávky se v hodnotě sérového TSH dříve neprojeví. U stabilizovaného pacienta stačí kontroly TSH a klinického stavu 1krát ročně.
Závěr
Hypotyreóza je u pacientů se srdečním onemocněním častým nálezem. Potvrzená manifestní hypotyreóza je vždy důvodem k substituční léčbě levotyroxinem, u pacientů se srdečním onemocněním vždy začínáme léčbu malou dávku a zvyšujeme postupně. Často se raději spokojíme s cílovými hodnotami TSH v horním pásmu normálního rozmezí, nebo i lehce nad ni, než abychom pacienta předávkovali. Benefit z léčby subklinické hypotyreózy by měl být u pacientů se srdečním onemocněním zvážen vždy individuálně.
doc. MUDr. Jan Jiskra, Ph.D.
jan.jiskra@vfn.cz
III. interní klinika 1. LF UK a
VFN v Praze
www.vfn.cz
Doručeno do redakce 27. 6. 2017
Přijato po recenzi 4. 9. 2017
Zdroje
1. Biondi B, Galderisi M, Pagano L et al. Endothelial-mediated coronary flow reserve in patients with mild thyroid hormone deficiency. Eur J Endocrinol 2009; 161(2): 323–329. Dostupné z DOI: <http://dx.doi.org/10.1530/EJE-09–0196>.
2. Abreu IM, Lau E, de Sousa Pinto B et al. Subclinical hypothyroidism: to treat or not to treat, that is the question! A systematic review with meta-analysis on lipid profile. Endocr Connect 2017; 6(3): 188–199. Dostupné z DOI: <http://dx.doi.org/10.1530/EC-17–0028>.
3. Andersen MN, Olsen AM, Madsen JC et al. Levothyroxine Substitution in Patients with Subclinical Hypothyroidism and the Risk of Myocardial Infarction and Mortality. PLoS One 2015; 10(6): e0129793. Dostupné z DOI: <http://dx.doi.org/10.1371/journal.pone.0129793>.
4. Andersen MN, Olsen AS, Madsen JC et al. Long-Term Outcome in Levothyroxine Treated Patients With Subclinical Hypothyroidism and Concomitant Heart Disease. J Clin Endocrinol Metab 2016; 101(11): 4170–4177.
5. Boucai L, Hollowell JG, Surks MI. An approach for development of age-, gender-, and ethnicity-specific thyrotropin reference limits. Thyroid 2011; 21(1): 5–11. Dostupné z DOI: <http://dx.doi.org/10.1089/thy.2010.0092>.
6. Bremner AP, Feddema P, Leedman PJ et al. Age-related changes in thyroid function: a longitudinal study of a community-based cohort. J Clin Endocrinol Metab 2012; 97(5): 1554–1562. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2011–3020>.
7. Curotto Grasiosi J, Peressotti B, Machado RA et al. Improvement in functional capacity after levothyroxine treatment in patients with chronic heart failure and subclinical hypothyroidism. Endocrinol Nutr 2013; 60(8): 427–432. Dostupné z DOI: <http://dx.doi.org/10.1016/j.endonu.2013.01.013>.
8. Franklyn JA. The thyroid – too much and too little across the ages. The consequences of subclinical thyroid dysfunction. Clin Endocrinol (Oxf) 2013; 78(1): 1–8. Dostupné z DOI: <http://dx.doi.org/10.1111/cen.12011>.
9. Garber JR, Cobin RH, Gharib H et al. [American Association Of Clinical Endocrinologists And American Thyroid Association Taskforce On Hypothyroidism In Adults]. Clinical practice guidelines for hypothyroidism in adults: cosponsored by the American Association of Clinical Endocrinologists and the American Thyroid Association. Thyroid 2012; 22(12): 1200–1235. Dostupné z DOI: <http://dx.doi.org/10.1089/thy.2012.0205>. Erratum in Thyroid 2013; 23(2): 251. Thyroid 2013; 23(1): 129.
10. Hollowell JG, Staehling NW et al. Serum TSH, T(4), and thyroid antibodies in the United States population (1988 to 1994): National Health and Nutrition Examination Survey (NHANES III). J Clin Endocrinol Metab 2002; 87(2): 489–499.
11. Iqbal A, Jorde R, Figenschau Y. Serum lipid levels in relation to serum thyroidstimulating hormone and the effect of thyroxine treatment on serum lipid levels in subjects with subclinical hypothyroidism: the tromso Study. J Intern Med 2006; 260(1): 53–61.
12. Mariotti S. Mild hypothyroidism and ischemic heart disease: Is age the answer? J Clin Endocrinol Metab 2008; 93(8): 2969–2971. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2008–1237>.
13. Monzani F, Di Bello V, Caraccio N et al. Effect of levothyroxine on cardiac function and structure in subclinical hypothyroidism: a double blind, placebo-controlled study. J Clin Endocrinol Metab 2001; 86(3): 1110–1115.
14. Nyirenda MJ, Clark DN, Finlayson AR et al. Thyroid disease and increased cardiovascular risk. Thyroid 2005; 15(7): 718–724.
15. Ochs N, Auer R, Bauer DC et al. Meta-analysis: subclinical thyroid dysfunction and the risk for coronary heart disease and mortality. Ann Intern Med 2008; 148(11): 832–845.
16. Razvi S, Ingoe L, Keeka G et al. The beneficial effect of lthyroxine on cardiovascular risk factors, endothelial function and quality of life in subclinical hypothyroidism: randomised, crossover trial. J Clin Endocrinol Metab 2007; 92(5): 1715–1723.
17. Roos A, Linn-Rasker SP, van Domburg R et al. The starting dose of levothyroxine in primary hypothyroidism treatment: a prospective, randomized, bouble-blind trial. Arch Intern Med 2005; 165(15): 1714–1720.
18. Shakoor SK, Aldibbiat A, Ingoe LE et al. Endothelial progenitor cells in subclinical hypothyroidism: the effect of thyroid hormone replacement therapy. J Clin Endocrinol Metab 2010; 95(1): 319–322. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2009–1421>.
19. Singer RB. Mortality in a complete 4year follow up of 85yearold residents of leiden, classified by serum level of thyrotropin and thyroxine. J Insur Med 2006; 38(1): 14–19.
20. Somwaru LL, Rariy CM, Arnold AM et al. The natural history of subclinical hypothyroidism in the elderly: the cardiovascular health study. J Clin Endocrinol Metab 2012; 97(6): 1962–1969. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2011–3047>.
21. Turhan S, Tulunay C, Ozduman Cin M et al. Effects of thyroxine therapy on right ventricular systolic and diastolic function in patients with subclinical hypothyroidism: a study by pulsed wave tissue Doppler imaging. J Clin Endocrinol Metab 2006; 91(9): 3490–3493.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2017 Číslo 9- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Magnosolv a jeho využití v neurologii
- S prof. Vladimírem Paličkou o racionální suplementaci kalcia a vitaminu D v každodenní praxi
-
Všechny články tohoto čísla
-
Úvodní slovo prof. MUDr. Michala Krška, CSc.,
spolueditora tohoto čísla časopisu Vnitřní lékařství - Onemocnění štítné žlázy v České republice: projekt EUthyroid a vyhodnocení epidemiologických dat VZP za období let 2012–2015
- Skríning tyreopatií v gravidite – odborné usmernenie v praxi
- Chlopenní vady při léčbě hyperprolaktinemie dopaminovými agonisty
- Hypotyreóza u pacientů se srdečním onemocněním
- Karcinomy štítné žlázy: současný pohled na diagnostiku a léčbu
- Diagnostika a manažment metastatického feochromocytómu a paragangliómu
- Kvalita kosti u akromegalikov
- Syndróm neprimeranej antidiurézy (SIAD) a súčasný manažment hyponatriémie
- Mužský hypogonadizmus indukovaný steroidními anaboliky: přehled poznatků a kazuistika
- Primární hyperparatyreóza – nové klinické formy onemocnění
- Efekt antidiabetickej liečby na kosť
- Adenozín – mediátor s multisystémovými účinkami (alebo hormón?)
-
Úvodní slovo prof. MUDr. Michala Krška, CSc.,
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Adenozín – mediátor s multisystémovými účinkami (alebo hormón?)
- Mužský hypogonadizmus indukovaný steroidními anaboliky: přehled poznatků a kazuistika
- Karcinomy štítné žlázy: současný pohled na diagnostiku a léčbu
- Primární hyperparatyreóza – nové klinické formy onemocnění
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání