-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Diagnostika a léčba Waldenströmovy makroglobulinémie
Vyšlo v časopise: Transfuze Hematol. dnes,28, 2022, No. Supplementum 1, p. 42-74.
Kategorie: Doporučené postupy
Doporučení vypracovaná Českou myelomovou skupinou (CMG), myelomovou sekcí České hematologické společnosti ČLS JEP a Kooperativní lymfomovou skupinou, lymfomovou sekcí České hematologické společnosti ČLS JEP.
Hlavní autoři
MUDr. Michal Kaščák
Klinika hematoonkologie LF OU a FN Ostrava
prof. MUDr. Roman Hájek, CSc.
Klinika hematoonkologie LF OU a FN Ostrava
doc. MUDr. Mgr. Jiří Minařík, Ph.D.
Hemato-onkologická klinika LF UP a FN Olomouc
Spoluautoři
Na vytvoření jednotlivých kapitol doporučení se podíleli další členové České myelomové skupiny a Kooperativní lymfomové skupiny, kteří jsou uvedeni v abecedním pořadí:
doc. MUDr. David Belada, Ph.D.
IV. interní hematologická klinika FN Hradec Králové
MUDr. Tomáš Jelínek Ph.D.
Klinika hematoonkologie LF OU a FN Ostrava
MUDr. Alexandra Jungová, Ph.D.
Hematologicko onkologické oddělení, LF UK a FN Plzeň
doc. MUDr. Jakub Radocha, Ph.D.
IV. interní hematologická klinika LF UK a FN Hradec Králové
prof. MUDr. Luděk Pour, Ph.D.
Interní hematologická a onkologická klinika LF MU a FN Brno
prof. MUDr. Marek Trněný, CSc.
I. interní klinika – klinika hematologie 1. LF UK a VFN v Praze
Recenzenti
prof. MUDr. Zdeněk Adam, CSc.
Interní hematologická a onkologická klinika LF MU a FN Brno
prof. MUDr. Vladimír Maisnar, Ph.D., MBA
IV. interní hematologická klinika LF UK a FN Hradec Králové
Obsah
Souhrn závěrečných doporučení z jednotlivých kapitol
1. Metodické postupy tvorby doporučení
2. Epidemiologie
3. Diagnóza
4. Prognóza
5. Vzorový zápis diagnózy Waldenströmova makroglobulinémie
6. Doporučení pro diagnostiku Waldenströmova makroglobulinémie
7. Indikace k léčbě
8. Strategie léčby
8.1. Nově léčená Waldenströmova makroglobulinémie
8.2. Léčba relapsu a refrakterní Waldenströmovy makroglobulinémie
9. Hodnocení léčebných odpovědí
10. Léčba Bing-Neelova syndromu
11. Podpůrná terapie a léčba komplikací
12. Sledování po léčbě
13. Doporučení pro léčbu Waldenströmova makroglobulinémie
Souhrn doporučení 2022
A. Doporučení pro diagnostiku Waldenströmovy makroglobulinémie
- Monitorování koncentrace monoklonálního imunoglobulinu (MIg) IgM by mělo být prováděno v jedné laboratoři a za použití vždy stejné metody.
- Vyšetření chladových aglutininů a kryoglobulinu je doporučené v době diagnózy a u pacientů s klinickými projevy poruch prokrvení a/nebo vaskulitídy či laboratorními projevy hemolýzy.
- Vyšetření kostní dřeně, nejlépe trepanobiopsie s adekvátní analýzou metodou průtokové cytometrie, je nezbytné pro stanovení diagnózy WM.
- Biopsie tkáně je doporučována u všech pacientů se suspektní histologickou transformací (u části nemocných s WM může dojít k transformaci do difuzního velkobuněčného B lymfomu (DLBCL)).
- Testování bodové mutace L265P v genu MYD88 je doporučeno u všech pacientů se zvažovanou diagnózou WM. Preferovaným vyšetřením je alelově specifická PCR z aspirátu kostní dřeně.
- Pro hodnocení rizika u symptomatických pacientů slouží mezinárodní prognostický skórovací systém pro nemocné s Waldenströmovou makroglobulinémií – IPSSWM.
- U pacientů se symptomatickou periferní neuropatií je doporučováno vyšetření specifických protilátek proti glykoproteinu myelinu („MAG“) nebo proti gangliosidu M1, tedy vyšetření anti-MAG a anti-GM-1 protilátek.
- Neurofyziologické testování pomocí elektromyografie (EMG) a neurografie (kondukční studie) je doporučeno při podezření na neuropatii a slouží k určení typu nervového poškození a usměrňuje další diagnostiku.
- Provedení vyšetření výpočetní tomografií (CT) nebo nukleární magnetickou rezonancí (MRI) (hrudníku, břicha, pánve) nebo celotělovou pozitronovou emisní tomografií v kombinaci s CT (PET/CT) je doporučováno u všech symptomatických pacientů před zahájením léčby.
- Pro hodnocení rizika u symptomatických pacientů slouží mezinárodní prognostický skórovací systém pro nemocné s Waldenströmovou makroglobulinémií – IPSSWM.
B. Doporučení pro diagnostiku Bing-Neelova syndromu
- K potvrzení diagnózy Bing-Neelova syndromu je potřebná: A) histologicky potvrzená infiltrace struktur centrálního nervového systému (CNS) buňkami lymfoplasmocytárního lymfomu (LPL), např. pomocí stereotaktické biopsie. Nebo B) Cytologický průkaz buněk LPL v likvoru bez klinických známek transformace v agresivnější lymfom a průkaz monoklonální B populace v likvoru pomocí metod průtokové cytometrie nebo molekulárně-genetický průkaz klonality pomocí přestavby genu pro imunoglobulin nebo průkaz mutace L265P v genu MYD88.
- Kontrastní vyšetření centrální nervové soustavy MRI s gadoliniem je doporučené provádět před samotným vyšetřením mozkomíšního moku, z důvodu možného falešného zobrazení sycení leptomening. Rozsah MRI vyšetření má být předem zkonzultován s radiologem pro výběr vhodných sekvencí a anatomických oblastí.
C. Doporučení pro léčbu Waldenströmovy makroglobulinémie
- Pacienty s asymptomatickou formou WM je vhodné pouze sledovat. Je doporučeno aktivní pravidelné celoživotní sledování. Sledování probíhá v 3měsíčních intervalech první 3 roky, poté v půlročních intervalech následující 2 roky a poté jednou ročně při stabilním stavu (úroveň důkazu III, stupeň doporučení B).
- Koncentrace IgM samotná není indikací k zahájení léčby (úroveň důkazu IIb, stupeň doporučení B).
- U pacientů s hyperviskozitou je indikovaná výměnná plazmaferéza před samotným zahájením systémové léčby (úroveň důkazu III, stupeň doporučení B).
- Pacienti se symptomatickou WM by měli být léčeni režimem obsahujícím rituximab a/nebo ibrutinib (úroveň důkazu Ib, stupeň doporučení A).
- Monoterapie rituximabem je kontraindikována u pacientů s hyperviskozitou před provedením výměnné plazmaferézy. V případě vysoké koncentrace IgM (> 40 g/l) není monoterapie rituximabem vhodná (úroveň důkazu IV, stupeň doporučení C).
- Pacienty s intolerancí rituximabu, charakterizovanou zhoršujícími se závažnými reakcemi při opakovaných podáních, lze léčit alternativní anti-CD-20 monoklonální protilátkou (např. obinutuzumabem) (úroveň důkazu IV, stupeň doporučení C).
- Režim BR (bendamustin, rituximab) je preferovaným režimem pro nově léčené pacienty s velkou nádorovou masou, hyperviskozitou a potřebou rychlého nástupu léčebné odpovědi (úroveň důkazu IV, stupeň doporučení C).
- Režim DRC (dexamethason, rituximab, cyklofosfamid) je alternativou režimu BR pro nově léčené pacienty s malou nádorovou masou, bez hyperviskozity a nevyžadující rychlý nástup léčebné odpovědi, nebo v případě, že je režim BR rizikový (úroveň důkazu IV, stupeň doporučení C).
- Režim BDR (bortezomib, dexamethason, rituximab), případně B-DRC (bortezomib, dexamethason, rituximab, cyklofosfamid) je preferovaným režimem pro nově léčené pacienty s velkou nádorovou masou, hyperviskozitou a potřebou rychlého nástupu léčebné odpovědi (úroveň důkazu IV, stupeň doporučení C).
- Monoterapie ibrutinibem (nebo zanubrutinibem) je alternativou pro pacienty nevhodné k imunochemoterapii (úroveň důkazu IIa, stupeň doporučení B).
- Kombinaci ibrutinib, rituximab lze zvážit pro léčbu WM s nemutovaným (wild-type) genem MYD88WT. Pro ostatní pacienty s WM toho času chybí dostatek vědeckých důkazů o jednoznačné výhodě kombinační léčby (úroveň důkazu IV, stupeň doporučení C).
- Pacienty v remisi po léčbě je vhodné pravidelně sledovat do symptomatické progrese (úroveň důkazu IV, stupeň doporučení C).
- Udržovací léčba rituximabem po léčbě imunochemoterapii není doporučená u pacientů s WM, kteří dosáhli parciální remisi nebo lepší léčebnou odpověď a/nebo netolerovali rituximab (úroveň důkazu IIb, stupeň doporučení B).
- Léčbu purinovými analogy provází infekční a myelosupresivní komplikace a významně vyšší výskyt sekundárních malignit, a proto není vhodná pro pacienty s nově léčenou WM (úroveň důkazu IIa, stupeň doporučení B).
Léčba druhé a další linie
- Pacienti bez adekvátní odpovědi na režim imunochemoterapie v první linii s přetrvávajícími symptomy nebo pacienti s primárně refrakterní WM mají být léčeni ibrutinibem (nebo zanubrutinibem) (úroveň důkazu IIa, stupeň doporučení B).
- Léčba ibrutinibem je vhodná pro léčbu relapsu pacientů s WM, zejména s přítomností mutace MYD88 (úroveň důkazu Ib, stupeň doporučení A).
- Kombinaci ibrutinib, rituximab lze zvážit pro léčbu WM s nemutovaným (wild-type) genem MYD88WT. Pro ostatní pacienty s WM toho času chybí dostatek vědeckých důkazů o jednoznačné výhodě kombinační léčby (úroveň důkazu IV, stupeň doporučení C).
- Opakování režimu imunochemoterapie první linie je možné u pacientů s pozdním relapsem s dlouhým trváním remise (obvykle čas do zahájení další léčby ≥ 3–4 roky) a dobrou tolerancí předchozího režimu (úroveň důkazu IIa, stupeň doporučení B).
- Pacienti se symptomatickým pozdním relapsem by měli znovu dostat režim obsahující rituximab a/nebo ibrutinib nebo zanubrutinib (úroveň důkazu IIa, stupeň doporučení B).
- Režim obsahující bortezomib je potenciální alternativou léčby symptomatického relapsu WM, preferovány jsou režimy s týdenním podáváním bortezomibu v podkožní formě s cílem předejít neurologické toxicitě, doporučována je profylaxe proti reaktivaci viru pásového oparu (herpes zoster virus – HZV) (úroveň důkazu IIa, stupeň doporučení B).
- V léčbě relapsu jsou používány režimy obdobné jako v léčbě první linie, ale také režimy obsahující bortezomib (bortezomib rituximab +/ – dexamethason), ixazomib, venetoclax, idealsib nebo kombinací obinutuzumab, idealisib. Režimy obsahující purinová analoga (např. fludarabin nebo cladribin spolu s rituximabem, případně i cyklofosfamidem; FR, FCR, CladR) je optimální používat pro léčbu opakovaného relapsu (více než 3. linie léčby) z důvodu vysoké pravděpodobnosti vzniku sekundárního nádoru. Volba režimu vyžaduje komplexní zhodnocení klinického stavu u konkrétního pacienta a také zvážení potenciální možnosti provedení transplantace krvetvorných buněk (SCT) (úroveň důkazu IIa, stupeň doporučení B).
- Pacienty s klinicky asymtomatickým relapsem projevujícím se pouze postupným vzestupem MIg je vhodné pouze sledovat a léčbu zahájit až v případě klinicky významné progrese WM (úroveň důkazu IV, stupeň doporučení C).
- Mladší pacienti s chemosenzitivním relapsem WM jsou kandidáty pro provedení SCT a měli by být diskutováni s transplantačním centrem (úroveň důkazu III, stupeň doporučení B).
D. Doporučení pro léčbu Bing-Neelova syndromu
- Asymptomatické pacienty s Bing-Neelovým syndromem je možné jenom pečlivě sledovat (úroveň důkazu IV, stupeň doporučení C).
- Výběr vhodné léčby a její intenzita se řídí klinickým stavem pacienta, lokalizací a formou postižení, dříve použitou léčbou a schopností podstoupit autologní transplantaci. K léčebným možnostem patří vysoké dávky cytostatik s dobrým průnikem hematoencefalickou bariérou (methotrexát, cytosinarabinosid), nukleosidová analoga ve standardních dávkách (fludarabin, cladribin a bendamustin) a standardní a vyšší dávky ibrutinibu (úroveň důkazu IIb/III, stupeň doporučení B/C).
- U čistě leptomeningeálního postižení lze individuálně zvážit intrathekální chemoterapii. Vhodnější je ale její kombinace s léčebou systémovou (úroveň důkazu IV, stupeň doporučení C).
- Stereotaktická radioterapie v dávkách 30–40 Gy je možnou formou léčby lokalizovaného intraparenchymatózního postižení (úroveň důkazu IV, stupeň doporučení C).
- Intenzivní chemoterapie s konsolidací autologní transplantací by měla být vždy zvažována u mladších pacientů. Optimální přípravný předtransplantační režim není známý. Konsenzuálně jsou preferované režimy používané v léčbě primárních CNS lymfomů (např. režim BCNU/thiotepa) (úroveň důkazu IV, stupeň doporučení C).
V ČR v roce 2021 je použití rituximabu v monoterapii (nebo v kombinaci s ibrutinibem), obinutuzumabu, bortezomibu, bendamustinu, ibrutinibu, ixazomibu, venetoclaxu a idealisibu při léčbě WM možné pouze po schválení revizním lékařem příslušné zdravotní pojišťovny. Zanubrutinib je od roku 2020 registrovaný Evrospkou agenturou pro léčivé přípravky (EMA) pro léčbu relabované/refrakterní Waldenströmovy makroglobulinémie po alespoň jedné linii léčby, nebo pro nově léčené pacienty nevhodné k imunochemoterapii. Zanubrutinib není v roce 2021 v České republice registrovaný.
Standardně jsou v ČR pro léčbu Waldenströmovy makroglobulinémie hrazena zatím pouze klasická cytostatika, rituximab v kombinaci s chemoterapií, kortikoidy a fludarabin.
1. METODICKÉ POSTUPY TVORBY DOPORUČENÍ
Předložené doporučení bylo vypracováno na základě medicíny založené na důkazech s cílem popsat všechny důležité oblasti diagnostiky a léčby Waldenströmovy makroglobulinémie (WM). Úrovně důkazů a stupně doporučení standardně používané v doporučeních jsou uvedeny v tab. 1.
Tab. 1. Úrovně důkazu a stupně doporučení používané ve směrnicích (guidelines) a principech medicíny založené na důkazech (evidence based medicine). 
2. EPIDEMIOLOGIE
WM je vzácně se vyskytující B lymfoproliferativní onemocnění s incidencí 3–3,8/1 milión obyvatel [Wang, 2012; Vos, 2013]. Medián věku v době diagnózy je 63–75 let [Treon, 2009; Teras, 2016; Kastritis, 2015].
3. DIAGNÓZA
Diagnóza WM vyžaduje jak průkaz lymfoplasmocytárních buněk/lymfoplazmocytárního lymfomu (LPL) v kostní dřeni, tak průkaz monoklonálního imunoglobulinu (MIg) typu IgM v séru [Owen, 2003; WHO, 2017]. WM vždy postihuje kostní dřeň, méně často současně i lymfatické uzliny a slezinu. Vyšetření kostní dřeně pomocí trepanobiopsie a/nebo aspirace je proto nevyhnutelné pro stanovení diagnózy. Při imunofenotypizačním vyšetření B lymfocytů je pak pro WM typická přítomnost následujících znaků: CD19, CD20, CD22lo, CD25, CD27 a IgM, zatímco znaky CD5, CD10, CD11c, CD23 a CD103 ve většině případů exprimovány nejsou [Paiva, 2014; Owen, 2014; Jelinek, 2017]. Podpůrným vyšetřením je stanovení přítomnosti mutace L265P v genu MYD88, která bývá detekována přibližně v 90 % případů WM. Samotná mutace MYD88L265P však není specifická pro toto onemocnění [Treon, 2012; Treon, 2015]. Diagnostická kritéria shrnují tab. 2 a 3.
Tab. 2. Diagnostická kritéria WM [Owen, 2003]. ![Diagnostická kritéria WM [Owen, 2003].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/140530882e3d770cd807663232b7e194.jpg)
Tab. 3. Diagnostická kritéria pro MGUS s IgM, symptomatickou a asymptomatickou WM [Owen, 2003]. ![Diagnostická kritéria pro MGUS s IgM, symptomatickou a asymptomatickou WM [Owen, 2003].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/5a4af77710a0390191eb393a10243d5e.jpg)
MGUS – monoklonální gamapatie nejasného významnu, WM – Waldenströmova makroglobulinémie 3.1. Příznaky nemoci
Klinické příznaky u pacientů s WM mohou být velice různorodé. Jsou způsobeny infiltrací kostní dřeně s potlačením fyziologické krvetvorby (anémie, trombocytopenie, neutropenie), dále extramedulární proliferací (lymfadenopatie, organomegalie vč. splenomegalie), dále monoklonálním imunoglobulinem (periferní neuropatie, hyperviskozita, kryoglobulinémie, nemoc chladových aglutininů, asociovaná amyloidóza) a paraneoplasticky (B symptomy, kožní a krvácivé projevy) [Treon, 2015]. Příznaky WM přehledně shrnuje tab. 4 [převzato a upraveno podle Adam, 2007].
Tab. 4. Příznaky Waldenströmovy makroglobulinémie. 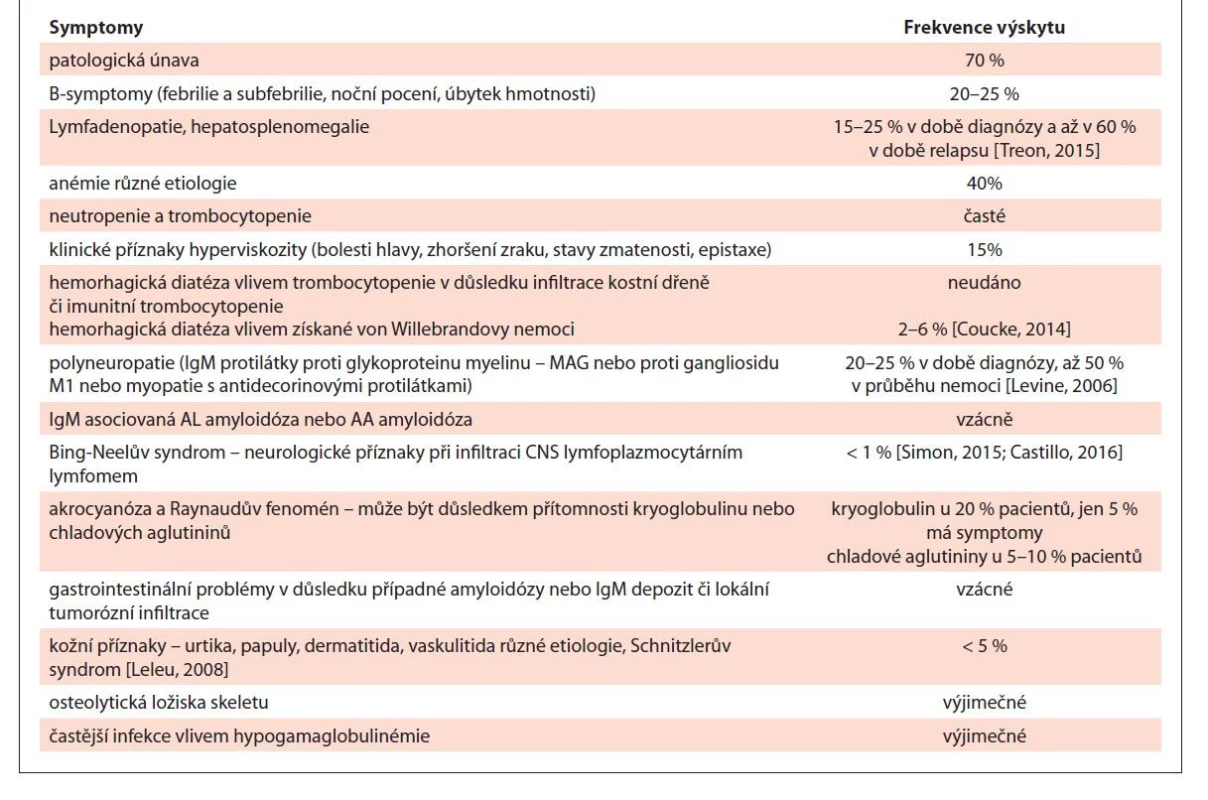
3.2. Doporučená vyšetření
Pokud je stanovena diagnóza WM, pak je doporučeno provést komplexní vyšetření, jehož cílem je zhodnotit rozsah nemoci a detekovat včas případné komplikace. Rozsah těchto vyšetření je uveden v tab. 5.
Tab. 5. Vyšetření prováděná u Waldenströmovy makroglobulinémie. 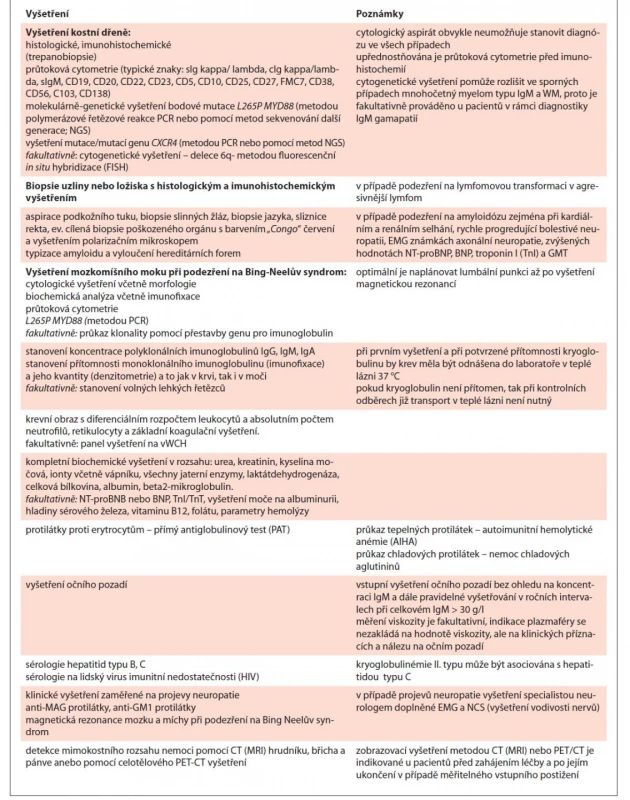
3.2.1. Elektroforéza séra a moče s imunofixací, kvantitativní stanovení imunoglobulinů
Základním vyšetřením u WM je průkaz zvýšené koncentrace monoklonálního, ale i celkového imunoglobulinu typu IgM. Stanovení MIg slouží pro sledování léčebné odpovědi a progrese a nepřímo pro monitorování míry infiltrace kostní dřeně lymfoplazmocytárním lymfomem (LPL). Korelace mezi hladinou MIg a mírou infiltrace kostní dřeně ale není vždy lineární [Treon, 2015]. Ve dvou třetinách případů jsou snížené koncentrace imunoglobulinů tříd IgG a IgA [Hunter, 2010]. Monitorování koncentrace MIg IgM by mělo být prováděno vždy ve stejné laboratoři a za použití stejné metody vyšetření (densitometrie či nefelometrie) [Owen, 2013]. První vyšetření má proběhnout s odběrem vzorků do teplé lázně s vyšetřením na přítomnost kryoglobulinů. Aktivita kryoglobulinů může vést k měření falešně nižších hodnot MIg [Stone, 2009].
Elektroforéza bílkovin séra by měla být vždy doplněná imunofixací, jelikož samostatné kvantitativní měření může přehlédnout nízké koncentrace paraproteinu. Vyšetřování sérových volných lehkých řetězců není rutinně doporučováno. Výjimkou jsou specifické situace, jako je např. podezření na amyloidózu z lehkých řetězců [Leleu, 2011]. Elektroforéza a imunofixace 24hodinového sběru moče může odhalit Bence Jonesovu proteinurii, odlitkovou nefropatii (agregáty volných lehkých řetězců; „free light chain“ FLC a Tamm-Horsfallův protein) či významnou selektivní nebo neselektivní proteinurii v rámci postižení ledvin [Gnemmi, 2012; Vos, 2015].
3.2.2. Cytogenetické vyšetření
Cytogenetické vyšetření není běžně vyžadováno, jelikož u WM nebyly popsány charakteristické cytogenetické aberace, které by potvrdily přítomnost onemocnění, resp. které by měly prognostický význam. Přesto jsou u WM některé cytogenetické změny obvyklé, např. delece chromosomu 6q a trisomie chromozomu 4 [Schop & Fonseca, 2003; Ocio, 2007; Braggio & Fonseca, 2013; Nguyen-Khac, 2013]. Cytogenetické vyšetření může posloužit i v diferenciální diagnostice k odlišení od jiných lymfoproliferací.
3.2.3. Molekulárně genetické vyšetření
Molekulárně genetické vyšetření mutací v genech MYD88 a CXCR4 významně zpřesňují diagnostiku WM. Bodová mutace L265P genu MYD88 je přítomna u 90–95 % případů WM a může být přítomna i u monoklonální gamapatie nejasného významu (MGUS) s IgM přibližně v 50 % případů [Treon, 2012; Jimenéz, 2013; Poulain, 2013]. Méně často (kolem 10 % případů) se vyskytuje u jiných lymfoproliferací, jako je lymfom marginální zóny či chronická lymfocytární leukemie, a nebyla popsána u mnohočetného myelomu [Chapman, 2011; Puente, 2011; Wang, 2011; Troen, 2013]. V 5–10 % případů není tato mutace přítomna (jde o tzv. „wild-type“ (WT) MYD88WT), přičemž její absence je obvykle spojena s horší léčebnou odezvou (např. na ibrutinib) a nepříznivou prognózou [Treon, 2015]. Vzácně byly popsány i alternativní mutace genu MYD88, které se běžně nevyšetřují [Treon, 2015].
Somatické aktivační mutace v genu pro chemokinový receptor CXCR4 provázejí 30–40 % případů WM, téměř vždy v asociaci s mutací genu MYD88 [Treon, 2014]. Byly již popsány desítky různých mutací tohoto genu – typu frameshift (FS) nebo nonsense (NS). Nejčastějšími mutacemi jsou S338X (v 50 % případů) a S338FS (ve 21 % případů) [Lisa MK 2021]. Ve studiích pacientů léčených ibrutinibem představovala přítomnost mutace CXCR4 faktor relativní rezistence [Treon, 2014; Treon, 2015]. Mutace v genu CXCR4 vznikají na subklonální úrovni prakticky vždy po mutaci genu MYD88 (> 90 %), to dává vzniknout 4 různým genotypům – MYD88L265P/CXCR4WT (62 %), MYD88L265P/CXCR4NS (27 %), MYD88L265P/CXCR4FS (11 %) a MYD88WT/ /CXCR4WT (< 10 %) [Lisa MK 2021]. Genotyp určuje biologické chování WM – pacienti s mutací CXCR4 mají agresivnější onemocnění (> IgM, > infiltrace kostní dřeně), pacienti s nemutovaným MYD88 mají zase vyšší riziko transformace [Treon, 2014]. Vysoká míra shody s kostní dření (≥ 90 %) umožňuje testovat uvedené mutace MYD88 a CXCR4 i z periferní krve [Growková, 2017]. Za nejvhodnější vstupní vyšetření pro detekci mutace L265P v genu MYD88 považujeme alelově specifickou PCR (AS PCR) ze vzorku kostní dřeně. Vyšetření mutací na předem CD19-selektované populaci buněk kostní dřeně nebo mononukleárních buňkách periferní krve zvyšuje citlivost metody [Treon, 2020]. Pro vyšetření mutací v genu MYD88 a CXCR4 lze využít i sekvenování nové generace (NGS). V případech negativního výsledku AS-PCR (MYD88WT) může NGS vyloučit alternativní mutace genu MYD88 (non-L265P mutace) [Xu L, 2013].
3.2.4. Zobrazovací vyšetření
Infiltrace kostní dřeně u WM je typicky difuzní. Osteolýza obdobná jako u myelomu se vyskytuje raritně. Bývá ale přítomno extramedulární postižení v podobě doprovodné lymfadenopatie, hepatosplenomegalie a výpotků. Mimokostní postižení bývá zjištěno přibližně u 15 % případů v době diagnózy a až v 60 % případů v období relapsu [Treon, 2009]. K dokumentaci extramedulárního postižení je doporučeným vyšetřením kontrastní CT krku, hrudníku, břicha a pánve. Alternativním doporučeným zobrazovacím vyšetřením je PET/CT. PET/CT je navíc velmi vhodným vyšetřením při podezření na lymfomovou transformaci [Banwait, 2011; Castilo, 2016].
3.3. Speciální vyšetření
Unikátní biochemické a imunologické vlastnosti molekuly monoklonálního imunoglobulinu IgM a biologické chování WM mohou vést k neobvyklým projevům a komplikacím. V následující části upozorňujeme na specifické situace a indikovaná speciální vyšetření ve snaze o jejich časnou detekci a pro výběr správné léčby.
3.3.1. Vyšetření při anémii
Cytopenie a speciálně anémie jsou častým projevem a důvodem k zahájení léčby u pacientů s WM [Adam, 2007]. Příčina anémie u WM je multifaktoriální a mimo přímou infiltraci kostní dřeně buňkami LPL, může být způsobena hemodilucí v rámci hyperviskozity, hemolýzou nebo sideropenií. Pacienti s WM a anémií s velmi nízkou saturací transferinu (< 10 %) nereagující na orální léčbu železem, mohou profitovat z parenterální suplementace železa [Treon, 2013]. Mezi méně časté příčiny anémie patří autoimunitní hemolýza. I když je výsledek přímého antiglobulinového testu pozitivní až u 10 % pacientů s WM, klinicky významná hemolýza se rozvíjí v méně než 5 % [Poulain, 2006]. Mimo standardní vyšetření přímým a nepřímým antiglobulinovým testem je důležité doplnit i vyšetření chladových aglutininů. Nemoc chladových aglutininů (CAD) vede k mírné chronické hemolýze exacerbované chladem, nicméně vzácně může způsobit i těžkou anémii s hladinou hemoglobinu < 70 g/l. CAD se vyskytuje u < 10 % pacientů s WM a bývá asociována s vysokými titry protilátek (obvykle > 1 : 1 000), typicky u izotypu IgM kappa reagujícím s antigenem I/i [Ghobrial, 2012].
3.3.2. Vyšetření při hyperviskózním syndromu a kryoglobulinémii
Biochemické vlastnosti molekuly IgM a vysoké koncentrace MIg typické pro WM významně zvyšují viskozitu séra a vedou k reologickým poruchám v podobě symptomatické hyperviskozity (HVS) u < 15 % pacientů v době diagnózy [Gustine, 2017]. Současně přítomná aktivita kryoglobulinu může ještě více zhoršit projevy HVS. Proto by měla být přítomnost kryoglobulinu vyšetřena vždy v případě HVS. Snaha o korekci anémie podáním transfuzních přípravků může obdobně vést ke zhoršení viskozity. Ke klinickým projevům HVS patří spontánní epistaxe, nové nebo zhoršené bolesti hlavy, rozmazané vidění nelepšící se korekční pomůckou, zhoršení sluchu, tinitus a vertigo [Stone, 2012]. HVS se prakticky nevyskytuje při hodnotách celkového IgM pod 30 g/l [Gustine, 2017; Ghobrial, 2012]. Medián času do rozvoje symptomatického HVS se zkracuje s narůstajícími hodnotami celkového IgM. Při hodnotách v rozmezích 30–40 g/l, 40–50 g/l a 50–60 g/l byl pozorován medián 156, 36 a 32 měsíců do rozvoje symptomatického HVS. Při extrémně vysokých hodnotách celkového IgM > 60 g/l dochází k rozvoji HVS velice časně (medián 3 měsíce) [Gustine, 2017]. Viskozita plazmy nemusí vždy korelovat s klinickými projevy HVS [Castilo, 2016]. Proto je doporučeno vyšetření očního pozadí, které může napomoci k odhalení i časných a bezpříznakových fází hyperviskozity. První změny lze pozorovat v periferních okrajích sítnice v podobě mikrokrvácení a změn vinutí retinálních cév [Menke, 2006]. Změny na sítnici z důvodu HVS jsou indikací k plazmaferéze a časnému zahájení systémové léčby [Castilo, 2016]. Pravidelné vyšetření očního pozadí v intervalu 12 měsíců je doporučeno u pacientů s hodnotami celkového sérového IgM > 30 g/l.
Kryoglobulinémie I. typu je způsobena MIg typu IgM, který v chladu gelifikuje, a tak způsobuje poruchu prokrvení malých cév. Porucha prokrvení vede k projevům podobným Raynaudovu fenoménu. Laboratorně jsou kryoglobuliny (typu I) detekovány až u 20 % pacientů sWM, symptomy se objeví u méně než 5 % [Ghobrial, 2012].
3.3.3. Vyšetření při periferních a centrálních neurologických projevech
Periferní neuropatie (PNP) je u pacientů s WM velice častá. Již v době diagnózy má 20 % pacientů určité projevy PNP a téměř polovinu postihne v průběhu nemoci [Levine, 2006]. Etiologie PNP může být velice různorodá od autoimunitního poškozování, depozice imunoglobulinu, amyloidózy a kryoglobulinémie způsobené MIg až po přímou lymfoplasmocytární infiltraci nervů. Jelikož se PNP vyskytuje u 2–8 % běžné populace, je vždy nutné zvážit i nenádorovou etiologii, jako jsou diabetes mellitus, alkohol, deficit kobalaminu a thiaminu, infekce, radikulopatie, vaskulitidy a chronická demyelinizační polyneuropatie [Martyn and Huges, 1997]. Úzká spolupráce se specialistou neurologem je velice důležitá. Nejtypičtější forma PNP asociované s WM je chronická, měsíce až léta pomalu progredující, symetrická, distální a převážně senzorická nebolestivá demyelinizační PNP s dominujícími projevy v podobě nestability, nerovnováhy, zhoršené citlivosti, třesem a slabostí dolních končetin [Baehring, 2008].
V případě klinického obrazu PNP je vhodné doplnit elektromyografii (EMG) a neurografii (kondukční studie – vyšetření vodivosti nervů). Obvyklý je obraz demyelinizace. Rychle progredující neuropatie s EMG známkami axonálního poškození u pacienta s WM je podezřelá z asociované amyloidózy [D’Sa, 2017]. Dalším diagnostickým krokem je odběr protilátek proti nervovým strukturám, tzv. anti-MAG protilátek. Anti-MAG protilátky v séru bývají pozitivní až v 50 % případů [Baldini, 1994]. Klinicky významné jsou vysoké titry protilátek nebo silně pozitivní výsledky [Nobile-Orazio, 1989]. Protilátky proti gangliosidům anti-GM-1 jsou asociovány s motorickou neuropatií [Vlam, 2015]. Diagnostika PNP u pacientů s WM je velice komplexní, a proto odkazujeme na podrobné mezinárodní konsenzuální doporučení pracovní skupiny IWWM-8 [D’Sa, 2017].
Infiltrace centrálního nervového systému buňkami LPL je velice vzácným projevem WM. Odhadovaný výskyt podle retrospektivních analýz je kolem 1 % pacientů s WM [Simon, 2015; Castillo, 2016]. Na Bing-Neelův syndrom (BNS) je nutné myslet vždy v případě vzniku centrálních neurologických deficitů, bolestí hlavy, při záchvatech, kvantitativních, kvalitativních poruchách vědomí a kognitivních a psychiatrických změnách. BNS může ale probíhat i pod obrazem atypické neuropatie s dominujícím senzorickým deficitem [Simon, 2015]. Nutno upozornit, že klinický průběh může být velice variabilní a až u pětiny pacientů trvá více než rok od prvních neurologických projevů ke stanovení diagnózy [Simon, 2015]. V rámci BNS může být přítomná jak leptomeningeální, tak intraparenchymatózní infiltrace CNS, nebo jejich kombinace. Pro ustanovení diagnózy BNS je dopručena bioptická verifikace CNS kompartmentu vždy, když je to možné. V případě rizikové lokalizace léze nebo při nebioptovatelném postižení je alternativou lumbální punkce. Pro potvrzení diagnózy pomocí lumbální punkce je nutný cytologický průkaz LPL v kombinaci s adekvátní analýzou výsledku vyšetření průtokovou cytometrii s nálezem monoklonálních B lymfocytů nebo molekulárně-genetický průkaz klonality pomocí přestavby genu pro imunoglobulin nebo průkaz mutace L265P v genu MYD88 v likvoru [Minnema, 2017]. Kontrastní magnetická rezonance (MRI) mozku a míchy je zásadní pro lokalizaci postižení, které je přítomné ve většině případů BNS, a k odlišení od jiných procesů [Simon, 2015; Castillo, 2016]. Obvyklým obrazem je difúzní infiltrace leptomeningeálních a perivaskulárních prostor nebo izolovaný, eventuálně multifokální, intraparenchymatózní tumor [Kim, 2009; Drappatz, 2008]. Negativní nález na MRI ale diagnózu BNS nevylučuje [Minnema, 2017]. Kontrastní vyšetření centrální nervové soustavy MRI s gadoliniem je doporučené provádět před samotným vyšetřením mozkomíšního moku, z důvodu možného falešného zobrazení sycení leptomening. Rozsah MRI vyšetření má být předem konzultován s radiologem pro výběr vhodných sekvencí a anatomických oblastí [Minnema, 2017].
3.3.4. Vyšetření při asociované amyloidóze
Amyloidóza je vzácnou komplikací WM, ale s potencionálně závažnými důsledky. Časná a přesná diagnóza je nevyhnutelná pro zlepšení prognózy pacientů. Dominantně převažující formou u WM je amyloidóza z depozice lehkých řetězců (AL amyloidóza). V méně než 5 % případů může jít o formu AA amyloidózy z depozice cirkulujícího sérového amyoidu s odlišnou formou léčby [Terrier, 2008].
V případě systémové formy AL amyloidózy dochází k ukládání amyloidogenních řetězců a tvorbě nerozpustných fibril amyloidu v tkáních a orgánech. Typickými cílovými orgány jsou ledviny, srdce, játra a periferní nervy.
Zásadní je odhalení amyloidózy před rozvojem nezvratného orgánového poškození. Citlivými ukazateli orgánového poškození jsou natriuretický peptid B (BNP) nebo N-terminální fragment BPN (NT-proBNP) a troponin I pro srdce, albuminurie pro ledviny, zvýšení alkalické fosfatázy (ALP) a glutamyltranferázy (GMT) pro játra [Merlini, 2013]. Monitorování těchto ukazatelů lze využít v rámci pravidelného skreeningu. Rychle se zhoršující bolestivá polyneuropatie tenkých vláken dolních končetin provázená vegetativní neuropatií nebo EMG známky axonálního poškození jsou podezřelé z přítomnosti amyloidózy [Rajkumar, 1998].
3.3.5. Vyšetření při krvácivých projevech
V případě spontánního krvácení nebo při časném krvácení po operaci nebo úrazu u pacienta s WM je nutno mimo trombocytopenii a hyperviskozitu pomýšlet i na diagnózu získané von Willebrandovy choroby (vWCH). U pacientů s WM s vysokými hodnotami IgM, hyperviskozitou a kryoglobulinémií je riziko vWCH vyšší [Hivert, 2012]. V případě klinického podezření na získanou vWCH se vyšetřují plazmatické hladiny von Willebrandova faktoru (vWf), fVIII a funkční aktivita ristocetin kofaktoru (vWf: RCo).
4. PROGNÓZA
Waldenströmova makroglobulinémie je nemoc s poměrně příznivou prognózou. Podle dat Evropského registru v letech 2000 až 2014 bylo 10leté celkové přežití 69 % [Buske, 2018]. Tato práce navíc nereflektuje dostupnost nových vysoce účinných léků a jejích kombinací [Treon, 2015; Treon, 2018; Treon, 2019; Buske 2021, Tam, 2018].
4.1. Riziko progrese asymptomatické Waldenströmovy makroglobulinémie
Jedna třetina pacientů s WM je v době diagnózy asymptomatických. Medián doby do progrese se pohybuje od 5–10 let [Kyle 2012, Dhodapkar 2009, Pophali 2019].
Riziko progrese do symptomatické nemoci lze odhadnout podle nového modelu rozdělujícího pacienty do tří rizikových skupin. Podle tohoto modelu jsou IgM ≥ 45 g/l, infiltrace kostní dřeně LPL ≥ 70 %, beta2-mikroglobulin ≥ 4 mg/l a albumin ≤ 35 g/l nezávislé prediktory progrese. U pacientů vysokého rizika je medián doby do progrese 1,8 roku, u středního rizika 4,8 roku a nízkého 9,3 roku. Pro výpočet je k dispozici webová aplikace (www.awmrisk.com) [Bustoros 2019]. Model může pomoci identifikovat vysoce rizikové asymptomatické pacienty, kteří mohou vyžadovat četnější sledování. Další nezávislý prediktor progrese je přítomnost nemutované WT formy genu MYD88WT [Bustoros 2019].
4.2. Prognóza symptomatické Waldenströmovy makroglobulinémie
Osud nemocných s WM jevelmi různorodý a více informací o prognóze u konkrétního pacienta nám mohou poskytnout prognostické indexy. Nejvýznamnějším z nich je Mezinárodní prognostický skórovací systém pro WM (IPSSWM), který je založen na hodnocení 5 klíčových parametrů, kterými jsou: věk, hodnota hemoglobinu, počet trombocytů, sérové koncentrace beta2-mikroglobulinu (B2-M) a MIg [Morel, 2009], podrobnosti jsou uvedeny v tab. 6. Skórovací systém IPSSWM je určený pro symptomatickou formu WM. Kombinace vysokého rizika podle IPSSWM a zvýšené laktát dehydrogenázy může pomoci identifikovat podskupinu vysoce rizikových pacientů s celkovým přežitím < 3 roky [Kastritis, 2009]. Nový revidovaný skórovací systém z roku 2019 stratifikuje symptomatickou WM do 5 prognostických skupin na základě věku (≤ 65 let, 66–75 let, ≥ 76 let), B2-M ≥ 4 mg/l, albuminu < 35 g/l a LDH ≥ 250 IU/l. Seřazeně od nejnižšího k nejvyššímu riziku je v jednotlivých skupinách frekvence úmrtí v souvislosti s WM ve 3 letech 0, 10, 14, 38 a 48 % (p < 0,001) a 10 leté přežití 84, 59, 37, 19 a 9 % (p < 0,001) [Kastritis, 2019]. Tento systém bude vyžadovat další validaci před rutinním klinickým využitím.
Tab. 6. Mezinárodní prognostický skórovací systém pro nemocné se symptomatickou Waldenströmovou makroglobulinémií – IPSSWM [Morel, 2009]. ![Mezinárodní prognostický skórovací systém pro nemocné se symptomatickou Waldenströmovou
makroglobulinémií – IPSSWM [Morel, 2009].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/94dcd3d24ca9a0e331eb56b29db9e2e6.jpg)
5. VZOROVÝ ZÁPIS DIAGNÓZY WM
Doporučený zápis diagnózy WM by měl být v následujícím formátu: C88.0 Morbus Waldenström / Waldenströmova makroglobulinémie; datum diagnózy, riziko dle IPSSWM nízké/intermediární/vysoké (v případě symptomatické nemoci); gen MYD88 mutovaný/nemutovaný (dopručeně, popis mutace např. L265P); gen CXCR4 mutovaný/nemutovaný (volitelně, popis mutace např. S338X); rozsah postižení (CT, MRI nebo PET/CT trupu v případě symptomatické nemoci); indikace k léčbě (hyperviskozita, nemoc chladových aglutininů, symptomatická kryoglobulinemie, IgM mediovaná neuropatie, lymfadenopatie, organomegalie, anémie s hemoglobinem < 100 g/l, trombocytopenie < 100×109/l).
6. DOPORUČENÍ PRO DIAGNOSTIKU WM
- Monitorování koncentrace MIg IgM by mělo být prováděno v jedné laboratoři a za použití vždy stejné metody.
- Vyšetření chladových aglutininů a kryo - globulinu je doporučené v době diagnózy a u pacientů s klinickými projevy poruch prokrvení a/nebo vaskulitidy či laboratorními projevy hemolýzy.
- Vyšetření kostní dřeně, nejlépe trepanobiopsie s adekvátní analýzou metodou průtokové cytometrie, je nezbytné pro stanovení diagnózy WM.
- Biopsie tkáně je doporučována u všech pacientů se suspektní histologickou transformací (u části nemocných s WM může dojít k transformaci do DLBCL).
- Testování bodové mutace L265P v genu MYD88 je doporučeno u všech pacientů se zvažovanou diagnózou WM. Preferovaným vyšetřením je alelově specifická PCR z aspirátu kostní dřeně.
- U pacientů se symptomatickou periferní neuropatií je doporučováno vyšetření specifických protilátek proti glykoproteinu myelinu nebo proti gangliosidu M1 (anti-MAG a anti-GM-1 protilátek).
- Neurofyziologické testování pomocí EMG a neurografie (kondukční studie) je doporučeno při podezření na neuropatii a slouží k určení typu nervového poškození a usměrňuje další diagnostiku.
- Provedení CT nebo MRI vyšetření (hrudníku, břicha, pánve) nebo celotělového PET/CT je je vhodné zvažit u všech symptomatických pacientů před zahájením léčby.
- Pro hodnocení rizika u symptomatických pacientů slouží mezinárodní prognostický skórovací systém pro nemocné s Waldenströmovou makroglobulinémií – IPSSWM
6.1. Doporučení pro diagnostiku Bing-Neelova syndromu
K potvrzení diagnózy Bing-Neelova syndromu je potřebná: A) histologicky potvrzená infiltrace struktur centrálního nervového systému (CNS) buňkami lymfoplasmocytárního lymfomu (LPL), např. pomocí stereotaktické biopsie. Nebo B) Cytologický průkaz buněk LPL v likvoru bez klinických známek transformace v agresivnější lymfom a průkaz monoklonální B populace v likvoru pomocí metod průtokové cytometrie nebo molekulárně-genetický průkaz klonality pomocí přestavby genu pro imunoglobulin nebo průkaz mutace L265P v genu MYD88.
Kontrastní vyšetření centrální nervové soustavy MRI s gadoliniem je doporučené provádět před samotným vyšetřením mozkomíšního moku, z důvodu možného falešného zobrazení sycení leptomening. Rozsah MRI vyšetření má být předem zkonzultován s radiologem pro výběr vhodných sekvencí a anatomických oblastí.
7. INDIKACE K LÉČBĚ
Současné léčebné možnosti mají potenciál dosáhnout dlouhotrvající léčebné odpovědi (remise nemoci) u velkého počtu pacientů. U většiny pacientů však není možná úplná eliminace maligního klonu. Nemoc obvykle po dosažení remise, trvající řádově měsíce či roky, opět recidivuje a vyžaduje další léčbu. Proto se u Waldenströmovy makroglobulinémie v současné době doporučuje asymptomatické nemocné pouze sledovat a se zahájením léčby vyčkat až do naplnění konsenzuálních kritérií uvedených níže [Leblond, 2016; D’Sa, 2017; Minnema, 2017].
Kritéria pro zahájení léčby:
- Klinické indikace pro zahájení léčby:
- opakované teploty, noční poty a necílený úbytek hmotnosti > 10 % během 6 měsíců a patologická únava
- hyperviskozita (vč. asymptomatických změn na očním pozadí)
- symptomatická či bulky (≥ 5 cm v největším průměru) lymfadenopatie
- symptomatická hepato/splenomegalie
- symptomatická organomegalie či infiltrace tkání/orgánů (vč. symptomatické formy Bing-Neelova syndromu)
- periferní neuropatie způsobená WM (symptomatická a progredující)
- symptomatická kryoglobulinémie
- Laboratorní indikace pro zahájení léčby:
- nemoc chladových aglutininů (chladová hemolytická anémie)
- autoimunitní hemolytická anémie či trombocytopenie
- nefropatie způsobená WM
- amyloidóza způsobená WM
- koncentrace hemoglobinu pod 100 g/l nebo počet trombocytů pod 100×109/1
Koncentrace monoklonálního imunoglobulinu IgM není sama o sobě indikací k zahájení léčby, nicméně pokud by koncentrace dosáhla 50 g/l, doporučuje se pátrat po možných projevech hyperviskozity (krvácení z nosu a z dásní, zhoršení vizu, bolesti hlavy, závratě, ataxie a změny psychiky). Vždy je nutné provést vyšetření očního pozadí. Pokud jsou přítomny klinické příznaky hyperviskozity, je akutně indikována plazmaferéza.
8. STRATEGIE LÉČBY
Skutečnost, že WM je velmi vzácným onemocněním s relativně dlouhým přežitím nemocných, limituje organizování velkých klinických studií. Proto informace o účinnosti léčby máme z menších studií, které obvykle hodnotí pouze počet léčebných odpovědí a délku remise, zatímco studie fáze III, které by srovnávaly vliv léčebných postupů na délku celkového přežití, jsou ojedinělé. Přehled vybraných publikovaných studií je uveden v tab. 7.
Tab. 7. Přehled režimů u nově léčené a relabované/refrakterní Waldenströmovy makroglobulinémie (WM). 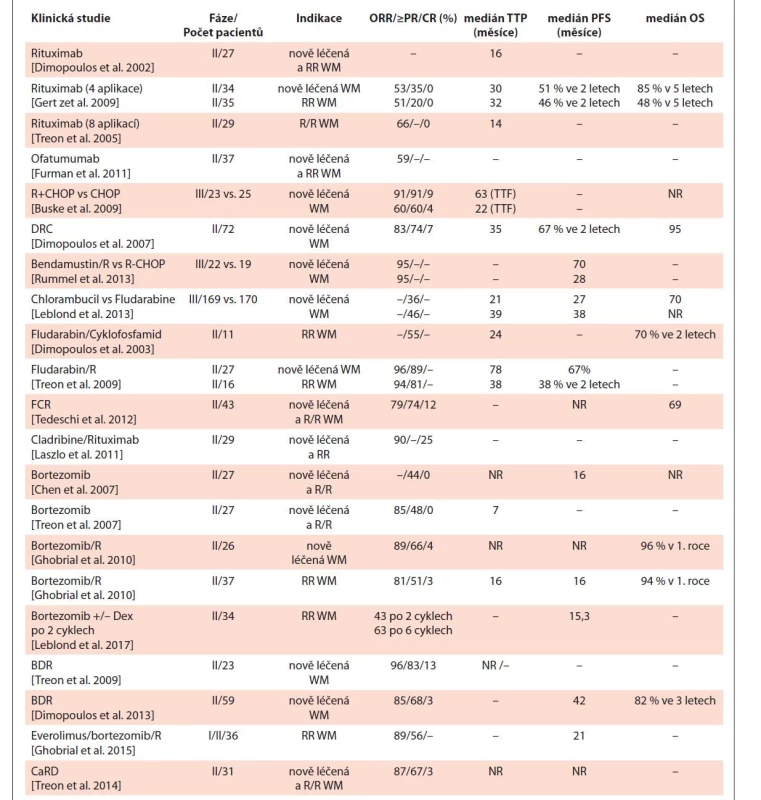
CR – kompletní remise, NR – neuvedeno, ORR – celkový podíl odpovědí, OS – celkové přežití, PFS – přežití bez progrese, PR – parciální remise, RR, R/R – refrakterní nebo relabující, TTF – čas do selhání léčby, TTP – čas do progrese, WM – Waldenströmova makroglobulinémie Tab. 7 – pokračování. Přehled režimů u nově léčené a relabované/refrakterní Waldenströmovy makroglobulinémie (WM). 
CR – kompletní remise, NR – neuvedeno, ORR – celkový podíl odpovědí, OS – celkové přežití, PFS – přežití bez progrese, PR – parciální remise, RR, R/R – refrakterní nebo relabující, TTF – čas do selhání léčby, TTP – čas do progrese, WM – Waldenströmova makroglobulinémie Strategie léčby v moderní hematologii respektuje, že WM je zpravidla neagresivní pozvolné onemocnění s dlouhodobým přežitím (10leté celkové přežití 69 %) při použití dostupné léčby (tato data nereflektují recentní dostupnost ibrutinibu) [Buske, 2018]. Lze tedy pozorovat trend ke zvýšení bezpečnosti režimů modulací intenzity léčby s ohledem na celkový stav nemocného. Ibrutinib je např. lékem, který ma velmi akceptovatelný toxický profil, jde o monoterapii s perorální cestou aplikace. Onemocnění dlouhodobě stabilizuje, přestože počet kompletních remisí je limitovaný. Rovněž postupně dochází k vyloučení léků, které způsobují závažné nežádoucí účinky nebo způsobují vyšší četnost sekundárních nádorů, což je např. případ fludarabinu.
8.1. Nově léčená Waldenströmova makroglobulinémie
Hlavním cílem léčby je dlouhodobá kontrola symptomů nemoci při zachování kvality života. Anti-CD20 protilátka rituximab a její kombinace tvoří nadále pilíř léčby pacientů s WM [Buske, 2013; Leblond, 2016; Kapoor, 2017; Kastritis, 2018; Castillo 2020, Kaščák, 2019]. Přidání rituximabu k chemoterapii významně zvyšuje procento léčebných odpovědí a jejich trvání [Buske, 2009]. Několik retrospektivních analýz potvrdilo pozitivní vliv rituximabu na délku bezpříznakového období a celkové přežití [Buske, 2018; Olszewski, 2017; Castillo, 2017]. Monoterapie alkylačními cytostatiky a purinovými analogy je málo účinná a s ohledem na dostupnost nových účinných a bezpečnějších léků není vhodná. Ibrutinib jak v monoterapii, tak v kombinaci s rituximabem představuje vysoce účinnou léčebnou alternativu k imunochemoterapii [Treon, 2015; Treon, 2018; Treon, 2019; Buske 2021]. Léčba ibrutinibem se zdá být méně vhodná u pacientů s IgM asociovanou amyloidózou [Pika, 2018]. Kombinace bortezomibu s dexamethasonem a rituximabem nebo dexamethasonem, rituximabem a cyklofosfamidem můžou být další léčebnou alternativou a jsou experty doporučovány v případě sekundární amyloidózy [Gavriatopolou, 2017; Buske, 2020; Treon, 2020]. Léčbu na bázi bortezomibu je ale nutno rozvážit u pacientů s preexistující neuropatií.
Určující pro výběr vhodné léčby je rozsah a charakter nádorového postižení, požadovaná rychlost dosažení léčebné odpovědi, věk pacienta a mutační status v genech MYD88 a CXCR4. Mutační status určuje rychlost nástupu léčebné odpovědi, její hloubku a přežití bez progrese, nejvýznamněji v případě léčby ibrutinibem v monoterapii [Treon, 2015; Dimopoulos 2017; Treon, 2018; Treon, 2019]. V přehledné tabulce jsou uvedeny publikovaná data o efektu mutací na výsledky léčby pomocí inhibitorů Brutonovy tyrosinkinázy, proteasomových inhibitorů a kombinace rituximabu a alkylačních cytostatik tab. 8. Léčebný algoritmus pro nově léčenou symptomatickou WM je uveden ve schématu 1.
Tab. 8. Efekt mutací v genech MYD88 a CXCR4 na výsledky léčby Waldenströmovy makroglobulinémie. 
Komentář k BTKi a jejich kombinacím:
Ibrutinib u pacientů s WM s genotypem MYD88L265P/CXCRWT má lepší léčebné výsledky v podobě rychlosti nástupu léčebné odpovědi, její hloubky a PFS. Pacienti s WM s genotypem MYD88L265P/CXCR4MUT mají prodlevu 4–5 měsíců do dosažení hluboké odpovědi (≥ PR). U pacientů s WM s MYD88WT nejsou dosahované hluboké léčebné odpovědi a trvání odpovědi je krátké (PFS < 5 měsíců). Zdá se že kombinace ibrutinibu a rituximabu dosahuje u pacientů s WM s MYD88WT významné aktivity a má potenciál překonat její negativní prognostický dopad.
Zanubrutinib má větší protinádorovou aktivitu a vede k hlubším léčebným odpovědím u MYD88WT a CXCR4MUT ve srovnání s ibrutinibem. Acalabrutinib má významnou protinádorovou aktivitu u MYD88WT.
BR – bendamustin, rituximab, BTKi – ihibitory Brutonove tyrosinkinázy, CR – kompletní remise, DRC – dexamethason, rituximab, cyklofosfamid, MUT – mutovaný, ORR – celkové léčebné odpovědi, NR – nedosaženo, OS – celkové přežití, PFS – bezpříznakové přežití, TTNT – čas do další léčby, PFS – bezpříznakové přežití, R – rituximab, R/R – relaps, refrakterní nemoc, SD – stabilní choroba, WT – wild- -type = nemutovanýTab. 8 – pokračování. Efekt mutací v genech MYD88 a CXCR4 na výsledky léčby Waldenströmovy makroglobulinémie. 
Komentář k léčbě na bázi alkylačních cytostatík:
CXCR mutační stav neměl dopad na ORR, PFS u pacientů léčených režimy BR a DRC. MYD88 stav neměl dopad na ORR. U pacientů s MYD88 WT byl pozorován trend ke kratšímu PFS ve dvou retrospektivních studiích, nicméně v jedné prospektivní studii tento trend pozorován nebyl.
BR – bendamustin, rituximab, BTKi – ihibitory Brutonove tyrosinkinázy, CR – kompletní remise, DRC – dexamethason, rituximab, cyklofosfamid, MUT – mutovaný, ORR – celkové léčebné odpovědi, NR – nedosaženo, OS – celkové přežití, PFS – bezpříznakové přežití, TTNT – čas do další léčby, PFS – bezpříznakové přežití, R – rituximab, R/R – relaps, refrakterní nemoc, SD – stabilní choroba, WT – wild- -type = nemutovanýSchéma 1. Nově léčená Waldenströmova makroglobulinémie. 
* nutné schválení revizním lékařem dle § 16 zákona č. 48/1997 Sb.
** Zanubrutinib je od roku 2020 registrovaný Evrospkou agenturou pro léčivé přípravky (EMA) pro léčbu relabované/refrakterní Waldenströmovy makroglobulinémie po alespoň jedné linii léčby, nebo pro nově léčené pacienty nevhodné k imunochemoterapii.
Zanubrutinib není v roce 2021 v České republice registrovaný.8.1.1. Monoterapie rituximabem
Monoterapií rituximabem je dosahováno do 40 % celkových léčebných odpovědí po 4 aplikacích a 65 % po 8 aplikacích s trváním odpovědí od 8 do 29 měsíců [Gertz, 2004; Treon, 2005; Dimopoulos, 2002]. Nástup léčebné odpovědi je velice pozvolný (medián 7 měsíců) [Treon, 2005]. Monoterapie rituximabem tedy není vhodná pro pacienty vyžadující urychlenou kontrolu nemoci. Až u poloviny pacientů dochází v prvních měsících léčby k přechodnému nárůstu IgM (≥ 25 %), takzvanému vzplanutí „IgM flare“ [Treon, 2005]. Toto může vést vzácně až k projevům hyperviskozity, zhoršit neuropatii, kryoglobulinémii nebo nemoc chladových aglutininů [Treon, 2004]. Proto se u pacientů s vysokými koncentracemi IgM > 40 g/l doporučuje provést plazmaferézu před prvním podáním rituximabu. Obecně u pacientů s hodnotami celkového IgM > 40 g/l není monoterapie rituximabem vhodná. Až u 7 % pacientů s WM léčených rituximabem jak v monoterapii, tak v kombinační léčbě byly zaznamenány významné infuzní reakce vedoucí k předčasnému ukončení léčby. Intolerance rituximabu je charakterizována horšícími se infuzními reakcemi. Část pacientů netolerujících rituximab byla posléze bezpečně léčená ofatumumabem [Castillo, 2015]. Ofatumumab ale již není dostupný na evropském trhu. Alternativou s nižším rizikem reakcí může být subkutánní rituximab (ve studii podán úspěšně u dvou pacientů s rozvojem infuzní reakce po intravenózním rituximabu) [Kersten, 2021]. V prospektivní studii fáze 2 u pacientů s WM léčených kombinačním režimem s obinutuzumabem nebyly zaznamenány žádně závažné infuzní reakce, celkově byl výskyt infuzních rekací (všechny lehkého stupně, ≤ 2) velmi nízký (5 %) [Tomowiak, 2021]. Pozitivní zkušenosti s obinutuzubam v kombinaci s chemoterapií u pacientky s anamnézou život ohrožující reakce při léčbě rituximabem dokladuje i recentní původní práce kolektivu Adam et al. 2021 [Adam, 2021]. U pacientů s intoleranci rituximabu lze zvážit léčbu obinutuzumabem. Monoterapii rituximabem lze zvážit pro specifické případy léčby imunologických komplikací IgM, jako je symptomatická kryoglobulinemie, na kortikoidy rezistentní významná hemolytická anemie, IgM asociovaná progredující neuropatie [Kastritis, 2018; Leblond, 2016; Kapoor, 2017]. U pacientů s rychle progredující těžší formou demyelinizační IgM asociované polyneuropatie, kteří mohou profitovat z rychlejšího nástupu léčebné odpovědi a její hloubky, má být alternativně zvážená léčba imunochemoterapií (např. režim bendamustin, rituximab alternativně dexamethason, rituximab, cyklofosfamid), nebo ibrutinibem v monoterapii či v kombinaci s rituximabem [Treon, 2016; Castellani 2020].
8.1.2. Kombinované režimy imunochemoterapie
Nebyl doposud stanoven jednotný optimální režim léčby a při jejím výběru jsou důležité rozdíly v profilu nežádoucích účinků. Predispozice k neuropatickým komplikacím u pacientů s WM brání léčbě thalidomidem, vinca-alkaloidy a za méně vhodné lze považovat i intenzifikované podání bortezomibu. Léčba antracyklinovými režimy je zatížená vyšším výskytem infekčních komplikací a má kardiotoxické účinky. Bez rizik není ani léčba purinovými analogy, kterou provází infekční, myelosupresivní komplikace a vyšší výskyt sekundárních malignit. U nově léčených pacientů jsou doporučovány režimy s akceptovatelným poměrem účinnosti a profilem nežádoucích účinků režim rituximab, cyklofosfamid, dexamethason (DRC) a kombinace bendamustin, rituximab (BR) [Kaščák, 2016].
Pomocí režimu dexamethason, rituximab a cyklofosfamid u pacientů s nově léčenou WM bylo dosaženo 83 % léčebných odpovědí, z toho 7 % kompletních remisí. Medián do nástupu léčebné odpovědi byl 4 měsíce. Tolerance režimu byla velmi dobrá [Dimopoulos, 2007]. Medián do zahájení další léčby byl až 51 měsíců. Medián celkového přežití 95 měsíců. [Kastritis, 2015]. Pravděpodobnost celkového přežití v 8 letech pro skupinu nízkého, středního a vysokého rizika podle IPSSWM byla 100 %, 55 % a 27 % (p = 0,005) [Dimopoulos, 2007; Kastritis, 2015].
Režim bendamustin (90 mg/m2), rituximab byl srovnán s režimem R-CHOP ve studii fáze 3. V obou ramenech bylo dosaženo shodně 95 % léčebných odpovědí. Medián přežití bez progrese v trvání téměř 70 měsíců vyšel ve prospěch režimu BR [Rummel, 2013]. Snížení počtu cyklů ze šesti na čtyři s redukcí dávky bendamustinu na 70 mg/m2/den nemělo negativní vliv na procento a hloubku léčebných odpovědí v jedné retrospektivní analýze [Castillo, 2016]. Ve dvou retrospektivních pracích byl zaznamenán trend delšího bezpříznakového přežití u režimu BR ve srovnání s DRC u neléčené WM. Tento trend ale nevedl k delšímu nemoc specifickému přežití [Castillo 2018, Paludo 2018].
Při výběru vhodného režimu je doporučené řídit se klinickými projevy, rozsahem nádorového postižení a požadavkem na rychlost dosažení léčebné odpovědi. Velkou nádorovou masu lze předpokládat u pacientů s těžkými cytopeniemi, s masivní organomegalií, lymfadenopatií anebo hyperviskozitou. Režim DRC je vhodný pro symptomatické pacienty s menším nádorovým postižením nevyžadující urychlený nástup léčebné odpovědi. Pro pacienty s větší nádorovou zátěží vyjádřenou vysokým rizikem podle IPSSWM (významná anémie, trombocytopenie, vysoké IgM a zvýšený B2M) se jeví režim DRC jako méně vhodný. Režim BR je vhodnou volbou pro pacienty s větším nádorovým postižením a potřebou rychlého nástupu léčebné odpovědi [Leblond, 2016; Kapoor, 2017; Kastritis, 2018]. Dávku bendamustinu a/nebo počet cyklů BR je vhodné přizpůsobit podle individuálních charakteristik pacienta a tolerance léčby [Castillo, 2016; Kastritis, 2018].
8.1.3. Kombinované režimy proteasomového inhibitoru a rituximabu
V prospektivních klinických studiích byly hodnocené kombinace bortezomibu, ixazomibu a karfilzomibu v kombinaci s rituximabem nebo imunochemoterapií u nově léčené WM [Treon, 2009; Ghobrial, 2018; Dimopoulos, 2013 Treon 2014; Castillo, 2018; Buske, 2020]. Ve studiích s bortezomibem podávaným 2× týdně a intravenózně byl zaznamenán významný výskyt závažné periferní neuropatie (stupně ≥ 3), která vedla k ukončení léčby u významného počtu pacientů (> 60 %) [Treon, 2009]. Týdenní podávaní bortezomibu a podkožní aplikace vedly k výraznému snížení výskytu závažné neuropatie [Ghobrial, 2010; Dimopoulos, 2013; Buske, 2020]. V recentní prospektivní randomizované klinické studii fáze 2 u nově léčené WM byla srovnávaná účinnost režimu DRC s přidáním subkutánního bortezomibu (B-DRC) jednou týdně s režimem DRC [Buske, 2020]. Rozdíl v odhadovaném přežití bez progrese ve 24 měsících sice nedosáhl statistické významnosti, ale výskyt významné toxicity (stupně ≥ 3) byl identický v obou ramenech a výskyt závažné neuropatie (stupně ≥ 3) byl pouze 2 % v experimentálním ramenu. Kombinace s karfilzomibem a ixazomibem představují režimy bez rizika rozvoje závažné neuropatie [Treon, 2014; Castillo, 2018]. Zvýšená pozornost je vyžadována v případě karfilzombu a jeho kardiovaskulárních nežádoucích účinků. Pomocí režimů s proteasomovým inhibitory jsou léčebné odpovědi dosahovány rychle (medián času do první odpovědi 2–3 měsíce) [Dimopoulos, 2013; Castillo, 2018; Buske, 2020]. Pro vybrané pacienty s potřebou rychlejší kontroly nemoci nebo specifickými komplikacemi jako asociovaná amyloidóza může být léčba proteasomovými režimy výhodná.
8.1.4. Inhibitory Brutonovy tyrosinkinázy
V současné době jsou registrovány pro léčbu WM dva inhibitory Brutonovy tyrosinkinázy, ibrutinib jako přestavitel první generace a zanubrutinib představitel druhé generace inhibitorů. Ibrutinib a zanubrutinib v monoterapii je indikován k léčbě pacientů s WM, kteří již podstoupili alespoň jednu předchozí terapii, nebo i v první linii u pacientů, u nichž není vhodná immunochemoterapie. Ibrutinib v kombinaci s rituximabem je indikovaný pro léčbu pacientů s nově diagnostikovanou i dříve léčenou WM. Registrace ibrutinibu v monoterapii u WM proběhla na základě výsledků studie fáze 2 u dříve léčených pacientů [Treon, 2015]. Finální analýza této studie ukázala dlouhotrvající léčebné výsledky s 5letým bezpříznakovým přežitím (PFS) 54 % a celkovým přežitím (OS) 87 % [Treon, 2015, Treon 2019]. V navazující studii s ibrutinibem u nově léčené WM byla léčebná odpověď dosažena u 100 % léčených, z toho 87 % ≥ PR a 4letým PFS 76 % a OS 100 % [Treon, 2018; Castillo, 2021]. Ibrutinib zvyšuje riziko krvácení, hypertenze a arytmie. Zvýšená pozornost je proto nutná u pacientů s preexistující arytmií a zvýšeným rizikem krvácení (např. antikoagulační léčba). Ibrutinib je nutné vysadit 3–7 dní před plánovaným operačním zákrokem. Přerušení léčby ibrutinibem běžně provází přechodný vzestup IgM a až u 20 % pacientů projevy syndromu z vysazení (únava, teploty a noční pocení). Projevy syndromu lze zmírnit podáváním prednisonu v dávce 10 mg 2× denně [Castillo, 2018].
Mutační status v genech MYD88 a CXCR4 je nezávislým prediktorem odpovědi při léčbě ibrutinibem v monoterapii [Treon, 2015, Treon 2019, Treon 2018]. Pacienti s genotypem MYD88L265P/CXCR4WT ve srovnání s pacienty s genotypem MYD88L265P/CXCR4MUT dosahují hlubší léčebné odpovědi (ORR/≥PR 100/97 % vs. 86/63 %) o 4–5 měsíců dříve a s delším trváním odpovědí (5leté PFS 71 vs. 34 %) [Treon 2019]. V případě nemutované varianty genu MYD88 (wild-type MYD88) je při léčbě ibrutinibem dosaženo podstatně méně léčebných odpovědí (ORR 50 %), nejsou dosahovány hluboké léčebné odpovědi (≥ PR: 0 %) a jejich trvání je krátké (medián PFS: 5 měsíců) [Treon, 2015; Dimopoulos, 2017 Treon 2019].
Ibrutinib je nově registrován pro léčbu symptomatické WM v kombinaci s rituximabem. Registrace proběhla na základě výsledku studie fáze 3 u dříve léčené i neléčené WM [Dimopoulos, 2018]. Klíčovým kritériem pro kohortu RR WM byla senzitivita k předchozímu režimu s rituximabem. Proti kontrolnímu ramenu rituximab, placebo byly kombinací rituximab, ibrutinib dosažené hluboké léčebné odpovědi nezávislé na předchozí léčbě nebo genotypu. U prognosticky nepříznivého genotypu MYD88WT/CXCR4WT bylo dosaženo 82 % léčebných odpovědí s benefitem bezpříznakového přežití proti ramenu rituximab, placebo (HR [95% CI]: 0,29) [Buske, 2020]. Kombinační léčba nezvyšuje toxicitu léčby.
Registrace zanubrutinibu v monoterapii u WM proběhla na základě výsledků studie fáze 3 u dříve léčených a neléčených pacientů s MYD88L265P WM [Tam, 2020]. Ve srovnání s ibrutinibem bylo v ramenu se zanubrutinibem stejné zastoupení léčebných odpovědí (93 % a 94 %) a hlubokých léčebných odpovědí (≥ PR 77 % a 78 %). V ramenu se zanubrutinibem bylo vyšší zastoupení VGPR/CR ve srovnání s ibrutinibem (28,4 vs. 19,2 %), nedosáhlo ale statistické významnosti při mediánu sledování 19,4 měsíce (p = 0,09). Nebyl rozdíl ani při jednoletém bezpříznakovém a celkovém přežití. Nejdůležitějším výstupem studie bylo potvrzení nižší toxicity zanubrutinibu. Léčba zanubrutinibem byla ve srovnání s ibrutinibem provázená nižším výskytem nehemetologických nežádoucích účinků (všech stupňů/stupeň ≥ 3), jako jsou fibrilace síní (2 vs. 15 % / 0 vs. 4 %), hypertenze (11 vs. 17 % / 6 vs. 12 %), krvácení (49 vs. 58 % / 6 vs. 8%), periferní otoky, průjmy a pneumonie. Výskyt neutropenie byl nižší u pacientů léčených ibrutinibem, ale celkový výskyt infekcí byl stejný [Garcia-Sanz, 2020]. Dalším klíčovým zjištěním byla demonstrace účinnosti zanubrutinibu u pacientů s nemutovaným MYD88WT (hodnoceno v samostatné kohortě). U této prognosticky nepřiznivé skupiny bylo dosaženo 81 % léčebných odpovědí, z toho 50 % hlubokých (≥ PR), 27 % VGPR a s 12měsíčním bezpříznakovým přežitím 72,4 % [Garcia-Sanz, 2020]. V pokročilých fázích klinického testování je druhá generace inhibitorů Brutonovy tyrosinkinázy (acalabrutinib, tirabrutinib).
8.1.5. Kandidát autologní transplantace
Autologní transplantace (ASCT) představuje důležitou léčebnou alternativu v léčbě opakovaného relapsu mladších pacientů s WM [Kaščák, 2016]. Včasný sběr v době nejmenšího nádorového postižení může snížit počet mobilizačních pokusů [Gertz, 2012]. V důsledku dostupných vysoce účinných a bezpečných léků pro WM je role ASCT v léčbě méně jasná. Expertní mezinárodní doporučení řadí ASCT až po předchozím selhání inhibitorů Brutonovy tyrosinkinázy [Castillo, 2020]. Výjimkou může být sekundární IgM asociovaná amyloidóza, při které je vhodné zvážit ASCT jako časnou konsolidaci [Sidiqi, 2019]. U všech pacientů vhodných k transplantaci krvetvorných buněk se nedoporučuje léčba purinovými analogy pro riziko selhání sběru kmenových buněk. U všech pacientů vhodných k transplantaci krvetvorných buněk doporučujeme zvážit mobilizaci a separaci periferních kmenových buněk po první dosažené léčebné odpovědi.
8.1.6. Udržovací rituximab
Na základě pozitivních výsledků několika retrospektivních analýz u pacientů s WM, několika prospektivních studií u indolentních B lymfoproliferací (vč. pacientů s WM) a části expertních doporučení byla od roku 2019 v českých léčebných doporučeních zavedená udržovací léčba rituximabem u všech pacientů v remisi po předchozí léčbě režimem s rituximabem (mimo monotrapie) [Treon, 2011, Castillo, 2017, Hochster, 2009; Salles, 2011; Barta, 2016]. Výjimkou byli pacienti nereagující na léčbu imunochemoterapií, pacienti s těžkou sekundární hypogamaglobulinémií nebo netolerující rituximab [Kanan, 2014; Castillo, 2016; Castillo, 2017]. Aktualizované doporučení upravuje indikace udržovací léčby rituximabem na základě předběžných výsledků prospektivní randomizované studie fáze 3 – MAINTAIN (NCT00877214). Ve studii byla hodnocená udržovací léčba subkutánním rituximabem co 2 měsíce po dobu 2 let u pacientů s nově léčenou WM po indukční léčbě bendamustin, rituximab. V této studii nebyli randomizováni pacienti, kteří dosáhli po indukční léčbě minimální léčebnou odpověď. Medián bezpříznakového přežití v udržovací kohortě byl 101 měsíců a v observační skupině 83 měsíců, tento rozdíl nebyl hodnocen jako statisticky významný [Rummel, 2019]. U pacientů starších 65 let a pacientů s vysokým rizikem podle IPSS bylo ale zaznamnenáno delší celkové přežití v ramenu s udržovací léčbou.
8.2. Léčba relapsu a refrakterní Waldenströmovy makroglobulinémie
Léčbu není obvykle nutné zahájit bezprostředně po zjištění laboratorní progrese. Symptomatickou progresi splňující indikace k zahájení léčby obvykle předchází o desítky měsíců progrese laboratorní [Kastritis, 2015].
8.2.1. Výběr vhodné léčby
Určujícími faktory při výběru vhodné léčby jsou typ předchozího použitého režimu, dosažená léčebná odpověď (zejména refrakterita k rituximabu) a délka jejího trvání, tolerance předchozí léčby, limitující komorbidity, mutační status genu MYD88 a schopnost podstoupit vysokodávkovanou chemoterapii s autologní transplantací krvetvorby. Léčebný algoritmus pro léčbu relapsu či refrakterní WM je uveden ve schématu 2.
Schéma 2. Léčba relapsu/refrakterní Waldenströmovy makroglobulinémie. 
* nutné schválení revizním lékařem dle § 16 zákona č. 48/1997 Sb.
** Zanubrutinib je od roku 2020 registrovaný Evrospkou agenturou pro léčivé přípravky (EMA) pro léčbu relabované/refrakterní Waldenströmovy makroglobulinémie po alespoň jedné linii léčby, nebo pro nově léčené pacienty nevhodné k imunochemoterapii.
Zanubrutinib není v roce 2021 v České republice registrovaný.8.2.2. Opakování režimu první linie
Zopakování režimu první linie lze zvážit u pacientů s dlouhým trváním léčebné odpovědi vyžadujících další léčbu po více než 3–4 letech od zahájení léčby předchozí (v případě léčby režimem s fixním trváním). Podmínkou je ale dobrá tolerance poslední léčby [Kastritis, 2015, mSMART Waldenstrom macroglobulinemia guidelines v5, Jan 2021]. S ohledem na efektivitu nových léků zaváděných do léčby relapsu WM se tento názor neustále vyvíjí.
8.2.3. Alternativní režimy
V případě intervalu kratšího než 3–4 roky do zahájení další léčby je nutno zvolit alternativní režim, než byl režim původní. V případě rituximab refrakterních pacientů je vhodná léčba ibrutinibem (v případě dostupnosti alternativně zanubrutinibem). Všeobecně akceptovanou definicí refrakterity je nedostatečná léčebná odpověď (stabilní choroba) nebo progrese do 6 měsíců po ukončení léčby režimem obsahujícím rituximab [Rezvani, 2011]. Před použitím režimu s kombinací rituximabu je vhodné ověřit CD20 pozitivitu imunofenotypizačním vyšetřením kostní dřeně. Za preferované režimy považujeme režim bendamustin, rituximab, režim DRC, režim bortezomib, rituximab bez (VR) nebo s přidáním dexamethasonu (BDR) [Treon, 2011; Tedeschi, 2015; Paludo, 2016; Paludo, 2017; Treon, 2007; Chen, 2007; Dimopoulos, 2005; Ghobrial, 2010]. S cílem snížení výskytu neuropatických komplikací bortezomibu doporučujeme jeho podkožní podání, preferenčně v týdenních intervalech [Kastritis, 2018]. Další generace proteasomových inhibitorů, jako je carfilzomib, ixazomib a oprozomib, prokázaly smysluplnou léčebnou aktivitu u RRWM [Treon, 2014; Vesole, 2018; Ghobrial, 2016; Kersten, 2019; Kersten, 2021]. Pomocí kombinace ixazomib, dexamethason, rituximab bylo u RR WM dosaženo 74 % léčebných odpovědí, 52 % hlubokých odpovědí (≥ PR) a při mediánu sledování 24 měsíců bylo bezpříznakového přežití 56 % a celkové přežití 88 % Kersten, 2019; Kersten, 2021]. Monoterapie inhibitorem fosfatydil-3-kinázy idealisibem u pacientů s RR WM ve studiích fáze 1/2 vedla k smyluplné protinádorové aktivitě s ORR 80 % a mediánem bezpříznakového přežití 22 měsíců. Nejčastější významná toxicita (≥ stupně 3), která léčbu provázela, byla neutropenie (28 %), průjem (28 %) a hepatopatie (16 %) [Gopal, 2014; Wagner-Johnston, 2019]. Jiná studie fáze 2 u pacientů s RR WM léčených idealisibem v monoterapii musela být předčasně ukončená z důvodu závažné hepatopatie [Castillo, 2017. Ve studii fáze 2 hodnotící kombinaci idealisibu s obinutuzumabem u RRWM bylo dosaženo 90 % léčebných odpovědí vč. 76 % hlubokých odpovědí (≥ PR). Léčba byla ale opět provázená významnou toxicitou a polovina léčených musela léčbu ukončit předčasně [Tomowiak, 2021]. Idealisib v monoterapii či v kombinaci s obinutuzumabem lze zvážit v případě opakovaného relapsu, ideálně po vyčerpání méně toxických léčebných alternativ.
Léčbu kombinací rituximabu s purinovými analogy (fludarabin, cladribine) je nutné indikovat s opatrností. Důvodem jsou obavy spojené se zvýšeným výskytem sekundárních malignit vč. transformací v agresivnější lymfom (4,7–8 %), sekundární myelodysplastický syndrom a akutní myeloidní leukemie [Tedeschi, 2012; Tam, 2006; Souchet-Compain, 2013; Souchet-Compain, 2016; Leleu, 2009; ]. V případě použití FCR v léčbě relapsu WM byl výskyt sekundárních malignit vč. myelodysplastického syndromu a akutní myeloidní leukemie až 32 % ve srovnání s 8 % ve skupině léčených režimem BR (p = 0,004) [Tedeschi, 2015]. K dalším léčebným možnostem léčby opakovaně relabované, refrakterní WM patří mTOR inhibitor everolimus v monoterapii či v kombinaci s rituximabem a bortezomibem [Ghobrial, 2014; Ghobrial, 2015].
8.2.4. Inhibitory Brutonovy tyrosinkinázy
Ibrutinib v monoterapii je schválený pro léčbu WM po minimálně jedné předchozí linii léčby. Léčebné odpovědi nejsou negativně ovlivněny počtem předchozích linií léčby či refrakteritou k poslední léčbě vč. rituximabu [Treon, 2015; Dimopoulos, 2017]. Při monoterapii ibrutinibem nelze u většiny léčených pacientů očekávat navození hlubších léčebných odpovědí (≥ velmi dobrá parciální remise), nicméně zpravidla dojde k dlouhodobé, léta trvající stabilizaci onemocnění (5leté PFS: 54 %) [Treon, 2015; Treon, 2017; Dimopoulos, 2017; Treon, 2019]. Ibrutinib je vhodný k léčbě časného relapsu WM s trváním léčebné odpovědi < 1 rok a k léčbě rituximab refrakterních pacientů. Monoterapie ibrutinibem probíhá nepřetržitě do selhání nebo nezvladatelné toxicity. Její přerušování je vhodné minimalizovat na co nejkratší dobu pro rizika rebound fenoménu a selhání léčby [Gustine, 2017].
Alternativou k monoterapii je kombinace ibrutinibu s rituximabem ideálně pro pacienty, kteří nejsou refrakterní k rituximabu a u nichž od poslední léčby uplynulo > 12 měsíců (podle vstupních kriterií registrační studie INNOVATE) [Dimopoulos, 2018]. Podle expertních doporučení a našeho názoru ale pro preferenci kombinace ibrutinibu s rituximabem před monoterapii ibrutinibem chybí dostatek vědeckých důkazů. Výjimkou může být pacient s MYD88WT genotypem. [Castillo, 2020]. Zanubrutinib má příznivější profil nežádoucích účinků a vysokou protinádorovou aktivitou i u nepříznívého MYD88WT genotypu [Garcia-Sanz, 2020].
8.2.5. Venetoclax
Preklinické studie prokázaly vysokou expresi antiapoptotického regulačního proteinu BCL-2 v buňkách WM [Cao, 2015]. Venetoclax je první BCL-2 antagonista, který byl hodnocený u pacientů s RR WM. Ve studii fáze 2 byla více než polovina pacientů dříve léčených inhibitorem Brutonovy tyrosinkinázy [Castillo, 2018]. Venetoclax byl podávaný ambulantně s postupným navyšováním do dávky 800 mg a u žádného pacienta nedošlo ke klinicky významnému syndromu nádorového rozpadu. Léčba probíhala kontinuálně po dobu 2 let. Celkově na léčbu odpovědělo 87 % léčených, z toho 81 % dosáhlo hluboké léčebné odpovědi (≥ PR) a 19 % VGPR. Nástup léčebné odpovědi byl rychlý s mediánem 1,9 měsíce. Nejčastějším nežádoucím účinkem byla neutropenie, anemie a průjem. U žádného pacienta nebyla ukončená léčba z důvodu toxicity. Přežití bez progrese ve 2 letech bylo 76 %. Venetoclax tedy představuje účinnou a bezpečnou léčbu u pacientů s opakovaně léčenou WM.
8.2.6. Autologní transplantace kostní dřeně
Indikace a správné načasování myeloablativní vysokodávkované chemoterapie s autologní transplantací krvetvorby (ASCT) u pacientů s relabovanou WM nebyly zkoumány v prospektivních studiích. Údaje o její efektivitě a bezpečnosti jsou čerpány z kooperativních a nadnárodních transplantačních registrů [Munshi, 2003; Kyriakou, 2010; Kyriakou,2007; Tournilhac, 2003; Anagnostopoulos, 2006; Gilleece, 2008; Anagnostopoulos, 2002; Dhedin, 2007]. Většina pacientů podstoupila transplantaci v chemosenzitivní fázi nemoci. Podle konsenzuálních expertních doporučení je ASCT vhodná v léčbě chemosenzitivní WM s agresivním klinickým průběhem a preferenčně po selhání léčby inhibitorem Brutonovy tyrosinkinázy [Kyriakou, 2017; Castillo, 2020].
8.2.7. Alogenní transplantace kostní dřeně
Vysoká peritransplantační mortalita alogenní SCT významně limituje její širší uplatnění v léčbě WM. Její použití lze zvažovat jenom u vybraných mladých pacientů s agresivní nemocí a vyčerpanými možnostmi jiné léčby [Kyriakou, 2010; Bachanova, 2012; Kyriakou, 2017].
9. HODNOCENÍ LÉČEBNÝCH ODPOVĚDÍ
Hodnocení účinku léčby u WM vychází z posuzování vývoje koncentrace MIg a celkové koncentrace IgM, klinických parametrů, měřitelného extramedulárního postižení a morfologického hodnocení kostní dřeně. Hodnocení kategorických odpovědí může probíhat jak pomocí kvantifikace MIg densitometrií, tak prostřednictvím měření celkové koncentrace sérového IgM pomocí nefelometrie. Obě metody serologického hodnocení vykazují podobnou míru korelace s odpovědí pozorovanou v kostní dřeni [Tripsas, 2012]. Při hodnocení je nutno upozornit na očekávanou biologickou variabilitu měření pomocí nefelometrie (13 %) a densitometrie (8 %) [Katzmann, 2011]. Dynamika nástupu léčebných odpovědí se může významně lišit v závislosti na použitém režimu. Proto se doporučuje vyšetření pravidelně opakovat po ukončení léčby. Kompletní remisi je nutno potvrdit druhou imunofixací. Obdobně se vyžaduje opakovat vyšetření pro potvrzení progrese. V případě, že by byl nárůst koncentrace IgM jediným kritériem pro potvrzení progrese, musí být o nejméně 5 g/l. Může docházet k významným diskrepancím mezi poklesem IgM a mírou infiltrace kostní dřeně. Toto je patrné zejména při monoterapii anti-CD20 protilátkou s cílenou CD20 B-buněčnou deplecí nebo monoterapií proteasomovým inhibitorem s výraznějším efektem na plasmocelulární komponentu WM. Vyšetření kostní dřeně je doporučeno provádět 4–6 týdnů po ukončené léčbě. Ke splnění podmínek definice kompletní remise postačuje morfologické vymizení infiltrace, hodnocené cytologií aspirátu a histologickým vyšetřením biopsie kostní dřeně. Nicméně se doporučuje při vyšetřování kostní dřeně současně provádět i imunofenotypizační a imunohistochemické vyšetření k posouzení zbytkové klonální populace [Owen, 2013]. Do budoucna lze očekávat vyšetřování minimální reziduální nemoci inkorporací průtokové cytometrie a testování MYD88 pomocí PCR [Treon, 2013]. V případě vstupního extramedulárního postižení je nutné zopakovat po dokončení léčby zobrazovací vyšetření (CT nebo MRI nebo PET/CT).
Kritéria pro hodnocení léčebných odpovědí byla naposledy revidována v roce 2013 v rámci 6. mezinárodního workshopu (tab. 9).
Tab. 9. Definice léčebných odpovědí u Waldenströmovy makroglobulinémie [Owen, 2013]. ![Definice léčebných odpovědí u Waldenströmovy makroglobulinémie [Owen, 2013].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/ed08718ec435f378418a9854811ae94d.jpg)
a nutno potvrdit druhou imunofixací, b vyšetření kostní dřeně je doporučeno provádět 4–6 týdnů po ukončené léčbě (poznámka: ke splnění podmínek definice kompletní remise postačuje morfologické vymizení infiltrace, hodnoceno cytologií aspirátu a histologií trepanobiopsie kostní dřeně; nicméně se doporučuje součastně provádět i imunofenotypizační a imunohistochemické vyšetření), c hodnocení kategorických odpovědí může probíhat jak pomocí kvantifikace MIg densitometrií, tak prostřednictvím měření celkové koncentrace sérového IgM pomocí nefelometrie 10. LÉČBA BING-NEELOVA SYNDROMU
Bing-Neelův syndrom (BNS) je extrémně vzácnou manifestací WM, typicky se vyskytující v období relapsu [Malkani, 2010]. BNS je způsoben nádorovou infiltrací centrálního nebo periferního nervového systému buňkami LPL. V roce 2017 byla publikována první mezinárodní doporučení o diagnostice, léčbě a hodnocení léčebných odpovědí Bing-Neelova syndromu [Minnema, 2017]. Doporučení byla vypracována na základě retrospektivních analýz malých souborů a kazuistických sdělení. Pacienti s BNS byli efektivně léčeni vysokými dávkami cytostatik s dobrým průnikem přes hematoencefalickou bariéru, jako je methotrexát a cytosinarabinosid [Hoang-Xuan, 2015]. Intenzivní indukční režimy byly u některých pacientů zakončeny vysokodávkovanou chemoterapií s autologní transplantací krvetvorby [Simon, 2015; Castillo, 2016; Abdallah, 2013]. S efektem byla použita i nukleosidová analoga fludarabin, cladribin a bendamustin ve standardních dávkách [Simon, 2015; Castillo, 2016; Varretoni, 2015]. Prvotní práce ukázaly, že standardní a vyšší dávky ibrutinibu, 480–560 mg/den, pronikají hematoencefalickou bariérou a vedly u několika pacientů k parciálním i kompletním remisím [Castillo, 2016; Cabannes-Hamy, 2016; Mason, 2017]. Recentní velká retrospektivní práce hodnotila monoterapii ibrutinibem v léčbě nově (39 %) a dříve (61 %) léčeného BNS v dávkách 420 mg (54 % léčených) a 560 mg (46 % léčených) [Castillo, 2019]. Po 3 měsících léčby došlo k symptomatickému a radiologickému zlepšení u 85 % a 60 % pacientů a u 58 % k negativní cytologii likvoru. Po 2 letech od zahájení léčby ibrutinibem byla 80% pravděpodobnost přežití bez progrese, úmrtí nebo neakceptovatelné toxicity. Role rituximabu v léčbě BNS není jasná, otázkou je její dostatečný průnik hematoencefalickou bariérou [Minnema, 2017]. Intrathekální chemoterapie samotná nevede k dlouhodobým remisím a je vhodné ji kombinovat se systémovou léčbou zejména u leptomeningeální formy BNS [Van Cauwenberge, 2015; Minnema, 2017]. V léčbě BNS lze použít i radioterapii [Abbi, 2013; Shimizu, 1993; Imai, 1995]. Stereotaktická radioterapie v dávkách 30–40 Gy je preferovanou formou léčby zejména lokalizovaného intraparenchymatózního postižení [Minnema, 2017]. Nicméně i u cílené radioterapie CNS je velmi častá oddálená neurotoxicita v podobě neurokognitivních deficitů [Saad, 2015].
Výběr vhodné léčby a její intenzita se řídí klinickým stavem pacienta, lokalizací a formou postižení, dříve použitou chemoterapií a schopností podstoupit autologní transplantaci. Asymptomatického pacienta s BNS je možné jenom pečlivě sledovat [Minnema, 2017, Castillo, 2019]. Na základě recentně publikovaných prací o aktivitě ibrutinibu u BNS je podle některých expertů u nově diagnostikovaného onemocnění preferovanou léčbou ibrutinib [Castillo, 2019]. U čistě leptomeningeálního postižení lze individuálně zvážit intrathekální chemoterapii. Lepší kontroly nemoci lze dosáhnout systémovou léčbou. Pro riziko transformace a negativní vliv na separaci kmenových buněk se obecně nedoporučuje opakovat léčbu nukleosidovými analogy. Intenzivní chemoterapie s konsolidací autologní transplantací by měla být vždy zvažována u mladších pacientů. Evropská neuro-onkologická asociace preferuje v léčbě pri - márních CNS lymfomů režim BCNU/thio - tepa [Hoang-Xuan, 2015]. Optimální před - transplantační režim u BNS ale není známý.
Konsenzuální dopoučení léčby BNS je uvedeno ve schématu 3.
Schéma 3. Konsenzuální doporučení léčby Bing-Neelův syndromu – upraveno podle [Minnema, 2017]. ![Schéma 3. Konsenzuální doporučení léčby Bing-Neelův syndromu – upraveno podle [Minnema, 2017].](https://pl-master.mdcdn.cz/media/image_pdf/0c3f503d95ed9a99642d0a33c1ea807d.jpg?version=1647897699)
10.1. Hodnocení léčby
Hodnocení efektu léčby u BNS sestává z kombinace klinického hodnocení, vyšetření magnetickou rezonancí, a v případě leptomeningeální formy postižení, vyšetření mozkomíšního moku. Jednotlivá vyšetření je nutné pravidelně opakovat, nejméně jednou v průběhu léčby a po ukončení léčby. Efekt kontinuální léčby se doporučuje monitorovat pravidelně ve 3–4měsíčních intervalech a později co 12 měsíců. Hodnocení efektu léčby BNS má probíhat nezávisle na hodnocení WM [Minnema, 2017]. Konsenzuální kritéria hodnocení efektu léčby jsou uvedená v tab. 10. a přehled doporučených léčebných režimů u WM v tab. 11.
Tab. 10. Hodnocení léčebných odpovědí u BNS [Minnema, 2017]. ![Hodnocení léčebných odpovědí u BNS [Minnema, 2017].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/d74b94b0bb4348a9c46281c9542e5257.jpg)
Tab. 11. Přehled doporučených léčebných režimů u WM (obsahuje jen vybrané režimy). 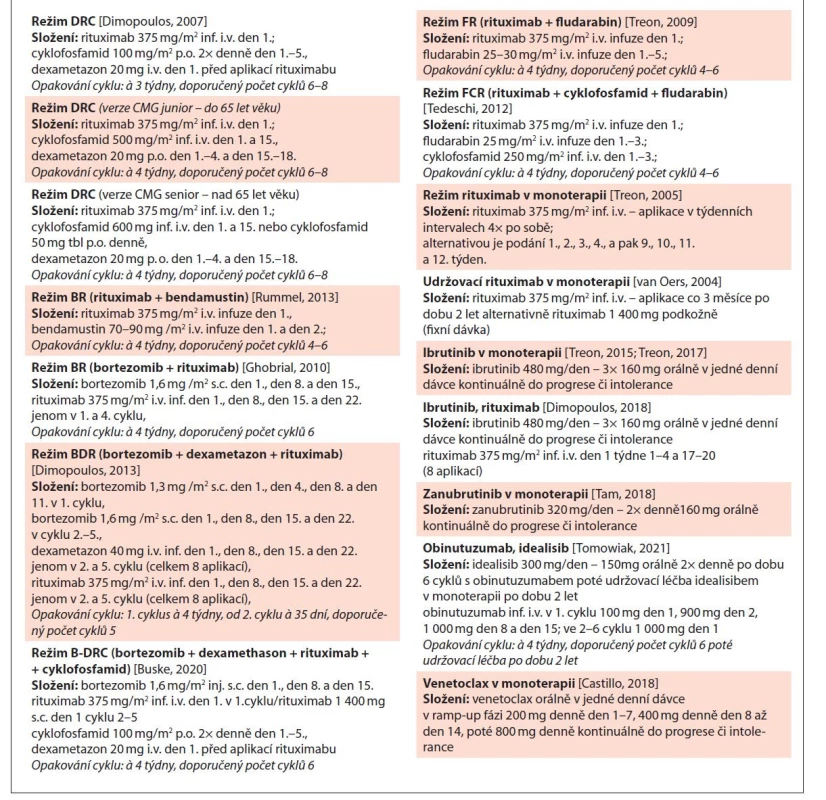
11. PODPŮRNÁ TERAPIE A LÉČBA KOMPLIKACÍ
11.1. Léčba hyperviskozity a další indikace plazmaferézy
Plazmaferéza je indikovaná u pacientů s klinicky závažnými příznaky hyperviskozity, samotná fyzikální hodnota naměřené viskozity přitom není indikací pro plazmaferézu.
Výměna 1–1,5 plazmatického objemu sníží viskozitu asi o 60–75 %. U pacientů s klinicky závažnými projevy hyperviskozity se proto doporučuje provést 1–2 plazmaferézy [Mahmood, 2006; Clark, 1999; Stone, 2012].
Opakované plazmaferézy s cílem udržení viskozity v přijatelných mezích jsou doporučovány jednak pro nemocné, jejichž nemoc je rezistentní na medikamentózní léčbu, a také pro nemocné, kteří nejsou schopni podstoupit účinnou medikamentózní léčbu. Efekt plazmaferézy nastupuje rychle a trvá 4–6 týdnů [Ansell, 2010; Menke, 2009; Drew, 2002].
Dle omezených zkušeností je plazmaferéza léčebnou alternativou u nemocí způsobených monoklonálním imunoglobulinem (IgM-related disorders), jako jsou závažná neuropatie nebo symptomatická kryoglobulinémie. Může být využita i jako iniciální krok před podáním cytoredukční léčby, která utlumí aktivitu nemoci.
Při plánování léčby si lékař musí být vědom možnosti dočasného zvýšení koncentrace monoklonálního IgM vlivem rituximabu a jeho podání naplánovat tak, aby nedošlo k tomuto jevu (flare efekt).
11.2. Léčba periferní neuropatie způsobené monoklonálním imunoglobulinem IgM
Při pomalu progredující neuropatii není léčba vždy nevyhnutelná. U pacientů s progredující neuropatií je doporučená léčba. Při agresivním průběhu se středně těžkou a těžkou neuropatií je vhodná vstupně léčebná plazmaferéza (obvykle týdenní plazmaferézy po dobu 2–3 měsíců) následovaná konsolidací imunochemoterapií nebo ibrutinibem. Při pomalejším průběhu a mírné neuropatii lze zvážit monoterapii rituximabem.
Při výrazných projevech senzorické neuropatie je v průběhu chemoterapie doporučená i symptomatická léčba s použitím gabapentinu, pregabalinu a duloxetinu, tyto léky indikuje a předepisuje neurolog.
12. SLEDOVÁNÍ PO LÉČBĚ
Součástí pravidelných kontrol sledování nemocného je anamnéza, fyzikální vyšetření, kontrolní panel odběrů vč. kvantifikace IgM každé 3 měsíce po dobu 2 let, každých 4–6 měsíců po dobu dalších 3 let, a následně v ročních intervalech se speciálním zaměřením na transformaci nemoci, sekundární malignity. Zobrazovací vyšetření (CT nebo PET/CT) je vhodné zopakovat po dokončení léčby v případě vstupního extramedulárního postižení a eventuálně i v jejím v průběhu při podezření na nereagující či progredující onemocnění [Castillo, 2016]. U části pacientů s WM může dojít k transformaci do lymfomu vyššího stupně malignity, typicky do difúzního velkobuněčného B lymfomu (DLBCL), v těchto případech je doporučována biopsie tkáně (nejčastěji lymfatické uzliny) a histologická verifikace.
13. DOPORUČENÍ PRO LÉČBU WM
- Pacienty s asymptomatickou formou WM je vhodné pouze sledovat. Je doporučeno aktivní pravidelné celoživotní sledování. Sledování probíhá v tříměsíčních intervalech první 3 roky, poté v půlročních intervalech následující 2 roky a poté jednou ročně při stabilním stavu (úroveň důkazu IIa, stupeň doporučení B).
- Koncentrace IgM samotná, není indikací k zahájení léčby (úroveň důkazu IIb, stupeň doporučení B).
- U pacientů s hyperviskozitou je indikovaná výměnná plazmaferéza před samotným zahájením systémové léčby (úroveň důkazu III, stupeň doporučení B).
- Pacienti se symptomatickou WM by měli být léčeni režimem obsahujícím rituximab a/nebo ibrutinib nebo zanubrutinib (úroveň důkazu Ib, stupeň doporučení A).
- Monoterapie rituximabem je kontraindikována u pacientů s hyperviskozitou před provedením výměnné plazmaferézy. V případě vysoké koncentrace IgM (> 40 g/l) není monoterapie rituximabem vhodná (úroveň důkazu IV, stupeň doporučení C).
- Režim BR (bendamustin, rituximab) je preferovaným režimem pro nově léčené pacienty s velkou nádorovou masou, hyperviskozitou a potřebou rychlého nástupu léčebné odpovědi (úroveň důkazu IV, stupeň doporučení C).
- Režim BDR (bortezomib, dexamethason, rituximab), případně B-DRC (bortezomib, dexamethason, rituximab, cyklofosfamid) je preferovaným režimem pro nově léčené pacienty s velkou nádorovou masou, hyperviskozitou a potřebou rychlého nástupu léčebné odpovědi (úroveň důkazu IV, stupeň doporučení C).
- Režim DRC (dexamethason, rituximab, cyklofosfamid) je alternativou režimu BR pro nově léčené pacienty s malou nádorovou masou, bez hyperviskozity a nevyžadující rychlý nástup léčebné odpovědi, nebo v případě, že je režim BR rizikový (úroveň důkazu IV, stupeň doporučení C).
- Monoterapie ibrutinibem (nebo zanubrutinibem) je alternativou pro pacienty nevhodné k imunochemoterapii (úroveň důkazu IIa, stupeň doporučení B).
- Kombinaci ibrutinib, rituximab lze zvážit pro léčbu WM s nemutovaným (wild-type) genem MYD88WT. Pro ostatní pacienty s WM toho času chybí dostatek vědeckých důkazů o jednoznačné výhodě kombinační léčby (úroveň důkazu IV, stupeň doporučení C).
- Pacienty v remisi po léčbě je vhodné pravidelně sledovat do symptomatické progrese (úroveň důkazu IV, stupeň doporučení C).
- Udržovací léčba rituximabem po léčbě imunochemoterapii není doporučená u pacientů s WM, kteří dosáhli parciální remisi nebo lepší léčebnou odpověď a/nebo netolerovali rituximab (úroveň důkazu IIb, stupeň doporučení B).
- Léčbu purinovými analogy provází infekční a myelosupresivní komplikace a významně vyšší výskyt sekundárních malignit, a proto není vhodná pro pacienty s nově léčenou WM (úroveň důkazu IIa, stupeň doporučení B).
Léčba druhé a další linie
- Pacienti bez adekvátní odpovědi na režim imunochemoterapie v první linii s přetrvávajícími symptomy nebo pacienti s primárně refrakterní WM mají být léčeni ibrutinibem (zanubrutinibem) (úroveň důkazu IIa, stupeň doporučení B).
- Léčba ibrutinibem je vhodná pro léčbu relapsu pacientů s WM, zejména s přítomností mutace MYD88 (úroveň důkazu Ib, stupeň doporučení A).
- Kombinaci ibrutinib, rituximab lze zvážit pro léčbu WM s nemutovaným (wild-type) genem MYD88WT. Pro ostatní pacienty s WM toho času chybí dostatek vědeckých důkazů o jednoznačné výhodě kombinační léčby (úroveň důkazu IV, stupeň doporučení C).
- Opakování režimu imunochemoterapie první linie je možné u pacientů s pozdním relapsem s dlouhým trváním remise (obvykle čas do zahájení další léčby ≥ 3–4 roky) a dobrou tolerancí předchozího režimu (úroveň důkazu IIa, stupeň doporučení B).
- Pacienti se symptomatickým pozdním relapsem by měli znovu dostat režim obsahující rituximab a/nebo ibrutinib nebo zanubrutinib (úroveň důkazu IIa, stupeň doporučení B).
- Režim obsahující bortezomib je potenciální alternativou léčby symptomatického relapsu WM, preferovány jsou režimy s týdenním podáváním bortezomibu v podkožní formě s cílem předejít neurologické toxicitě, doporučována je profylaxe proti reaktivaci HZV (úroveň důkazu IIa, stupeň doporučení B).
- V léčbě relapsu jsou používány režimy obdobné jako v léčbě první linie, ale také režimy obsahující bortezomib (bortezomib rituximab +/ – dexamethason), ixazomib, venetoclax idealisib nebo kombinací obinutuzumab, idealisib. Režimy obsahující purinová analoga (např. FR, FCR, CladR) je optimální používat pro léčbu opakovaného relapsu (> 3. linie léčby). Volba režimu vyžaduje komplexní zhodnocení klinického stavu u konkrétního pacienta a také zvážení potenciální možnosti provedení SCT (úroveň důkazu IIa, stupeň doporučení B).
- Pacienty s klinicky asymtomatickým relapsem projevujícím se pouze postupným vzestupem MIg je vhodné pouze sledovat a léčbu zahájit až v případě klinicky významné progrese WM (úroveň důkazu IV, stupeň doporučení C).
- Mladší pacienti s chemosenzitivním relapsem WM jsou kandidáty pro provedení transplantace (SCT) a měli by být diskutováni s transplantačním centrem (úroveň důkazu III, stupeň doporučení B).
Doporučení pro léčbu Bing-Neelova syndromu
- Asymptomatické pacienty s Bing-Neelovým syndromem je možné jenom pečlivě sledovat (úroveň důkazu IV, stupeň doporučení C).
- Výběr vhodné léčby a její intenzita se řídí klinickým stavem pacienta, lokalizací a formou postižení, dříve použitou léčbou a schopností podstoupit autologní transplantaci. K léčebným možnostem patří vysoké dávky cytostatik s dobrým průnikem hematoencefalickou bariérou (methotrexát, cytosinarabinosid), nukleosidová analoga ve standardních dávkách (fludarabin, cladribin a bendamustin) a standardní a vyšší dávky ibrutinibu (úroveň důkazu IIb/III, stupeň doporučení B/C).
- U čistě leptomeningeálního postižení lze individuálně zvážit intrathekální chemoterapii. Vhodnější je ale její kombinace s léčebou systémovou (úroveň důkazu IV, stupeň doporučení C).
- Stereotaktická radioterapie v dávkách 30–40 Gy je možnou formou léčby lokalizovaného intraparenchymatózního postižení (úroveň důkazu IV, stupeň doporučení C).
- Intenzivní chemoterapie s konsolidací autologní transplantací by měla být vždy zvažována u mladších pacientů. Optimální přípravný předtransplantační režim není známý. Konsenzuálně jsou preferované režimy používané v léčbě primárních CNS lymfomů (např. režim BCNU/thiotepa) (úroveň důkazu IV, stupeň doporučení C).
V ČR v roce 2021 je použití rituximabu v monoterapii (nebo v kombinaci s ibrutinibem), obinutuzumabu, bortezomibu, bendamustinu, ibrutinibu, ixazomibu, venetoclaxu a idealisibu při léčbě WM možné pouze po schválení revizním lékařem příslušné zdravotní pojišťovny. Zanubrutinib je od roku 2020 registrovaný Evrospkou agenturou pro léčivé přípravky (EMA) pro léčbu relabované/refrakterní Waldenströmovy makroglobulinémie po alespoň jedné linii léčby, nebo pro nově léčené pacienty nevhodné k imunochemoterapii. Zanubrutinib není v roce 2021 v České republice registrovaný.
Standardně jsou v ČR pro léčbu Waldenströmovy makroglobulinémie hrazena zatím pouze klasická cytostatika, rituximab v kombinaci s chemoterapií, kortikoidy a fludarabin.
SEZNAM POUŽITÝCH ZKRATEK
AIHA – autoimunitní hemolytická anémie
anti GM-1 – protilátky proti gangliosidům
anti-MAG – protilátky proti glykoproteinům asociovaným s myelinem
ASCT – autologní transplantace
B2M – beta-2-mikroglobulin
BCNU – carmustin
BNP – natriuretický peptid (brain natriuretic peptide)
BNS – Bing-Neelův syndrom
BR – bendamustin, rituximab
CAD – nemoc chladových aglutininů
CD – antigenní znak (cluster of differentiation)
CladR – cladribin, rituximab
CNS – centrální nervový systém
CR – kompletní remise
CT – výpočetní tomografie
DLBCL – difuzní velkobuněčný B lymfom
DRC – dexamethason, rituximab, cyklofosfamid
EMG – elektromyelogram
fVIII – koagulační faktor VIII
FCR – fludarabin, cyklofosfamid, rituximab
FISH – flourescenční in situ hybridizace
FLC – volné lehké řetězce
FR – fludarabin, rituximab
GMT – gamm glutamyl transferáza
Gy – gray
HD-AraC – vysokodávkovaný cytosinarabinosid
HD-MTX – vysokodávkovaný methotrexát
Hg – hemoglobin
HIV – lidský virus získané imunodeficience
HR – hazard ratio
HVS – hyperviskózní syndrom
HZV – virus herpes zoster
IgA – imunoglobulin třída A
IgG – imunoglobulin třídy G
IgM – imunoglobulin třídy M
Inf. – infuze
IPSSWM – mezinárodní prognostický skórovací systém pro nemocné s Waldenströmovou makroglobulinémií
ITP – imunitní trombocytopenie
i.v. – nitrožilně
LDH – laktát dehydrogenáza
LPL – lymfoplasmocytární lymfom
MGUS – monoklonální gamapatie nejasného významu
MIg – monoklonální imunoglobulin
MUT – mutovaný
MR – minimální léčebná odpověď
MRI – nukleární magnetická rezonance
NCS – elektrofyziologické vyšetření vodivosti nervů (nerve conduction studies)
PAT – přímý antiglobulinový test
PCR – polymerázová řetězová reakce
PD – progrese nemoci
PET – pozitronová emisní tomografie
PNP – periferní polyneuropatie
p. o. – per os
PR – parciální remise
RR WM – relabovaná refrakterní Waldenströmova makroglobulinémie
SD – stabilní nemoc
SCT – transplantace kostní dřeně
TnI – troponin I
TnT – troponin T
USG – ultrasonografie
VGPR – velmi dobrá parciální remise
VR – bortezomib, dexamethason
vWCH –vonWillebrandova choroba
vWf: RCo – funkční aktivita ristocetin kofaktoru
WHIM – syndrom vrozeného imunodeficitu Warts, Hypogammaglobulinemia, Infections and Myelokathexis
WM – Waldenströmova makrogobulinémie
PODĚKOVÁNÍ
Děkujeme recenzentům jednotlivých kapitol, členům předsednictva CMG a zástupcům KLS podílejícím se na přípravě doporučení.
Souhrn doporučení 2021 pro diagnostiku a léčbu Waldenströmovy makroglobulinémie (WM)
PODÍL AUTORŮ NA RUKOPISU
M.K. – napsání rukopisu, revize rukopisu
R.H., J.M. – napsání dílčí části rukopisu, revize rukopisu
T.J. – revize rukopisu
D.B., A.J., V.M., L.P., M.T. – připomínky, revize rukopisu
KONFLIKT ZÁJMŮ
R.H. – honoráře, přednášky, konzultace a nefinanční podpora od firmy Janssen
M.K., J.M., T.J., Z.A., D.B., A.J., V.M., L.P a M.T. – nemají v souvislosti se vznikem a přípravou rukopisu žádný konflikt zájmů
Doručeno do redakce dne: 17. 1. 2022.
prof. MU Dr. Roman Hájek, CSc.
Klinika hematoonkologie
FN Ostrava
17. listopadu 1790
708 52 Ostrava – Poruba
e-mail: roman.hajek@fno.cz
Zdroje
LITERATURA PRO DIAGNOSTICKOU ČÁST
- • Adam Z, Šmardová J, Ščudla V. Waldenströmova makroglobulinémie – klinické projevy, diferenciální diagnostika a prognóza nemoci. Vnitřní Lék. 2007; 53 : 1325–1337.
- • Baehring JM, Hochberg EP, Raje N, et al. Neurological manifestations of Waldenström macroglobulinemia. Nat Clin Pract Neurol. 2008; 4 (10): 547–556.
- • Baldini L, Nobile-Orazio E, Guffanti A, et al. Peripheral neuropathy in IgM monoclonal gammopathy and Wäldenstrom’s macroglobulinemia: a frequent complication in elderly males with low MAG-reactive serum monoclonal component. Am J Hematol. 1994; 45 : 25–31.
- • Banwait R, O‘Regan K, Campigotto F, et al. The role of 18F-FDG PET/CT imaging in Waldenstrom macroglobulinemia. Am J Hematol. 2011; 86 (7): 567–572.
- • Braggio E, Fonseca R. Genomic abnormalities of Waldenström macroglobulinemia and related low-grade B-cell lymphomas. Clin Lymphoma Myeloma Leuk. 2013; 13 (2): 198–201.
- • Buske C, Sadullah S, Kastritis E, et al. Treatment and outcome patterns in European patients with Waldenström’s macroglobulinaemia: a large, observational, retrospective chart review. Lancet Haematol. 2018; 5 (7): e299–e309.
- • Buske C, Tedeschi A, Trotman J, et al. Ibrutinib plus rituximab versus placebo plus rituximab for Waldenström‘s macroglobulinemia: final analysis from the randomized phase III iNNOVATE study. J Clin Oncol. 2022; 40 (1): 52–62.
- • Bustoros M, Sklavenitis-Pistofidis R, Kapoor P, et al. Progression risk stratification of asymptomatic Waldenström macroglobulinemia. J Clin Oncol. 2019; 37 (16): 1403–1411.
- • Castillo JJ, D‘Sa S, Lunn MP, et al. Central nervous system involvement by Waldenström macroglobulinaemia (Bing-Neel syndrome): a multi-institutional retrospective study. Br J Haematol. 2016; 172 (5): 709–715.
- • Castillo JJ, Garcia-Sanz R, Hatjiharissi E, et al. Recommendations for the diagnosis and initial evaluation of patients with Waldenström macroglobulinaemia: a task force from the 8th International Workshop on Waldenström macroglobulinaemia. Br J Haematol. 2016; 175 (1): 77–86.
- • Coucke L, Marcelis L, Deeren D, et al. Lymphoplasmacytic lymphoma exposed by haemoptysis and acquired von Willebrand syndrome. Blood Coagul Fibrinolysis. 2014; 25 (4): 395–397.
- • Chapman MA, Lawrence MS, Keats JJ, et al. Initial genome sequencing and analysis of multiple myeloma. Nature. 2011; 471 (7339): 467–472.
- • Dhodapkar MV, Hoering A, Gertz MA et al.; Long-term survival in Waldenstrom macroglobulinemia: 10-year follow-up of Southwest Oncology Group-directed intergroup trial S9003. Blood. 2009; 113 (4): 793–796.
- • D’Sa S, Kersten MJ, Castillo JJ, et al. Investigation and management of IgM and Waldenström-associated peripheral neuropathies: recommendations from the IWWM-8 consensus panel. Br J Haematol. 2017; 176 (5): 728–742.
- • Drappatz J, Akar S, Fisher DC, et al. Imaging of Bing-Neel syndrome. Neurology. 2008; 70 (16): 1364.
- • Ghobrial IM. Are you sure this is Waldenstrom macroglobulinemia? Hematology Am Soc Hematol Educ Program. 2012; 2012 : 586–594.
- • Gnemmi V, Leleu X, Provot F, et al. Cast nephropathy and light-chain deposition disease in Waldenström macroglobulinemia. Am J Kidney Dis. 2012; 60 (3): 487–491.
- • Growková K, Kufová Z, Ševčíková T, et al. Diagnostické přístupy u Waldenströmovy makroglobulinemie – nejvhodnější dostupné možnosti neinvazivního a dlouhodobého monitorování nemoci. Klin Onkol. 2017; 30 (Suppl 2): 81–91.
- • Gustine JN, Meid K, Dubeau T, et al. Serum IgM level as predictor of symptomatic hyperviscosity in patients with Waldenström macroglobulinaemia. Br J Haematol. 2017; 177 (5): 717–725.
- • Hivert B, Caron C, Petit S, et al. Clinical and prognostic implications of low or high level of von Willebrand factor in patients with Waldenstrom macroglobulinemia. Blood. 2012; 120 (16): 3214–3221.
- • Hunter ZR, Manning RJ, Hanzis Ch, et al. IgA and IgG hypogammaglobulinemia in Waldenström’s macroglobulinemia. Haematologica. 2010; 95 (3): 470–475.
- • Jelinek T, Bezdekova R, Zatopkova M, et al. Current applications of multiparameter flow cytometry in plasma cell disorders. Blood Cancer J. 2017; 7 (10): e617.
- • Jiménez C, Sebastián E, Chillón MC, et al. MYD88 L265P is a marker highly characteristic of, but not restricted to, Waldenström’s macroglobulinemia. Leukemia. 2013; 27 (8): 1722–1728.
- • Kaiser LM, Hunter ZR, Treon SP, et al. CXCR4 in Waldenström’s Macroglobulinema: chances and challenges. Leukemia. 2021; 35 : 333–345.
- • Kastritis E, Zervas K, Repoussis P, et al. Prognostication in young and old patients with Waldenström’s macroglobulinemia: importance of the International Prognostic Scoring System and of serum lactate dehydrogenase. Clin Lymphoma Myeloma. 2009; 9 (1): 50–52.
- • Kastritis E, Kyrtsonis MCH, Morel P, et al. Competing risk survival analysis in patients with symptomatic Waldenström macroglobulinemia: the impact of disease unrelated mortality and of rituximab-based primary therapy. Haematologica. 2015; 100 (11): e446–e449.
- • Kastritis E, Morel P, Duhamel A, et al. A revised international prognostic score system for Waldenström’s macroglobulinemia. Leukemia. 2019; 33 : 2654–2661.
- • Kim HJ, Suh S, Kim JH, et al. Brain magnetic resolution imaging to diagnose Bing-Neel syndrome. J Korean Neurosurg Soc. 2009; 46 : 588–591.
- • Kyle RA, Benson JT, Larson DR et al. Progression in smoldering Waldenström macroglobulinemia: long-term results. Blood. 2012; 119 (19): 4462–4466.
- • Leleu X, Roccaro AM, Moreau AS, et al. Waldenstrom macroglobulinemia. Cancer Lett. 2008; 270 (1): 95–107.
- • Leleu X, Xie W, Bagshaw M, et al. The role of serum immunoglobulin free light chain in response and progression in waldenstrom macroglobulinemia. Clin Cancer Res. 2011; 17 (9): 3013–3018.
- • Levine T, Pestronk A, Florence J, et al. Peripheral neuropathies in Waldenström’s macroglobulinaemia. J Neurol Neurosurg Psychiatry. 2006; 77 (2): 224–228.
- • Martyn CN, Hughes RA. Epidemiology of peripheral neuropathy. J Neurol Neurosurg Psychiatry. 1997; 62 (4): 310–318.
- • Menke MN, Feke GT, McMeel JW, et al. Hyperviscosity-related retinopathy in Waldenström macroglobulinemia. Arch Ophthalmol. 2006; 124 (11): 1601–1606.
- • Merlini G, Wechalekar AD, Palladini G. Systemic light chain amyloidosis: an update for treating physicians. Blood. 2013; 121 : 5124–5130.
- • Minnema MC, Kimby E, D‘Sa S, et al. Guideline for the diagnosis, treatment and response criteria for Bing-Neel syndrome. Haematologica. 2017; 102 (1): 43–51.
- • Morel P, Duhamel A, Gobbi P, et al. International prognostic scoring system for Waldenström macroglobulinemia. Blood. 2009; 113 (18): 4163–4170.
- • Nguyen-Khac F, Lambert J, Chapiro E, et al. Chromosomal aberrations and their prognostic value in a series of 174 untreated patients with Waldenström’s macroglobulinemia. Haematologica. 2013; 98 (4): 649–654.
- • Nobile-Orazio E, Francomano E, Daverio R, et al. Anti-myelin-associated glycoprotein IgM antibody titers in neuropathy associated with macroglobulinemia. Ann Neurol. 1989; 26 (4): 543–550.
- • Owen RG, Kyle RA, Stone MJ, et al. Response assessment in Waldenström macroglobulinaemia: update from the VIth International Workshop. Br J Haematol. 2013; 160 (2): 171–176.
- • Ocio EM, Schop RFJ, Gonzalez B, et al. 6q deletion in Waldenström macroglobulinemia is associated with features of adverse prognosis. Br J Haematol. 2007; 136 : 80–86.
- • Owen RG. Developing diagnostic criteria in Waldentrom’s macroglobulinemia. Semin Oncol. 2003; 30 : 196–200.
- • Owen RG, Pratt G, Auer RL, et al. Guidelines on the diagnosis and management of Waldenström macroglobulinaemia. Br J Haematol. 2014; 165 (3): 316–333.
- • Paiva B, Montes MC, García-Sanz R, et al. Multiparameter flow cytometry for the identification of the Waldenström’s clone in IgM-MGUS and Waldenström’s macroglobulinemia: new criteria for differential diagnosis and risk stratification. Leukemia. 2014; 28 (1): 166–173.
- • Poulain S, Dervite I, Leleu X, et al. Autoimmune hemolytic anemias and IgG antierythrocyte autoantibodies in Waldenström’s macroglobulinemia: association with FcgammaRIIa polymorphism. Leukemia. 2006; 20 : 1179–1181.
- • Poulain S, Roumier C, Decambron A, et al. MYD88 L265P mutation in Waldenstrom macroglobulinemia. Blood. 2013; 121 (22): 4504–4511.
- • Pophali PA, Bartley A, Kapoor P, et al. Prevalence and survival of smouldering Waldenström macroglobulinaemia in the United States. Br J Haematol. 2019; 184 (6): 1014–1017.
- • Puente XS, Pinyol M, Quesada V, et al. Whole-genome sequencing identifies recurrent mutations in chronic lymphocytic leukaemia. Nature. 2011; 475 (7354): 101–105.
- • Rajkumar SV, Gertz MA, Kyle RA. Prognosis of patients with primary systemic amyloidosis who present with dominant neuropathy. Am J Med. 1998; 104 : 232–237.
- • Schop RFJ, Fonseca R. Genetics and cytogenetics of Waldenstrom’s macroglobulinemia. Semin Oncol. 2003; 30 : 142–145.
- • Simon L, Fitsiori A, Lemal R, et al. Bing-Neel syndrome, a rare complication of Waldenström macroglobulinemia: analysis of 44 cases and review of the literature. A study on behalf of the French Innovative Leukemia Organization (FILO). Haematologica. 2015; 100 (12): 1587–1594.
- • Stone MJ. Waldenström’s macroglobulinemia: hyperviscosity syndrome and cryoglobulinemia. Clin Lymphoma Myeloma. 2009; 9 (1): 97–99.
- • Stone MJ, Bogen SA. Evidence-based focused review of management of hyperviscosity syndrome. Blood. 2012; 119 : 2205–2208.
- • Tam CS, LeBlond V, Novotny W et al. A head-to-head Phase III study comparing zanubrutinib versus ibrutinib in patients with Waldenström macroglobulinemia. Future Oncol. 2018; 14 (22): 2229–2237.
- • Teras LR, DeSantis CE, Cerhan JR, et al. US lymphoid malignancy statistics by World Health Organization subtypes. CA Cancer J Clin. 2016; 66 (6): 443–459.
- • Terrier B, Jaccard A, Harousseau JL, et al. The clinical spectrum of IgM-related amyloidosis: a French nationwide retrospective study of 72 patients. Medicine (Baltimore). 2008; 87 (2): 99–109.
- • Treon SP. How I treat Waldenström macroglobulinemia. Blood. 2009; 114 (12): 2375–2385.
- • Treon SP, Xu L, Yang G, et al. MYD88 L265P somatic mutation in Waldenström’s macroglobulinemia. N Engl J Med. 2012; 367: 826–833.
- • Treon SP, Tripsas CK, Ciccarelli BT, et al. Patients with Waldenström macroglobulinemia commonly present with iron deficiency and those with severely depressed transferrin saturation levels show response to parenteral iron administration. Clin Lymphoma Myeloma Leuk. 2013; 13 (2): 241–243.
- • Treon, SP, Cao Y, Xu L, et al. Somatic mutations in MYD88 and CXCR4 are determinants of clinical presentation and overall survival in Waldenstrom macroglobulinemia. Blood. 2014; 123 : 2791–2796.
- • Treon SP, Xu L, Hunter Z. MYD88 Mutations and response to ibrutinib in Waldenström’s macroglobulinemia. N Engl J Med. 2015; 373 (6): 584–586.
- • Treon SP, Tripsas CK, Meid K et al. Ibrutinib in previously treated Waldenström‘s macroglobulinemia. Engl J Med. 2015; 372 (15): 1430–1440.
- • Treon SP. How I treat Waldenström macroglobulinemia. Blood. 2015; 126 (6): 721–732.
- • Treon SP, Gustine J, Meid K et al. Ibrutinib monotherapy in symptomatic, treatment-naïve patients with Waldenström macroglobulinemia. Clin Oncol. 2018; 36 (27): 2755–2761.
- • Treon SP, Meid K, Gustine J, et al. Ibrutinib monotherapy produces long-term disease control in previously treated Waldenström’s macroglobulinemia: Final report of the Pivotal trial (NCT01614821). Hematol Oncol. 2019; 37 (Suppl): 184-185 (abstr 135).
- • Treon SP, Xu L, Guerrera ML, et al. Genomic landscape of Waldenström macroglobulinemia and its impact on treatment strategies. J Clin Oncol. 2020; 38 (11): 1198–1208.
- • Trøen G, Warsame A, Delabie J. CD79B and MYD88 mutations in splenic marginal zone lymphoma. ISRN Oncol. 2013; 252318.
- • Vlam L, Piepers S, Sutedja NA, et al. Association of IgM monoclonal gammopathy with progressive muscular atrophy and multifocal motor neuropathy: a case-control study. J Neurol. 2015; 262 (3): 666–673.
- • Vos JMI, Minnema MC, Wijermans PW, et al. Guideline for diagnosis and treatment of Waldenström’s macroglobulinaemia. Neth J Med. 2013; 71 : 54–62.
- • Vos JM, Manning RR, Meid K, et al. Defining the incidence, pathology and clinical outcomes of kidney disease related to Waldenstrom’s macroglobulinemia and IgM MGUS. Blood. 2015; 126 : 3926.
- • Wang, L, Lawrence MS, Wan Y, et al. SF3B1 and other novel cancer genes in chronic lymphocytic leukemia. N Engl J Med. 2011; 365 : 2497–2506.
- • Wang H, Chen Y, Li F, Delasalle K, et al. Temporal and geographic variations of Waldenström macroglobulinemia incidence: a large population-based study. Cancer. 2012; 118 (15): 3793–3800.
- • WHO classification of tumours of haematopoietic and lymphoid tissues. Vol. 2 (Ed Revised 4th Edition). Geneva: WHO Press 2017.
- • Xu L, Hunter ZR, Yang G, et al. MYD88 L265P in Waldenström macroglobulinemia, immunoglobulin M monoclonal gammopathy, and other B-cell lymphoproliferative disorders using conventional and quantitative allele-specific polymerase chain reaction. Blood. 2013; 121 (11): 2051–2058.
LITERATURA PRO LÉČEBNOU ČÁST
- • Abbi KKS, Muzaffar M, Gaudin D, et al. Primary CNS lymphoplasmacytic lymphoma: a case report and review of literature. Hematol Oncol Stem Cell Ther. 2013; 6 (2): 76–78.
- • Abdallah AO, Atrash S, Muzaffar J, et al. Successful treatment of Bing-Neel syndrome using intrathecal chemotherapy and systemic combination chemotherapy followed by BEAM auto-transplant: a case report and review of literature. Clin Lymphoma Myeloma Leuk. 2013; 13 (4): 502–506.
- • Adam Z, Krejčí M, Pour L, et al. Obinutuzumab v léčbě pacientky s Waldenströmovou makroglobulinémií netolerující rituximab: popis případu. Transfuze Hematol Dnes. 2021; 27 (2): 160–165.
- • Anagnostopoulos A, Giralt S. Stem cell transplantation (SCT) for Waldenstrom’s macroglobulinemia (WM). Bone Marrow Transplant. 2002; 29 : 943–947.
- • Anagnostopoulos A, Hari PN, Pérez WS, et al. Autologous or allogeneic stem cell transplantation in patients with Waldenstrom’s macroglobulinemia. Biol Blood Marrow Transplant. 2006; 12 (8): 845–854.
- • Ansell SM, Kyle RA, Reeder CB, et al. Diagnosis and management of Waldenström macroglobulinemia: Mayo stratification of macroglobulinemia and risk-adapted therapy (mSMART) guidelines. Mayo Clin Proc. 2010; 85 : 824–833.
- • Bachanova V, Burns LJ. Hematopoietic cell transplantation for Waldenstrom macroglobulinemia. Bone Marrow Transplant. 2012; 47 (3): 330–336.
- • Barta SK, Li H, Hochster HS, et al. Randomized phase 3 study in low-grade lymphoma comparing maintenance anti-CD20 antibody with observation after induction therapy: A trial of the ECOG-ACRIN Cancer Research Group (E1496). Cancer. 2016; 122 (19): 2996–3004.
- • Buske C, Hoster E, Dreyling M, et al. The addition of rituximab to front-line therapy with CHOP (R-CHOP) results in a higher response rate and longer time to treatment failure in patients with lymphoplasmacytic lymphoma: results of a randomized trial of the German Low-Grade Lymphoma Study Group (GLSG). Leukemia. 2009; 23 (1): 153–161.
- • Buske C, Leblond V. How to manage Waldenstrom’s macroglobulinemia. Leukemia. 2013; 27 : 762–772.
- • Buske C, Sadullah S, Kastritis E, et al. Treatment and outcome patterns in European patients with Waldenström’s macroglobulinaemia: a large, observational, retrospective chart review. Lancet Haematol. 2018; 5 (7): e299–e309.
- • Buske C, Dimopoulos MA, Grunenberg A, et al. Bortezomib in combination with dexamethasone, rituximab and cyclophosphamide (B-DRC) as first-line treatment of Waldenstrom‘s macroglobulinemia: results of a prospectively randomized multicenter European phase II trial. Blood. 2020; 136 (Supplement 1): 26.
- • Buske C, Tedeschi A, Trotman J, et al. Ibrutinib plus rituximab versus placebo plus rituximab for Waldenström‘s macroglobulinemia: final analysis from the randomized phase III iNNOVATE study. J Clin Oncol. 2022; 40 (1): 52–62.
- • Cabannes-Hamy A, Lemal R, Goldwirt L, et al.Efficacy of ibrutinib in the treatment of Bing-Neel syndrome. Am J Hematol. 2016; 91 (3): e17–e19.
- • Cao Y, Yang G, Hunter ZR, et al. The BCL2 antagonist ABT-199 triggers apoptosis, and augments ibrutinib and idelalisib mediated cytotoxicity in CXCR4Wild-type and CXCR4WHIM mutated Waldenstrom macroglobulinaemia cells. Br J Haematol. 2015; 170 : 134–138.
- • Castellani F, Visentin A, Campagnolo M et al.; The Bruton tyrosine kinase inhibitor ibrutinib improves anti-MAG antibody polyneuropathy. Neurol Neuroimmunol Neuroinflamm. 2020; 7 (4): e720.
- • Castillo JJ, Kanan S, Meid K, et al. Rituximab intolerance in patients with Waldenström macroglobulinaemia. Br J Haematol. 2016; 174 (4): 645–648.
- • Castillo JJ, D‘Sa S, Lunn MP, et al. Central nervous system involvement by Waldenström macroglobulinaemia (Bing-Neel syndrome): a multi-institutional retrospective study. Br J Haematol. 2016; 172 (5): 709–715.
- • Castillo JJ, Gustine JN, Meid K, et al. Idelalisib in Waldenström macroglobulinaemia: high incidence of hepatotoxicity. Leuk Lymphoma. 2017; 58 : 1002–1004.
- • Castillo JJ, Gustine J, Meid K, et al. Bendamustine and bortezomib-containing regimens produce higher response rates and more durable responses versus cyclophosphamide-based therapy in frontline Waldenström macroglobulinemia. Blood. 2017; 130 : 1488.
- • Castillo JJ, SP. Toward personalized treatment in Waldenström macroglobulinemia. Hematology Am Soc Hematol Educ Program. 2017; 365–370.
- • Castillo JJ, Meid K, Gustine JN, et al. Prospective clinical trial of ixazomib, dexamethasone, and rituximab as primary therapy in Waldenstrom macroglobulinaemia. Clin Cancer Res. 2018; 24 : 3247–3252.
- • Castillo JJ, Gustine JN, Meid K, et al. Response and survival for primary therapy combination regimens and maintenance rituximab in Waldenström macroglobulinaemia. Br J Haematol. 2018; 181 : 77–85.
- • Castillo JJ, Gustine JN, Meid K, Dubeau T, Severns P, Treon SP. Ibrutinib withdrawal symptoms in patients with Waldenström macroglobulinaemia. Haematologica. 2018; 103: e307–e310.
- • Castillo JJ, Gustine JN, Meid K, et al. Multicenter prospective phase II study of venetoclax in patients with previously treated Waldenstrom macroglobulinaemia. Blood. 2018; 132 (Suppl): 2888 (abstr).
- • Castillo JJ, Itchaki G, Paludo J, et al. Ibrutinib for the treatment of Bing-Neel syndrome: a multicenter study. Blood. 2019; 133 : 299–305.
- • Castillo JJ, Treon SP. How we manage Bing–Neel syndrome. Br J Haematol. 2019; 187 : 277–285.
- • Castillo J J, Advani RH, Branagan AR, et al. Consensus treatment recommendations from the tenth International Workshop for Waldenström Macroglobulinaemia 2020. Lancet Haematol. 2020; 7 (11): e827–e837.
- • Castillo JJ, Meid K, Flynn CA, et al. Ixazomib, dexamethasone, and rituximab in treatment-naive patients with Waldenström macroglobulinemia: long-term follow-up. Blood Adv. 2020; 4 (16): 3952–3959. doi: 10.1182/bloodadvances.2020001963.
- • Castillo JJ, Meid K, Gustine JN, et al. Long-term follow-up of ibrutinib monotherapy in treatment-naive patients with Waldenström macroglobulinemia. Leukemia; publikováno electronicky 16. září 2021. doi: 10.1038/s41375-021-01417-9..
- • Chen CI, Kouroukis CT, White D, et al. Bortezomib is active in patients with untreated or relapsed Waldenstrom’s macroglobulinemia: a phase II study of the National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol. 2007; 25 (12): 1570–1575.
- • Clark WF, Rock GA, Buskard N, et al. Therapeutic plasma exchange: an update from the Canadian Apheresis Group. Ann Intern Med. 1999; 131 : 453–462.
- • D‘Sa S, Kersten M J, Castillo JJ, et al. Investigation and management of IgM and Waldenström associated peripheral neuropathies: recommendations from the IWWM8 consensus panel. Br J Haematol. 2017 : 176 : 728–742.
- • Dhedin N, Tabrizi R, Bulabois PE, et al. Hematopoietic stem cell transplantation (HSCT) in Waldenstrom macroglobulinemia (WM): update of the French experience in 54 cases. Haematologica. 2007; 92 (S): 228.
- • Dimopoulos MA, Zervas C, Zomas A, et al. Treatment of Waldenström’s macroglobulinemia with rituximab. J Clin Oncol. 2002; 20 (9): 2327–2333.
- • Dimopoulos MA, Hamilos G, Efstathiou E, et al. Treatment of Waldenstrom‘smacroglobulinemia with the combination of fludarabine and cyclophosphamide. LeukLymphoma. 2003; 44 (6): 993–996.
- • Dimopoulos MA, Anagnostopoulos A, Kyrtsonis MC, et al. Treatment of relapsed or refractory Waldenström’s macroglobulinemia with bortezomib. Haematologica. 2005; 90 (12): 1655–1658.
- • Dimopoulos MA, Anagnostopoulos A, Kyrtsonis MC, et al. Primary treatment of Waldenström macroglobulinemia with dexamethasone, rituximab, and cyclophosphamide. J Clin Oncol. 2007; 25 (22): 3344–3349.
- • Dimopoulos MA, Garcia-Sanz R, Gavriatopoulou M, et al. Primary therapy of Waldenström macroglobulinemia (WM) with weekly bortezomib, low-dose dexamethasone, and rituximab (BDR): long-term results of a phase 2 study of the European Myeloma Network (EMN). Blood. 2013; 122 (19): 3276–3282.
- • Dimopoulos MA, Trotman J, Tedeschi A, et al. Ibrutinib for patients with rituximab-refractory Waldenström’s macroglobulinaemia (iNNOVATE): an open-label substudy of an international, multicentre, phase 3 trial. Lancet Oncol. 2017; 18 (2): 241–250.
- • Dimopoulos MA, Tedeschi A, Trotman J, et al. iNNOVATE Study Group and the European Consortium for Waldenström’s Macroglobulinemia. Phase 3 trial of ibrutinib plus rituximab in Waldenström’s macroglobulinemia. N Engl J Med. 2018; 378 (25): 2399–2410.
- • Drew MJ. Plasmapheresis in the dysproteinemias. Ther Apher. 2002; 6 : 45–52.
- • Furman RR, Eradat H, DiRienzo CG, et al. A Phase II Trial of Ofatumumab in Subjectswith Waldenstrom‘s Macroglobulinemia. Blood. 2011; 118 (21): 1581–1581.
- • Garcia-Sanz R, Dimopoulos MA, Lee H-P, et al. Updated results of the ASPEN trial from a cohort of patients with MYD88 wild-type (MYD88WT) Waldenström macroglobulinemia (WM). J Clin Oncol. 2020; 38 (15_suppl): e20056-e20056.
- • Gavriatopoulou M, García-Sanz R, Kastritis E et al. BDR in newly diagnosed patients with WM: final analysis of a phase 2 study after a minimum follow-up of 6 years., Blood. 2017; 129 (4): 456–459.
- • Gertz MA, Rue M, Blood E, et al. Multicenter phase 2 trial of rituximab for Waldenström macroglobulinemia (WM): an Eastern Cooperative Oncology Group Study (E3A98). Leuk Lymphoma. 2004; 45 (10): 2047–2055.
- • Gertz MA, Abonour R, Heffner LT, et al. Clinical value ofminor responses after 4 doses of rituximab in Waldenstrom macroglobulinaemia: afollow-up of the Eastern Cooperative Oncology Group E3A98 trial. Br J Haematol.2009; 147 (5): 677–680.
- • Gertz MA, Reeder CB, Kyle RA, et al. Stem cell transplant for Waldenström macroglobulinemia: an underutilized technique. Bone Marrow Transplant. 2012; 47 : 1147–1153.
- • Ghobrial IM, Hong F, Padmanabhan S, et al. Phase II trial of weekly bortezomib in combination with rituximab in relapsed or relapsed and refractory Waldenstrom macroglobulinemia. J Clin Oncol. 2010; 28 (8): 1422–1428.
- • Ghobrial IM, Gertz M, Laplant B, et al. Phase II trial of the oral mammalian target ofrapamycin inhibitor everolimus in relapsed or refractory Waldenstrommacroglobulinemia. J Clin Oncol. 2010; 28 (8): 1408–1414.
- • Ghobrial IM, Witzig TE, Gertz M, et al. Long-term results of the phase II trial of the oral mTOR inhibitor everolimus (RAD001) in relapsed or refractory Waldenstrom Macroglobulinemia. Am J Hematol. 2014; 89 (3): 237–242.
- • Ghobrial IM, Redd R, Armand P, et al. Phase I/II trial of everolimus in combination with bortezomib and rituximab (RVR) in relapsed/refractory Waldenstrom macroglobulinemia. Leukemia. 2015; 29 (12): 2338–2346.
- • Ghobrial IM, Savona MR, Vij R, et al. Final results from a multicenter, open-label, dose-escalation phase 1b/2 study of single-agent oprozomib in patients with hematologic malignancies. Blood. 2016 128 : 2110.
- • Gilleece MH, Pearce R, Linch DC, et al. The outcome of haemopoietic stem cell transplantation in the treatment of lymphoplasmacytic lymphoma in the UK: a British Society Bone Marrow Transplantation study. Hematology. 2008; 13 : 119–127.
- • Gopal AK, Kahl BS, de Vos S, et al. PI3Kd inhibition by idelalisib in patients with relapsed indolent lymphoma. N Engl J Med. 2014; 370 : 1008–1018.
- • Gustine JN, Meid K, Dubeau T, et al. Ibrutinib discontinuation in Waldenström macroglobulinemia: Etiologies, outcomes, and IgM rebound. Am J Hematol. 2018; 93 (4): 511–517.
- • Gustine J, Meid K, Dubeau T, et al. Impact of ibrutinib dose intensity on patient outcomes in previously treated Waldenström macroglobulinemia. Blood. 2017; 130 (Suppl 1): 4051.
- • Hoang-Xuan K, Bessell E, Bromberg J, et al. Diagnosis and treatment of primary CNS lymphoma in immunocompetent patients: guidelines from the European Association for Neuro-Oncology. Lancet Oncol. 2015; 16 (7): e322–e332.
- • Hochster H, Weller E, Gascoyne RD, et al. Maintenance rituximab after cyclophosphamide, vincristine, and prednisone prolongs progression-free survival in advanced indolent lymphoma: results of the randomized phase III ECOG1496 Study. J Clin Oncol. 2009; 27 (10): 1607–1614.
- • Imai F, Fujisawa K, Kiya N, et al. Intracerebral infiltration by monoclonal plasmacytoid cells in Waldenstrom‘s macroglobulinemia – case report. Neurol Med Chir (Tokyo). 1995; 35 (8): 575–579.
- • Kanan S, Meid K, Treon SP, et al. Clinical characteristics of rituximab intolerance in patients with Waldenstrom’s macroglobulinemia. Blood. 2014; 124 : 2610.
- • Kapoor P, Ansell SM, Fonseca R, et al. Diagnosis and management of Waldenström macroglobulinemia: Mayo stratification of macroglobulinemia and risk-adapted therapy (mSMART) Guidelines 2016. JAMA Oncol. 2017; 3 (9): 1257–1265.
- • Kastritis E, Gavriatopoulou M, Kyrtsonis MCh, et al. Dexamethasone, rituximab, and cyclophosphamide as primary treatment of Waldenström macroglobulinemia: final analysis of a phase 2 study. Blood. 2015; 126: 1392–1394.
- • Kastritis E, Leblond V, Dimopoulos MA, et al. Waldenström’s macroglobulinaemia: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2018; 29 (Suppl 4): iv41–iv50.
- • Kastritis E, Dimopoulos MA. Proteasome inhibitors in Waldenström macroglobulinemia. Hematol Oncol Clin North Am. 2018; 32 : 829–840.
- • Kaščák M, Hájek R, Minařík J, et al. M. Diagnostika a léčba Waldenströmovy makroglobulinemie. Transfuze Hematol Dnes. 2019; 25 (Suppl. 1): 7–33.
- • Kaščák M, Kufová Z, Growková K, et al. Waldenströmova makroglobulinémie v roce 2016: optimalizace imunochemoterapie s cílem minimalizace nežádoucích účinků. Onkológia Prax. 2016; 5 : 291–295.
- • Kaščák M, Ďuraš J, Navrátil M, et al. Autologní transplantace kmenových buněk u Waldenströmovy makroglobulinémie. Transfuze Hematol Dnes. 2016; 22 (1): 28–38.
- • Katzmann JA, Snyder MR, Rajkumar SV, et al. Long-term biological variation of serum protein electrophoresis M-spike, urine M-spike, and monoclonal serum free light chain quantification: implications for monitoring monoclonal gammopathies. Clin Chem. 2011; 57 (12): 1687–1692.
- • Kersten MJ, Minnema MC, Vos JM, et al. Ixazomib, rituximab and dexamethasone (IRD) in patients with relapsed or progressive Waldenstrom’s macroblobulinaemia: results of the prospective phase I/II HOVON 124/Ecwm-R2 Trial. Blood. 2019; 134 : 344.
- • Kersten MJ, Amaador K, Minnema MC, et al. Combining ixazomib with subcutaneous rituximab and dexamethasone in relapsed or refractory Waldenström‘s macroglobulinemia: final analysis of the phase I/II HOVON124/ECWM-R2 study. J Clin Oncol. 2022; 40 (1): 40–51.
- • Kyriakou C, Canals C, Taghipour G, et al. Autologous stem cell transplantation (ASCT) for patients with Waldenstrom’s macroglobulinaemia: an analysis of 201 cases from the European Bone Marrow Transplant Registry (EBMT). Haematologica. 2007; 92 (S2): 228.
- • Kyriakou C, Advani RH, Ansell SM, et al. Indications for hematopoietic stem cell transplantation in patients with Waldenstrom’s macroglobulinemia: a consensus project of the EBMT Lymphoma Working Party (LWP) / European Consortium for Waldenstrom’s Macroglobulinemia (ECWM) /International Waldenstrom’s Macroglobulinemia Foundation (IWMF). Blood. 2017; 130 : 2026.
- • Kyriakou C, Canals C, Sibon D, et al. High-dose therapy and autologous stem-cell transplantation in Waldenstrom macroglobulinemia: the Lymphoma Working Party of the European Group for Blood and Marrow Transplantation. J Clin Oncol. 2010; 28 (13): 2227–2232.
- • Laribi K, Poulain S, Willems L et al. Bendamustine plus rituximab in newly-diagnosed Waldenström macroglobulinaemia patients. A study on behalf of the French Innovative Leukaemia Organization (FILO). Br J Haematol. 2019; 186 (1): 146–149.
- • Laszlo D, Andreola G, Rigacci L, et al. Rituximab and subcutaneous 2-chloro-2 ‚-deoxyadenosine as therapy in untreated and relapsed Waldenstrom‘s macroglobulinemia. Clinical Lymphoma Myeloma & Leukemia. 2011; 11 (1): 130–132.
- • Leblond V, Johnson S, Chevret S, et al. Results of a randomized trial of chlorambucilversus fludarabine for patients with untreated Waldenstrom macroglobulinemia, marginalzone lymphoma, or lymphoplasmacytic lymphoma. J Clin Oncol. 2013; 31 (3): 301–307.
- • Leblond V, Kastritis E, Advani R, et al. Treatment recommendations from the Eighth International Workshop on Waldenström’s Macroglobulinemia. Blood. 2016; 128 (10): 1321–1328.
- • Leleu X, Soumerai J, Roccaro A, et al. Increased incidence of transformation and myelodysplasia/acute leukemia in patients with Waldenström macroglobulinemia treated with nucleoside analogs. J Clin Oncol. 2009; 27 (2): 250–255.
- • NCCN Guidelines Version 1.2018 Waldenström’s Macroglobulinemia/Lymphoplasmacytic lymphoma. Dostupné on-line na: https: //www.nccn.org/professionals/physician_gls/default.aspx#site.
- • Mahmood A, Sodano D, Dash A, et al. Therapeutic plasma exchange performed in tandem with hemodialysis for patients with M-protein disorders. J Clin Apher. 2006; 21 (2): 100–104.
- • Malkani RG, Tallman M, Gottardi-Littell N, et al. Bing-Neel syndrome: an illustrative case and a comprehensive review of the published literature. J Neurooncol. 2010; 96 (3): 301–312.
- • Mason C, Savona S, Rini JN, et al. Ibrutinib penetrates the blood brain barrier and shows efficacy in the therapy of Bing Neel syndrome. Br J Haematol. 2017; 179 (2): 339–341.
- • Menke MN, Feke GT, McMeel JW, et al. Ophthalmologic techniques to assess the severity of hyperviscosity syndrome and the effect of plasmapheresis in patients with Waldenström‘s macroglobulinemia. Clin Lymphoma Myeloma. 2009; 9 : 100–103.
- • Minnema MC, Kimby E, D’Sa S, et al. Guideline for the diagnosis, treatment and response criteria for Bing-Neel syndrome. Haematologica. 2017; 102 (1): 43–51.
- • Munshi NC, Barlogie B. Role for high-dose therapy with autologous hematopoietic stem cell support in Waldenstrom’s macroglobulinemia. Semin Oncol. 2003; 30 : 282–285.
- • Olszewski AJ, Treon SP, Castillo JJ. Comparative effectiveness of rituximab-based immunochemotherapy in Waldenstrom’s macroglobulinemia (WM). Blood. 2016; 128 : 2986.
- • Olszewski AJ, Chen C, Gutman R, et al. Comparative outcomes of immunochemotherapy regimens in Waldenström macroglobulinaemia. Br J Haematol. 2017; 179 : 106–115.
- • Owen RG, Kyle RA, Stone MJ, et al. Response assessment in Waldenström macroglobulinaemia: update from the VIth International Workshop. Br J Haematol. 2013; 160 (2): 171–176.
- • Owen RG, McCarthy H, Rule S, et al. Acalabrutinib monotherapy in patients with Waldenström macroglobulinemia: a single-arm, multicentre, phase 2 study. Lancet Haematol. 2020; 7 (2): e112–e121.
- • Paludo J, Abeykoon JP, Hesse AB, et al. Bendamustine and rituximab versus dexamethasone, rituximab and cyclophosphamide in patients with Waldenstrom macroglobulinemia (WM). Blood. 2016; 128 : 2968.
- • Paludo J, Abeykoon JP, Kumar S, et al. Dexamethasone, rituximab and cyclophosphamide for relapsed and/or refractory and treatment-naïve patients with Waldenstrom macroglobulinemia. Br J Haematol. 2017; 179 (1): 98–105.
- • Pika T, Hegenbart U, Flodrova P, et al. First report of ibrutinib in IgM-related amyloidosis: few responses, poor tolerability, and short survival. Blood. 2018; 131 (3): 368–371.
- • Rezvani AR, Maloney DG. Rituximab resistance. Best Pract Res Clin Haematol. 2011; 24 : 203–216.
- • Rummel MJ, Niederle N, Maschmeyer G, et al. Bendamustine plus rituximab versus CHOP plus rituximab as first-line treatment for patients with indolent and mantle-cell lymphomas: an open-label, multicentre, randomised, phase 3 non-inferiority trial. Lancet. 2013; 381 (9873): 1203–1210.
- • Rummel MJ, Lerchenmüller C, Hensel M, et al. Two years rituximab maintenance vs observation after first line treatment with bendamustine plus rituximab (B-R) in patients with Waldenström’s macroglobulinaemia (MW): results of a prospective, randomised, multicentre phase 3 study (the StiL NHL7-2008 MAINTAIN trial). Blood. 2019; 134 (suppl 1): 343.
- • Saad S, Wang TJC. Neurocognitive deficits after radiation therapy for brain malignancies. Am J Clin Oncol. 2015; 38 : 634–640.
- • Salles G, Seymour JF, Offner F, et al. Rituximab maintenance for 2 years in patients with high tumour burden follicular lymphoma responding to rituximab plus chemotherapy (PRIMA): a phase 3, randomised controlled trial. Lancet. 2011; 377 (9759): 42–51.
- • Shimizu K, Fujisawa K, Yamamoto H, et al. Importance of central nervous system involvement by neoplastic cells in a patient with Waldenström’s macroglobulinemia developing neurologic abnormalities. Acta Haematologica. 1993; 90 : 206–208.
- • Sidiqi MH, Buadi FK, Dispenzieri A et al.; Autologous stem cell transplant for IgM-associated amyloid light-chain amyloidosis. Biol Blood Marrow Transplant. 2019; 25 (3): e108–e111.
- • Simon, L, Fitsiori A, Lemal R, et al. Bing-Neel syndrome, a rare complication of Waldenström macroglobulinemia: analysis of 44 cases and review of the literature. A study on behalf of the French Innovative Leukemia Organization (FILO). Haematologica. 2015; 100 (12): 1587–1594.
- • Sklavenitis-Pistofidis R, Capelletti M, Liu CJ et al.; Bortezomib overcomes the negative impact of CXCR4 mutations on survival of Waldenstrom macroglobulinemia patients. Blood. 2018; 132 (24): 2608–2612.
- • Souchet-Compain L, Nguyen S, Choquet S, et al. Primary therapy of Waldenström macroglobulinemia with nucleoside analogue-based therapy. Clin Lymphoma Myeloma Leuk. 2013; 13 : 227–230.
- • Souchet L, Levy V, Ouzegdouh M, et al. Efficacy and long-term toxicity of the rituximab-fludarabine-cyclophosphamide combination therapy in Waldenstrom’s macroglobulinemia. Am J Hematol. 2016; 91 (8): 782–786.
- • Stone MJ, Bogen SA. Evidence-based focused review of management of hyperviscosity syndrome. Blood. 2012; 119 : 2205–2208.
- • Tam CS, Wolf M, Prince HM, et al. Fludarabine, cyclophosphamide, and rituximab for the treatment of patients with chronic lymphocytic leukemia or indolent non-Hodgkin lymphoma. Cancer. 2006; 106 (11): 2412–2420.
- • Tam CS, LeBlond V, Novotny W, et al. A head-to-head Phase III study comparing zanubrutinib versus ibrutinib in patients with Waldenström macroglobulinemia. Future Oncol. 2018; 14 (22): 2229–2237.
- • Tam CS, Opat S, D’Sa S, et al. A randomised phase 3 trial of Zanubrutinib versus Ibrutinib in symptomatic Waldenström macroglobulinaemia: the ASPEN study. Blood. 2020; 136 : 2038–2050.
- • Tedeschi A, Benevolo G, Varettoni M, et al. Fludarabine plus cyclophosphamide and rituximab in Waldenstrom macroglobulinemia: an effective but myelosuppressive regimen to be offered to patients with advanced disease. Cancer. 2012; 118 (2): 434–443.
- • Tedeschi A, Picardi P, Ferrero S, et al. Bendamustine and rituximab combination is safe and effective as salvage regimen in Waldenström macroglobulinemia. Leuk Lymphoma. 2015; 56 (9): 2637–2642.
- • Tedeschi A, Picardi P, Goldaniga MC, et al. Long term toxicity and follow-up of Waldenstrom’s macroglobulinemia patients after salvage treatment with fludarabine cyclophosphamide rituximab or bendamustine and rituximab. Blood. 2015; 126 : 3958.
- • Tomowiak C, Poulain S, Herbaux C, et al. on behalf of the FILO Group, Obinutuzumab and idelalisib in symptomatic patients with relapsed/refractory Waldenström macroglobulinemia. Blood Adv. 2021; 5 (9): 2438–2446.
- • Tournilhac O, Leblond V, Tabrizi R, et al. Transplantation in Waldenstrom’s macroglobulinemia – the French experience. Semin Oncol. 2003; 30 : 291–296.
- • Treon SP, Emmanouilides C, Kimby E, et al. Extended rituximab therapy in Waldenström’s macroglobulinemia. Ann Oncol. 2005; 16 (1): 132–138.
- • Treon SP, Branagan AR, Hunter Z, et al. Paradoxical increases in serum IgM and viscosity levels following rituximab in Waldenstrom’s macroglobulinemia. Ann Oncol. 2004; 15 (10): 1481–1483.
- • Treon SP, Hunter ZR, Matous J, et al. Multicenter clinical trial of bortezomib in relapsed/refractory Waldenstrom’s macroglobulinemia: results of WMCTG Trial 03-248. Clin Cancer Res. 2007; 13 (11): 3320–3325.
- • Treon SP, Soumerai JD, Branagan AR, et al. Thalidomide and rituximab in Waldenstrom macroglobulinemia. Blood. 2008; 112 (12): 4452–4457.
- • Treon SP, Soumerai JD, Branagan AR et al., Lenalidomide and Rituximab in Waldenstrom‘s Macroglobulinemia. Clin Cancer Res. 2009; 15 (1): 355–360. doi: 10.1158/1078-0432.CCR-08-0862.
- • Treon SP, Branagan AR, Ioakimidis L, et al. Long-term outcomes to fludarabine and rituximab in Waldenström macroglobulinemia. Blood. 2009; 113 : 3673–3678.
- • Treon SP, Ioakimidis L, Soumerai JD, et al. Primary therapy of Waldenström macroglobulinaemia with bortezomib, dexamethasone, and rituximab: WMCTG clinical trial 05-180. J Clin Oncol. 2009; 27 : 3830–3835.
- • Treon SP, Hanzis C, Manning RJ, et al. Maintenance rituximab is associated with improved clinical outcome in rituximab naïve patients with Waldenstrom macroglobulinaemia who respond to a rituximab-containing regimen. Br J Haematol. 2011; 154 (3): 357–362.
- • Treon SP, Hanzis C, Tripsas C, et al. Bendamustine therapy in patients with relapsed or refractory Waldenström’s macroglobulinemia. Clin Lymphoma Myeloma Leuk. 2011; 11 (1): 133–135.
- • Treon SP, Hunter ZR. A new era for Waldenstrom macroglobulinemia: MYD88 L265P. Blood. 2013; 121 (22): 4434–4436.
- • Treon SP, Tripsas CK, Meid K, et al. Carfilzomib, rituximab, and dexamethasone (CaRD) treatment offers a neuropathy-sparing approach for treating Waldenström’s macroglobulinemia. Blood. 2014; 124 (4): 503–510.
- • Treon SP, Tripsas ChK, Meid K, et al. Ibrutinib in previously treated Waldenström’s macroglobulinemia. N Engl J Med. 2015; 372 : 1430–1440.
- • Treon SP, Gustine J, Meid K, et al. Ibrutinib is highly active as first line therapy in symptomatic Waldenstrom’s macroglobulinemia. Blood. 2017; 130 : 2767.
- • Treon SP, Meid K, Gustine J, et al. Long-term follow-up of previously treated patients who received ibrutinib for symptomatic Waldenstrom’s macroglobulinemia: update of pivotal clinical trial. Blood. 2017; 130 : 2766.
- • Treon SP, Gustine J, Meid K, et al. Ibrutinib monotherapy in symptomatic, treatment-naïve patients with Waldenström macroglobulinemia. J Clin Oncol. 2018; 36 (27): 2755–2761.
- • Treon SP, Meid K, Gustine J, et al. Ibrutinib monotherapy produces long-term disease control in previously treated Waldenström’s macroglobulinemia: Final report of the Pivotal trial (NCT01614821). Hematol Oncol. 2019; 37 (Suppl): 184–185 (abstr 135).
- • Treon SP, Xu L, Guerrera ML, et al. Genomic landscape of Waldenström macroglobulinemia and its impact on treatment strategies. J Clin Oncol.2020; 38 (11): 1198–1208.
- • Tripsas C, Ioakimidis LI, Hunter ZR, et al. Comparative response assessment by total serum IgM and IgM M‐component in Waldenstrom‘s macroglobulinemia. J Clin Oncol. 2012; 30: e18575.
- • Trotman J, Opat S, Gottlieb D, et al. Zanubrutinib for the treatment of patients with Waldenström macroglobulinemia: three years of follow-up. Blood. 2020; 136 : 2027–2037.
- • Van Cauwenberge MG, Depreter B, Dumoulin EN, et al. Bing-Neel syndrome: Two unexpected cases and a review of the literature. Neurol Sci. 2015; 356 (1–2): 19–26.
- • van Oers MHJ, Van Glabbeke M, Teodorovic I, et al. Chimeric antiCD20 monoclonal antibody (rituximab; Mabthera®) in remission induction and maintenance treatment of relapsed/resistant follicular nonHodgkin’s lymphoma: a phase III randomized intergroup clinical trial. Blood. 2004; 104 : 41A.
- • Varettoni M, Marchioni E, Bonfichi M, et al. Successful treatment with rituximab and bendamustine in a patient with newly diagnosed Waldenström‘s macroglobulinemia complicated by Bing-Neel syndrome. Am J Hematol. 2015; 90 (8): e152–e153.
- • Vesole DH, Richter J, Biran N, et al. Carfilzomib as salvage therapy in Waldenstrom macroglobulinemia: a case series. Leuk Lymphoma. 2018; 59 (1): 259–261.
- • Wagner-Johnston ND, Schuster SJ, de Vos S, et al. Long-term follow-up of idelalisib monotherapy in patients with double refractory marginal zone lymphoma or lymphoplasmacytic lymphoma/ Waldenstrom’s macroglobulinaemia. Blood. 2019; 134 (suppl): 4006.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2022 Číslo Supplementum 1- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
Nejčtenější v tomto čísle- Diagnostika a léčba Waldenströmovy makroglobulinémie
- Diagnostika a léčba systémové AL amyloidózy
- Editorial
- Editorial
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



