-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Idiopatické střevní záněty
Idiopatické střevní záněty
Crohn’s disease (CD) and ulcerative colitis (UC) are chronic inflammatory bowel diseases (IBD) of unknown origin with a distinct west-east and north-south gradient in their geographic distribution. Unidentified external factors in combination with genetic predisposition and intestinal microbiome are supposed to cause both diseases. Periods of clinical activity and quiescent phases are typical of the disease course. Patients suffer from abdominal pain and diarrhoea, bloody stools usually occur in UC, while CD patients frequently develop purulent complications – intra-abdominal or perianal abscesses and fistulas. Patients have to use long-term medical treatment with aminosalicylates, corticosteroids, immunosuppressive drugs or biologic therapy. Despite medical therapy, many patients undergo surgery for their IBD. Most patients suffer from iron deficiency or iron deficiency anaemia, and there is also a risk of adverse effects of medical therapy.
Keywords:
Crohn´s disease – ulcerative colitis – medical therapy – surgical therapy
Autoři: M. Bortlík
Působiště autorů: Klinické a výzkumné centrum pro střevní záněty ISCARE I. V. F a. s., Praha Interní klinika 1. LF UK a ÚVN, Praha
Vyšlo v časopise: Kardiol Rev Int Med 2014, 16(3): 240-243
Kategorie: Interní medicína
Souhrn
Crohnova choroba (CD) a ulcerózní kolitida (UC) jsou chronické střevní záněty (IBD) neznámého původu, v jejichž výskytu pozorujeme zřetelný západo-východní a severo-jižní gradient. Předpokládaná patogeneze zahrnuje působení dosud neidentifikovaných vnějších vlivů u geneticky predisponovaných jedinců za účasti některých složek střevní mikroflóry. V klinickém obraze obou nemocí se střídají období aktivity s fázemi klidovými; dominujícími symptomy jsou bolesti břicha a průjmy, typickým projevem UC jsou krvavé stolice. Nemocní s CD jsou často postiženi hnisavými komplikacemi v podobě abscesů a píštělí nitrobřišních nebo perianálních. Základem léčby je dlouhodobá medikamentózní terapie aminosalicyláty, kortikosteroidy, imunosupresivy nebo biologickou léčbou. Navzdory léčbě musí být značná část pacientů během života pro střevní zánět operována. Nejčastější komplikací obou nemocí je sideropenie a sideropenická anemie, nemocní jsou ohroženi také nežádoucími účinky podávaných medikamentů.
Klíčová slova:
Crohnova choroba – ulcerózní kolitida – medikamentózní léčba – chirurgická léčbaÚvod
Mezi idiopatické střevní záněty (IBD – inflammatory bowel disease) patří dvě nozologické jednotky – Crohnova choroba (CD – Crohn´s disease) a ulcerózní kolitida (UC – ulcerative colitis). Etiologie obou nemocí zůstává stále obestřena tajemstvím, navzdory množství informací jsme na tom podobně i s poznáním přesných patogenetických mechanizmů. Neznámý původ a jen zčásti poznaná patogeneze obou chorob jsou hlavní příčinou dvou charakteristických rysů těchto onemocnění: neznáme způsob, jak jim předejít, a neumíme je definitivně vyléčit.
Epidemiologie IBD
Je zřejmé, že výskyt CD i UC v naší populaci narůstá, podobně jako v jiných zemích, pro něž je charakteristický vývoj směrem k ekonomické prosperitě a přijímání „západního“ způsobu života. Nárůst je nejvíce patrný ve věkové kategorii adolescentů a mladých dospělých, kdy jsou obě choroby (zejména to platí pro CD) nejčastěji diagnostikovány. Aktuální epidemiologická data z rozsáhlé panevropské studie ukazují celkovou incidenci IBD 15,2 na 100 tisíc obyvatel za rok, evidentní je západo-východní gradient – incidence v západní Evropě (18,5) je více než dvojnásobná oproti stavu na východě kontinentu (8,1), v obou částech mírně převažuje výskyt UC [1]. V uvedené studii jsou zahrnuty i nejnovější údaje z vybraných regionů ČR (Praha, jižní Čechy), incidence zde dosahuje 12,7 nových případů na 100 tisíc obyvatel za rok, podíl CD a UC je prakticky identický. Informace o prevalenci IBD v ČR poskytují data Ústavu zdravotnických informací a statistiky, podle nichž by v naší zemi mělo být přibližně 42 000 pacientů s oběma formami střevního zánětu [2] (hlášení zde však nepodléhají splnění přísných diagnostických kritérií). V oblastech s nejvyšším výskytem střevních zánětů – západní Evropě a severní Americe – předpokládáme postižení 0,3–0,4 % populace.
Etiopatogeneze IBD
V etiopatogenezi IBD se uplatňuje jednak velmi komplexní a stále málo prozkoumaná genetická predispozice (zejména u Crohnovy choroby), jednak některé faktory zevního prostředí (tab. 1). Významnou roli má střevní mikroflóra, jejíž přítomnost se zdá být nezbytnou pro vznik těchto onemocnění. Jedna z teorií vzniku IBD vychází z představy nedostatečné imunitní tolerance, která je odpovědná za nepřiměřenou reaktivitu střevního imunitního systému na různé antigenní stimuly pravděpodobně mikrobiálního původu. Příčinou může být paradoxně nadměrná „čistota“, v níž se od narození pohybují lidé v ekonomicky vyspělých zemích, kde je také výskyt obou chorob nejvyšší (tzv. hygienická hypotéza vzniku IBD) [3]. U geneticky predisponovaných jedinců tak může zvýšená aktivita imunokompetentních buněk (epiteliálních buněk, lymfocytů, dendritických buněk aj.) indukovat chronický zánět střeva s projevy UC nebo CD. Jiná teorie staví na počátek střevního zánětu poruchu systému přirozené imunity (zřejmě geneticky podmíněnou) projevující se defektní tvorbou antimikrobiálních látek produkovaných ve sliznici trávicí trubice (tzv. defenziny). Jejich hlavním zdrojem jsou Panethovy buňky usídlené především v terminální části ilea – tedy v místě nejčastěji postiženém Crohnovou chorobou [4].
Tab. 1. Faktory zevního prostředí ovlivňující vznik a průběh idiopatických střevních zánětů. 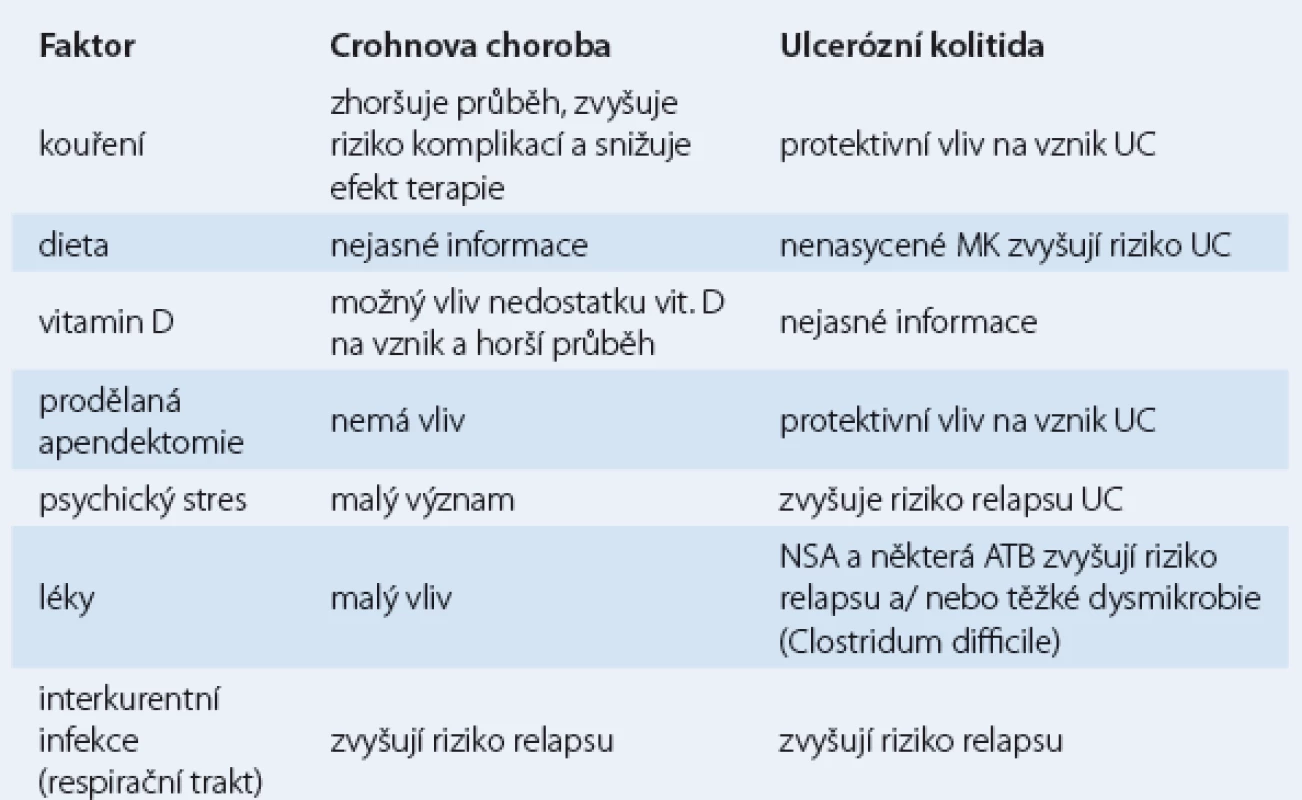
Stále častěji je v literatuře zmiňován také význam vitaminu D, jehož hladina v populaci velmi dobře koreluje s tzv. severo-jižním gradientem výskytu IBD. Nedostatek vitaminu D, látky s předpokládaným významným imunomodulačním účinkem, může být jedním z faktorů vysvětlujících zvýšený výskyt IBD v populaci vyspělých průmyslových zemí „severu“ (nižší intenzita slunečního záření, častější pobyt v uzavřených prostorách). Zčásti by mohl vysvětlit i sezónní výkyvy aktivity IBD [5].
Klinický obraz UC a CD
Typickými projevy UC jsou průjem, krvácení z konečníku a tenezmy. Intenzita obtíží závisí především na aktivitě zánětu, s narůstajícím rozsahem postiženého střeva pak stoupá tíže onemocnění. U nemocných s vysokou aktivitou a postižením větší části tračníku může dojít k alteraci celkového stavu s nutností hospitalizace a intenzivní terapie. Vzácnou, nicméně život ohrožující komplikací může být následná toxická dilatace tračníku (toxické megakolon) obvykle vyžadující chirurgické řešení.
V praxi se nejčastěji setkáváme s nemocnými s UC postihující rektum a esovitou kličku (tzv. ohraničený tvar UC) nebo s levostrannou kolitidou nepřesahující slezinné ohbí tračníku. U třetiny pacientů ovšem dochází během deseti let k progresi zánětu orálním směrem, extenze zánětu je častější u nemocných se začátkem UC v mladém věku. Extenzivní postižení pak zvyšuje pravděpodobnost kolektomie, její frekvence je ovšem ovlivněna i dalšími faktory, např. geografickou lokalizací. V severní části Evropy je tak podíl operovaných pacientů až trojnásobný oproti zemím jižním. Příznivým signálem z posledních let je klesající riziko kolorektálního karcinomu jako nejzávažnější komplikace UC – nejspíše v důsledku účinnější medikamentózní léčby onemocnění a včasné indikace chirurgického výkonu při její inefektivitě [6].
Klinický obraz CD je podstatně mnohotvárnější a pestřejší. CD typicky postihuje oblast ileocékální, v takovém případě bývají v popředí bolesti břicha, méně často průjem nebo celkové projevy – především hubnutí, celková nevýkonnost a únava. Postižení proximální části tenkého střeva se manifestuje malabsorpčním syndromem, dominuje-li postižení tračníku, bývá symptomatologie podobná projevům ulcerózní kolitidy. Až v polovině případů se setkáváme s některým z mimostřevních projevů IBD. Ty postihují nejčastěji periferní klouby (artritidy velkých kloubů nebo artralgie drobných ručních kloubů) nebo axiální skelet (ankylozující spondylitida, sakroileitida), kůži (nodózní erytém a gangrenózní pyodermie) a oči (episkleritida, iridocyklitida). Pro CD jsou navíc typické perianální zánětlivé projevy – abcsesy a perianální píštěle. V některých případech dokonce perianální choroba předchází o měsíce či roky manifestaci vlastního střevního zánětu [7].
Diagnostika
Neexistuje žádný specifický marker UC nebo CD, a stanovení diagnózy IBD je proto založeno na skládání mozaiky sestávající ze zevrubné anamnézy, laboratorního vyšetření a výsledků endoskopických a dalších zobrazovacích vyšetření – tento fakt je podstatný zejména u CD. Základem je koloskopie s intubací terminálního ilea. K vyšetření tenkého střeva používáme CT nebo MR enterografii; narozdíl od klasické enteroklýzy umožní tyto techniky zobrazit i strukturální změny ve stěně střeva a mimo jeho lumen (obr. 1). Přínosem je enteroskopie, zejména její nová forma – tzv. balonková enteroskopie (jedno - či dvojbalonová). Populární kapslová enteroskopie má v diagnostice CD význam okrajový. CD v ileocékální lokalizaci umožňuje i využití klasické či kontrastní sonografie. V diagnostice (a také léčbě) perianálních projevů je nutno vždy spolupracovat se zkušeným chirurgem. Největší přínos má u těchto pacientů MR perianální oblasti, popřípadě rektální endosonografie, ve většině případů je nezbytné vyšetření anu v celkové anestezii chirurgem. Laboratorní parametry přinesou informace o aktivitě a tíži zánětu (CRP, KO, feritin), nutričním stavu pacienta (albumin, lipidy), případně komplikacích (jaterní testy, urea, kretainin, speciální mikrobiologická vyšetření apod.). Zvýšené titry protilátek proti pivovarským kvasnicím (Saccharomyces cerevisiae – ASCA) jsou přítomny u 60 % nemocných s CD, protilátky proti cytoplazmě neutrofilů lokalizované perinukleárně (pANCA) častěji nacházíme u nemocných s UC.
Obr. 1. CT enterografie. Pacientka s Crohnovou chorobou v ileocékální lokalizaci, stenózou a ztluštěním terminálního ilea. 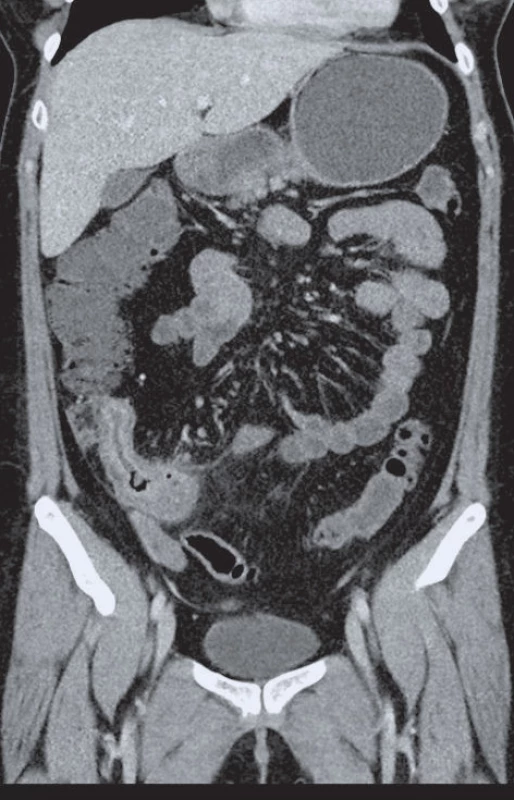
I přes množství vyšetřovacích metod zůstává diagnóza střevního zánětu nevyjasněna u 5–10 % nemocných. Tzv. diagnostická prodleva, tj. doba od prvních projevů do stanovení správné diagnózy, se v případě CD pohybuje mezi pěti a devíti měsíci, u nemocných s UC je tato doba podstatně kratší [8].
Medikamentózní a chirurgická léčba IBD
Dlouhodobé podávání medikamentů je základem terapie obou nemocí. Ve fázi aktivity je cílem indukční léčby potlačení akutních projevů zánětu a nastolení klidového stadia – remise. I poté je nutno v léčbě pokračovat a dlouhodobou udržovací terapií snížit riziko nového vzplanutí choroby. I přes některé odlišnosti je medikamentózní léčba obou nemocí podobná a využívá čtyř základních lékových skupin: aminosalicylátů, kortikosteroidů, imunosupresiv a biologické léčby. V některých specifických situacích používáme rovněž antibiotika a probiotika.
Mesalazin (kyselina 5-aminosalicylová, 5-ASA) je základním lékem v terapii mírné a středně těžké UC, rovněž je nejčastěji využívaným preparátem pro udržovací léčbu v remisi. Jeho účinnost u nemocných s CD je podstatně nižší, nicméně nemocní s lehkým průběhem nebo pacienti po resekci ileocékální oblasti mohou z léčby mesalazinem ve vyšších dávkách (3–4 g/den) rovněž profitovat. Nejednoznačná je role mesalazinu jako chemopreventivního léku; většina odborníků se dnes přiklání k názoru, že protinádorový efekt mesalazinu byl prokázán a jeho podávání riziko kolorektálního karcinomu snižuje [9].
Středně a vysoce aktivní CD i UC vyžadují obvykle podání kortikosteroidů – topických (budesonid) nebo systémových. Systémové kortikoidy mají při dostatečné úvodní dávce (prednisolon nebo metylprednisolon 1 mg/kg/den) rychlý a dramatický účinek, při krátkodobé aplikaci je tato léčba obvykle dobře snášena. Jiná je situace při dlouhodobém užívání kortikoidů, které je zatíženo množstvím závažných metabolických komplikací. Závislost na kortikoidech (kortikodependence) vzniká u čtvrtiny až třetiny nemocných s IBD, kterým jsou tyto léky někdy podány.
Od 80. let minulého století jsou v léčbě IBD používaná imunosupresiva, především thiopuriny (azathioprin a 6-merkaptopurin). Jejich doménou je dlouhodobá udržovací terapie CD, méně často i UC. Přesný mechanizmus jejich protizánětlivého účinku není znám, nejspíše je zprostředkován snížením produkce cytotoxických T lymfocytů a stimulací apoptózy T buněk. Nejčastějším nežádoucím účinkem thiopurinových imunosupresiv je právě útlum krvetvorby v kostní dřeni – trvalá monitorace krevního obrazu včetně diferenciálního rozpočtu je nutná po celou dobu užívání [7].
Biologická léčba dnes sice stojí na vrcholu terapeutické pyramidy, ani ona ale nevede k trvalému vyléčení nemoci u většiny pacientů. Je určena pro nemocné nereagující na běžnou konzervativní terapii IBD nebo pro pacienty s velmi komplikovaným průběhem nemoci a vysokým rizikem opakovaných chirurgických zákroků či dlouhodobých komplikací IBD. Její použití se však posouvá do stále časnějších fází nemoci s cílem zabránit ireparabilním změnám a nutnosti opakovaných chirurgických výkonů.
V klinické praxi jsou dnes používány tři biologické preparáty – protilátky proti TNFα: infliximab (Remicade – originální infliximab, Remsima a Inflectra – tzv. biosimilární infliximab, i.v. infuze), adalimumab (Humira) a golimumab (Simponi), které jsou aplikovány subkutánně. V krátké době je očekáváno další biologikum – vedolizumab (Entyvio), které potlačuje zánět blokádou tzv. integrinových receptorů na leukocytech migrujících z cirkulace do tkáně (střeva). Kromě vysoké aktivity luminální choroby je biologická léčba (přesvědčivá data jsou zejména u infliximabu) přínosem i v terapii perianálních píštělí [10].
V souvislosti s medikamentózní léčbou IBD je nutno zdůraznit faktor tzv. nonadherence, tedy redukce dávky (nebo vysazení) předepsaného léčiva pacientem. V případě aminosalicylátů se nonadherence pohybuje kolem 40 % a bylo opakovaně prokázáno, že nedodržování léčebného režimu zvyšuje riziko relapsů a celkově nepříznivého průběhu onemocnění [11].
Z praktického hlediska je důležité zdůraznit, že většina medikamentů používaných v léčbě IBD je akceptovatelná i v graviditě a laktaci. Výjimkou je metotrexát (potenciální teratogen) používaný sporadicky k léčbě CD.
Asi tři čtvrtiny nemocných s CD a 15 % pacientů s UC musí podstoupit chirurgický resekční výkon. Nejčastějším typem operace je u CD ileocékální resekce nebo resekce jiné postižené a zpravidla stenotické části střeva. Zlatým standardem léčby perianálních píštělí je jejich dlouhodobá drenáž pomocí nekonečných drenů a následná plastika vnitřního ústí píštěle v oblasti anorektální junkce.
U pacientů po předchozí resekci střeva s novou stenózou v anastomóze je alternativou chirurgické léčby balonová dilatace během koloskopie. Jde o metodu velmi účinnou, s minimálním rizikem závažných komplikací (masivní krvácení, perforace střeva). Její využití může odvrátit opakované resekce ohrožující pacienta syndromem krátkého střeva (obr. 2) [12].
Obr. 2. Endoskopická balonová dilatace stenotické anastomózy u nemocného s Crohnovou chorobou. A – stenóza před dilatací. B – dilatační balon zavedený do stenózy. C – lumen střeva po dilataci. 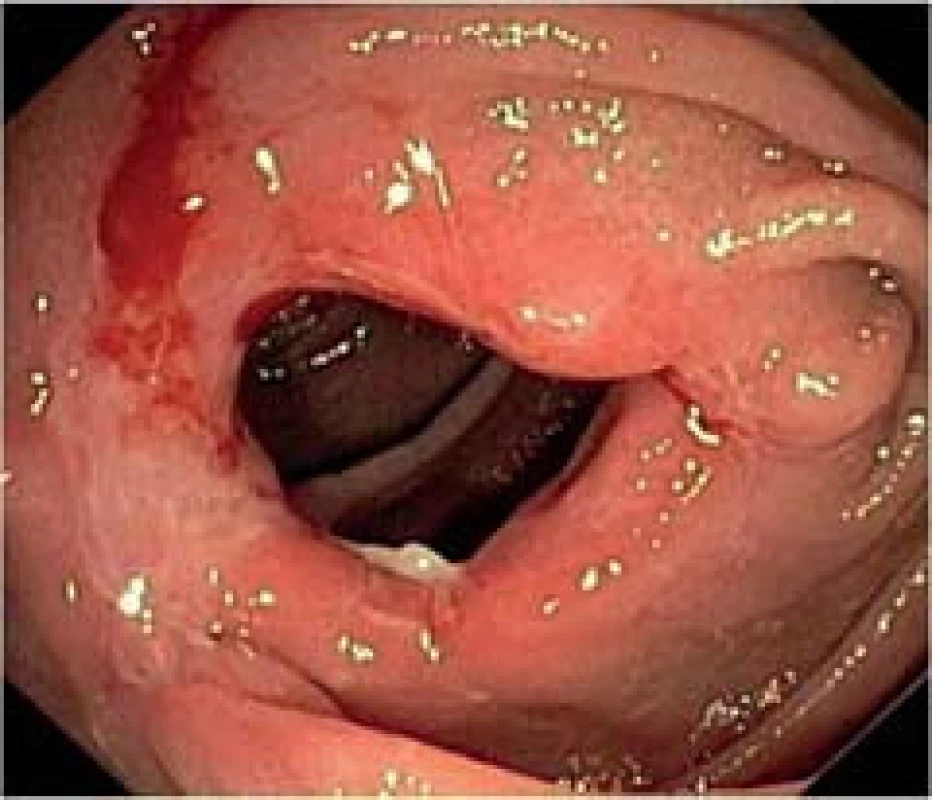
Komplikace doprovázející IBD a jejich léčbu
U části nemocných nelze žádnou medikamentózní léčbou dosáhnout uspokojivého zklidnění zánětu a tito pacienti pak vyžadují (někdy opakované) chirurgické zákroky. Naproti tomu intenzivní medikamentózní léčba s imunosupresivními účinky je většinou efektivní a umožní dosažení úplné nebo částečné remise, někdy však za cenu významných komplikací. V současné době se v klinické praxi setkáváme častěji právě s komplikacemi podávané léčby spíše než s důsledky těžce probíhajícího střevního zánětu.
Z dlouhodobého hlediska je nejobávanější komplikací IBD v tlustém střevě kolorektální karcinom (KRK). Jeho riziko narůstá s délkou trvání choroby, rozsahem postižení tlustého střeva, rodinnou anamnézou KRK a také u nemocných s koincidující primární sklerozující cholangoitidou (PSC). Klíčovým faktorem je tíže zánětu, tedy přítomnost morfologických změn na sliznici střeva. Množství pozánětlivých polypů a prominencí, rigidita střevní stěny nebo dokonce přítomnost stenózy u pacienta s UC spolu s diagnózou PSC zvyšují několikanásobně riziko malignity ve střevě [13].
Imunosupresivní léčba přináší riziko dvou typů komplikací: nádorových onemocnění a infekcí (především oportunních). Thiopuriny mírně zvyšují relativní riziko lymfoproliferativních onemocnění a pravděpodobně i kožních nemelanomových nádorů. V případě protilátek proti TNF se hovoří o možném vlivu na vznik maligního melanomu. V každém případě však panuje jasná shoda v tom, že benefit léčby převyšuje rizika s ní spojená [14].
Nejvýznamnější komplikace – oportunní infekce – představují zcela reálnou hrozbu pro nemocné s imunosupresivními léky. Zpočátku bývá jejich průběh nenápadný, manifestují se např. horečkou či celkovou nevýkonností. Po příčině takových obtíží je však u pacientů s imunosupresivy nutno aktivně pátrat, a to nejen pomocí standardních diagnostických postupů (kultivace, výtěry, odběry hemokultury), ale často i speciálními metodami (např. molekulárně genetickými). Léčba oportunní infekce musí být razantní, často je v úvodu nutná hospitalizace. Kromě pečlivého sledování těchto pacientů je vhodná před zahájením imunosupresivní a biologické terapie vakcinace proti pneumokokové infekci, chřipce a hepatitidě B, v případě potřeby též proti viru varicella-zoster [15].
Nemocní s vysokou aktivitou střevního zánětu jsou vystaveni i zvýšenému riziku tromboembolických komplikací. Těžký relaps a zejména hospitalizace pacienta vyžadují proto vždy preventivní aplikaci antikoagulační léčby.
Závěr
Narůstající počty nemocných s Crohnovou chorobou a ulcerózní kolitidou přinášejí nutnost rozšiřovat nejdůležitější informace o těchto nemocech a jejich terapii mezi široký okruh lékařů a zdravotnických pracovníků. Současná léčba, jakkoli účinná, nedokáže ani jednu z těchto chorob vyléčit. Většina pacientů je proto odkázána na dlouhodobou medikamentózní terapii spojenou s rizikem vedlejších účinků. Spolu s vlastním střevním zánětem je proto nezbytné monitorovat a včas léčit i potenciální či již prokázané komplikace medikamentózní léčby.
Doručeno do redakce: 10. 6. 2014
Přijato po recenzi: 24. 6. 2014
MUDr. Martin Bortlík, Ph.D.
www.iscare.cz
mbortlik@seznam.cz
Zdroje
1. Burisch J, Pedersen N, Čukovic-Čavka S et al. East–West gradient in the incidence of inflammatory bowel disease in Europe: the ECCO-EpiCom inception cohort. Gut 2014; 63 : 588–897. doi: 10.1136/gutjnl-2013-304636.
2. Typltová J. Činnost oboru gastroenterologie v ČR v roce 2013. ÚZIS ČR, Aktuální informace č. 43/2013. [online] Dostupné z: http: http://www.uzis.cz/rychle-informace/cinnost-oborugastroenterologie-cr-roce-2012.
3. Lukáš M, Bortlík M. Etiologie a patogeneze ulcerózní kolitidy. Stále více otazníků než jasných odpovědí. Gastroent Hepatol 2011; 65 : 56–64.
4. Wehkamp J, Salzman NH, Porter E et al. Reduced Paneth cell alpha-defensins in ileal Crohn´s disease. Proc Natl Acad Sci U S A 2005; 102 : 18129–18134.
5. Hlavatý T, Krajčovičová A, Payer J. Význam vitamínu D pri nešpecifických črevných zápalových ochoreniach. Gastroent Hepatol 2012; 66 : 37–43.
6. Jess T, Rungoe C, Peyrin-Biroulet L. Risk of colorectal cancer in patients with ulcerative colitis: a meta-analysis of population-based cohort studies. Clin Gastroenterol Hepatol 2012; 10 : 639–645. doi: 10.1016/j.cgh.2012.01.010.
7. Lukáš M et al. Idiopatické střevní záněty. Praha: Galén 1998.
8. Vavricka SR, Spigaglia SM, Rogler G et al. Systematic evaluation of risk factors for diagnostic delay in inflammatory bowel disease. Inflamm Bowel Dis 2012; 18 : 496–505. doi: 10.1002/ibd.21719.
9. Prokopová L, Ďuricová D, Bortlík M et al. Doporučené postupy pro podávání aminosalicylátů u nemocných s idiopatickými střevními záněty. Gastroent Hepatol 2012; 66 : 391–400.
10. Lukáš M. Perspektivy biologické léčby idiopatických střevních zánětů. Gastroent Hepatol 2014; 68 : 225–229.
11. Červený P, Lukáš M, Bortlík M et al. Non-adherence k medikamentózní léčbě idiopatických střevních zánětů a její nejčastější formy. Čes a Slov Gastroent a Hepatol 2006; 60 : 207–212.
12. Bortlík M, Bouzková E, Ďuricová D et al. Postavení endoskopické dilatace v léčbě pooperačních stenóz u nemocných s Crohnovou chorobou. Endoskopie 2010; 19 : 121–124.
13. Lukáš M. Idiopatické střevní záněty a kolorektální karcinom. Nové souvislosti a další perspektivy. Čes a Slov Gastroent a Hepatol 2006; 60 : 113–118.
14. Magro F, Peyrin-Biroulet L, Sokol H et al. Extra-intestinal malignancies in inflammatory bowel disease: results of the 3rd ECCO Pathogenesis Scientific Workshop (III). J Crohns Colitis 2014; 8 : 31–44. doi: 10.1016/j.crohns.2013.04.006.
15. Stehlík J, Mareš K, Lukáš M et al. Doporučení pro vakcinaci nemocných s Crohnovou chorobou a ulcerózní kolitidou na imunosupresivní a biologické léčbě. Čes a Slov Gastroent a Hepatol 2010; 64 : 40–48.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie Kardiologie
Článek vyšel v časopiseKardiologická revue – Interní medicína
Nejčtenější tento týden
2014 Číslo 3- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
-
Všechny články tohoto čísla
- prof. MUDr. Miloš Štejfa, DrSc., FESC (*28. 5. 1929)
- Léčba akutního srdečního selhání
- Pravidelné supraventrikulární tachykardie – diagnóza, léčba a zkušenosti vysokoobjemového kardiocentra
- Moderní trendy v léčbě dlouhodobé perzistující fibrilace síní
- Standardizace ošetřovatelské péče k dekanylaci sheathu na intervenčních pracovištích v České republice
- HOT lines na sjezdu České kardiologické společnosti
- AUTORSKÁ SOUTĚŽ ČASOPISU KARDIOLOGICKÁ REVUE – INTERNÍ MEDICÍNA
- Editorial – Interní medicína
- Perorální endoskopická myotomie (POEM) – nová endoskopická možnost léčby achalázie jícnu
- Refluxní nemoc jícnu
- Léčba inhibitory protonové pumpy
- Celiakie – současný pohled na etiopatogenezi, diagnostiku a terapii
- Dráždivý tračník – diagnostika a léčba
- Divertikulární choroba tlustého střeva – nové trendy v léčbě
- Screening kolorektálního karcinomu
- Idiopatické střevní záněty
- Chronická pankreatitida
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Divertikulární choroba tlustého střeva – nové trendy v léčbě
- Dráždivý tračník – diagnostika a léčba
- Chronická pankreatitida
- Léčba inhibitory protonové pumpy
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání





