-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaAplikace autologního séra-očních kapek vede ke statisticky významnému zlepšení stavu spojivky pacientů se syndromem suchého oka – pilotní studie
The Application of the Autologous Serum Eye Drops Results in Significant Improvement of the Conjunctival Status in Patients with the Dry Eye Syndrome
Aim:
To detect the changes on the conjunctiva surface before and after the application of the autologous serum (AS) eye drops in patients with dry eye syndrome, using both clinical and laboratory approaches, supplemented with subjective assessing the discomfort status.Materials and methods:
The AS eye drops were applied during the period of 3 months in 8 patients with dry eye syndrome (Schirmer test < 5 mm and break-up time < 5 seconds), with the highest (maximum) frequency 8 times a day. The clinical (Schirmer test, break-up time, rose Bengal staining, examination of the tear meniscus, detritus and superficial punctate keratitis) and laboratory examinations (morphological assessment of the conjunctiva, detection of apoptotic cells) were performed at the start and at the end of the 3 months treatment period. Each day, patients reported their ocular status (dryness, discomfort, foreign body sensation, light sensitivity).Results:
The AS eye drops application improved significantly the values of the Schirmer test, detritus and superficial punctate keratitis as well. The goblet cells density on the conjunctival surface increased and the number of apoptotic cells decreased. The intensity of unpleasant feelings reported by the patients decreased significantly in all of the assessed categories.Conclusion:
Because the application of AS eye drops caused the improvement of conjunctival status as well as the decrease of the severity of difficulties reported by the patients, the AS eye drops application should become common therapeutic practice in patients with dry eye syndrome.Key words:
dry eye syndrome, autologous serum eye drops, conjunctiva
Autoři: K. Jirsová 1,2; E. Hrdličková 1,3; A. Alfakih 1,2,3; K. Juklová 1; M. Filipec 1,4; V. Faltus 5; V. Veselá 1,2
Působiště autorů: Laboratoř biologie a patologie oka, Ústav dědičných metabolických poruch VFN a 1. LF UK, Praha, vedoucí prof. MUDr. Milan Elleder, DrSc. 1; Oční tkáňová banka VFN a 1. LF UK, Praha, vedoucí MUDr. Marcela Černická, MBA 2; Oční klinika VFN a 1. LF UK, Praha, vedoucí doc. MUDr. Bohdana Kalvodová, CSc. 3; Oční klinika Lexum, Praha, vedoucí prof. MUDr. Martin Filipec, CSc. 4; EuroMISE centrum, Ústav informatiky AV ČR v. v. i., Praha, vedoucí prof. RNDr. Jana Zvárová, DrSc. 5
Vyšlo v časopise: Čes. a slov. Oftal., 64, 2008, No. 2, p. 52-56
Souhrn
Cíl:
Zjistit objektivní stav spojivky a míru subjektivních obtíží pacientů se syndromem suchého oka před a po aplikaci autologního séra-očních kapek.Soubor pacientů a metody:
Osmi pacientům s těžkým syndromem suchého oka bylo aplikováno autologní sérum-oční kapky po dobu 3 měsíců, a to úměrně počtu aplikací umělých slz, maximálně však 8krát denně. Klinické testy (Schirmerův test, čas potřebný k roztržení slzného filmu, barvení bengálskou červení, vyšetření menisku, detritu a keratitis punctata superficialis), laboratorní testy (morfologické vyšetření spojivky, detekce apoptotických buněk) byly provedeny před a po ukončení aplikace autologního séra-očních kapek. Během studie pacienti denně posuzovali subjektivní stav očí (pocit sucha, diskomfort, pocit cizího tělesa v oku a světloplachost).Výsledky:
Aplikace autologního séra-očních kapek vedla ke statisticky významnému zlepšení hodnot Schirmerova testu, vyšetření detritu a keratitis punctata. Na povrchu spojivky došlo k zvýšení počtu pohárkových buněk a ke snížení počtu buněk apoptotických. Ve všech pacienty hodnocených kategoriích stavu oka došlo k významnému snížení intenzity nepříjemných pocitů.Závěr:
Aplikace AS-očních kapek vede k objektivnímu zlepšení stavu spojivky i ke snížení subjektivních obtíží vnímaných pacienty. Pozitivní působení AS-očních kapek při syndromu suchého oka je zřejmý a jeho aplikace má předpoklady stát se běžnou léčebnou praxí.Klíčová slova:
syndrom suchého oka, autologní sérum-oční kapky, spojivkaÚVOD
Syndrom suchého oka, keratoconjunctivitis sicca (KCS), je stav charakterizovaný patologickými změnami na povrchu oka, ke kterým dochází na základě nízké produkce slz, jejich zvýšeným vypařováním, či při abnormálním složení slzného filmu [26].
Farmakoterapie KCS v současné době spočívá zejména v aplikaci umělých slz. Pacientům s mírnou formou se tradičně podávají umělé slzy s přítomností konzervačních látek, pacientům s těžší a těžkou formou jsou aplikovány umělé slzy bez konzervans, v případě potřeby lze přidat lubrikační mast na noc. Pokud jsou tato opatření nedostatečná, je třeba zvážit dočasnou či trvalou okluzi slzných kanálků, případně tarzorafii. Dalšími možnostmi léčby jsou lokální aplikace cyklosporinu A, kortikosteroidů, pomocnou metodou je i nošení ochranných brýlí [4, 19, 25, 30].
Intenzita KCS, často násobená toxickým působením konzervačních látek při intenzivní lokální léčbě, se odráží i v míře poškození povrchu oka [9]. Dochází ke kvalitativním i kvantitativním změnám v buněčném složení jeho povrchu, a to především v oblasti spojivky [28]. Charakteristickým rysem KCS je skvamózní metaplazie, projevující se snížením počtu až vymizením pohárkových buněk, snížením jádro-cytoplazmatického poměru epitelových buněk (zvětšení cytoplazmy oproti jádru) a jejich keratinizací [20, 31]. V epitelu spojivky vzrůstá i počet HLA-DR pozitivních buněk, jejichž přítomnost je charakteristickým projevem probíhajícího zánětlivého procesu [2]. Během KCS se zvyšuje počet odumírajících a mrtvých buněk na povrchu oka. Bylo prokázáno, že k zániku buněk spojivky pacientů s KCS dochází na základě apoptózy [1].
Navzdory léčbě si mnoho pacientů trpících KCS stěžuje na přetrvávání příznaků této choroby (pálení očí, pocit sucha či pocit cizího tělesa v oku), svědčících o poškození povrchu oka, přičemž objektivní klinický nález nemusí vždy míře subjektivních obtíží odpovídat. U těchto pacientů může být účinná aplikace přípravků, podporujících proliferaci a diferenciaci epitelu. Mezi takové patří autologní sérum (AS), jehož příznivý účinek na zlepšení hodnot některých klinických testů i subjektivní vnímání intenzity choroby pacienty byl v léčbě KCS prokázán [23].
Úspěch terapie AS je dán komplexním působením celé řady látek, které jsou v něm obsaženy. Jedná se především o růstové faktory, vitaminy, ale i základní nutriční komponenty, jejichž množství může být v slzách pacientů s KCS sníženo, nebo mohou úplně chybět. Vedle toho AS-oční kapky zvlhčují povrch oka, aniž by byly aplikovány pro organismus cizorodé látky a nemusíme se tedy obávat alergické reakce. Epidermální růstový faktor (epidermal growth factor, EGF) podporuje proliferaci a hojení epitelu [24, 36]. Fibronektin zvyšuje migraci epitelových buněk a jejich uchycení v oblasti defektu [21]. Transformující růstový faktor beta (TGFβ) moduluje účinky EGF a fibronektinu, při absenci EGF může proliferaci epitelu inhibovat [17]. Retinol brzdí progresi skvamózní metaplazie během KCS, ale v klinických studiích se jeho účinky nepotvrdily [32, 33]. V AS přítomné proteiny (především albumin) zvyšují stabilitu slzného filmu [29]. Přítomnost oleje v AS může nahradit lipidovou složku produkovanou meibomskými žlázami [10]. V kultivovaných buňkách spojivky zvyšuje aplikace AS expresi mucinu [11, 34]. Díky neurotropním faktorům: substanci P, inzulinovému a nervovému růstovému faktoru má AS i účinky neuroprotektivní [14]. Předností AS je i jeho antiinfekční působení dané přítomností lysozymu a imunoglobulinů [18]. V případě epitelových lézí na povrchu oka vede působení všech těchto látek v místě poškození ke stimulaci a urychlení hojení [30]. Vzhledem k tomu, že biomechanické a biochemické vlastnosti AS jsou velmi podobné slzám (pH ani osmolarita se téměř neliší), je jeho použití v prostředí oka velmi šetrné [8]. Nežádoucí účinky AS jsou ojedinělé (vznik imunoglobulinových depozit, periferní infiltrace a ulcerace u pacienta s revmatoidní artritidou) [16, 27].
Klinicky bylo AS úspěšně použito k léčbě těžkého syndromu suchého oka, přetrvávajících defektů epitelu, horní limbální keratokonjunktivitidy, recidivujících erozí rohovky, neurotrofické keratopatie i k zastavení zevní filtrace z filtračních polštářků po trabekulotomii [14, 15, 22, 27, 35, 37].
Cílem této studie bylo zjistit objektivní změny na spojivce a míru subjektivních obtíží pacientů s KCS před a po aplikaci AS-očních kapek.
SOUBOR PACIENTŮ, METODY
Studie byla schválena Etickou komisí VFN a 1. LF UK; všichni pacienti byli do studie zařazeni po podepsání informovaného souhlasu s odběrem krve pro přípravu AS-očních kapek a s provedením otiskové cytologie spojivky.
Sledovaný soubor tvořilo osm pacientů (7 žen, 1 muž, hodnoceno 16 očí), s těžkým syndromem suchého oka: Schirmerův test < 5 mm, čas potřebný k roztržení slzného filmu (break-up-time test, BUT) < 5 sekund. Průměrný věk pacientů byl 54,8 let (rozmezí: 28–70 let). Šest z těchto pacientů trpělo primárním Sjőgrenovým syndromem, 2 pacienti měli KCS nejasné etiologie. Terapie sledovaných osob umělými slzami se neměnila nejméně po dobu 3 měsíců před začátkem a po celou dobu studie. Tři pacienti aplikovali Hypotears SDU PLUS, 3 pacienti Hylocomod, 1 pacient Lacrysin a 1 pacient Tears Natural II.
Příprava a aplikace AS-očních kapek: pacientům bylo odebráno 40 ml venózní krve, ta byla centrifugována (4000/min, po dobu 15 minut), sérum odebráno a zředěno fyziologickým roztokem na 20 %, plněno po cca 3–5 ml do sterilních označených lahviček. Připravené AS-oční kapky byly zamrazeny na -20 °C a po provedení kontroly sterility předány pacientům. Ti byli poučeni, jak AS-oční kapky uchovávat a aplikovat (zásobní kapky je třeba uchovávat v mrazáku při -20 °C, používané kapky v lednici při 4–8 °C). Pacienti si kapali AS-oční kapky po dobu 3 měsíců, a to úměrně počtu aplikací umělých slz, maximálně však 8krát denně. AS-oční kapky byly podávány asi 15 minut po aplikaci umělých slz.
Z klinických testů byl proveden Schirmerův test I, BUT (měřen čas potřebný k roztržení slzného filmu v s), vitální barvení 1% roztokem bengálské červeně (intenzita zbarvení na rohovce a interpalpebrální spojivce byla hodnocena pomocí pětistupňové škály 0–4). Ve škále 0–4 byly hodnoceny keratitis punctata superficialis a přítomnost detritu. Vyšetření menisku slzného filmu bylo provedeno při okraji dolního víčka a hodnoceno v mm.
Pro laboratorní testy byly použity vzorky získané pomocí otiskové cytologie, která byla provedena přitisknutím odběrového materiálu na horní a dolní bulbární spojivku ve vzdálenosti 2 mm od limbu po dobu 3–5 sekund [20, 31].
Odběr z horní a dolní bulbární spojivky byl proveden na nitroacetátcelulózové filtrační papíry (Millipore GSWP 0.4700, velikost pórů 0,22 μm) a vzorky použity pro morfologické vyšetření. Odběr ve stejných lokalizacích byl proveden i na membrány Millicell (Biopore MILLICELL®-CM, PICM 01250, Millipore), vzorky byly použity pro imunofluorescenční vyšetření.
Vzorky pro morfologické vyšetření byly fixovány a obarveny [12]. Počet epitelových a pohárkových buněk/mm2 byl zjištěn pomocí programu pro obrazovou analýzu LUCIA (Laboratory Imaging, Česká republika), vždy nejméně z 5 fotografií snímaných pomocí kamery Vosskühler VDS CCD-1300 (VDS Vosskühler, GmbH, Německo) z mikroskopu Olympus BX 51. Zakódované vzorky byly hodnoceny nezávisle dvěma pracovníky; ve výsledcích jsou uvedeny průměrné hodnoty.
Detekce apoptotických buněk byla provedena na membránách Millicell po fixaci (1 min) koncentrovaným acetonem. Membrány uvolněné působením acetonu z plastikového nosiče byly umístěny na kulatá krycí skla (12 mm) a buňky permeabilizovány 0,2% tritonem (Triton X-100, Sigma-Aldrich Corp, St Luis, MO, USA) ve fosfátovém pufru. Pro detekci apoptózy byl použit In Situ Death Detection Kit, Fluorescein (Roche Applied Science, Mannheim, Německo). Principem detekce je značení volných 3’-OH konců DNA vznikajících během apoptózy vazbou fluorescenčně značených nukleotidů (deoxyuridin trifosfát) pomocí terminální deoxynukleotidyl transferázy [7]. Vzorky byly montovány pomocí média Vectashield (Vector Laboratories, Inc. Burlingame, USA) s propidium jodidem, který interkaluje s DNA a zviditelňuje buněčná jádra. Vzorky byly hodnoceny pomocí fluorescenčního mikroskopu Olympus BX 51 a procento apoptotických buněk zjišťováno na základě hodnocení alespoň 1000 buněk.
Statistická analýza
Pro analýzu dat byl použit statistický software R (v.2.2.1). K testování hypotézy nulového efektu použit párový Wilcoxonův test. K výpočtu exaktních p-hodnot byla použita R-knihovna exactRankTests (v.0.8-12). Za statisticky významnou byla považována hladina rovná nebo nižší než 5 %.
VÝSLEDKY
Hodnoty klinických testů před a po aplikaci AS-očních kapek jsou zaznamenány v tabulce 1.
Tab. 1. Hodnoty klinických testů před a po aplikaci AS-očních kapek 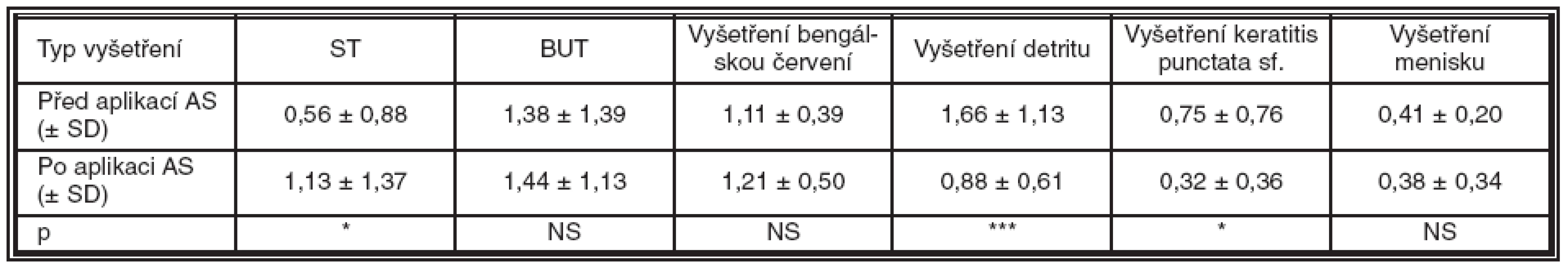
Statistická významnost výsledků klinických testů po aplikaci AS-očních kapek v porovnání s výsledky před aplikací AS-očních kapek: NS – nesignifikantní, *p < 0,05, **p < 0,01, ***p < 0,001.
K statisticky významnému zlepšení došlo u ST (p = 0,04492), vyšetření detritu (p = 0,00098), a keratitis punctata (p = 0,03125). U vyšetření BUT a menisku došlo ke zlepšení, které nebylo statisticky významné. U barvení bengálskou červení došlo k mírnému statisticky nevýznamnému zhoršení.
Z laboratorních testů došlo ke statisticky významnému zvýšení průměrného počtu pohárkových buněk z 35 na 68 buněk/mm2 (tj. na 194 % původních hodnot, p = 0,01038, *) na horní bulbární spojivce a z 34 na 79 buněk/mm2 (tj. na 232 % původních hodnot, p = 0,00085, ***) na dolní bulbární spojivce. V počtu epitelových buněk došlo k mírnému statisticky nevýznamnému nárůstu (z 2660 na 2761 buněk/mm2) na horní spojivce a k mírnému statisticky nevýznamnému poklesu (z 2479 na 2447 buněk/mm2) na spodní spojivce. Rozdíl mezi povrchem spojivky před a po aplikaci AS-očních kapek byl u většiny pacientů dobře patrný (obrázek 1).
Obr. 1. Otisková cytologie spojivky: vzorek zdravé spojivky – A, vzorek pacienta před – B, a vzorek pacienta po aplikaci AS – očních kapek – C 
Aplikace AS-očních kapek vedla ke snížení počtu apoptotických buněk na povrchu spojivky z 6,6 na 5,1 %.
K zmírnění vnímání nepříjemných pocitů u hodnocených pacientů došlo ve všech sledovaných kategoriích a to v průměru o 0,6 stupně (tabulka 2).
Tab. 2. Subjektivní hodnocení pacientů před a po tříměsíční aplikaci AS-očních kapek 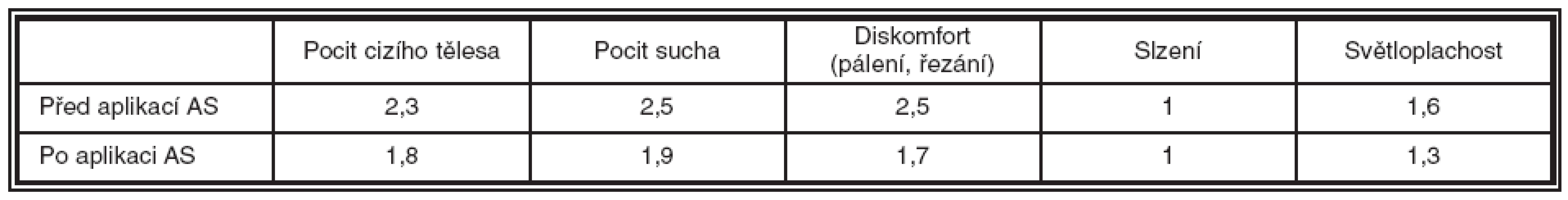
Výraznější zlepšení udávali pacienti, kteří vnímali své obtíže před začátkem studie jako výrazné. Pacienti, kteří byli stabilizovaní a relativně bez intenzivně vnímaných potíží, rozdíl před a po podávání AS-očních kapek nevnímali jako výrazný.
DISKUSE
Ačkoliv byla první náhrada slz autologním sérem popsána již v roce 1984 – právě u pacientů s KCS [6], širší uplatnění nachází AS v léčbě oka až začátkem 21. století. Rozkvět v jeho používání nastal díky studiím, které odkryly mechanismy jeho působení a především díky pozitivním výsledkům, které byly po léčbě AS zaznamenány u celé řady onemocnění projevujících se poškozením epitelu na povrchu oka.
K statisticky významnému zlepšení po aplikaci AS-očních kapek došlo kromě syndromu suchého oka, v léčbě KCS s reakcí štěpu proti hostiteli, přetrvávajících defektů epitelu, limbální keratokonjunktivitidy, neurotrofní keratitidy, recidivujících erozí rohovky, defektů epitelu vzniklých v důsledku refrakčního laserového zákroku [3, 5, 10, 13, 22, 34, 37].
Úspěch AS spočívá v náhradě celé řady základních nutričních látek na povrchu oka, které při KCS mohou být sníženy nebo chybět, ale i růstových faktorů, antioxidačních a dalších příznivě působících látek [23, 34]. Aniž by byly aplikovány pro organismus cizorodé látky zvlhčuje AS povrch oka. AS také – na rozdíl od řady komponent umělých slz – nenarušuje integritu buněčných membrán [27]. Další výhodou AS-očních kapek je, že je lze aplikovat poměrně často – i více než 10krát denně [10, 23].
AS se používá koncentrované, ale častěji ředěné na 50 až 20 % [23, 27, 30, 37]. V současnosti je vzhledem k 5krát vyšší koncentraci TGF‚ [34] v séru než v slzách a možnému antiproliferačnímu působení TGF‚ při vyšších koncentracích, aplikováno téměř výhradně 20% AS [34]. Pro zachování stability TGF‚ trvající při -20°C asi 3 měsíce [35], jsme připravovali AS-oční kapky pro aplikaci nepřesahující toto období. V některých studiích přidávali do AS-očních kapek i antibiotika [27]. V naší studii jsme podobně, jako celá řada autorů, vycházeli z faktu, že látky s antiinfekčním působením obsažené v séru ochrání před případnou kontaminací kapky samotné, ale i povrch oka po jejich aplikaci [34].
Při léčbě KCS bylo ve většině studií AS aplikováno současně s umělými slzami [30, 34], v některých však jejich aplikaci zcela nahrazuje [13, 23].
Absolutní kontraindikace použití AS se neuvádí, relativní kontraindikace se liší i v rámci evropských států. Například relativní kontraindikací aplikace AS je séropozitivita pro HIV, hepatitidu A, B, C a syfilis, relativní kontraindikací odběru většího množství krve (nad 100 ml) může být anémie (hemoglobin < 11g/dl) či vážné kardiovaskulární onemocnění [8].
Výsledky naší studie ukazují, že aplikace AS-očních kapek po dobu 3 měsíců vedla k zlepšení většiny klinických testů (ST, BUT, vyšetření detritu, keratitis punctata superficialis a menisku slzného filmu). Mírné statisticky významné zlepšení hodnot Schirmerova testu odpovídá i hodnotám zjištěným v jiných studiích [30]. Za významné lze považovat i snížení přítomnosti detritu a keratitis punctata superficialis, které dosud po působení AS nebylo dokumentováno.
Statisticky nevýznamné zhoršení, které nastalo u barvení bengálskou červení, by mohlo souviset s obnovou buněk epitelu trvající po dobu aplikace AS-očních kapek. Ke zlepšení výsledků barvení bengálskou červení ovšem na rozdíl od našich výsledků došlo po aplikaci AS u pacientů s KCS v několika studiích [23, 30, 34].
Zásadní pozitivní změny byly zaznamenány v buněčném složení povrchu spojivky, kde se statisticky významně zvýšil počet pohárkových buněk. Zhodnocením písemných záznamů účastníků studie o stavu oka, jsme zjistili, že došlo k významnému snížení intenzity nepříjemných pocitů ve všech hodnocených kategoriích. Při závěrečném zhodnocení působení AS-očních kapek však dva pacienti rozdíly nevnímali. Jednalo se o pacienty, kteří před začátkem studie svůj stav vnímali jako stabilizovaný a výraznější problémy neudávali. Šest pacientů udává mírné až výrazné zlepšení. Všichni tito pacienti před začátkem studie vnímali stav svých očí jako nepříjemný. Přestože pacienti byli poučeni, aby během studie neměnili dávkování stávající terapie, vedlo dva pacienty subjektivní zlepšení stavu očí ke spontánnímu snižování počtu denních dávek umělých slz. Čtyři ze sledovaných pacientů po ukončení studie přišli s přáním v aplikaci AS-očních kapek pokračovat. Naše výsledky jsou v souladu s jinými studiemi, ve kterých bylo rovněž zaznamenáno subjektivní zlepšení [23, 30].
Na základě těchto výsledků můžeme shrnout, že aplikace AS-očních kapek vede k zlepšení subjektivního stavu pacienta, ale i k objektivnímu zlepšení stavu spojivky ve většině sledovaných parametrů zjištěných jak klinickými, tak i laboratorními metodami. Pozitivní působení AS při KCS a hojení epitelu povrchu oka je zřejmý a jeho aplikace má tak předpoklady stát se běžnou léčebnou praxí.
PODĚKOVÁNÍ
Tato studie byla podpořena projektem Sicca research 2005 (Bauch and Lomb) a VZ MŠMT 002160806/20610011. Autoři děkují firmě Ursapharm za poskytnutí přípravku HYLO-COMOD pacientům začleněným do této studie.
Mgr. Kateřina Jirsová, PhD.
VFN a 1. LF UK
U Nemocnice 2
128 08 Praha 2
e-mail: katerina.jirsova@vfn.cz
Zdroje
1. Brignole, F., De Saint-Jean, M., Goldschild, M. et al.: Expression of Fas-Fas ligand antigens and apoptotic marker APO2.7 by the human conjunctival epithelium. Positive correlation with class II HLA DR expression in inflammatory ocular surface disorders. Exp Eye Res., 67, 1998, 6 : 687–697.
2. Brignole, F., Pisella, P.J., Goldschild, M., et al.: Flow cytometric analysis of inflammatory markers in conjunctival epithelial cells of patients with dry eyes. Invest Ophthalmol Vis Sci., 41,2000, 6 : 1356–1363.
3. del Castillo, J.M., de la Casa, J.M., Sardina, R.C. et al.: Treatment of recurrent corneal erosions using autologous serum. Cornea, 21, 2002, 8 : 781–783.
4. Djalilian, A.R., Mahesh, S.P., Koch, C.A. et al.: Survival of donor epithelial cells after limbal stem cell transplantation. Invest Ophthalmol Vis Sci., 46, 2005, 3 : 803–807.
5. Esquenazi, S., He, J., Bazan, H.E. et al.: Use of autologous serum in corneal epithelial defects post-lamellar surgery. Cornea, 24, 2005, 8 : 992–997.
6. Fox, R.I., Chan, R., Michelson, J.B. et al.: Beneficial effect of artificial tears made with autologous serum in patients with keratoconjunctivitis sicca. Arthritis Rheum., 27, 1984, 4 : 459–461.
7. Gavrieli, Y., Sherman, Y.Ben-Sasson, S.A.: Identification of programmed cell death in situ via specific labeling of nuclear DNA fragmentation. J Cell Biol., 119, 1992, 3 : 493–500.
8. Geerling, G., Maclennan, S.Hartwig, D.: Autologous serum eye drops for ocular surface disorders. Br J Ophthalmol., 88, 2004, 11 : 1467–1474.
9. Gobbels, M.Spitznas, M.: Corneal epithelial permeability of dry eyes before and after treatment with artificial tears. Ophthalmology, 99, 1992, 6 : 873–878.
10. Goto, E., Shimmura, S., Shimazaki, J. et al.: Treatment of superior limbic keratoconjunctivitis by application of autologous serum. Cornea, 20, 2001, 8 : 807–810.
11. Hori, Y., Spurr-Michaud, S., Russo, C.L. et al.: Differential regulation of membrane-associated mucins in the human ocular surface epithelium. Invest Ophthalmol Vis Sci., 45, 2004, 1 : 114–122.
12. Jirsova, K., Juklova, K., Vesela, V. et al.: Morphological and immunocytochemical characterization of snake-like chromatin cells. Histol Histopathol., 21, 2006, 4 : 355–360.
13. Kojima, T., Ishida, R., Dogru, M. et al.: The effect of autologous serum eyedrops in the treatment of severe dry eye disease: a prospective randomized case-control study. Am J Ophthalmol., 139, 2005, 2 : 242–246.
14. Matsumoto, Y., Dogru, M., Goto, E. et al.: Autologous serum application in the treatment of neurotrophic keratopathy. Ophthalmology 111,2004, 6 : 1115–1120.
15. Matsuo, H., Tomidokoro, A., Tomita, G. et al.: Topical application of autologous serum for the treatment of late-onset aqueous oozing or point-leak through filtering bleb. Eye 19,2005, 1 : 23–28.
16. McDonnell, P.J., Schanzlin, D.J.Rao, N.A.: Immunoglobulin deposition in the cornea after application of autologous serum. Arch Ophthalmol 106,1988, 10 : 1423–1425.
17. Mishima, H., Nakamura, M., Murakami, J. et al.: Transforming growth factor-beta modulates effects of epidermal growth factor on corneal epithelial cells. Curr Eye Res 11,1992, 7 : 691–696.
18. Nelson, J.D.: Diagnosis of keratoconjunctivitis sicca. Int Ophthalmol Clin 34,1994, 1 : 37–56.
19. Nelson, J.D.Farris, R.L.: Sodium hyaluronate and polyvinyl alcohol artificial tear preparations. A comparison in patients with keratoconjunctivitis sicca. Arch Ophthalmol 106,1988, 4 : 484–487.
20. Nelson, J.D., Havener, V.R.Cameron, J.D.: Cellulose acetate impressions of the ocular surface. Dry eye states. Arch Ophthalmol 101,1983, 12 : 1869–1872.
21. Nishida, T., Ohashi, Y., Awata, T. et al.: Fibronectin. A new therapy for corneal trophic ulcer. Arch Ophthalmol 101,1983, 7 : 1046–1048.
22. Noble, B.A., Loh, R.S., MacLennan, S. et al.: Comparison of autologous serum eye drops with conventional therapy in a randomised controlled crossover trial for ocular surface disease. Br J Ophthalmol., 88, 2004, 5 : 647–652.
23. Ogawa, Y., Okamoto, S., Mori, T. et al.: Autologous serum eye drops for the treatment of severe dry eye in patients with chronic graft-versus-host disease. Bone Marrow Transplant., 31, 2003, 7 : 579–583.
24. Ohashi, Y., Motokura, M., Kinoshita, Y. et al.: Presence of epidermal growth factor in human tears. Invest Ophthalmol Vis Sci., 30, 1989, 8 : 1879–1882.
25. Perry, H.D.Donnenfeld, E.D.: Dry eye diagnosis and management in 2004. Curr Opin Ophthalmol., 15, 2004, 4 : 299–304.
26. Pflugfelder, S.C., Solomon, A.Stern, M.E.: The diagnosis and management of dry eye: a twenty-five-year review. Cornea, 19,2000, 5 : 644–649.
27. Poon, A.C., Geerling, G., Dart, J.K. et al.: Autologous serum eyedrops for dry eyes and epithelial defects: clinical and in vitro toxicity studies. Br J Ophthalmol., 85, 2001, 10 : 1188–1197.
28. Rivas, L., Oroza, M.A., Perez-Esteban, A. et al.: Morphological changes in ocular surface in dry eyes and other disorders by impression cytology. Graefes Arch Clin Exp Ophthalmol 230,1992, 4 : 329–334.
29. Shimmura, S., Ueno, R., Matsumoto, Y. et al.: Albumin as a tear supplement in the treatment of severe dry eye. Br J Ophthalmol., 87,2003, 10 : 1279–1283.
30. Tananuvat, N., Daniell, M., Sullivan, L.J. et al.: Controlled study of the use of autologous serum in dry eye patients. Cornea, 20, 2001, 8 : 802–806.
31. Tseng, S.C.: Staging of conjunctival squamous metaplasia by impression cytology. Ophthalmology, 92, 1985, 6 : 728–733.
32. Tseng, S.C.: Topical tretinoin treatment for dry-eye disorders. Int Ophthalmol Clin., 27, 1987, 1 : 47–53.
33. Tseng, S.C., Maumenee, A.E., Stark, W.J., et al.: Topical retinoid treatment for various dry-eye disorders. Ophthalmology, 92, 1985, 6 : 717–727.
34. Tsubota, K., Goto, E., Fujita, H., et al.: Treatment of dry eye by autologous serum application in Sjogren’s syndrome. Br J Ophthalmol., 83, 1999, 4 : 390–395.
35. Tsubota, K., Goto, E., Shimmura, S., et al.: Treatment of persistent corneal epithelial defect by autologous serum application. Ophthalmology, 106, 1999, 10 : 1984–1989.
36. van Setten, G.B., Viinikka, L., Tervo, T., et al.: Epidermal growth factor is a constant component of normal human tear fluid. Graefes Arch Clin Exp Ophthalmol., 227, 1989, 2 : 184–187.
37. Young, A.L., Cheng, A.C., Ng, H.K., et al.: The use of autologous serum tears in persistent corneal epithelial defects. Eye, 18, 2004, 6 : 609–614.
Štítky
Oftalmologie
Článek vyšel v časopiseČeská a slovenská oftalmologie
Nejčtenější tento týden
2008 Číslo 2- Stillova choroba: vzácné a závažné systémové onemocnění
- Familiární středomořská horečka
- Diagnostický algoritmus při podezření na syndrom periodické horečky
- Možnosti využití přípravku Desodrop v terapii a prevenci oftalmologických onemocnění
- Normotenzní glaukom: prevalence a zásady terapie
-
Všechny články tohoto čísla
- Využití DNA diagnostiky u pacientů s povrchovou keratitidou virového původu
- ŽIVOTNÍ JUBILEUM DOC. MUDr. KARLA KUBĚNY, CSc.
- Aplikace autologního séra-očních kapek vede ke statisticky významnému zlepšení stavu spojivky pacientů se syndromem suchého oka – pilotní studie
- Artériovenózna dekompresia pri parciálnej oklúzii centrálnej vény sietnice so zlúpnutím vnútornej membrány sietnice pre edém makuly
- Spontánne premakulárne krvácanie
- Léčba recidivujících pterygií
- GDx pred a po LASIK u strednej a vyššej myopie
- Výskyt syndromu suchého oka a rohovkových komplikací u pacientů s revmatoidní artritidou a jeho souvislost s polymorfismem -174 genu pro interleukin 6
- „Kádrový posudek“ na Josefa Schöbla z 19. 12. 1882
- Neblahá role armád v šíření nakažlivých očních onemocnění
- Česká a slovenská oftalmologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Aplikace autologního séra-očních kapek vede ke statisticky významnému zlepšení stavu spojivky pacientů se syndromem suchého oka – pilotní studie
- Léčba recidivujících pterygií
- Spontánne premakulárne krvácanie
- Využití DNA diagnostiky u pacientů s povrchovou keratitidou virového původu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



