-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Pokroky v terapii myasthenia gravis na obzoru
28. 3. 2024
Výzkum nových léčiv pro generalizovanou formu myasthenia gravis se v posledních letech posunul výrazně dopředu. Jak si stojí nová specifická terapie? A blížíme se k radikální změně léčebné strategie?
Myasthenia gravis v kostce
Myasthenia gravis (MG) je chronické autoimunitní onemocnění vyvolané protilátkami namířenými proti receptorům a proteinům v oblasti postsynaptické membrány nervosvalové ploténky.
- U většiny pacientů se jedná o protilátky proti acetylcholinovému receptoru (AChR Ab) patřící zejména do podtřídy imunoglobulinů IgG1 a IgG3. Po vazbě protilátky na AChR dochází k aktivaci komplementové kaskády. Aktivované proteiny komplementu vytvoří tzv. membránu atakující komplex, jehož působením dochází k přímému poškození buněk nervosvalové ploténky.
- Malé procento pacientů má diagnostikované pozitivní protilátky proti svalově specifické tyrosinkináze (MuSK Ab), případně proti proteinu 4 příbuznému s receptorem pro LDL (LRP4 Ab). U LRP4 Ab je imunopatogeneze shodná jako u pacientů s pozitivitou AChR Ab. Protilátky MuSK jsou zejména podtřídy IgG4 a po navázání neaktivují komplement. Blokádou MuSK je ovlivněna interakce postsynaptických proteinů, a tím selhává nervosvalový přenos postsynapticky.
Důsledkem patologických procesů je tedy blokáda nervosvalového přenosu. Klinicky je onemocnění charakterizované kolísající svalovou slabostí a unavitelností. MG se může projevovat poruchou řeči, obtížným polykáním či žvýkáním, dušností, ptózou a/ nebo diplopií a slabostí končetin, což má značný vliv na kvalitu života.
InzerceSpecifická terapie na vzestupu
Léčbou MG 1. volby jsou inhibitory cholinesterázy, v případě progrese onemocnění nebo manifestace slabosti orofaryngeálních či dýchacích svalů je doporučeno nasazení kortikosteroidů, většinou v kombinaci s dalšími imunosupresivy. Thymektomie se provádí u MG s časnou manifestací nebo u MG asociované s thymomem. Zásadní komplikaci představuje myastenická krize – život ohrožující stav, který potká alespoň jednou za život každého pátého pacienta.
I přes zdokonalení léčebných strategií a zlepšení prognózy se při využití konvenčních terapeutických postupů nedaří udržet onemocnění dostatečně pod kontrolou přibližně u 15 % pacientů. Nejen u této skupiny si v posledních letech nacházejí místo specificky působící moderní biologika – inhibitory komplementu, blokátory neonatálního receptoru Fc, léčiva vyvolávající depleci B a T lymfocytů a další. Výhodou těchto léčivých přípravků je rychlejší efekt a obecně menší výskyt nežádoucích účinků.
Rozanolixizumab – blokátor neonatálních receptorů Fc
Jedním z těchto moderních přístupů k léčbě MG je zacílení na neonatální receptory Fc. Jejich zablokováním dochází ke snížení koncentrace imunoglobulinů IgG včetně autoprotilátek. Imunoglobuliny IgG jsou vazbou na neonatální receptor Fc chráněny před lyzosomovou eliminací, bez vazby na tento receptor jsou naopak ve zvýšené míře degradovány. Příkladem biologika z této skupiny, jehož registrační studie (MycarinG) byla recentně ukončena a dochází k jeho postupnému zavedení do praxe, je rozanolixizumab.
Metodika, průběh a cíle studie
MycarinG byla randomizovaná dvojitě zaslepená placebem kontrolovaná adaptační studie fáze III probíhající na 81 ambulantních pracovištích. Do studie byli zařazeni dospělí pacienti s generalizovanou MG (Myasthenia Gravis Foundation of America, třída II–IVa), s prokázanou AChR Ab nebo MuSK Ab, se skóre Myasthenia Gravis Activities of Daily Living (MG-ADL) ≥ 3 (bez okulární symptomatiky) a s kvantitativním MG skóre ≥ 11.
Pacienti byli náhodně rozděleni do 3 stejně velkých skupin:
- subkutánní infuze rozanolixizumabu v dávce 7 mg/kg 1× týdně po dobu 6 týdnů
- subkutánní infuze rozanolixizumabu v dávce 10 mg/kg 1× týdně po dobu 6 týdnů
- podávání placeba
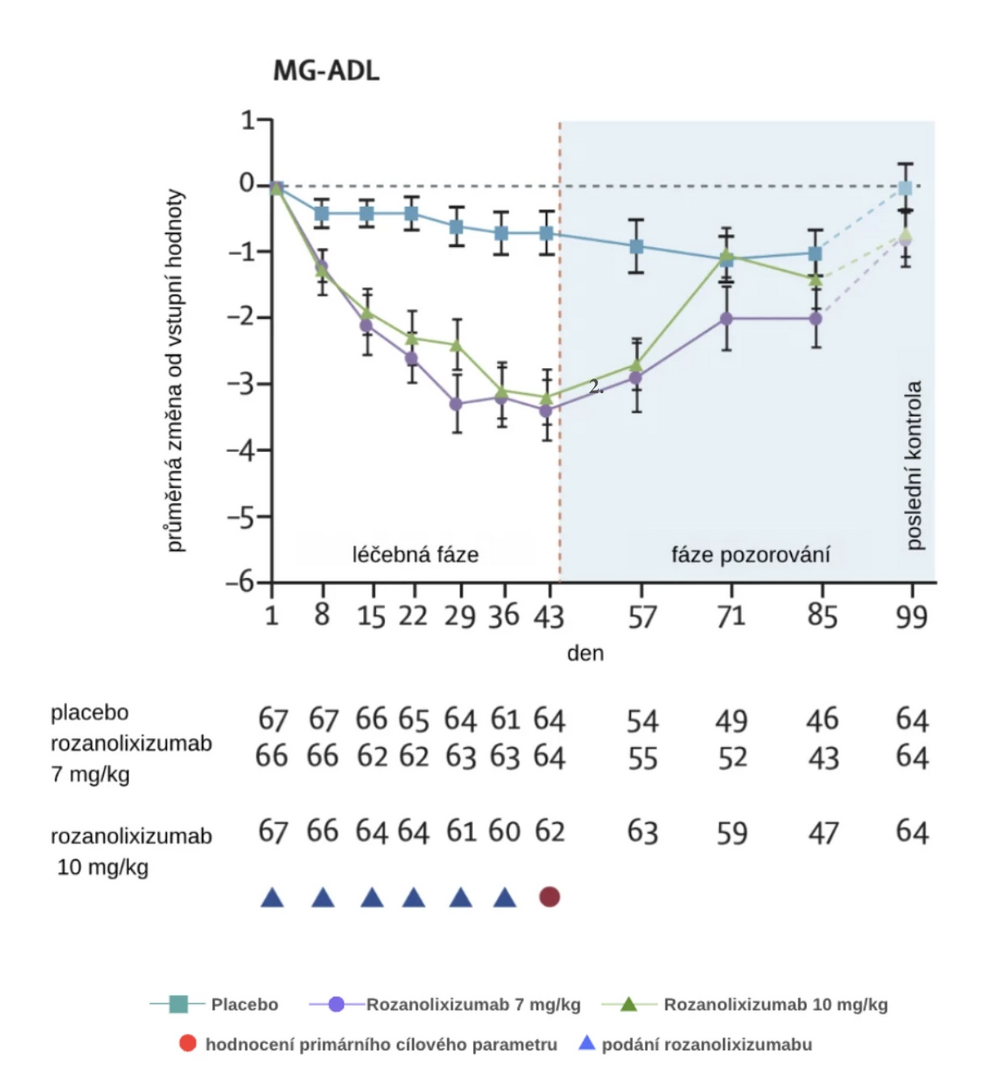
Randomizace byla stratifikována podle stavu autoprotilátek AChR a MuSK. Primárním cílovým ukazatelem účinnosti byla změna ve skóre MG-ADL za 43 dní, hodnocena byla i bezpečnost léčiva.
Výsledky
Do studie bylo mezi červnem 2019 a 2021 zařazeno 200 pacientů. Byl prokázán efekt u obou podávaných dávek, a to u pacientů s AChR Ab i MuSK Ab. U skupiny s dávkou 7 mg/kg bylo pozorováno zlepšení MG-ADL průměrně o 3,37 bodu (o 2,59 bodu více než ve skupině s placebem) a u skupiny s dávkou 10 mg/kg o 3,40 bodu (o 2,62 bodu více než ve skupině s placebem).
Nežádoucí příhody související s léčbou (TEAEs) se vyskytly u 52 (81 %) pacientů v skupině s dávkou 7 mg/kg, u 57 (83 %) ve skupině s 10 mg/kg a u 45 (67 %) ve skupině s placebem. Nejčastější byly bolesti hlavy (45 % v skupině 7 mg/kg, 38 % ve skupině 10 mg/kg, 19 % ve skupině s placebem), průjem (25 %, 16 %, resp. 13 %) a horečka (13 %, 20 %, resp. 1 %). Závažné TEAEs byly zaznamenány u 5 (8 %) pacientů ve skupině s 7 mg/kg, 7 (10 %) ve skupině s 10 mg/kg a 6 (9 %) ve skupině s placebem. Nebylo hlášeno žádné úmrtí související s léčbou.
Závěr
Výzkum nových léčiv u generalizované formy MG se v posledních letech posunul výrazně dopředu. Dobrou ukázkou jsou příznivé výsledky klinické studie s rozanolixizumabem, který blokádou neonatálního receptoru Fc zvyšuje degradaci protilátek v krvi. Účinek byl prokázán u obou podávaných dávek (7 i 10 mg/kg/den) a léčivo bylo dobře tolerováno. Navíc nejde o jedinou nově příchozí léčivou látku v této indikaci. Vyvstává tedy otázka, zda výhledově nedojde k radikální změně strategie léčby u generalizované formy MG včetně eliminace chronického podávání kortikoidů, jako tomu bylo například u roztroušené sklerózy.
(dos)
Zdroje:
1. Bril V., Drużdż A., Grosskreutz J. et al. Safety and efficacy of rozanolixizumab in patients with generalised myasthenia gravis (MycarinG): a randomised, double-blind, placebo-controlled, adaptive phase 3 study. Lancet Neurol 2023 May; 22 (5): 383−394, doi: 10.1016/S1474-4422(23)00077-7.
2. Menon D., Bril V. Pharmacotherapy of generalized myasthenia gravis with special emphasis on newer biologicals. Drugs 2022; 82 (8): 865−887, doi: 10.1007/s40265-022-01726-y.
3. Piťha J. Refrakterní myasthenia gravis – klinická charakteristika a možnosti biologické léčby. Česká a slovenská neurologie a neurochirurgie 2019; 82(5): 490−495, doi: 10.14735/amcsnn2019490.
4. Týblová M. Novinky v léčbě myasthenia gravis. Neurologie pro praxi 2023; 24 (4): 286−292, doi: 10.36290/neu.2023.057.
Líbil se Vám článek? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Štítky
Neurochirurgie Neurologie Praktické lékařství pro dospělé Dětská neurologie
Nejnovější kurzy
Autoři: MUDr. Stanislav Voháňka, MBA. CSc.
Přejít do kurzů
Nejčtenější tento týden Celý článekPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



