-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Cenobamát jako cesta krok za krokem k bezzáchvatovosti u pacientů s farmakorezistentní epilepsií
26. 9. 2024
Co patří mezi hlavní překážky dosáhnutí bezzáchvatovosti u epilepsie? Jaké důsledky má nekontrolovaná epilepsie? A proč je důležitá snaha optimalizovat léčbu cenobamátem pro co nejlepší výsledky u pacientů? Odpovědi na tyto otázky nabídl v půlce června bratislavský seminář nazvaný „Späť v hre: Krok za krokom k životu bez záchvatov“, který se věnoval léčbě pacientů s farmakorezistentní epilepsií a konal se pod záštitou II. neurologické kliniky LF UK a UN Bratislava a s podporou společnosti Angelini.
Stigma epilepsie trvá i v 21. století
Při léčbě epilepsie je stěžejní uvědomovat si, že neléčíme nemoc, ale pacienta, a že tudíž je třeba zohledňovat jeho zdravotní, sociální a další potřeby. V úvodní přednášce to připomněla odborná garantka semináře doc. MUDr. Gabriela Timárová, Ph.D. Shrnula historii a hlavní milníky terapie epilepsie a zdůraznila, že za tisíce let se nezměnil závažný společenský dopad epilepsie, včetně izolace a diskriminace pacientů.
Čím vším si musí pacient a jeho blízcí projít po prvním záchvatu a diagnostikování epilepsie, popsala doc. MUDr. Eva Feketeová, Ph.D., z Neurologické kliniky LF UPJŠ v Košicích. V této souvislosti upozornila na recentní cílený přehled literatury věnované široké škále protizáchvatových léků (ASMs) běžně používaných při terapii vývojových a epileptických encefalopatií. Jeho autoři se zabývali nejnovějšími důkazy o účincích těchto látek na chování, náladu, kognici, sedaci a spánek i o jejich bezpečnostním profilu, respektive výskytu nežádoucích příhod (NP) při jejich užívání.
InzerceV registrované sekci můžete po přihlášení zhlédnout kompletní záznam celého semináře: přístup z Česka, přístup ze Slovenska.
Terapeutický nihilismus není na místě
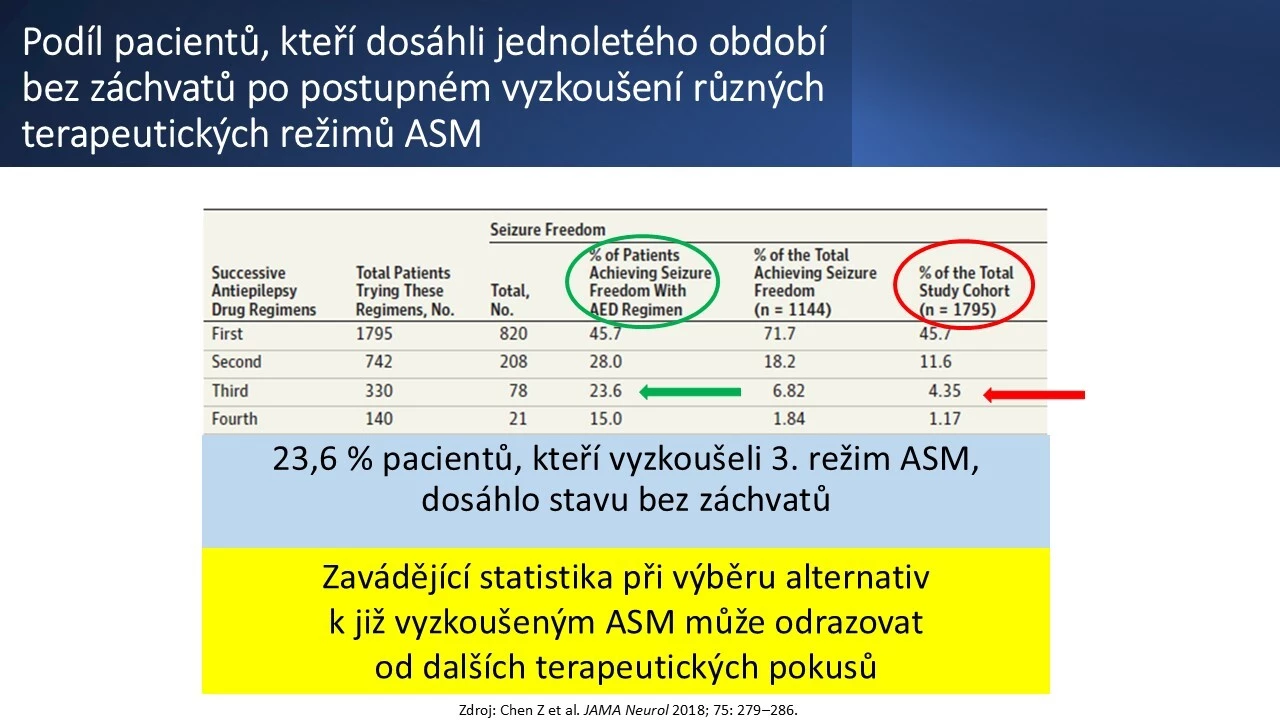
S očekávanou přednáškou vystoupila prof. Simona Lattanzi z Neurologické kliniky Polytechnické univerzity v Anconě. Připomněla, že léčba epilepsie je stále hlavně symptomatická. Hlavním cílem je ovšem úplné osvobození od záchvatů (SF – seizure freedom), a to s minimálními nežádoucími účinky (NÚ) terapie, ještě lépe zcela bez nich. Skutečným primárním cílem je pak dosažení dobrého zdraví a dobré kvality života. Nic se nezměnilo ani na faktu, že účinnost každého dalšího ASMs klesá s každým dalším vyzkoušeným terapeutickým režimem. Je fakt, že již na třetím režimu ASMs dosáhlo bezzáchvatovosti jen dalších 4,35 % pacientů z celého hodnoceného souboru. Bylo to však zároveň 23,6 % pacientů z těch, kteří ho užívali. Slovy přednášející i po pěti šesti vyzkoušených lécích pořád existuje pravděpodobnost dosažení bezzáchvatovosti, byť již malá. Není proto na místě terapeutický nihilismus, ale naopak má stále smysl zkoušet další léky.

Hlavní překážky na cestě k osvobození od záchvatů mohou tvořit faktory na straně onemocnění (zejména etiologie), pacienta i managementu léčby, jako jsou chyby v diagnostice (tzv. pseudonekontrolovaná epilepsie), zpožděné načasování léčby a její nedostatečná optimalizace. Faktory související se samotnou terapií, pseudofarmakorezistenci a zpožděné nastavení léčby lze přitom jednoznačně ovlivnit.
Následky nekontrolované epilepsie
Nedosažení SF s sebou nese výrazné zhoršení kvality života pacientů. Z randomizovaných kontrolovaných studií přitom vyplývá, že významně a příznivě dokáže ovlivnit kvalitu života pouze úplné odstranění záchvatů. Hlavním cílovým ukazatelem v evropském prostředí je obvykle míra odpovědi (nikoliv bezzáchvatovost), tedy snížení frekvence záchvatů o ≥ 50 %; to však podle studií ke zlepšení kvality života pacientů nestačí. S nekontrolovanou epilepsií souvisí například nezaměstnanost. Podle nedávných dat z Německa tvořil jediný prediktor pokračování v zaměstnání benigní průběh epilepsie se záchvaty v remisi.
Pacienti s nekontrolovanou epilepsií jsou také vystaveni zvýšenému riziku předčasného úmrtí. Většinou to přímo souvisí s příčinou epilepsie, mezi další důvody patří náhlé úmrtí při epilepsii (SUDEP), úrazy, sebevraždy a status epilepticus. V nedávné zahraniční studii se ukázalo, že výskyt ≥ 3 generalizovaných tonicko-klonických záchvatů za rok již byl spojen s dramaticky zvýšeným rizikem SUDEP (poměr šancí [OR] 15,46).
Co přinesl do managementu protizáchvatové léčby cenobamát
Významný pokrok při snaze o dosažení SF prokázal cenobamát, zástupce 3. generace ASMs. Tato generace léčiv se před jeho příchodem sice vyznačovala lepší snášenlivostí a menším výskytem lékových interakcí než generace předchozí, ale podle longitudinálních dat nezvýšila podíl pacientů, kteří dosáhli SF. Cenobamát byl nepřímo porovnán s jinými ASMs (brivaracetam, eslikarbazepin, lakosamid, perampanel) v síťové metaanalýze (4) a oproti nim signifikantně zvýšil míru odpovědí i podíl pacientů, u nichž klesl výskyt záchvatů o ≥ 50 %. Tento lék měl dle autorů analýzy největší pravděpodobnost stát se nejlepší možností z hlediska dosažení bezzáchvatovosti v porovnání s ostatními zástupci 3. generace ASMs.

Důležitost titrace dle SPC a úprava konkomitantní protizáchvatové medikace
S podáváním cenobamátu je spojená potřeba titrace alespoň do doporučené terapeutické dávky 200 mg (do klinické praxe přešlo titrační schéma vyplývající ze studie C021) i sledování známých lékových interakcí. Titrace by měla pokračovat až do dosažení cílové udržovací dávky (200−400 mg denně), s výjimkou situace, kdy je stavu SF dosaženo při nižších dávkách, daří se jej udržet a zároveň pacient užívá už jen malé množství léků. Cílem má být snížit celkovou lékovou zátěž; podle přednášející je vhodné postupně zvyšovat dávku cenobamátu s tím, že se sníží dávka jiného léku nebo je tento zcela vysazen. To potvrdila i post hoc analýza multicentrické otevřené studie fáze III (5), ve které bezmála čtvrtina pacientů, kteří pokračovali v přídatné léčbě cenobamátem, kompletně vysadila 1 či více protizáchvatových léků. Doporučení, jak upravit dávky konkomitantní medikace ASMs při titraci dávky cenobamátu, bylo publikováno v roce 2022.

Účinnost i snášenlivost cenobamátu závisejí na dávce
Literatura ukazuje, že největší efekt cenobamátu se projevuje při dávce 400 mg denně. Nejlepší rovnováha mezi účinností a snášenlivostí se pak podle autorky sdělení obvykle vyskytuje v rozmezí denních dávek 150−350 mg, přičemž i zde často dochází k dosažení bezzáchvatovosti.
Určitě je žádoucí úprava a snížení konkomitantní medikace s cílem zlepšit snášenlivost i adherenci pacientů k medikaci, zmírnit lékovou zátěž (polyfarmacii) a vyhnout se farmakokinetickým a farmakodynamickým interakcím. Dosažení udržovací dávky 200 mg denně to podle prof. Lattanzi umožňuje. Velmi vhodné je, pokud po úpravě souběžné medikace cenobamát představuje jediný blokátor sodíkových kanálů ve zvoleném farmakoterapeutickém režimu (kombinaci ASMs). Zásadní je snaha co nejvíce rozvinout racionální polyterapii, respektive vyhnout se polyterapii iracionální – tedy léčit správně a neléčit nadměrně ani nedostatečně.
Celou přednášku si můžete zhlédnout zde.
Eva Srbová
redakce proLékaře.czZdroje:
1. Timárová G. Epilepsia vtedy a teraz – nestrácať už viac čas. Seminář „Späť v hre: Krok za krokom k životu bez záchvatov“, Bratislava, červen 2024.
2. Feketeová E.Niečo za niečo alebo ako získať maximálny účinnok. Seminář „Späť v hre: Krok za krokom k životu bez záchvatov“, Bratislava, červen 2024.
3. Lattanzi S. Uncontrolled epilepsy and barriers to seizure freedom – optimizing treatment in clinical practice. Seminář „Späť v hre: Krok za krokom k životu bez záchvatov“, Bratislava, červen 2024.
4. Lattanzi S., Trinka E., Zaccara G. et al. Third-generation antiseizure medications for adjunctive treatment of focal-onset seizures in adults: a systematic review and network meta-analysis. Drugs 2022; 82 (2): 199−218, doi: 10.1007/s40265-021-01661-4.
5. Rosenfeld W. E., Abou-Khalil B., Aboumatar S. et al. Post hoc analysis of a phase 3, multicenter, open-label study of cenobamate for treatment of uncontrolled focal seizures: effects of dose adjustments of concomitant antiseizure medications. Epilepsia 2021; 62 (12): 3016−3028, doi: 10.1111/epi.17092.
6. Strzelczyk A., Schubert-Bast S. Psychobehavioural and cognitive adverse events of anti-seizure medications for the treatment of developmental and epileptic encephalopathies. CNS Drugs 2022; 36 (10): 1079−1111, doi: 10.1007/s40263-022-00955-9.
Líbil se Vám článek? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Štítky
Neurologie
Nejnovější kurzy
Autoři: MUDr. Jana Zárubová, MUDr. Jana Amlerová, Ph.D., MUDr. Adam Kalina
Autoři: doc. MUDr. Martin Pail, Ph.D.
Přejít do kurzů
Nejčtenější tento týden Celý článekPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




