-
Medical journals
- Career
Abdominální kompartment syndrom u polytraumat
Authors: Jan Stránský; Milan Šír; Leopold Pleva
Authors‘ workplace: Lékařská fakulta Ostravské univerzity ; Traumatologické centrum Fakultní nemocnice Ostrava
Published in: Úraz chir. 25., 2017, č.4
Overview
Úvod:
Traumatický abdominální kompartment syndrom je závažnou a potenciálně život ohrožující komplikací, vyskytující se u těžkých poranění břicha. Vzniká jako důsledek nárůstu intraabdominálního tlaku a jeho vlivu na ventilaci a cirkulaci včetně mikrocirkulace. To se projevuje hypoventilací, negativním dopadem na srdeční činnost a orgánovou dysfunkcí. K jeho diagnostice využíváme nejčastěji měření intravezikálního tlaku spolu s hodnocením klinického stavu.
Materiál:
V našem sdělení uvádíme soubor 15 pacientů s rozvinutým traumatickým abdominálním kompartment syndromem hospitalizovaných na Klinice úrazové chirurgie Ostrava v letech 2006 – 2015. Tito pacienti vycházejí ze skupiny 422 nemocných, kteří byli na našem pracovišti v daném období operovaní pro poranění břicha.
Výsledky:
Ze skupiny 15 pacientů s rozvinutým abdominálním kompartment syndromem zemřelo šest pacientů. Ve všech případech se jednalo o závažná polytraumata. Dekompresní operace byla provedena u dvou pacientů ihned po příjmu do nemocnice, u zbylých pacientů byl výkon proveden v průměru po 2,81 dnech. V podrobném textu pak rozebereme podrobnější rozbor vývoje stavu u vybraných případů.
Závěr:
Hodnoty intraabdominálního tlaku nad 20 mmHg se současnou přítomností klinických příznaků považujeme za indikaci k provedení dekompresní laparostomie. Tento výkon můžeme provést rovněž preventivně u těžkých abdominálních traumat, kde již podle vstupního nálezu můžeme očekávat vysoké riziko rozvoje abdominálního kompartment syndromu.
Klíčová slova:
Abdominální kompartment syndrom, poranění břicha, intraabdominální tlak, laparostomie.
ÚVOD
Kompartment syndrom je obecně uváděn jako stav, kdy v ohraničeném anatomickém prostoru dochází k vzestupu tlaku, který nepříznivě ovlivňuje cirkulaci a ohrožuje funkčnost a vitalitu tkání či orgánů v tomto prostoru. K tomuto stavu může docházet v osteofasciálních prostorách končetin, v prostoru intrakraniálním, hrudníku a v dutině břišní [7].
Abdominální kompartment syndrom (ACS) je definován jako pozdní manifestní projev zvýšeného intraabdominálního tlaku (IAP). Tento stav je spojen s významnou morbiditou i letalitou [8]. V posledních letech bylo publikováno množství prací věnovaných této problematice, na základě kterých společnost World Society of the Abdominal Compartment Syndrome (WSACS) vypracovala konsenzuální definice pojmů a doporučení léčebných postupů ACS.
Při úrazech dochází ke zvýšení IAP a případnému následnému ACS nejčastěji u těžkých abdominálních poranění, a to buď primárnímu nebo sekundárnímu [18].
Příčiny vzniku primárního ACS:
- masivní intraabdominální a retroperitoneálního krvácení,
- krvácení v důsledku rozvoje potraumatické koagulopatie,
- distenze a edém střevních kliček při poranění mezenteriálních cév,
- nahromadění koagul, případně tamponáda nechirurgického krvácení v subfrenickém, pánevním nebo retroperitoneálním prostoru,
- perforační poranění GIT s následným rozvojem peritonitidy a ileozního stavu.
Příčiny vzniku sekundárního ACS:
- resuscitace nadměrným množstvím krystaloidů,
- uzávěr břišní stěny pod napětím.
Typický klinický obraz rozvinutého ACS:
- Distenze břišní stěny (obr. 4).
- Ventilační insuficience, spojená s nárůstem inspiračních tlaků v důsledku zvýšeného stavu bránice, hypoxií a hyperkapnií.
- Snížený srdeční výkon.
- Oligurie až anurie zachovalém MAP.
NEMOCNÍ
V Traumacentru FN Ostrava jsme v letech 2006 - 2015 provedli 422 operací pro poranění břicha (tab. 1). Velká část těchto poranění byla součástí rozsáhlejších polytraumat. Etiologicky dominují dopravní úrazy a pády z výšky (tab. 2). Další významnou skupinou jsou pracovní úrazy ve smyslu přimáčknutí stroji či zavalení zeminou a břemeny. Skupina kriminálních úrazů jako bodná a střelná poranění byla častěji zastoupena spíše jako poranění izolovaná, či sdružená s méně závažným postižením dalších tělesných regionů.
V souboru našich pacientů jsme zaznamenali celkem 15 případů rozvinutí ACS, zastoupeno bylo devět mužů a šest žen. Věkové spektrum od 10 do 69 let (průměr 43,4, medián 43). V převážné většině se jednalo o závažná polytraumata s ISS 27 - 66 (průměr 39,8, medián 38), pouze v jednom případě se jednalo o izolované poranění břicha po kopnutí koněm s lacerací jater. Mezi příčinami dominují dopravní úrazy (celkem osm). Dále jsou tři pády z výšky, jeden případ brachiálního násilí mezi partnery, jeden případ - zavalení kmenem při kácení stromů a jeden případ suicidálního pokusu skokem pod vlak.
Ve 14 případech bylo přítomno závažné břišní poranění (tab. 3). U 11 pacientů bylo přidruženo poranění hrudníku (mnohočetné fraktury žeber, poranění plic), u pěti pacientů významné končetinové poranění, u tří pacientů komplexní zlomenina pánve. Ve dvou případech jsme zaznamenali poranění břišní aorty, jednou řešeno suturou a jednou stentáží. U jedné pacientky bylo současně přítomno těžké kraniotrauma, které bylo nakonec příčinou smrti šestý den po úrazu.
VÝSLEDKY
Z našeho souboru zemřelo šest pacientů. Čtyři úmrtí byly v důsledku rozvinutí MODS a MOF v rozmezí 24 h až 30 dnů od úrazu. Jedno úmrtí bylo způsobeno výše zmíněným kraniotraumatem a poslední úmrtí bylo zapříčiněno irreverzibilním hemoragicko-traumatickým šokem u pacientky po suicidálním pokusu skokem pod vlak. U této pacientky byla po přijetí v kritickém stavu emergentně dokončena traumatická amputace obou dolních končetin a pravé horní končetiny, následně provedeno CT vyšetření s průkazem minima volné tekutiny v břiše. S odstupem 21 h od úrazu při horšícím se celkovém stavu i klinickému nálezu na břiše provedena laparotomie s nálezem drobných ruptur mezenteria, céka a ilea s okolními rozsáhlými kontuzemi. Provedeny sutury a laparostomie, po dalších pěti hodinách však dochází k exitu.
Dekomprese břišní dutiny byla u dvou pacientů provedena ihned po přijetí do naší péče. V obou případech se jednalo o příjem s odstupem 12–15 hodin od úrazu. 38letá žena, zbita doma partnerem, nalezena s poruchou vědomí, předána na urgentní příjem již na UPV, hypotenzní s podporou vazopresorů. Klinicky distenze břišní stěny, absence peristaltiky, četné hematomy. Na CT nález hemo-pneumoperitonea se suspektním poraněním duodena a kontuzí ledviny. Provedena revize dutiny břišní, s nálezem téměř kompletní ruptury duodena v segmentu D2 a rozsáhlé nekrózy mezokolon. Provedena hemikolektomie a resekce duodena s jeho slepým uzávěrem. Ponechán „open-abdomen“. Po 16 hodinách dochází k exitu v důsledku rozvinutého septického šoku. Ve druhém případě se jednalo o 36letého muže, chodce sraženého osobním automobilem. Primárně přijat na ARO okresní nemocnice. Iniciálně neklidný, intubován. Na RTG zjištěna symfyzeolýza dva centimetry a fraktura acetabula vlevo. USG neprokázala volnou tekutinu v dutině břišní, CT mozku popsáno jako nehodnotitelné, dále fraktura bérce a mnohočetné kontuze měkkých tkání. S rozvíjející se oběhovou nestabilitou pro obavy z pánevního krvácení naložena na operačním sále pánevní svorka a provedena explorativní laparotomie, bez nálezu významnějšího zdroje krvácení, s kompletním uzávěrem břišní dutiny. Celkem v rámci resuscitace podáno 7,5 l tekutin, 26 TU EBR a 22 TU FFP, Novoseven, Fibrinogen, trombonáplavy. Následně letecký transport do TC FNO cca 12 hodin od úrazu. Při příjmu pacient na UPV, tuhé, distendované břicho (obr. 1) bez slyšitelné peristaltiky, chladná periferie s obleněnou kapilaritou, anurický. Na CT drobný SAK T-O bilat., drobné kontuze F-P vpravo, P vlevo, zlomenina nosních kůstek, prokrvácení PND, fluidothorax bilat., dorzobazálně plicní kontuze, bubliny vzduchu v portálním řečišti, lemy tekutiny pod játry, slezinou a kolem pankreatu, lem tekutiny kolem psoatu vlevo, mezikličkový hematom, výrazná distenze kliček střevních, obraz paralýzy střevní, vzduch ve stěně střevní a v žilním systému mezenteria a horní mezenterické žíly (obr. 2), zlomeniny těl Th11 a Th12, zlomeniny dolního raménka kosti stydké vpravo, předního pilíře acetabula vpravo, symfyzeolýza. Bezprostředně provedena revize břišní dutiny s nálezem minimálního hemoperitonea, rozsáhlé gangrény tenké kličky (obr. 3) a ascendentu, sterkorální peritonitidy a masivního retroperitoneálního hematomu. Provedena resekce tenké kličky s hemikolektomií (obr. 4), ponecháním laparostomie a stabilizace pánve zevním fixátorem. Přes následnou resuscitační péči dochází po dalších 24 hodinách k exitu.
Image 1. Klinický obraz ACS – distenze břišní stěny 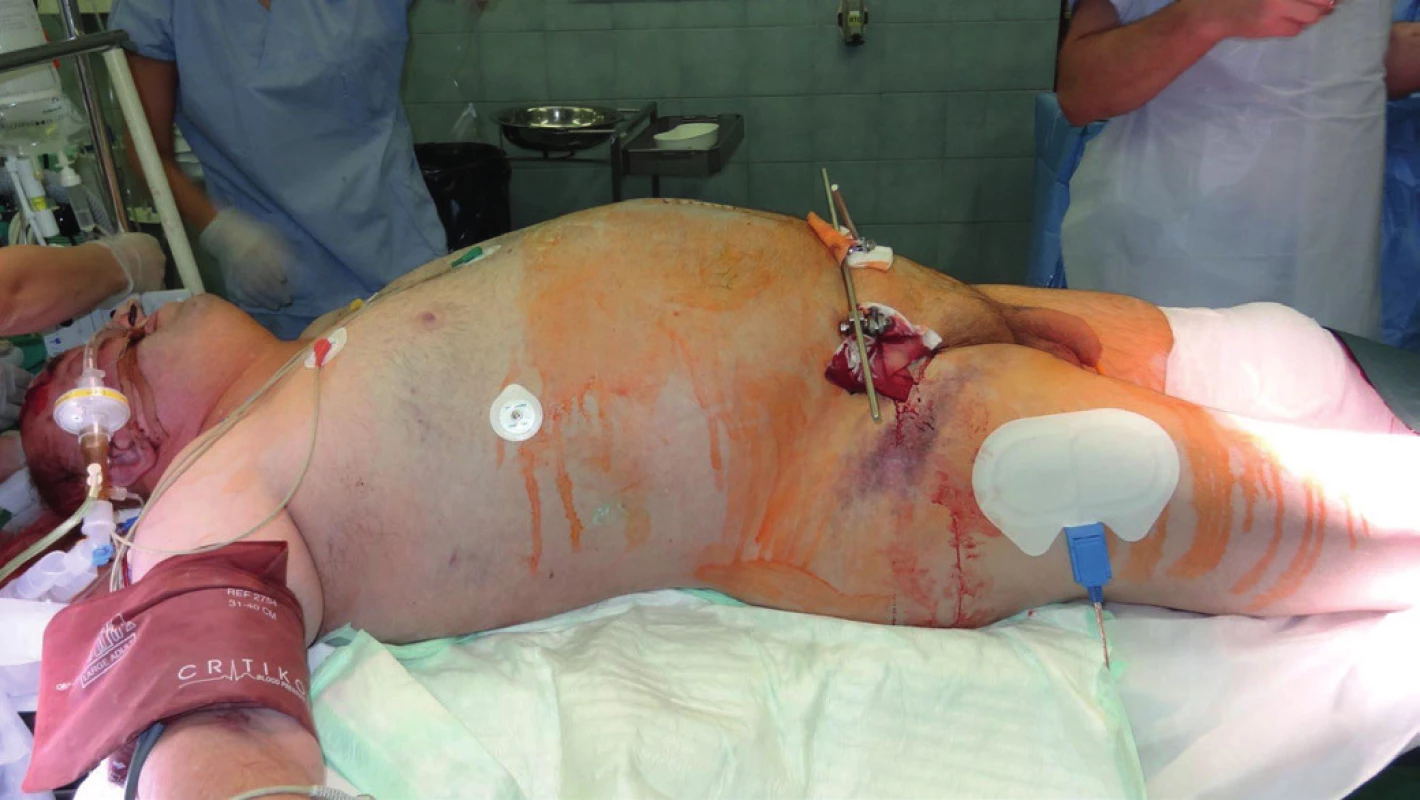
Image 2. CT nález při rozvinutém ACS – mezikličkový hematom, výrazná distenze kliček, obraz střevní paralýzy, vzduch ve stěně střevní a v žilním systému mezenteria 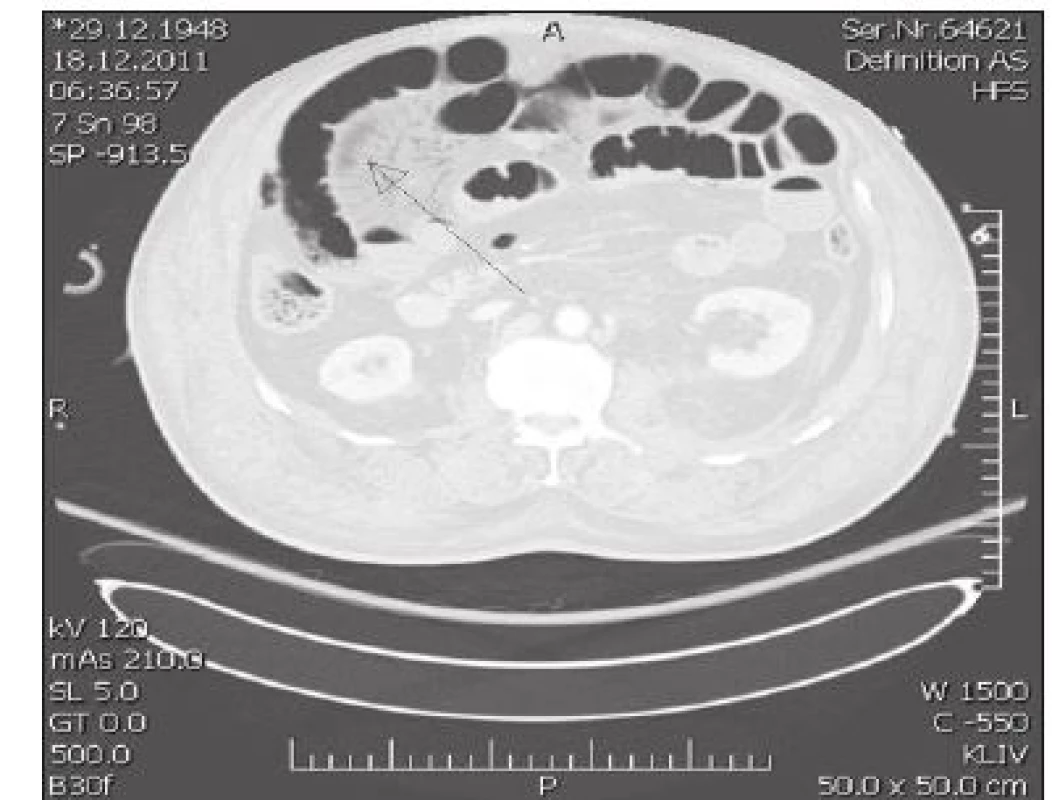
Image 3. Nekróza kličky tenkého střeva při rozvinutém ACS 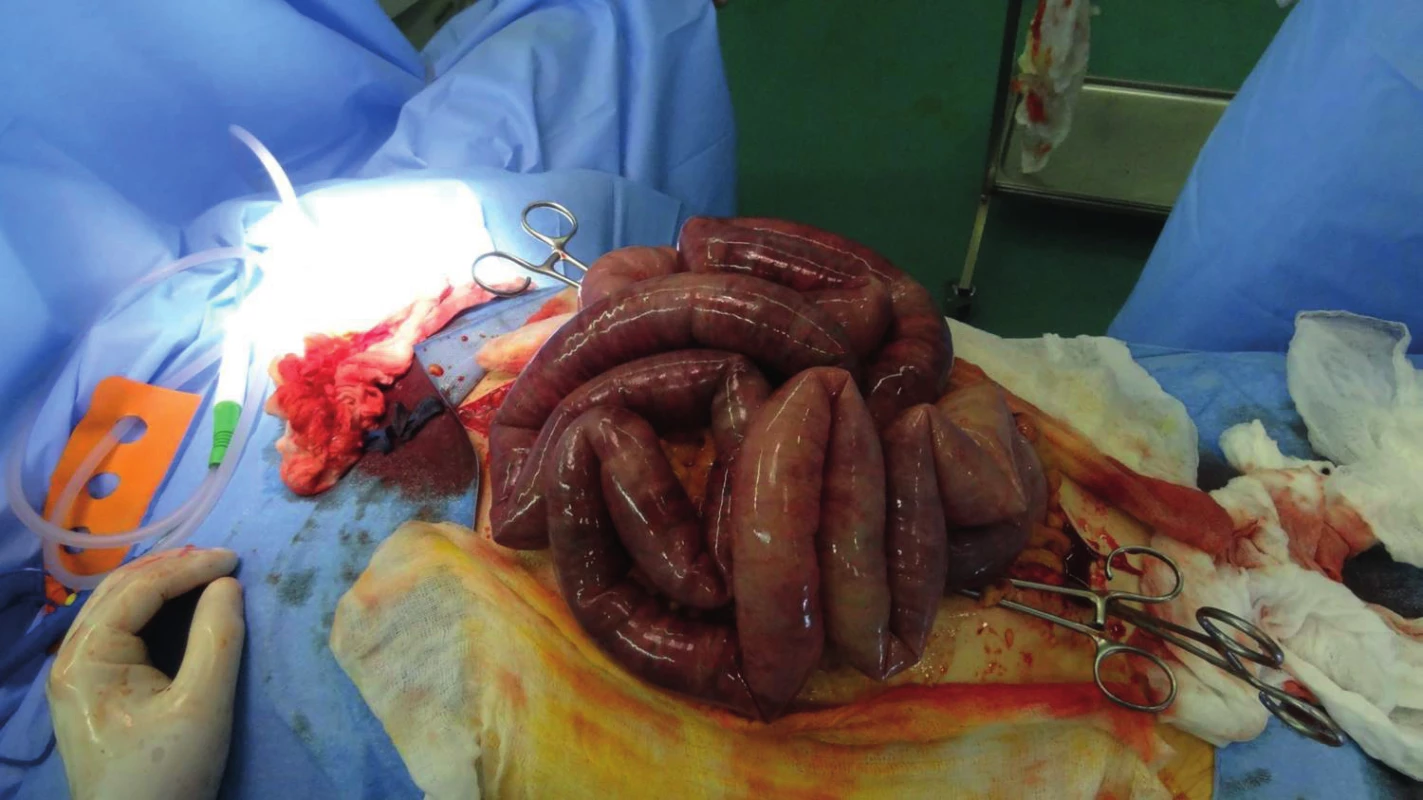
U ostatních pacientů byla dekompresní operace provedena v průměru 2,81 dne od úrazu (medián 2). Ve všech případech byla provedena laparostomie a dočasný uzávěr dutiny břišní pomocí nesmáčivých roušek, Ethizipu, případně za použití VAC systému (obr. 5).
Image 4. Resekát nekrotické tenké kličky a céka 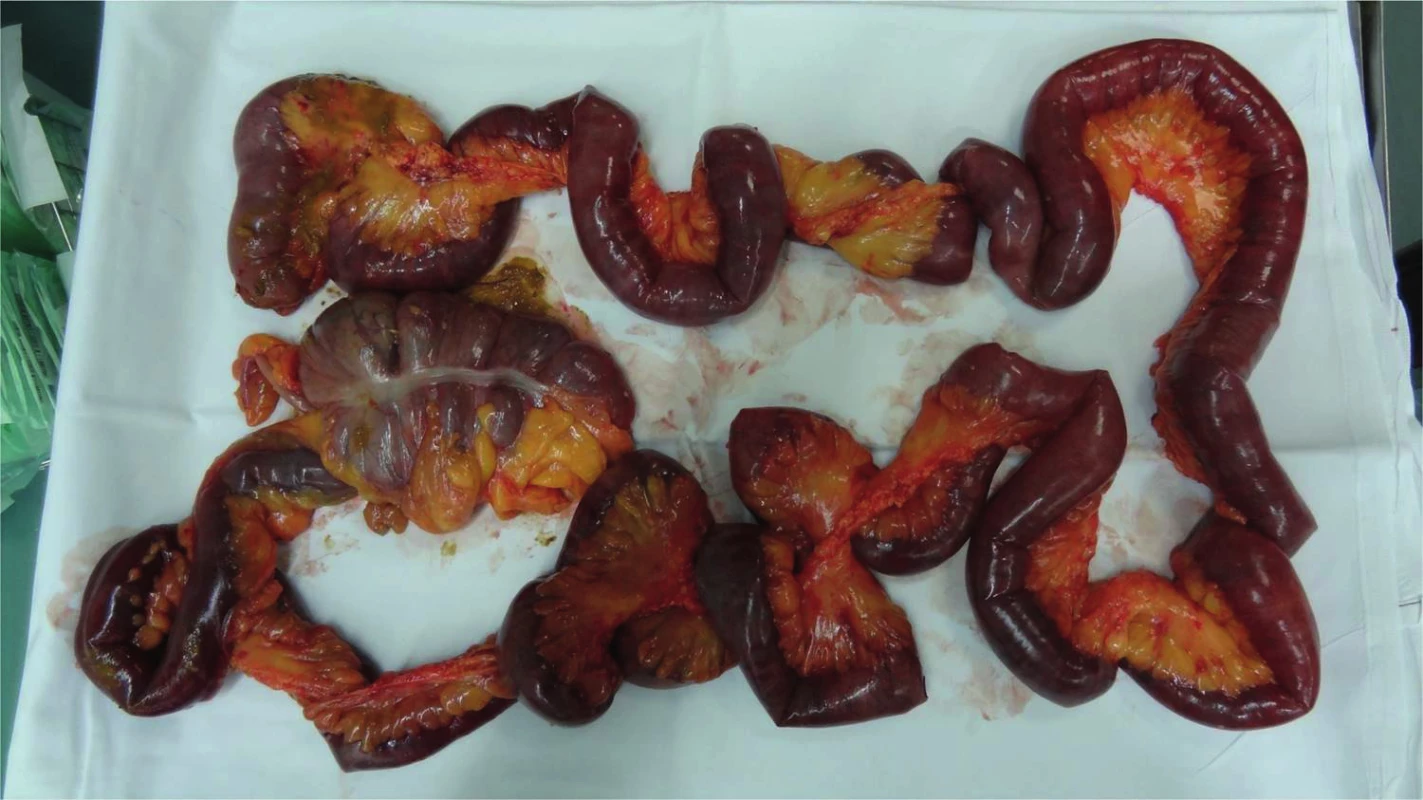
Image 5. Laparostomie s využitím VAC systému 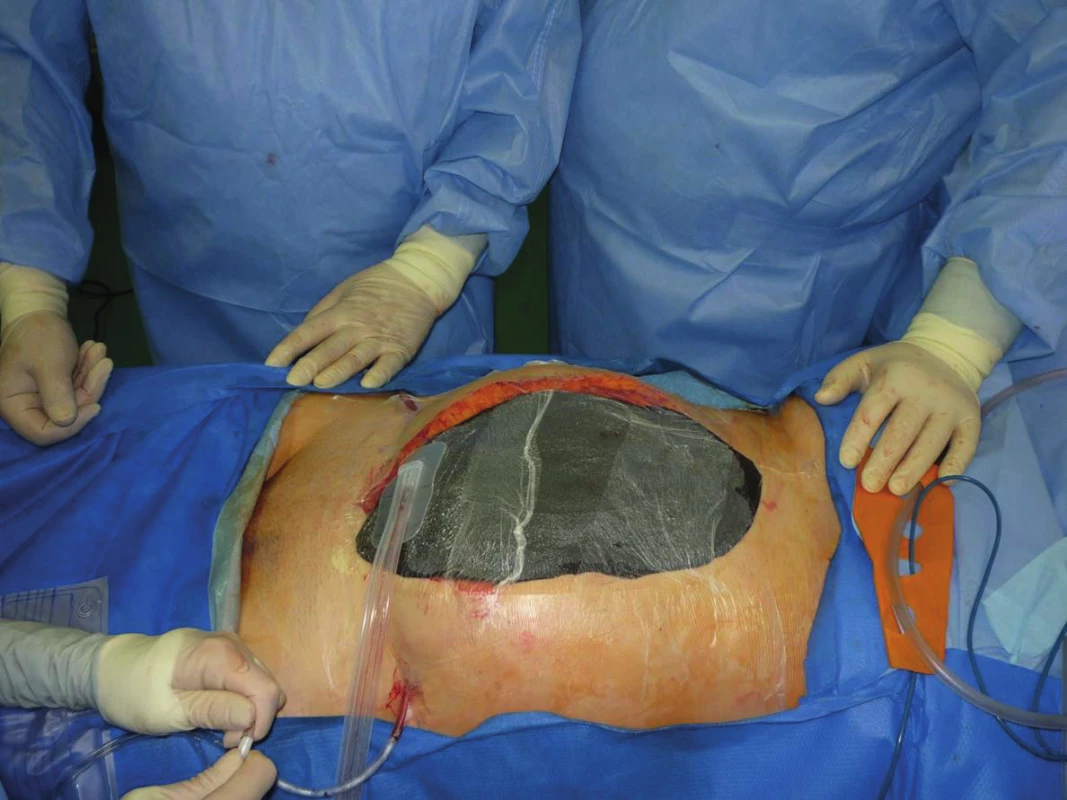
Definitivní uzávěr jsme provedli nejdříve po třech dnech, nejpozději pak po 10 dnech. V jednom případě pak byl „open-abdomen“ ponechán celkem 30 dnů u pacienta s disekcí aorty, kde byly prováděny opakované revize břicha a retroperitonea. Stav progredoval k exitu 30 dnů od úrazu v důsledku MOF a MODS. V celém souboru našich pacientů se dostáváme k incidenci ACS 3,6 %, což je v souladu s hodnotami uváděnými ve světové literatuře u pacientů s poraněním břicha.
DISKUZE
ACS má závažné důsledky abdominální i systémové [11]. Mortalita fulminantního ACS je až 67 % [1]. Mimo typického klinického obrazu zmíněného v úvodu, má vzestup IAP a rozvoj ACS další patofyziologické vazby. V rámci cirkulačního systému jde zejména o snížení srdečního výdeje, snížený venózní návrat a vzestup periferní vaskulární rezistence. Experimentální práce prokázaly, že zvýšený IAP zapříčiňuje zhoršenou intestinální perfuzi vedoucí ke zvýšené produkci volných kyslíkových radikálů a bakteriální translokaci přes střevní stěnu [6]. Další experimentální práce prokazuje, že nárůst IAP nad 25 mmHg po dobu 60 minut vede ke snížení parciálního tlaku kyslíku ve střevní sliznici na méně než 30 % [3]. Zvýšený IAP způsobuje také alteraci hepatálních funkcí s prohloubením metabolické acidózy a koagulopatie, což v kruhu dále podporuje růst IAP. Vzhledem k tomu, že rozvojem ACS jsou významně ohroženi polytraumatizovaní pacienti, nezřídka s přidruženým kraniocerebrálním poraněním, nelze opomenout vazbu mezi nárůstem IAP a intrakraniálního tlaku (ICP) se snížením cerebrálního perfuzního tlaku a nebezpečím ischemického poškození [2].
K včasnému rozpoznání nebezpečí plynoucího z rostoucího IAP a předcházení ACS je nutná monitorace IAP u rizikových pacientů. Jednoduchou a spolehlivou metodou, která je zároveň minimálně invazivní, a proto je v současnosti využívána pro tento účel zřejmě nejčastěji, je intravezikální měření. Základ této metody popsal Kron et al. v roce 1984. Měření provádíme aplikací 50–100 ml fyziologického roztoku přes Folyeův katetr do močového měchýře. Katetr je následně zasvorkován a přes aspirační port je připojen převodníkový systém s manometrem [14]. Byly prokázány významné rozdíly při měření IAP v závislosti na pozici tlakového převodníku (úroveň symfýzy či flebostatické osy). Pro zajištění porovnatelných měření je doporučováno brát jako referenční úroveň u ležícího pacienta střední axilární linii [4]. V současné době existuje řada komerčních setů určených k tomuto měření. Na základě těchto hodnot definuje WSACS 4 stupně intraabdominální hypertenze (IAH) (tab. 3). Chirurgická dekomprese je pak indikována při třetím a čtvrtém stupni [17].
WSACS uvádí ACS jako IAP > 20 mmHg refrakterní ke konzervativním postupům a s projevem orgánového selhávání [15]. V tomto případě je jednoznačně indikovaná chirurgická dekomprese dutiny břišní. U pacientů s přítomností dvou a více rizikových faktorů pro IAH/ACS by měl být prováděn monitoring IAP po celou dobu trvání kritického stavu v intervalu maximálně 4 h [10]. Tito rizikoví pacienti vyžadují zapojení dostupných konzervativních prostředků ke snaze o normalizaci IAP a zábraně rozvinutí ACS. Tyto postupy zahrnují evakuaci obsahu GIT, se zavedením gastrické sondy a rektální rourky a podporu pasáže prokinetiky. Omezení objemu enterální výživy, případně přechod čistě na výživu parenterální. Zavedení analgetizace, přiměřené sedace a svalové relaxace, za současné pozornosti k jejich možným negativním dopadům. Držet vyrovnanou tekutinovou bilanci s omezením excesivní resuscitace tekutinami, kterou lze podpořit diureticky, podáváním hyperosmolárních roztoků a koloidů. Udržení abdominálního perfuzního tlaku (APP) nad 60 mmHg podáváním vazopresorů [9]. Důraz je kladen na polohu těla, se snahou o omezení pronační pozice a zamezení elevace horní poloviny těla o více než 20° vzhledem k lůžku, což významně zvyšuje IAP [16]. Chirurgická léčba spočívá v dekompresní operaci. Při ní odstraňujeme z dutiny břišní krev, důkladně všechna koagula a případný jiný sekret. Důkladně revidujeme a ošetřujeme případné krvácení (ligatury, opich…). Nechirurgické pokračující krvácení řešíme tamponádou. Dutinu břišní proplachujeme teplým fyziologickým roztokem [18]. Ponecháváme „open-abdomen“. K uzavření laparotomie lze pak využít řady metod. Nesmáčivé fólie, Ethizip, Bogota bag, vakuum-asistovaný uzávěr (VAC) a další (obr. 6, 7).
Image 6. Léčba ACS – dekomprese, nesmáčivé roušky 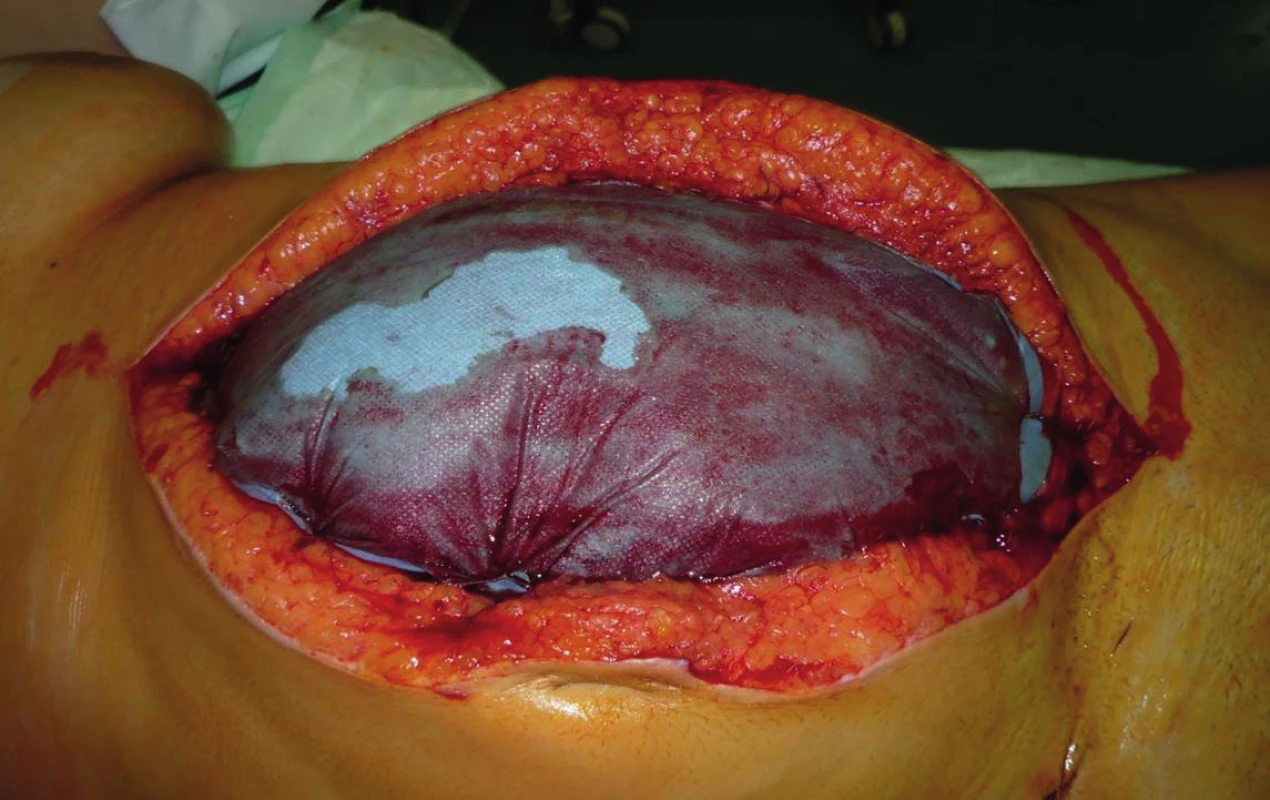
Image 7. Laparostomie kryta pomocí „Steri-Drape“ 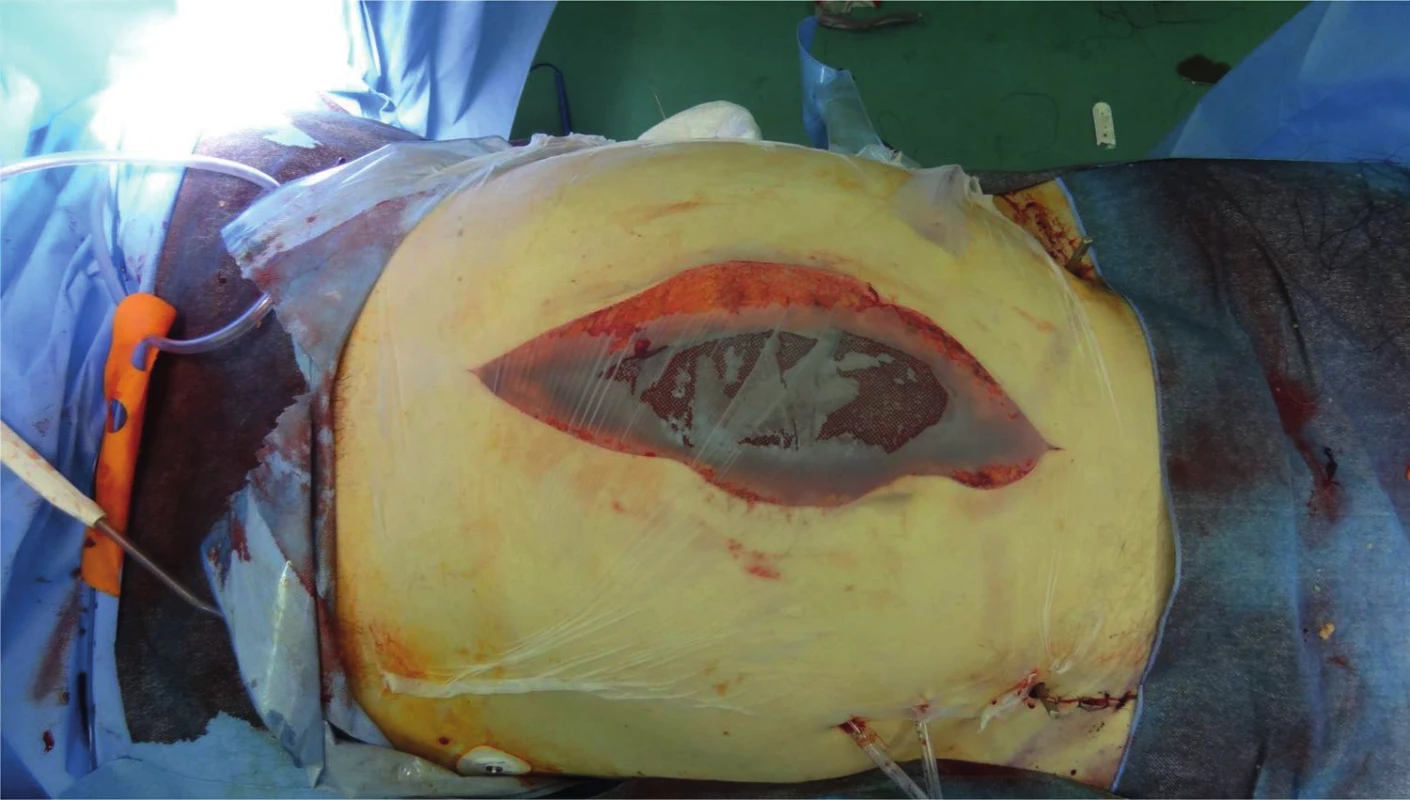
Dekompresní laparostomie vede k rychlé úpravě oxygenace a plicní compliance, rychle se upravují inspirační tlaky a promptně se obnovuje diuréza [1]. Dekomprese břišní dutiny může být následována rozvojem reperfuzního syndromu projevujícího se až asystolií. Za příčinu je považován náhlý pokles periferní vaskulární rezistence s následnou těžkou hypovolémií [13] nebo vyplavením anaerobních metabolitů z hypoperfundované splanchnické oblasti. K redukci těchto příznaků se doporučuje v maximální možné míře důsledná korekce acidobazické rovnováhy a hladin elektrolytů a také objemový „pre-load“ oběhu dvěma litry fyziologického roztoku a mannitolem a bikarbonátem před výkonem [5]. U pacientů, u kterých byla dekomprese provedena včasně před rozvojem významného orgánového selhání, lze provést primární fasciální uzávěr za pět až sedm dnů [8].
ZÁVĚR
Rozvinutý abdominální kompartment syndrom je závažný, život ohrožující stav, vyžadující neodkladné chirurgické řešení. Na jeho možný rozvoj musíme pomýšlet nejen u pacientů s těžkým abdominálním poraněním, ale také u pacientů po protrahovaných břišních operacích s masivní objemovou resuscitací [18]. U těchto rizikových pacientů je nezbytná pravidelná monitorace intraabdominálního tlaku. Tuto v současné době provádíme nejsnáze formou měření tlaku v močovém měchýři. Vzestup IAP nad 20 mmHg můžeme považovat za indikaci k provedení dekompresní laparostomie. Při rozvaze o postupu se však nelze opírat pouze o hodnoty IAP a je třeba se řídit rozvojem klinických příznaků při nedostatečné odpovědi na konzervativní léčbu. Nápadná distenze břišní stěny se pojí s ventilační insuficiencí, nárůstem ventilačních tlaků, oběhovou nestabilitou a alterací renálních funkcí. Tyto příznaky i při hraničních hodnotách IAP by nás měly vést k neprodlenému chirurgickému řešení – dekompresní laparostomii. Chirurgické řešení je sice nezbytný, ale až poslední stupeň v péči o pacienty ohrožené rozvojem ACS. Tito pacienti vyžadují již od úvodu komplexní multidisciplinární intenzivní péči, v níž musí být do maximální možné míry využity konzervativní postupy redukce IAP. Založení preventivní primární laparostomie je rovněž postupem, který při ošetření závažných břišních traumat má své místo.
MUDr. Jan Stránský
Sources
1. Asensio, AJ., Trunkey, DD. Current Therapy of Trauma and Surgical Critical Care. Philadelphia: Mosby, 2008. 785 s. ISBN 978-0-323-04418-9.
2. Bloomfield, GL., Dalton, JM., Sugerman, HJ. et al. Treatment of increasing intracranial pressure secondary to the acute abdominal compartment syndrome in patient with combined abdominal and head trauma. J Trauma. 1995, 39, 1168 - 1170. ISSN 0022-5282.
3. Bongard, F., PIANIM, N., dubecz, s. et al. Adverse consequences of increased intraabdominal pressure on bowel tissue oxygen. J Trauma. 1995, 39, 519-524. ISSN 0022-5282.
4. De Waele, JJ., De Laet, I., De Keuleaner, B. et al. The effect of different reference transducer positions on intra-abdominal pressure maeasurement: a multicenter analysis. Intensive Care Med. 2008, 34, 1299-1303. ISSN 0342-4642.
5. Eddy, V., Nunn, C., Morris, JA. Abdominal compartment syndrome. The Nashville experience. Surg Clin North Am. 1997, 77, 801-812. ISSN 0039-6109.
6. Eleftheriadis, E., kotzaMPASSI, k., pAPANOTAS, k. et al. Gut ischaemia, oxidative stress, and bacterial translocation in elevated abdominal pressure in rats. World J Surg. 1996, 20,11-16. ISSN 0364-2313.
7. Hildebrand, F. , Pape, HC. Acute compartment syndrome. Eur J Trauma Emerg Surg. 2014, 40, 519-520. ISSN 1863-9933.
8. Cheatham, ML. Abdominal compartment syndrome. Curr Opin Crit Care. 2009, 15, 154-162. ISSN 1070-5295.
9. Cheatham, ML. Nonoperative management of intraabdominal hypertension and abdominal compartment syndrome. World J Surg. 2009, 33, 1116-1122. ISSN 0364-2313.
10. Cheatham, ML., Malbrain, ML., Kirkpatrick, A. et al. Results from the International conference of experts on intra-abdominal hypertension and abdominal compartment syndrome. II. Recommendations. Intensive Care Med. 2007, 33, 951-962. ISSN 0342-4642.
11. Ivatury, RR., Porter, JM., Simon, RJ., et al. Intra-abdominal hypertension after life-threatening penetrating abdominal trauma: prophylaxis, incidence, and clinical relevance to gastric mucosal pH and abdominal compartment syndrome. J Trauma. 1998, 44, 1016-1021. ISSN 0022-5282.
12. Ivatury, RR., Diebel, l., porter, jm. et al. Intra-abdominal hypertension and the abdominal compartment syndrome. Surg Clin North Am. 1997, 77, 783-80. ISSN 0039-6109.
13. Kitka, M., Pleva, L. Poranenia orgánov brušnej dutiny. Košice : Klinika úrazovej chirurgie LF UJPŠ a FNLP, 2003. 71 s. ISBN 80-968824-5-7.
14. Kron, IL., harman, pk., nolan, sp. The measurement of intra-abdominal pressure as a criterion for abdominal re-exploration. Ann Surg. 1984, 199, 28-30. ISSN 0003-4932.
15. Malbrain, ML., Cheatham, ML., Kirkpatrick, A. et al. Results from the International conference of experts on intra-abdominal hypertension and abdominal compartment syndrome. I. Definitions. Intensive Care Med. 2006, 32, 1722-1732. ISSN 0342-4642.
16. McBeth, PB., Zygun, DA., Widder, S. et al. Effect of patient positioning on intra-abdominal pressure monitoring. Am J Surg. 2007, 193, 644-647. ISSN 0002-9610.
17. Meldrum, DR., MOORE, FA., MOORE, EE. et al. Prospective characterization and selective management of the abdominal compartment syndrome. Am J Surg. 1997, 174, 667-673. ISSN 0002-9610.
18. Pleva, L., Mayzlík, J., Šír, M. Abdominální kompartment syndrom u polytraumatu. Úrazová chirurgie. 2003, 11, 7-12. ISSN 1211-7080
Labels
Surgery Traumatology Trauma surgery
Article was published inTrauma Surgery

2017 Issue 4-
All articles in this issue
- Chirurgická stabilizace hrudní stěny – vývoj metody a současné trendy
- Abdominální kompartment syndrom u polytraumat
- Tupé poranění jater a sleziny v důsledku fraktury distálních žeber
- Zhodnocení střednědobých výsledků operačního řešení zlomenin krčku talu na Klinice úrazové chirurgie Fakultní nemocnice Brno
- Trauma Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Abdominální kompartment syndrom u polytraumat
- Tupé poranění jater a sleziny v důsledku fraktury distálních žeber
- Chirurgická stabilizace hrudní stěny – vývoj metody a současné trendy
- Zhodnocení střednědobých výsledků operačního řešení zlomenin krčku talu na Klinice úrazové chirurgie Fakultní nemocnice Brno
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

