-
Medical journals
- Career
Theralite a mnohočetný myelom – známe už odpověď na efektivitu léčby nefrologa s hematologem?
Authors: J. Lachmanová; Z. Hrušková; R. Ryšavá; M. Mysliveček; J. Straub 1; V. Tesař
Authors‘ workplace: Klinika nefrologie a I. Interní klinika1 Všeobecné fakultní nemocnice v Praze a 1. lékařské fakulty Univerzity Karlovy
Published in: Transfuze Hematol. dnes,26, 2020, No. 2, p. 131-138.
Category: Original Papers
Overview
Mnohočetný myelom spojený s nadprodukcí monoklonálních lehkých řetězců (FLC) vede u 20–40 % pacientů k renálnímu selhání a u 10 % vyžaduje dialyzační léčbu. V posledních 10 letech se užívá pro hemodialýzu Theralite, dialyzátor s vysoce propustnou high cut-off membránou (HCO), která umožní během dialýzy snížit koncentraci FLC o 70–90 %, a pokud je současně efektivní hematologická léčba, je možná i reparace renálních funkcí. Náš soubor v letech 2012–2018 tvořilo 37 pacientů s mediánem 8 hemodialýz (HD) na 1 pacienta a jen 1 pacient zemřel během dialyzačního léčení s HCO membránou. Bez dialyzační léčby do 3 měsíců (tzv. úspěšná skupina) bylo 24 pacientů (65 %), kteří měli medián 7 HD s HCO membránou (HCO-HD)/1 pacienta. Třináct pacientů (tzv. neúspěšná skupina) v další dialyzační léčbě pokračovalo a mělo 10 HCO-HD/1 pacienta. Sledovali jsme i osud těchto pacientů léčených v daném období a zjistili jsme mortalitu ve skupině úspěšné 21 % (5 úmrtí) a ve skupině neúspěšné 69 % (9 úmrtí). Pro prognózu pacienta je během finančně náročné dialyzační léčby s HCO membránou vhodné sledovat koncentrace FLC před i po HD a z grafického vyjádření lze předvídat efektivnost léčby HCO-HD. Nezbytná je úzká spolupráce s hematologem, který upřesní diagnózu a řídí chemoterapii.
Klíčová slova:
mnohočetný myelom – selhání ledvin – volné lehké řetězce – high cut-off membrána (Theralite)
Úvod
Renální selhání u pacientů s mnohočetným myelomem (MM) není žádnou vzácností a na jeho rozvoji se uplatňuje řada patogenetických mechanismů – nadprodukce FLC (free light chains) maligními plazmatickými buňkami, hyperkalcemie, nefrotoxické léky (např. nesteroidní antirevmatika či ATB) aj. [1, 2]. MM ze všech maligních nemocí tvoří 1,2 % a po lymfomu je druhou nejčastější hematologickou malignitou. U 20–40 % pacientů s MM se najde různý stupeň renálního poškození, ale jen 10 % vyžaduje dialyzační léčbu, incidence se pohybuje mezi 3–4/100 000 a u osob nad 70 let se zvyšuje téměř dvojnásobně [3].
Patofyziologicky se na selhání ledvin u MM nejvíce uplatňuje nadprodukce monoklonálních lehkých řetězců FLC (free light chain) kappa (κ) nebo lamda (λ) maligními plazmatickými buňkami, které v ledvinách vytváří histologický obraz LCCN (light chain cast nephropathy). FLC jsou i u zdravých ledvin v glomerulech filtrovány a zpět absorbovány v buňkách proximálního tubulu a do moči se denně vylučuje < 30 mg. Při nadprodukci FLC je reabsorpce nedostatečná a FLC se váží s uromodulinem (Tammův-Horsfallův mukoprotein) v tlustém raménku Henleovy kličky a vytváří matrix válců, které vedou k obstrukci distálního tubulu a tlakem způsobí i přímé poškození tubulárních buněk rupturou jejich membrány s extravazací FLC do intersticia s následnou zánětlivou buněčnou reakcí a s pozdním přechodem do fibrózy [4, 5]. Výsledkem těchto procesů je renální selhání, někdy i nezvratné, vyžadující trvalou náhradu funkce ledvin. Riziko pro LCCN stoupá s koncentrací FLC v krvi a v moči. Diagnózu LCCN lze spolehlivě prokázat renální biopsií (RB), ale ta není vždy proveditelná z důvodu zvýšeného rizika krvácivých komplikací po RB při velmi časté tromocytopenii i koagulopatii, a může být odložena na později. Za dostačující informaci pro diagnózu LCCN se dnes považuje vysoká koncentrace FLC v krvi při současných laboratorních známkách selhání ledvin a při negativní ledvinné anamnéze.
Úkolem nefrologa je omezit riziko trvalého poškození ledvin při LCCN rychlým snížením koncentrace FLC (dříve plazmaferézou, dnes obvykle hemodialýzou s HCO membránou (high cut-off) [6, 7]) a současně účinnou chemoterapií v úzké spolupráci s hematologem potlačit tvorbu FLC [7, 8, 9]. Pacienti s onemocněním MM přichází i k nefrologovi jako renální selhání nejasné příčiny, a proto by v takových případech mělo být vždy provedeno vyšetření FLC, ale v praxi někdy diagnózu odhalí až výsledek renální biopsie. Naopak, pokud přijde pacient nejprve k hematologovi pro podezření na MM a s vysokou koncentrací FLC, je vždy nutné doplnit laboratorní vyšetření pro možné poškození ledvinných funkcí.
Začátkem 21. století se objevují zprávy o dialyzátoru firmy GAMBRO – HCO 1100 – high cut-off s vysoce propustnou membránou s plochou 1,1 m2, která významně odstraňuje FLC ze séra. Později byla plocha dialyzátoru zvýšena na 2,1 m2, dialyzátor dostal název Theralite a efektivita v odstraňování FLC se ještě výrazně zvýšila [10, 11, 12]. Membrána je ze syntetického materiálu a je s „velkými póry“, což umožní vysokou prostupnost pro látky s molekulovou hmotností (m. hm.) 15–45 kDa, jako jsou právě řetězce FLC (κ = 22,5 kDa a λ = 45 kDa). Koeficient prostupnosti (tzv. sieving koeficent) tímto dialyzátorem je pro FLC 1, a proto po dialýze jsou významně snížené hodnoty FLC (až o 60–90 %). Nevýhodou je malá ztráta albuminu (m. hm. 67) během dialýzy, kde koeficient prostupnosti je 0,2. Náhrada „ztrát“ albuminu musí být zajištěna v mimodialyzační době podle aktuálních hodnot v krvi. Výhodou této membrány je neprostupnost pro koagulační faktory, které se naopak významně snižují membránovou plazmaferézou, jež se dříve používala ke snížení hladin FLC. Hemodialýzy (HD) s Theralite označujeme HCO-HD a liší se od standardních časovou náročností pro pacienta, kdy délka jedné HCO-HD je 5–6 hodin – v denním nebo obdenním intervalu. Efektivnost HCO-HD se hodnotí v % odstranění FLC (tj. z hodnot FLC před a po HD) a při každé této HD by mělo být odstraněno alespoň 60 % FLC. Současně musí být podávána účinná chemoterapie (ideálně trojkombinace obsahující vždy bortezomib (proteazomový inhibitor) + cyklofosfamid + kortikoid), kterou řídí hematolog. I podle českých doporučení pro diagnostiku a léčbu mnohočetného myelomu z roku 2018 je v případě akutního renálního selhání zapříčiněného velkým množstvím volných lehkých řetězců indikovaným postupem kombinace protinádorové léčby současně s využitím dialyzační HCO membrány [13].
Cíle naší práce
- Odpovědět na otázku, komu indikovat tento dialyzátor pro jeho finanční náročnost a jak dlouho dialýzu touto membránou provádět (tzn. kolik výkonů bude potřeba k efektivnímu snížení hladiny FLC).
- Odpovědět na otázku, jaký byl osud těchto pacientů v dlouhodobém sledování (2012–2018).
Soubor pacientů
Od 1. 4. 2012 do 31. 12. 2018 jsme dialyzovali s HCO membránou (Theralite) 37 pacientů (M 23 a Ž 14) s diagnózou MM de novo, s mediánem věku = 66 let (rozpětí 37–81 let). U 24 pacientů byly nalezeny řetězce FLC κ a u 13 FLC λ. Šestnáct pacientů bylo přijato s diagnózou MM rovnou na I. interní (hematologickou) kliniku a 21 pacientů bylo přijato pro renální selhání na Kliniku nefrologie ke zjištění příčiny selhání ledvin, anebo již s podezřením na tuto diagnózu. Mezi oběma klinikami je úzká spolupráce již řadu let, a tak stanovení nebo potvrzení diagnózy MM je rychlé. Hemodialýza probíhá vždy na oddělení akutního dialyzačního střediska Kliniky nefrologie a diagnostiku MM i speciální hematologickou léčbu zajištuje hematolog I. interní kliniky co nejdříve, od 1. HCO-HD, pokud nebyla zahájena i dříve. Všichni nemocní měli selhání ledvin různého stupně, vyžadovali dialyzační léčbu různě dlouhou dobu a měli i různý počet HD s HCO membránou. Efektivnost každé HCO-HD se počítá z koncentrace FLC před HD (FLCs) a z hodnoty koncentrace po HD (FLCe) a % odstranění FLC je vypočítáno z těchto hodnot (FLCs – FLCe/ FLCs) × 100. Po skončené dialyzační léčbě s Theralite se celkové % odstranění FLC spočítalo z koncentrace FLCs před 1. HD a FLCe po poslední HCO-HD podle stejného vzorce.
Podle dalšího průběhu jsme soubor pacientů rozdělili do 2 skupin: I. skupinu (n = 24) tvořili pacienti bez potřeby dialyzační léčby v intervalu < 3 měsíců od zahájení léčby HCO-HD (= tzv. úspěšná skupina) a II. skupinu (n = 13) pacienti, kteří pokračovali v dialyzační léčbě nadále standardní HD i po 3 měsících (= skupina neúspěšná). Nicméně obě skupiny zůstaly i nadále v hematologické péči a u některých pacientů byla provedena autologní transplantace periferních kmenových buněk (ASCT) – 13× u 9 pacientů a další jsou v přípravě. K 31. 12. 2018 jsme sledovali osud všech námi léčených pacientů od r. 2012 (7 let) a hodnotili jsme kumulativní přežití křivkou a sledovali jsme mortalitu a rozdíl mezi oběma skupinami.
Výsledky
Celkem jsme provedli u 37 pacientů 296 HCO-HD (8/1 pac.) a během těchto dialýz zemřel 1 pacient (věku 77 let). U 5 pacientů se objevily v průběhu léčby tyto komplikace: 4× infekční a u 1 CMP (drobné krvácení při trombocytopenii), ale interval mezi jednotlivými HCO-HD jsme neměnili. V grafu 1 uvádíme počet pacientů, kteří byli zařazeni v jednotlivých letech (2012–2018). V tabulce 1 uvádíme sledované parametry celého souboru (n = 37) vyjádřené mediánem a rozpětím: FLCs před 1. HCO-HD a FLCe po poslední HCO-HD, celkové % odstranění FLC včetně počtu HCO-HD/1 pacient i počet dní s léčbou na HCO membráně. V tabulce 2 jsou uvedeny parametry podle jednotlivých skupin (úspěšné – skupina I (n = 24) a neúspěšné – skupina II (n = 13)), včetně statistického porovnání. Dialyzační léčbu do 3 měsíců nevyžadovalo 24 pacientů (65 %) a 13 pacientů (35 %) pokračovalo v další standardní dialyzační léčbě (bez HCO membrány). Z 37 pacientů během sledovaného období zemřelo celkem 14 (38 %), ale s významným rozdílem mezi oběma skupinami (graf 2). V I. skupině (n = 24), tj. úspěšné (nepokračovali po 3 měsících v další dialyzační léčbě), zemřelo 5 pacientů – mortalita byla 21 %, zatímco ve II. skupině (n = 13), tj. neúspěšné (pacienti pokračovali ve standardní HD), jich zemřelo 9 a mortalita byla 69 %. Pro zajímavost uvádíme ještě graf 3 – křivku kumulativního přežívání našich pacientů v letech 2012–2018.
Graph 1. Počet pacientů zařazených v jednotlivých letech k HCO léčbě 
Graph 2. Počet pacientů ve skupině I a II a počet zemřelých v těchto skupinách 
Graph 3. Kumulativní křivka přežívání pacientů s MM na HCO 2012–2018 v našem souboru 
Table 1. Sledované parametry celého souboru pacientů (n = 37) vyjádřené mediánem a rozpětím 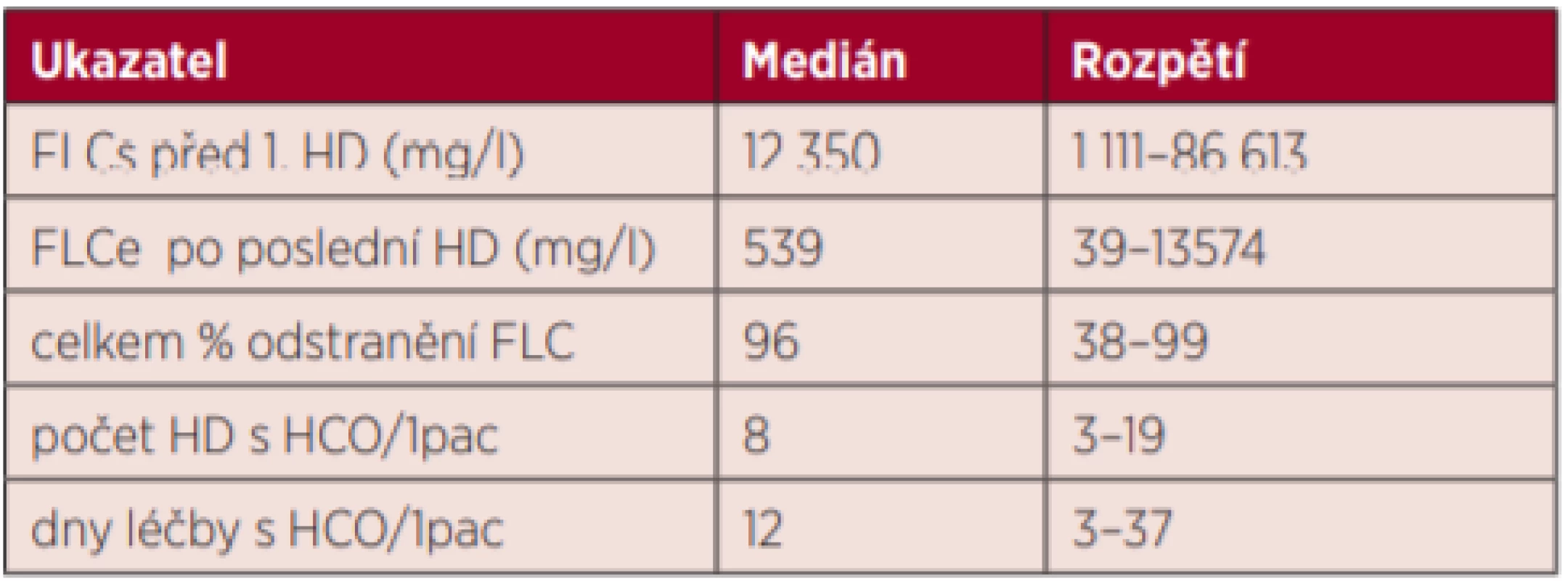
FLC – volné lehké řetězce, FLCs – koncentrace FLC před HD, FLCe – koncentrace po HD, HD – hemodialýza, HCO-HD – high cut-off HD Table 2. Porovnání obou skupin pacientů (I a II) ve sledovaných ukazatelích 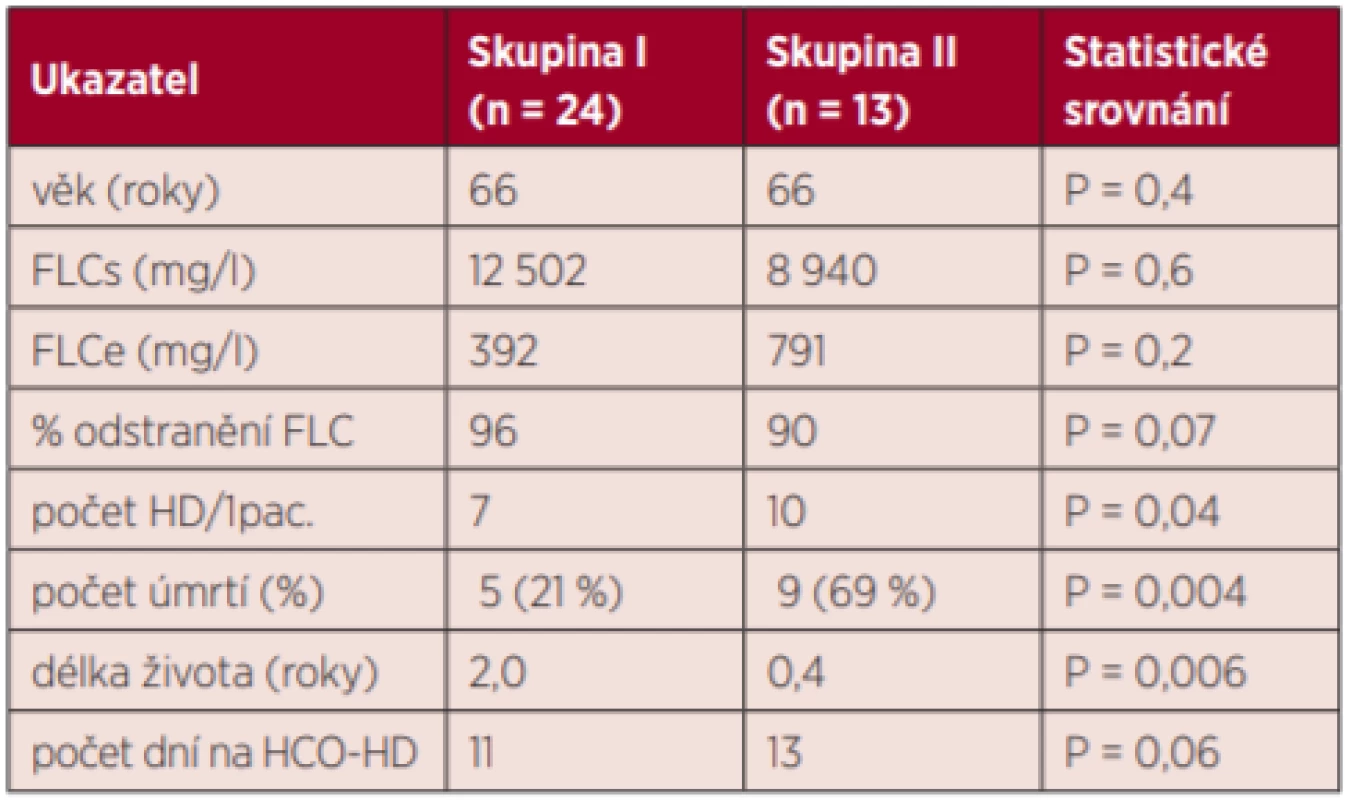
FLCs – koncentrace FLC před HD, FLCe – koncentrace po HD, FLC – volné lehké řetězce, HD – hemodialýza, HCO-HD – high cut-off HD Pro důležitost v rozhodování délky léčby s HCO-HD uvádíme 2 stručné kazuistiky: první kazuistiku úspěšného pacienta a druhou kazuistiku neúspěšně léčeného. Z naší zkušenosti je nezbytné sledování koncentrací FLC (před i po HCO-HD) nejen číselně v tabulce, ale i grafem. U úspěšného pacienta (tab. 3, graf 4) klesá FLC trvale a před každou HD je hodnota vždy nižší než u předcházející HD. U neúspěšného pacienta mají hodnoty před HD vždy vysokou variabilitu (tab. 4) a v grafickém vyjádření není vyznačen sestupující trend (graf 5).
Graph 4. Vývoj koncentrace volných lehkých řetězců - Kazuistika 1 
Graph 5. Vývoj koncentrace volných lehkých řetězců – Kazuistika 2 
Table 3. Vývoj koncentrace volných lehkých řetězců – Kazuistika 1 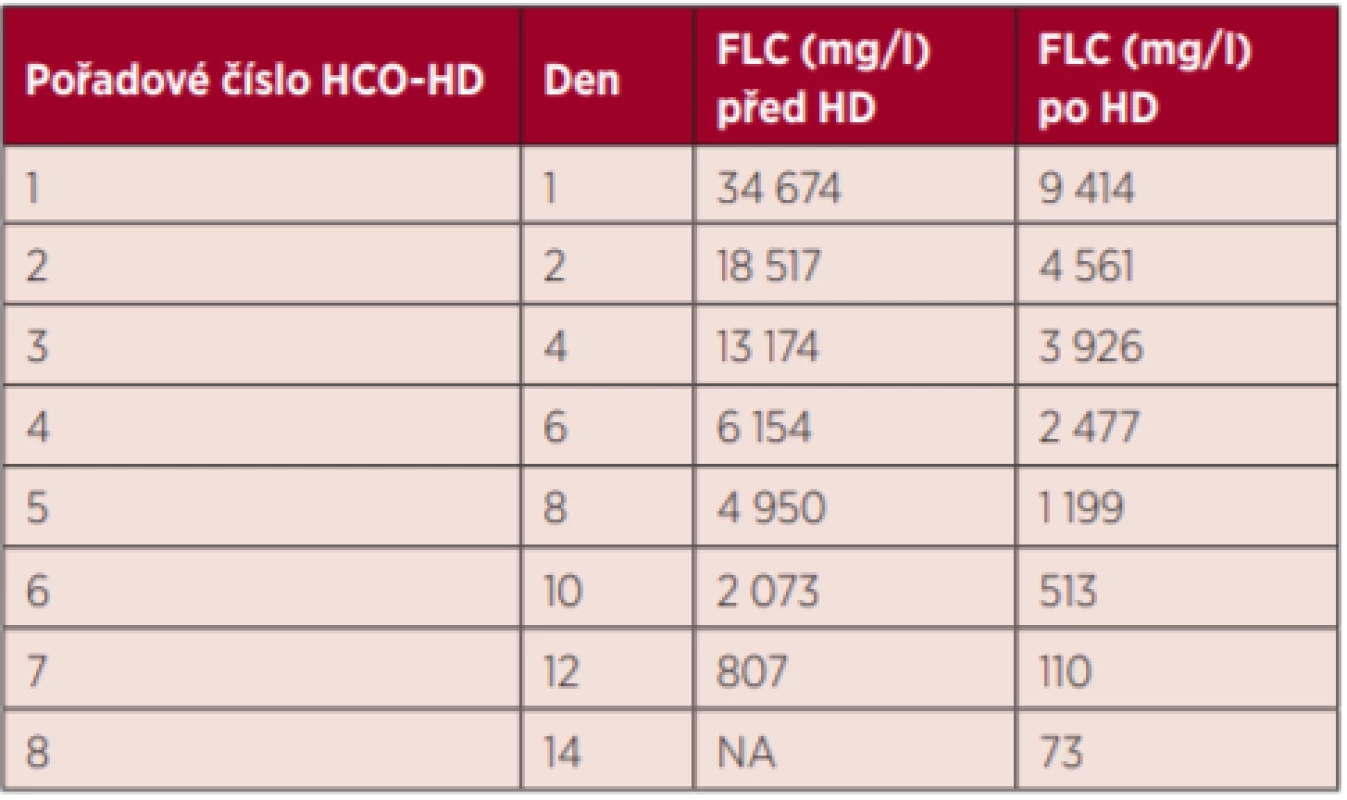
FLC – volné lehké řetězce, HD – hemodialýza, HCO-HD – high cut-off HD Table 4. Vývoj koncentrace volných lehkých řetězců – Kazuistika 2 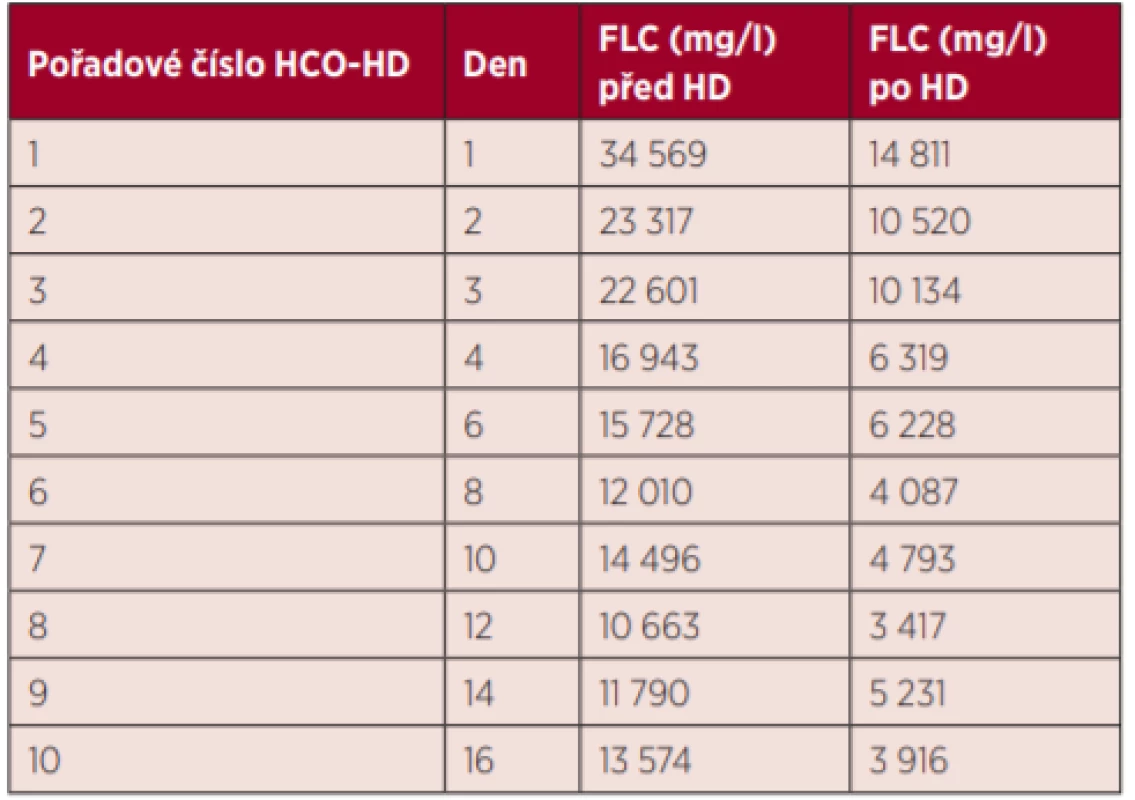
FLC –volné lehké řetězce, HD – hemodialýza, HCO-HD – high cut-off HD KAZUISTIKA 1 – ÚSPĚŠNÉHO pacienta (tab. 3, graf 4)
67letý muž měl 3 měsíce bolesti páteře v oblasti LS při pohybu, později i v klidu. Chodil na rehabilitaci a užíval ibuprofen, žádný efekt se nedostavil, a proto byl odeslán na interní oddělení nemocnice k celkovému vyšetření. Výsledky laboratorních hodnot svědčily pro selhání ledvin a pacient byl přeložen na naši kliniku k urgentní hemodialýze a ke zjištění příčiny selhání. Před 1. (standardní) HD byly tyto hodnoty: K 5,7 mmol/l, kreatinin 1834 µmol/l, urea 54,4 mmol/l, KO: leu 8,1 × 109/l, HB 92 g/l, ery 2,69 × 1012/l, trombo 205 × 109/l a byla přítomna oligoanurie. Sonografické vyšetření ledvin vyloučilo obstrukci močových cest. Byly provedeny 2 standardní HD. Hodnoty FLC byly známy před 3. HD a pro extrémně vysoké hodnoty (tab. 3) byla zahájena HCO-HD, celkem jich bylo provedeno 8 a odstraněno bylo 99 % FLC. Následovalo ještě několik standardních HD v nepravidelném režimu a HD byly ukončeny do 3 měsíců od zahájení. Pacient žije již 3,9 roku bez HD a hodnoty renálních funkcí jsou dlouhodobě stabilizované.
KAZUISTIKA 2 – NEÚSPĚŠNÉHO pacienta (tab. 4, graf 5)
75letá žena byla přijata k nám pro renální selhání nejasné etiologie z jiného pracoviště, kde byla již 4× dialyzována. Dominující a jedinou stížností byly bolesti zad i žeber trvající 2 měsíce. Na RTG byla zjištěna fraktura žeber, trauma pacientka popírala. Při přijetí k nám již s těmito nálezy jsme vyšetřili v krvi FLC a zahájili HCO-HD a chemoterapii. Celkem jsme provedli 10 HCO-HD a odstranili 65 % FLC. Vzhledem ke stále vysokým hodnotám FLC před HD jsme pacientku převedli na standardní HD, nadále byla léčena chemoterapií v dialyzačním programu a po 128 dnech od 1. HD zemřela.
Diskuse
Prognóza nemocných s MM je výrazně horší, pokud dojde i k selhání ledvin s LCCN a pokud pacienti pokračují v chronické dialyzační léčbě, tak riziko úmrtí je 2,77× vyšší oproti pacientům jen s nefrologickou diagnózou [14]. Řecká studie z roku 2017 [15] ukázala i nevýhodu věku – pacienti do 65 roků mají lepší prognózu pro obnovu renální funkce ve srovnání s pacienty staršími (75 % : 38 %). Autoři ještě nalezli závislost na vstupní hodnotě FLC nad 9 000 mg/l, kdy obnova renální funkce trvá delší dobu. V naší práci jsme tento vztah nenašli, a naopak ve skupině I. (úspěšné) byla vstupní hladina FLC spíše vyšší než ve skupině II, i když bez statistické významnosti. Tento rozdíl proti výše uvedené studii si vysvětlujeme malým počtem pacientů s velkou variabilitou hodnot FLC.
První zprávy o účinném odstraňování FLC membránou HCO o více jak 60 % během dialýzy jsou známé od r. 2006 [12] a i my jsme to potvrdili v naší práci. V posledních deseti letech se objevovaly studie, většinou ale retrospektivní či s malým počtem pacientů, kdy kombinovaná léčba MM bortezomibem a HCO-HD zlepšila prognózu pacientů – 60 % pacientů se do 3 měsíců stane nezávislých na dialýze [9, 11, 16].
Dlouho se pak čekalo na výsledky dvou velkých randomizovaných studií EuLITE (anglické) [17, 18] s 90 pacienty a MYRE (francouzské) s 98 pacienty [19]. Cílem studií byla nezávislost na HD (reparace renální funkce) v časovém rozmezí do 3 měsíců (primární cíl) a v dlouhodobém sledování (resp. po 6 měsících – druhotný cíl) při terapii standardní HF-HD porovnávané s HCO-HD (tab. 5). Do 3 měsíců nebyl žádný rozdíl mezi použitými dialyzačními metodami (p = NS) i oběma studiemi, obě studie tedy nesplnily primární cíl. V dalším sledování byly dosaženy výsledky trochu odlišné, i když je přímé porovnání obtížné pro metodické i jiné rozdíly mezi studiemi: renální funkci v dlouhodobém sledování v EuLITE obnovilo 66 % pacientů s HF-HD vs. 58 % pacientů s HCO-HD (p = NS) a v MYRE po 6 měsících jen 35 % léčených HF-HD a 57 % léčených HCO-HD (p = 0,04), nicméně lepší renální přežívání v 6. měsíci nemělo vliv na celkové přežívání po 12 měsících [20]. Ve studii EuLITE byla navíc zjištěna vyšší celková mortalita a vyšší incidence nežádoucích příhod (zejména infekcí) ve skupině s HCO-HD a ve skupině s HCO-HD byla také popsána menší účinnost hematologické léčby [20]. Závěry studií (původně publikovaných v abstraktech a později i in extenso) byly opakovaně diskutovány s vcelku rozdílnými stanovisky [20–23]. Zatímco někteří metodu spíše odsoudili [21] a sami autoři studie EuLITE [18] v závěru uvádí, že výsledky nepodporují provedení studie fáze 3, objevují se i méně striktní stanoviska [20, 22] zdůrazňující nutnost dalších dat. V časopise Journal of Onco-Nephrology z r. 2017 [23] se autoři K. Finkel a P. Fabbrini vyjádřili k oběma studiím sami sobě položenou otázkou HCO-HD for myeloma cast nephropathy: Do we finally have answer? A odpověď: S HCO-HD je návrat renální funkce signifikantně vyšší než v minulosti, ale rutinní použití bez dalších dat nemůže být doporučeno.
Table 5. Studie MYRE a EuLITE v přehledu údajů (upraveno podle [22]) ![Studie MYRE a EuLITE v přehledu údajů (upraveno podle [22])](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/874843a0fbd10622fe93848f5e3748e1.png)
MM – mnohočetný myelom, sFLC – sérové volné lehké řetězce, HD – hemodialýza, HF-HD – high-flux HD, HCO-HD – high cut-off HD Dimopoulos et al. v článku z r. 2017 [15] hodnotí kombinovanou léčbu hematologickou s HCO-HD velmi pozitivně nejen ve zlepšené renální funkci, ale i v délce přežívání pacientů (medián = 29 měsíců) a s největší úmrtností v 1. roce léčby. Srovnání s naším souborem bylo následující: Úspěšní pacienti přežívali (medián) 24 měsíců (rozpětí 5–79), proti skupině neúspěšné, kteří přežívali o mnoho kratší dobu – v mediánu méně než 5 měsíců (1–24). A také v mortalitě je velký rozdíl – 21 % ve skupině úspěšné, proti 69 % ve skupině neúspěšné. Rovněž práce A. Curti et al. [24] z roku 2016 srovnává pacienty léčené HCO-HD se standardní HD se závěrem jasného benefitu při použití HCO membrány – urychluje návrat renální funkce, snižuje mortalitu a prodlužuje délku života nemocných. Navíc se zmiňuje o finanční náročnosti obou metod HCO-HD : HD standard je cena 230 000 : 223 000 ve švýcarských francích (CHF). Nevýhodou této práce je malý počet pacientů a autoři pro definitivní závěr (tzv. doporučení) navrhují prospektivní kontrolovanou studii.
Z našich zkušeností sedmiletého používání HCO-HD u nově diagnostikovaného MM je tato metoda pro pacienty přínosem z těchto důvodů: rychlé snížení koncentrace FLC snižuje riziko poškození ledvin a reparace renálních funkcí je rychlejší při současně podané efektivní chemoterapii hematologem tak, jak uvádí i Gerth [25]. Domníváme se ale, že z dlouhodobého hlediska je pro pacienta zásadní časné stanovení diagnózy a zahájení léčby. Také úspěch hematologické léčby a pokles produkce FLC je pro pacienta podstatný a bez úspěchu hematologické léčby není celková (ani nefrologická) prognóza dobrá. Pro pacienta s reparovanou funkcí je velkým zlepšením kvalita jeho života, tj. bez dialyzační léčby 3× týdně, a značné ušetření finančních prostředků (náklady na 1 rok 1 dialyzovaného nemocného činí cca 1 000 000 Kč). HCO-HD se liší od standardní HD jen cenou dialyzátoru (18 352 : 500 Kč) a my musíme rozhodnout, jak dlouho se bude dialyzátor s HCO membránou používat. K tomu nám pomáhá sestupující trend křivky FLC, jak jsme ukázali v kazuistice úspěšně léčeného pacienta.
Závěr
Prognóza pacientů s MM a renálním selháním se v posledních letech zlepšila díky účinnější chemoterapii a zřejmě i efektivnímu odstranění FLC HCO membránou, i když randomizované studie jednoznačně nepotvrdily benefit této metody proti standardní HD s high-flux membránou. Z naší zkušenosti průměrně u 60 % pacientů léčených HCO-HD dojde k reparaci renální funkce a nepotřebují další drahou dialyzační léčbu. Pacientům se odpojením od HD zkvalitní život i jeho délka. Zatím není určeno dopředu, pro koho HCO-HD bude ziskem, ale napoví tomu již několik prvních HCO-HD s klesajícím trendem predialyzačních hodnot FLC.
Čestné prohlášení
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou společností.
Podíl autorů na přípravě rukopisu
JL – námět studie, nefrologická diagnostika a léčba nemocných, sběr dat, příprava rukopisu, kontrola a revize manuskriptu
ZH – kontrola a revize manuskriptu
RR – nefrologická diagnostika a léčba nemocných, kontrola a revize manuskriptu
MM – podíl na sběru dat a přípravě manuskriptu, kontrola a revize manuskriptu
JS – hematologická diagnostika a léčba nemocných, kontrola a revize manuskriptu
VT – garant práce, kontrola a revize manuskriptu
Poděkování
Práce byla podpořena projektem PROGRES Q25/LF1 a RVO-VFN 64165.
Doručeno do redakce dne 1. 11. 2019.
Přijato po recenzi dne 17. 12. 2019.
MUDr. Jana Lachmanová
Klinika nefrologie VFN v Praze a 1. LF UK
U Nemocnice 2
128 08 Praha 2
e-mail: jana.lachmanova@vfn.cz
Sources
- Heher EC, Rennke HG, Laubach JP, et al. Kidney disease and multiple myeloma. Clin J Am Soc Nephrol. 2013;8 : 2007–2017.
- Ryšavá R. Postižení ledvin u mnohočetného myelomu a novinky v léčbě. Postgrad Med. 2015;17 : 489–498.
- Tsakiris DJ, Stel VS, Finne P, et al. Incidence and outcome of patients starting renal replacement therapy for end - stage renal disease due to multiple myeloma or light-chain deposition disease an ERA-EDTA Registry study. Nephrol Dial Transplant. 2010;25 : 1200–1206.
- Lachmanová J, Tesař V, Ryšavá R. Theralite a mnohočetný mye-lom. Vnitř Lék. 2016;62(suppl 6):9–13.
- Herrera GA, Sanders PW. Paraproteinemic renal diseases that involve the tubuloinbterstitium. Contrib Nephrol. 2007;153 : 105–115.
- Cockwell P, Hutchinson C. Management options for cast nephropathy in multiple myeloma. Cur Opinn Nephrol Hypertens. 2010;19 : 550–555.
- Hutchinson C, Bradwell A, Cook M, et al. Treatment of acute renal failure secondary in multiple myeloma with chemotherapy and extended High Cut Off Hemodialysis. Clin J Am Soc Nephrology. 2009;4 : 419–426.
- Ludwig H, Drach J, Graf H, et al. Reversal of acute renal failure by bortezomib -based chemotherapy in patients with multiple myeloma. Haemotalogica. 2007;92 : 1411–1414.
- Zanneti BA, Zamagni E, Santostefano M, et al. Bortezomib-based therapy combined with high cut off hemodialysis is highly effective in new diagnosed multiple myeloma patients with severe renal impairment. Am J Hematol. 2015;90 : 647–652.
- Hutchinson C, Cockwell P, Basnayake K, et al. Removal of free light chains by extended hemodialysis in patients with cast nephropathy: A phase ½ clinical trial. Nephrol Dial Trial. 2007;22(Suppl 6):vi58.
- Hutchinson C, Cockwell P, Stringer S, et al. Early reduction of serum-free light chains associates with renal recovery in myeloma kidney. J Am Soc Nephrol. 2011;22 : 1129–1136.
- Bradwell, AR. Serum free light chain analysis. 4th ed. Rhondda, Wales UK: HSWprint, 2006.
- Kolektiv autorů: Diagnostika a léčba mnohočetného myelomu 2018. Transfuze Hematol Dnes. 2018;24(Suppl.1):7–23.
- Wirk B. Renal failure in multiple myeloma: a medical emergency. Bone Marrow Transplant. 2011 : 46 : 771–783.
- Dimopoulos MA, Roussou M, Gavriatopoulos M, et al. Outcomes of newly diagnosed myeloma patients requiring dialysis: renal recovery, importance of rapid response and survival benefit. Blood Cancer J. 2017;7:e571.
- Chanan-Khan AA, Kaufman JL, Mehta J, et al. Activity and safety of bortezomib in multiple myeloma with advanced renal failure. Blood. 2007;109 : 2604–2606.
- Hutchinson CA, Cook M, Heyne N, et al. European trial of free light chain by extended haemodyalysis in část nephropathy (EuLITE) a randomised control trial. Trials. 2008 : 9:55.
- Hutchison CA, Cockwell P, Moroz V, et al. High cut-off versus high-flux haemodialysis for myeloma cast nephropathy in patients receiving bortezomib-based chemotherapy (EuLITE): a phase 2 randomised controlled trial. Lancet Haematol. 2019;6:e217–e228.
- Bridoux F, Carron PL, Pegourie B, et al. Effect of high cut-off hemodialysis vs conventional hemodialysis on hemodialysis independence among patients with myeloma cast nephropathy: a randomized clinical trial. JAMA. 2017;318 : 2099–2110.
- Ryšavá R. Je léčbě dialýzou s HCO membránou u nemocných s myelomovou ledvinou odzvoněno? Postgrad Nefrol. 2019;17 : 14–16.
- Sallée M, Burtey S. Myeloma cast nephropathy: the dusk of high cut-off haemodialysis. Lancet Haematol. 2019;6:e174–e176.
- Bridoux F, Chevret S, Fermand JP. High cut-off haemodialysis in myeloma cast nephropathy: further investigation is needed. Lancet Haematol. 2019;6:e347.
- Finkel K, Fabbrini P. High cut-off hemodialysis for myeloma cast nephropathy – do we finally have answer? J Onco-Nephrol. 2017;1 : 67–70.
- Curti A, Schwarz A, Trachsler J, Tomonaga Y, Ambühl PM. Therapeutic efficacy and cost effectiveness of high cut-off dialyzers compared to conventional dialysis in patients with cast nephropathy. PLoS ONE. 2016;11:e0159942.
- Gerth HU, Pohlen M, Görlich D, et al. Impact of high-cut-off dialysis on renal recovery in dialysis-dependent multiple myeloma patients: results from a case-control study. PLoS ONE. 2016;11:e0154993.
Labels
Haematology Internal medicine Clinical oncology
Article was published inTransfusion and Haematology Today

2020 Issue 2-
All articles in this issue
- Editorial
- Trombotické mikroangiopatie
- Castlemanova nemoc, jedna z příčin chronické systémové zánětlivé reakce, někdy i retence tekutin, vaskulitid a poruch imunity – Mezinárodní diagnostická kritéria z roku 2017
- Léčba histiocytózy z Langerhansových buněk u dospělých osob
- Závěr života nemocných s nehodgkinským lymfomem, analýza souboru zemřelých během šesti let (2012–2017) na jednom pracovišti, integrace paliativní péče
- Skladování erytrocytů při nestandardní teplotě
- Theralite a mnohočetný myelom – známe už odpověď na efektivitu léčby nefrologa s hematologem?
- Překvapivý nález v kostní dřeni: co za ním je?
- Životní jubileum pana profesora Jiřího Mayera
- Transfusion and Haematology Today
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Castlemanova nemoc, jedna z příčin chronické systémové zánětlivé reakce, někdy i retence tekutin, vaskulitid a poruch imunity – Mezinárodní diagnostická kritéria z roku 2017
- Trombotické mikroangiopatie
- Překvapivý nález v kostní dřeni: co za ním je?
- Léčba histiocytózy z Langerhansových buněk u dospělých osob
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

