-
Medical journals
- Career
Prognostické faktory u chronické myeloidní leukemie: můžeme kombinací získat více?
: Z. Čermáková 1; J. Fürstová 2; T. Fürst 3; I. Marešová 4; I. Skoumalová 4; P. Rohoň 4; K. Indrák 4; T. Papajík 4; E. Faber 4
: Onkologická klinika FN Ostrava 1; 1. LF UK Praha 2; PřF UP v Olomouci 3; Hemato-onkologická klinika FN a LF UP v Olomouci 4
: Transfuze Hematol. dnes,22, 2016, No. 1, p. 6-13.
: Comprehensive Reports, Original Papers, Case Reports
Pro určení prognózy pacientů s chronickou myeloidní leukemií (CML) léčených inhibitory tyrozinové kinázy (TKI) je v současnosti používáno několik skórovacích systémů (index EUTOS, Sokalovo a Hasfordovo skóre). Individuální pacient může být zařazen podle jednotlivých skóre do skupin s různou prognózou. Nelze vyloučit, že kombinací skórovacích systémů by nebylo možné zlepšit odhad prognózy pacientů. Pro ověření prediktivní hodnoty nově vytvořeného skóre byl použit soubor 193 pacientů s CML léčených na Hemato-onkologické klinice v Olomouci v letech 1989–2013. Sběr a kontrola dat byly provedeny retrospektivně. K vyhodnocení přežití byla použita metoda podle Kaplana a Meiera v kombinaci s log-rank testem. Šlo o 77 žen (39,9 %) a 116 mužů (60,1 %) ve věku 17–88 let (medián 54) let. Pacienti byli sledováni po dobu v mediánu 89,1 (3,6–296,6) měsíců. 72 pacientů (37,3 %) bylo předléčeno interferonem alfa po dobu v mediánu 9,33 měsíců. Statistická analýza potvrdila dobrou prediktivní hodnotu indexů podle Sokala a Hasforda pro odhad celkového přežití a přežití bez progrese. Pomocí indexu EUTOS nebylo možno statisticky významně odlišit pacienty s dobrou a špatnou prognózou pro celkové přežití, pro přežití bez progrese mělo toto skóre nejhorší prediktivní hodnotu. K výpočtu nového skóre jsme riziko podle Sokalova a Hasfordova skóre převedli na body (nízké = 1, střední = 2, vysoké = 3). Součet bodů měl u jednotlivých pacientů hodnotu 2–6. Nové skóre vytvořené na tomto součtu umožnilo zlepšit jak odhad prognózy celkového přežití, tak i přežití bez progrese pacientů. Naše nové skóre mělo ve srovnání s ostatními zmíněnými skórovacími systémy lepší schopnost odhadu prognózy také u skupiny pacientů, kteří nebyli předléčeni interferonem. Přidání skóre EUTOS do kombinace už dále významně nezvýšilo predikci. Naše analýzy ukazují, že jednoduchou kombinací existujících prognostických indexů lze u pacientů s CML zlepšit odhad prognózy. Výsledky je nezbytné potvrdit na větších souborech pacientů.
Klíčová slova:
chronická myeloidní leukemie – Hasfordův index – Sokalův index – EUTOS skóre – prognóza – inhibitory tyrozinové kinázyÚVOD
Chronická myeloidní leukemie (CML) je chronické myeloproliferativní onemocnění, jehož incidence je dlouhodobě stabilizovaná. Jeho prevalence však významně narůstá díky cílené léčbě, umožněné zásadními poznatky patogeneze onemocnění. CML je prvním lidským nádorovým onemocněním, u něhož byla popsána souvislost se specifickou chromozomovou změnou [1]. Hlavním znakem leukemických buněk je chromozom Philadephia (Ph1), který vzniká reciprokou translokací mezi chromozomy 9 a 22 [2]. Diagnóza bývá potvrzena po vyslovení podezření na základě výsledků vyšetření krevního obrazu cytogenetickým nebo molekulárním vyšetřením na přítomnost Ph chromozomu nebo BCR-ABL1 genu, který hraje v patogenezi CML klíčovou roli. Produktem BCR-ABL1 je tyrozinová kináza, nejčastěji protein p210, jehož konstitutivní aktivita zapříčiňuje fenotypové vlastnosti leukemické buňky. K cílené léčbě CML se dnes používají inhibitory této tyrozinové kinázy (TKI; v České republice zejména: imatinib, dasatinib, nilotinib), s jejichž zavedením do léčby CML byl pozorován až 75% pokles mortality [3].
Přes velký úspěch léčby TKI, která u nemocných optimálně odpovídajících na léčbu pravděpodobně vyrovná jejich šance na přežití s ostatní populací, stále existují nemocní, u nichž je pozorována primární nebo sekundární rezistence k TKI nebo pacienti, u nichž dojde k náhlé akceleraci nebo blastickému zvratu CML. Vzhledem k chybějícím dostatečně validním biologickým nebo molekulárním markerům, výpočet prognostického skóre z výsledků získaných před zahájením léčby zůstává kromě přítomnosti přídatných cytogenetických změn jedinou možností, jak před zahájením léčby TKI odhadnout prognózu pacienta. Dalším velmi důležitým faktorem je odpověď na léčbu monitorovaná podle aktuálních doporučení v předem stanovených intervalech [4]. Pro odhad odpovědi na cílenou léčbu a celkový odhad prognózy jsou u CML pacientů stále s větším či menším úspěchem používány skórovací systémy, které byly původně určeny k odhadu prognózy nemocných léčených perorální chemoterapií nebo interferonem alfa (Sokalovo a Hasfordovo skóre) a nový index EUTOS [5–7]. Výpovědní hodnota těchto systémů je odlišná v různých souborech nemocných, přičemž u skóre EUTOS nebyla v některých případech adekvátní [8, 9]. Podle aktuálních doporučení pro léčbu CML jsou pro odhad prognózy doporučena všechna 3 popisovaná skóre [4]. Cílem naší práce bylo pokusit se zlepšit odhad prognózy pomocí kombinace těchto nejčastěji užívaných systémů.
METODY
Do studie jsme zařadili pacienty s CML léčené konzervativně pomocí TKI, bez ohledu na to, zda byli před nasazením TKI léčeni interferonem alfa. Nebyli zařazeni nemocní, u kterých byla z různých důvodů a v rozličné linii léčby provedena alogenní transplantace krvetvorných buněk. Obdobně nebyli zařazeni aktuálně neléčení pacienti v dlouhodobé molekulární odpovědi po interferonu alfa a pacienti, u nichž nebyly známy hodnoty prognostických indexů. Prognostické indexy byly vypočteny podle vzorců uváděných v příslušných literárních zdrojích [5–7].
Sběr a kontrola dat s aktualizací podle posledních vyšetření byly provedeny retrospektivně. Délka celkového přežití byla hodnocena od stanovení diagnózy po poslední kontrolu, respektive po úmrtí pacienta. Přežití bez progrese (PFS) bylo hodnoceno od data stanovení diagnózy po progresi CML (akceleraci, blastický zvrat, hematologickou progresi, cytogenetickou progresi, nebo úmrtí pacienta na CML) nebo k datu poslední kontroly, podle toho, ke které události došlo dříve. Statistická významnost rozdílů v délce přežití mezi různě rizikovými skupinami byla hodnocena log-rank testem. Kombinace tří skóre byla řešena následovně: hodnoty skóre rizikových skupin byly převedeny na body, kdy u Sokalova a Hasfordova skóre znamenalo nízké riziko jeden, střední 2 a vysoké 3 body. U indexu EUTOS byl za nízké riziko přidělen pacientovi jeden a za vysoké 2 body. Body všech skórovacích systému se sčítaly, součet se tedy u jednotlivých pacientů pohyboval mezi hodnotou 3–8. Nízké riziko bylo podle nové stupnice rovno 3 a 4, střední 5 a 6 a vysoké 7 a 8. Dále byly zkoušeny varianty analýz s použitím pouze dvou skóre (Sokal a Hasford), kdy se hodnoty výsledného skóre mohly pohybovat mezi 2–6 body a také byly ověřovány možnosti rozdělení pacientů pouze do dvou prognostických skupin (vysoké a nízké riziko), jakož i možnost přidělení 3 bodů v případě kategorie vysokého rizika v EUTOS skóre.
Prediktivní síla jednotlivých indexů byla měřena takzvanou konkordancí [10]. Konkordance měří pravděpodobnost souladu časů přežití náhodně vybrané dvojice pacientů s hodnotami jejich skóre. Za soulad se považovalo, pokud pacient s kratší dobou přežití (nebo PFS) měl zároveň vyšší hodnotu skóre. Konkordance bylo vždy číslo mezi 0,5 (pokud skóre nemělo žádnou prediktivní hodnotu pro přežití) a 1,0 (pokud byla skóre všech dvojic pacientů v souladu s jejich přežitím). Konkordance je v textu značena písmenem c.
VÝSLEDKY
V dostupných archivech na Hemato-onkologické klinice FN a LF UP v Olomouci bylo nalezeno 193 nemocných s CML, léčených konsekutivně bez použití alogenní transplantace krvetvorných buněk. Šlo o 77 žen a 116 mužů ve věku od 17 do 88 let s věkovým mediánem 54 let. Sledování a léčba pacientů probíhala v letech 1989–2013. Pacienti byli sledováni po dobu v mediánu 89,1 měsíců (3,6–296,6). Celkem 72 pacientů (37,3 %) bylo předléčeno interferonem alfa po dobu v mediánu 9,33 měsíců. 116 pacientů (60,1 %) bylo léčeno v první linii léčby imatinibem a 5 pacientů (2,6 %) nilotinibem. V 2. linii bylo léčeno 37 pacientů (19,2 %) nilotinibem či dasatinibem. Z těchto bylo dále léčeno 12 pacientů (6,2 %) v 3. linii dalším TKI. Míra rizika podle indexu EUTOS byla u 158 pacientů (81,9 %) vypočítána jako nízká (hodnota indexu ≤ 87), u 35 pacientů (18,1 %) jako vysoká (> 87). Podle Hasfordova skóre bylo u 63 pacientů (32,7 %) konstatované nízké riziko (hodnota skóre < 780), u 95 (49,2 %) střední (780–1480) a u 35 (18,1 %) vysoké (> 1480). Podle Sokalova vzorce byla míra rizika u 64 pacientů (33,1 %) nízká (< 0,8), u 75 (38,9 %) středně vysoká (0,8–1,2) a u 54 (28 %) vysoká (> 1,2). Z celkového počtu pacientů jich 41 (21,2 %) zemřelo. CML byla příčinou exitu u 19 (9,9 %) pacientů. K progresi podle naší definice PFS došlo u 63 (32,6 %) pacientů. Statistickou analýzou byla potvrzena dobrá prediktivní hodnota indexů podle Sokala a Hasforda pro odhad OS (cSOK = 0,637; cHAS = 0,633; rozdíl mezi nízko a středně rizikovou skupinou byl statisticky významný pro oba indexy HRSOK21 = 2,37, HRHAS21 = 2,56, (HR – hazard ratio; poměr rizik) rozdíl mezi vysoko a nízko rizikovou skupinou taktéž HRSOK31 = 3,51, HRHAS31 = 4,58) (obr. 1 a 2) i PFS (cSOK = 0,658, cHAS = 0,622; rozdíl mezi nízko a středně rizikovou skupinou byl statisticky významný pouze pro Hasfordův index HRHAS21 = 2,40, rozdíl mezi vysoko a nízko rizikovou skupinou je významný pro oba indexy HRSOK31 = 3,80, HRHAS31 = 3,10). Pomocí indexu EUTOS nebylo možno statisticky významně oddělit pacienty s dobrou a špatnou prognózou OS (log rank test; p = 0,27) (obr. 3), pro PFS mělo toto skóre nejhorší prediktivní sílu (cEUT = 0,556). Kombinací Sokalova a Hasfordova indexu po převedení rizika jednotlivých indexů na body a jejich součtem se podařilo významně zlepšit odhad prognózy OS (cHAS+SOK = 0,674) (obr. 4) i PFS (cHAS+SOK = 0,664) (obr. 5). Přidání skóre EUTOS do kombinace (se 2 nebo 3 body pro vysoké riziko) nezlepšilo predikci. Naše nové skóre mělo ve srovnání s ostatními zmíněnými skórovacími systémy lepší schopnost odhadu prognózy také pro OS a PFS u skupiny pacientů, kteří nebyli předléčeni interferonem (výsledky neprezentujeme).
1. Celkové přežití pacientů s CML podle Sokalova skóre 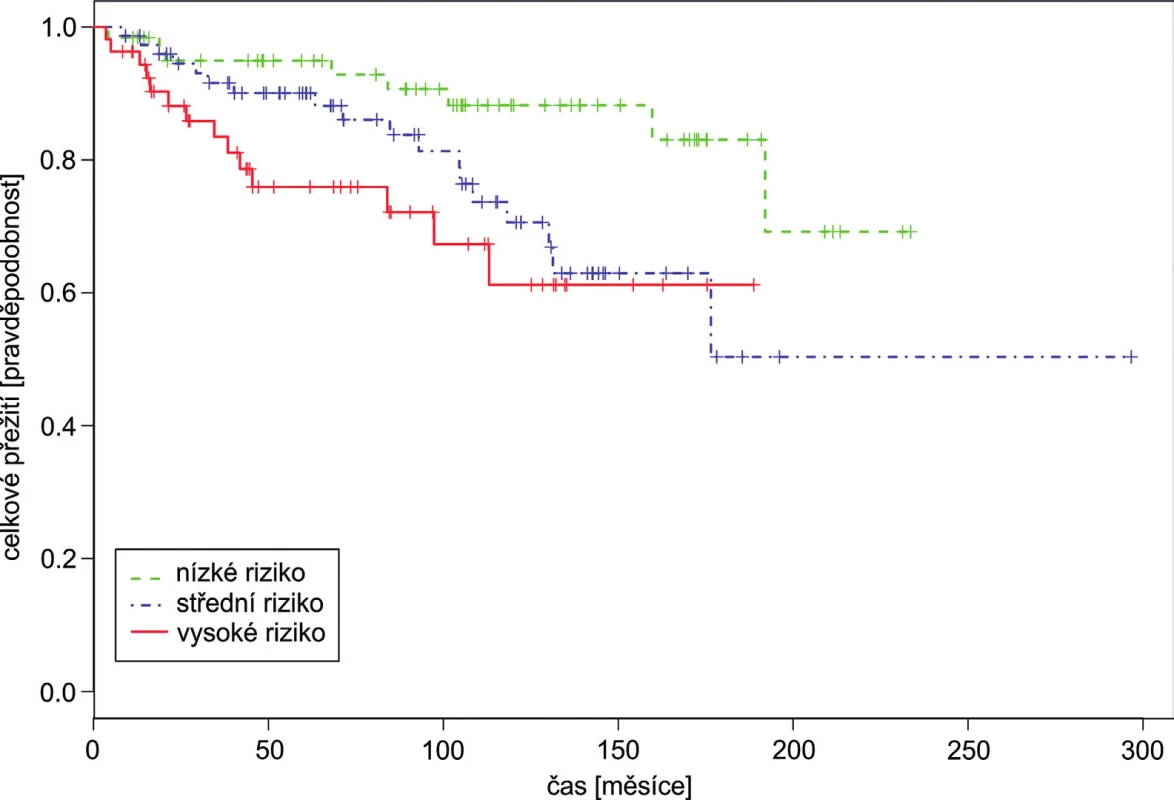
Konkordance cSOK = 0,637; rozdíl mezi středně a nízko rizikovou skupinou byl statisticky významný HRSOK21 = 2,37, p = 0,044, rozdíl mezi vysoko a nízko rizikovou skupinou taktéž HRSOK31 = 3,51, p = 0,006. 2. Celkové přežití pacientů s CML podle Hasfordova skóre 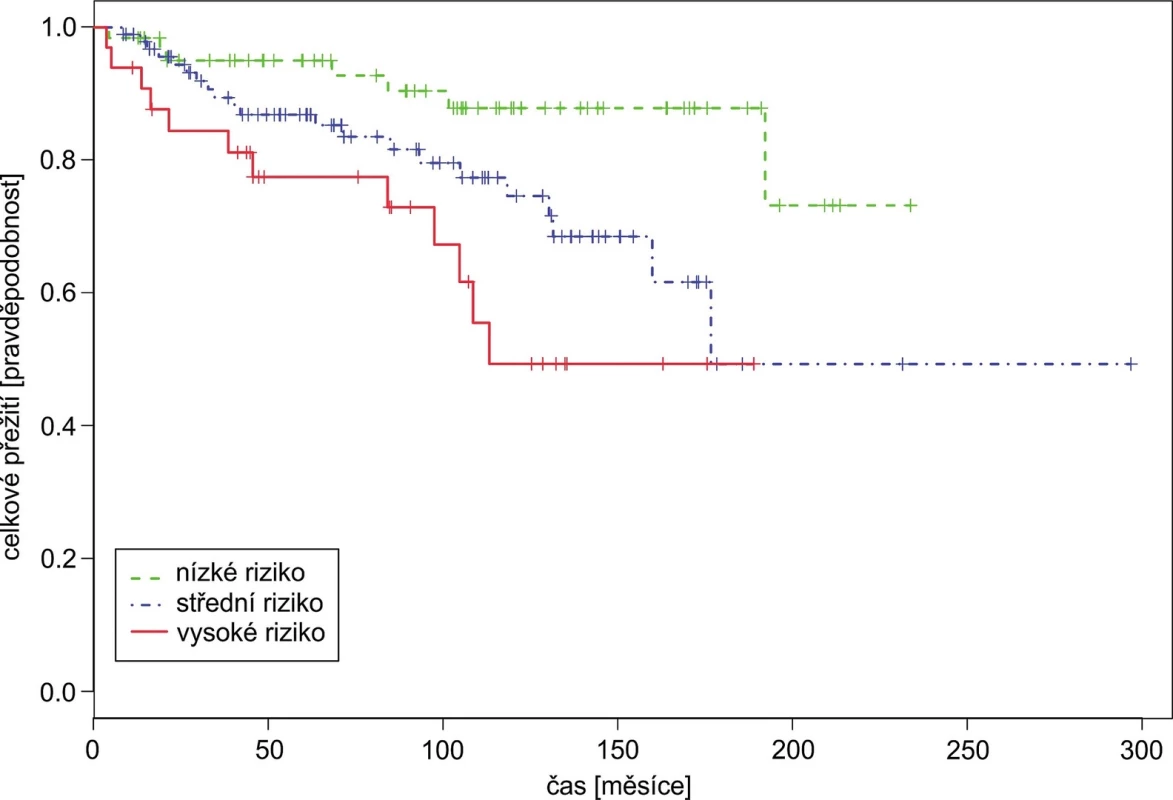
Konkordance cHAS = 0,633; rozdíl mezi středně a nízko rizikovou skupinou byl statisticky významný HRHAS21 = 2,56, p = 0,033, rozdíl mezi vysoko a nízko rizikovou skupinou taktéž HRHAS31 =4,58, p = 0,002. 3. Celkové přežití pacientů podle skóre EUTOS 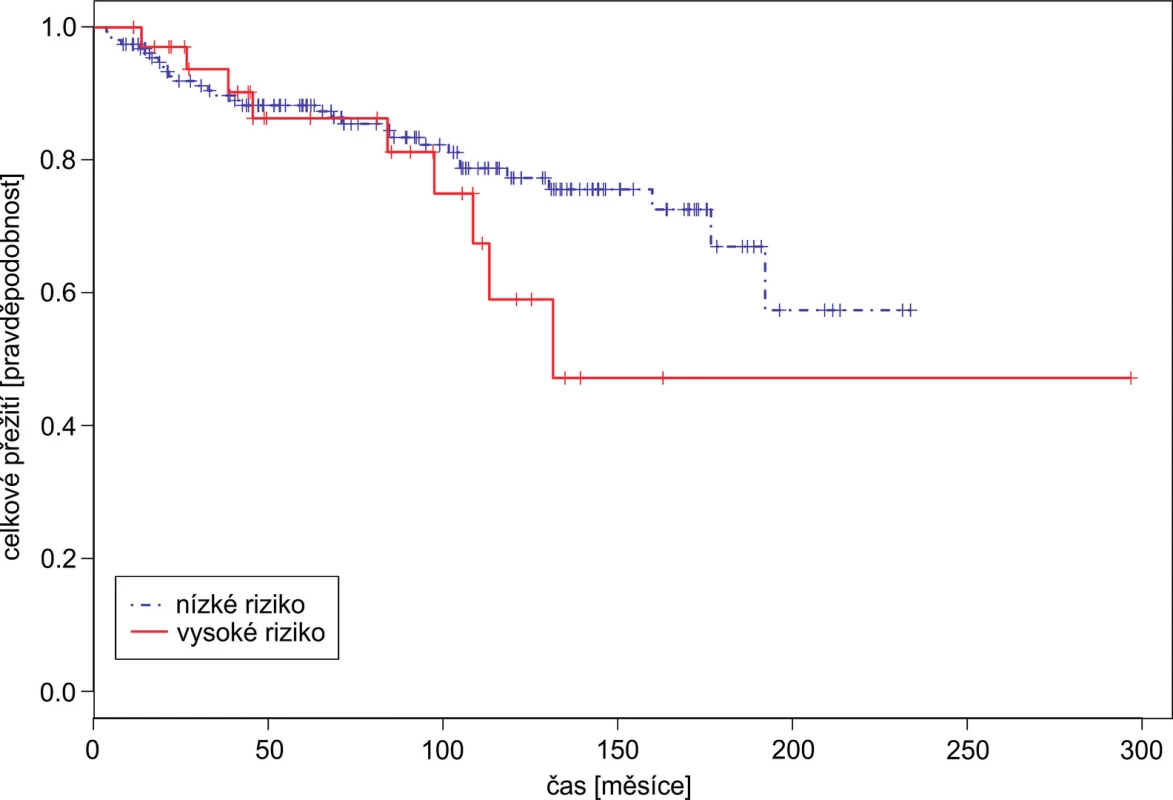
Konkordance cEUT = 0,515; rozdíl mezi oběma rizikovými skupinami nebyl statisticky významný, log rank test; p = 0,271. 4. Celkové přežití pacientů podle nového skóre vytvořeného součtem Hasfordova skóre (1–3 body) a Sokalova skóre (1–3 body). 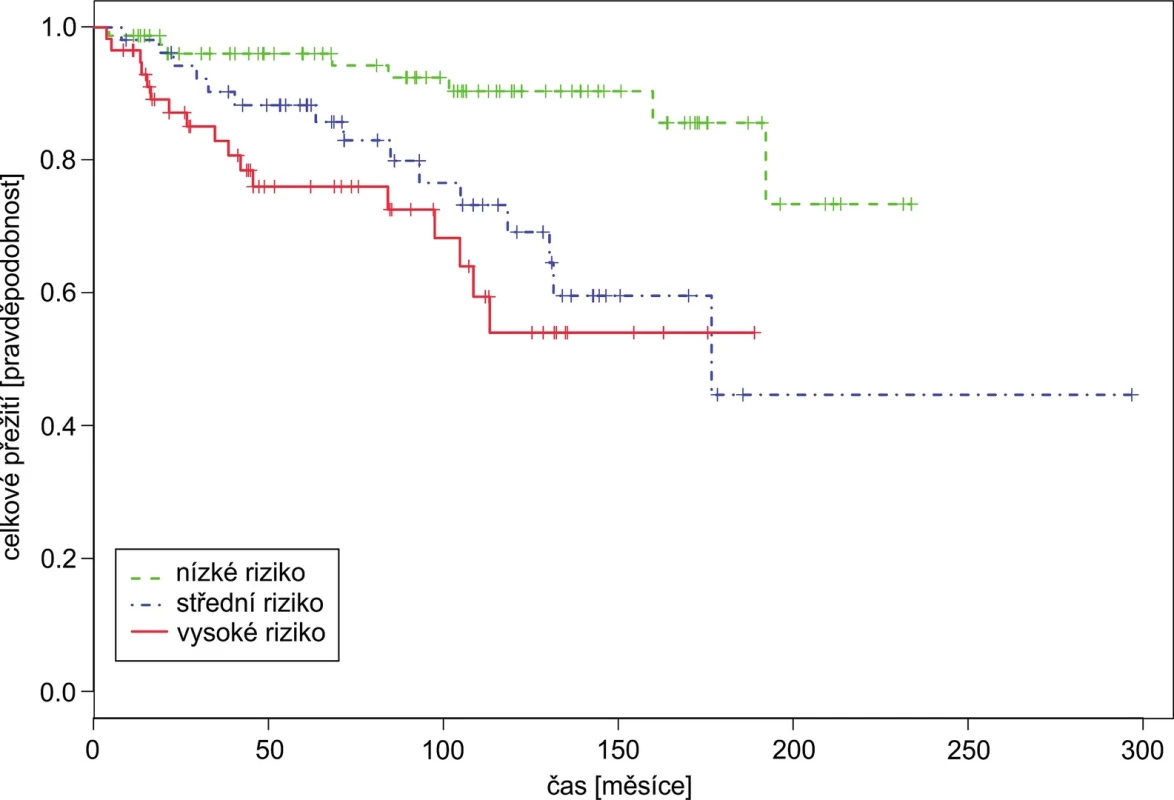
Populace byla rozdělena na tři kategorie: nízké riziko (Has+Sok ≤ 3), střední riziko (Has+Sok = 4) a vysoké riziko (Has+Sok ≥ 5). Konkordance cHAS+SOK = 0,674; rozdíl mezi středně a nízko rizikovou skupinou byl statisticky významný HR(HAS+SOK)21 = 3,41, p = 0,006, rozdíl mezi vysoko a nízko rizikovou skupinou taktéž HR(HAS+SOK)31 = 5,00, p < 0,001. 5. Přežití do progrese pacientů podle nového skóre vytvořeného součtem Hasfordova a Sokalova skóre stejným způsobem jako v obrázku 4 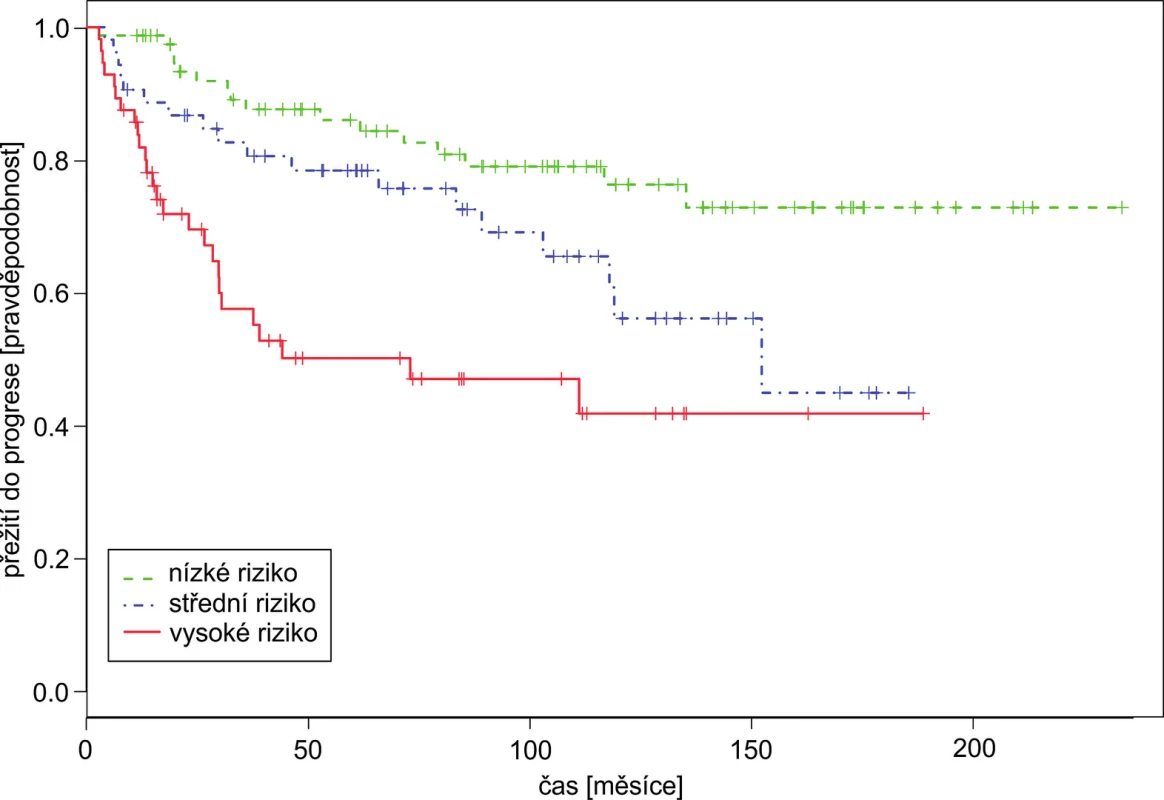
Konkordance cHAS+SOK = 0,664; rozdíl mezi středně a nízko rizikovou skupinou byl hraničně významný HR(HAS+SOK)21 = 1,92, p = 0,059, rozdíl mezi vysoko a nízko rizikovou skupinou byl významný HR(HAS+SOK)31 = 3,92, p < 0,001. DISKUSE
S pokusy stanovit prognózu pacientů s CML začali v roce 1981 Tura se spolupracovníky ve studii, do níž zařadili 153 pacientů léčených perorální chemoterapií [11]. Statistickou analýzou určili jako významné tyto faktory: velikost sleziny, jater, dále počet trombocytů, leukocytů, promyelocytů, myelocytů a blastů v periferii. Prediktivní hodnota jejich skóre vyšla statisticky významně, nicméně nebyla potvrzena na dalších souborech nemocných. V roce 1982 Cervantes se spoluautory testovali soubor 121 pacientů a rozdělili nemocné do 3 skupin podle vzorce, v němž použili jako prognostické faktory velikost jater, sleziny a počet erytroblastů v periferní krvi a blastů v kostní dřeni [12]. Jeden z dalších skórovacích systémů vyvinul Kantarjian, který v něm mimo jiné zohlednil i rasu a věk nemocného [13]. V současnosti, v éře TKI, jsou stále používané dva prognostické indexy původně určené k odhadu prognózy nemocných s CML léčených chemoterapií (Sokalovo skóre) nebo interferonem alfa (Hasfordovo nebo také Euro skóre) [5, 6]. Sokalovo skóre bylo publikováno v roce 1984 mezinárodním týmem a testováno na 813 pacientech [5]. Je odvozeno z velikosti sleziny a několika parametrů z krevního obrazu. Skóre se vypočítává podle poměrně složitého vzorce, což představuje do určité míry nevýhodu. Velikost vyšetřovaného souboru a kvalita statistického zpracování dat nejspíše způsobily, že Sokalovo skóre lze úspěšně používat dodnes. Skóre EUTOS bylo vypočteno v roce 2011 s cílem připravit jednoduchý prognostický index, použitelný pro nemocné léčené pomocí TKI [7]. Jako cílový parametr bylo při jeho přípravě použito dosažení kompletní cytogenetické odpovědi po 12 měsících léčby TKI, jako faktoru, který v analýzách nejvíce koreloval s přežitím nemocných a výsledkem léčby. Skóre se vypočítá pouze z procenta periferních bazofilů a velikosti sleziny v centimetrech. Zavedení EUTOS skóre se na řadě pracovišť neosvědčilo, nedokázalo odlišit v některých kohortách pacientů statisticky významné skupiny s odlišným přežitím [8, 9], zatímco v jiných sestavách nemocných bylo ověřeno úspěšně [14]. V našem souboru pacientů jsme s EUTOS skóre měli negativní zkušenost.
Myšlenka připravit „kombinovaný“ skórovací systém vychází z poznatku, že v různých skórovacích systémech můžou mít jednotliví pacienti různé hodnoty výsledného rizika. Tohoto faktu si všimli také korejští autoři, kteří zjistili, že nemocní, kteří mají ve všech systémech vysoké nebo nízké riziko, mají odlišné přežití než nemocní s různě vysokým rizikem podle jednotlivých skóre [15]. My jsme způsob určení nového kombinovaného skóre dále upravili pomocí přidělení bodů podle různého rizika v jednotlivých systémech a určení finálního skóre podle konečného součtu těchto bodů. Tento postup podle našeho názoru lépe odliší vysoce rizikové nemocné od nemocných se střední nebo dobrou prognózou. Náš systém se vyhýbá klasickému postupu, při němž se ve velkém souboru nemocných určí faktory, které mají v tomto souboru nezávislý prediktivní význam a podle jejich váhy se připraví vzorec pro výpočet skóre. Skóre se tak přizpůsobuje aktuálně hodnocenému souboru pacientů („nafituje“ se na daný soubor). Možnou chybu tohoto přístupu náš návrh obchází.
Pokoušeli jsme se optimalizovat složení našeho kombinovaného skóre zařazením dvou až tří prognostických systémů (Sokal, Hasford v první i finální verzi, EUTOS), přidělením různého počtu bodů za vysoké riziko podle skóre EUTOS a také pomocí rozdělení do dvou, respektive tří skupin (se skupinou s intermediár-ní prognózou nebo bez ní). Žádná z kombinací jednoznačně nepřekonala kombinaci dvou indexů podle Sokala a Hasforda s rozdělením do tří prognostických skupin. Podle našeho názoru to bylo díky kombinaci některých odlišných faktorů, z nichž jsou oba indexy odvozeny, a také tím, že samotné indexy mají významnou prediktivní schopnost.
Jsme si plně vědomi toho, že výsledky naší analýzy jsou do určité míry zkreslené zařazením nemocných předléčených interferonem alfa. Tato skupina nemocných byla zařazena s cílem zvýšit počet pacientů, na nichž bude nový index validován. Soubor díky tomu není ideálně homogenní, což by bylo dosaženo v případě zařazení nemocných léčených výhradně TKI (nejlépe jedním druhem TKI) v první linii. Na druhé straně jsme přesvědčeni, že výsledek statistické analýzy přežití nemocných nebyl tímto naprosto zásadně ovlivněn, protože pro podobnou statistickou analýzu je důležité, aby byli pacienti léčeni obdobně účinnou léčbou. Analýzy provedené pouze na podskupině pacientů interferonem nepředléčených (jejichž výsledky pro přehlednost neuvádíme) to dokládají. Z našich předchozích studií vyplývá, že nemocní předléčení na našem pracovišti interferonem alfa měli po TKI velmi dobrou prognózu a výsledky jejich přežití patří k nejlepším popisovaným v literatuře [16]. Nelze také vyloučit, že sekvenční léčba TKI po interferonu alfa zlepšuje u určité skupiny nemocných konečnou odpověď na terapii. Medián délky trvání léčby interferonem byl 9,33 měsíce, nicméně část nemocných byla léčena před převedením na TKI interferonem alfa velmi krátce. Konečně, prezentované výsledky považujeme za první krok, po němž bude provedena validace nového skóre na větších skupinách přísně homogenně léčených pacientů s CML.
ZÁVĚR
Prognostické skórovací systémy představují jednu z mála možností, jak odhadnout prognózu nemocných s CML ještě před zahájením léčby. Ideální by bylo, aby umožnily identifikovat všechny nemocné, kteří nebudou reagovat na léčbu optimálně. Heterogenní biologické vlastnosti leukemických klonů, jejich různé zastoupení při stanovení diagnózy a omezené možnosti vyšetření pravděpodobně nikdy neumožní přesný odhad prognózy jednotlivého pacienta. Doposud se nepodařilo doplnit stávající skóre o nový biologický nebo molekulární marker, který by dokázal nahradit základní klinické a hematologické parametry používané v současnosti. Otázkou zůstává, zda je vůbec nezbytné zabývat se pátráním po nejdokonalejším vzorci pro odhad prognózy a nestačí se řídit časnou odpovědí na léčbu v situaci, kdy po TKI má naprostá většina nemocných velmi dobrou prognózu. Používaná skórovací schémata pro stanovení míry rizika onemocnění u pacientů s CML mají různou prediktivní hodnotu. Použití kombinace dvou v současnosti používaných skórovacích systémů podle našeho návrhu může odhad rizika zlepšit. Úspěšnost nového „kombinovaného“ skóre je nezbytné ověřit na větším souboru pacientů s CML léčených přísně homogenně.
Podíl autorů na přípravě rukopisu
ČZ – sběr a kontrola dat, příprava první verze rukopisu
FJ, FT – statistická analýza dat, design nového skóre
MI – sběr a kontrola dat
SI, RP, IK, PT – léčba pacientů, kritická revize rukopisu
FE – design studie, léčba pacientů, kontrola dat, kritická revize a finalizace rukopisu
Poděkování
Práce byla podpořena grantem UP IGA-LF-2016-001.
Čestné prohlášení autorů
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Doručeno do redakce dne 7. 10. 2015.
Přijato po recenzi dne 18. 12. 2015.
prof. MUDr. Edgar Faber, CSc.
Hemato-onkologická klinika
Fakultní nemocnice Olomouc
Lékařská fakulta Univerzity Palackého v Olomouci
I. P. Pavlova 6
775 20 Olomouc
e-mail: faber@fnol.cz
Sources
1. Nowell PC, Hungerford DA. A minute chromosome in human granulocytic leukemia. Science 1960; 132 : 1497.
2. Rowley JD. A new consistent chromosomal abnormality in chronic myelogenous leukemia identified by quinacrine fluorescence and Giemsa staining. Nature 1973; 243 : 290–293.
3. Björkholm M, Ohm L, Eloranta S, et al. Success story of targeted the-rapy in chronic myeloid leukemia: a population-based study of patients diagnosed in Sweden from 1973 to 2008. J Clin Oncol 2011; 29 : 2514–20.
4. Baccarani M, Deininger MW, Rosti G, et al. European LeukemiaNet recommendations for the management of chronic myeloid leukemia: 2013. Blood 2013; 122 : 872–884.
5. Sokal JE, Cox EB, Baccarani M, et al. Prognostic discrimination in “good-risk” chronic granulocytic leukemia. Blood 1984; 63 : 789–799.
6. Hasford J, Pfirrmann M, Hehlmann R, et al. A new prognostic score for the survival of patients with chronic myeloid leukemia. J Natl Cancer Inst 1998; 90 : 850.
7. Hasford J, Baccarani M, Hoffmann V, et al. Predicting complete cytogenetic response and subsequent progression-free survival in 2060 patients with CML on imatinib treatment: the EUTOS score. Blood 2011; 118 : 686–692.
8. Marin D, Amr R, Ibrahim AR, Goldman JM. European Treatment and Outcome Study (EUTOS) score for chronic myeloid leukemia still requires more confirmation. J Clin Oncol 2011; 29 : 3944–3945.
9. Jabbour E, Cortes J, Nazha A, et al. EUTOS score is not predictive for survival and outcome in patients with early chronic phase chronic myeloid leukemia treated with tyrosine kinase inhibitors: a single institution experience. Blood 2012; 119 : 4524–4526.
10. Harrell FE, Lee KL, Mark DB. Tutorial in biostatistics. Stat Med 1996;15 : 361–387.
11. Tura S, Baccarani M, Corbelli G, et al. Staging of chronic myeloid leukaemia. Br J Haematol 1981; 47 : 105–119.
12. Cervantes F, Rozman C. A multivariate analysis of prognostic factors in chronic myeloid leukemia. Blood 1982; 60 : 1298–1304.
13. Kantarjian HM, Keating MJ, Smith TL, et al. Proposal for a simple synthesis prognostic staging system in chronic myelogenous leukemia. Am J Med 1990; 88 : 1–8.
14. Hoffmann VS, Baccarani M, Lindoerfer D, et al. The EUTOS prognostic score: review and validation in 1288 patients with CML treated frontline with imatinib. Leukemia 2013; 27 : 2016–2022.
15. Yahng SA, Jang EJ, Choi SY, Lee SE, Kim SH, Kim DW. Prognostic discrimination for early chronic phase chronic myeloid leukemia in imatinib era: comparison of Sokal, Euro, and EUTOS scores in Korean population. Int J Hematol 2014; 100 : 132–140.
16. Rohoň P, Rožmanová Š, Zapletalová J, et al. Výsledky liečby pacientov v chronickej fáze chronickej myelocytovej leukémie na HOK v Olomouci v rokoch 2000–2009: prognostický význam Sokalovho indexu a ELN kritérií. Transfuze Hematol dnes 2010; 16(4): 202–209.
Labels
Haematology Internal medicine Clinical oncology
Article was published inTransfusion and Haematology Today

2016 Issue 1-
All articles in this issue
- Prognostic factors in chronic myeloid leukemia: can we gain more from combination?
- Analysis of serum free light chains ratio (FLC-r, FreeliteTM), immunoglobulin heavy/light chain pairs ratio (HLC-r, HevyliteTM) and the results of plasma cell multiparametric flow cytometry in relation to progression free survival in multiple myeloma
- Autologous stem cell transplantation in Waldenström macroglobulinemia
- Consensual guidelines of the Czech National Haemophilia Programme (CNHP) for factor replacement therapy in patients with haemophilia during invasive procedures and surgery
- Consensual guidelines of the Czech National Haemophilia Programme (CNHP) for the diagnosis and treatment of patients with congenital haemophilia and inhibitors to FVIII/FIX
- Chronic myeloid leukaemia – standardization of BCR-ABL1 transcript level monitoring in the Czech Republic
- Transfusion and Haematology Today
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Prognostic factors in chronic myeloid leukemia: can we gain more from combination?
- Chronic myeloid leukaemia – standardization of BCR-ABL1 transcript level monitoring in the Czech Republic
- Consensual guidelines of the Czech National Haemophilia Programme (CNHP) for factor replacement therapy in patients with haemophilia during invasive procedures and surgery
- Analysis of serum free light chains ratio (FLC-r, FreeliteTM), immunoglobulin heavy/light chain pairs ratio (HLC-r, HevyliteTM) and the results of plasma cell multiparametric flow cytometry in relation to progression free survival in multiple myeloma
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

