-
Medical journals
- Career
Robotické plicní segmentektomie, iniciální zkušenosti v České republice
Authors: J. Kolařík 1; J. Tavandžis 1; R. Novysedlák 1; J. Vachtenheim 1; D. Sibřina 2,3; M. Švorcová 1; J. Pozniak 1; J. Šimonek 1; J. Schützner 1; R. Lischke 1
Authors‘ workplace: III. chirurgická klinika 1. lékařské fakulty Univerzity Karlovy a Fakultní nemocnice v Motole, Praha, Česká republika 1; Durham University, United Kingdom 2; Institut klinické a experimentální medicíny, Praha, Česká republika 3
Published in: Rozhl. Chir., 2023, roč. 102, č. 5, s. 199-203.
Category: Original articles
doi: https://doi.org/10.33699/PIS.2023.102.5.199–203Overview
Úvod: Zavedení screeningového programu plicního karcinomu v České republice a jeho diagnóza v časnějších stadiích zvyšuje potřebu provádění anatomických plicních segmentektomií. Cílem této studie je popsání časných výsledků prvních roboticky asistovaných torakoskopických segmentektomií v Česku.
Metody: Naše centrum provedlo 151 robotických anatomických plicních resekcí od zahájení programu v srpnu 2020 a dosáhlo statutu centra pro proktoring a case observation. Program robotických segmentektomií jsme zahájili po dokončení 70 robotických lobektomií. Retrospektivně jsme analyzovali výsledky našich prvních 20 pacientů indikovaných k robotické segmentektomii.
Výsledky: Průměrný věk pacientů byl 60 let, 11 žen a 7 mužů. Hlavní indikací byla primární plicní malignita (n=13), plicní metastáza (n=2) a abenigní léze (n=3). Provedli jsme 11 prostých segmentektomií, 6 komplexních (S2, S3, S1a+2, S10 vpravo) a jednu S6 segmentektomii vpravo s bronchoplastikou. Průměrný počet odebraných uzlin u NSCLC byl 20, průměrná krevní ztráta 25 ml (od 10 do 100 ml) a průměrný operační čas 200 minut. Všechny resekční okraje byly bez nádoru. Nebyla třeba žádná konverze k torakotomii, ve dvou případech jsme konvertovali k robotické lobektomii pro lokalizaci ložiska v blízkosti intersegmentální hranice a tyto pacienty vyloučili ze studie. Komplikace se vyskytly u 1 pacienta, a to paréza nervus laryngeus recurrens. Hrudní drenáž trvala průměrně 1,9 dne a doba hospitalizace 3,9 dne.
Závěr: Zahájení programu robotických segmentektomií po dokončení robotické učicí křivky nabízí dle naší zkušenosti nadějné výsledky. Robotická technologie a předoperační plánování usnadňuje tento technicky náročný výkon zejména při nutnosti bronchoplastiky.
Klíčová slova:
karcinom plic – robotické plicní segmentektomie – učicí křivka – bronchoplastika – mediastinální lymfadenektomie
ÚVOD
V souvislosti se zaváděním screeningového programu plicního karcinomu v České republice [1] a stále časnější diagnostikou karcinomů v ranných stadiích narůstají indikace k provádění plicních segmentektomií. Miniinvazivní hrudní chirurgie a v poslední době zejména robotická je na výrazném vzestupu [2]. Počet hrudně-chirurgických robotických center v Evropě vzrostl v poslední dekádě exponenciálně. Robotická technika v kombinaci s předoperačním plánováním, 3D rekonstrukcemi a rozšířenou realitou významně usnadňuje tyto technicky náročné výkony [3].
Cílem této studie je popsání časných výsledků prvních roboticky asistovaných torakoskopických segmentektomií v Česku.
METODY
Naše robotické centrum zahájilo plicní operativu v srpnu 2020 za dodržení doporučeného postupu včetně case observation, e-learningu, simulátoru, dry lab, nácviku ve vet lab a proktoringu. Od té doby jsme provedli 151 anatomických plicních resekcí pomocí robotické platformy daVinci Xi, Intuitive Surgical, Sunnyvale, CA, USA (Graf 1). Díky počtu provedených resekcí jsme získali statut case observation centra pro robotickou hrudní chirurgii a proktoring dalších nově vznikajících robotických center. Program robotických segmentektomií jsme zahájili po dokončení 70 robotických lobektomií, tedy bezpečně po absolvování učicí křivky. Používáme techniku 4 ramen a asistentského portu, počáteční lymfadenektomie s peroperačním histologickým vyloučením uzlinového šíření usnadňuje další preparaci jednotlivých bronchovaskulárních struktur. Pro plánování segmentektomií a lepší představu o častých anatomických anomáliích segmentálních cév či průdušek využíváme CT 3D modely platformy speciálně upravené verze virtuální a rozšířené reality aplikace VRlab od IKEM pro naše účely (Obr. 1).
Graph 1. Počty robotických anatomických plicních resekcí
Graph 1: Number of robotic anatomical resections
Image 1. CT 3D rekonstrukce pro rozšířenou a virtuální realitu, žlutě znázorněn tumor před segmentektomií linguly
Fig. 1: CT 3D recontruction for augmented and virtuál reality, yellow marked tumor before segmentectomy of lingula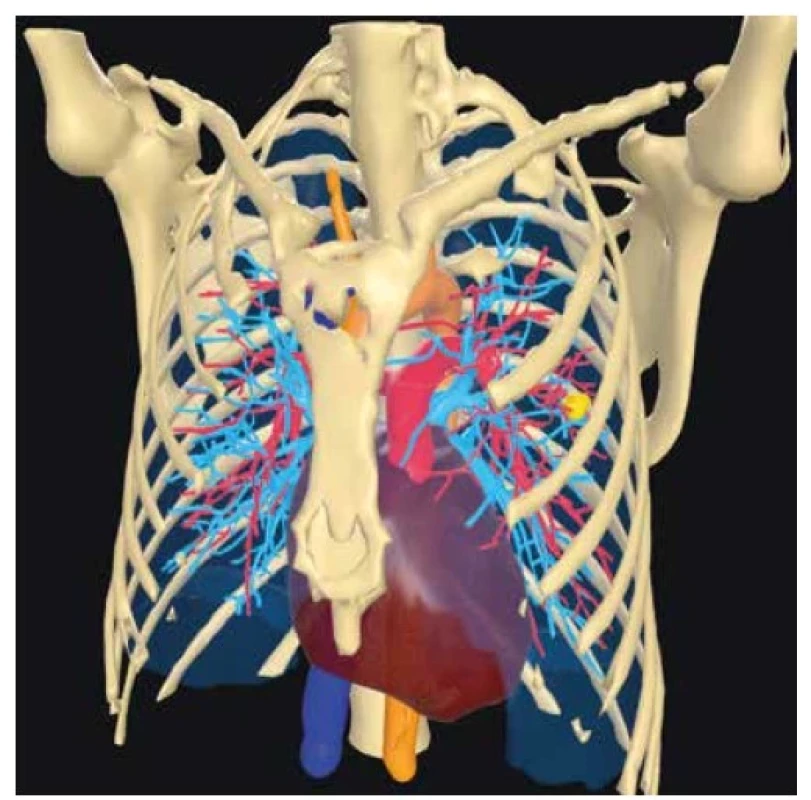
Retrospektivně jsme analyzovali výsledky našich prvních 20 pacientů indikovaných k robotické segmentektomii.
VÝSLEDKY
V našem souboru nebyla žádná konverze k torakotomii, ve dvou případech jsme konvertovali k robotické lobektomii pro lokalizaci ložiska v blízkosti intersegmentální hranice a tyto 2 pacienty vyloučili ze studie. Dokončili jsme tedy 18 segmentektomií (Graf 2). Průměrný věk pacientů byl 60±15 let; včetně 11 (61,1 %) žen. Hlavní indikací byla primární plicní malignita 13 (72,2 %), z toho nemalobuněčný karcinom plic (NSCLC) v prvním stadiu 9 (69,2 %), malobuněčný karcinom plic (SCLC) v časném stadiu u pacientky s limitovanou plicní rezervou 1 (7,7 %), typický karcinoid 2 (15,4 %) a sarkom 1 (7,7 %). Z dalších diagnóz se jednalo o plicní metastázu kolorektální 2 (11,1 %), bronchiektazie 1 (11,1 %) a centrálně uložený hamartom 2 (22,2 %) (Graf 3). Provedli jsme 11 (61,1 %) prostých segmentektomií, 6 (33,3 %) komplexních (Obr. 2) a jednu (5,5 %) S6 segmentektomii vpravo s bronchoplastikou, kdy se jednalo o typický karcinoid intraluminálně rostoucí z B6 vpravo do bronchus intermedius. Přerušili jsme A6, vypreparovali odstup B6, který jsme robotickými nůžkami otevřeli, luxovali intralumilální tumor z bronchu (Obr. 3), identifikovali stopku karcinoidu periferněji v B6, dokončili segmentektomii a provedli robotickou suturu původního odstupu B6 V-lock 3/0 [Obr. 4]. Rozložení jednotlivých operovaných segmentů viz (Graf 4). Průměrný počet odebraných uzlin u NSCLC byl 20±7,7, průměrná krevní ztráta 24±25 ml (od 10 do 100 ml) a průměrný operační čas 200±15 minut. Všechny resekční okraje byly bez nádoru. Výskyt komplikací byl u 1 (5,5 %) pacienta, který měl parézu nervus laryngeus recurrens a fibrilaci síní. Hrudní drenáž trvala 1,9±0,9 dne a celková doba hospitalizace 3,9±0,9 dne (Graf 5, 6).
Graph 2. Poměr robotických lobektomií a segmentektomií
Graph 2: Percentage of robotic lobectomies and segmentectomies
Graph 3. Diagnózy indikované k segmentektomii
Graph 3: Diagnosis indicated for segmentectomy
Graph 4. Zastoupení operovaných segmentů
Graph 4: Distribution of operated segments
Image 2. Robotické segmentektomie S1a+2 vpravo pro 15mm adenokarcinom při hranici S2 a S1, preparát
Fig. 2: Robotic segmentectomy S1a+2 right for 15 mm adenocarcinoma at the border of S2 and S1, specimen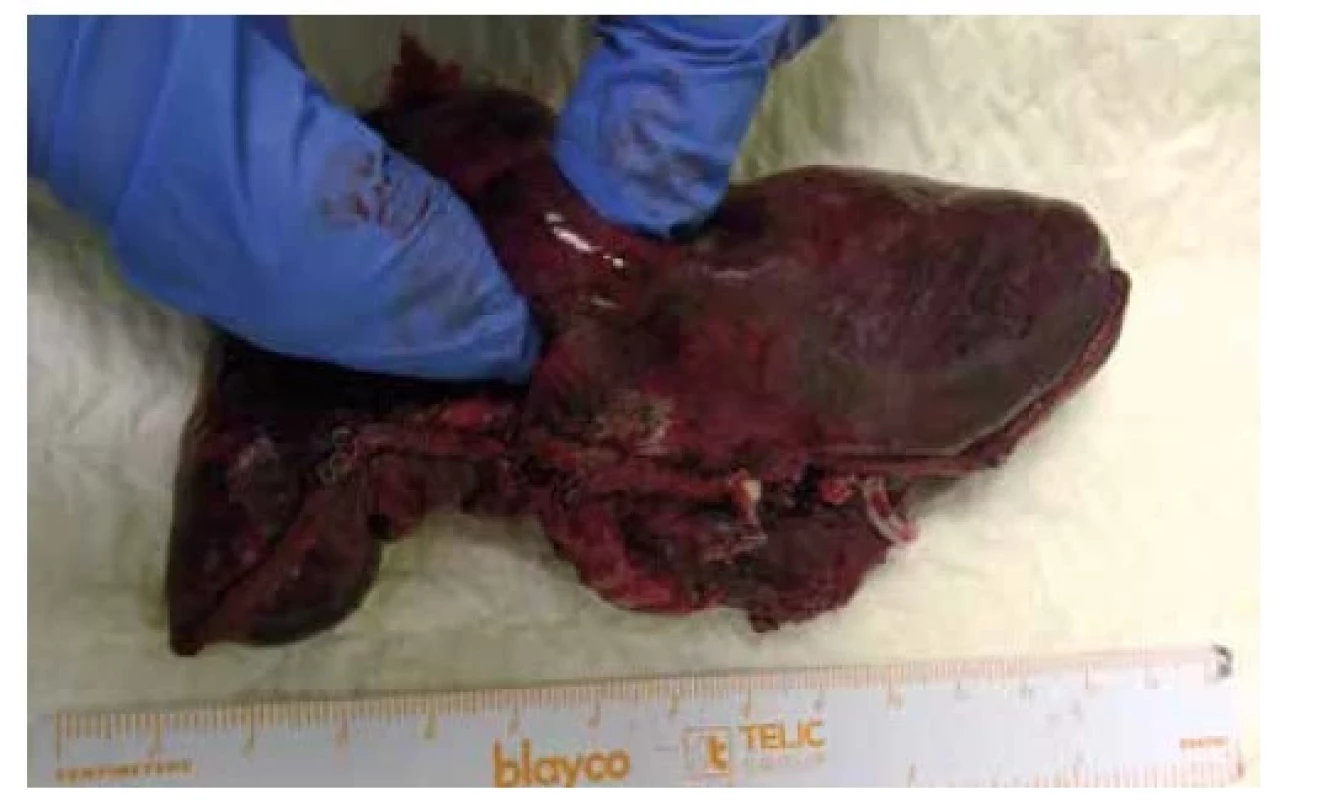
Image 3. Robotická segmentektomie S6 vpravo pro typický karcinoid, nůžky otevírají segmentární bronchus a dislokují bělavou masu karcinoidu z intraluminálního šíření do bronchus intermedius
Fig. 3: Robotic segmentectomy S6 right for typical karcinoid with intraluminal growth into bronchus intermedius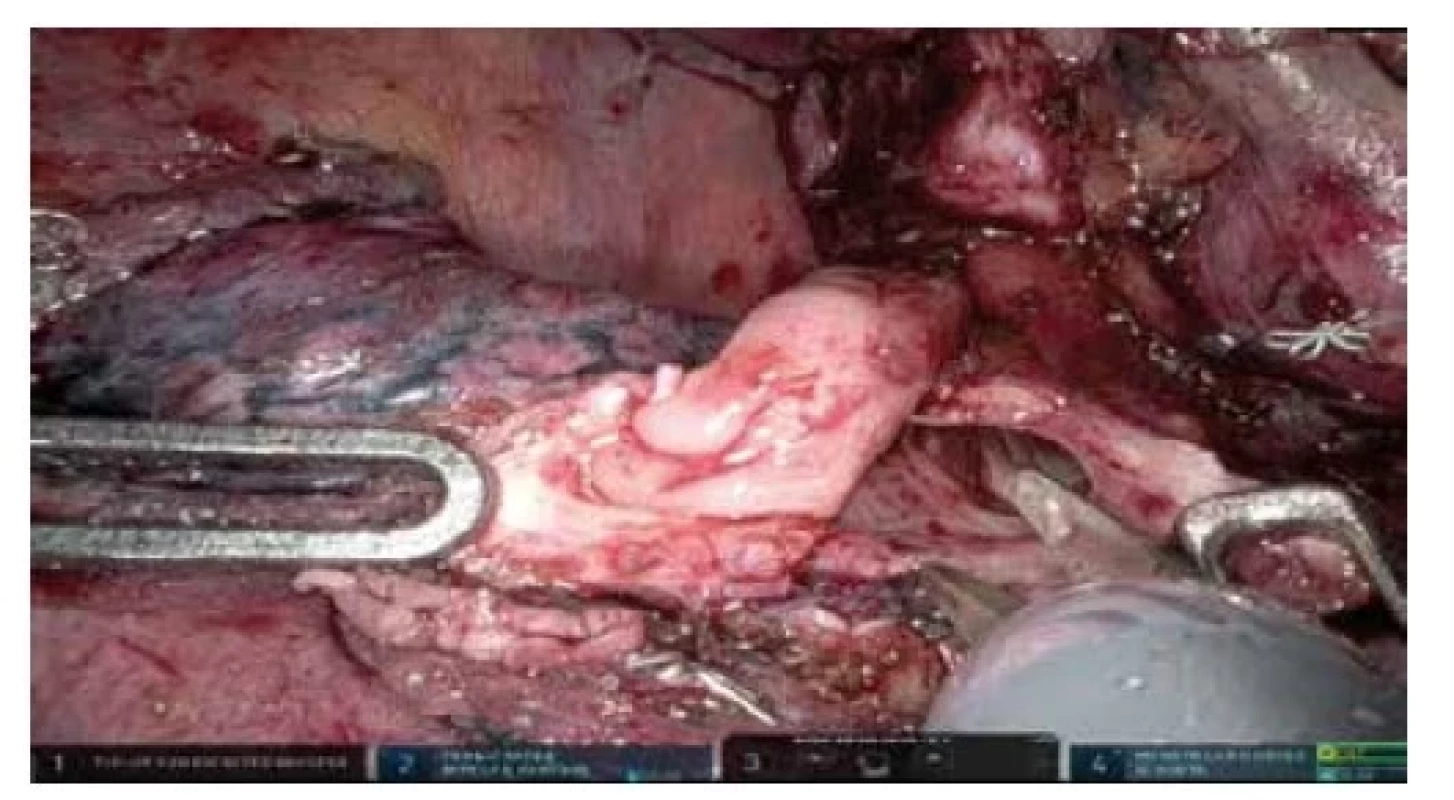
Image 4. Robotická segmentektomie S6 vpravo, robotická sutura bronchiálního defektu
Fig. 4: Robotic segmentectomy S6 right, robotic suture of a bronchial defect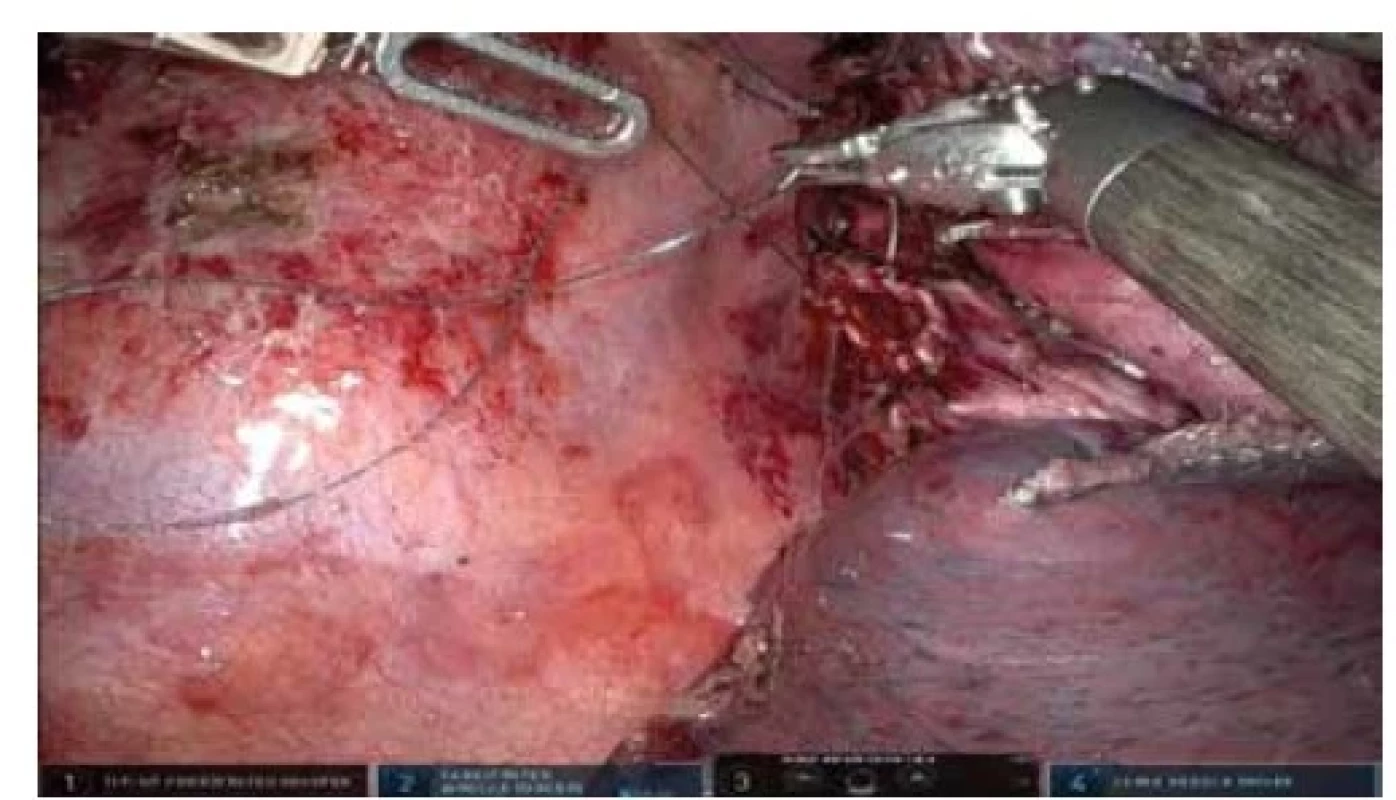
Graph 5. Pooperační den propuštění (ve dnech)
Graph 5: Postoperative day of dimision (in days)
Graph 6. Délka hospitalizace (ve dnech)
Graph 6: Length of stay (in days)
DISKUZE
Lobektomie je dlouhodobě považována za zlatý standard operační léčby bronchogenního karcinomu. Přispěly k tomu i závěry Ginsbergovy prospektivní multicentrické randomizované studie z roku 1995, která v léčbě NSCLC velikosti do 3 cm porovnávala sublobární resekce včetně klínovitých resekcí a lobektomie. Sublobární resekce byly spojeny s trojnásobným rizikem lokoregionální recidivy a horším přežíváním [4]. Recentně však byly publikovány dlouho očekávané výsledky fáze 3 dvou velkých multicentrických prospektivních randomizovaných studií, japonské Japan Clical Oncology Group (JCOG) JCOG 0802/WJOG4607L [5] a Altorkiho americké Cancer and Leukemia Group B (CALGB) [6], které potvrdily noninferioritu segmentektomií v případě první studie a sublobárních resekcí obecně v případě druhé oproti lobektomiím u NSCLC menšího než 2 cm, lokalizovaného v konkrétním segmentu v periferní třetině plicního parenchymu. Skupina segmentektomií zaznamenala lepší celkové přežívání [5]. Jednovteřinová vitální kapacita rok po operaci byla ve skupině segmentektomií vyšší jen o 3,5 % [5]. Analýza databáze European Society of Thoracic Surgeons (ESTS) prokázala 35% redukci mortality u skupiny vysoce rizikových pacientů v případě segmentektomií oproti lobektomiím [7]. Rozdíl v zachování respirační funkce po segmentektomii oproti lobektomii závisí na typu segmentektomie. Zachování respirační funkce favorizuje dle Taneho práce segmentektomii S1+2 oproti levé horní lobektomii, na rozdíl od kulminektomie (segmentektomie S1+2+3) [8].
Retrospektivní analýza dat 3 institucí ověřila srovnatelné výsledky komplexních segmentektomií s lobektomiemi odpovídající lokalizace u karcinomů do 2 cm [9].
Pacienti, kteří jsou operovaní pro bronchogenní karcinom, zůstávají i nadále rizikovou skupinou. U pacientů již jednou operovaných se v 2–5 % vyvine v průběhu života další primární plicní karcinom [4,10]. Pokud byla u těchto pacientů první operace segmentektomie, tak je větší pravděpodobnost, že budou mít dostatečnou respirační rezervu i na operaci nového primárního tumoru.
Z miniinvazivní plicní operace obecně nejvíce profitují pacienti s hraniční respirační rezervou. Kombinace s parenchym šetřící segmentektomií může být u některých pacientů jedinou nadějí, jak dosáhnout na chirurgickou modalitu léčby. Segmentektomie u pacientů, které indikujeme jako plně radikální operaci, se označují jako „intenced segmentectomy“. U pacientů, kteří mají limitovanou plicní rezervu či vzhledem k věku a komorbiditám jsou příliš rizikoví k jinak indikované lobektomii, hovoříme o „compromised segmentectomy“.
ZÁVĚR
Zahájení programu robotických segmentektomií po dokončení robotické učicí křivky nabízí dle naší zkušenosti i v českém prostředí bezpečnost a nadějné výsledky. Robotická technologie a předoperační plánování usnadňuje tento technicky náročný výkon zejména při nutnosti bronchoplastiky. Robotický výkon umožňuje velmi radikální lymfadenektomii, minimalizaci krevní ztráty a časnou dimisi pacientů.
Seznam zkratek:
NSCLC – nemalobuněčný karcinom plic
SCLC – malobuněčný karcinom plic
JCOG – Japan Clical Oncology Group
CALGB – Cancer and Leukemia Group B
ESTS – European Society of Thoracic Surgeons
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
MUDr. Jan Kolařík
III. chirurgická klinika
1. LF UK a FN v Motole, Praha
e-mail: jan.kolarik@fnmotol.cz
Sources
1. Lambert L, Janouskova L, Novak M, et al. Early detection of lung cancer in Czech high-risk asymptomatic individuals (ELEGANCE): A study protocol. Medicine (Baltimore) 2021 Feb 5;100(5):e23878. doi:10.1097/MD.0000000000023878. PMID: 33592843; PMCID: PMC7870244.
2. Subramanian MP, Liu J, Chapman WC Jr, et al. Utilization trends, outcomes, and cost in minimally invasive lobectomy. Ann Thorac Surg. 2019 Dec;108(6):1648–1655. doi:10.1016/j.athoracsur.2019.06.049. Epub 2019 Aug 7. PMID: 31400324; PMCID: PMC6878158.
3. Baste JM, Soldea V, Lachkar S, et al. Development of a precision multimodal surgical navigation system for lung robotic segmentectomy. J Thorac Dis. 2018 Apr;10(Suppl 10):S1195 – S1204. doi:10.21037/jtd.2018.01.32. PMID: 29785294; PMCID: PMC5949399.
4. Ginsberg RJ, Rubinstein LV. Randomized trial of lobectomy versus limited resection for T1 N0 non-small cell lung cancer. Lung Cancer Study Group. Ann Thorac Surg. 1995 Sep;60(3):615–622; discussion 622–623. doi:10.1016/0003-4975(95)00537-u. PMID: 7677489.
5. Altorki N, Wang X, Kozono D, et al. Lobar or sublobar resection for peripheral stage IA non-small-cell lung cancer. N Engl J Med. 2023 Feb 9;388(6):489–498. doi:10.1056/NEJMoa2212083. PMID: 36780674.
6. Saji H, Okada M, Tsuboi M, et al. West Japan Oncology Group and Japan Clinical Oncology Group. Segmentectomy versus lobectomy in small-sized peripheral non-small-cell lung cancer (JCOG0802/WJOG4607L): a multicentre, open-label, phase 3, randomised, controlled, non-inferiority trial. Lancet. 2022 Apr 23;399(10335):1607–1617. doi:10.1016/S0140-6736(21)02333-3. PMID: 35461558.
7. Brunelli A, Decaluwe H, Gossot D, et al. Perioperative outcomes of segmentectomies versus lobectomies in high-risk patients: an ESTS database analysis. Eur J Cardiothorac Surg. 2020 Sep 15:ezaa308. doi:10.1093/ejcts/ezaa308. Epub ahead of print. PMID: 32929479.
8. Tane S, Nishio W, Fujibayashi Y, et al. Thoracoscopic left S1 + 2 segmentectomy as a good resolution for preserving pulmonary function. Interact Cardiovasc Thorac Surg. 2020 Sep 1;31(3):331–338. doi:10.1093/icvts/ivaa105. PMID: 32747959.
9. Handa Y, Tsutani Y, Mimae T, et al. Oncologic outcomes of complex segmentectomy: A multicenter propensity scorematched analysis. Ann Thorac Surg. 2021 Mar;111(3):1044–1051. doi:10.1016/j.athoracsur. 2020.06.020. Epub 2020 Aug 12. PMID: 32795524.
10. Lee DS, LaChapelle C, Taioli E, et al. Second primary lung cancers demonstrate similar survival with wedge resection and lobectomy. Ann Thorac Surg. 2019 Dec;108(6):1724–1728. doi:10.1016/j.athoracsur.2019.06.023. Epub 2019 Jul 31. PMID: 31376378.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2023 Issue 5-
All articles in this issue
- Chirurgický trénink v systému specializačního vzdělávání v ČR
- Massive transfusion protocol
- Magnetic resonance imaging – evaluation of mesorectal lymphadenopathy in patients with rectal cancer
- Robotic pulmonary segmentectomy, initial experience in the Czech Republic
- Peroral endoscopic myotomy (POEM) in the treatment of severe postfundoplication dysphagia
- Pneumatosis cystoides intestinalis as a rare cause of non-surgical pneumoperitoneum
- Open revascularization in a patient with chronic mesenteric ischemia and a history of aorto-bifemoral bypass − a case report
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Massive transfusion protocol
- Pneumatosis cystoides intestinalis as a rare cause of non-surgical pneumoperitoneum
- Peroral endoscopic myotomy (POEM) in the treatment of severe postfundoplication dysphagia
- Robotic pulmonary segmentectomy, initial experience in the Czech Republic
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

