-
Medical journals
- Career
Akutní hemoragická cholecystitida jako vzácná příčina hemobilie
Authors: M. Bockova 1; F. Pazdírek 1; J. Šťovíček 2; A. Stolz 1
Authors‘ workplace: Chirurgická klinika 2. lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Motol v Praze 1; Interní klinika 2. lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Motol v Praze 2
Published in: Rozhl. Chir., 2023, roč. 102, č. 2, s. 80-84.
Category: Case Report
doi: https://doi.org/10.33699/PIS.2023.102.2.80–84Overview
Hemobilie je vzácným typem krvácení do zažívacího traktu způsobeným nejčastěji iatrogenním poraněním, traumatem či neoplazií. Akutní cholecystitida jako příčina hemobilie je považována za raritní. V našem sdělení prezentujeme případ pacientky, u které byla zdrojem krvácení arodovaná sliznice žlučníku při těžké kalkulózní cholecystitidě. Pacientka v období před krvácením podstoupila akutní ERCP pro obstrukční ikterus s extrakcí konkrementů s následným rozvojem těžké akutní pankreatitidy. Tyto faktory zprvu sváděly k mylným předpokladům a diagnózám. Krvácení nebylo hemodynamicky závažné a běžné vyšetřovací metody neodhalily jeho přesný zdroj. Velkou pomocí bylo použití přímé choledochoskopie (SpyGlassTM), které vyloučilo poranění nebo tumorózní změny hlavních žlučových cest a výrazně posílilo domněnku zdroje krvácení z nitra žlučníku. Chirurgická revize pak tuto příčinu potvrdila a následná cholecystektomie potíže nemocné vyřešila.
Klíčová slova:
cholangioskopie – hemobilie – hemoragická cholecystitida – choledochoskopie – endoskopické zákroky
ÚVOD
Hemobilie je vzácným typem krvácení do zažívacího traktu. Jedná se o krvácení do intrahepatálních nebo extrahepatálních žlučových cest. Klinický obraz byl v literatuře prvně popsán v r. 1654 Glissonem v díle Anatomia Hepatis [1−2], pojem „hemobilie“ byl zaveden Sanblomem v r. 1948 [1]. Etiologicky se na hemobilii nejčastěji podílejí iatrogenní poranění, zevní trauma jater, méně často maligní i benigní tumory, cévní malformace, litiáza a záněty [2,3−5]. Zatímco dle prací z minulého století dominovala jako příčina tupá nebo penetrující traumata jater, od začátku 21. století s rozvojem diagnostických i terapeutických technologií v hepatobiliární oblasti se na prvním místě uplatňují iatrogenní poranění, která tvoří až dvě třetiny případů [6]. Po perkutánních intervencích, jako jsou perkutánní jaterní biopsie nebo perkutánní transhepatická cholangiografie, event. s drenáží (PTC/PTD), je udáváno riziko krvácivých komplikací 1−14 % [3,7] po ERCP, zejména s EPT dojde k hemoragii u 0,76−2,0 % pacientů [8]. Cholelitiáza jako příčina hemobilie je dle některých prací uváděna v 5−15 % případů [4−5]. Žlučové kameny mohou svým tlakem způsobit přímé poranění sliznice žlučníku či žlučovodu, arozi cév a z toho rezultující krvácení [4−5].
Klinický obraz je dán rozsahem krvácení i vyvolávající příčinou. Když krev se žlučí projde přes Vaterskou papilu do duodena, projeví se hemobilie jako hemateméza nebo meléna. Krevní koagula mohou způsobit obstrukci dc. choledochus s klinickými i laboratorními projevy obstrukčního ikteru [4−5]. Často si pacienti stěžují na bolesti v pravém podžebří [1,4,5]. Tradičně popisovaná Quinkeho triáda příznaků – ikterus, bolest břicha a známky krvácení do GIT – je přítomna jen u cca 1/3 případů [1].
Krvácení do žlučových cest způsobené litiázou, neoplazmaty či záněty nebývá velké, zpravidla se opakuje, epizody hemoragie střídá období klidu [3−4], což může znesnadňovat lokalizaci zdroje krvácení, stejně jako tomu bylo u naší pacientky. Takové krvácení často ustane samo. Oproti tomu krvácení z aneurysmat a pseudoaneurysmat cystické nebo hepatické arterie bývá masivní, až život ohrožující [4]. Závažnost krvácení se odrazí v hemodynamické stabilitě, resp. nestabilitě, při prudkém krvácení se projeví až obrazem hypovolemického šoku. Zajímavostí je, že v případech traumatu nebo při iatrogenních příčinách se hemobilie může manifestovat až za týdny či měsíce od inzultu [3].
V rámci dif. dg. krvácení do GIT je třeba myslet i na možnost hemobilie, a to zejména předcházelo-li trauma, invazivní vyšetření nebo chirurgie hepatobiliárního systému, dále u pacientů s ikterem, bolestmi v epigastriu a patologií jaterních testů nebo koagulačních parametrů. Prvním krokem je, jako v ostatních případech krvácení, zajištění pacienta, tekutinová a oběhová resuscitace, korekce anemie a poruch srážlivosti.
Endoskopickými metodami lze až v 60 % stanovit diagnózu [9], v určitých případech i terapeuticky zasáhnout. Urgentní gastrofibroskopie eliminuje ostatní zdroje krvácení do horní části GIT, v 12−30 % může odhalit výtok krve z oblasti Vaterské papily [9]. Přístrojem s axiální optikou je papila obvykle špatně přehledná. Předpokladem k endoskopickému ošetření krvácení v oblasti papily je schopnost endoskopicky pracovat s lateroskopem. Pokud je vyvolávající příčinou krvácení z papily po EPT, lze se pokusit krvácení ošetřit injekcí adrenalinu, klipy, balonkovou tamponádou, argon plazma koagulací, event. aplikací pokrytých biliárních stentů [9−10]. ERCP zobrazí žlučové cesty a žlučník, lze hodnotit dilataci dc. choledochus, mohou se zobrazit defekty v náplni kontrastu způsobené kameny nebo krevními koaguly. ERCP nabízí možnost terapeuticky ovlivnit obstrukci žlučových cest, extrahovat kameny, koagula, k prevenci recidivy obstrukce zavést stent. Ke zlepšení diagnostiky a terapie lézí extrahepatálních žlučových cest byly již od 70. let minulého století vyvíjeny drobné katétry k provedení přímé choledoskopie. Od r. 2006 je k dispozici přístroj SpyGlassTM firmy Boston Scientific Europe [13], který je na rozdíl od předchozích typů ovládán pouze jedním endoskopistou. Standardně se provádí přímá choledochoskopie současně s ERCP. Duodenoskopem je protažen tenký flexibilní endoskop, který disponuje zdrojem světla, kanálem pro irrigaci a sukci a pracovním kanálem pro zavedení nástrojů, např. elektrokoagulační elektrodu, klíšťky k odběru cílené biopsie, laserový zdroj pro provedení litotrypse. Těmito způsoby je možné ošetřit litiázu, stenózu či provést odběr biopsie pod přímou zrakovou kontrolou [14−15]. Bohužel přímá choledochoskopie neumožňuje v současnosti endoskopickou terapii krvácení. Pracovní kanál choledochoskopu je příliš malý a nejsou k dispozici vhodná akcesoria.
Ze zobrazovacích metod bývá standardně prováděn UZ břicha, při nejasném nálezu i po použití předešlých metod zobrazujeme pomocí CT břicha. Výhodné je provést CT angiografii, která častěji zobrazí zdroj i drobnějšího krvácení. Výjimečně je použito jiných zobrazení, např. MRCP nebo selektivní angiografie.
Cílem terapie je kromě zástavy krvácení i zprůchodnění žlučových cest. Jsou preferovány metody endoskopické, pokud je zdroj krvácení pro endoskop dostupný, anebo techniky radiointervenční, nejčastěji selektivní angiografie s embolizací zdroje krvácení.
Operační řešení je indikováno v případě chirurgicky řešitelného zdroje krvácení, např. u cholecystitidy, nebo resekabilních tumorů nebo i jinými způsoby neřešitelného hemodynamicky závažného krvácení. Pacientů vyžadujících chirurgickou revizi je v současnosti menšina. Dle příčiny krvácení je prováděna cholecystektomie, anatomické i neanatomické resekce jater, operace pooperačních pseudoaneurysmat [3,11,12].
KAZUISTIKA
68letá obézní kuřačka se známou cholecystolitiázou podstoupila na jiném pracovišti akutní ERCP s EPT (endoskopickou papilotomií), litotrypsí a extrakcí konkrementu pro choledocholitiázu. Ošetření se komplikovalo rozvojem pankreatitidy, jejíž léčení probíhalo konzervativně nejprve za hospitalizace, poté v domácím prostředí. Tři týdny po ERCP byla pacientka přijata akutně na naši kliniku pod obrazem akutní cholecystitidy. Vstupní laboratoř ukázala elevaci zánětlivých parametrů, bilirubinu a obstrukčních enzymů. Na ultrazvukovém vyšetření byla popsána mnohočetná cholecystolitiáza se známkami akutní cholecystitidy, bez dilatace žlučových cest. CT vyšetření břicha potvrdilo cholecystolitázu, akutní cholecystitidu charakteru hydropsu, přetrvávající edém pankreatu a v jeho okolí neohraničený, solidně - cystický útvar 10×11×5 cm suspektních nekrotických změn. U pacientky nebyly přítomny známky peritoneálního dráždění ani jiné projevy sepse, proto bylo postupováno konzervativně. Nemocné se zprvu ulevilo. Za čtyři dny od přijetí ale došlo k prudkému zhoršení stavu. Pacientka si stěžovala na kolikovité bolesti v epigastriu, následně začala zvracet krev. Na provedené urgentní gastroskopii bylo v D2 části duodena viditelné adherující koagulum, zpod kterého vytékala intermitentně čerstvá krev. Vzhledem k lokalitě jsme měli podezření, že se jedná o komplikaci po předchozím ERCP, a indikovali jsme nové ERCP. Vyšetření ukázalo dilataci dc. choledochus s defekty v náplni kontrastem, košíčkem se podařilo evakuovat koagula a zavést zajišťovací stent. V dalších dnech ale u nemocné progredovala anemie a po přechodném snížení došlo opět k elevaci obstrukčních enzymů. Kontrolním CT vyšetřením se opět nezobrazil jasný zdroj krvácení. Rentgenolog při porovnání obrazů CT provedeného po přijetí a aktuálního vyšetření poukázal na změnu charakteru obsahu ve žlučníku a vyslovil domněnku, že by se mohlo jednat o hemoragickou cholecystitidu (Obr. 1). Dalším ERCP (Obr. 2) byl opět nalezen dc. choledochus vyplněný koaguly, ale oproti předchozímu vyšetření po jejich extrakci dále mírně přitékala další krev ze žlučových cest. Dříve zavedený drén vycestoval do tenkého střeva. Provedli jsme přímou choledochoskopii, během které bylo vyloučeno přímé poranění nebo jiný zdroj krvácení z oblasti dc. choledochus, junkce i částí dc. hepaticus dx. a sin. Krev přitékala z místa předpokládaného ústí dc. cysticus. Endoskopicky nebylo možné dc. cysticus nasondovat ani krvácení jinak ošetřit. Po opětovném zajištění žlučových cest novým stentem byla pacientka indikována k operační revizi. Operace potvrdila těžkou akutní cholecystitidu v terénu změn při akutní pankreatitidě. Cholecystektomie byla technicky náročná pro rozsáhlé zánětlivé změny, k orientaci o průběhu dc. choledochus napomohl zavedený stent. Lumen žlučníku obsahovalo zbytková koagula, na sliznici byly patrné těžké zánětlivé změny (Obr. 3). Po provedení cholecystektomie byl vyhledán a z enterotomie odstraněn vycestovaný drén zavedený při druhém ERCP (Obr. 4−5). Pooperační průběh probíhal bez pozoruhodností. Histologické vyšetření potvrdilo akutní ulceroflegmonózní cholecystitidu.
Image 1. (a−d): CT obrazy pacientky po příjmu (vlevo) a po epizodě hemobilie (vpravo)
Na časnějším vyšetření je patrný konkrement vyplňující Hartmannovu kapsu (žlutá šipka) a obsah žlučníku charakteru hydropsu (oranžová šipka). Na kontrolním snímku se poloha konkrementů změnila (žlutá šipka) a obsah ve žlučníku je více denzní, nehomogenní (oranžová šipka), což naznačuje možnost přítomnosti koagul.
Fig.1 (a−d): CT scan of the patient at the time of admission (left) and after the hemorrhagic episode (right)
The picture taken earlier shows a stone filling the Hartmann pouch (yellow arrow) and the content of the bladder which seems to be hydropic (orange arrow). In the later picture, the stones moved (yellow arrow) and the content of the bladder is denser, non-homogeneous (orange arrow), indicating the possible presence of blood clots.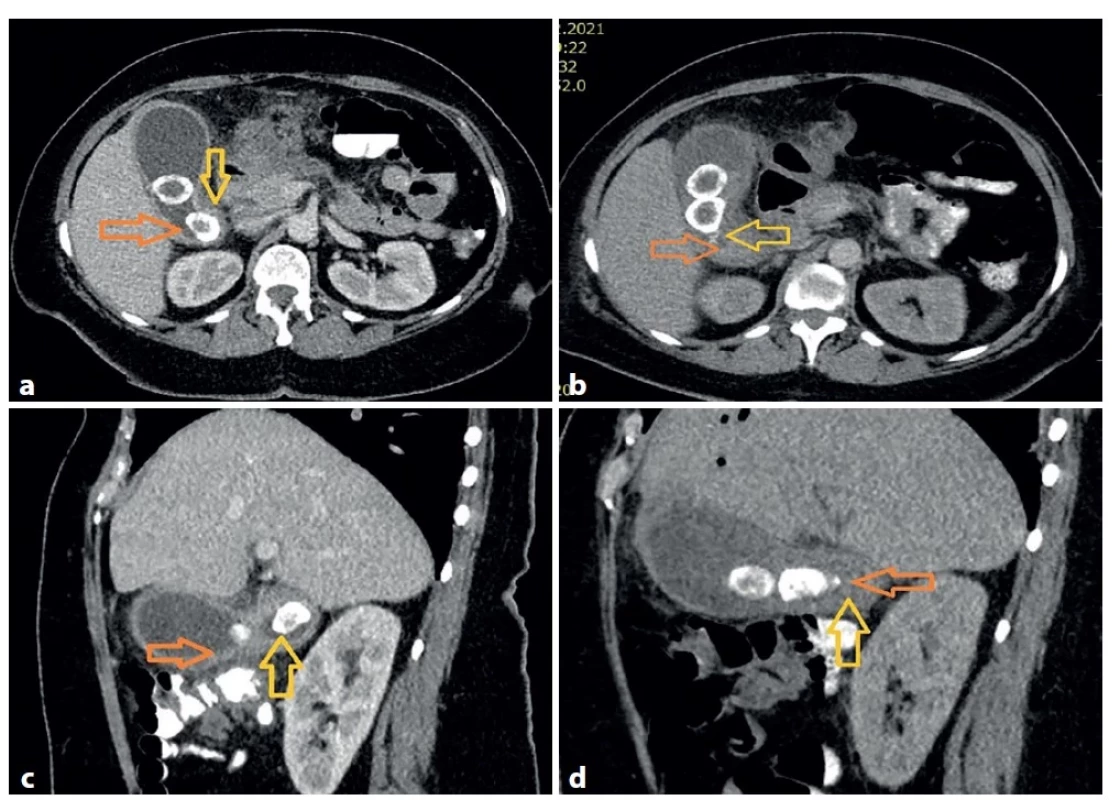
Image 2. ERCP zobrazující dilataci dc. choledochus (modrá šipka), dva objemné konkrementy ve žlučníku (žlutá šipka)
Fig. 2: ERCP showing the dilatation of the common bile duct (blue arrow) and two massive stones in the bladder (yellow arrow)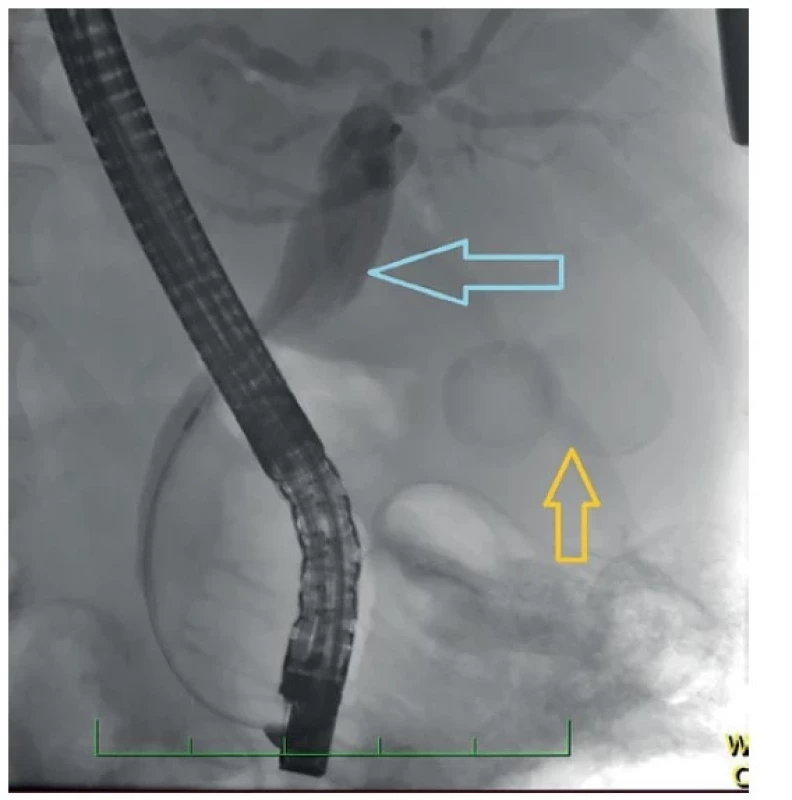
Image 3. Peroperační snímek − rozstřižený žlučník se ztluštělou stěnou a sliznicí s ulceracemi
Fig. 3. Perioperative picture − the opened gallbladder with wall thickening and mucosal ulcers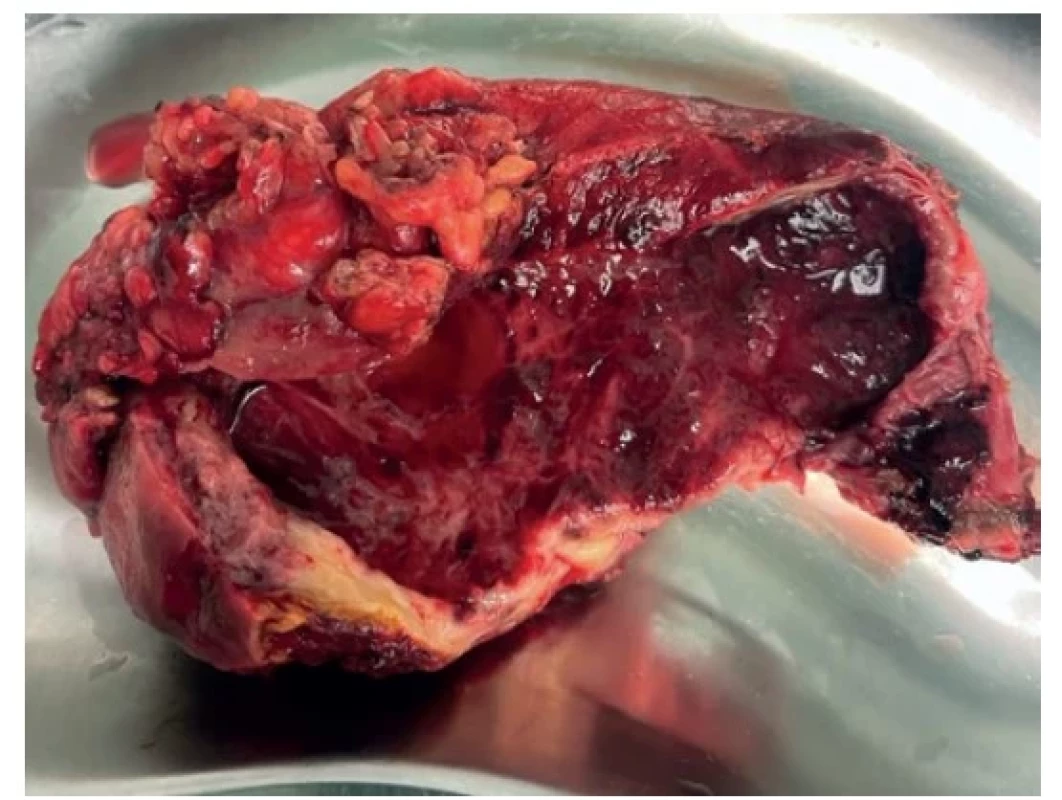
Image 4. (a−b) CT – drén vycestovaný z dc. choledochus do tenkého střeva (modrá šipka)
Fig. 4 (a−b) CT scan – the drain, moved from the common bile duct into the small bowel (blue arrow)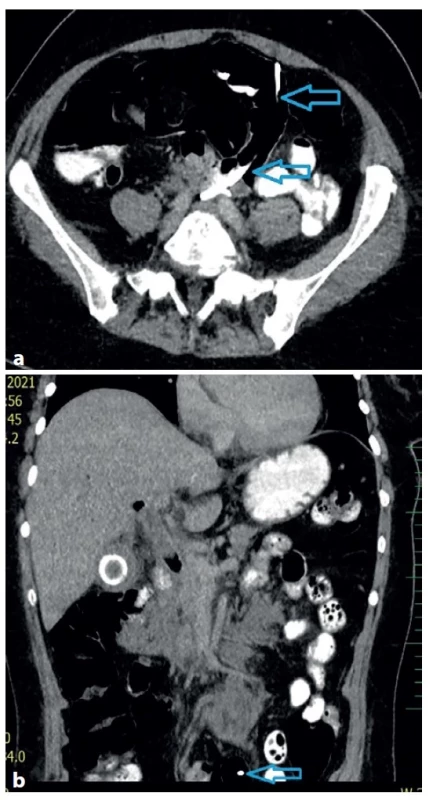
Image 5. Dislokovaný drén vyhledán a odstraněn peroperačně z enterotomie
Fig.5: Localization and removal of the dislocated drain by enterotomy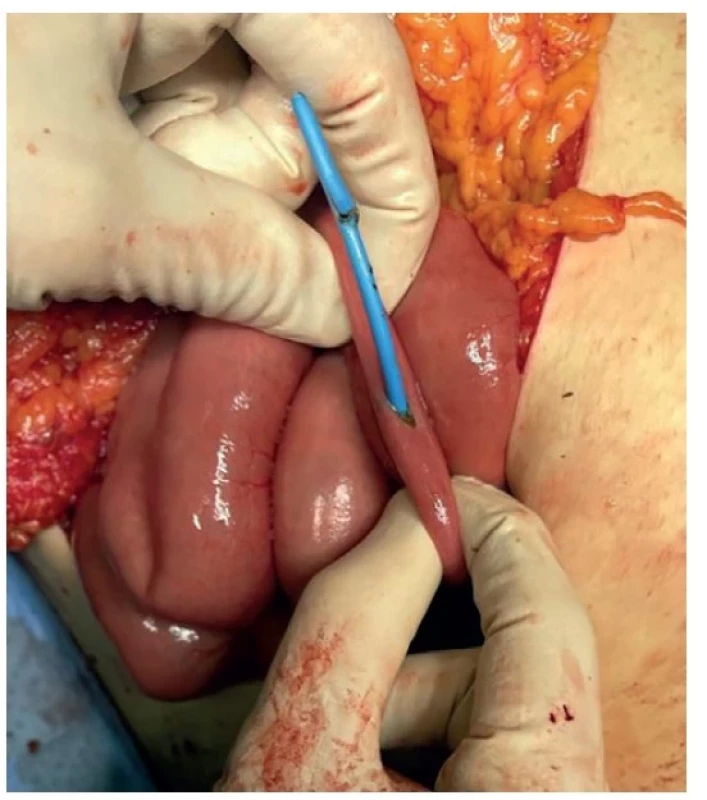
DISKUZE
Důvodem přijetí pacientky na naše pracoviště byla akutní cholecystitida. Nebylo možné určit přesný počátek obtíží, chyběla detailní data o předchozí hospitalizaci na jiném pracovišti a na vstupním CT byly stále patrné zánětlivé změny pankreatu, což nás vedlo k rozhodnutí postupovat konzervativně, jelikož provedení cholecystektomie se jevilo technicky obtížné a rizikové. Když se u pacientky objevila hemateméza a zhoršení bolestí břicha, ikterus ještě nebyl klinicky vyjádřen. V dif. dg. zdroje hemoragie byl zvažován stresový vřed a krvácení z papilotomie po předchozím ERCP. Při následných endoskopických vyšetřeních byla vředová léze vyloučena a aktivní krvácení jsme již nezachytili. Krevní ztráta nebyla natolik významná, aby způsobila hemodynamickou odezvu, ale při opakování krvácení došlo v řádu dní k anemizaci, recidivovala obstrukce žlučových cest, pojistný stent ze žlučových cest dokonce vycestoval do tenkého střeva. Ani opakováním endoskopií či CT jsme nedosáhli zobrazení zdroje krvácení. K tomu dopomohlo až následné provedení přímé choledoskopie, které lokalizovalo krvácení do oblasti dc. cysticus, resp. žlučníku samotného, druhé čtení a porovnání vstupního a kontrolního CT upozornilo na posun objemných konkrementů. Obsah žlučníku na novém CT budil dojem, že se jedná o krev. Teprve tato komplexní série moderních vyšetření nás navedla na domněnku, že zdrojem hemobilie může být vzácná hemoragická cholecystitida a nejedná se o komplikaci ERCP.
ZÁVĚR
Objasnit zdroj hemobilie může být diagnostickým oříškem. Je třeba znát i méně časté příčiny krvácení do žlučových cest, věnovat pozornost drobným změnám v klinickém stavu a paraklinických nálezech. U pacientky se ukázalo přínosné použití přímé cholechoskopie. Je jistým paradoxem, že série vyšetření s využitím nejmodernějších technologií vedla k nutnosti otevřené cholecystektomie, chirurgické technice známé již více než 130 let.
Seznam zkratek:
ERCP – endoskopická retrográdní cholangiopankreatografie
MRCP – cholangiopankreatografie pomocí magnetické rezonance
PTC/ PTD – perkutánní transhepatická cholangiografie, perkutánní transhepatická drenáž
EPT – endoskopická papilosfinkterotomie
Autoři článku děkují za spolupráci MUDr. Radce Havlové z Kliniky zobrazovacích metod FN Motol.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
MUDr. Markéta Bocková
V Úvalu 84
150 06 Praha 5
e-mail: Marketa.Bockova@fnmotol.cz
ORCID ID: 0000-0002-0296-5944
Sources
1. Zhornitskiy A, Berry R, Han JY, et al. Hemobilia: Historical overview, clinical update, and current practices. Liver Int. 2019;39(8):1378−1388. doi: 10.1111/ liv.14111.
2. Šiller J, Havlíček K, Turnovský P, et al. Hemobilie, vzácná příčina krvácení do GIT. Rozhl Chir. 2008;87(2):89−91.
3. Murugesan SD, Sathyanesan J, Lakshmanan A, et al. Massive hemobilia: a diagnostic and therapeutic challenge. World J Surg. 2014;38(7):1755-62. doi: 10.1007/s00268-013-2435-5.
4. Chang CHW, Wu YH, Liu HL. Upper gastrointestinal bleeding with hemobilia caused by gallstones. J Emerg Med. 2020;58(5): e227-e229. doi: 10.1016/j. jemermed.2020.03.035.
5. Kim YCH, Park MS, Chung YE, et al. Gallstone spillage caused by spontaneously perforated hemorrhagic cholecystitis. World J Gastroenterol. 2007;13(41):5525−5526. doi: 10.3748/ wjg.v13.i41.5525.
6. Green MH, Duell RM, Johnson CD, et al. Haemobilia. Br J Surg. 2001;88(6):773−786. doi: 10.1046/j.1365 - 2168.2001.01756.x.
7. Chin, MW, Enns R. Hemobilia. Curr Gastroenterol Rep. 2010;12 : 121–129. doi: 10.1007/s11894-010-0092-5.
8. Johnson KD, Perisetti A, Tharian B, et al. Endoscopic retrograde cholangiopancreatography - related complications and their management strategies: A „scoping“ literature review. Dig Dis Sci. 2020;65(2):361−375. doi: 10.1007/ s10620-019-05970-3.
9. Berry R, Han J, Girotra M, et al. Hemobilia: Perspective and role of the advanced endoscopist. Gastroenterol Res Pract. 2018;12;3670739. doi: 10.1155/2018/3670739.
10. Szary NM, Al-Kawas AH. Complications of endoscopic retrograde cholangiopancreatography: How to avoid and manage them. Gastroenterol Hepatol (NY). 2013; 9(8):496–504.
11. Vyhnánek F. Současný postup u poranění jater. Úraz chir. 2012;20(2):1−7.
12. Hoch J. An unusual combination of hemobilia and hemoperitoneum. Rozhl Chir. 1990;69(3):132−134.
13. Boston Scientific. SpyGlass™ DS Direct Visualization System [on line]. c2022 [cit. 2022-08-15]. Available at: https://www. bostonscientific.com/en-IN/products/ direct-visualization-systems/spyglass-direct - visualization-system.html.
14. Chen YK, Pleskow KD. SpyGlass single-operator peroral cholangiopancreatoscopy system for the diagnosis and therapy of bile-duct disorders. Gastrointest Endosc. 2007;65(6):832−841. doi: 10.1016/j. gie.2007.01.025.
15. Urban O, Arnelo U, Kliment M, et al. Cholangiopankreatoskopie pomocí Spy - GlassTM direct visualization system. Gastroent Hepatol. 2013;67(2):124−126.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2023 Issue 2-
All articles in this issue
- Editorial
- Maisonneuveova zlomenina hlezna
- Náhlé příhody břišní v onkochirurgii
- Postavení chirurgické léčby v rámci step-up managementu těžké akutní pankreatitidy
- Akutní hemoragická cholecystitida jako vzácná příčina hemobilie
- Adenokarcinom tenkého střeva asociovaný s Crohnovou chorobou
- Borreliový pseudolymfom obočí u dospělého pacienta
- Aktuální kontroverze v léčbě varixů dolních končetin a jejich komplikací
- Zápis z jednání Redakční rady časopisu Rozhledy v chirurgii, konané online dne 23. 2. 2023.
- Čerstvý tepenný allograft jako náhrada infikované protézy v oblasti arteria femoralis communis a recidivujícího pseudoaneurysmatu
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Maisonneuveova zlomenina hlezna
- Náhlé příhody břišní v onkochirurgii
- Postavení chirurgické léčby v rámci step-up managementu těžké akutní pankreatitidy
- Čerstvý tepenný allograft jako náhrada infikované protézy v oblasti arteria femoralis communis a recidivujícího pseudoaneurysmatu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

