-
Medical journals
- Career
Ruptura aneuryzmatu dolní pankreatikoduodenální tepny jako příčina hemoperitonea – kazuistika a review literatury
Authors: P. Skalický 1; M. Loveček 1; Dušan Klos 1; Č. Neoral 1; V. Prášil 2; L. Starý 3; K. Knápková 3; J. Tesaříková 3
Authors‘ workplace: 1. chirurgická klinika Fakultní nemocnice Olomouc 1; Radiologická klinika Fakultní nemocnice Olomouc 2; 1. chirurgická klinika Lékařské fakulty Univerzity Palackého, Olomouc 3
Published in: Rozhl. Chir., 2021, roč. 100, č. 1, s. 32-36.
Category: Case Report
doi: https://doi.org/10.33699/PIS.2021.100.1.32–36Overview
Úvod: Výdutě tepen pankreatikoduodenální arkády (PDA) tvoří přibližně 2 % všech aneuryzmat viscerálních tepen. Navzdory nízké incidenci je tato skupina výdutí klinicky významná vzhledem k vysokému riziku jejich ruptury.
Kazuistika: Prezentujeme případ 45letého pacienta, u kterého se jednalo o kombinaci ruptury výdutě PDA s těsnou stenózou odstupu truncus coeliacus (TC). Retrográdní krevní tok z horní mezenterické tepny (AMS) do hepatické tepny (AH) přes PDA limitoval možnosti terapie s ohledem na potřebu zachování perfuze jater. Pacient byl indikován k radiologickému intervenčnímu ošetření, které spočívalo v perkutánní transluminální angioplastice (PTA) se zavedením stentu do kmene TC a následně provedení transarteriální embolizace (TAE) − trappingu aneuryzmatu pomocí coilů. Vzhledem ke klinickým známkám nitrobřišního compartment syndromu byla do 24 hodin po radiologickém ošetření indikována laparotomie. Při ní již nebyly zjištěny známky aktivního krvácení, byla evakuována koagula z dutiny břišní v množství 800 ml a založena laparostomie s dočasným uzávěrem pomocí síťky. Definitivní uzávěr dutiny břišní byl proveden 20. pooperační den od původního výkonu. Kontrolní CT břicha u prezentovaného pacienta provedené 22 měsíců po TAE je bez známek recidivy výdutě.
Závěr: Ruptura představuje závažnou náhlou příhodu břišní vyžadující urgentní řešení. Preferovaným přístupem ošetření ruptury aneuryzmatu PDA je endovaskulární řešení pomocí TAE, které je spojeno s nižší morbiditou a mortalitou než ošetření chirurgické. Současná přítomnost stenózy TC vyžaduje rozvahu o zachování dostatečné perfuze v jeho povodí po TAE výdutě PDA, která do té doby plní funkci kolaterálního oběhu do jater. Rozhodnutí o volbě léčebného postupu u konkrétního pacienta je individuální s přihlédnutím k výše uvedeným doporučením.
Klíčová slova:
aneuryzma pankreatikoduodenální tepny – ruptura – stenóza truncus coeliacus
Úvod
Pankreatikoduodenální arkáda je tvořená větvemi horní pankreatikoduodenální tepny, která odstupuje z gastroduodenální tepny, a větvemi dolní pankreatikoduodenální tepny, která je zásobena z AMS. Výdutě těchto arterií tvoří přibližně 2 % všech aneuryzmat viscerálních tepen [1]. Navzdory nízké incidenci je tato skupina výdutí klinicky významná vzhledem k vysokému riziku jejich ruptury, které je v literatuře uváděno až u 65 % pacientů, mortalita spojená s rupturou výdutě dosahuje prakticky 50 % [2,3].
Ruptura aneuryzmatu PDA většinou vede ke krvácení do retroperitoneálního prostoru, méně často do zažívacího traktu. V některých případech symptomy spojené s krvácením imitují gastroduodenální, biliární nebo pankreatické onemocnění, a ztěžují tak rychlou diagnostiku a léčbu [4,5,6].
Možnosti terapie ruptury výdutě PDA jsou endovaskulární léčba, otevřený chirurgický přístup nebo jejich kombinace. Při endovaskulárním přístupu je nejčastěji provedena embolizace coily nebo implantace stentgraftu, která aneuryzma exkluduje z krevního oběhu. Tato terapie je spojena s nižší mortalitou než chirurgická léčba a uplatňuje zkušenosti z řešení krvácivých komplikací v pankreatické chirurgii [7,8].
Kazuistika prezentuje pacienta, u kterého se jednalo o kombinaci ruptury výdutě PDA s těsnou stenózou odstupu TC a retrográdním krevním tokem z AMS do AH přes PDA, čímž byly limitovány možnosti terapie s ohledem na potřebu zachování perfuze jater.
Kazuistika
Muž, 45 let, bez anamnézy traumatu, byl vyšetřen v říjnu 2018 na urgentním příjmu spádové okresní nemocnice pro 3 dny trvající difuzní bolesti břicha, bolesti na hrudi, zvracení a průjmy. Klinické vyšetření zjistilo maximum palpační bolestivosti v oblasti pupku, bez přítomnosti známek peritoneálního dráždění. Laboratorně byla přítomná hyperamylazemie (3,95 µkat/l), parametry krevního obrazu (hemoglobin 160 g/l, leukocyty 9,5×109/l) i koagulace byly v normě. Ultrazvukové vyšetření břicha diagnostikovalo volnou tekutinu v dutině břišní, následné CT břicha s kontrastem potom retroperitoneální hematom a hemoperitoneum. Jednoznačný zdroj krvácení nebyl patrný, byla suspekce na krvácení z oblasti duodenojejunálního přechodu. Pacient byl indikován k akutní operační revizi. Peroperační nález odhalil objemný hematom retroperitonea zasahující k radixu mezenteria se sekundární rupturou listu peritonea v délce 10 cm a hemoperitoneem v objemu 1000 ml. Ruptura radixu mezenteria byla ošetřena suturou, současně byla provedena toileta a drenáž dutiny břišní. Pooperační průběh na JIP probíhal bez komplikací, pacient byl oběhově stabilní, bez nutnosti podání transfuzních přípravků. Po přeložení na standardní oddělení se 7. pooperační den jednorázově objevila v drénech hemoragická sekrece v množství 500 ml, laboratorně došlo k poklesu hemoglobinu na 68 g/l. U pacienta, který byl toho času kardiopulmonálně kompenzovaný, byl domluven překlad na vyšší pracoviště FN Olomouc. Po překladu bylo na CT angiografii zjištěno aneuryzma PDA bez známek aktivního krvácení, současně byl přítomen uzávěr odstupu TC (Obr. 1, 2). Pacient byl indikován k radiologickému intervenčnímu ošetření, které spočívalo v PTA se zavedením stentu do kmene TC a následně provedení TAE − trappingu aneuryzmatu pomocí coilů jak přístupem z AMS, tak z TC (Obr. 3, 4). Na kontrolní angiografii bylo aneuryzma vyřazeno z oběhu. Po výkonu byla ihned zahájena duální antiagregace. Během 24 hodin po intervenci došlo u pacienta k nárůstu intraabdominálního tlaku na 25 cm H20, rozvoji oběhové nestability s nutností podpory oběhu a respiračnímu selhání s nutností umělé plicní ventilace. Vzhledem ke klinickým známkám nitrobřišního compartment syndromu byl nemocný indikován k chirurgické revizi. Peroperačně byl zjištěn paralytický ileus s přítomností koagul v mezikličkovém prostoru v množství asi 800 ml, nebyly však známky aktivního krvácení. Po toiletě dutiny břišní byla vzhledem k abdominálnímu compartment syndromu založena laparostomie s dočasným uzávěrem pomocí síťky COM 30, výrobce VÚP. Definitivní uzávěr dutiny břišní byl proveden 20. pooperační den od původního výkonu. V dalším průběhu hospitalizace se již známky krvácení neobjevily, pacient byl přeložen na standardní oddělení a postupně realimentován. Kontrolní CT vyšetření potvrdilo příznivý nález bez známek reperfuze aneuryzmatu a průchodný stent v TC. Pacient byl propuštěn do domácí péče.
Image 1. CT břicha s kontrastem Patrné aneuryzma PDA (označeno šipkou) s rupturou a hemoperitoneem
Fig. 1: CT of the abdomen with contrast Visible is the PDA aneurysm (indicated by the arrow) with the rupture and haemoperitoneum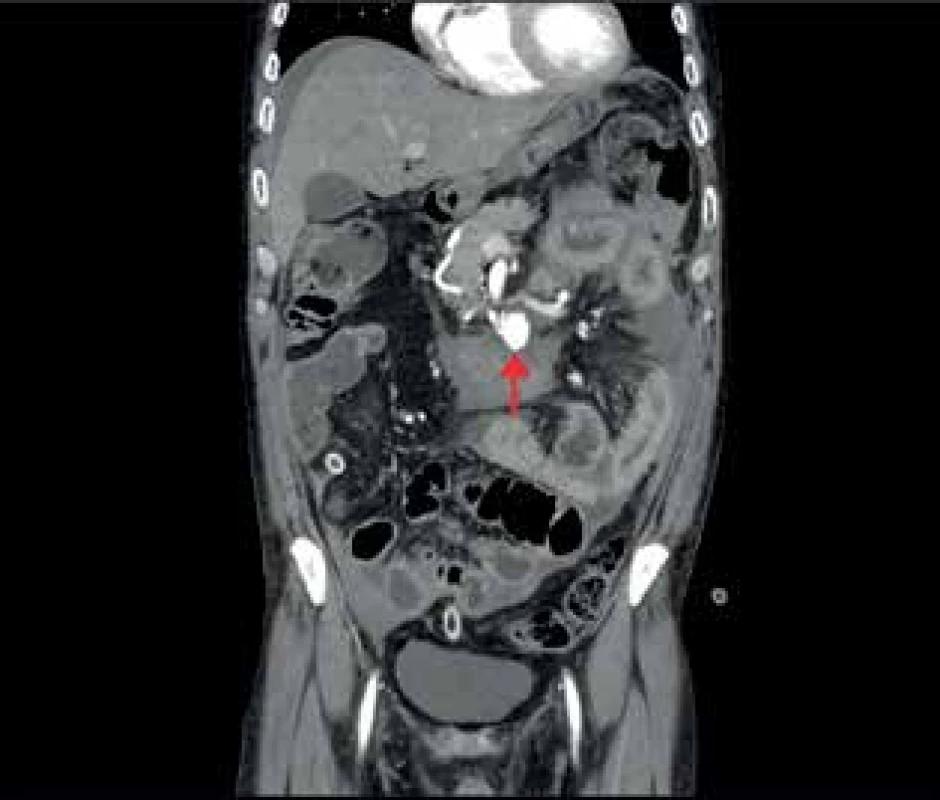
Image 2. CT angiografie s nálezem stenózy kmene TC u prezentovaného pacienta (označeno šipkou)
Fig. 2: CT angiography with the finding of TC stenosis in the presented patient (marked by the arrow)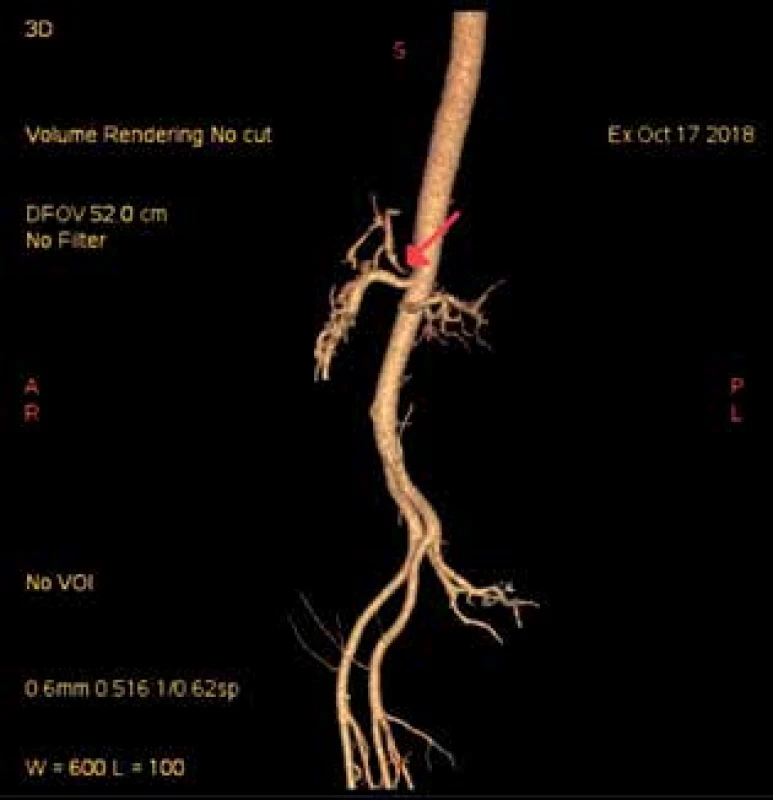
Image 3. Stav po transarteriální embolizaci aneuryzmatu PDA se zavedenými coily – snímky digitální subtrakční angiografie
Fig. 3: Condition after transarterial embolisation of the PDA aneurysma with deployed coils – images of digital subtraction angiography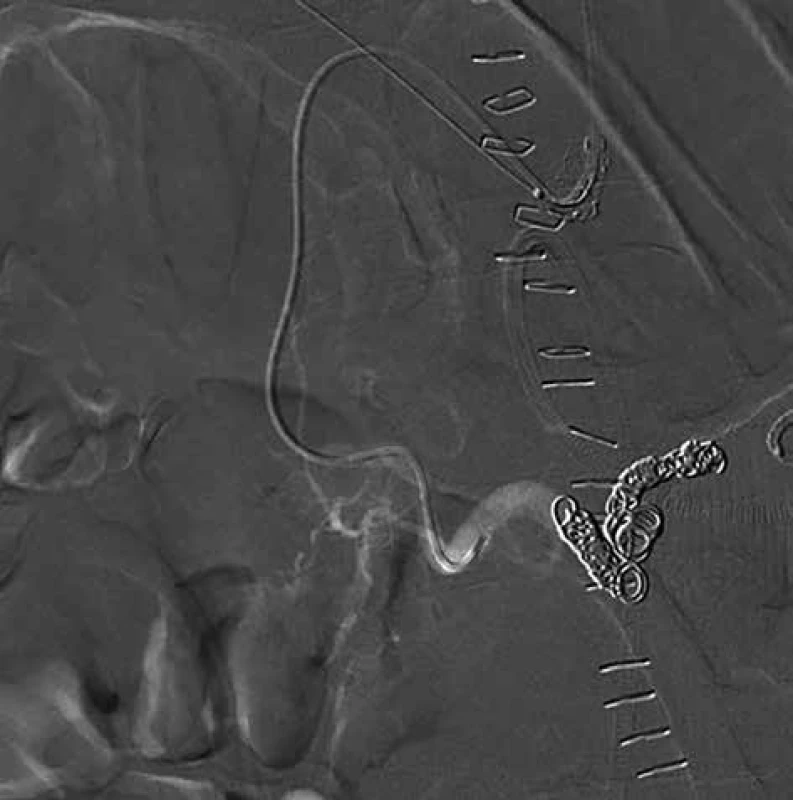
Image 4. PTA stenózy kmene TC se zavedením stentu – snímky digitální subtrakční angiografie
Fig. 4: PTA of the TC stenosis with the placed stent – images of digital subtraction angiography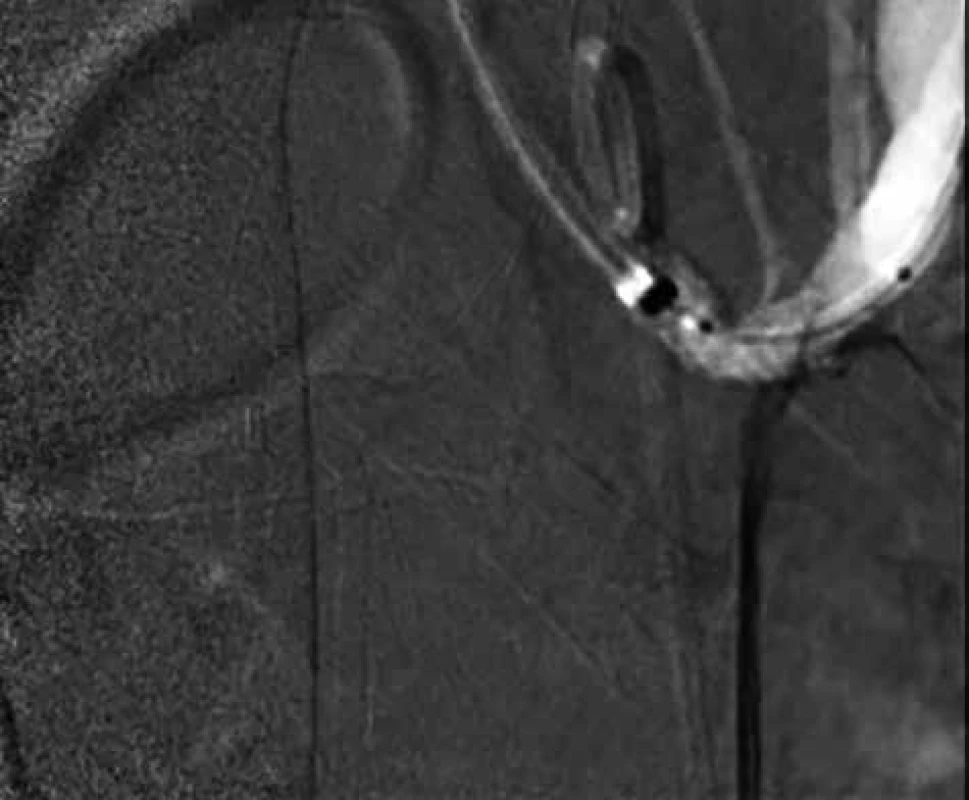
Diskuze
Aneuryzma PDA tvoří asi 2 % všech výdutí viscerálních tepen. Zatímco u pseudoaneuryzmatu je etiologie jeho vzniku spojována s infekcí, pankreatitidou, endoskopickým nebo chirurgickým traumatem [9], v případě pravého aneuryzmatu se jako jeden z etiologických faktorů jeví redistribuce krevního toku při stenóze TC [10]. Vysoký průtok a turbulentní proudění v tenkých větvích PDA vedou k poškození endotelu, vzniku erozí a jeho zvýšené permeabilitě. Tím dochází k ovlivnění hlubších vrstev cévní stěny, které jsou zodpovědné za integritu a elasticitu cév. Vzniklá dysfunkce vede k lokálnímu oslabení stěny cévy a vzniku aneuryzmatu [11]. Koincidence stenózy TC je dnes popisována u 50−80 % výdutí PDA [12], přičemž podkladem stenózy jsou nejčastěji aterosklerotické změny nebo zevní komprese způsobená ligamentum arcuatum medianum [10].
Na rozdíl od pseudoaneuryzmatu PDA, jehož častým příznakem je krvácení do zažívacího traktu, v případě ruptury pravého aneuryzmatu PDA je krvácení spojeno s rozvojem retroperitoneálního hematomu, případně intraperitoneálním krvácením. Základním symptomem proto bývá akutní bolest břicha, u většiny pacientů spojená s hypotenzí a rozvojem šoku. Retroperitoneální hematom může způsobit útlak duodena nebo rozvoj obstrukčního ikteru [2,13].
Základem diagnostiky ruptury aneuryzmatu PDA je CT kontrastní vyšetření břicha. V případě asymptomatických lézí bez ruptury je možné k detekci využít CT angiografii s 3D rekonstrukcí, případně kontrastní MR angiografii, které přinášejí vyšší senzitivitu a specificitu u výdutí menších než 1 cm a umožňují i přesné zhodnocení případných stenóz na TC a AMS [14].
Možnosti terapie ruptury výdutě PDA jsou endovaskulární léčba, otevřený chirurgický přístup nebo jejich kombinace. V review publikovaném Collem a spol. byla mortalita u operovaných pacientů 20 % ve srovnání s 0 % u pacientů řešených endovaskulárně [15]. Obdobně Morita a spol. uvádějí mortalitu u chirurgického přístupu 12,9 % ve srovnání s 2,1 % u endovaskulární terapie [16]. Techniky chirurgického řešení zahrnují opich větví zásobujících výduť, resekci aneuryzmatu nebo bypassové operace v případě plánovaného ošetření aneuryzmatu bez jeho ruptury. Limitující pro operační přístup je lokalita PDA, která je přístupná až po mobilizaci duodena a hlavy pankreatu z retroperitonea. Operační revize v takto anatomicky delikátní oblasti, navíc v terénu retroperitoneálního hematomu s aktivním krvácením, nemá často potenciál rychlejšího dosažení hemostázy ve srovnání s endovaskulární léčbou. Snaha o rychlé a „nouzové“ ošetření může být navíc spojena s rizikem poranění kmene AMS nebo vznikem pooperační pankreatické píštěle. Endovaskulární řešení tak v dnešní době představuje metodu volby v ošetření ruptury PDA. Zásadními podmínkami pro její úspěšné uplatnění je včasná diagnostika ruptury aneuryzmatu a dostupnost zkušeného radiointervenčního pracoviště. Urgentní chirurgický výkon zůstává vyhrazen pacientům, u kterých i přes podpůrnou terapii progreduje oběhová nestabilita a endovaskulární ošetření není možné provést.
U prezentovaného pacienta byla primární diagnostika a terapie provedena na spádovém okresním pracovišti. Vstupně provedené CT kontrastní vyšetření břicha prokázalo retroperitoneální hematom a hemoperitoneum s podezřením na zdroj krvácení v oblasti duodenojejunálního přechodu. Aneuryzma PDA nebylo jednoznačně patrné, důvodem byla patrně jeho menší velikost a použití standardního břišního CT protokolu. Ani operační revize v terénu rozsáhlého retroperitoneálního hematomu zdroj krvácení jednoznačně neobjasnila, byla provedena jen toileta a drenáž dutiny břišní. Při recidivě krvácení, ke které došlo 7. pooperační den po primárním výkonu, byl nemocný přeložen na vyšší pracoviště. Provedená CT angiografie již vedla k diagnostice výdutě PDA a uzávěru kmene TC. Pacient splňoval kritéria oběhové stability, a proto bylo zvoleno endovaskulární řešení. Vzhledem k vinutosti PDA v místě aneuryzmatu nebylo technicky možné místo přemostit implantací stentgraftu přístupem přes arteria pankreatikoduodenalis inferior. PDA byla současně kolaterálou zajišťující zásobení jater při uzávěru kmene TC. Zvolené řešení zahrnovalo PTA a zavedení stentu do TC a následně provedení trappingu aneuryzmatu pomocí coilů. Úspěšnost ošetření výdutě pomocí TAE je v literatuře udávána od 57 do 98 % [17,18,19]. Současná endovaskulární terapie stenózy TC spolu s TAE aneuryzmatu zůstává mezi autory kontroverzní. Zatímco někteří doporučují revaskularizaci z důvodu prevence rekurence výdutě a ischemie jaterní tkáně [20], další nevidí tuto intervenci jako klinicky relevantní [2,3,13,21,22,23]. Flood a kol. [24] publikovali sestavu vlastních 14 pacientů bez ošetření stenózy TC, u kterých v průběhu 4letého období sledování nedošlo k recidivě výdutě PDA.
U našeho pacienta došlo během 24 hodin po endovaskulárním ošetření k rozvoji břišního compartment syndromu a respirační insuficienci. Příčinou bylo hemoperitoneum spolu s paralytickým ileem, které bylo řešeno dekompresní laparotomií. Literárně nejobávanější komplikací po TAE je reperfuze aneuryzmatu s následným krvácením. Incidence závisí na technické úspěšnosti výkonu a je uváděna v 5−20 % případů [25]. Pacienti z tohoto důvodu vyžadují přísné radiologické sledování, které je doporučeno každých 6 měsíců v průběhu prvního roku a poté alespoň 1× ročně [14]. Dalšími komplikacemi jsou ischemie jater, pankreatu nebo duodena s možnou perforací nebo tvorbou abscesových ložisek [26]. Kontrolní CT břicha u prezentovaného pacienta provedené 22 měsíců po TAE je bez známek recidivy výdutě.
Závěr
Ruptura aneuryzmatu PDA představuje závažnou náhlou příhodu břišní vyžadující urgentní řešení. Preferovaným přístupem je endovaskulární řešení pomocí TAE, které je spojeno s nižší morbiditou a mortalitou než ošetření chirurgické. Prezentovaný případ ukazuje na úskalí časné diagnostiky, která je zcela zásadní pro rozhodnutí o strategii léčby. Současná přítomnost stenózy TC vyžaduje rozvahu o zachování dostatečné perfuze v jeho povodí po TAE výdutě PDA, která do té doby plní funkci kolaterálního oběhu do jater. Rozhodnutí o volbě léčebného postupu u konkrétního pacienta je individuální s přihlédnutím k výše uvedeným doporučením.
Podpořeno grantem DRO FNOL 00098892 (MEX 87-94).
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
MUDr. Jana Tesaříková
I. chirurgická klinika FNOL,
I. P. Pavlova 6
779 00 Olomouc
e-mail: jana.tesarikova@fnol.cz
Sources
- Paty PS, Cordero JA, Darling RC, et al. Aneurysms of the pancreaticoduodenal artery. J Vasc Surg. 1996;23 : 710−713. doi:10.1016/s0741-5214(96)80054-1.
- de Perrot M, Berney T, Deleaval J, et al. Management of true aneurysms of the pancreaticoduodenal arteries. Ann Surg. 1999;229(3):416–420. doi:10.1097/00000658-199903000-00016.
- Kallamadi R, de Moya MA, Kalva SP. Inferior pancreaticoduodenal arteryaneurysms in association with celiac stenosis/occlusion. Sem Intervent Radiol. 2009;26(3):215–223. doi.org/10.1055/s-0029-1225671.
- Buresta P, Freyrie A, Paragona O, et al. Ruptured pancreaticoduodenal artery aneurysm. A case report and review of the literature. J Cardiovasc Surg. 2004;45 : 153–157.
- Takeuchi H, Isobe Y, Hayashi M, et al. Ruptured pancreaticoduodenal artery aneurysm with acute gangrenous cholecystitis: a case report and review of the literature. Hepatogastroenterology 2004;51 : 368–371.
- Mihara Y, Kubota K, Nemoto T, et al. Successful treatment for rupture of pancreaticoduodenal artery aneurysm: two case reports. Hepatogastroenterology 2005;52 : 264–269.
- Murata S, Tajima H, Fukunaga T, et al. Management of pancreaticoduodenal artery aneurysms: results of superselective transcatheter embolization. AJR Am J Roentgenol. 2006;187 : 290−298. doi:10.2214/AJR.04.1726.
- Lovecek M, Havlik R, Köcher M, et al. Pseudoaneurysm of the gastroduodenal artery following pancreatoduodenectomy. Stenting for hemorrhage. Wideochir Inne Tech Maloinwazyjne 2014;9(2):297−301. doi:10.5114/wiitm.2011.38178.
- Tarazov PG, Ignashov AM, Pavlovskij AV, et al. Pancreaticoduodenal artery aneurysm associated with celiac axis stenosis: combined angiographic and surgical treatment. Digestive Diseases and Sciences 2001;46(6):1232–1235. doi:10.1155/2017/6989673.
- Katsura M, Gushimiyagi M, Takara H, et al. True aneurysm of the pancreaticoduodenal arteries: a single institution experience. Journal of Gastrointestinal Surgery 2010;14(9):1409–1413. doi:10.1007/s11605-010-1257-0.
- Lasheras JC. The biomechanics of arterial aneurysms. Annual Review of Fluid Mechanics 2007;39 : 293–319. doi:10.1146/annurev.fluid.39.050905.110128.
- Mano Y, Takehara Y, Sakaguchi T, et al. Hemodynamic assessment of celiaco-mesenteric anastomosis in patients with pancreaticoduodenal artery aneurysm concomitant with celiac artery occlusion using flow-sensitive four-dimensional magnetic resonance imaging. European Journal of Vascular and Endovascular Surgery 2013;46(3):321–328. doi:10.1016/j.ejvs.2013.06.011.
- Brocker JA, Maher JL, Smith RW, et al. True pancreaticoduodenal aneurysms with celiac stenosis or occlusion. Am J Surg. 2012;204 : 762–768. doi:10.1016/j.amjsurg.2012.03.001.
- Sgroi MD, Kabutey NK, Krishnam M, et al. Pancreaticoduodenal artery aneurysms secondary to median arcuate ligament syndromemay not need celiac artery revascularization or ligament release. Annals of Vascular Surgery 2015;29(1):122–122. doi:10.1016/j.avsg.2014.05.020.
- Coll DP, Ierardi RT, Kerstein MD, et al. Aneurysms of the pancreaticoduodenal arteries: a change in management. Ann Vasc Surg. 1998;22 : 286–291. doi:10.1007/s100169900155.
- Morita Y, Hasegawa T, Hanawa M. Transcatheter arterial embolization for the pancreaticoduodenal artery aneurysms. IVR Int Radiol. 1999;14 : 334–342. doi:10.1007/s00270-003-0032-y.
- Suzuki K, Yasushi T, Ito S, et al. Endovascular management of ruptured pancreaticoduodenal artery aneurysms associated with celiac axis stenosis. Cardiovasc Intervent Radiol. 2008;31 : 1082–1087. doi:10.1007/s00270-008-9343-3.
- Fankhauser GT, Stone WM, Naidu SG, et al. The minimally invasive management of visceral artery aneurysms and pseudoaneurysms. J Vasc Surg. 2011;53 : 966−970. doi:10.1016/j.jvs.2010.10.071.
- Tulsyan N, Kashyap VS, Greenberg RK, et al. The endovascular management of visceral artery aneurysms and pseudoaneurysms. J Vasc Surg. 2007;45 : 276−283. doi:10.1016/j.jvs.2006.10.049.
- Tien YW, Kao HL, Wang HP. Celiac artery stenting: a new strategy for patients with pancreaticoduodenal artery aneurysm associated with stenosis of the celiac artery. Journal of Gastroenterology 2004;39(1):81–85. doi:10.1007/s00535-003-1251-3.
- Stambo GW, Hallisey MJ, Gallagher JJ. Arteriographic embolization of visceral artery pseudoaneurysms. Annals of Vascular Surgery 1996;10(5):476–480. doi:10.1007/BF02000596.
- Lossing AG, Grosman H, Mustard RA, et al. Emergency embolization of a ruptured aneurysm of the pancreaticoduodenal arcade. Canadian Journal of Surgery 1995;38(4):363–365.
- Savastano S, Feltrin GP, Miotto D, et al. Embolization of ruptured aneurysm of the pancreaticoduodenal artery secondary to long-standing stenosis of the celiac axis: case reports. Vascular and Endovascular Surgery 1995;29(4):309–314. doi:10.1177/153857449502900409.
- Flood K, Nicholson AA. Inferior pancreaticoduodenal artery aneurysms associated with occlusive lesions of the celiac axis: diagnosis, treatment options, outcomes, and review of the literature. Cardiovasc Intervent Radiol. 2013;36 : 578–587. doi:10.1007/s00270-012-0473-2.
- Sachdev-Ost S. Visceral artery aneurysms: review of current management options. Mount Sinai Journal of Medicine 2010;77(3):296–303. doi:10.1002/msj.20181.
- Izumi M, Rju M, Cho A, et al. Ruptured pancreaticoduodenal artery aneurysm treated by superselective transcatheter arterial embolization and preserving vascularity of pancreticoduodenal arcades. Journal of Hepato-Biliary-Pancreatic Surgery 2004;11(2):145–148. doi:10.1007/s00534-003-0859-2.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2021 Issue 1-
All articles in this issue
- Nebezpečí bakteriální translokace pro chirurgického pacienta
- Gigantické nitrobřišní tumory – zkušenosti jednoho centra
- Souběžné onemocnění štítné žlázy u pacientů operovaných pro primární hyperparatyreózu
- Chirurgia štítnej žľazy u detí: naše skúsenosti
- Endometrióza v jazve po cisárskom reze: naše recentné skúsenosti
- Ruptura aneuryzmatu dolní pankreatikoduodenální tepny jako příčina hemoperitonea – kazuistika a review literatury
- Plynová embolie po výplachu incize periproktálního abscesu peroxidem vodíku − kazuistika Měl by být peroxid vodíku v chirurgii nadále využíván?
- 100. výročí založení odborného časopisu Rozhledy v chirurgii
- 140. výročí zahájení výuky chirurgie v českém jazyce na I. chirurgické klinice v Praze
- Zápis z jednání Redakční rady časopisu Rozhledy v chirurgii, konané dne 15. 12. 2020
- Poznámka k recenzím příspěvků zaslaných redakci Rozhledů v chirurgii
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Endometrióza v jazve po cisárskom reze: naše recentné skúsenosti
- Plynová embolie po výplachu incize periproktálního abscesu peroxidem vodíku − kazuistika Měl by být peroxid vodíku v chirurgii nadále využíván?
- Nebezpečí bakteriální translokace pro chirurgického pacienta
- Chirurgia štítnej žľazy u detí: naše skúsenosti
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

