-
Medical journals
- Career
Obstrukce tlustého střeva nádorem – co je prioritou léčby?
Authors: J. Hoch
Authors‘ workplace: Chirurgická klinika 2. lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Motol, Praha
Published in: Rozhl. Chir., 2019, roč. 98, č. 1, s. 4-9.
Category: Review
Overview
Obstrukce nádorem je důvodem více než poloviny všech neodkladných operací tlustého střeva. Výsledky léčby závisejí na typu a rozsahu operace, založení nebo vyloučení anastomózy, počtu operačních dob, dosažené radikalitě, případně modalitách léčby. Mortalita a morbidita mají příčinu v lokálních a systémových poruchách vyplývajících z obstrukce a z pooperačních komplikací, v případě jednodobých resekcí především z poruch anastomózy. Taktika a technika řešení neprůchodnosti se mění. Ze snahy o onkologickou radikalitu vyplývá otázka, jaká je priorita léčby těchto stavů. K odpovědi byly revidovány aktuální práce se závěrem, že prioritou je vyřešit obstrukci a teprve na dalším místě, pokud to je možné, odstranit její příčinu.
Klíčová slova:
tlusté střevo – nádorová obstrukce – volba postupu – volba operace – priority ošetření
Úvod
Mezi afekce tlustého střeva, které jsou příčinou akutních stavů a důvodem neodkladné léčby, patří obstrukce, perforace, zánět, cévní léze a krvácení. Pojmu akutní onemocnění se záměrně vyhýbám, protože akutním onemocněním je například zánět. Střevní neprůchodnost způsobená nádorem je komplikací nádoru, podobně jako peritonitida z perforace divertiklu je komplikací divertikulární choroby. Mezi zmíněnými afekcemi tlustého střeva je obstrukce nádorem nejčastější a je důvodem více než poloviny všech neodkladných operací tlustého střeva. Podle údajů ESMO (European Society for Medical Oncology) se rozvojem obstrukce projeví 8 až 40 % kolorektálních karcinomů, podle lokalizace převažují nádory v levé polovině [1]. Komplikace, kterou je perforace nebo obstrukce střeva, je faktorem špatné prognózy.
Ošetření neprůchodnosti prošlo během dvou století a především během posledních desetiletí podstatným vývojem, který v mnoha ohledech změnil a dále mění taktiku a techniku řešení neprůchodnosti. Neošetřená obstrukce má fatální konec, ať orgánovým selháním, nebo peritonitidou z distenční perforace střeva. S ohledem na nádor jako příčinu stavu je třeba se ptát, jaký je hlavní cíl neodkladné operace a jaké jsou další momenty ošetření.
Historicky nejstarším řešením obstrukce je stomie. Prvenství zřejmě náleží profesoru Finemu, který v Ženevě roku 1779 založil transverzostomii 63leté ženě pro obstrukci způsobenou nádorem rekta. Se stejnou indikací provedl D. Pring v Bathu r. 1820 sigmoideostomii. Resekce střeva byly v té době ojedinělým a zpravidla neúspěšným výkonem. Úspěšná resekce střeva se v písemnictví přiznává Thierschovi, který operaci, dokonce v ileózním stavu, provedl r. 1843. Rozvoj anestezie ve druhé polovině 19. století umožnil operovat na střevě a především na rektu. Počet resekcí střeva byl nevelký, mortalita způsobená peritonitidou vysoká, kritickým momentem byla anastomóza, operační postupy směřovaly k jejímu vyloučení, pokud ne trvalému, pak alespoň k odsunutí na co nejvzdálenější údobí. Obava ze selhání anastomózy vedla k resekcím střeva ve více dobách, postup byl trojdobý: v prvé době stomie, v další resekce postiženého úseku a v poslední uzávěr stomie. I resekční výkony končily v prvé době vytvořením stomií v různých modifikacích, jak je navrhli Billroth, Gussenbauer, Martin, Schede, Czerny, Heineke, Weir, Hartmann a Mikulicz. Postup s resekcí postiženého úseku, stomií na orální straně a slepým uzávěrem nebo mukózní píštělí na straně aborální, známý pod eponymy obou posledně uvedených, je platnou alternativou i v současnosti. Vyloučit stomii a resekovat v jedné době propagoval až v roce 1941 Smithwick a o dva roky později, v roce 1943, Dixon.
Ještě naléhavěji směřovalo k co nejmenším výkonům ošetření akutních stavů. Mortalita při ileu tlustého střeva ještě v roce 1940 přesahovala 40 %. Výrazného zlepšení výsledků léčby se podařilo některým chirurgům dosáhnout jednodobou resekcí, dokonce v ileózním stavu. Prvním, kdo tak postupoval, byl v roce 1931 von Haberer, který později v roce 1940 referoval o snížení úmrtnosti na 19 %. Následovali: Wangensteen (1949), Baronofski (1950), Wright (1951), Crile (1954), Goligher (1957) a další. Ani u nás se radikálnější postup neprosazoval příliš rychle. Např. v roce 1940 A. Jirásek napsal, že „resekci střevní při náhlé příhodě obturační nebude nikdo zkušený dobrovolně provádět, protože steh střevní je nejistý pro nečekaně vysoko sahající změny střevní nad překážkou“. Významně pokrokový byl o desetiletí později názor Kosteleckého a v šedesátých letech Michněvičův. Jednodobé řešení akutních stavů propagovali u nás později Vlasák s Urbanem, potom Vlasák, Faltýn a Třebický a krátce poté Antoš a Hoch [2]. Subtotální kolektomie jako další varianta akutního řešení byla v českém chirurgickém písemnictví zaznamenána poprvé v roce 1990 [3]. Od vydání Akutní chirurgie tlustého střeva [2], uvádějící nejen souhrn publikovaných názorů, jak efektivně tyto stavy řešit, ale také podrobná autorova doporučení, jak zajistit bezpečnost jednodobých výkonů, uplynula dvě desetiletí. Pokrok a zlepšení diagnostiky neodkladných stavů, perioperační intenzivní a resuscitační péče, operačních a také neoperačních přístupů v mnoha ohledech změnily možnosti a výsledky léčby i při obstrukci tlustého střeva nádorem.
Možnosti léčby závisejí na ovlivnitelných a neovlivnitelných faktorech. Neovlivnitelnými faktory jsou věk, komorbidity, pokročilost nádoru, přítomnost metastatického postižení a určitou měrou i poruchy homeostázy vyplývající z akutního stavu. Hodnocení výchozího nálezu záleží na chirurgické diagnostice, interním a anesteziologickém vyšetření včetně využití skórovacích systémů s odhadem únosnosti operace a interních rizik. Ovlivnitelná je předoperační příprava a perioperační péče a typ operace. Obstrukci může způsobit pouze pokročilý nádor. Ošetření nemocných s pokročilým nádorem směřuje od počátku k řešení obstrukce, když lokální nález, metastatické postižení nebo generalizace vylučují úvahu o odstranění nádoru. Očekávatelně odstranitelný nádor rozvahu mění. Vedle volby rozsahu operace a rozhodnutí, zda resekce a zda primárně s anastomózou, nebo bez a se stomií, případně zda kolektomie, je třeba zvažovat výhledově jiné možnosti léčby, onkologickou radikalitu atd. I k těmto otázkám je zaměřen další text.
Metody
Diagnostika
Stanovit diagnózu ileózního stavu je ve většině případů možné již z anamnézy a fyzikálního vyšetření, příčinu při nádoru konečníku vyšetřením per rectum. Nativní rentgenový (rtg) snímek je základním zobrazovacím vyšetřením, nemůže-li se vyšetřovaný postavit, snímek horizontálním paprskem. Vyšetření je průkazné asi v 60 % případů. Potvrzujícím nálezem jsou hladiny, hydroaerické rozhraní, podle jejichž distribuce lze odhadnout lokalizaci překážky, míru distenze střeva a tím i rizika distenční perforace. Současně se nativním snímkem potvrdí nebo vyloučí přítomné pneumoperitoneum. Ultrasonografické vyšetření je limitováno plynovou náplní a zkušeností vyšetřujícího. Při pochybnostech o povaze a příčině neprůchodnosti (včetně vyloučení pseudoobstrukce) je CT vyšetřením volby. CT vyšetření v akutním stavu vyřadilo akutně provedenou irrigografii. CT bez kontrastu může být podle některých doporučení prvým zobrazovacím vyšetřením, následované při nejasnosti kontrastním CT vyšetřením [4,5] (Obr. 1, 2). MRI se v této indikaci užívá jen výjimečně. Rtg sledovaná pasáž, resp. enteroklýza na rozdíl od tenkého střeva význam nemá. Endoskopické vyšetření – rektoskopie, sigmoideoskopie a koloskopie – může identifikovat překážku v rektu a v levé polovině tračníku a vyloučit pseudoobstrukci. Podmínkou užití uvedených diagnostických metod je neohrozit nemocného odkladem operace, zejména hrozí-li distenční perforace [6].
Image 1. a,b,c: CT nález. Ileózní stav při nádoru c. transversum
Fig. 1a,b,c: CT finding. Large bowel obstruction caused by tumor of transverse colon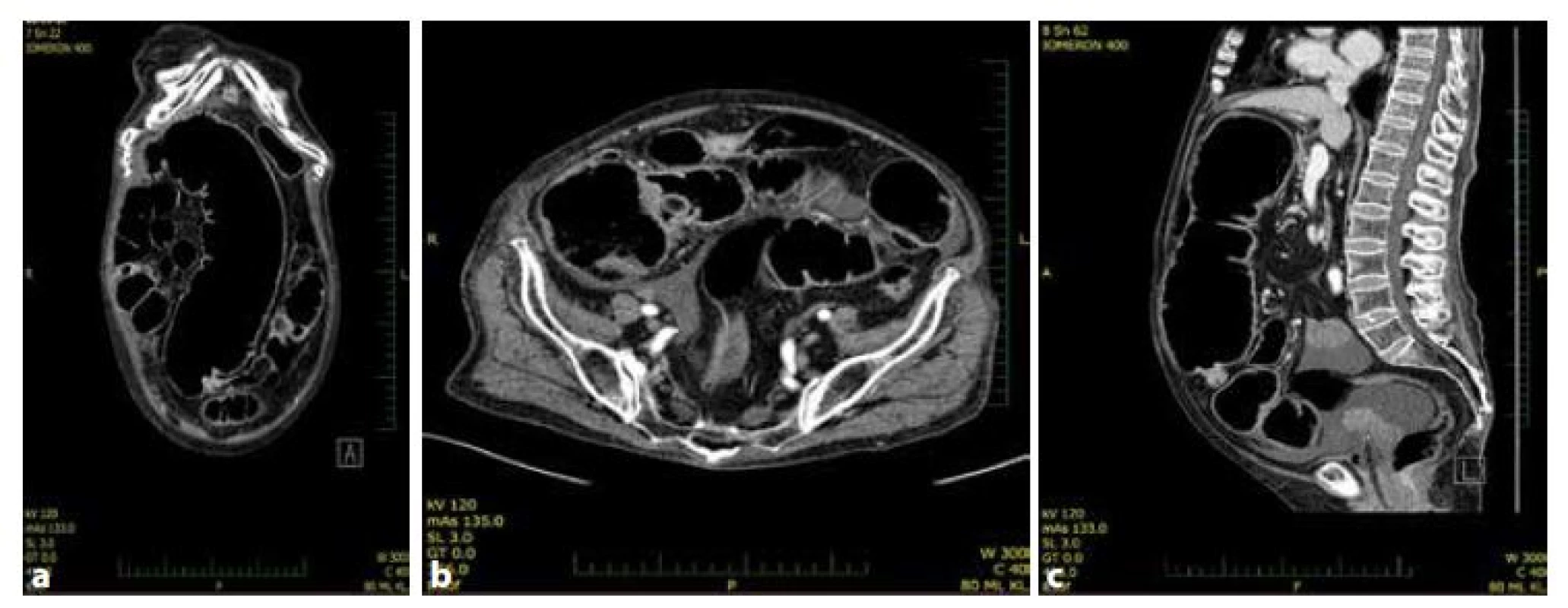
Image 2. a,b,c: CT nález. Vyšetření provedeno k ověření, že se jedná o ileus. Jeho příčinou byl stenotický nádor c. sigmoideum
Fig. 2a,b,c: CT finding. CT performed to verify obstruction. The obstruction resulted from stenotic sigmoid cancer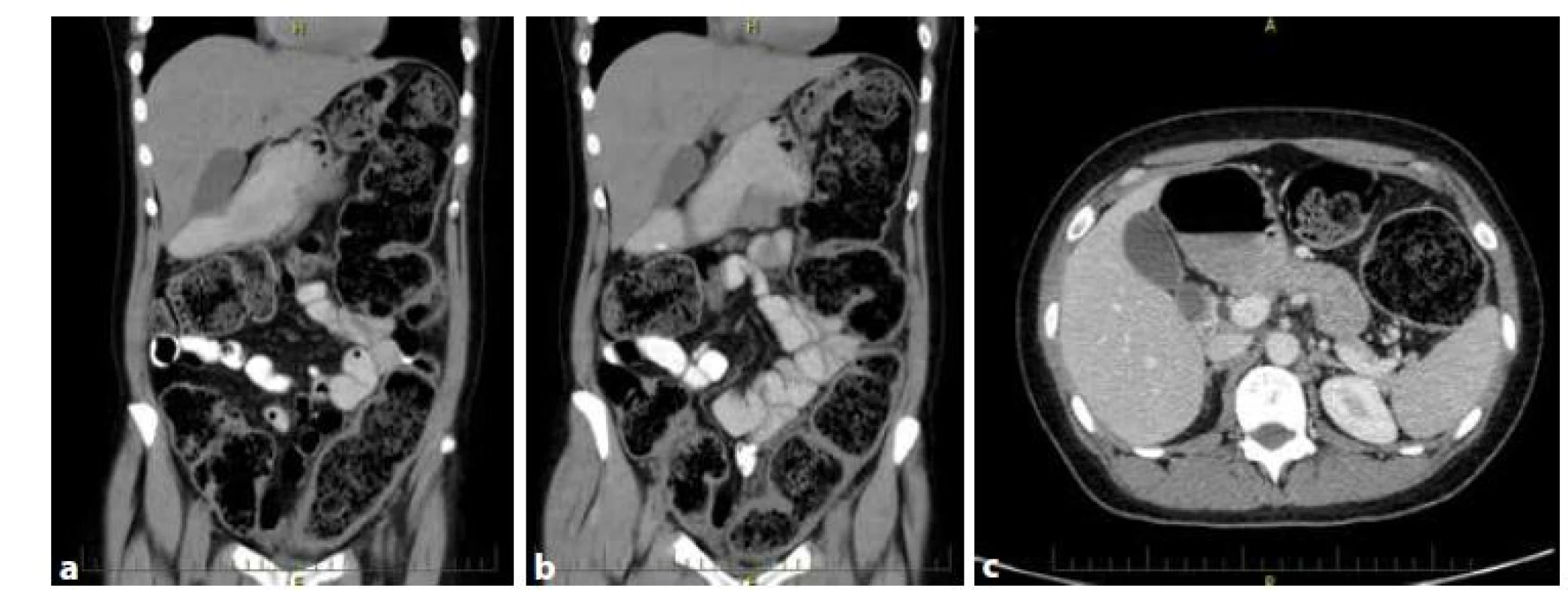
Resekční výkony
Resekce střeva s anastomózou – primární resekce – v prvé, resp. jedné době je definitivním chirurgickým řešením akutního stavu i afekce, která k němu vedla, splňuje tedy současně onkologický požadavek co nejčasnějšího odstranění nádoru. Přes riziko pooperačních komplikací mají primární resekce menší mortalitu než v případě vícedobého postupu, a to nejen po dokončení celého postupu, ale i jen výkonech prvé etapy. To prokázala již v minulosti řada studií uvádějících mortalitu mezi 6 a 19 %. Již před dvaceti lety bylo za další přínos postupu považováno zkrácení hospitalizace, která činila 11 až 22 dnů [2]. Podle naší zkušenosti činila doba hospitalizace po primárních resekcích operovaných pro obstrukci 14,8 dne. Příznivý výsledek primární resekce s anastomózou závisí kromě dokonalého technického zvládnutí výkonu také v rozvaze, kdy lze výkon provést bez nepřiměřeného rizika. Základními podmínkami resekce jsou resekabilní léze a nemocný, který snese rozsáhlejší výkon. Resekce je nevhodná při metastatickém postižení. Zakládat anastomózu není vhodné při sterkorální peritonitidě, při pochybnosti o vitalitě anastomózovaných střevních okrajů nebo při změnách způsobených zánětem nebo iradiací. Založení anastomózy je nevhodné také při rozsáhlé distenzi střeva nad překážkou nebo při stagnaci tuhé stolice nad či pod uvažovaným místem anastomózy. Dalšími důvody, proč se anastomóze vyhnout, jsou poruchy nutrice, oběhová instabilita, případně vysoký věk. Zatímco stagnující střevní obsah je operačně technickým problémem, který, nezpůsobil-li distenzí ischemii střevní stěny, lze vyřešit odsátím nebo „on-table“ laváží střeva [7], nutriční poruchu rychle sanovat nelze, stejně jako věk a s ním související komorbidity. Primární resekce teoreticky přináší prospěch starým nemocným vyloučením další operace, současně ale zvyšuje riziko, že případnou komplikaci nezvládnou.
Vedle segmentárních resekcí je jiným jednodobým výkonem subtotální kolektomie s distální ileokolickou anastomózou. Postup umožňuje omezit riziko kontaminace stagnujícím obsahem, aniž by bylo třeba se starat o dekompresi střeva nad překážkou, pomine vysoký stav bránice, uzávěr laparotomie je snadný, odstraní se eventuální synchronní léze a zmenší riziko vzniku lézí metachronních. V devadesátých letech se toto riziko udávalo v rozmezí 2–5 % [8], ve studii z r. 2013 byla další léze ve střevě potvrzena ve 3,4 % [9]. Nejpodstatnější indikací k subtotální kolektomii je překážka v levé polovině tračníku s hrozící nebo již přítomnou distenční perforací proximální části tračníku [4]. Hlavním záporem postupu je rozsah výkonu a vysoká frekvence stolic, těžko zvládaná fragilními nemocnými. I recentní údaje v písemnictví se shodují, že subtotální kolektomie snižuje riziko selhání anastomózy, zatímco mortalita se neliší proti nemocným, jimž byla provedena segmentární resekce [5]. Např. v citované sestavě tak bylo ošetřeno 15 nemocných, žádný neměl komplikaci anastomózy, přesto mortalita dosáhla 15,8 %, zatímco ve srovnávané sestavě byla mortalita segmentárních resekcí 13,3 %, průměrný věk zemřelých byl 83,3 roku [5]. Otázka, zda k ošetření obstrukce tlustého střeva při resekabilním nádoru je vhodnější segmentární resekce nebo subtotální kolektomie, zůstává nezodpovězena.
Další možností resekce v akutním stavu jsou operace dle Hartmanna nebo Mikulicze. Jejich společným záporem je, že k obnově střevní kontinuity se neobejdou bez další operace. Nepřehlédnutelné části operovaných stomií zůstanou navždy [10], hlavně pro nepřiměřeně vysoké operační riziko, přijatelné jen při operaci z vitální indikace.
Stomie a by-pasy
Vyřešení ileu založením střevní spojky je vyhrazeno jen pro obstrukci neodstranitelným nádorem zejména v pravé polovině tlustého střeva, stomie v akutním stavu jsou alternativou i u resekabilních nádorů. Zvládnutím ileu lze připravit podmínky k resekci střeva s nádorem k elektivní operaci dle onkochirurgických pravidel. Záporem postupu je potřeba další operace, pozdější odstranění nádoru, opakovaná hospitalizace a vyšší náklady, přínosem vytvoření podmínek pro plánovanou resekci při respektování všech onkochirurgických podmínek. Jen zdánlivě je shoda, že lepší výsledky poskytují resekce v první době než léčba ve více dobách [5,11,12,13,14,15]. Recentní americká metaanalýza hodnotící výsledky léčby levostranné obstrukce po resekci a po primárním založení stomie, v níž byly analyzovány údaje z 5 studií zahrnujících celkem 2424 pacientů, prokázala, že v 30denní mortalitě a morbiditě nebyl žádný rozdíl (OR=0,77; 95%CI 0,3–1,96 a OR=0,76; 95%CI 0,51–1,1), ale nemocným po kolostomii a následné elektivní resekci zůstala dlouhodobě méně často trvalá kolostomie (OR=0,17; 95%CI 0,11–0,26 a OR=0,22; 95%CI 0,11–0,46) [16]. Jiná studie dokládá bezpečnost postupu s 30denní mortalitou 5 % a průměrnou délkou hospitalizace 20 dnů, během níž byly provedeny oba výkony [9].
Rekanalizace, stenty
Léčba obstrukce zprůchodněním nádoru se odvíjí od dostupnosti vhodných instrumentů. Při ileu z nádoru v levé polovině, především na rektu a sigmoideu, se jako neoperační řešení nabízejí balonová dilatace, rekanalizace laserem [17] nebo zavedení stentu [18,19,20]. Úspěch se dá očekávat zejména tehdy, není-li obstrukce kompletní. K provedení je nezbytná koloskopie, podmínkou instrumentace je přehled v lumen a alespoň základní příprava střeva. Dalšími podmínkami jsou takto řešitelný nález a instrumentální a personální zajištění. Hlavním cílem je vyřešit akutní stav, vyhnout se akutní operaci a umožnit elektivní operaci po odpovídající přípravě [20,21,22]. Výpovědní je multicentrická studie z let 2005−2010, v pěti britských centrech bylo založeno 334 stentů, z nich 264 paliativně a 52 (15,6 %) jako „bridge to surgery“. Technicky se provedení obešlo bez příhod u 292 (87,4 %) nemocných a s komplikací u 46 (13,8 %) nemocných, nový stent byl nezbytný u 39 (14,8 %) nemocných stentovaných pro nádor paliativně a u 16 (6,1 %) z nich byla následně nutná kolostomie. Nejvýznamnějším prediktivním ukazatelem špatného výsledku bylo ASA≥3 (OR 0,43; P=0,04) [23]. Až 97% úspěch při zavedení stentu uvádí letošní japonská práce, a to včetně údajů o dlouhodobém sledování nemocných, pro které zůstal stent definitivním řešením [24], 75% úspěšnost rovněž letošní práce z Memorial Sloan Kettering Cancer Center při ošetření obstrukce střeva nádorem nevycházejícím ze střeva [25].
Timing operace
Důležitým momentem, který rozhoduje o výsledku léčby ileu, je včasnost ošetření. Ileózní stav je náhlou příhodou, a tak je třeba k němu přistupovat. V drtivé většině by ke stanovení diagnózy stačila anamnéza a řádné fyzikální vyšetření. Dostupnost, možnosti a kvalita soudobých zobrazovacích metod poskytují již před operací velmi dobrou představu o nálezu, operace tak mohou být cílenější a operujícího chirurga ušetří pochybností o povaze a lokalizaci překážky. Současně však vyšetření mají odvrácenou tvář. Operace jsou sice akutní a čas do operace umožní základní přípravu, rehydrataci atd., ale vyšetřováním vzrůstá riziko odkladu operace. O tom, že se nejedná o bezvýznamný moment léčby, vypovídá zpráva z American Hospital Association: pacienti operovaní po 5 dnech hospitalizace měli ve srovnání s operovanými ihned po přijetí vyšší mortalitu (6,1 % vs. 1,8 %, p<.001), více komplikací (15,4 % vs. 4,0 %; p<.001) a byli déle hospitalizováni (9 vs. 5 dnů, p<.001) [26].
Onkologická radikalita
Radikalita akutních operací by se neměla lišit od operací elektivních. Zatímco o bezpečné vzdálenosti resekčních okrajů od nádoru na tlustém střevě se nediskutuje a je obvykle dobře dosažitelná, předmětem pozornosti v elektivní střevní chirurgii je rozsah a úplnost mezokolické excize, resp. rozsah lymfadenektomie a počty a etáže odstraněných uzlin. Význam excize mezokola jako kompartmentu a důsledky pro dlouhodobé přežití je spojen především s prací W. Hohenbergera a P. Westa z let 2008 a 2009 [27,28]. Rozsáhlejší lymfadenektomii a odstranění vyššího počtu uzlin potvrdily např. práce týmů Changa a Lykkise. V prvé, hodnotící přežití v 17 studiích o souhrnném počtu 60 000 operovaných, bylo v 16 z nich prokázáno lepší přežití ve stadiu II závisle na vyšším počtu uzlin, ve stadiu III se zlepšení potvrdilo ve 4 ze 6 studií, v dalších zvýšení počtu uzlin ke zlepšení přežití nevedlo [29]. Shodnou zkušenost uvádí dánská autorská skupina [30]. Rovněž z Dánska je další rozsáhlá analýza z roku 2015, srovnávající výsledky resekcí s kompletní excizí mezokola (CME) a nekompletní excizí (nCME) u téměř patnácti set operovaných. Názor, že vyšší počet uzlin souvisí s disekcí v embryonálně založených vrstvách se zachováním mezokolické fascie a odstraněním celého prostoru, dokládají v CME skupině získáním 15,9 uzliny po CME a jen 10 uzlin po nCME. 4leté přežití operovaných ve stadiu II činilo po nCME 77,9 %, po CME 91,9 %, ve stadiu III po nCME 67,5 % a po CME 73,5 % [31]. Potvrzuje se tak dřívější myšlenka, že rozsáhlejší resekce souvisí s rozsahem chirurgické excize [32], bez ohledu na to, zda lymfadenektomie je podle evropské terminologie skryta za mezokolickou excizí, vyžadující centrální cévní ligaci, nebo D3 uzlinovou disekcí, jak se postup uvádí např. v japonských pracích [33]. Prospěch rozsáhlejších výkonů vyjádřený odstraněním vyššího počtu uzlin, dosažením resekčních okrajů ve větší vzdálenosti od nádoru, ve výsledku prodloužením přežití ve II. i III. stadiu má pochopitelně také zápory. Těmi je prodloužení operačních časů, větší krevní ztráty a významně vyšší počet pooperačních komplikací, jak potvrzuje např. recentní metaanalýza 12 studií zahrnujících více než 8500 pacientů [34].
Dalších momentů léčby nádorové obstrukce je řada. Při kompletní obstrukci způsobené nádorem rekta má mít přednost řešení ileu s ohledem na operačně technickou náročnost resekce rekta. Příčinou obstrukce je vždy pokročilý nádor, radiochemoterapie může jeho podmínky k resekci a přežití zlepšit. Podle některých údajů přibližně 40 % takových nádorů nelze primárně ani po radiochemoterapii odstranit [35,36]. Volba přístupu, zda operovat konvenčně, laparoskopicky nebo roboticky, daleko přesahuje téma sdělení i racionalitu podobné úvahy. Podobně je nad rámec sdělení, zda se při ileu pokusit o resekci primárního nádoru při inoperabilním metastatickém postižení. Prospěch z takové resekce uvádí v elektivní chirurgii např. retrospektivní analýza z r. 2017, srovnávající výsledek léčby po resekci a bez ní na souboru 65 543 nemocných s kolorektálním karcinomem ve IV. stadiu: 55 % nemocných podstoupilo resekci a dosáhlo mediánu přežití 22 měsíců, nemocní bez resekce 13 měsíců [37].
Naše zkušenost
Frekvence ošetření nemocných s obstrukcí tlustého střeva nádorem na našem pracovišti se během dvou desetiletí zvýšila, přestože se v ošetření akutních stavů nyní střídají dvě kliniky. Za desetiletí 1985–1994 bylo pro střevní neprůchodnost způsobenou nádorem operováno 130 nemocných. V posledních třech letech, tzn. 2015, 2016 a 2017, bylo ošetřeno celkem 83 nemocných, v jednotlivých letech 36, 23 a 24 nemocných. 60 nemocných mělo obstrukci nádorem v levé polovině kolorekta, z nich 26 nádorem rekta, jen 23 nemocných mělo obstrukci při nádoru v pravé polovině kolon. Průměrný věk v sestavě činil 69,6 roku, nejmladší byl dvaadvacetiletý, nejstarší třiadevádesátiletý. Při obstrukci v pravé polovině byla 18 nemocným provedena primárně resekce s anastomózou, třem byl založen střevní by-pas a dvěma ileostomie. Všem 26 nemocným s obstrukcí z nádoru rekta byla v akutním stavu založena stomie, z nich 10 podstoupilo po radiochemoterapii resekci. Ze 34 nemocných s levostrannou obstrukcí byla dvěma provedena subtotální kolektomie, 17 primární resekce a 15 založena stomie, z nich 11 z lokálních či celkových příčin jako definitivní. Po primárních resekcích byla zaznamenána porucha anastomózy 1x po pravostranné hemikolektomii a 2x po levostranné segmentární resekci. 4 zemřeli (4,8 %). Diagnostika se v mezidobí rozšířila o možnost akutního CT vyšetření, změnilo se zajištění a vedení anestezie a dostupnost velmi intenzivní péče včetně UPV. Volbu operačního postupu a zásady ošetření respektujeme shodně v obou obdobích.
Závěr
Nádorová obstrukce tlustého střeva je vždy projevem pokročilého nádoru. Léčbu dosud provází vysoká mortalita a morbidita, jejímiž příčinami jsou lokální i systémové poruchy vyplývající z obstrukce a pooperační komplikace. Na nich se po jednodobých resekcích významně podílejí poruchy anastomózy [38,39]. Lze-li nádor resekovat, operace v další době může proběhnout za standardních podmínek, odklad resekce po ošetření ileu v prvé době perspektivu nemocného neohrožuje. Jen za optimálních podmínek je vhodným řešením jednodobá segmentární resekce, při které má klíčové místo chirurg v hodnocení stavu a možností nemocného [40], perioperačním vedení a volbě a provedení operace [41]. Neexistuje jednoznačné doporučení, zda volit jednodobé, nebo dvoudobé řešení akutního stavu. Zato odpověď na prioritu neodkladné operace je zřejmá – vyřešit obstrukci a teprve na dalším místě, pokud to je možné, odstranit její příčinu.)
prof. MUDr. Jiří Hoch, CSc.
Chirurgická klinika 2. LF UK a FN Motol
V Úvalu 84
150 06 Praha 5
e-mail: jiri.hoch@fnmotol.cz
Sources
-
Formisano V, Di Muria A, Connola G, at al. Our experience in the management of obstructing colorectal cancer. Ann Ital Chir 2014;85 : 563−8.
-
Hoch J. Akutní chirurgie tlustého střeva. Praha, Maxdorf Jessenius 1998.
-
Suchý T, Krtička F, Pafko P, et al. Subtotální kolektomie v léčbě obturujících nádorů levé poloviny tračníku. Rozhl Chir 1990;69 : 153−8.
-
Matheson NA. Management of obstructed and perforated large bowel carcinoma. Baileres Clin Gastroenterol 1989;3 : 671−97.
-
Käser SA, Glauser PM, Künzli B, et al. Subtotal colectomy for malignant left-sided colon obstruction is associated with a lower anastomotic leak rate than segmental colectomy. Anticancer Res 2012;32 : 3501−5.
-
Sabbagh C, Siembida N, Yzet T, et al. What are the predictive factors of caecal perforation in patients with obstructing distal colon cancer? Colorectal Dis 2018. Available from: https://www.ncbi.nlm.nih.gov/pubmed/29495118
-
Dudley HAF, Radcliffe AG, McGeehan D. Intraoperative irrigation of the colon to permit primary anastomosis. Br J Surg 1980;67 : 80−1.
-
Schwenk W, Stock W, Hansen O. Therapie und Nachsorge multipler kolorektaler Karzinome-Ehrfahrung nach 13 Jahre Nachsorge. Akt Chir 1994;29 : 77−81.
-
Chéreau N, Lefevre JH, Lefrancois M, et al. Management of malignant left colonic obstruction: is an initial temporary colostomy followed by surgical resection a better option? Colorectal Dis 2013;15:e646−53.
-
Bielecki K, Kaminsky P. Hartmann´s procedure and what after? Int J Colorect Dis 1995;10 : 49−52.
-
Maurer CA, Renzulli P, Naef M, et al. Surgical therapy of ileus of the large intestine. Zentralbl Chir 1998;123 : 1346−54.
-
Deutsch AA, Zelikovski A, Sternberg, et al. One-stage subtotal colectomy with anastomosis for obstructing carcinoma of the left colon. Dis Colon Rectum 1983;26 : 227−30.
-
Hennekine-Mucci S, Tuech JJ, Brehant O, et al. Emergency subtotal/total colectomy in the management of obstructed left colon carcinoma. Int J Colorectal Dis 2006;21 : 538−41.
-
Mealy K, Salman A, Arthur G. Definitive one-stage emergency large bowel surgery. Br J Surg 1988;75 : 1216−9.
-
Eu KW. Systematic review of intraoperative colonic irrigation vs. manual decompression in obstructed left-sided colorectal emergencies. Int J Colorectal Dis 2009;24 : 1031−7.
-
Amelung FJ, Mulder CL, Verheijen PM, et al. Acute resection versus bridge to surgery with diverting colostomy for patients with acute malignant left sided colonic obstruction: Systematic review and meta-analysis. Surg Oncol 2015;24 : 313–21.
-
Kiefhaber P, Kiefhaber K, Huber F. Preoperative Neodymium YAG laser treatment of obstructive colon cancer. Endscopy 1986;18,Suppl.1 : 44−6.
-
Fazio W, Tjandra JJ. Primary therapy of carcinoma of the large bowel. World J Surg 1991;15 : 568−75.
-
Geraghty J, Sarkar S, Cox T, et al. Management of large bowel obstruction with self-expanding metal stents. A multicentre retrospective study of factors determining outcome. Colorectal Dis 2014;16 : 476–83.
-
Hong SP, Sung Pil Hong, Tae Il Kim. Colorectal stenting: an advanced approach to malignant colorectal obstruction. World J Gastroenterol 2014;21 : 16020–8.
-
Young CJ, De-Loyde KJ, Young JM, et al. Improving quality of life for people with incurable large-bowel obstruction: randomized control trial of colonic stent insertion. Dis Colon Rectum 2015;58 : 838–49.
-
van den Berg MW, Ledeboer M, Dijkgraaf MG, et al. Long-term results of palliative stenting of colonic obstructing cancer. Surg Endosc 2015;29 : 1580–5.
-
Matsuda AA, Miyashita M, Matsumoto S, et al. Comparison of long-term outcomes of colonic stent as „bridge to surgery” and emergency surgery for malignant large - bowel obstruction: a meta-analysis. Ann Surg Oncol 2015;22 : 497–504.
-
Imai M, Kamimura K, Takahashi Y, et al. The factors influencing long-term outcomes of stenting for malignant colorectal obstruction in elderly group in community medicine. Int J Colorectal Dis 2018;33 : 189−97.
-
Faraz S, Salem SB, Schattner M, et al. Predictors of clinical outcome of colonic stents in patients with malignant large-bowel obstruction because of extracolonic malignancy. Gastrointest Endosc 2018;87 : 1310−7.
-
Kothari AN, Liles JL, Holmes CJ, et al. „Right place at the right time” impacts outcomes for acute intestinal obstruction. Surgery 2015;158 : 116–25.
-
Hohenberger W, Weber K, Matzel K, et al. Standardized surgery for colonic cancer: complete mesocolic excision and central ligation – technical notes and outcome. Colorectal Dis 2009;11 : 354–64; discussion 364−5.
-
West NP, Hohenberger W, Finan PJ, et al. Mesocolic plane surgery and old but forgotten technique? Colorectal Disease 2009;11 : 988−9.
-
Chang, GJ. Lymph node evaluation and survival after curative resection of colon cancer: systematic review. J Natl Cancer Inst 2007;99 : 433−41.
-
Lykke J, Roikjaer O, Jess P. Danish Colorectal Cancer Group: The relation between lymph node status and survival in Stage I-III colon cancer: results from a prospective nationwide cohort study. Colorectal Dis 2013;15 : 559−65.
-
Bertelsen CA and Danish Colorectal Cancer Group: Disease free survival after complete mesocolic excision compared with conventional colon cancer surgery: a retrospective population-based study. Oncology 2015;14 : 141–68.
-
Enkler WE, Laffer UT, Block GE. Enhanced survival of patients with colon and rectal cancer is based upon wide anatomic resection. Ann Surg 1979;190 : 350−60.
-
West NP, Kobayashi H, Takahashi K, et al. Understanding optimal cancer surgery: A comparison of Japanese 3 D surgery and complete mesocolic excision with central vascular ligation. J Clin Oncol 2012;20;30 : 1763−9.
-
Wang C, Gao Z, Shen K, et al. Safety, quality and effect of complete mesocolic excision vs. non-complete mesocolic excision in patients with colon cancer: a systemic review and meta-analysis. Colorectal Dis 2017;19 : 962−72.
-
Trakamsanga A, Ithimakin S, Weiser MR. Treatment of locally advanced rectal cancer: controversies and questions. World J Gastroenterol 2012;18 : 5521−32.
-
Pelikán A, Tulinský L, Peteja M, et al. Mění se chirurgická léčba stenotického karcinomu rekta? Gastroenterol Hepatol 2017;71 : 62−8.
-
Tsung-Ming Chen, Yen-Ta Huang, Guan-Chyuan Wang. Outcome of colon cancer initially presenting as colon perforation and obstruction. World J Surg Oncol 2017;15 : 164.
-
Maroney S, Chavez de Paz C, Reeves ME, et al. Benefit of surgical resection of the primary tumor in patients undergoing chemotherapy for stage IV colorectal cancer with unresected metastasis. J Gastrointest Surg 2018;22 : 460–6.
-
Breitenstein S, Rickenbacher A, Berdajs D, et al. Systematic evaluation of surgical strategies for acute malignant left-sided colonic obstruction. Br J Surg 2007;94 : 1451−60.
-
Törer N. Morbidity and mortality of colorectal cancer surgery in octogenarians. Eur Surg 2016;48 : 215–20.
-
Morita S, Ikeda K, Komori T, et al. Outcomes in colorectal surgeon-driven management of obstructing colorectal cancers. Dis Colon Rectum 2016;59 : 1028−33.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2019 Issue 1-
All articles in this issue
- Obstrukce tlustého střeva nádorem – co je prioritou léčby?
- Timing ERCP u akutní biliární pankreatitidy
- Současná léčba difuzních peritonitid – je kvadrantová laváž stále aktuální?
- Spontánní retroperitoneální hematom – naše zkušenosti s aktivním chirurgickým přístupem
- Mezenteriální divertikly tenkého střeva jako příčina náhlé příhody břišní
- Náhlé příhody břišní u pacientů s Crohnovou chorobou − kazuistiky
- Náhlé příhody břišní u drogově závislých
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Spontánní retroperitoneální hematom – naše zkušenosti s aktivním chirurgickým přístupem
- Mezenteriální divertikly tenkého střeva jako příčina náhlé příhody břišní
- Timing ERCP u akutní biliární pankreatitidy
- Současná léčba difuzních peritonitid – je kvadrantová laváž stále aktuální?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

