-
Medical journals
- Career
Výsledky limitované resekce karcinomu gastroezofageální junkce
Authors: R. Vrba; R. Aujeský; Č. Neoral
Authors‘ workplace: I. chirurgická klinika FN Olomouc, přednosta: doc. MUDr. Č. Neoral, CSc.
Published in: Rozhl. Chir., 2012, roč. 91, č. 7, s. 368-372.
Category: Original articles
Overview
Úvod:
Autoři prezentují výsledky chirurgické resekční léčby u adenokarcinomu gastroezofageální junkce.Materiál a metodika:
Sestava nemocných obsahovala celkem 14 pacientů, ve složení 7 mužů a 7 žen. Věkový průměr byl 72 let. V souboru byli zastoupeni pouze nemocní v počátečních stadiích maligního onemocnění, dle EUS kategorie T1, 2, N0. PET/CT u všech vyloučilo generalizaci onemocnění. Dalším kritériem pro indikaci tohoto typu výkonu byla celková polymorbidita a vyšší věk pacientů. U všech byla provedena resekce distálního jícnu a horní polární resekce žaludku s lymfadenektomií. V šesti případech byla provedena splenektomie. Pasáž zažívacího traktu byla obnovena ezofagogastroanastomózou, standardně byla provedena pyloromyotomie. Ve dvou případech byla provedena resekce distálního jícnu z pravostranné torakotomie.Výsledky:
Během operace jsme nezaznamenali žádnou závažnější komplikaci. U jednoho nemocného byla k horní polární resekci žaludku přidružena cholecystektomie pro empyém žlučníku, při které došlo k poranění žlučových cest. Žlučové cesty byly ošetřeny hepatikojejunoanastomózou na exkludovanou jejunální kličku. V pooperačním období byla u čtyř pacientů prokázána píštěl v anastomóze. Konzervativní léčbou došlo ke zhojení píštěle ve dvou případech, chirurgickou léčbou v jednom. Jedna pacientka exitovala na následky píštěle s rozvojem septického šoku a respiračního selhání.Závěr:
Horní polární resekce žaludku a distálního jícnu, pokud splňuje kritéria RO resekce, je léčebnou terapií u nemocných v počátečních stadiích adenokarcinomů GE junkce.Klíčová slova:
adenokarcinom gastroezofageální junkce – chirurgická terapie – RO resekceÚvod
Základní terapií karcinomu gastroezofageální junkce je radikální resekční chirurgický výkon. Charakter výkonu je modifikován na základě typu adenokarcinomu klasifikovaného dle mezinárodní klasifikace adenokarcinomů GE junkce. V našem sdělení jsou prezentovány výsledky limitované chirurgické resekce u nemocných s adenokarcinomem GE junkce. Do sestavy byli zařazeni nemocní v iniciálních stadiích maligního onemocnění s přidruženými závažnými komorbiditami ve vyšších věkových skupinách.
Materiál a metodika
Na I. chirurgické klinice byla od roku 2007 provedena limitovaná resekce pro karcinom gastroezofageální junkce u 14 nemocných. Dominantními výkony pro tento typ adenokarcinomu jsou na našem pracovišti u karcinomů kardie a subkardie totální gastrektomie, u karcinomů přerůstajících na aborální partii jícnu ezofagektomie. Do sestavy operovaných byli zařazeni pouze nemocní s endoskopicky prokázaným tumorem GE junkce, u kterých byla na endosonografickém vyšetření popsána pouze stadia onemocnění v kategorii T1,2 bez regionální lymfadenopatie. Standardně bylo u všech nemocných provedeno PET/CT vyšetření k vyloučení metastatického procesu ve vzdálených lymfatických uzlinách a jiných orgánech (Obr. 1). Dalším kritériem k provedení méně náročného a rozsáhlého výkonu byl celkový stav nemocných, kdy u většiny byly v anamnéze přidruženy významné komorbidity. V souboru bylo zastoupeno 7 mužů a 7 žen s průměrným věkem 72 roků, věkové rozmezí bylo od 61 do 82 let. V anamnéze byla u nemocných dominantním symptomem dysfagie, celkem u 8 (57,1 %) nemocných. Čtyři pacienti měli v anamnéze dyspeptické potíže s bolestmi epigastria, jeden pacient byl přešetřován pro melénu a jeden pro anemii. Endoskopické vyšetření u všech nemocných prokázalo tumor v oblasti GE junkce. Histologicky byl potvrzen adenokarcinom. Pacienti byli indikováni k chirurgickému resekčnímu výkonu, u všech byla provedena horní polární resekce žaludku s resekcí distálního jícnu. Resekční linie na jícnu byla ve vzdálenosti nejméně 3 cm nad tumorem, ve všech případech bylo provedeno kryostatické vyšetření resekční linie k vyloučení nádorové infiltrace. Distální resekční linie, která byla provedena staplerově, byla 10 cm pod hranicí tumoru na žaludku. Ve všech případech byla součástí výkonu lymfadenektomie. Splenektomie byla provedena v 6 (42,8 %) případech. Pasáž zažívacího traktu byla u 13 nemocných obnovena gastroezofageální anastomózou, která byla konstruována s využitím kruhových staplerů o průměru 21 a 25 mm. V jednom případě byla anastomóza konstruována ručně. Součástí výkonu byla ve všech případech pyloroplastika dle Holla. Do dutiny břišní byly standardně založeny dva drény. Jeden k bráničnímu hiátu, druhý do levého hypochondria. V pooperačním období byla zajištěna nutrice nemocných kombinací parenterální a enterální výživy zavedenou nutritivní nazojejunální biluminální sondou. U všech nemocných bylo 7. pooperační den provedeno RTG vyšetření pasáže horní etáže zažívacího traktu vodnou kontrastní látkou k ověření suficience anastomózy (Obr. 2).
Image 1. Obraz tumoru kardie na PET/CT Fig. 1: PET/CT scan of tumor of the gastroesophageal junction 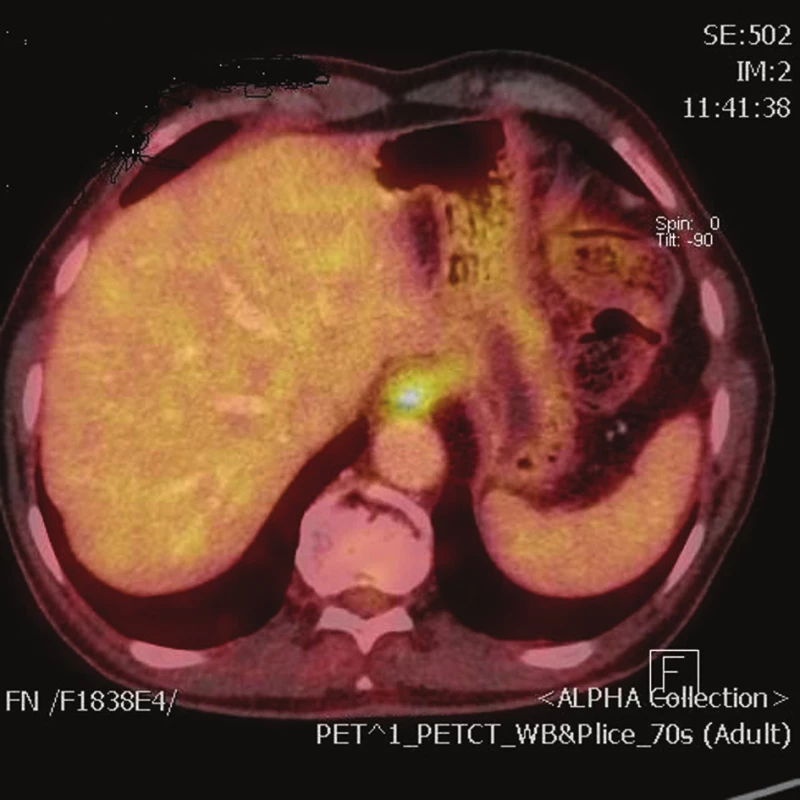
Image 2. Kontrolní pasáž s vodnou kontrastní látkou 7. pooperační den s příznivým nálezem Fig. 2: Follow-up swallow with water-based contrast 7. day after operation, good result of examination 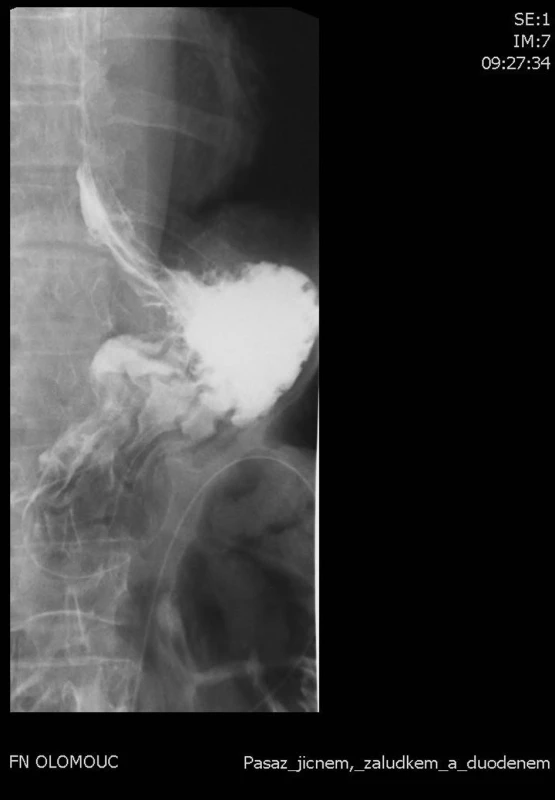
Výsledky
Celkem u 12 (85,7 %) nemocných byla provedena operace zcela bez komplikací, průměrná operační doba byla 157 minut. U dvou pacientů bylo z pravostranné torakotomie nezbytné provést resekci distálního jícnu pro pozitivní resekční linii prokázanou při histologickém vyšetření na zmrzlo. V obou případech byla konstruována jednovrstevná ezofagogastroanastomóza pokračujícím stehem. V jednom případě byla k primárnímu výkonu připojena cholecystektomie pro empyém žlučníku, který se nacházel v infiltrátu se žlučovými cestami. Pro nepřehledný terén byla po cholecystektomii provedena biligrafie, která potvrdila přerušení hepatocholedochu. Poraněné žlučové cesty byly ošetřeny hepatikojejunoanastomózou na exkludovanou Rouxovu jejunální kličku. V pooperačním období bylo 10 (71,4 %) nemocných bez komplikací. Kontrolní RTG vyšetření pasáže s vodnou kontrastní látkou bylo s příznivým nálezem. Nemocní byli postupně zatíženi stravou a v celkově dobrém stavu propuštěni do péče praktických lékařů. Ve čtyřech případech jsme zaznamenali píštěl nebo dehiscenci anastomózy. Vždy se jednalo o nemocné, u kterých byla ezofagogastroanastomóza konstruována kruhovým staplerem o průměru 21 mm. Ve dvou případech byla prokázána minimální píštěl v rámci kontrolní pasáže sedmý pooperační den. Oba pacienti byli bez alterace celkového stavu. Konzervativní léčbou došlo k postupnému uzavření píštěle. Pro septický stav se známkami peritonitidy byla u jednoho nemocného 6. pooperační den provedena akutní revize dutiny břišní s průkazem dehiscence anastomózy v terénu peritonitidy. Vzniklý stav byl chirurgicky ošetřen drenáží v lokalizaci dehiscentní anastomózy, laváží dutiny břišní. Pacient byl zajištěn širokospektrými antibiotiky. V dalším průběhu došlo k normalizaci celkového stavu, ale na kontrolním RTG vyšetření opakovaně přetrvávala drobná píštěl v anastomóze. Píštěl byla úspěšně ošetřena implantací biodegradabilního stentu do distálního jícnu. Následně byl nemocný bez komplikací postupně realimentován a propuštěn do péče praktického lékaře. Kontrolní endoskopie po třech měsících od propuštění popsala zhojenou píštěl, stent degradoval, endoskopicky nebyl nalezen. V sestavě nemocných jsme zaznamenali jeden exitus 5. pooperační den na následky respirační insuficience a septického šoku při dehiscenci anastomózy, která byla potvrzena chirurgickou revizí čtyři dny po primární operaci. Průměrná doba hospitalizace byla celkem 27,4 dne, u nemocných bez komplikací 14,1, s komplikacemi 58,3 dne. U 10 nemocných byla dle definitivního histologického vyšetření splněna kritéria R0 resekce. Mortalita souboru byla 7,1 %, morbidita 28,5 %. Definitivní histologické vyšetření popsalo v 11 případech adenokarcinom. V jednom případě u nemocného po neadjuvantní radiochemoterapii nebyl v definitivním preparátu popsán maligní tumor. U tohoto nemocného byla po onkologické léčbě prokázána kompletní odezva na tuto terapii. Vzhledem k jeho celkové polymorbiditě bylo odstoupeno od původně zamýšlené exstirpace jícnu a byl zvolen pro pacienta méně náročný výkon horní polární resekce žaludku. Dle TNM klasifikace byla v naší sestavě zastoupena tato stadia onemocnění: stadium I. A (T1N0M0) 4 pacienti, I.B (T2N0M0) 4 pacienti, II.A (T3N0M0) 1 pacient, II.B(T3N1M0) 4 pacienti. Dle klasifikace adenokarcinomů GE junkce byly zastoupeny tyto typy: I. 4 (28,6 %) pacienti, II. 5 (35,7 %) pacientů, III. 5 (35,7 %) pacientů.
Table 1. Seznam operovaných nemocných s typem resekce, stadiem onemocnění dle TNM klasifikace, typem adenokarcinomu GE junkce a komplikacemi Tab. 1: List of operated patients with type of resection, stage of disease according to TNM classification, type of adenocarcinoma of the GE junction and complications 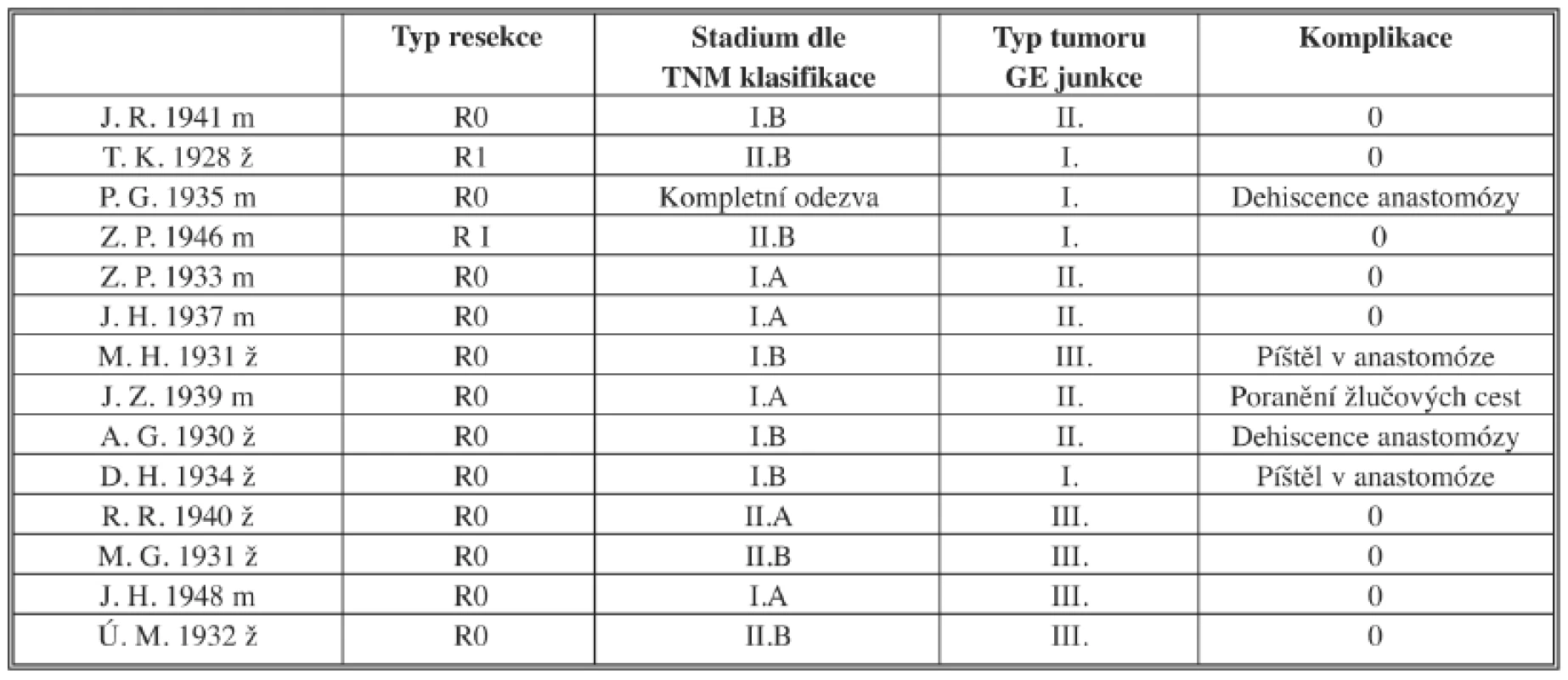
Diskuze
Karcinom GE junkce patří mezi skupinu nádorových onemocnění, která zejména v západní populaci zaznamenávají v posledních dekádách vzrůstající incidenci [1, 2]. Mezinárodní organizace pro onemocnění jícnu (ISDE) klasifikuje 3 typy adenokarcinomu GE junkce: typ I: adenokarcinom distálního jícnu (30–35 %), typ II: adenokarcinom kardie (20–25 %), typ III. subkardiální adenokarcinom žaludku (40–45 %) [3, 4]. U prvního typu byla jednoznačně potvrzena souvislost adenokarcinomu s refluxní nemocí jícnu a následným rozvojem Barrettova jícnu [5, 6]. Karcinomy II. a III. typu jsou dávány do souvislosti s karcinomem žaludku. Metastazování těchto karcinomů je převážně lymfatickou cestou podél a. gastrica sinistra do oblasti truncus coeliacus s následným postižením paraaortální oblasti. Zhruba jedna třetina pacientů má metastázy v mediastinálních lymfatických uzlinách [1]. V sestavách operovaných nemocných referovaných Siewertem, Streitzem, Milikanem, Walshem a dalšími byla dle TNM klasifikace zastoupena tato stadia onemocnění: stadium 0. 0,6 %, stadium I. 10,4 %, stadium II. 25,8 %, stadium III. 43,8 %, stadium IV. 19 % [7]. Klinicky se manifestují primárně tumory I. a II. typu, pro které jsou charakteristické dysfagie [7]. Do diagnostického algoritmu kromě endoskopie s biopsií tumoru jsou zařazeny endoskopická ultrasonografie a PET/CT. Endoskopická ultrasonografie stanoví infiltraci stěny GE junkce tumorem dle T kategorie a popíše stav uzlin v okolí tumoru (N kategorie) [8, 9]. PET/CT slouží především k vyloučení metastatického procesu v typických lokalitách, jako jsou vzdálené lymfatické uzliny, játra, plíce, kosti [10]. Na našem pracovišti jsou standardně tato vyšetření provedena u všech nemocných s maligním onemocněním horní etáže zažívacího traktu. V definitivní TNM klasifikaci na základě histologického vyšetření jsme zaznamenali diskrepanci s endosonografickým vyšetřením v pěti případech. U pěti nemocných byla popsána infiltrace stěny jícnu T2, definitivně se však jednalo o T3 kategorii. U všech nemocných byly popsány negativní uzliny, histologické vyšetření ve čtyřech případech popsalo N1 kategorii. Kompletní resekce tumoru s lymfadenektomií v rozsahu R0 resekce je základním pilířem léčby tumorů této lokality [1, 8, 16]. Tento typ resekce umožňuje nemocným dosáhnout nejlepších výsledků dlouhodobého přežívání [1]. Resekabilita je udávána v rozmezí od 41 do 88 % [7]. Operační léčba zahrnuje široké spektrum operačních výkonů v rozsahu od extenzivní ezofagogastrektomie k limitované resekci GE junkce. U tumorů typu I. se většina autorů (Siewert, Rahden) přiklání k ezofagektomii, která je kombinována s neoadjuvantní onkologickou radiochemoterapií [1, 8, 11]. Vzhledem k postižení distální části jícnu jsou preferovány transhiatální výkony, které prokazují nižší morbiditu ve srovnání s transtorakální ezofagektomií. U typu II. a III. je preferována gastrektomie s transhiatální resekcí distálního jícnu [8, 12, 13]. Rahden popisuje morbiditu gastrektomie ve srovnání s ezofagektomií 1,9 vs. 5,6 % [8]. Dle stadia onemocnění na základě definitivního histologického vyšetření je indikována adjuvantní onkologická léčba. Na našem pracovišti u nádorů distálního jícnu typu I. primárně indikujeme neoadjuvantní radiochemoterapii, ve druhé době je proveden chirurgický výkon v podobě ezofagektomie. Při nádorech kardie a subkardie, (typy II. III.), je chirurgickou terapií totální gastrektomie. V literatuře bylo pro tyto případy rovněž diskutováno provedení ezofagogastrektomie, která však pro výraznou morbiditu a mortalitu nepřináší nemocným výrazný benefit [1, 8]. Samostatnou kapitolou jsou limitované resekce GE junkce s ezofagogastro anastomózou nebo s ezofagojejunální anastomózou s využitím jejunální interpozice. Tento typ výkonu, jak uvádějí Siewert, Furukawa, a další je indikován pouze u časných tumorů s postižením sliznice nebo podslizničního vaziva bez přítomnosti metastatického procesu v lymfatických uzlinách [1, 14]. Literární odkazy u tohoto typu resekce poukazují na dobré bezprostřední i dlouhodobé pooperační výsledky s vysokou kvalitou života nemocných [8, 15]. Na našem pracovišti provádíme tento typ resekce u pacientů v iniciálních stadiích onemocnění zejména u pacientů vyšších věkových kategorií při současném výskytu výrazných komorbidit. K obnovení pasáže zažívacího traktu preferujeme ezofagogastrickou anastomózu. Při tomto typu anastomózy jsme komplikace plynoucí z možného biliárního refluxu v rámci dlouhodobé dispenzarizace u žádného nemocného nezaznamenali. Klademe důraz, stejně jako většina autorů, na provedení R0 resekce s lymfadenektomií. Z komplikací jsme zaznamenali pouze jedinou, ale o to závažnější, v podobě dehiscence ezofagogastroanastomózy. Incidence vzniku píštěle je popisována v rozmezí 4–19 % [18]. V naší sestavě se vyskytla vždy po použití kruhového stapleru o průměru 21 mm. Na základě této závažné komplikace jsme u nemocných s malým průměrem jícnu změnili operační strategii a konstrukci anastomózy provádíme ručně. Zatím tento typ anastomózy byl proveden u jedné pacientky, anastomóza se zhojila primárně bez komplikací. Pokud je však tato komplikace zaznamenána a je adekvátně zaléčena, nemusí mít pro nemocné fatální následky [17]. V našem souboru nemocných jsme potvrdili u většiny dobré bezprostřední operační výsledky. Z dlouhodobého hlediska jsou pacienti dispenzarizováni v gastroenterologické poradně I. chirurgické kliniky. Celkem 9 nemocných je sledováno bez přítomnosti základního onemocnění. U dvou nemocných byla na PET/CT prokázána generalizace onemocnění do jater, osud dalších dvou nemocných není známý.
Závěr
Horní polární resekce žaludku a distálního jícnu s lymfadenektomií a obnovením pasáže s využitím ezofagogastroanastomózy s připojenou pyloroplastikou je vhodnou alternativou chirurgické léčby v iniciálních stadiích adenokarcinomů GE junkce. Pro optimální výsledky tohoto operačního postupu je nezbytná správná indikace výkonu a provedení resekce tumoru v rozsahu RO. Správně indikovaný výkon má příznivý vliv na krátkodobé i dlouhodobé výsledky operovaných nemocných.
MUDr. R. Vrba, Ph.D.
I. chirurgická klinika LF UP a FN
I. P. Pavlova 6
775 20 Olomouc
e-mail: radek.vrba@fnol.cz
Sources
1. Stein HJ, Feith M, Siewert JR. Cancer of the esophagogastric junction, Surgical Oncology 2000;9.35–41.
2. Devesa SS, Blot WJ, Fraumeni Jr., JF. Changing patterns in the incidence of esophageal and gastric carcinoma in the United States. Cancer 1998;83 : 2049–53.
3. Kalish RJ, Klensey PE, Orringer MD, Appelman HD. Clinical, epidemiologic and morphologic comparison between adenocarcinomas arising in Barretts esophageal mucosa and gastric cardia. Gastroenterology 1984, 86,461–467.
4. Thomson JJ, Zinsser KR, Enterline HC. Barretts metaplasia and adenocarcinoma of the esophagus and gastroesophageal junction, Hum Pathol 1983;14 : 42–61.
5. Lagergren J, Bergstrom R, Lindgren A, Nyren O. Symptomatic gastroesophageal reflux as a risk factor for esophageal adenocarcinoma N Engl J Med 1999;340 : 825–831.
6. Rosenberg JC, Buder H, Edwards RC, Singal S, Steiger Z, Sundareson AS. Analyse of adenocarcinoma in Barretts esophagus utilising a staging system. Cancer 1958;55 : 1353–60.
7. Becker HD, Hohenberger W, Junginger T, Schlag PM. Chirurgická onkologie, Grada, Praha 2005 : 343–358.
8. Rahden BH, Stein HJ, Siewert JR. Surgical management of esophagogastric junction tumors, World J Gastroenterol 2006;12 : 6608–6613.
9. Mariette C, Castel B, Balon JM, Van Seuningen I, Triboulet JP. Extend of esophageal resection for adenocarcinoma of the esophagogastric junction, Eur J Surg Oncol 2003;29 : 588–593.
10. Ondrák M, Šefr R. Role PET a CT vyšetření v managmentu léčby zhoubného onemocnění tlustého střeva a konečníku – review, Rozhledy v chirurgii 2007;9 : 461–465.
11. Feith M, Stein HJ, Siewert JR. Pattern of lymphatic spred of Barretts cancer, World J Surg 2003 27 : 1052–57.
12. Graham AJ, Finley RJ, Clifton JC, Evans KG, Fradet G. Surgical management of adenocarcinoma of the cardia. Am J Surg 1998;175 : 418–421.
13. Papachristou DN, Fortner JG. Adenocarcinoma of the gastric cardia. The choice of gastrectomy. Am Surg 1980;192 : 58–64.
14. Furukawa H, Hiratsuka M, Imaoka S et all. Limited surgery for early gastric cancer in cardia. Annals of Surgical Oncology 1998;5 : 338–41.
15. Harwick RH, Williams GT. Staging of esophageal adenocarcinoma. Br J Surg 2002; 89 : 1076–1077.
16. Gatěk J, Duben J, Bakala J, Miča T, Dudešek B, Haša E, Musil T, Hnátek L. Lymfadenektomie u časného karcinomu žaludku, Rozhledy v chirurgii 2004;9 : 428–438.
17. Vrba R, Neoral Č, Aujeský R. Karcinom žaludku – výskyt a řešení komplikací chirurgické léčby, Rozhledy v chirurgii 2010;3 : 178–183.
18. Oh SJ, Choi WB, Song J, Hyung WJ, Choi SH, Noh SH. Complications requiring reoperation after gastrectomy for gastric cancer: 17 years experiance in a single institute, J Gastrointest Surg 2009;13 : 239–345.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2012 Issue 7-
All articles in this issue
- Výsledky limitované resekce karcinomu gastroezofageální junkce
- Rekonstrukce prsů přenosem autologního tuku
- Perzistence foramen ovale patens a riziko paradoxní embolizace žilních bublin u potápěčů – cave pro sklerotizaci varixů pěnovou metodou
- Chirurgické řešení komplikované jaterní echinokokózy u dvou bulharských občanů na dvou pracovištích v České republice
- Segmentální duodenektomie (D3, D4) pro angiosarkom
- Endosonografie jícnu v diagnostice a léčbě tumorů jícnu
- Descendentní nekrotizující mediastinitida – chirurgická léčba
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Chirurgické řešení komplikované jaterní echinokokózy u dvou bulharských občanů na dvou pracovištích v České republice
- Descendentní nekrotizující mediastinitida – chirurgická léčba
- Segmentální duodenektomie (D3, D4) pro angiosarkom
- Endosonografie jícnu v diagnostice a léčbě tumorů jícnu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

