-
Medical journals
- Career
Nové možnosti diagnostiky karcinómu pankreasu
Authors: J. Kaťuchová; J. Bober; P. Harbuľák; J. Radoňak
Authors‘ workplace: I. chirurgická klinika LF UPJŠ a UNLP Košice, Slovenská republika, prednosta: prof. MUDr. J. Radoňak, CSc.
Published in: Rozhl. Chir., 2011, roč. 90, č. 3, s. 184-189.
Category: Monothematic special - Original
Overview
Úvod:
Karcinóm pankreasu je zákerné ochorenie. Päťročné prežívanie 5–15 %, medián prežívania 13–17 mesiacov. Hľadanie nových možností v diagnostike môže pomôcť odhaliť karcinóm pankreasu vo včasných štádiách.Materiál a metódy:
Na I. chirurgickej klinike LF UPJŠ a UNLP v Košiciach, bola vykonaná porovnávacia štúdia prežívania pacientov s karcinómom pankreasu po radikálnej resekcii v dvoch skupinách, staršia skupina A od 1. 1. 1996 do 31. 12. 2000 a novšia skupina B od 1. 1. 2005 do 31. 12. 2009.
Od 1. 1.2007 do 31.12.2009 bola vykonaná prospektívna štúdia s cieľom diagnostikovať pacientov v počiatočnom štádiu ochorenia. Boli vykonávané histopatologické a imunohistochemické vyšetrenia lymfatických uzlín, zachytených počas lymfadenektómie.Výsledky:
V skupine A (1. 1. 1996–31. 12. 2000) bolo zastúpených 29 pacientov, 5 ročné prežívanie bolo zaznamenané u dvoch pacientov (6,8 %) medián prežívania 14 mesiacov. V skupine B (1. 1. 2005–31. 12. 2009) bolo zastúpených 51 pacientov, 5-ročné prežívanie u žiadneho pacienta, medián prežívania bol 14 mesiacov.
Od 1. 1. 2007 do 30. 12. 2009 bolo hospitalizovaných 108 pacientov s karcinómom pankreasu. Radikálna resekcia s regionálnou lymfadenektómiou bola vykonaná u 36 pacientov. Počas štandardnej lymfadenektómie bolo zistených 19 pacientov, ktorí mali 119 negatívnych lymfatických uzlín pri histopatologickom vyšetrení. Tieto uzliny boli vyšetrované imunohistochemicky, pričom bola zaznamenaná pozitivita v 37 lymfatických uzlinách na malígne ochorenie, 6 pacientov.Záver:
Pacienti diagnostikovaní v skorých štádiách karcinómu pankreasu majú medián prežívania lepší ako pacienti v pokročilých štádiách. Vykonávaním imunohistochemických vyšetrení histopatologicky negatívnych lymfatických uzlín je možné odhaliť pozitívne lymfatické uzliny a diagnostikovať pacientov vo včasných štádiách karcinómu pankreasu.Kľúčové slová:
karcinóm pankreasu – prežívanie – lymfatické uzliny – histopatologické vyšetrenie – imunohistochemické vyšetrenieÚVOD
Karcinóm pankreasu je na Slovensku šiestym najčastejším nádorovým ochorením, v USA štvrtým a vo Veľkej Británii šiestym, je to druhý najčastejší nádor tráviaceho traktu. Najviac je pozorovaný v populácii 65–75-ročných [1, 2, 3, 4]. Väčšina pacientov prichádza v pokročilom štádiu ochorenia, kde je možnosť resekčných výkonov nízka [5, 6].
Duktálny pankreatický adenokarcinóm je najčastejším epiteliálnym exokrinným pankreatickým tumorom a je zastúpený okolo 85 % všetkých pankreatických nádorov, pričom je v 80–90 % prítomný v hlave pankreasu. Metastatické postihnutie lymfatických uzlín je okolo 20 – –70 % v prípadoch resekabilných nádorov. Takisto je pomerne častá perineurálna invázia v 70–77 %, perivaskulárna v 45 % a lymfatická v 80 % v resekabilných štádiách ochorení [7, 8, 9].
Pacienti s karcinómom pankreasu zvyčajne prichádzajú s príznakmi ožltnutia, chudnutia a bolestí v chrbte, avšak tieto klinické príznaky neurčujú presne diagnózu. Takisto je mnoho príznakov, ktoré môžu smerovať k diagnóze karcinómu pankreasu, ako sú nedávny vznik cukrovky alebo nevysvetliteľný atak akútnej pankreatitídy [3, 10].
Duodenopankreatektómia je vykonávaná u pacientov s karcinómom pankreasu pričom mortalita v súčasnosti klesá pod 5 %, morbidita pretrváva okolo 20–70 %. Päťročné prežívanie po duodenopankreatektómii je pre karcinóm pankreasu okolo 5–15 %, s mediánom prežívania okolo 17 mesiacov [11, 12]. Mortalita a morbidita nemá súvis s typom vykonanej duodenopankreatektómie. Rozšírená lymfadenektómia, radikálna rozšírená lymfadenektómia a resekcia časti portálnej vény je uskutočňovaná s porovnateľnou morbiditou a mortalitou ako štandardná Whipplova operácia, no nemá vplyv na zlepšenie prežívania [13, 14, 15, 16]. Duodenopankreatektómia poskytuje pacientom s karcinómom pankreasu jedinú šancu na prežitie [17].
Pri karcinóme v oblasti hlavy pankreasu je nutné vykonať cholecystektómiu, preťatie spoločného hepatiku, preťatie pankreasu, rozdeliť Treitzove ligamentum a vykonať pylorus záchovnú alebo klasickú Whippleovu operáciu. Lymfadenektómie sa rozdeľujú podľa rozsahu odstránených lymfatických uzlín na štandardné, radikálne a rozšírene radikálne. Pri štandardnej duodenopankreatektómii sa vykonáva regionálna lymfanektómia okolo duodena a pankreasu (zahrnuté sú uzliny 12b1, 12b2, 12c, 13a, 13b, 14a, 14b, 17a, 17b, klasifikované podľa Japonskej pankreatickej spoločnosti). Pri radikálnej duodenopankreatektómii sa okrem regionálnej lymfadenektómie vykonáva skeletizácia hepatálnej artérie, skeletizácia mezenterickej artérie medzi aortou a dolnou pankreatikoduodenálnou artériou, skeletizácia truncus coeliacus, disekcia laterálne od aorty a vena cava inferior zahrňujúca Gerotovu fasciu (zahrnuté sú uzliny celá oblasť 8, 9, všetky 12, všetky 14, 16a2, 16b1). Pri rozšírenej radikálnej duodenopankreatektómii sa vykonáva radikálna duodenopankreatektómia s odstránením tkaniva prednej strany aorty od odstupu v hiatus aorticus bránice okolo truncus coeliacus až po vetvenie spoločných ilických artérií (zahrnuté sú všetky LU skupiny 16). Ľavostranná adrenalektómia je ponechaná na voľbe operatéra [16]. Pri karcinóme v oblasti tela a chvosta pankreasu sa pretína pankreas priamo nad spojením hornej mezenterickej vény s portálnou vénou a odstraňuje sa slezina. Štandardná ľavostranná pankreatektómia sa vykonáva s regionálnou lymfadenektómiou LU skupín truncus coeliacus, hílus sleziny, pozdĺž lienálnej artérie a dolný okraj tela a chvosta pankreasu (zahrňuje LU skupiny 9, 10, 11, 18). Pri radikálnej ľavostrannej pankreatektómii sa vykonáva regionálna lymfadenektómia a navyše lymfadenektómia pozdĺž hepatálnej artérie a anterolaterálnej strany aorty a vena cava inferior zahrňujúce Gerotovu fasciu (zahrňuje skupiny LU 8a, všetky 14, 16a2, 16b1). Ľavostranná adrenalektómia je ponechaná na voľbe operatéra (Obr. 1, 2) [16].
Image 1. Schéma odstránenia lymfatických uzlín pri štandardnej lymfadenektómii, radikálnej lymfadenektómii a rozšírenej radikálnej lymfadenektómii podľa Pedrazzoliho [16], obrázok nižšie znázorňuje detail lymfatických uzlín úrovne 16 podľa JPS Fig. 1. Standard lymphadenectomy, radical lymphadenectomy and extended radical lymphadenectomy modified by Pedrazzoli [16], picture below – detail of sixteen lymphnodes ![Schéma odstránenia lymfatických uzlín pri štandardnej lymfadenektómii, radikálnej lymfadenektómii a rozšírenej radikálnej lymfadenektómii podľa Pedrazzoliho [16], obrázok nižšie znázorňuje detail lymfatických uzlín úrovne 16 podľa JPS
Fig. 1. Standard lymphadenectomy, radical lymphadenectomy and extended radical lymphadenectomy modified by Pedrazzoli [16], picture below – detail of sixteen lymphnodes](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/8a630bdbffca7b0630aefa968592adf6.jpg)
Image 2. Schéma rozsahu vykonania štandardnej lymfadenektómie pri karcinóme v oblasti tela a chvosta pankreasu podľa Pedrazzoliho [16], dolný obrázok znázorňuje detailnejšie lymfatické uzliny úrovne 16 Fig. 2. Standard lymphadenectomy in pancreatic cancer of body and tail of pancreas modified by Pedrazzoli [16], picture below – detail of sixteen lymphnodes ![Schéma rozsahu vykonania štandardnej lymfadenektómie pri karcinóme v oblasti tela a chvosta pankreasu podľa Pedrazzoliho [16], dolný obrázok znázorňuje detailnejšie lymfatické uzliny úrovne 16
Fig. 2. Standard lymphadenectomy in pancreatic cancer of body and tail of pancreas modified by Pedrazzoli [16], picture below – detail of sixteen lymphnodes](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/c8dc7c4e55a5ed19281a4695a7a761e0.jpg)
MATERIÁL A METODIKA
Na I. chirurgickej klinike LF UPJŠ a UNLP v Košiciach, bola vykonaná porovnávacia štúdia prežívania pacientov s karcinómom pankreasu po radikálnej resekcii v dvoch skupinách, staršia skupina A od 1. 1. 1996 do 31. 12. 2000 a novšia skupina B od 1. 1. 2005 do 31. 12. 2009.
Od 1. 1. 2007 bola vykonaná prospektívna štúdia s cieľom diagnostikovať pacientov s karcinómom pankreasu v skorých štádiách ochorenia. Boli vykonávané histopatologické a imunohistochemické vyšetrenia lymfatických uzlín, zachytených počas lymfadenektómie. V prípade histopatologicky negatívneho nálezu v lymfatických uzlinách bolo vykonané imunohistochemické vyšetrenie pomocou monoklonálnych antiepiteliálnych protilátok Ber-EP4 proti tumoróznym bunkám.
Lymfatické uzliny boli odstraňované počas radikálnej operácie, resekcie pankreasu, vykonávaná bola štandardná lymfadenektómia.
Pacienti boli sledovaní v Hepatopankreatobiliárnej poradni I. chirurgickej kliniky LF UPJŠ a UNLP v Košiciach, prvá kontrola tridsať dní po operácii. Ďalší stav pacientov bol hodnotený v trojmesačných intervaloch.
Na vyjadrenie miery významnosti rozdielov stredných hodnôt vybraných ukazovateľov medzi jednotlivými skupinami sme použili nepárový t-test u parametrických dát, resp. neparametrický Mannov-Whitneyho test. Analýza prežívania sledovaných parametrov bola vyhodnotená Kaplanovou-Meierovou metódou. U všetkých testov sme za hladinu štatistickej významnosti zvolili p = 0,05.
VÝSLEDKY
Bola vykonaná porovnávacia štúdia prežívania pacientov s karcinómom pankreasu po radikálnej resekcii v dvoch skupinách, staršia skupina A od 1. 1. 1996 do 31. 12. 2000 a novšia skupina B od 1. 1. 2005 do 31. 12. 2009.
V skupine A bolo zastúpených 29 pacientov, 20 mužov a 9 žien, priemerný vek pacientov 58,9 rokov (33–74), v skupine B bolo zastúpených 51 pacientov, 29 mužov a 22 žien, priemerný vek pacientov 60,1 rokov (32–79). Nebol zaznamenaný štatisticky významný rozdiel vo vekovom zastúpení v oboch sledovaných skupinách pacientov (Tab. 1).
Table 1. Vekové zastúpenie pacientov v skupinách A a B Tab. 1. Age of patients in group A and B 
V sledovanom súbore bolo v skupine A zaznamenané 5-ročné prežívanie u dvoch pacientov (6,8 %), medián prežívania bol 14 mesiacov. V jednotlivých štádiách ochorenia boli pacienti zastúpení nasledovne, v štádiu IA nebol prítomný pacient, IB 3 pacienti, IIA 14 pacientov, IIB 11 pacientov, III nebol sledovaný pacient a v štádiu IV 1 pacient. Medián prežívania bol v týchto skupinách zaznamenaný IB 45 mesiacov, IIA 14 mesiacov, IIB 8 mesiacov, v IV štádiu 13 mesiacov. Paradoxne lepšie prežívanie bolo zaznamenané v skupine IV štádia, avšak v tejto skupine bol sledovaný len jeden pacienta, ide o chybu malých čísel, štatisticky nie významnú.
V sledovanom súbore bolo v skupine B nebolo zaznamenané 5-ročné prežívanie u žiadneho pacienta, medián prežívania bol 14 mesiacov. V jednotlivých štádiách ochorenia boli pacienti zastúpení nasledovne, v štádiu IA 1 pacient, IB 5 pacienti, IIA 19 pacientov, IIB 23 pacientov, III 1 pacient a v štádiu IV 2 pacienti. Medián prežívania bol v týchto skupinách zaznamenaný IB 28 mesiacov, IIA 14 mesiacov, IIB 13 mesiacov, v IV štádiu 2 mesiace. Štádiá IA a III boli zastúpené jedným pacientov, obaja pacienti k 1.1.2010 prežívajú, v štádiu IA 5 mesiacov od operácie a v štádiu III 6 mesiacov, medián prežívanie nebolo možné určiť (Tab. 2, Graf 1, 2, 3, 4, 5).
Table 2. Medián prežívania pacientov s karcinómom pankreasu po radikálnej resekcii, zaznamenané podľa štádia ochorenia, porovnanie v skupinách A,B Tab. 2. Median survival pancreatic cancer patients after pancreatic resection according to staging of the disease, comparing in group A, B 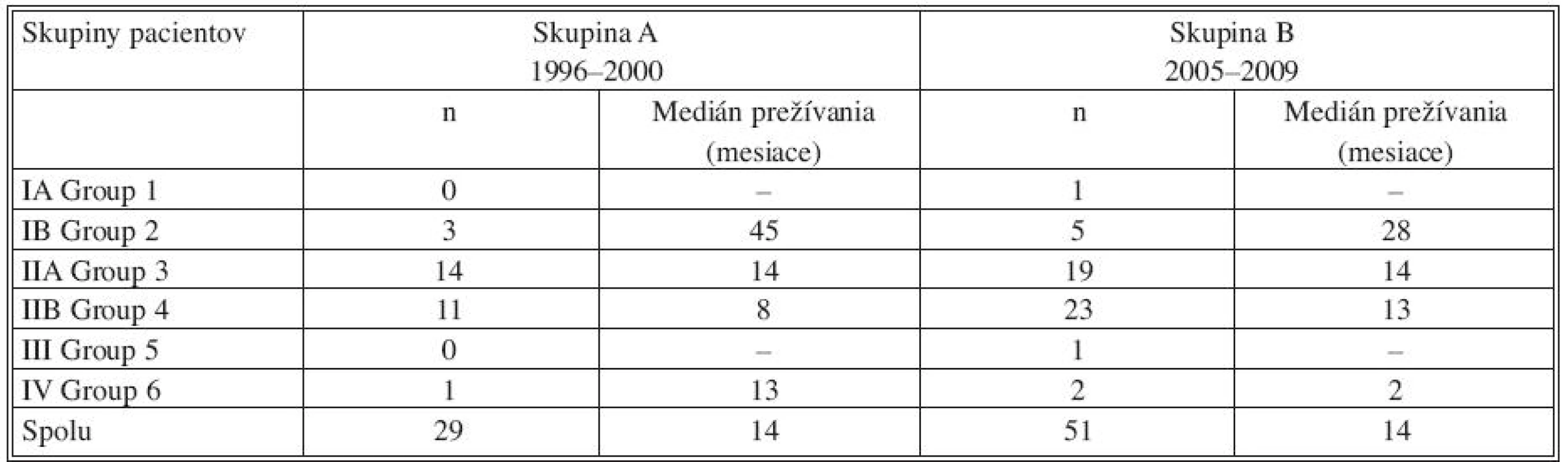
Graph 1. Prežívanie pacientov s karcinómom pankreasu po radikálnej resekcii skupina A operovaní 1. 1. 1996–31. 12. 2000 Graph 1. Survival rate of pancreatic cancer patients after pancreatic resection group A operation 1. 1. 1996–31. 12. 2000 
Graph 2. Prežívanie pacientov s karcinómom pankreasu po radikálnej resekcii skupina A operovaní 1. 1. 1996–31. 12. 2000, podľa jednotlivých štádií ochorenia Graph 2. Survival rate of pancreatic cancer patients after pancreatic resection group A operation 1. 1. 1996–31. 12. 2000, according to staging of the disease 
Graph 3. Prežívanie pacientov s karcinómom pankreasu po radikálnej resekcii skupina B operovaní 1. 1. 2005–31. 12. 2009 Graph 3. Survival rate of pancreatic cancer patients after pancreatic resection group B operation 1. 1. 2005–31. 12. 2009 
Graph 4. Prežívanie pacientov s karcinómom pankreasu po radikálnej resekcii skupina B operovaní 1. 1. 2005–31. 12. 2009, podľa jednotlivých štádií ochorenia Graph 4. Survival rate of pancreatic cancer patients after pancreatic resection group B operation 1. 1. 2005–31. 12. 2009, according to stage of the disease 
V jednotlivých štádiách ochorenia, karcinómu pankreasu, boli zastúpení pacienti približne v porovnateľnom počte. V skupine A, pacienti operovaní od 1. 1. 1996 do 31. 12. 2000 ako aj v skupine B, pacienti operovaní od 1. 1. 2005 do 31. 12. 2009, bol zaznamenaný rovnaký medián prežívania 14 mesiacov. Bolo zistené, že ani v časovom odstupe takmer desať rokov nedochádza k zlepšeniu prežívania pacientov s karcinómom pankreasu.
V skorých štádiách ochorenia v oboch skupinách prežívali pacienti výrazne lepšie ako v pokročilých štádiách.
V druhej časti štúdie vykonanej na I. chirurgickej klinike LF UPJŠ a UNLP v Košiciach boli sledované nové možnosti v diagnostike pacientov s karcinómom pankreasu v skorých štádiách ochorenia.
Na I. chirurgickej klinike LF UPJŠ a UNLP v Košiciach bolo od 1. 1. 2007 do 31. 12. 2009 bolo hospitalizovaných 108 pacientov s karcinómom pankreasu. Radikálna resekcia s regionálnou lymfadenektómiou bola vykonaná u 36 pacientov. V súbore bolo 12 žien a 24 mužov, vekové zastúpenie bolo 32–79 rokov, priemerný vek pacientov 60,6 rokov.
Duodenohemipankreatektómia bola vykonaná v modifikácii Child-Stulhofer (pankreato-jejunoanastomóza end to end) 24-krát, Whipple (pankreatojejunoanastomóza end to side) 3-krát, Traverso-Longmire (pylorus záchovná resekcia pankreasu) v jednom prípade a distálna (ľavostranná) hemipankreatektómia bola vykonaná 7 pacientom a totálna pankreatektómia u jedného pacienta.
U všetkých pacientov bola vykonávaná radikálna resekcia pankreasu s tumorom a štandardná lymfadenektómia. Pozitivita lymfatických uzlín bola zaznamenaná u 17 pacientov. Týmto pacientom bola odporučená adjuvantná onkologická liečba. U zvyšných 19 pacientov, ktorí mali histopatologicky negatívne lymfatické uzliny, bolo vykonané imunohistochemické vyšetrenie lymfatických uzlín. V tejto skupine pacientov bolo vyšetrených 119 lymfatických uzlín hodnotených ako histopatologicky negatívne na prítomnosť metastázy karcinómu pankreasu. Všetky lymfatické uzliny boli vyšetrené imunohistochemicky s použitím antiepiteliálnych monoklonálnych protilátok Ber-EP4 proti tumoróznym bunkám. Imunohistochemicky pozitívnych bolo zistených 37 pozitívnych a 82 negatívnych lymfatických uzlín.
V sledovanom súbore pacientov, bolo zistených 6 pacientov s negatívnymi lymfatickými uzlinami histopatologicky avšak imunohistochemicky pozitívnymi, 13 pacientov bolo hodnotených s lymfatickými uzlinami negatívnymi histopatologicky aj imunohistochemicky.
Pacienti, ktorí mali vyšetrené lymfatické uzliny histopatologicky aj imunohistochemicky negatívne na prítomnosť metastázy karcinómu pankreasu, boli hodnotení ako pacienti v skorých štádiách ochorenia bez potreby adjuvantnej onkologickej liečby. Títo pacienti sú pravidelne sledovaní v hepatopankreatobiliárnej poradni.
Pacienti, ktorí mali vyšetrené lymfatické uzliny histopatologicky negatívne avšak imunohistochemicky pozitívne na prítomnosť metastázy karcinómu pankreasu, boli konzultovaní a bola im doporučená adjuvantná onkologická liečba, rádioterapia.
Traja pacienti liečbu neabsolvovali pre vysoký vek a pridružené ochorenia, traja ďalší pacienti absolvovali adjuvatnú rádioterapiu, títo pacienti prežívajú 5, 15 a 24 mesiacov po operácii k 1. 1. 2010.
DISKUSIA
Prežívanie pacientov, ktorí podstúpili resekčný výkon, duodenohemipankreatektómiu, pre nemetastázujúce ochorenie je od 7 po 25 %, s mediánom od 11 po 20 mesiacov [10, 11, 12, 19, 20, 21]. V sledovanom súbore nebola zaznamenaná zmena v prežívaní v období od 1. 1. 1996 do 31. 12. 2000, skupina A, oproti obdobiu od 1. 1. 2005 do 31. 12. 2009, skupina B. V sledovanom súbore bolo v skupine A zaznamenané 5-ročné prežívanie u dvoch pacientov (6,8 %), medián prežívania bol 14 mesiacov. V sledovanom súbore bolo v skupine B nebolo zaznamenané 5-ročné prežívanie u žiadneho pacienta, medián prežívania bol 14 mesiacov.
Včasný metastatický relaps ochorenia po radikálnej resekcii sa zdá byť v dôsledku nezistenia nádorových buniek v regionálnych lymfatických uzlín bežným histologickým vyšetrením [18, 20, 21, 22]. Monoklonálne protilátky proti epiteliálnym tumoróznym bunkám sa ukazujú byť významné v detegovaní lymfatických uzlín negatívnych na nádorové bunky pri bežnom histologickom vyšetrení [18, 21, 23].
Izbicki a kol. sledovali pozitivitu lymfatických uzlín na nádorové ochorenie s použitím histopatologických vyšetrení ako aj imunohistochemických vyšetrení lymfatických uzlín. Výsledky oboch vyšetrení ukázali, že napriek negatívnym nálezom pri bežnom histologickom vyšetrení, imunohistochemické vyšetrenie dokázalo prítomnosť adenokarcinómu v tretine všetkých lymfatických uzlín. Z celkového počtu vyšetrených 148 LU s negatívnym histologickým výsledkom bol v 56 LU pri vyšetrení imunohistochemicky pozitívny nález. Pri sledovaní dlhodobého prežívania zisťujú, že v prípade negatívnych výsledkov vyšetrení lymfatických uzlín bežným histologickým vyšetrením, ak boli vyšetrenia LU imunohistochemicky protilátkami Ber-EP4 negatívne pacienti prežívali bez príznakov ochorenia až v 60 %, avšak ak boli LU pozitívne pri tomto vyšetrení pacienti prežívali 5 rokov len v 10 %. Izbicki a kol. uvádzajú ako najdôležitejší prognostický faktor pacientov s pankreatickým duktálnym adenokarcinómom identifikáciu lymfatických uzlín histopatologicky. V tejto štúdii poukazujú však aj na ďalší nezávislý prognostický faktor a to vyšetrenie imunohistochemické [18].
V sledovanom súbore bolo zistených 19 pacientov, ktorí mali histopatologicky negatívne lymfatické uzliny, 119 lymfatických uzlín. Všetky lymfatické uzliny boli vyšetrené imunohistochemicky s použitím antiepiteliálnych monoklonálnych protilátok Ber-EP4 proti tumoróznym bunkám. Imunohistochemicky pozitívnych bolo zistených 37 pozitívnych a 82 negatívnych lymfatických uzlín.
ZÁVER
Táto štúdia potvrdila, že karcinóm pankreasu je veľmi agresívne ochorenie so zlou prognózou, u ktorého nedochádza k zlepšeniu prežívania. Výrazne lepšie prežívajú pacienti v skorých štádiách ochorenia.
Vykonávaním histopatologického a imunohistochemického vyšetrenia lymfatických uzlín odstránených pri regionálnej lymfadenektómii počas resekcie pankreasu pre karcinóm je možné zachytiť včasné štádiá tohto zákerného ochorenia.
MUDr. Jana Kaťuchová, Ph.D.
I. chirurgická klinika LF UPJŠ a UNLP
Tr. SNP l
040 01 Košice
Slovenská republika
e-mail: jana.katuchova@upjs.sk
Sources
1. Alexalis, N., Halloran, C., Raraty, M., et al. Current standards of surgery for pancreatic cancer. Br. J. Surg., 2004; 91 : 410–427.
2. Beger, H. G., Matsuno, S., Cameron, J. L. Diseases of the pancreas. 1st ed. Berlin Heidelberg New York, Springer-Verlag, 2008.
3. Bober, J., Blažej, I., Sabo-Nácko, J., et al. Karcinóm pankreasu-diagnostika, chirurgická liečba, výsledky. Folia Medica Cassoviensia Universitas Šafarikiana, 1996; 53 : 84–89.
4. Kothaj, P. Chirurgická liečba rakoviny pankreasu. 1. vyd. Banská Bystrica, Spektrum 1997.
5. Brennan, M. F., Kattan, M. W., Klimstra, D., et al. Prognostic nomogram for patients undergoing resection for adenocarcinoma of the pancreas. Ann. Surg., 2004; 240 : 293–298.
6. Ryder, N. M., Reber, H. A. Pancreatic surgery. Curr. Opin. Gastroenterol., 2000; 16 : 426–430.
7. Doi, R., Kami, K., Ito, D., et al. Prognostic implication of para-aortic lymph node metastasis in resectable pancreatic cancer. World J. Surg., 2007; 31 : 147–154.
8. Neoptolemos, J. P., Stocken, D. D., Dunn, J. A., et al. Influence of resection margins on survival for patients with pancreatic cancer treated by adjuvant chemoradiation and/or chemotherapy in the ESPAC-1 randomized controlled trial. Ann. Surg., 2001; 234 : 758–768.
9. Zervos, E. E., Rosemurgy, A. S., Al-Saif, O., et al. Surgical management of early-stage pancreatic cancer. Cancer control, 2004; 11 : 23–31.
10. Krechler, T., Novotný, J., Zeman, M., et al. Karcinom pankreatu a diabetes mellitus. Čas. Lék. Čes., 2004; 143 : 97–100.
11. Schmidt, C. M., Powel, W. S., Yiannoutsos, C. T., et al. Pancreaticoduodenectomy. A 20-years experience in 516 patients. Arch. Surg., 2004; 139 : 718–727.
12. Yeo, C. J.,Cameron, J. L., Lillemoe, K. D., et al. Pancreaticoduodenectomy with or without distal gastrectomy and extended retroperitoneal lymphadenectomy for periampullary adenocarcinoma, part 2. Randomized control trial evaluating survival, mortality and morbidity. Ann. Surg., 2002; 236 : 355–368.
13. Nakao, A. Debate: extended resection for pancreatic cancer; the affirmative case. J. Hepatobiliary Pancreat. Surg., 2003; 10 : 57–60.
14. Pawlik, T. M., Abdalla, E. K., Barnett, C. C., et al. Feasibility of a randomized trial of extended lymphadenectomy for pancreatic cancer. Arch. Surg., 2005; 140 : 584–591.
15. Siriwardana, H. P., Siriwardena, A. K. Systematic review of outcome of synchronous portal-superior mesenteric vein resection during pancreatectomy for cancer. Br. J. Surg., 2006; 93 : 662–673.
16. Pedrazzoli, S., Beger, H. G., Obertop, H., et al. A surgical and pathological based classification of resective treatment of pancreatic cancer. Dig. Surg., 1999; 16 : 337–345.
17. Wagner, M., Redaeelli, C., Lietz, M., et al. Curative resection is the single most important factor determining outcome in patients with pancreatic adenocarcinoma. Br. J. Surg., 2004; 91 : 586–594.
18. Bogoevski, D., Yekebas, E. F., Schurr, P., et al. Mode of spread in the early phase of lymphatic metastasis in pancreatic ductal adenocarcinoma: Prognostic significance of nodal microinvolvement. Ann. Surg., 2004; 240 : 993–1001.
19. Zavoral, M., et al. Karcinom pankreatu. 1. vyd. Praha, Galén, 2005.
20. Scheunemann, P., Stoecklein, N., Bidde, M., et al. Occult tumor cells in lymph nodes as a predictor for tumor relapse in pancreatic adenocarcinoma. Langenbecks Arch. Surg., 2008; 393 : 359–365.
21. Niedrgethmann, M., Rexin, M., Hildebrand, R., et al. Prognostic implications of routine immunohistochemical, and molecular staging in resectable pancreatic adenocarcinoma. Am. J. Surg. Pathol., 2002; 26 : 1578–1587.
22. Gockel, I., Domeyer, M., Wolloscheck, T., et al. Resection of the mesopancreas (RMP): a new surgical classification of a known anatomical space. World Journal of Surgical Oncology, 2007; 5 : 44–51.
23. Mizano, T., Ishizaki, Y., Ogura, K., et al. Clinical significance of immunohistochemically detectable lymph node metastasis in adenocarcinoma of the ampula of Vater. Br. J. Surg., 2006; 93 : 221–225.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2011 Issue 3-
All articles in this issue
- Role VATS v léčení empyému hrudníku
- Vzdálený syndrom zraněného gliomu po stereotaktické biopsii – kazuistika
- Biliární komplikace po velkých resekcích jater
- Jednotná klasifikace plicních lymfatik. Cesta ke status quo
- Přednosti klasického operačního přístupu v chirurgické léčbě plicních metastáz
- Kvalita života po laparoskopické fundoplikaci v závislosti na předoperační symptomatologii
- Vplyv pooperačných komplikácií na prežívanie pacientov s karcinómom pankreasu
- Laparoskopické ošetření poranění tlustého střeva při kolonoskopii
- Nové možnosti diagnostiky karcinómu pankreasu
- Metastáza světlobuněčného renálního karcinomu do ductus choledochus
- Laparoskopická resekce pankreatu v experimentu a klinické praxi
- Laparoskopická distálna pankreatektómia pre neuroendokrinné nádory pankreasu – prvé skúsenosti
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Kvalita života po laparoskopické fundoplikaci v závislosti na předoperační symptomatologii
- Laparoskopická distálna pankreatektómia pre neuroendokrinné nádory pankreasu – prvé skúsenosti
- Laparoskopické ošetření poranění tlustého střeva při kolonoskopii
- Vplyv pooperačných komplikácií na prežívanie pacientov s karcinómom pankreasu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


