-
Medical journals
- Career
Mezenterická ischémia – neskoro rozpoznaná diagnóza, alebo zle liečené ochorenie?
: J. Radoňak; L. Lakyová; T. Toporcer; J. Bober
: L. Pasteura, Košice, Slovenská republika ; I. chirurgická klinika, Lekárska fakulta Univerzity Pavla Jozefa Šafárika, Košice, Fakultná nemocnica
: Rozhl. Chir., 2010, roč. 89, č. 4, s. 242-246.
: Monothematic special - Original
Cieľ:
Diagnostika a terapia mezenterickej ischémie ako príčiny náhlej príhody brušnej je vážnym problémom vzhľadom na jej 60–80% mortalitu. Štúdia prezentuje vlastné skúsenosti s diagnostikou a liečbou tohto ochorenia a porovnáva ich s výsledkami v literatúre.Materiál a výsledky:
V priebehu rokov 2000–2009 bolo chirurgicky ošetrených 39 pacientov (17 mužov, 21 žien, priemerný vek 73 Ī 9,43) s mezenterickou ischémiou. Resekciu tenkého a hrubého čreva podstúpilo 38,46 % pacientov, u 33,3 % sa resekovala časť tenkého čreva a v dvoch prípadoch (5,13 %) bol resekčný výkon kombinovaný s embolektómiou z artéria mesenterica superior. U 23,1 % sa vykonala vzhľadom na rozsah postihnutia iba exploratívna laparotómia. Štyria pacienti boli reoperovaní (dehiscencia anastomózy, perforácia tenkého čreva, dehiscencia operačnej rany, enterokutánna fistula). U 23 % pacientov nastali pooperačné komplikácie vyžadujúce si UPV pre respiračnú insuficienciu, ťažkú sepsu a kardiogénne príčiny. Mortalita predstavovala 53,8 %. V klinickom obraze dominovala bolesť brucha (79 %), zvracanie (61, 5%) a subileózny stav (35,9 %). Leukocyty vykazovali zvýšenú hladinu u 58,97 % pacientov. RTG sa ukázalo ako nešpecifické, USG malo 42,3% úspešnosť pri diagnostike.Záver:
Nízka výťažnosť použitých zobrazovacích metód, nešpecifický klinický obraz, komorbidita pacientov vo vysokom veku a oneskorený príchod do nemocnice výrazne zvyšujú mortalitu pacienta.Kľúčové slová:
mezenterická ischémia – USG – laboratórny skríning – nekróza čreva – resekcia – mortalitaÚVOD
Akútna črevná ischémia je život ohrozujúci stav, ktorého úspešný manažment predstavuje veľký problém [1]. Napriek pokrokom v diagnostike, v liečbe a pochopením patofyziológie ochorenia, za posledných niekoľko desaťročí sa mortalita tohto ochorenia znížila iba nepatrne. V priebehu posledných dvadsiatich rokov mortalita je udávaná medzi 60–80 percentami počas hospitalizácie na túto diagnózu [2]. Diagnostiku sťažuje zriedkavosť diagnózy, nešpecifické príznaky v klinickom obraze pacienta, limitovanosť niektorých zobrazovacích metód pri ileóznom stave, no výsledky zhoršuje aj prevažne vysoký vek postihnutých pacientov, komorbidita a neskorý príchod do nemocnice. Rovnako ako v diagnostike, ani v chirurgickej liečbe u tejto náhlej príhody brušnej neexistuje štandardizovaný postup [3]. Zložité rekonštrukčné výkony na cievach výrazne nezvyšujú prežívanie u pacientov porovnaním s jednoduchým resekčným výkonom.
Cieľom tejto retrospektívnej analýzy bolo porovnať desaťročné skúsenosti s diagnostikou a chirurgickou liečbou nášho pracoviska s výsledkami v zahraničnej literatúre.
MATERIÁL A METODA
Na podklade retrospektívnej analýzy boli do súboru boli zaradení všetci pacienti s diagnózou črevnej ischémie prijatí v priebehu desiatich rokov (2000–2009) na I. chirurgickú kliniku LF UPJŠ a FN LP v Košiciach. Každý zo súboru bol anamnesticky a klinicky vyšetrený na ambulancii alebo pri konziliárnom vyšetrení nášho chirurga na inom pracovisku. Po príjme na oddelenie bola u pacienta odobraná krvná vzorka na rutinné laboratórne vyšetrenie spracované hematologickým a biochemickým laboratóriom (krvný obraz, diferenciál a biochemický skríning). Za leukocytózu sa považovala hodnota > 10 000 buniek/mm3 a za referenčnú hodnotu C-reaktívneho proteínu v medziach normy sa podľa laboratória, kde boli spracované vzorky považuje hodnota < 5 mg/l. Dvadsaťšesť pacientov bolo zároveň aj ultrazvukovo vyšetrených a 28 pacientov malo urobený natívny röentgenový snímok brucha v stoji. Retrospektívna analýza hodnotí výskyt predispozičných faktorov pre toto ochorenie, percentuálne zastúpenie ťažkostí pacienta, úspešnosť diagnostických metód, časový postup v manažmente pacienta, ako aj výsledky operačnej intervencie, ich komplikácie a mortalitu na tomto pracovisku.
VÝSLEDKY
Súbor pacientov
Súbor 39 pacientov s diagnózou akútnej mezenterickej ischémie tvorí 17 mužov v priemernom veku 73 Ī 11,04 a 21 žien vo veku 73 Ī 8,53 (rozmedzie 43–84 rokov). Priemerný čas ťažkostí doma, ktorý udával pacient, bol 41 Ī 22,49 hod. a čas od prijatia do nemocnice po operačnú revíziu bol 12,32 Ī 14,33 hod.. Priemerná doba hospitalizácie predstavovala 7,32 Ī 6,65 dní.
Chirurgická liečba a komplikácie
V súbore 39 pacientov podstúpilo resekčný výkon na črevách 76,9 % pacientov a u ostatných vzhľadom na rozsiahly nález nezlučiteľný so životom sa vykonala iba exploratívna laparotómia. U 38,46 % pacientov bola pri revízii nájdená gangréna tenkého aj hrubého čreva, u 33,3 % pacientov sa resekovala iba časť tenkého čreva a v dvoch prípadoch (5,13 %) sa resekčný výkon kombinoval s embolektómiou z arteria mesenterica superior.
23,07 % pacientov bolo po operácii preložených na Kliniku anesteziológie a intenzívnej medicíny FNLP – traja pacienti pre respiračnú insuficienciu, traja pre septický šok a traja pre kardiogénnu príčinu. Jeden pacient bol preložený na Kliniku cievnej chirurgie pre embóliu do dolnej končatiny na tretí pooperačný deň.
Dvaja pacienti absolvovali „second look“ revíziu v druhý pooperačný deň vzhľadom na zhoršený pooperačný priebeh s podozrením na progresiu ischémie čreva, pričom v jednom prípade sa našla o perforácia jejuna nad anastomózou a v druhom prípade sa musela vykonať reresekcia jejuna pre pokračujúcu gangrénu. Jeden pacient bol v 13. pooperačný deň resuturovaný pre dehiscenciu operačnej rany a ďalší podstúpil operačnú revíziu a resekciu čreva v 24. pooperačný deň pre vznik enterokutánnej fistuly.
V 53,8 % došlo v pooperačnom období k exitu z dôvodu ťažkého generalizovaného stavu a rozvoju MODS (9 pacientov po exploratívnej laparotómii) a u ostatných dvanástich pacientov po resekčnom výkone sa konštatoval exitus pre kardiogénne príčiny (1x IM, 2x kardiálna dekompenzácia, 1x malígna dysrytmia), či pre ťažký septický šok. Priemerný čas od operácie po exitus bol 3,4 Ī 4,27 dňa.
Ultrazvukové vyšetrenie (USG)
USG bolo vykonané v 66,6 % prípadoch (26 pacientov). V skupine vyšetrených pacientov sme zaznamenali 15 falošne negatívnych USG nálezov s vylúčením možnosti akútnej mezenterickej ischémie a jedenásť pozitívnych nálezov, čo predstavuje 42,3% úspešnosť tohto zobrazovacieho vyšetrenia. Z celkovo trinástich ultrazvukom nevyšetrených pacientov deväť nebolo odoslaných na USG vzhľadom na príznaky peritoneálneho dráždenia, alebo pokročilého ileózneho stavu, podľa ktorých bola indikovaná neodkladná operačná revízia z vitálnej indikácie. V prípade falošne negatívnych nálezov bol vo väčšine prípadov röentgenológom interperetovaný nález ako ťažko hodnotiteľný vzhľadom na plynatosť čreva (Tab. 1).
1. Výsledky zobrazovacích a laboratórnych vyšetrení u pacientov s mezenterickou ischémiou Tab. 1. Results of depicting and laboratory examinations in patients with mesenteric ischemia 
RTG brucha
71,79 % pacientov malo natívny snímok brucha v stoji, prípadne niektorí boli vyšetrení horizontálnym lúčom. Z celkovo 28 vyšetrených pacientov u 13 sa zobrazili ojedinelé alebo viaceré hladinky ako príznak ileózneho stavu, u ostatných pacientov išlo o obraz meteorizmu hrubého čreva (Tab. 1).
Laboratórne vyšetrenia
Leukocyty vykazovali zvýšenú hladinu u 58,97 % všetkých pacientov. Priemerná hodnota bola 16,19 Ī 12,49 a to v rozmedzí 2,2–64 x 103/ml. Hladina CRP bola elevovaná v 43, 58 %, priemerná hodnota bola 23, 86 Ī 17,65 (Tab. 1).
Anamnéza a klinický obraz
Až 82 % pacientov s diagnózou akútnej mezenterickej ischémie mali pri prijatí v anamnéze ischemickú chorobu srdca s fibriláciou predsiení. Tretina z nich prekonala v minulosti infarkt myokardu alebo cievnu mozgovú príhodu. Až 71 % sa liečilo na arteriálnu hypertenziu a 23 % malo diabetes mellitus 2. typu. Všetky sledované predispozičné faktory pre vznik mezenterickej ischémie s percentuálnym zastúpením v našom súbore sú uvedené v tabuľke 2.
2. Percentuálne vyjadrený výskyt predispozičných faktorov pre vznik mezenterickej ischémie v súbore pacientov Tab. 2. Percentage rates of predisposing factors for the development of mesenteric ischemia in the patient group 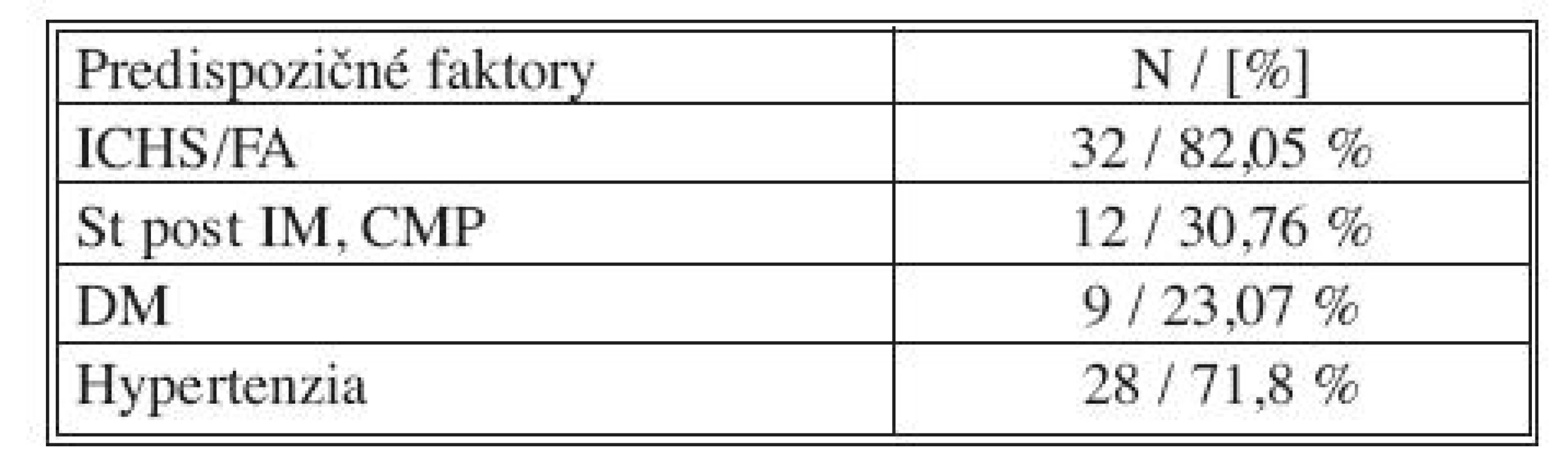
V klinickom obraze dominovala bolesť brucha prevažne viscerálneho charakteru (79 %). Niektorí pacienti udávali skôr kolikovitú bolesť ktorá sa zhoršila po jedle. Pätina pacientov mala v čase hospitalizácie už príznaky peritoneálneho dráždenia. Viac ako polovica pacientov mala nauzeu, či emézu, ani jeden pacient neudával hematemézu. Tretina pacientov udávala zástavu vetrov a stolice, pričom RTG nález svedčil pre subileózny až ileózny stav. Menšia časť pacientov mala naopak hnačkovité stolice, niektorí s prímesou krvi, či melénou (Graf 1).
1. Percentuálne vyjadrený výskyt symptómov u pacientov s diagnózou mezenterickej ischémie Graph 1. Percentage rates of symptoms in patients with mesenteric ischemia 
DISKUSIA
Akútna mezenterická ischémia predstavuje iba 1 % zo všetkých gastrointestinálnych ochorení [4], no jej následky sú katastrofálne. Napriek úspešnej a včasnej terapii 50–80 % pacientov zomiera v pooperačnom období [5]. Logistická regresná analýza ukázala vek nad 70 rokov, predĺženú dobu symptomaticky a z laboratórnych parametrov eleváciu AST a urei ako nezávislé prediktory mortality [6, 7]. Naopak pohlavie, predchádzajúca medikácia, iniciálne symptómy a príčina mezenterickej ischémie nevykazuje štatistickú signifikantnosť pri porovnaní skupiny pacientov, ktorí prežili so skupinou exitovaných [7].
Oneskorená diagnostika a operácia ešte viac zvyšuje úmrtnosť na túto diagnózu. Odklad operácie v intervale 10 hodín predstavuje 59% mortalitu a interval 37 hodín až 71% úmrtnosť [8]. Dokonca iní autori pripisujú 24 hodinovému odkladu nárast mortality zo 71 % na 87 % [9]. Je nutné si uvedomiť, že ide o diagnózu, ktorá postihuje vyššie vekové kategórie, ktoré reagujú často anergicky a ich príchod do nemocnice je už s niekoľkodňovou anamnézou neurčitých predchádzajúcich ťažkostí. Časová analýza v našej štúdii ukázala až priemernú 41 hodinovú dobu anamnézy ťažkostí pred hospitalizáciou a priemerný 12hodinový odklad operácie v dobe po prijatí do nemocnice. Tento čas bol nevyhnutný nielen na diagnostiku, ale aj pre predoperačnú prípravu pacienta a úpravu nízkych hemokoagulačných parametrov vzhľadom na častú antikoagulačnú terapiu v liekovej anamnéze pacienta pred operačným zákrokom. Odklad chirurgickej intervencie vedie k väčšej distenzii čriev, elevácii laktátu v krvnom sére, k akútnemu zlyhaniu obličiek, nutnej vazopresorickej podpore a k zmierneniu klinických príznakov bolestivosti brucha [10]. Preto skoré rozpoznanie akútnej mezenterickej ischémie je základom pre záchranu života pacienta, keďže ireverzibilná nekróza čriev je rozpoznaná u množstva pacientov až v časte explorácie abdomenu. V našej štúdii 76,9 % pacientov potrebovalo už resekciu čreva pri prvej operácii, v 34,1 % prípadoch bol dokonca stav hodnotený ako neresekabilný vzhľadom na excesívnu črevnú nekrózu. Iba v 5 percentách bola vykonaná úspešná embolektómia z arteria mesenterika superior s následným dlhodobým prežívaním po operácii. Podľa výsledkov niektorých autorov, pacienti, ktorí podstúpia embolektómiu alebo trombektómiu s resekciou čreva, majú vyššie prežívanie než pacienti iba s resekčným výkonom [9]. V niektorých prípadoch boli popísané pozitívne skúsenosti s mechanickou fragmentáciou trombu a súčasnou implantáciou stentu do stenotického miesta na podklade chronických zmien. U týchto pacientov s akútnou intestinálnou ischémiou lokálny stav nevyžadoval resekciu čreva [11]. Ide však skôr o kazuistiky než rozsiahle štúdie, keďže takáto liečba sa podarí iba vo výnimočných prípadoch včasnej diagnostiky. Na druhej strane rekonštrukčné výkony ako je bypass a grafting, lokálna endarterektómia a transaortálna endarterektómia neznižuje v konečnom dôsledku u akútnej mezenterickej ischémie mortalitu. Naopak, iní autori dosiahli lepšie výsledky po rekonštrukčnom výkone na cievach iba u chronickej mezenterickej ischémie, u akútnej formy sa týmto výkonom neznížila mortalita [3].
Názory na „second look“ revíziu od 12 do 48 hodín po prvej operácii sa rôznia. V jednej štúdii „second look“ operácia bola vykonaná v 40 % a ukázala až 72% malperfúziu. Mortalita sa pritom pohybovala od 59–100 % [9], čo je veľmi vysoké číslo. Iná štúdia preferuje druhú revíziu iba v prípade ponechania úseku čreva, kde je jeho vitalita otázna, teda v prípade, kedy pacient má rozsiahle poškodenie a snahou chirurga je zachrániť v čo najvyššej miere každý centimeter čreva. Je to najspoľahlivejšia metóda zistenia vitality čreva [12]. Okrem toho niektorí autori udávajú aj častý výskyt vazospazmu po revaskularizácii čreva. „Second-look“ pomocou laparoskopie dnes už substituuje možnosť „second look“ pomocou laparotómie, no jej spoľahlivosť ešte stále nie je hodnoverná [13]. V súbore našich pacientov sme pozorovali iba dva prípady potreby reresekcie čreva v dobe do 48 hodín po prvej operácii. Vzhľadom na vysokú komorbiditu a priemerný vek nad 70 rokov sme „second look“ revíziu indikovali iba v nutných prípadoch pri zhoršenom klinickom a laboratórnom náleze a prítomnosti väčšej produkcie z drénov, či náleze množstva tekutinových kolekcií v dutine brušnej podľa USG. Náš názor na neinvazívny pooperačný postup podporuje aj univariatná analýza, ktorá ukazuje, že renálna insuficiencia, vek nad 70 rokov, metabolická acidóza, dlhé trvanie symptómov a resekcia kľučiek čriev pri „second look“ operácii je asociovaná s vyššou mortalitou. U pacientov s pokročilým postihnutím čreva „second look“ neovplyvní významnou mierou výsledok chirurgickej liečby ani nezníži mortalitu. Preto je viac preferovaný individuálny prístup na podklade klinického obrazu a skúsenosti chirurga než univerzálny postup pri „second look“ operácii [14].
Úspešnosť predoperačného vyšetrenia sa pohybuje okolo 41 % [8]. V klinickom obraze dominuje bolesť brucha (95 %) [15], druhým najčastejším prezentujúcim sa symptómom v našej štúdii bola nauzea a zvracanie (61 %). Príznaky peritonitídy sa prejavili iba u dvadsiatich percent postihnutých. RTG brucha v stoji je nešpecifické, preto by sa malo použiť iba na vylúčenie obštrukcie resp. perforácie GIT. Pozitívny nález hladiniek je už neskorým príznakom ileózneho stavu [16]. V našej štúdii u 46 % pacientov s realizovaným RTG vyšetrením boli nájdené ojedinelé hladinky alebo dilatované kľučky tenkého čreva vyplnené tekutinou a vzduchom, čo svedčilo o ileóznom stave. USG vyšetrenie bolo často limitované meteorizmom, jeho záchytnosť predstavovala 42,3% úspešnosť. Serosanguinolentná tekutina v brušnej dutine u starších pacientov s bolesťami brucha, hemokoncentáciou a leukocytózou je silne podozrivá na mezenterickú venóznu trombózu. Hoci žiaden z laboratórnych testov nie je schopný potvrdiť ani vylúčiť mezenterickú ischémiu [17], je nevyhnutné urobiť všetky základné vyšetrenia. V rámci krvného obrazu často dominuje elevácia leukocytov, ktoré pri progresii ochorenia stúpa rovnako ako zápalovo parametre. Niektoré štúdie odporúčajú v skoro štádiu vyšetriť D-dimér ako skorý marker mezenterickej ischémie, no iné zas tvrdia, že tento parameter nie je senzitívny [18, 19]. Pravdepodobnosť rozvoja arteriálnej mezenterickej ischémie sa signifikantne zvyšuje s anamnézou predsieňovej fibrilácie, alebo predošlej anamnézy infarktu myokardu. Pravdepodobnosť sa zvyšuje aj s arteriálnou hypertenziou a príznakmi abdominálnej angíny [20], čo potvrdili aj výsledky našej štúdie.
Okrem klasických laboratórnych a zobrazovacích metód využívaných na väčšine pracovísk sú v literatúre popísané aj skúsenosti s inými menej konvenčnými vyšetrovacími metódami. V rámci niektorých štúdií bolo použité endoskopické vyšetrenie, pri ktorom sa však ukázalo, že nemá adekvátnu senzitivitu a špecificitu pri detekcii ischemických zmien a navyše nie je schopné vizualizovať tenké črevo, ktoré je často postihnuté. Magnetická rezonancia je sľubnou metodikou pri detekcii zmeny prietoku artérie mezenteriky superior pri chronickej ischémii, ale jej výťažnosť zatiaľ nie je odskúšaná v randomizovaných štúdiách [21]. Navyše relatívna zlá prístupnosť a nemožnosť použitia MRI v prípade urgentného stavu znemožňuje použitie tejto diagnostickej metódy na väčšine pracovísk u nás. CT-angiografia s 3D-rekonštrukciou je metódou diagnostickej voľby. Dnes sa konvenčná angiografia používa v kombinácii s endovaskulárnou liečbou (lýza, PTA, stenty). Skúsenosti nášho pracoviska s angiografickým vyšetrením nie sú bohaté, keďže ju nevyužívame štandardne pri každom podozrení na akútnu mezenterickú ischémiu, no objavili sa aj prípady falošnej pozitivity pri diagnostike uzáveru niektorej z hlavných vyživovacích artérií, čo viedlo k zbytočnej explorácii u pacienta. Analýza peritoneálnej tekutiny môže vykazovať elevovaný počet leukocytov, laktátdehydrogenázy a fosfátov, ibaže toto vyšetrenie nie je všeobecne akceptované v klinickej praxi [22].
Pri peroperačnej diagnostike vitality čreva niekedy nestačí iba vizuálne vyšetrenie povrchu čreva pri operačnej revízii pri rozpoznaní ischémie. Ide najmä o nonokluzívnu formu, pri ktorej sa seróza zdá byť vitálna napriek infarktizovanej mukóze. Použitie intravenózneho fluoresceínu pod Woodovou lampou sa ukázalo byť senzitívnym a špecifickým vyšetrením, no táto metóda nie je rozšírená a všeobecne akceptovaná [23]. Peroperačná dopplerova ultrasonografia je alternatívnou cestou zistenia vitality čreva, no množstvo štúdií nepozorovalo žiadnu výhodu v definitívnom výsledku pre pacienta porovnaním tohto vyšetrenia s klinickým posúdením črevnej vitality [24]. Predoperačná dopplerova ultrasonografia je úspešná v diagnostike stenóz nad 50 % pri chronickej mezenteriálnej oklúzii, no ako sa zdá, jej úloha pri diagnostike akútnej mezenteriálnej embolizácie je limitovaná a to najmä v prípade vzduchom naplnených kľučiek čreva [2, 25].
V experimentálnej medicíne sú skúšané rôzne neinvazívne diagnostické metódy na zistenie poruchy prietoku krvi, ako je napríklad rádionuklidové zobrazenie na identifikáciu infarktizácie čriev, alebo PET zobrazenie prietoku pečene. Výrazné obmedzenie prietoku krvi pečeňou perzistuje počas reperfúzie čreva, preto sa táto metóda dá využiť aj po revaskularizačnom výkone na črevách [26]. Niektoré experimentálne štúdie sa zaoberajú diagnostikou akútnej mezenterickej ischémie vyšetrením laboratórnych parametrov z krvného séra, ako napríklad plazminogénu, ako štatisticky signifikantného markeru skorej diagnostiky arteriálnej a venóznej mezenterickej ischémie [27].
ZÁVER
Úlohou chirurga pri diferenciálnej diagnóze mezenterickej ischémie je správna a rýchla indikácia na operáciu tak, aby zredukovala v čo najvyššej možnej miere katastrofické následky pokročilej gangrény čreva nezlučiteľnej so životom. Ani v dobe moderných zobrazovacích metód sa pri diagnostike sa neznížila vysoká mortalita tohto ochorenia. Pri diagnostike sa na väčšine pracovísk používa klinické vyšetrenie, laboratórny skríning a zo zobrazovacích metód ultrazvukové vyšetrenie. Pozitívna anamnéza predispozičných faktorov, promptne využité moderné zobrazovacie techniky v diagnostike a rýchle rozhodnutie chirurga pre revíziu znižuje mortalitu a morbiditu v pooperačnom období pacienta.
Prof. MUDr. Jozef Radoňak
tr. SNP 1
040 11 Košice
Slovenská republika
e-mail: radonak@gmail.com
Sources
1. Kassahun, W. T., Schulz, T., Richter, O., Hauss, J. Unchanged high mortality rates from acute occlusive intestinal ischemia: six year review. Langenbecks Arch. Surg., 2008; 393 : 163–171.
2. Debus, E. S., Diener, H., Larena-Avellaneda, A. Acute intestinal ischemia. Chirurg., 2009; 80 : 375–385.
3. Cho, J. S., Carr, J. A., Jacobsen, G., Shepard, A. D., Nypaver, T. J., Reddy, D. J. Long-term outcome after mesenteric artery reconstruction: a 37-year experience. J. Vasc. Surg., 2002; 35 : 453–460.
4. Schneider, T. A., Longo, W. E., Ure, T., Vernava Mesenteric ischemia: acute arterial syndromes. Dis. Colon Rectum, 1994; 37 : 1163–1174.
5. Stamatakos, M., Stefanaki, C., Mastrokalos, D., Arampatzi, H., Safioleas, P., et al. Mesenteric ischemia: still a deadly puzzle for the medical community. Tohoku J. Exp. Med., 2008; 216 : 197–204.
6. Kougias, P., Lau, D., El Sayed, H. F., Zhou, W., Huynh, T. T., Lin, P. H. Determinants of mortality and treatment outcome following surgical interventions for acute mesenteric ischemia. J. Vasc. Surg., 2007; 46 : 467–474.
7. Huang, H. H., Chang, Y. C., Yen, D. H., Kao, W. F., Chen, J. D., Wang, L. M., Huang, C. I., Lee, C. H. Clinical factors and outcomes in patients with acute mesenteric ischemia in the emergency department. J. Chin. Med. Assoc., 2005; 68 : 299–306.
8. Luther, B., Moussazadeh, K., Müller, B. T., Franke, C., Harms, J. M., Ernst, S., Sandmann, W. The acute mesenteric ischemia – not understood or incurable? Zentralbl. Chir., 2002; 127 : 674–684.
9. Safioleas, M. C., Moulakakis, K. G., Papavassiliou, V. G., Kontzoglou, K., Kostakis, A. Acute mesenteric ischaemia, a highly lethal disease with a devastating outcome. Vasa, 2006; 35 : 106–111.
10. Eltarawy, I. G., Etman, Y. M., Zenati, M., Simmons, R. L., Rosengart, M. R. Acute mesenteric ischemia: the importance of early surgical consultation. Am. Surg., 2009; 75 : 212–219.
11. Demirpolat, G., Oran, I., Tamsel, S., Parildar, M., Memis, A. Acute mesenteric ischemia: endovascular therapy. Abdominal imaging, 2007; 32 : 299–303.
12. Landis, M. S., Rajan, D. K., Simons, M. E., Hayeems, E. B., Kachura, J. R., Sniderman, K. W. Percutaneous management of chronic mesenteric ischaemia: outcomes after intervention. J. Vasc. Intervent. Adiol., 2005; 16 : 1319–1325.
13. Seshadri, P. A., Poulin, E. C., Mamazza, J., Schlachta, C. M. Simplified laparoscopic approach to second-look laparotomy: a review. Surg. Laparosc. Endosc. Percutan. Tech., 1999; 9 : 286–289.
14. Kaminsky, O., Yampolski, I., Aranovich, D., Gnessin, E., Greif, F. Does a second look operation improve survival in patients with peritonitis due to acute mesenteric ischemia? A five-year retrospective experience. World J. Surg., 2005; 29 : 645–648.
15. Park, W. M., Gloviczki, P., Cherry, K. J., Hallett, J. W., Bower, T. C., Panneton, J. M., et al. Contemporary management of acute mesenteric ischemia: Factors associated with survival. J. Vasc. Surg., 2002; 35 : 445–452.
16. Yasuhara, H. Acute Mesenteric Ischemia: The Challenge of Gastroenterology. Surg. Today, 2005; 35 : 185–195.
17. Sreenarasimhaiah, J. Diagnosis and management of intestinal ischamemic disorders. B.M.J., 2003; 326 : 1372–1376.
18. Altinyollar, H., Boyabatli, M., Berberoglu, U. D-dimer as a marker for early diagnosis of acute mesenteric ischemia. Thromb. Res., 2006; 117 : 463–467.
19. Kurt, Y., Akin, M. L., Demirbas, S., Uluutku A. H., Gulderen, M., Avsar, K., Celenk, T. D-dimer in early diagnosis of acute mesenteric ischaemia secondary to arterial occlusion in rats. Eur. Surg. Res., 2005; 37 : 216–219.
20. Vokurka, J., Olejnik, J., Jedlicka, V., Vesely, M., Ciernik, J., Paseka, T. Acute mesenteric ischemia, 2008 ; 85 : 1349–1352.
21. Ha, H. K., Rha, S. E., Kim, A. Y., Auh, Y. H. CT and MR diagnoses of intestinal ischemia. Semin. Ultrasound CT MR, 2000; 21 : 40–55.
22. Kurland, B., Brandt, L. J., Delaney, H. M. Diagnostic tests for intestinal ischemia. Surg. Clin. North Am., 1992; 72 : 85–105.
23. Galandiuk, S., Fazio, V. W., Petras, R. E. Fluorescein endoscopy: a technique for noninvasive assessment of intestinal ischemia. Dis. Colon Rectum, 1988; 31 : 848–853.
24. Ballard, J. L., Stone, W. M., Hallett, J. W., Pairolero, P. C., Cherry, K. J. A critical analysis of adjuvant techniques used to assess bowel viability in acute mesenteric ischemia. Am. Surg., 1993; 59 : 309–311.
25. Zwolak, R. M. Can duplex ultrasound replace arteriography in screening for mesenteric ischemia? Semin. Vasc. Surg., 1999; 12 : 252–260.
26. Kiss, J., Naum, A., Kudomi, N., Knuuti, J., Iozzo, P., Savunen, T., Nuutila, P. Non-invasive diagnosis of acute mesenteric ischaemia using PET. Eur. J. Nucl. Med. Mol. Imaging, 2009; 36 : 1338–1345.
27. Gunerhan, Y., Koksal, N., Kayahan, M., Eryavuz, Y., Sekban, H. Diagnostic value of plasminogen activity level in acute mesenteric ischemia. World J. Gastroenterol., 2008; 14 : 2540–2543.
28. Gearhart, S. L., Delaney, C. P., Senagore, A. J., Banbury, M. K., Remzi, F. H., Kiran, R. P., et al. Prospective assessment of the predictive value of alpha-glutathione S-transferase for intestinal ischemia. Am. Surg., 2003; 69 : 324–329.
29. Evennett, N. J., Petrov, M. S., Mittal, A., Windsor, J. A. Systematic and pooled estimates for the diagnostic accurancy and serological markers for intestinal ischemia. World J. Surg., 2009; 33 : 1374–1383.
30. Sizlan, A., Guven, A., Uysal, B., Yanarates, O., Atim, A., et al. Proanthocyanidin protects intestine and remote organs against mesenteric ischemia/reperfusion injury. World J. Surg., 2009; 33 : 1384–1391.
31. Edwards, E. M., Cherr, G. S., Crave, T. E., Olsen, A. W., Plonk, G. W., Geary, R. L., et al. Acute occlusive mesenteric ischemia: Surgical management and outcomes. Annals of vascular surgery, 2003; 17 : 72–79.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2010 Issue 4-
All articles in this issue
- Spinal Cord Stab Injury Associated with Modified Brown-Séquard Syndrome Symptoms – A Case Review and Literature Overview
- Reliability of Load-Sharing Classification in Indications for Anterior Vertebral Body Replacement in Thoracolumbar Spine Fractures
- Peroperative Detection of Pulmonary Lesions during Mini-invasive Surgery
- Iatrogenic Injuries of the Pulmonary Artery
- Malignant Ascites – Optional Management using Hyperthermic Peroperative Chemotherapy (HIPEC)
- Mesenteric Ischemia – Late Diagnosis or Managed Disease?
- Perforation of the Intestine – Rare Complication of Choledocholithiasis
- Rare Tumors of the Gallbladder and Bile Ducts. A Case Review
- Surgical Treatment of Liver and Pulmonary Metastases of Colorectal Carcinoma
- Stapler Procedure for Anal Prolapse and Hemorrhoids: Long-term Results
- Improving of Treatment Safety in Emergency Thoracic Surgery
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Malignant Ascites – Optional Management using Hyperthermic Peroperative Chemotherapy (HIPEC)
- Mesenteric Ischemia – Late Diagnosis or Managed Disease?
- Stapler Procedure for Anal Prolapse and Hemorrhoids: Long-term Results
- Rare Tumors of the Gallbladder and Bile Ducts. A Case Review
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

