-
Medical journals
- Career
Střednědobé výsledky a přežití nemocných po radikální retropubické prostatektomii (RRP) v současných podmínkách českého zdravotnictví
: L. Šafařík 1; R. Bílek 2; J. A. Víšek 3; K. Novák 1; J. Ťuíková 1; Martin Pešl 1; J. Stolz 1; J. Dvořáček 1
: Urologická klinika 1. LF UK a VFN Praha, přednosta prof. MUDr. J. Dvořáček, DrSc. 1; Endokrinologický ústav Praha, přednosta doc. MUDr. V. Hainer, CSc. 2; Fakulta sociálních věd UK, CESES FSV UK, děkan prof. RNDr. J. A. Víšek, CSc. 3
: Rozhl. Chir., 2009, roč. 88, č. 1, s. 21-26.
: Monothematic special - Original
Autoři podávají přehled střednědobých (5 let) výsledků přežití skupiny nemocných po radikální retropubické prostatektomii (RRP) ve vztahu k předoperačním i pooperačním parametrům jednotlivých nemocných. Zatímco 5leté přežití je možno očekávat v 92,4 %, pak relativně vyšší věk (většina > 65 let) s sebou přináší vyšší riziko pooperačních komplikací, které jsou však porovnatelné s mezinárodními standardy. Nebyla zaznamenána perioperační mortalita (0 %), mikční obstrukcí po operaci trpělo 13,4 % pacientů, ale ta byla vždy vyřešena endoskopicky. Kontinence s maximálně jednou vložkou na 24 hodin byla u 77,2 % nemocných, zatímco těžká inkontinence byla v 3,3 % případů. Spontánní erektilní funkce byla zachována jen minimálně 4,3 %, ale kromě vyššího věku v souboru se na tom jistě podílelo i více objektivních faktorů.
Klíčová slova:
radikální prostatektomie – karcinom prostaty – přežití – komplikaceÚVOD
Adenokarcinom prostaty (KP) byl v roce 2005 poprvé častěji diagnostikován v ČR než nové případy karcinomu plic a dosáhl počtu 4 846 nově diagnostikovaných onemocnění. Stal se tak nejčastěji diagnostikovaným nádorem mužů. Nárůst je dáván do souvislosti se zlepšenou diagnostikou a prodloužením věku populace než absolutním zvýšením incidence. Úmrtnost, která do roku 2004 stoupala, však v roce 2005 poprvé poklesla na 27,9/100 000 z 31,5 v předchozím roce. [1] Je to trend patrný ve všech rozvinutých zemích, kde sice není rutinně prováděn skrínink, ale je prováděna časná detekce u poučené populace. Vzhledem k tomu, že není dosud známá příčina vzniku tohoto onemocnění – diskutují se vlivy supresorových genů TrKA, p53, MXI, PTEN, případně chromozomální delece 10q24 – radikální operace je nejlepším způsobem léčby orgánově ohraničeného karcinomu na prostatu (OCD). Metodou volby je radikální prostatektomie prováděná retropubickým, laparoskopickým nebo perineálním způsobem. Pokud je nemocný schopen tuto operaci absolvovat, pak jeho vyhlídky na přežití 7 i více let jsou vyšší než 90 % (cancer specific survival) [2, 3]. Výsledky onkologické i funkční (kontinence, erektilní funkce), stejně jako celkové a nádorově specifické přežití se liší nejen mezi pracovišti, ale i mezi jednotlivými chirurgy. V daném případě byl vyhodnocen soubor 92 nemocných, kteří byli indikováni k RRP na Urologické klinice 1. LF UK a VFN Praha a byli operováni modifikovanou technikou podle Walshe pouze jedním chirurgem [4, 5].
MATERIÁL A METODA
Nemocní byli indikováni k operaci na základě vyšetření PSA, digitálního rektálního vyšetření DRE a transrektální bioptické punkce prostaty TRUS Bx. Přestože je zvykem indikovat nemocné k této operaci s hodnotami PSA pod 20 ng/ml, v souboru se vyskytují i nemocní s hodnotami podstatně vyššími, u nichž vlastní přání a obava z nádoru byly vyhodnoceny jako rozhodující. Podobně tomu bylo i s kalendářním věkem nemocných a případně celkové rizikovosti hodnocené podle 4 stupňů ASA. Přehled o vyhodnocené skupině podává tabulka 1. Nezanedbatelnou roli hrály i technické faktory. Přestože operace byly prováděny na univerzitním pracovišti, v současné době nepatří zdaleka ke standardnímu vybavení brýle pro mikrochirurgii, čelní světlo s možností pedálové fokusace, použití malých klipů v oblasti apexu prostaty k oddělení nervově cévního svazku a sada speciálních zahnutých pravoúhlých peanů. Z výše jmenovaných důvodů byly operace prováděny především se zaměřením na kompletní odstranění nádorem postižené prostaty a následně s ohledem na další faktory. Rozdíly proti výše citované Walshově technice spočívaly v tom, že po obšití dorzálního Santorinského plexu Vicrylem byla přerušena uretra pod apexem bez okamžitého naložení anastomotických stehů, prostata byla retrográdně oddělena od rekta na podvazech a po její separaci od baze měchýře byla sliznice měchýře evertována a zúžena do tvaru ,Mercedes‘ na prostup pinzety. Následně byly naloženy na uretru 4 stehy, které zabíraly jen malou část sliznice, zato větší část hlubokého příčného pánevního svalu na místech 2, 4, 8 a 10 (po směru hodin s č. 12 pod sponou). Po protažení Foleyovy cévky 18-20 F do měchýře byly stehy zakotveny ve stěně měchýře a dotaženy. U všech nemocných s PSA nad 10,1 ng/ ml a/nebo Gleasonovým skóre byla provedena lymfadenektomie.
1. Celková charakteristika souboru Tab. 1. Overall Characteristics of the Subject Group 
VÝSLEDKY
Přežití ve vztahu k základnímu onemocnění
Shrnutí základních charakteristik souboru podává tabulka 1. Ačkoli byl medián věku 65 let, více než polovina pacientů tento věk překročila a věkový průměr této skupiny byl 69 let. Zatímco ve většině vyspělých zemích je RP prováděna u OCD na základě zvýšené hodnoty PSA a následné verifikace TRUS Bx (stadium Tlc), pak v tomto případě to bylo jen u 57,6 % nemocných. Z toho vyplývá i poměrně vysoké procento lokálně pokročilých nádorů, přesahujících pouzdro prostaty (pT3a) a infiltrujících semenné váčky (pT3b) – celkem 23,9 %. Pozitivní okraj chirurgického řezu byl však jen ve 3 případech (3,3 %). Vzestup PSA nad 0,4 ng/ml po operaci v různém časovém intervalu byl zjištěn u 18 (19,6 %) pacientů, z toho 2 byli původně ve stadiu pTl (jeden však bral neoadjuvantní hormonální terapii, druhý zemřel na ICHS po necelých 4 letech s poslední hodnotou PSA 0,51).
Celkové přežití v souboru bylo 90,22 % za dobu 98 měsíců, tj. 8 let a 2 měsíce. Nádorově specifické přežití bylo 96,74 % (Kaplan-Meier) (graf 1). Nemocní, kteří zemřeli na generalizaci přežili po operaci 12,5, 22,4 a 42 měsíců (Tab. 2). Kumulativní celkové přežití nemocných nebylo závislé na věku p < 0,65489, na vstupním PSA p < 0,60289, na adjuvantní radioterapii p < 0,49894 ani na kombinaci adjuvantní radioterapie a hormonální terapie, p < 0,68056. Bylo však významně závislé na tom, zda nemocný po operaci měl či neměl biochemickou recidivu PSA p < 0,04174. U nemocných zemřelých na generalizaci byla závislost ještě zřetelnější, p < 0,00102.
1. Celkové přežití nemocných po RRP Graph 1. Overall survival rates of patients following RRP 
2. Zemřelí po RRP Tab. 2. Deaths following RRP 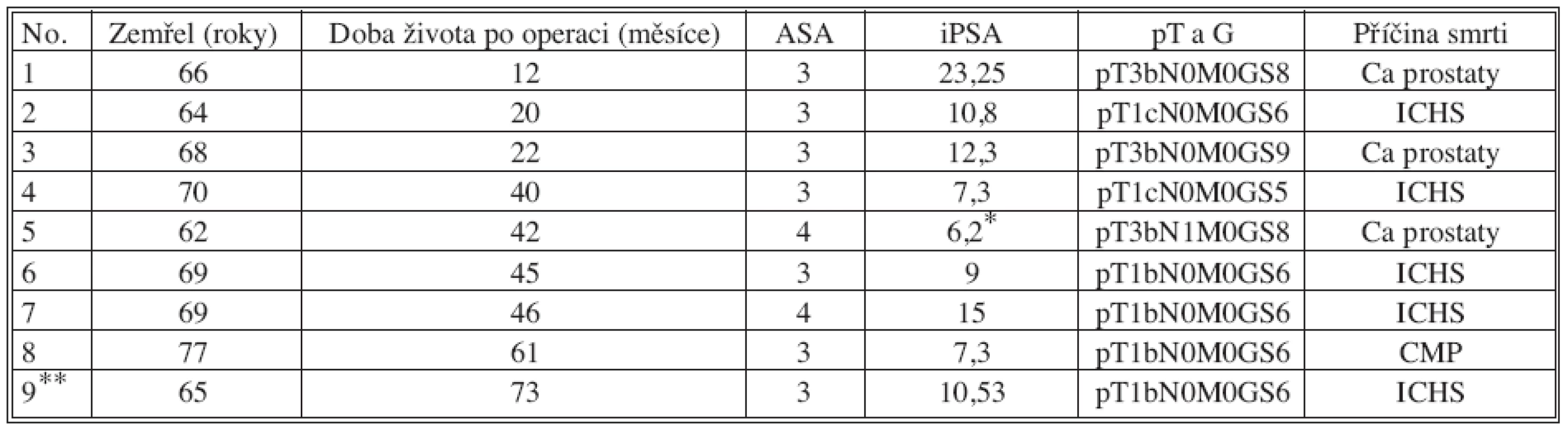
* – známá neoadjuvantní terapie ** – též po radikální operaci pro adenokarcinom ledviny (RCC) Pětileté přežití po RRP v celém souboru bylo 92,4 % (85 z 92) bez ohledu na příčinu úmrtí a bylo významně závislé na biochemické recidivě (> 0,4), p < 0,011. Na adjuvantní radioterapii a/nebo hormonální terapii však závislé nebylo, p < 0,34238. U 10 nemocných z 18 (55,6 %), kteří měli po operaci biochemickou recidivu, se podařilo získat alespoň 3 výsledky PSA a po zkonstruování Gompertzovy křivky odečíst zdvojovači čas (DT). Přestože nejde o velký soubor, výsledky jsou zajímavé. Rozpětí zdvojovacího času je 21–783 dní, přičemž nemocný s nejkratší hodnotou zemřel na generalizaci v nejkratším intervalu (Graf 2), zatímco nemocní s hodnotami nad 70 dní přežívají bez klinických obtíží léta (Graf 3). Jeden nemocný s DT 37 dní má recidivu až po 3 letech, ale jde o mladšího nemocného, který měl bezprostředně po operaci radioterapii a nyní je na hormonální blokádě. Nesignifikantnost výsledků je ale jistě ovlivněna 2 nemocnými, zemřelými na generalizaci, u nichž se nepodařilo získat výsledky PSA před úmrtím z jiných pracovišť. Byla nalezena významná pozitivní korelace mezi dobou přežití po operaci a mezi dobou, která uplynula mezi datem operace a datem překročení hranice PSA 0,4 ng/ml po operaci, Spearman Rank Order = 0,667, p < 0,05. Nepřímo úměrné a statisticky významné bylo porovnání předoperační hodnoty PSA a DT pomocí párového T-testu, p < 0,014, t = -3,03. Pokud byla srovnána hodnota pooperačního nadiru (nejnižší hodnoty) PSA s DT, pak byla signifikantnost testu ještě vyšší, p < 0,009, t < -3,28 (čím nižší nadir, tím delší čas k překročení hranice 0,4).
2. Doubling time (DT) – 21 dní 
3. Doubling time (DT) – 261 dní 
Přežití ve vztahu k celkovému stavu nemocných
Vzhledem k tomu, že RRP patří mezi nejnáročnější operace v urologii nejen proto, že jde o to zbavit nemocného malignity a prodloužit jeho přežití, ale že tyto operace přicházejí v úvahu prakticky vždy ve věku nad 50 let. V našem souboru jde většinou o nemocné ve věku nad 65 let (Tab. 1). Proto je nutné počítat s celou řadou komorbidit, které významným způsobem ovlivňují nejen samu operaci, ale i pooperační průběh. Jde o celkový interní stav vyjádřený kvantitativně kategoriemi AS A (1–4). Krevní ztráty jsou ovlivněny nejen faktorem operujícího a jeho technickými možnostmi při předpokládaných normálních koagulačních parametrech, ale i pokročilostí aterosklerotických změn na cévách v tomto věku, přítomnosti diabetů a dalších systémových onemocnění. Z hlediska návratu kontinence, erektilní funkce případně vytvoření striktury v dolních močových cestách je důležitá i perfuze (event. ischemizace) oblasti nově vytvořené uretro-vezikální anastomózy. Závislosti jednotlivých komplikací v souboru na předoperačních parametrech jsou uvedeny v tabulce 3.
3. Peroperační parametry a korelace komorbidit Tab. 3. Intraoperative variables and correlation between comorbidities 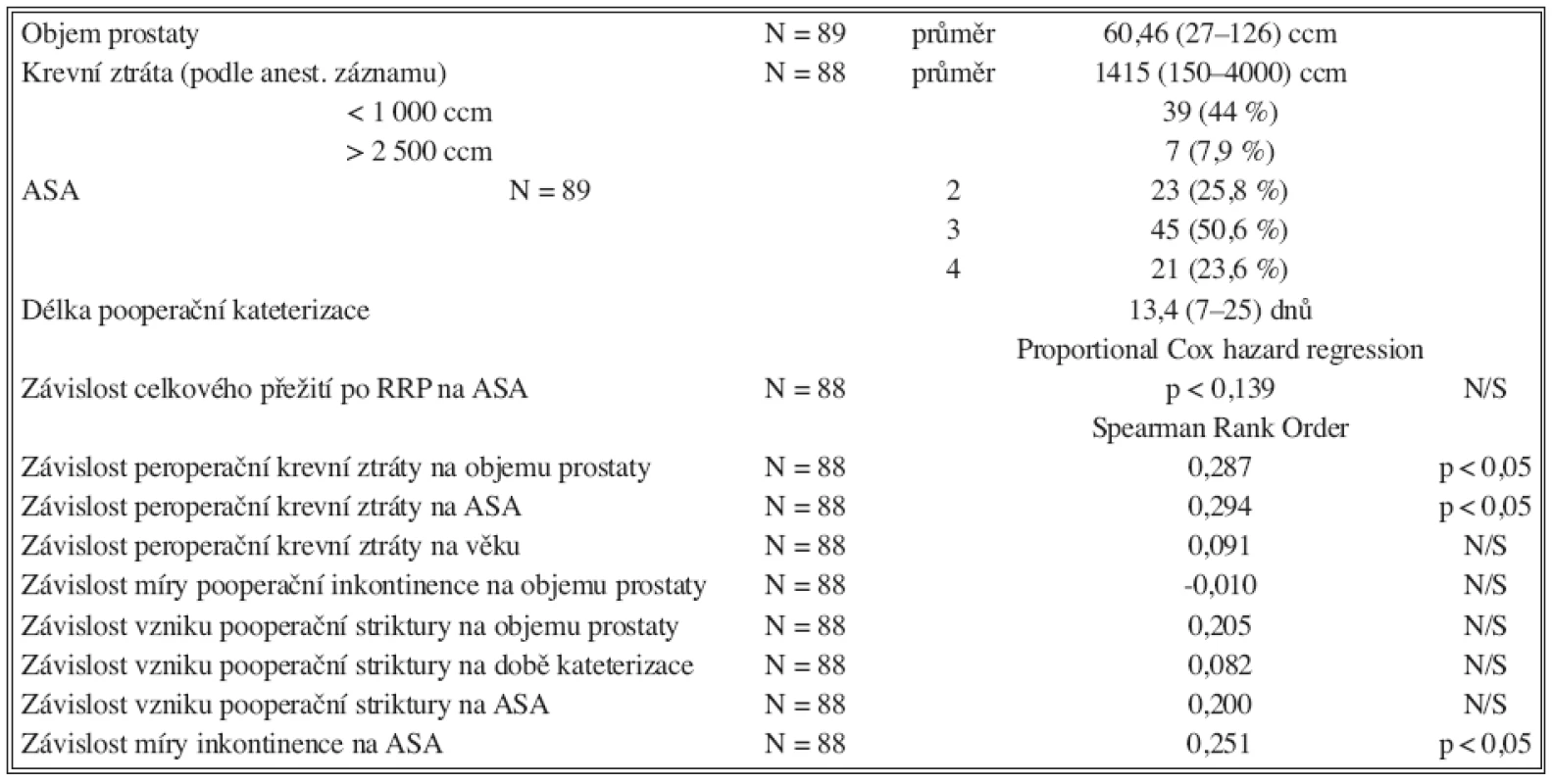
N/S – nesignifikantní Komplikace
Zaznamenali jsme jednu (1,1 %) bezprostřední pooperační revizi (do 24 hodin) pro krvácení u 69letého nemocného, který měl velmi těžký diabetes na inzulinu, jež nebyl dobře kompenzován dlouhodobě před operací (r. 2003). Krevní ztráta dohromady i s operací byla cca 4 000 ml. Nemocný se po revizi a současné kompenzaci diabetů zhojil, ale měl opakované infekce močových cest i v dalším průběhu. Přesto žije dodnes, je po adjuvantní radioterapii 71 Gy pro pT3N0M0GS7 nález, jeho PSA z předoperačních 18,1 kleslo na 0,042 a v době psaní tohoto článkuje opět na interně pro kompenzaci diabetů. Peri - operační mortalita (< 30 dní) nebyla zaznamenána (0 %).
Celkem 12 (13,4 %) nemocných mělo pooperačně strikturu v místě anastomózy nebo v uretře, která byla řešena optickou uretrotomií podle Sachse. Incize byla důsledně provedena na č. 12 bez vodícího drátu a na 48 hodin byla ponechána tenká cévka, zpravidla 14 F. U 2 nemocných bylo nutné operaci opakovat a 2 nemocní měli v důsledku obstrukce cystolitiázu vyžadující další řešení.
Z hlediska pooperační kontinence bylo zjištěno, že jen 3 (3,3 %) nemocní potřebují 3 a více vložek denně. Střední stupeň inkontinence (1–2 vložky/24 hodin) vykazovalo 18 nemocných (19,6 %). Jeden nemocný si nechal implantovat umělý svěrač, při čemž opakovaně uvedl, že potřebuje jen 2 vložky za 24 hodin a urodynamicky měl zachovalou aktivitu sfinkteru s kapacitou měchýře > 300 ccm. Tíže pooperační inkontinence byla výrazně závislá na věku a patologickém stadiu pT, p < 0,001 (Wilcoxonův párový test). Jen 4 nemocní uvedli, že mají po operaci erekci dostatečnou k tomu, aby mohli uskutečnit pohlavní styk za současného použití farmakoterapie.
DISKUSE
Prezentovaný soubor nemocných po RRP představuje skupinu mužů, u které byl diagnostikován klinicky ohraničený adenokarcinom prostaty a kteří byli schopni/přáli si radikální operaci. Na rozdíl od většiny podobných souborů, jen o málo více než polovinu tvořili nemocní s opravdu lokalizovaným karcinomem prostaty pTl-2. Naopak více jak polovina nemocných byla starší 65 let. Tyto faktory spolu s technickými možnostmi pracoviště do značné míry limitují možnosti provedení operace se zachováním nervově cévních svazků k obnovení časné kontinence a zachování erektilní funkce po operaci. Přesto je patrné, že pokud byli operováni a do souboru zahrnuti nemocní s lokálně pokročilým onemocněním, u nichž byla prostata odstraněna i s okolní tukovou a lymfatickou tkání (tzv. free margin), pak to celkové přežití nijak významně negativně neovlivnilo. Naopak reziduální nádor (positive margin) vedl vždy v poměrně krátké době k úmrtí nemocného – medián 22 měsíců. Biochemická recidiva se vyskytla u 19,6 % nemocných, ale nevedla bezprostředně k úmrtí. Podobné hodnoty byly zjištěny u jiných souborů, Witjes et al. 23 % po 4 letech, Soloway et al. 21,6 % po 2 letech, AUS et al. 40,6 % po 3,16 letech [2]. Mnohem podstatnější byla dynamika růstu pooperačního PSA. Zdvojovací čas (PSADT) se statisticky významně zkracoval s narůstající hodnotou PSA před operací. Arlen at al. potvrdili, že pokud PSADT je < 3 měsíce, pak prognóza nemocného (metastázy a smrt) je velmi špatná. Naopak pokud je tato doba > 15 měsíců, pak nezjistili úmrtí ani po 15 letech poté, co bylo PSA detekovatelné po operaci. V rozpětí mezi 3 a 15 měsíci zatím nebylo možné najít jednotné rozhraní, které by indikovalo dobrou nebo špatnou prognózu [11, 12]. Doba celkového přežití nemocných pozitivně korelovala s prodlužující se dobou, během které nemocný dosáhl hranice biochemického relapsu 0,4 ng/ml [13]. Tento nález je v souladu s tím, že adenokarcinom prostaty se chová velmi individuálně a posuzovat prognózu jen podle absolutní hodnoty PSA je zcela nedostatečné. Současné možnosti adjuvantní léčby jsou zatím omezené a následná radioterapie a/nebo hormonální terapie nevedly ke statisticky významnému prodloužení života.
Nejobávanější peroperační komplikací RRP je krvácení, především z dorzálního Santorinského plexu. Vzhledem k četnosti a velikosti žil, které zde vertikálně prorážejí pánevní dno a relativně užší pánvi u mužů, bývá někdy obtížné udržet krevní ztrátu v hodnotách pod 1 000 ml/operace, zvláště pokud je nemocný obézní [14]. Rabbani uvádí v souboru 3465 RRP operovaných v Memoriál Sloan Kettering Cancer Center v New Yorku v 6,1 % peroperační krevní ztrátu vyšší než 2 500 ml (!), tj. u 211 nemocných. Hodnoty daleko nižší, kolem 300 ccm, jsou dosahovány zpravidla u laparoskopických operací, pokud je provádí zkušený operatér. Pokud má nemocný obstrukční příznaky, pak se zpravidla jedná o strikturu v místě anastomózy, méně často o strikturu uretry a někdy dokonce jen o akutní infekci močových cest, pro kterou relativní zúžení v místě vezikouretrální anastomózy není dočasně průchodné. Procenta komplikací v Rabbaniho souboru byla: retence 4,3 %, striktura uretry 3,9 %, infekce 3,5 % [15]. Našich 13,4 % zcela odpovídá součtu citovanému Rabbanim z nejnovější doby. Nejlepším řešením obstrukce v dolních močových cestách po operaci je dočasné založení epicystostomie bez pokusu o katetrizaci. Po přeléčení infekce se často může průchodnost anastomózy spontánně obnovit. Sami jsme toto pozorovali nejméně ve 2 případech, zatímco pokusy o katetrizaci mnohdy skončí strikturou z poranění uretry. Vyskytne-li se cystolitiáza, pak je mnohem lepší zvážit otevřenou cystolitotomii než relativně dlouhé drcení endoskopicky. To pak vede zpravidla k výraznému zhoršení inkontinence a nezřídka i k restriktuře v oblasti anastomózy (v našem souboru zaznamenáno 1x). Výjimkou je možnost použití flexibilního cystoskopu s holmiovým laserem. Určitý podíl nemocných má obtíže s kontinencí, a to i po době delší než 1 rok. Nicméně téměř 80 % nemocných bylo s kontinencí spokojeno a případnou vložku nosili spíše pro jistotu. Zajímavé, i když nikoli nevysvětlitelné, bylo naše zjištění korelace míry pooperační inkontinence s celkovým interním stavem nemocného (Spearman Rank Order = 0,251, p < 0,05). Penson et al. nejnověji uvádějí, že 5 let po RRP je zcela plně kontinentních jen 35 % (!) pacientů, naopak zcela inkontinentních jsou jen 3 %. Výrazné potíže s kontinencí má 11 %. Pokud nemocní hodnotí stav kontinence jakožto kvalitu snižující jejich životní standard, pak po 5 letech nemá žádný problém jen 45 % nemocných a menší problém 42 %, ostatní (13 %) mají obtíže velké nebo zcela invalidizující [16]. Zajímavé srovnání nabízejí Wilt et al., kteří uvádějí, že zatímco v mortalitě nemocných po RRP a ponechání reziduálního nádoru není rozdíl mezi operatéry provádějícími více či méně než 43 operací ročně za předpokladu, že jde o větší centra, pak morbidita spojená s inkontinencí byla nižší u operatérů, provádějících větší počet operací ročně [17, 18]. Autoři vyhodnotili několik studií zabývající se touto problematikou a dospěli k názoru, že i méně zkušený operatér, je-li pod kontrolou zkušenějšího, a má-li zázemí dobré následné péče, dosáhne dlouhodobě lepších peroperačních výsledků, než pokud by pracoval na malém pracovišti a prováděl jen několik RRP ročně (< 10). Výsledný efekt pro pacienta z hlediska kvality jeho dalšího života je ale odvislý od zkušenosti a precizní techniky, kterou je spíše schopen uplatnit zkušenější operatér.
Erektilní funkce nebyla v našem souboru statisticky vyhodnocena. Jen 4 nemocní uvedli možnost pohlavního styku po operaci, ale zde je nutné vycházet i z jiných faktorů. Ve srovnání se zahraničními prameny, kde celá řada nemocných užívá farmakoterapii na podporu erekce hned od operace, většina našich nemocných ji ani nechtěla, převážně z ekonomických důvodů. Dalším faktorem byl průměrně vyšší věk nad 65 let a v neposlední řadě byla uváděna i absence vhodné partnerky. Ve výše citované studii 1 288 nemocných 5 let po RRP je uvedeno, že po této době má jen 28 % nemocných pohlavní styk, zatímco 55 % jej není vůbec schopno. Sildenafil zlepší erektilní funkci u 62 % nemocných, ale jen v případě, že jejich věk je pod 60 let. Nad 65 let věku je možno očekávat zlepšení po sildenafilu jen v 8 % a 61 % nemocných v tomto a vyšším věku uvedlo, že nepozorovalo žádné zlepšení.
ZÁVĚR
Radikální prostatektomie prováděna retropubicky (RRP) je stále nejčastěji prováděnou operací pro klinicky lokálně ohraničený karcinom prostaty (OCD) u nás. V našich podmínkách je možné dosáhnout 5leté přežití po operaci v 92,4 % případů při celkem přijatelné morbiditě nemocných. Lepších výsledků je možno dosáhnout zlepšenou časnou detekcí KP a operací většího podílu nemocných ve stadiu Tlc a v mladším věku. Hodnocení úspěšnosti operace by mělo vycházet ze sledování alespoň 5 let a mělo by být zaměřeno především na přežití, onkologickou a funkční problematiku. Při aplikaci srovnatelných technických podmínek z referenčních pracovišť je možné zlepšit i funkční výsledky především u erektilní funkce u nemocných. Je však možné, že s postupem miniaturizace techniky nakonec i tyto operace budou indikovány převážně pro laparoskopické nebo robotické výkony.
MUDr. L. Šafařík, CSc., FEBU
Urologická klinika 1. LF UK a VFN Praha
Ke Karlovu 6
128 00 Praha 2
e-mail: lsafarik@hotmail.com
Sources
1. Aktuální informace č. 59/2007, ÚZIS ČR, s. 3.
2. Eastham, J. A., Scardino, P. T. Radical prostatectomy. In: Campbell‘s Urology, 8th Ed., Saunders 2002 : 3080–3106.
3. Kattan, M. W., Wheeler, T. M., Scardino, P. T. Postoperative nomogram for disease recurrence after radical prostatectomy for prostate cancer. J. Clin. Oncol., 1999; 17 : 1499–1507.
4. Walsh, P. C., Donker, P. J. Impotence following radical prostatectomy: Insight into etiology and prevention. J. Urol., 1982; 128 : 492–497.
5. Walsh, P. C., Quinlan, D. M., Morton, R. A., et al. Radical retropubic prostatectomy. Improved anastomosis and urinary continence. Urol. Clin. North Am., 1990; 17 : 679–685.
6. Gleason, D. F., Mellinger, G. T. VACURG: Prediction and prognosis for prostatic adenocarcinoma by combining histologie grading and clinical staging. J. Urol., 1974; 111 : 58–64.
7. Steinberg, D. M., Sauvageot, J., Piantadosi, et al. Correlation of prostate needle biopsy and radical prostatectomy Gleason grade in academie and community settings. Am. J. Surg. Pathol., 1997; 21 : 566–576.
8. Foster, L. S., Jajodia, P., Fournier, G. J., et al. The value of prostate specific antigen and transrectal ultrasound guided biopsy in detecting prostatic fossa recurrences following radical prostatectomy. J. Urol., 1993; 149 : 1024–1028.
9. Malkowicz, S. B. Sérum prostate-specific antigen elevation in the post-radical prostatectomy patient. Urol. Clin. N. Am., 1996; 23 : 665–675.
10. Laird, A. K. Dynamics of tumor growth. Br. J. Cancer, 1964; 18 : 490–502.
11. Arlen, P. M., Bianco, F., Dahut, W. L., et al. Prostate specific antigen working group: Guidelines on prostatě specific antigen doubling time. J. Urol., 2008; 179 : 2181–2186.
12. Ramírez, M. L., Nelson, E. C., deVere White, R. W., et al. Current applications for Prostate-specific antigen doubling time. Eur. Urol., 2008; 54 : 291–302.
13. Pound, C. R., Partin, A.W., Eisenberger, M. A., et al. Natural history of progression after PSA elevation following radical prostatectomy. JAMA, 1999; 281 : 1591–1597.
14. Walsh, P. C. Anatomie radical retropubic prostatectomy. In: Campbell‘s Urology, 8th ed., Saunders 2002 : 3107–3129.
15. Rabbani, F. The incidence and predictors of complications of radical prostatectomy. AUA NY Section, Berlin, Germany, Sept. 6–13, 2008.
16. Penson, D. F., McLerran, D., Feng, Z., et al. 5-year urinary and sexual outcomes after radical prostatectomy: results from the prostatě cancer outcomes study. J. Urol. Suppl., 2008; 179: s. 40–45.
17. Wilt, J. T., Shamlyian, T. A., Taylor, B. C., et al. Association between hospital and surgeon radical prostatectomy volume and patient outcomes: a systematic review. J. Urol., 2008; 180 : 820–829.
18. Koppie, T. M., Guillonneau, B. Predictors of incontinence after radical prostatectomy: where do we stand? Eur. Urol., 2007; 52 : 22–25.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2009 Issue 1-
All articles in this issue
- Metastasis of Melanoma Malignum in Distal Ileum like Rare Causation of Ileocoecal Invagination – Case Report
- Laparoscopic Splenectomy – Our Experience
- Ruptured Mycotic Aneurysm of the Abdominal Aorta Managed Using a Superficial Femoral Vein Graft– A Case Review
- Neurogenous Cervical Tumors
- Postoperative Monitoring of the Esophageal Gastroplasty Perfusion Rate
- Mid-term Outcomes and Survival Rates in Patients with Radical Retropubic Prostatectomy (RRP) Under Current Czech Healthcare System
- A Necrotizing Fasciitis of an Abdominal Wall after a Cholecystectomia – A Case Report
- Surgical Treatment in Vertical Talus
- Necrotizing Fasciitis – A Rare Complication of Laparoscopic Appendectomy
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Necrotizing Fasciitis – A Rare Complication of Laparoscopic Appendectomy
- Neurogenous Cervical Tumors
- Laparoscopic Splenectomy – Our Experience
- Mid-term Outcomes and Survival Rates in Patients with Radical Retropubic Prostatectomy (RRP) Under Current Czech Healthcare System
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

