-
Medical journals
- Career
18F-FDG PET/CT obraz Erdheimovy-Chesterovy nemoci – přehled českých pacientů
Authors: Zdeněk Řehák 1,2; Renata Koukalová 1; Jiří Vašina 1; Václav Ptáčník 3; Petr Szturz 4; Josef Karban 5; Jindřich Polívka 5; Zdeněk Adam 4
Authors‘ workplace: Oddělení nukleární medicíny, MOÚ Brno, ČR 1; Regionální centrum aplikované molekulární onkologie, MOÚ Brno, ČR 2; Ústav nukleární medicíny, 1. lékařské fakulty UK a Všeobecné fakultní nemocnice v Praze, ČR 3; Interní hematologická a onkologická klinika, LF MU a FN Brno, ČR 4; I. interní klinika – klinika hematologie, 1. lékařské fakulty UK a Všeobecné fakultní nemocnice v Praze, ČR 5
Published in: NuklMed 2018;7:50-52
Category: Original Article
Overview
Úvod:
Erdheimova–Chesterova nemoc (ECD) je vzácné onemocnění ze skupiny histiocytárních chorob. Cílem práce bylo porovnat 18F-FDG PET/CT nálezy u pacientů s touto chorobou v ČR
Metody:
V ČR bylo provedeno celkem 44 18F-FDG PET/CT vyšetření u 6 pacientů s touto nemocí. Ve stagingových vyšetřeních 6 pacientů jsme hodnotili akumulaci 18F-FDG v místech obvyklého postižení, a to ve skeletu, mozku, v orbitě, paranasálních dutinách, periaortálně, v srdci, v plicích, perirenálně a na kůži.
Výsledky:
U všech pacientů bylo patrné 18F-FDG avidní postižení skeletu, u 5 z nich s maximem na dolních končetinách. U 5 ze 6 osob bylo zobrazeno postižení maxilárních dutin.
U 4 ze 6 nemocných bylo patrno vaskulární postižení a perirenální postižení. U 2 ze 6 pacientů bylo patrné 18F-FDG avidní postižení kůže a rovněž hypofýzy. U 1 ze 6 osob bylo patrné i postižení retrobulbárně a postižení srdce. U žádného ze 6 pacientů jsme nepozorovali postižení plic.
Závěr:
U všech 6 pacientů bylo 18F-FDG avidní postižení skeletu hlavní a pravidelnou částí PET/CT obrazu Erheimovy-Chesterovy nemoci. I další nálezy 18F-FDG avidního postižení (kardiovaskulární, CNS, paranasálních dutin, orbit, kůže, perirenálně) tak potvrzují známá pozorovaní u ECD.
Klíčová slova:
18F-FDG, PET/CT, Erdheimova-Chesterova nemoc
Úvod
Erdheimova-Chesterova nemoc (Erdheim-Chester disease (ECD) je idiopatická, velmi vzácná nemoc ze skupiny histiocytárních chorob. První popis této choroby zveřejnili v roce 1930 kardiolog William Chester spolu s vídeňským kolegou, patologem Jakobem Erdheimem, jako lipoid granulomatosis. 1 ECD je definována typickým histologickým obrazem xantogranulomatozního ložiska infiltrovaného pěnitými histiocyty s tukovými inkluzemi, foamy histiocytes, s typickým imunofenotypem (CD68+, CD1a-, a zpravidla i S100-) při imunohistochemickém vyšetření. 2 Tyto patologické histiocyty pravidelně proliferují v dlouhých kostech dolních končetin, což vede k typickému obrazu zbytnění trabekul a kortikalis v tibiích a femurech. Mohou však infiltrovat i oblasti retroperitonea, mediastina, plic, srdce, sleziny a jater, kůže či orbity a CNS se vznikem zánětlivých a fibrotických změn. 3 Počet popsaných případů ve světě se pohyboval v roce 2004 kolem 100 případů, v roce 2011 kolem 400 případů. 4 Zkušenosti s využitím 18F-FDG PET/CT vyšetření jsou relativně malé, spíše kazuistické. Onemocnění se vyskytuje až v dospělém věku, s průměrem 54 let, má velmi variabilní příznaky a je proto obtížně diagnostikovatelné. Klasickým a téměř vždy přítomným projevem je osteoskleróza tibií a femurů provázená bolestí končetin 5, např. Estrada-Veras a kol. udávají až v 95 % případů. 6 Mimokostní postižení je popisováno asi v 50 % případů. Nejzávažnější známky nemoci jsou plicní fibróza provázená dušností a srdeční selhání. 4,7–10 Někdy mohou být v popředí i celkové nespecifické příznaky či systémová zánětlivá reakce a důvodem k vyšetřování je tzv. horečka neznámého původu. 11
Cíl práce
Našim cílem bylo zjistit, kolik pacientů s ECD je sledováno v PET centrech v České republice, kolik u nich bylo provedeno 18F-FDG PET/CT vyšetření. Dále jsme chtěli zhodnotit nálezy nepředléčených pacientů a vzájemně je porovnat i se zkušenostmi jiných autorů.
Soubor a metodika
Cíleně byla oslovena všechna PET centra v ČR, ať již vybavena hybridními PET/CT či PET/MR skenery, s dotazem na evidenci pacientů s touto nemocí. Stagingová 18F-FDG PET/CT vyšetření všech pacientů jsme zpětně hodnotili na našem pracovišti. Jmenovitě jsme hodnotili akumulaci 18F-FDG v lokalizacích spojovaných s tímto onemocněním. Akumulace 18F-FDG přesahující referenční akumulaci jaterního parenchymu v dané studii jsme hodnotili jako pozitivní +, v případě překročení dvojnásobku akumulace jaterní jako silně pozitivní ++ v parametru SUVmax. V případě kostního postižení jsme hodnotili i jeho rozsah a přítomnost hot knees sign. V případě postižení hlavy jsme hodnotili infiltraci orbity, paranasálních dutin, v retroperitoneu jsme hodnotili přítomnost perirenálních akumulací 18F-FDG a fibrózy, v případě postižení kardiovaskulárního systému periaortální fibrózy, výpotky a postižení srdce, v případě postižení CNS infiltraci hypofýzy a jakékoli další postižení mozku či mening. Kožní postižení a xantelasmata byla hodnocena i z dokumentace pacientů. Pátrali jsme i po dalších postižených místech.
Výsledky
Zpětnou vazbou byla získána informace (datováno k 1. 7. 2018), že v PET centrech v ČR je evidováno 6 nemocných se známou a histologicky verifikovanou ECD. Tito pacienti podstoupili celkem 44 18F-FDG PET/CT, 1x 18F-FLT (tymidinové) PET/CT a 1x 18F-NaF (fluoridové) PET/CT vyšetření. Analyzována byla iniciální, předléčebná 18F-FDG PET/CT vyšetření 6 nemocných. Jednalo se o 4 muže a 2 ženy ve věku 36–76 let. U všech osob bylo postižení skeletu končetin, u 5 osob s vyšetřenými koleny i s typickým obrazem hot knees sign. Maximum akumulace 18F-FDG ve skeletu bylo u 3 pacientů v proximálních tibiích, u 2 v distálních femurech a u jednoho v lopatce. U 4 ze 6 nemocných jsme nalezli 18F-FDG avidní periaortální fibrózy (jako součást kardiovaskulárního postižení) a v jednom případě i s postižením srdce, perikardiálním výpotkem. Postižení paranasálních dutin jsme zaznamenali u 5 ze 6 nemocných, a to ve formě infiltrace maxilární dutiny (u jednoho pacienta i s histologickým ověřením). Plicní postižení nebylo zaznamenáno u žádného z pacientů. Postižení CNS jsme zaznamenali u dvou pacientů ve formě infiltrace stopky hypofýzy. Náznak metabolicky aktivních ložisek v mozku i thalamu jsme pak zobrazili ještě u 1 dalšího pacienta (toto postižení bylo jasně patrno na MR vyšetření mozku). Periorbitální a kožní postižení bylo patrno na 18F-FDG PET/CT vyšetření u 2 nemocných (dle dokumentace však bylo vizuálně přítomno periorbitálně u 3 nemocných, jiné typy kožního postižení byly u 2 osob). Z dalších postižených míst jsme u 1 ze 4 pacientů nalezli i metabolicky aktivní mesenteriální infiltrát. U 3 pacientů byl protrahovaný febrilní stav uveden jako jeden z vedoucích symptomů onemocnění. U 3 pacientů byl uveden v žádance o vyšetření i centrální diabetes insipidus. Podrobněji uvádíme výsledky hodnocení v tabulce a typické nálezy v obrázku.
Image 1. Sumarizace nálezů 18F-FDG PET/CT vyšetření u pacienta č. 1. Černobílé MIP projekce ukazují jednak rozsah snímání, ale zároveň dobře odráží i rozsah kostního postižení. Fúzované obrazy v axiální rovině pak ukazují detaily kostního, paranasálního, retroperitoneálního, kardiovaskulárního i hypofyzárního postižení 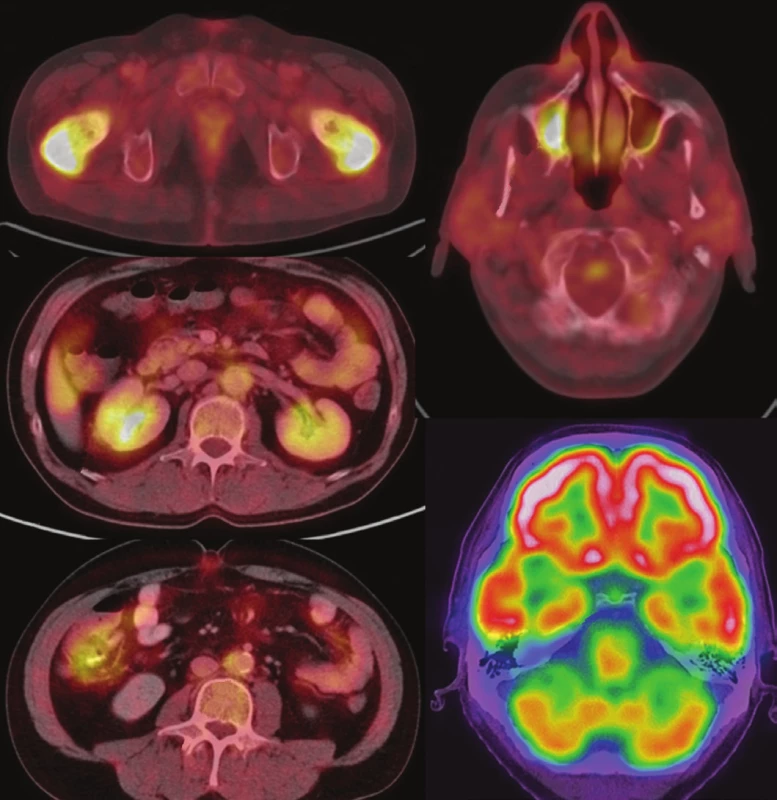
Diskuze
Je nám známo, že evidence všech pacientů v ČR vyšetřených pomocí 18F-FDG PET/CT vyšetření nemusí být úplná. Přesto jsme zachytili 6 nemocných, jejichž obrazy na 18F-FDG PET/CT můžeme považovat za staginová vyšetření ECD, neovlivněná terapií.
Image 2. (nahoře) Sumarizace nálezů 18F-FDG PET/CT vyšetření u pacienta č. 2. Černobílé MIP projekce ukazují rozsah snímání, odráží i rozsah kostního postižení. Fúzované obrazy pak ukazují detaily paranasálního, kardiovaskulárního, kostního, retroperitoneálního postižení. 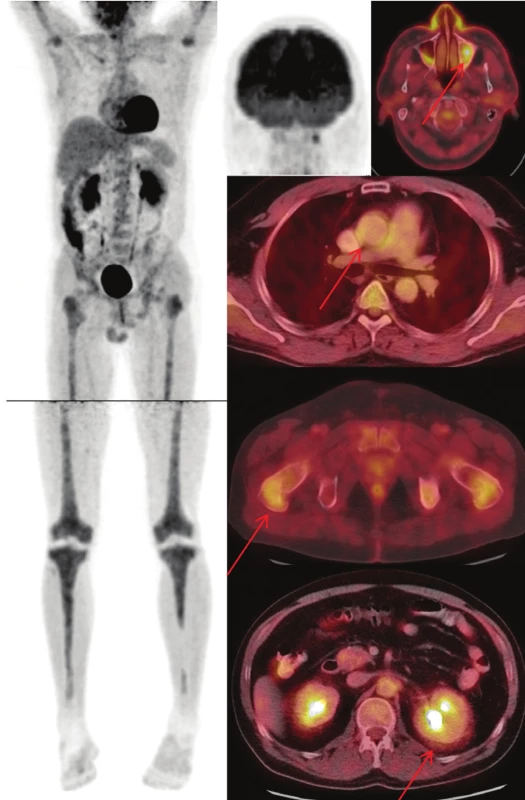
Image 3. (vlevo) Sumarizace nálezů 18F-FDG PET/CT vyšetření u pacienta č. 3. Černobílé MIP projekce ukazují rozsah snímání, odráží i rozsah kostního postižení. Fúzované obrazy pak ukazují detaily retroperitoneálního, kardiovaskulárního, kostního, paranasálního, orbitálního a kožního postižení. 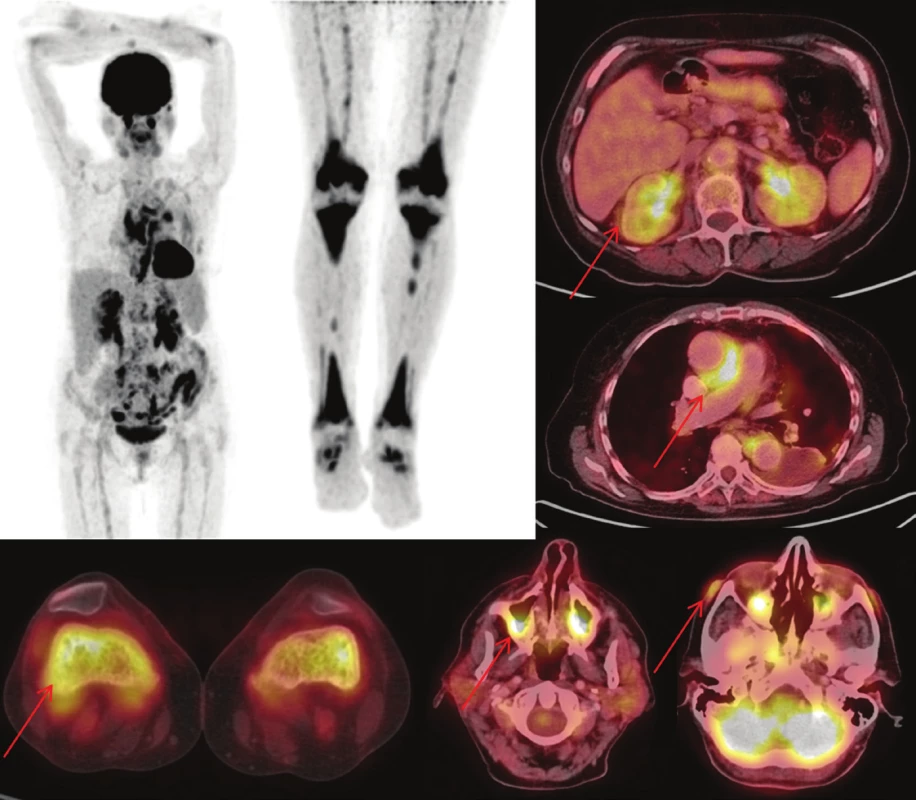
Table 1. Přehled pacientů, jejich PET/CT vyšetření i podrobně nálezů ve stagingových 18F-FDG PET/CT vyšetřeních. + označuje pozitivní nález ve smyslu akumulace 18F-FDG vyšší než akumulace jaterní v parametru SUVmax ++ označuje silně pozitivní nález ve smyslu akumulace 18F-FDG vyšší než 2násobek akumulace jaterní v parametru SUVmax 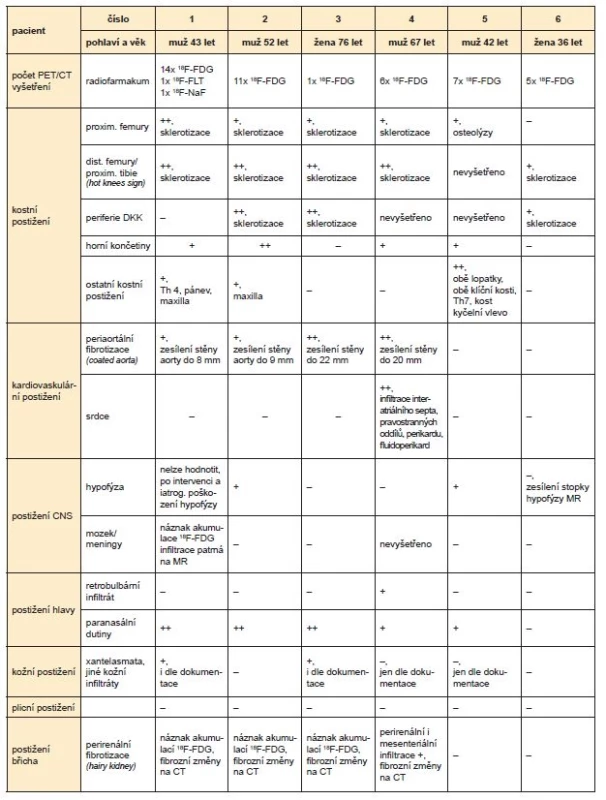
Kostní postižení
Kostní postižení je nejběžnějším typem postižení, postihuje typicky symetricky dlouhé kosti, častěji na dolních končetinách. Denzita kosti je ložiskově či difuzně zvýšena, bývá patrné zesílení trabekul, sklerózy a zesílení kortikalis. Proces postihuje zejména diafýzy a metafýzy s minimálními změnami v epifýzách. 2–4 Vysoká akumulace osteotropních radiofarmak při scintigrafii skeletu v distálních femurech a proximálních tibiích, hot knees sign, je typickým nálezem. 12,13 V některých případech jsou popisována i další místa postižení skeletu (zejména pánev a lebka, obratle). K zobrazení patologických ložisek ve skeletu lze použít jak scintigrafické vyšetření (asi nejběžnější), tak i vyšetření pomocí 18F-FDG PET/CT. 14,15 18F-FDG PET/CT vyšetření nabízí i možnost zhodnocení mimoskeletálního postižení nemoci. 18F-FDG avidní postižení bylo patrno i u všech 6 našich pacientů, včetně hot knees sign, u dvou z našich pacientů se kostní postižení blíží až extrémně rozvinutým nálezům známým z literatury. 11 Pro zobrazení kostního postižení nemoci pomocí 18F-NaF PET/CT vyšetření jsou dosud jen 2 kazuistiky. 16,17 Je pravděpodobné, že i takových vyšetření bude časem přibývat a dojde ke zhodnocení a porovnání se scintigrafickým vyšetřením nebo s 18F-FDG PET/CT vyšetřením.
Image 4. Sumarizace nálezů 18F-FDG PET/CT vyšetření u pacienta č. 4. Černobílé MIP projekce ukazují rozsah snímání, odráží i rozsah kostního postižení. Fúzované obrazy pak ukazují detaily kardiovaskulárního, retroperitoneálního, paranasálního, orbitálního i kostního postižení. 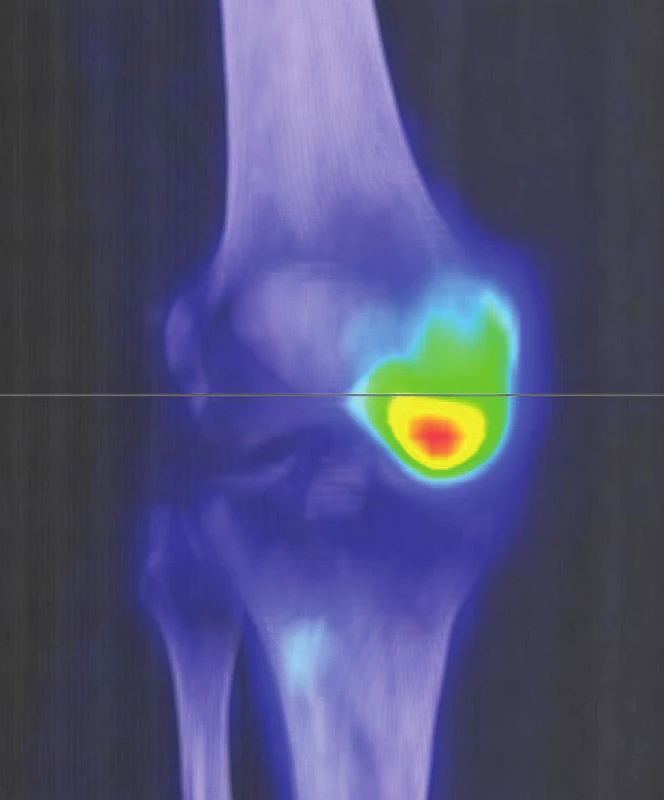
Postižení hlavy
Postižení hlavy může být u ECD několika typů. Jedním z nich jsou retrobulbární infiltráty (zpravidla symetrické) vedoucí až k exoftalmu. Jinými typy postižení hlavy jsou infiltrace paranasálních dutin nebo kožní infiltrace kolem očnice (vizuálně patrné) zvané xantelasma palpebrarum. 3–5,18,19 U našich nemocných jsme nacházeli v 5 případech ze 6 18F-FDG avidní infiltraci maxilárního sinu (v jednom případě i histologicky ověřenou) a 1x retrobulbární postižení. Hodnocení kožních změn typu xantelasma palpebrarum bylo retrospektivně z obrazové dokumentace omezené, v dokumentaci byla zmínka o periorbitálním kožním postižení u 3 ze 6 případů, a toto bylo patrné 2x i na 18F-FDG PET/CT vyšetření (zbytnění kůže, 18F-FDG avidní infiltrát). Jak až může vypadat extrémní případ 18F-FDG avidního retrobulbárního postižení ukázali např. Beylergil a kol. 20
Image 5. (vlevo) Sumarizace nálezů 18F-FDG PET/CT vyšetření u pacienta č. 5. Černobílá MIP projekce ukazuje rozsah snímání, odráží i rozsah kostního postižení ve snímaném rozsahu. Fúzované obrazy pak ukazují detaily hypofyzárního, paranasálního i kostního postižení. 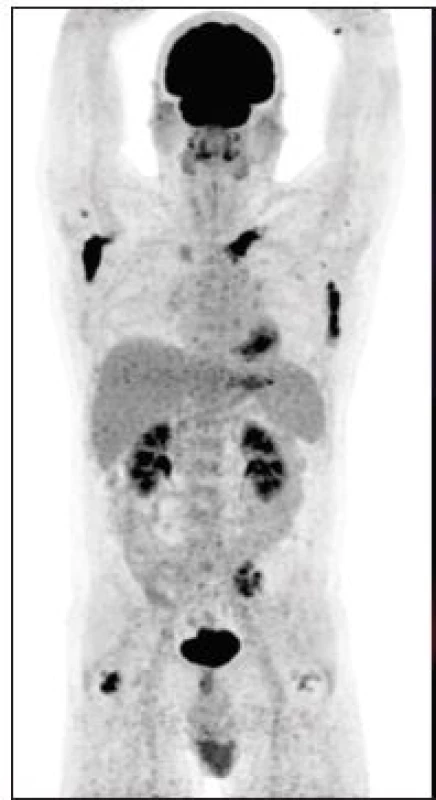
Image 6. (vpravo) Sumarizace nálezů 18F-FDG PET/CT vyšetření u pacienta č. 6. Černobílá MIP projekce ukazuje rozsah snímání, odráží i rozsah kostního postižení. Fúzované obrazy pak ukazují detaily kostního postižení v úrovní distálních femurů, proximálních a distálních tibií. 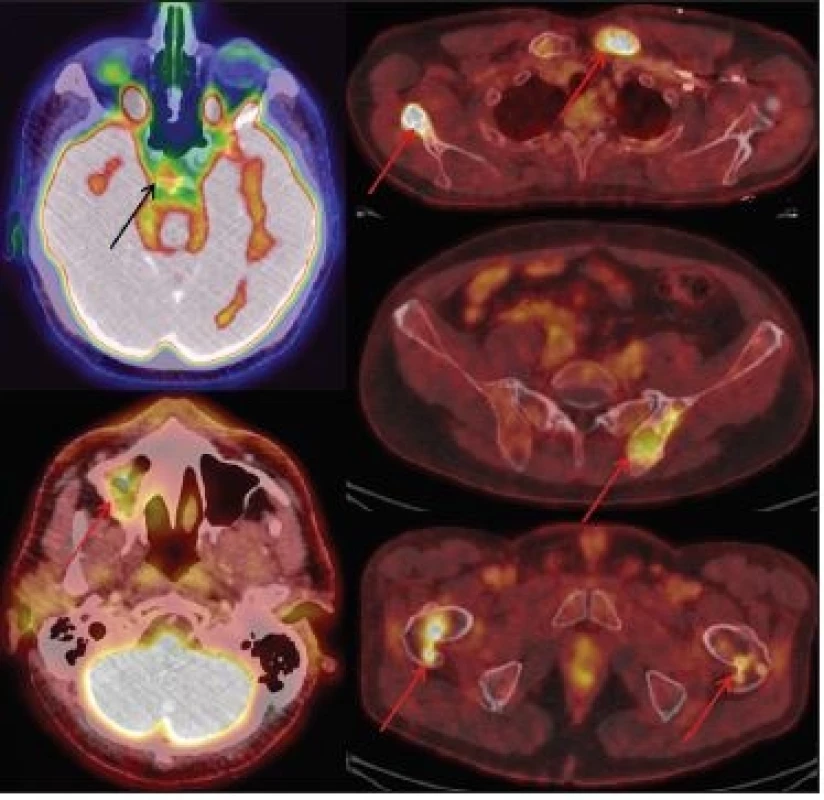
Postižení CNS
Tato nemoc postihuje i CNS. Téměř u poloviny pacientů jsou infitrace mozkového kmene, mozečku i mozku. Část pacientů (přibližně 1/3) mívá meningeální tumory. Nemoc má zvýšenou afinitu i k hypofýze nebo její stopce, projevující se hormonálně jako diabetes insipidus, a tento příznak může být i prvním projevem onemocnění. 21 Platí však, že pro nálezy zahrnuté do postižení CNS je metodou volby vyšetření pomocí MR. 22–24 18F-FDG PET/CT má spíše doplňkovou roli, nicméně u 2 ze 4 pacientů bylo zobrazitelné i 18F-FDG avidní postižení stopky hypofýzy. Jak mohou taková postižení vypadat i na 18F-FDG PET/CT vyšetření ukazují např. Garcia-Gomez a kol. (extrémní případ hypofyzární infiltrace) 14 a Sioka a kol. (postižení mozku). 25
Perirenální fibrotizace
Perirenální, retroperitoneální fibrotizace a infiltrace jsou nejčastějšími známkami postižení břicha, někdy se označují jako hairy kidney. 4 Pokročilé postižení může vést k hydronefróze s renálním selháním. Známky perirenálních fibrotizací byly patrny u 4 ze 6 našich pacientů spíše na CT vyšetření. Zvýšená akumulace 18F-FDG byla patrna jasně jen u jednoho z nich, u dalších spíše jen v diskrétních náznacích. Extrémním případem 18F-FDG avidního postižení ledvin a okolních tkání by mohl být případ, který publikovali Byeon a kol. 26, sekční nález masivního postižení ledvin dokumentovali Ohara a kol. 7 Postižení jater či sleziny je relativně vzácné. 27
Kardiovaskulární postižení
Běžnou známkou ECD bývá i periaortální fibróza, někdy nazývaná i coated aorta, a to až u 62 % případů, méně často bývá i srdeční postižení (pravostranné oddíly, perikard). 3,5,6,9,28 U 4 našich nemocných ze 6 byly patrné známky 18F-FDG avidní periaortální fibrózy, u jednoho i postižení pravostranných srdečních oddílů, perikardiální výpotek. Extrémní případy 18F-FDG avidního postižení ukazují např. Antunes a kol. 29 Sekční nález masivního kardiovaskulárního postižení dokumentovali Ohara a kol. 7
Plicní postižení
Onemocnění se může projevit plicními infiltracemi a vést až k plicní fibróze. U našich pacientů jsme tuto formu postižení nepozorovali. Naopak vyjádřena je plicní forma např. v publikaci bratislavských autorů. 30
Jsou nám známy pouze 3 práce, ve kterých by byly popisovány soubory pacientů s touto nemocí vyšetřených pomocí 18F-FDG PET/CT vyšetření. Garcia-Gomez a kol. publikovali soubor 6 nemocných, kteří 18F-FDG PET/CT vyšetření podstoupili v rámci stagingu. U jednoho ze 6 nemocných se jednalo jen o kožní postižení s negativním 18F-FDG PET/CT skenem i scintigrafickým vyšetřením skeletu. U 5/6 osob (84 %) ale byl 18F-FDG avidní nález ve skeletu a u 3/6 osob bylo patrno postižení CNS při PET/CT vyšetření. 14 Estrada-Veras a kol. publikují úctyhodných 58 vyšetřených, z toho 54 pacientů (93 %) mělo pozitivní 18F-FDG PET/CT sken. V souboru však mají velmi heterogenní skupinu pacientů nepředléčených, léčených i sledovaných, přesto jejich údaje o nejčastějších 18F-FDG avidních místech postižení považujeme za jedinečné. Nejčastější lokalizací byly oboustranně femury 74 %, oboustranně tibie 67 %, perirenální oblasti 35 %, oboustranně humery 24 %, plíce 24 %, mediastinum 24 %. 6 Arnaud a kol. publikovali soubor 31 pacientů (z toho 23 nepředléčených), u kterých udávají typické postižení dlouhých kostí u 55 %, postižení mozku u 26 %, vaskulární postižení u 38 %, postižení srdce u 19 %, postižení plic u 13 %, perirenální postižení u 3 %, postižení paranasálních dutin u 16 % a orbitální postižení u 13 %. 23 Objevují se rovněž zkušenosti s využitím 18F-FDG PET/CT vyšetření i ke sledování efektu terapie ECD. 23,30–32 Rovněž většina z provedených 18F-FDG PET/CT vyšetření u českých pacientů byla provedena až v průběhu léčby již známé nemoci v rámci hodnocení efektu či restagingu.
Závěr pro praxi
U nemocných s ECD lze pomocí 18F-FDG PET/CT vyšetření zobrazit postižení skeletu typicky na dolních končetinách, dále i kardiovaskulární, retroperitoneální, orbitální, paranasální postižení či postižení CNS nebo plic. ECD patří mezi velmi vzácné nemoci, lze tedy přepokládat, že jednotlivá PET centra se s touto nemocí mohou setkat ojediněle. Typy nálezů u ECD rovněž ukazují, že vyšetření ve standardním rozsahu vyšetření trupu (od baze lební k proximálním stehnům) nemusí pokrýt všechna typická místa (infiltrace CNS či hypofýzy, retrobulbární infiltrace, infiltrace distálních částí horních i dolních končetin). Naším cílem bylo informovat o obrazu této nemoci, což může pomoci v rámci širší diferenciální diagnostiky nejasných febrilních stavů, při diabetes insipidus i při nálezech vysoké akumulace osteotropních radiofarmak v končetinách při scintigrafickém vyšetření skeletu.
Podpořeno: MZ ČR – RVO (MOÚ, 00209805), MZ ČR – RVO (FNBr, 65269705), projekt LO 1413.
Sources
- Chester W. Uber Lipoidgranulomatose. Virchows Arch 1930;279 : 561–602
- Mazor RD, Manevich-Mazor M, Shoenfeld Y. Erdheim-Chester Disease: a comprehensive review of the literature. Orhanet Journal of Rare Diseases 2013;8 : 137 doi.org/10.1186/1750-1172-8-137
- Szturz P, Adam Z, Koukalová R et al. Erdheimova-Chesterova nemoc v obrazech. Vnitřní lékařství 2010;56(Suppl 2):2S170-178
- Arnaud L, Hervier B, Neel A et al. CNS involvement and treatment with interferon-alpha are independent prognostic factors in Erdheim-Chester disease: a multicenter survival analysis of 53 patients. Blood 2011;117 : 2778–2782
- Haroche J, Arnaud L, Amoura Z. Erdheim–Chester disease. Current opinion in rheumatology 2012;24 : 53-59
- Estrada-Veras JI, O’Brien KJ, Boyd LC et al. The clinical spectrum of Erdheim-Chester disease: an observational cohort study. Blood Advances 2017 : 1:357-366
- Ohara Y, Kato S, Yamashita D et al. An autopsy case report: Differences in radiological images correlate with histology in Erdheim–Chester disease. Pathology International 2018; 68 : 374–381
- Loeffler AG, Memoli VA. Myocardial involvement in Erdheim-Chester disease. Arch Pathol Lab Med 2004;128 : 682–685
- Berti A, Ferrarini M, Ferrero E et al. Cardiovascular manifestations of Erdheim-Chester disease. Clin Exp Rheumatol 2015;33(2 Suppl 89):155-163
- Haroche J, Cluzel P, Toledano D et al. Images in cardiovascular medicine. Cardiac involvement in Erdheim-Chester disease: magnetic resonance and computed tomographic scan imaging in a monocentric series of 37 patients. Circulation 2009;119:e597-e598
- Li N, Chen M, Sun H et al. Fever of unknown origin as the first manifestation of Erdheim-Chester disease. Case Reports in Clinical Medicine 2013;2 : 351-357
- Zanglis A, Valsamaki P, Fountos G. Erdheim-Chester disease: symmetric uptake in the (99 m)Tc-MDP bone scan. Hell J Nucl Med. 2008;11 : 164–167
- Pena Pardo FJ, Banzo Marraco I, Quirce Pisano R et al. Bone scintigraphy in Erdheim-Chester disease. Rev Esp Med Nucl. 2003;22 : 253–256
- García-Gómez FJ, Acevedo-Báñez I, Martínez-Castillo R et al. The role of 18FDG, 18FDOPA PET/CT and 99mTc bone scintigraphy imaging in Erdheim–Chester disease. European Journal of Radiology 2015;84 : 1586-1592
- Balink H, Hemmelder MH, de Graaf W et al. J. Scintigraphic diagnosis of Erdheim-Chester disease. Journal of Clinical Oncology 2011;29:e470-e472
- Caoduro C, Ungureanu CM, Rudenko B et al. 18F-fluoride PET/CT aspect of an unusual case of Erdheim-Chester disease with histologic features of Langerhans cell histiocytosis. Clinical Nuclear Medicine 2013; 38 : 541-542
- Sabino D, Vale RHBD, Duarte PS et al. Complementary findings on 18F-FDG PET/CT and 18F-NaF PET/CT in a patient with Erdheim-Chester disease. Radiologia Brasileira 2017; Epub May 18, 2017, doi.org/10.1590/0100-3984.2015.0172
- Arora A, Sharma S, Pushker N et al. Unusual orbital involvement in Erdheim Chester disease: a radiological diagnosis. Orbit 2012;31 : 338-340
- Karcioglu ZA, Sharara N, Boles TL et al. Orbital xanthogranuloma: clinical and morphologic features in eight patients. Ophthal Plast Reconstr Surg 2003;19 : 372–381
- Beylergil V, Carrasquillo JA, Hyman DM et al. Visualization of orbital involvement of Erdheim-Chester disease on PET/CT. Clinical Nuclear Medicine 2014;39 : 660-661
- Adam Z, Balšíková K, Pour L et al. Diabetes insipidus, následovaný po 4 letech dysartrií a lehkou pravostrannou hemiparézou – první klinické příznaky Erdheimovy-Chesterovy nemoci. Popis a zobrazení případu s přehledem informací o této nemoci.Vnitř Lek 2009;55 : 1173–1188
- Drier A, Haroche J, Savatovsky J et al. Cerebral, facial, and orbital involvement in Erdheim-Chester disease: CT and MR imaging findings. Radiology. 2010;255 : 586-594
- Arnaud L, Malek Z, Archambaud F et al. 18F-fluorodeoxyglucose-positron emission tomography scanning is more useful in follow up than in the initial assessment of patiens with Erdheim-Chester disease. Arthritis Rheum 2009; 60 : 3128–3138
- Lachenal F, Cotton F, Desmurs-Clavel H et al. Neurological manifestations and neuroradiological presentation of Erdheim-Chester disease: report of 6 cases and systematic review of the literature. J Neurol 2006; 253 : 1267–1277
- Sioka C, Estrada-Veras J, Maric I et al. FDG PET images in a patient with Erdheim-Chester disease. Clinical Nuclear Medicine 2014;39: doi: 10.1097/RLU.0b013e31828da5e6
- Byeon J, Kim KA, Hwang SS et al. Erdheim-Chester Disease with Perirenal Masses Containing Macroscopic Fat Tissue. Journal of the Korean Society of Radiology 2015;72 : 143-146
- Gupta A, Aman K, Al-Babtain M et al. Multisystem Erdheim‐Chester disease; a unique presentation with liver and axial skeletal involvement. British Journal of Hematology 2007;138 : 280-280
- Fudim M, Thorpe MP, Chang LL et al. Cardiovascular Imaging With 18F-Fluorodeoxyglucose Positron Emission Tomography/Computed Tomography in Patients With Fibroinflammatory Disorders. JACC: Cardiovascular Imaging 2018;11 : 365-368
- Antunes C, Graça B and Donato P. Thoracic, abdominal and musculoskeletal involvement in Erdheim-Chester disease: CT, MR and PET imaging findings. Insights into imaging 2014;5 : 473-482
- Šteňová E, Šteňo B, Povinec P et al. FDG-PET in the Erdheim–Chester disease: its diagnostic and follow-up role. Rheumatology International, 2012;32 : 675-678
- Adam Z, Petrášová H, Řehák Z et al. Hodnocení pětileté léčby Erdheimovy-Chesterovy nemoci anakinrou – kazuistika a přehled literatury. Vnitřní lékařství 2016; 62 : 44-56
- Janku F, Amin HM, Yang D et al. Response of histiocytoses to imatinib mesylate: fire to ashes. Journal of Clinical Oncology 2010;28,e633-e636
Labels
Nuclear medicine Radiodiagnostics Radiotherapy
Article was published inNuclear Medicine
2018 Issue 3
Most read in this issue- Přínos SPECT/CT pro diagnostiku osteochondrálního poškození kolenních kloubů
- 18F-FDG PET/CT obraz Erdheimovy-Chesterovy nemoci – přehled českých pacientů
- LYMFOSCINTIGRAFIE provedení vyšetření a jeho interpretace
- 55. DNY NUKLEÁRNÍ MEDICÍNY
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


