-
Medical journals
- Career
Protilátkové repetitorium – vyšetření protilátek proti koronaviru v běžné praxi
Authors: Zuzana Krátká 1,6; Václav Fejt 2; Radek Kučera 3; Hana Zelená 4,5
Authors‘ workplace: Imunologická laboratoř GENNET, s. r. o., Praha 1; Oddělení společných laboratoří, Nemocnice Havlíčkův Brod 2; Oddělení imunochemické diagnostiky, Fakultní nemocnice Plzeň 3; Centrum klinických laboratoří, Zdravotní ústav se sídlem v Ostravě 4; Katedra biomedicínských oborů LF OU v Ostravě 5; BIN – Centrum pro bayesovskou inferenci 64
Published in: Čas. Lék. čes. 2021; 160: 52-56
Category: Review Article
Overview
Stanovení protilátek proti koronaviru je významným diagnostickým nástrojem, který umožňuje potvrdit prodělanou infekci SARS-CoV-2. Zatímco v České republice se mu stále nedostává žádoucí pozornosti, v USA se již vyšetření protilátek stalo součástí diagnostických algoritmů.
Práce poskytuje ucelené informace o problematice testování protilátek, kinetice tvorby protilátek, typech testů, problematice virus neutralizačního testu. Zvláštní pozornost je věnována i správné interpretaci výsledků testů a problematice reinfekcí.
Klíčová slova:
protilátky – SARS-CoV-2 – COVID-19 – reinfekce – séroprevalence – virus-neutralizační test
ÚVOD
Česká republika patří k nejhůře zasaženým zemím koronavirovou epidemií. K 21. květnu 2021 evidujeme více než 1,65 milionu lidí po prodělaném onemocnění COVID-19 (15,5 % populace) a na 30 tisíc zemřelých (1). Počty lidí, kteří COVID-19 prodělali, velmi rychle rostou, ale my jako bychom si nevšimli, že se v populaci během této doby naprosto dramaticky změnil poměr „k infekci náchylných“ a „již odolných“ osob. Počet imunních osob je vyšší, než kolik uvádějí statistiky. Kapacita PCR laboratoří není neomezená a vyšetření není dostupné všem nemocným lidem, takže velké množství jich prodělá infekci bez provedení PCR nebo je u nich provedeno pozdě (a test už je negativní). Řada nemocných na test nejde záměrně, aby nemuseli být v karanténě. Další skupinu tvoří lidé s asymptomatickou infekcí. Všichni tito lidé nejsou evidovaní a proběhlou infekci u nich může odhalit stanovení protilátek.
Zatímco v Česku se vyšetření protilátek využívá zatím málo, americké Centrum pro kontrolu a prevenci nemocí (CDC) doporučuje hladiny protilátek sledovat (2). Podle CDC osoba s pozitivními protilátkami zjištěnými maximálně před 3 měsíci nebo v době kontaktu s infekční osobou a současně nevykazující známky infekce SARS-CoV-2 je vůči infekci imunní a nemusí být v karanténě. CDC provádí také pravidelné séroprevalenční studie ve všech státech USA s využitím vzorků od dárců krve (3). Poslední data z těchto měření jsou z poloviny března 2021, kdy byla v nejzasaženějších státech USA zjištěna 32 % séroprevalence (tedy potvrzení infekce na základě výskytu specifických protilátek). Jelikož je na tom Česko hůře než USA, můžeme očekávat, že u nás bude séroprevalence obdobná, možná i vyšší.
V článku shrnujeme naše zkušenosti s laboratorním vyšetřením protilátek u běžné populace. Naše doporučení byla v únoru a březnu 2021 publikována na webu proLékaře.cz jako dvoudílný seriál. Jelikož jde ovšem o velmi rychle se vyvíjející oblast, museli jsme původní texty zaktualizovat tak, aby jejich závěry byly platné i v době publikace tohoto článku.
KDY STANOVOVAT PROTILÁTKY
Pro potvrzení prodělané infekce se doporučuje stanovovat IgG protilátky v odstupu minimálně 2 týdnů po pozitivním PCR/antigenním testu, resp. po prvních klinických příznacích (4, 5). IgG protilátky se tvoří jako poslední (až po izotypech IgM a IgA), jsou nejspecifičtější a nejdéle přetrvávají v organismu. Produkce protilátek je velmi individuální a závisí na průběhu infekce, množství virové nálože, genetických predispozicích i věku pacientů. Protilátky se po infekci tvoří v různém množství a různě rychle.
V případě břevnické studie, prováděné u skupiny seniorů s průměrným věkem 85 let (6), byly vysoké hladiny IgG protilátek zjištěny ještě 10 měsíců po prodělané infekci. U mladých osob s mírným průběhem onemocnění poměrně často zjišťujeme jen nižší koncentrace protilátek a k jejich poklesu dochází poměrně záhy. Tedy nelze jednoznačně říci, kdy už protilátky nebudou prokazatelné, ale nejjistější je stanovit je do 3 měsíců od prodělaného onemocnění.
Využití průkazu protilátek pro potvrzení probíhající koronavirové infekce u pacientů s PCR negativním výsledkem
Pro průkaz akutně probíhající infekce se používá PCR nebo antigenní test. V případech s příznaky typickými pro COVID-19, ale s opakovaně negativním PCR testem, můžeme stanovit protilátky izotypu IgM či IgA nebo „celkový imunoglobulin“ a probíhající COVID-19 prokázat sérologicky. Nevýhodou těchto vyšetření je nižší specificita, proto je vhodné vyšetření doplnit konfirmačním virus-neutralizačním testem (VNT) specificky detekujícím protilátky pouze proti viru SARS-CoV-2. Není-li VNT dostupný, pak je vhodné později zopakovat vyšetření protilátek a sledovat vzestup IgG protilátek (5).
Využití protilátek pro potvrzení již získané imunity (a neinfekčnosti) u PCR-pozitivních osob
Po prodělané infekci může být RNA viru detekována na sliznicích po řadu týdnů až měsíců, ale daná osoba už nemusí být infekční. S tím počítáme u pacientů, kteří COVID-19 prodělali, a 3 měsíce po prodělaném onemocnění je pomocí PCR netestujeme. Jenže v případě, že člověk o prodělané nemoci neví, se dostáváme do diagnostické pasti. Jedinec je PCR-pozitivní, ale přitom už dávno po infekci. Toto vídáme nejčastěji u bezpříznakových jedinců, kteří podstupují rutinní PCR před operací či nástupem na rehabilitační pobyt. Tam, kde si jsou tohoto rizika vědomi, doplňují vyšetření protilátek, a jsou-li protilátky pozitivní a PCR nález je spojen s nízkou koncentrací viru (má Ct > 35), je osoba s pozitivním IgG považována za neinfekční (7).
PROTILÁTKY PROTI KORONAVIRU – TYPY A MOŽNOSTI VYŠETŘENÍ
Reakce na infekci není u všech stejná; protilátky se liší podle toho, s jakým virovým antigenem reagují. Ochranné protilátky (tzv. neutralizační) se tvoří proti proteinu S (spike). Jiné protilátky reagují s proteinem N (nukleokapsidovým). Zatímco struktura proteinu N je podobná u SARS-CoV-2 a jiných běžných koronavirů, struktura proteinu S, jeho podjednotek S1, S2 a oblasti pro vazbu receptoru (RBD), je pro SARS-CoV-2 specifická. Protilátky proti proteinu N jsou detekovány s vyšší senzitivitou, ale protilátky proti proteinu S jsou specifičtější (4, 8). Nedaří-li se u osob po prodělané infekci prokázat protilátky jednoho typu, je vhodné vyšetřit protilátky typu jiného.
Vyšetření protilátek se provádí z periferní, případně z kapilární krve. Nově se na trh dostala i odběrová souprava dried blood spot (Euroimmun), která je určena k odběru kapilární krve (v ordinaci či v domácím prostředí) na papírovou šablonu. Vzorek krve se nechá zaschnout, vloží do obálky a pošle do laboratoře. Zde se vysekne terčík definované velikosti a vloží se do roztoku, ve kterém se krev rozpustí a uvolní se i protilátky. Poté se provede stanovení metodou ELISA. Výhodou systému je jednoduchý odběr, který si může provést kdokoliv sám (píchnutím do prstu), a dlouhá stabilita vzorku (30 dní). Systém jsme vyzkoušeli na rodinách s dětmi a velmi dobře se osvědčil.
K vyšetření protilátek používáme nejčastěji metody chemiluminiscenční (CLIA) nebo enzymoimunoanalytické (ELISA, EIA) (4, 8). Z prověřených metod máme dobré zkušenosti s metodami zahraničních výrobců Diasorin, Abbott, Roche, Beckman Coulter, Euroimmun, jejichž parametry spolehlivosti byly testovány i americkým Úřadem pro kontrolu léčiv a potravin (FDA) (8), ale použitelné jsou rovněž metody českých výrobců Testline a Vidia (1, 4). Přehled testů, se kterými máme zkušenost, včetně cut-off hodnot je uveden v tab. 1.
Table 1. Přehled vybraných metod používaných ke stanovení protilátek proti SARS-CoV-2. Specificity a senzitivity jsou uvedeny v dokumentech výrobců. 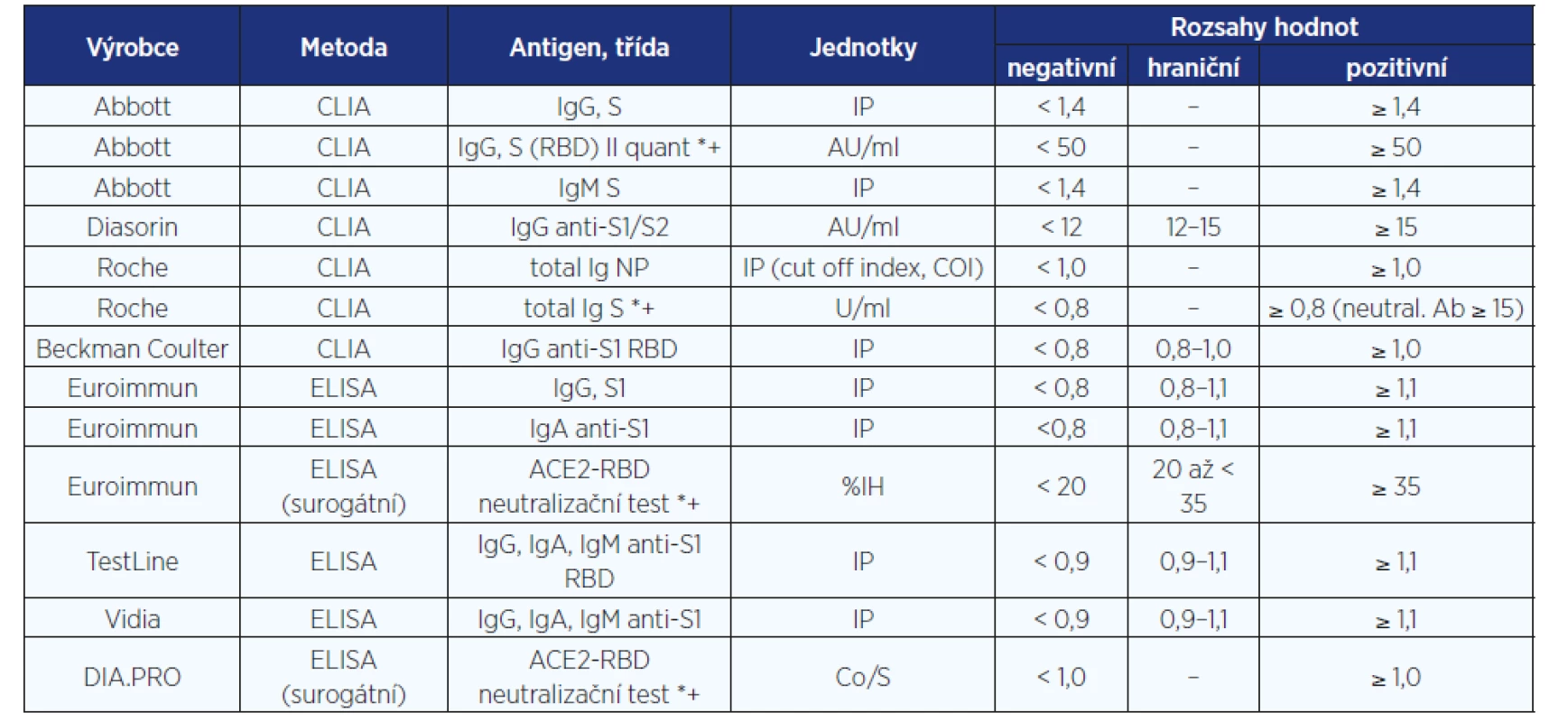
Pozn.: * = kvantitativní; + = vztažené k VNT; IP = index pozitivity (signál vzorku/signál hraniční kontroly); %IH = procento inhibice vazby;
Co/S = inhibice daná výpočtem, obdoba %IH.Výrobci své soupravy neustále zlepšují a dodávají nové verze. V současnosti už je dostupný i mezinárodní standard, který umožňuje stanovit koncentrace protilátek, nejen stanovit poměr optické denzity sledovaného vzorku ku kalibrátoru výrobce. Pro pacienty i lékaře není jednoduché se vyznat v tom, zda je či není zjištěná hodnota dostatečně vysoká. Z tohoto důvodu je nezbytné, aby laboratoře vydávaly výsledky s názvy použitých souprav, hraničními hodnotami a s komentářem. Interpretace výsledků vyžaduje zkušenost a nelze ji provádět bez informací o pacientovi.
S tzv. rychlotesty (na principu laterální imunodifuze) nemáme úplně dobré zkušenosti; lze však najít takové, které akceptovatelnou senzitivitu mají. Přehled specificit a senzitivit rychlotestů, stanovených nezávislými laboratořemi, je uveden např. na stránkách FIND (9). Rychlotesty mají velmi nízkou senzitivitu, a proto jsou jejich výsledky často falešně negativní; setkali jsme se však také s falešně pozitivními výsledky. Rychlotesty sice poskytují zájemcům výsledek na počkání, ale kvalita výsledku vysoké ceně vyšetření neodpovídá.
STANOVENÍ PROTEKTIVITY PROTILÁTEK VIRUS-NEUTRALIZAČNÍM TESTEM
Protektivitu protilátek můžeme stanovit funkčním virus-neutralizačním testem (VNT). Toto vyšetření však provádí jen několik laboratoří v Česku, jež pracují v ochranném režimu a mohou pracovat s živým virem. Neutralizační protilátky se váží na povrchové proteiny viru (protein S) a tím zalepí viru „klíč“ pro vstup do buňky. Ve virologické laboratoři se sérum pacienta smíchá s živou virovou suspenzí a buněčnou linií a tato směs buněk se několik dní kultivuje (10). Pokud byly v séru neutralizační protilátky, pak buňky zůstanou živé, virus se nenamnoží – osoba je vůči infekci imunní. Pokud však v séru neutralizační protilátky nebyly, virus buňky napadne, v nich se namnoží a buňky odumřou. První zkušenosti sbíráme s tzv. surogátními testy, jež na principu ELISA stanovují narušení vazby ACE2R a RBD protilátkou ze vzorku.
V plzeňské a ostravské laboratoři byly provedeny testy porovnávající hladiny protilátek stanovené „standardními testy“ a VNT. Z hodnot vyšetření protilátek metodami ELISA nebo CLIA je tak již možné predikovat hladinu neutralizačních protilátek. Díky tomu je možné určit nejen protektivitu daného množství protilátek, ale třeba i vytipovat vhodné dárce rekonvalescentní plazmy (10).
JAK SPRÁVNĚ INTERPRETOVAT VÝSLEDKY VYŠETŘENÍ PROTILÁTEK
Protilátky je vhodné stanovovat v 1.–2. měsíci po prodělaném onemocnění. Pro správnou interpretaci je vhodné mít k dispozici informace o pacientovi, zda a kdy měl pozitivní výsledek PCR, zda a jaké měl klinické příznaky, zda byl v kontaktu s infekční osobou. Většina výsledků vyšetření bude v souladu s našimi očekáváními. Stává se, že výsledek stanovení protilátek vyjde negativně, i když daná osoba prodělala onemocnění (byla PCR-pozitivní) a měla významné klinické příznaky. Podle jednoho z vysvětlení imunitní systém reagoval tvorbou takových protilátek, které použitý test nezaznamenal (např. se vytvořily jen protilátky proti proteinu N, ale test detekuje protilátky proti proteinu S). Pak je vhodné za 14 dní vyšetření zopakovat, a je-li možnost, doplnit vyšetření protilátek proti jinému antigenu. Zejména mladí lidé, kteří měli asymptomatický průběh nebo jen mírné potíže, aktivují především buněčnou imunitu a při nižší virové náloži většina kontaktu imunitního systému s virem probíhá na sliznicích. Vyšetření protilátek u nich proto může být negativní, přesněji řečeno nacházíme protilátky pod hranicí pozitivity (nikoliv zcela nulové). Zatím nemáme dostatek dlouhodobých dat a nevíme, zda tento nález zajišťuje dlouhodobou imunitu.
Někteří lidé nemusí protilátky vytvořit vůbec a to, že již infekci prodělali, poznáme jen testem buněčné aktivace (stanovením IFN-γ po in vitro stimulaci plné krve testy IGRA Euroimmun nebo Quantivac Quigen nebo stanovením podílu aktivovaných T lymfocytů pomocí průtokové cytometrie nebo metodou ELISPOT). S testy buněčné aktivace se v současné době seznamujeme (jde o soupravy zatím určené jen pro výzkumné využití) a doufáme, že budou v blízké době k dispozici i jako IVD soupravy.
DLOUHODOBÁ IMUNITA PO PRODĚLANÉM ONEMOCNĚNÍ A REINFEKCE
V Česku byly publikovány výsledky s průkazem pozitivních protilátek po 10 měsících od prodělané infekce, máme první skupiny pacientů s pozitivními protilátkami po roce od infekce. Senioři z břevnické studie (6), kteří byli nemocní v březnu a dubnu 2020, byli sledováni po celou dobu epidemie. V zařízení byl zachycen u 2 členů personálu koronavirus v prosinci 2020, ale průběh onemocnění byl asymptomatický a nikdo další nakažen nebyl.
Na obr. 1 jsou zobrazeny hodnoty IgG protilátek v závislosti na době uběhlé od testu PCR. Jednalo se o zaměstnance společnosti GENNET a pacienty imunologické ambulance. Z grafu vyplývá, že IgG protilátky jsou velmi často pozitivní i 6 měsíců od infekce. Imunita může být i delší, proto budeme tyto osoby dál sledovat. V několika případech se v našich laboratořích u námi dříve vyšetřených pacientů prokázala opakovaná infekce koronavirem se slabými klinickými příznaky. V několika případech byla zjištěna „reinfekce“ i u osob, jež měly klinické příznaky respiračního onemocnění, ale neměly provedený PCR test a měly napoprvé jen slabě pozitivní IgG a negativní IgA. U nich jsme zvažovali falešnou pozitivitu protilátek. Při „druhé“ infekci protilátky IgG a IgA stouply.
Image 1. Pozitivita protilátek proti koronaviru v závislosti na době, která uplynula od infekce. Hodnoty vyšetření protilátek metodou ELISA IgG anti-SARS-CoV-2 (S1), Euroimmun. PCR-pozitivní osoby znázorněny červeně, PCR-negativní osoby znázorněny zeleně. Osa x – počet dní od testu PCR, osa y – dekadický log hodnoty OD ratio plus 1. Přerušovanou čárou je uvedené hraniční rozmezí (OD ratio 0,8–1,1), hodnota 0,6 na ose y odpovídá OD ratio 4,0; hodnota 1,0 odpovídá OD ratio 10. 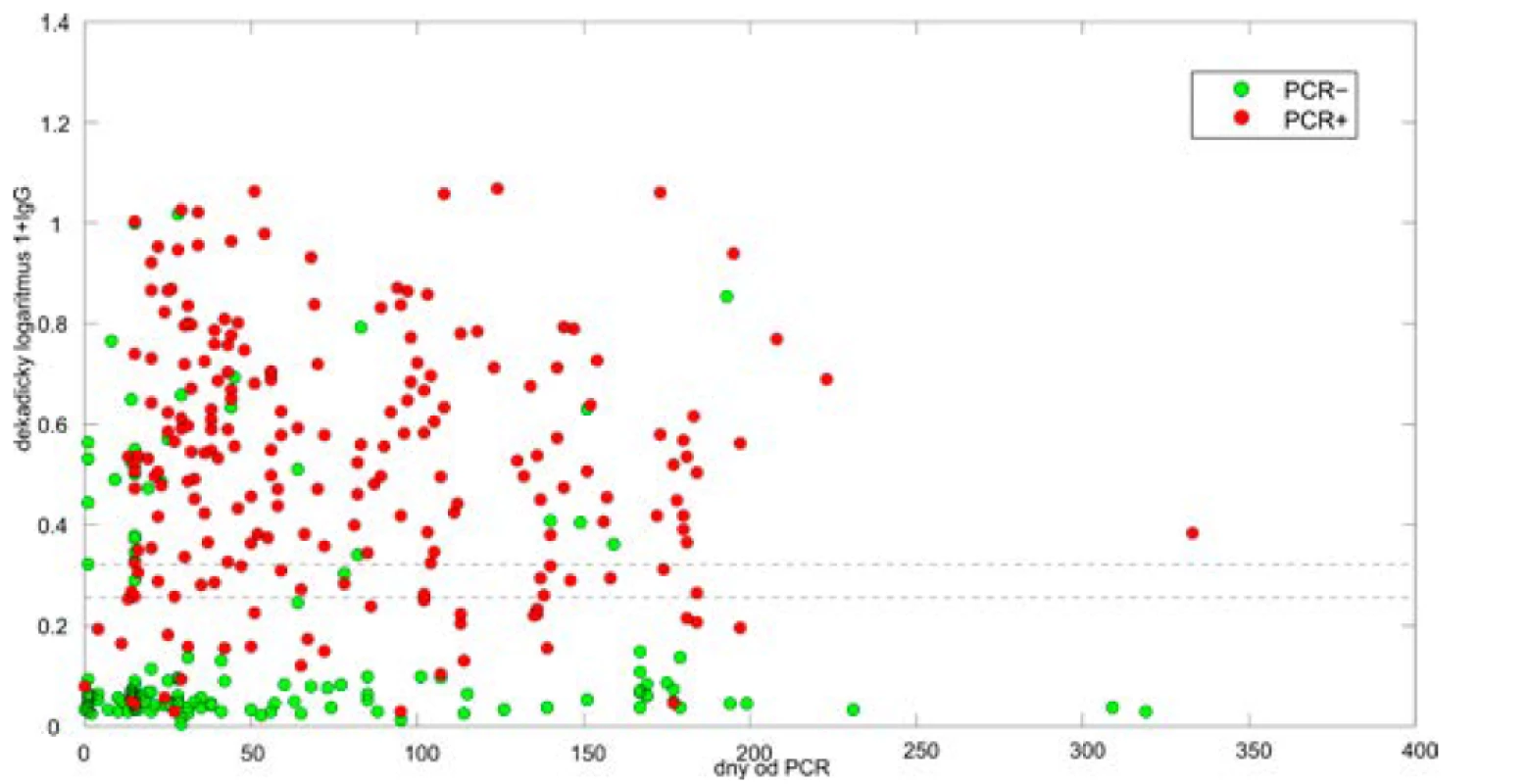
V GENNETu jsme prakticky ověřovali, zda jsou naši zaměstnanci imunní vůči britské variantě koronaviru, když jsme zaznamenali v březnu 2021 její výskyt u skupiny osob. Zaměstnanci již dříve imunní po infekci původním kmenem znovu neonemocněli.
Reinfekce jsou mimořádně vzácné (12). Státní zdravotní ústav (SZÚ) uvádí ve své zprávě ze dne 23. 3. 2021, že bylo nahlášeno 1400 opakovaných symptomatických infekcí z 1,25 milionu prokázaných prvoinfekcí. Reinfekce byla tedy zjištěna přibližně u 1 z 1000 nemocných.
Při obrovských počtech nakažených je nicméně zákonité, že k reinfekci tu a tam dojde. Vysvětlení máme několik:
- Větší část reportovaných reinfekcí jde patrně na vrub nesprávné interpretaci výsledku testů. Specificita testování PCR není stoprocentní. I kdyby bylo pouhé 1 % pozitivních testů PCR falešně pozitivních, což považujeme za dolní odhad, znamenalo by to, že asi 10 tisícům lidí vyšetřených v Česku v minulých měsících byl sdělen falešně pozitivní výsledek. Pokud se takový člověk později skutečně koronavirem nakazí, bude se to téměř jistě interpretovat jako reinfekce. „Reinfekce” se může samozřejmě odehrát i v opačném pořadí – první infekce mohla být COVID-19 a druhá bude mít falešně pozitivní PCR výsledek u respiračního onemocnění jiného typu.
- Pokud byly klinické projevy mírné a nedošlo k dostatečně silné specifické imunitní reakci, může při opakovaném nakažení vyšší dávkou viru dojít k výraznějšímu onemocnění.
- Ani stanovení protilátek IgG není 100% specifické a „reinfekce“ detekujeme u lidí s hraničními protilátkami IgG a negativními protilátkami IgA. Jev je možné vysvětlit přítomností zkříženě reagujících protilátek. Výrobci jako riziková uvádějí séra pacientů s EBV, CMV, chřipkou, autoimunitními onemocněními (např. s pozitivním revmatoidním faktorem). Pozor si musíme také dát, zaznamenáme-li přítomnost pouze protilátek IgA nebo pouze IgM bez pozitivních IgG. V tomto případě s časovým odstupem 2 týdnů vyšetření protilátek zopakujeme, a nedojde-li k sérokonverzi (tvorbě IgG), pak tato pozitivita spíše neznamená prodělané onemocnění, nýbrž jde patrně o falešnou pozitivitu. Zvláštní podskupinou jsou lidé s imunodeficity, u kterých je sérologická diagnostika infekce SARS-CoV-2 obtížnější.
VÝZNAM OČKOVÁNÍ PRO LIDI PO PRODĚLANÉM ONEMOCNĚNÍ
Otázka nutnosti vakcinace u lidí po prodělaném onemocnění COVID-19 se nadále diskutuje a vzhledem k logické nedostupnosti dlouhodobých dat se ještě diskutovat bude. Vakcinace není u lidí po prodělaném onemocnění COVID-19 kontraindikovaná, ale v období 3 měsíců po infekci se nedoporučuje (13). Je možné, že imunita bude přetrvávat po řadu let a že opakovaným kontaktem s infekcí bude docházet k přirozené opakované stimulaci imunitního systému. K 21. květnu 2021 máme bezmála 1,2 milionu osob s dokončeným očkováním a dalších 2,2 milionu osob má zatím aplikovánu první dávku (1). Jelikož vakcín zatím není dostatek, je možné u osob nerizikových s očkováním počkat. Naočkovat potřebujeme nejprve rizikové osoby.
ZÁVĚR
Protilátky proti SARS-CoV-2 jsou ukazatelem poinfekčního stavu. Tyto protilátky jsou známkou imunního stavu a je možné je snadno stanovovat. Protilátková odpověď vykazuje značné individuální rozdíly kvantitativní, kvalitativní i co do trvání v čase. Jejich stanovením můžeme s rozumnou mírou jistoty odpovědět na otázku, zda je jedinec v danou chvíli vnímavý k infekci koronavirem, či nikoliv.
COVID-19 je z pohledu imunologa běžná virová infekce, která ovšem může mít u rizikových osob závažný průběh. Hlavní nebezpečí spočívalo v tom, že postihla imunologicky naivní populaci. Vymýcení koronaviru není možné a nám nezbývá než se smířit s tím, že se tento virus se stane novým členem široké rodiny virů, jež osídlují naše sliznice. Než si na virus zvykneme, je třeba činit uvážlivá preventivní opatření, abychom přílišným počtem nemocných nezatížili zdravotnický systém, ale současně tato opatření musejí umožnit, abychom se vrátili do normálního života.
Čestné prohlášení
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou ani zadavatelem studie.
Seznam zkratek
CDC Centers for Disease Control and Prevention
CMIA chemiluminescent immunoassay
COVID-19 coronavirus disease 2019
Ct tzv. prahový cyklus PCR
ELISA enzyme-linked immunosorbent assay
EIA enzyme immunoassay
FDA U.S. Food and Drug Administration
IgA, IgG, IgM imunoglobuliny A, G, M
IGRA interferon gamma release assay (test buněčné aktivace)
%IH procento inhibice vazby
IP index pozitivity (poměr signálu vzorku/signál hraniční kontroly)
N nukleokapsidový antigen
OD ratio poměr optických hustot vzorku a kalibrátoru v testu ELISA
PCR polymerázová řetězová reakce
RBP receptor-binding protein, součást S1
RT-PCR reverse transcription polymerase chain reaction
S spike protein
SARS-CoV-2 severe acute respiratory syndrome coronavirus 2
VNT virus-neutralizační test
Adresa pro korespondenci:
RNDr. Zuzana Krátká, Ph.D.
Imunologická laboratoř GENNET, s. r. o.
Na Poříčí 26, 110 00 Praha 1
Tel.: 242 456 845
e-mail: zuzana.kratka@gennet.cz
Sources
- Worldometer. Reported Cases and Deaths by Country, Territory, or Conveyance. 2021. www.worldometers.info/coronavirus/#countries
- Centers for Disease Control and Prevention. Interim Guidelines for COVID-19 Antibody Testing. CDC, 2021. Dostupné na: www.cdc.gov/coronavirus/2019-ncov/lab/resources/antibody-tests-guidelines.html#anchor_1616006658343
- Centers for Disease Control and Prevention. Nationwide Commercial Laboratory Seroprevalence Survey. CDC, 2021. Dostupné na: covid.cdc.gov/covid-data-tracker/#national-lab
- Ministerstvo zdravotnictví ČR. Strategie testování onemocnění COVID-19 pro sezónu respiračních onemocnění 2020/2021. Příloha 3 – Průřezové studie protilátkové imunity. MZ ČR, 29. 9. 2020. Dostupné na: koronavirus.mzcr.cz/wp-content/uploads/2020/10/Strategie-testov%C3%A1n%C3%AD-COVID-19_def_200929.pdf
- Krátká Z, Luxová Š, Malíčková K a kol. Testování COVID-19 – co bychom měli mít na paměti. Časopis lékařů českých 2020; 159 : 72–77.
- Fejt V, Krátká Z, Zelená H, Fürst T. Stáří vpřed: Vývoj hladiny ochranných protilátek proti koronaviru SARS-CoV-2 u seniorů z Domova Břevnice. Časopis lékařů českých 2020; 159 : 303–311.
- Společnost pro lékařskou mikrobiologii ČLS JEP. Komentář k interpretaci slabě pozitivních nálezů metodou PCR s vysokými hodnotami Ct. SPLM, 5. 3. 2021 Dostupné na: www.splm.cz/article/komentar-k-interpretaci-slabe-pozitivnich-nalezu-metodou-pcr-s-vysokymi-hodnotami-ct
- U.S. Food and Drug Administration. EUA Authorized Serology Test Performance. FDA, 2021. Dostupné na: www.fda.gov/medical-devices/coronavirus-disease-2019-covid-19-emergency-use-authorizations-medical-devices/eua-authorized-serology-test-performance
- FIND. FIND evaluation of SARS-CoV-2 antibody (Ab) detection tests. Dostupné na: www.finddx.org/wp-content/uploads/2020/11/Av-eval-results20201127.jpg
- Šimánek V, Pecen L, Krátká Z et al. Five commercial immunoassays for SARS-CoV-2 antibody determination and their comparison and correlation with the virus neutralization test. Diagnostics 2021; 11 : 593.
- Ledford H. COVID reinfections are unusual — but could still help the virus to spread. Nature. 2021 Jan 14, doi: 10.1038/d41586-021-00071-6.
- Státní zdravotní ústav. Počet případů reinfekcí covid-19 v ČR vzrostl. SZÚ, 23. 3. 2021. Dostupné na: www.szu.cz/tema/prevence/pocet-pripadu-reinfekci-covid-19-v-cr-vzrostl
- Doporučení pro očkování proti onemocnění covid-19 mRNA vakcínami. Společné stanovisko České vakcinologické společnosti (ČVS), České společnosti alergologie a klinické imunologie (ČSAKI), Společnosti infekčního lékařství (SIL) a Společnosti pro epidemiologii a mikrobiologii (SEM) ČLS JEP ze dne 21. 1. 2021. Dostupné na: www.csaki.cz/dokumenty/Covid_vakcinace.pdf
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental Hygienist
Article was published inJournal of Czech Physicians

2021 Issue 2-3-
All articles in this issue
- Allocation of scarce resources in a pandemic
- COVID-19 antibody testing: examination of the antibody response to coronavirus in common practice
- Stress management techniques for healthcare workers as an important professional tool to fight (not only) COVID-19 pandemics
- Use of cognitive-behavioral approach to overweight and obesity therapy in STOB activities
- Non-alcoholic fatty liver disease – how to effectively fight the nowadays most common liver disease?
- ATP-sensitive potassium channels: key players in pathophysiology of many diseases
- The risk of insect-borne diseases transmission in the Czech Republic and Slovakia
- Principles of evidence-based medicine: from Robert Koch’s postulates to a current EBM concept
- On the origins of European gynaecology: the archaeological and literary sources to the development of gynaecology in Greece before 500 BC
- Computer vision syndrome – symptoms and prevention
-
Gertrude Belle Elionová
(1918–1999) - Zamyšlení nad Spolkem českých lékařů v Praze
-
K devadesátinám prof. MUDr.
Jany Pařízkové, DrSc. - Sedmdesát let prof. Aleše Žáka
- Vzpomínka na prof. Rostislava Koďouska
- ÚVODEM
- Pitvy před Vesaliem a Jeseniem
- Špitální péče řádu sv. Jana na evropské půdě do 18. století
- Představujeme publikaci
- Journal of Czech Physicians
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- COVID-19 antibody testing: examination of the antibody response to coronavirus in common practice
- The risk of insect-borne diseases transmission in the Czech Republic and Slovakia
- Computer vision syndrome – symptoms and prevention
- Non-alcoholic fatty liver disease – how to effectively fight the nowadays most common liver disease?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

