-
Medical journals
- Career
Vliv mechanické srdeční podpory na dynamiku renálních funkcí u pacienta v terminálním stadiu srdečního selhání
: Marián Urban 1; Ivan Netuka 1,3; Alena Paříková 2; Jiří Malý 1,3; Ondrej Szárszoi 1,3; Jan Pirk 1,3
: Klinika kardiovaskulární chirurgie IKEM, Praha 1; Klinika nefrologie IKEM, Praha 2; Centrum výzkumu srdce a cév 3
: Čas. Lék. čes. 2010; 149: 129-132
: Case Report
Renální insuficience je poměrně častá u pacientů s chronickým srdečním selháním. Etiologicky se na tomto typu renální insuficience podílí dva patologické procesy: pokles perfúze periferních orgánů při nízkém minutovém výdeji selhávajícího myokardu a vaskulární nefroskleróza při povšechné ateroskleróze v rámci základního onemocnění. Tato práce je zaměřena na zhodnocení efektu mechanické srdeční podpory na reverzibilitu selhání ledvin u pacienta s kardiorenálním syndromem. Na kasuistice pacienta s dilatační kardiomyopatií a renálním selháním demonstrujeme rychlou restituci ledvinných funkcí po implantaci biventrikulární mechanické podpory, umožňující původní indikaci ke kombinované transplantaci srdce ledvina omezit pouze na transplantaci srdce.
Klíčová slova:
chronické srdeční selhání, chronická renální insuficience, mechanická srdeční podpora, kardiorenální syndrom, transplantace srdce ledvina, transplantace srdce.ÚVOD
Renální insuficience je poměrně častá u pacientů s chronickým srdečním selháním. Spojení kardiovaskulárního poškození a onemocnění ledvin je v posledních letech označováno v literatuře jako kardiorenální syndrom (1). Stupeň renálního postižení se pak typicky mění v závislosti na celkovém klinickém stavu, farmakoterapii a aktuální hemodynamické situaci. U akutního srdečního selhání, včetně akutní dekompenzace CHSS, vede pokles srdečního výdeje ke snížení renální perfuze a zvýšení žilního tlaku s významným poklesem glomerulární filtrace. U pacientů s chronickou srdeční insuficiencí se na renálním poškození v různé míře podílí zejména hypertenzní nefropatie a ischemické postižení ledvin (ischemická nefropatie) v důsledku aterosklerotického zúžení renálního řečiště, které odráží závažnost aterosklerózy v srdci a ledvinách. Ve skutečnosti je však vztah mezi srdečním selháním a renální insuficiencí mnohem složitější a zcela jistě v něm sehrávají důležitou roli také neurohumorální mechanismy. Mezi klíčové mediátory intrarenální redistribuce krevního průtoku (kortikální vazokonstrikce a medulární vazodilatace) patří endothelin a oxid dusnatý (2).
Vztahem renálního selhání s chronickým srdečním selháním se zabývala studie CHARM (Candasertan in Heart Failure. Assesment of Reduction in Mortality and Morbidity). Výsledky této studie jednoznačně prokázaly, že renální insuficience je významným rizikovým faktorem mortality u pacientů s chronickým srdečním selháním (3).
U pacientů v terminální fázi srdečního selhání, po vyčerpání všech možností farmakologické léčby přichází jako poslední definitivní řešení v úvahu transplantace srdce, eventuálně zavedení mechanické srdeční podpory k přemostění pacienta do doby její uskutečnitelnosti.
Renální insuficience u příjemců v době transplantace je významným rizikovým faktorem jednoroční posttransplantační morbidity (4). International Society For Heart and Lung Transplant (ISHLT) dokonce uvádí ve svých standardech renální insuficienci s GFR < 40 ml/min/1,73m2 jako relativní kontraindikaci k transplantaci srdce. Neexistuje však žádná maximální hodnota kreatininu, resp. minimální hodnota GFR, která by byla absolutní kontraindikací.
V klinické praxi je pak pacientům, kteří jsou z hlediska renální insuficience kontraindikováni k transplantaci srdce nabídnuta kombinovaná transplantace srdce a ledviny. Z celkového počtu transplantací srdce, tvoří kombinované transplantace zhruba 1,5 % (5). Dle ISHLT je přežívání po kombinované transplantaci 76 % po jednom roce a 67 % po dvou letech (6). Vzhledem k uspokojivým výsledkům se počet kombinovaných výkonů v posledních letech neustále zvyšuje. Indikační kritéria pro kombinované transplantace se liší od pracoviště k pracovišti a jsou založena na většinou velice limitovaných zkušenostech jednotlivých institucí. Například Temple University Hospital ve Philadelphii považuje za indikovanou transplantaci srdce a ledviny u pacientů, kteří jsou na dialýze, nebo mají clearance endogenního kreatininu méně než 30 ml/min/1,73m2 (7). National Taiwan University Hospital používá hodnoty clearance endogenního kreatininu méně než 20 ml/min/m2, nebo hladinu kreatininu v séru více než 265 μmol/L (8).
Výsledky kombinované transplantace jsou povzbudivé, nicméně přežívání a komplikace jsou stále signifikantně horší než u izolovaných transplantací srdce a ledviny. Zcela nové možnosti do celé problematiky přinesly mechanické srdeční podpory, které se používají pro překlenutí pacientů v terminální fázi srdečního selhání do transplantace (9). U pacientů s hemodynamicky podmíněnou renální insuficiencí dochází po obnovení adekvátního průtoku k restituci ledvinových funkcí (10). Otázka, zda je i mechanická podpora s nefyziologickým (nepulzatilním) kontinuálním průtokem schopna adekvátně perfundovat cílové orgány byla jednoznačně kladně zodpovězena v práci Sandera et al. (11).
Není tedy pochyb o tom, že mechanická srdeční podpora je schopna díky eliminaci extrarenální složky selhání ledvin identifikovat pacienty s jejich reverzibilním postižením, kteří se pak stanou vhodnými kandidáty ke klasické izolované transplantaci srdce (a vyhnou se náročnější kombinované transplantaci). V této terapeutické rozvaze je nutné zohlednit dva protichůdné mechanismy: na straně jedné je zlepšení renálních funkcí po implantaci mechanické srdeční podpory, na straně druhé jsou pak zejména infekční komplikace spojené s implantací, které zhoršují prognózu po transplantaci. U pacientů v terminálním stadiu srdečního selhání, kteří mají současně selhávající ledviny, pak přicházejí v úvahu dvě možné varianty léčebného postupu. Implantovat mechanickou srdeční podporu jako ,,bridge to candidacy“ a po zlepšení renálních funkcí pak transplantovat samotné srdce, nebo pacienty rovnou indikovat ke kombinované transplantaci srdce ledvina. Z tohoto pohledu by bylo s výhodou identifikovat skupinu pacientů, kteří budou ze zavedení podpory profitovat nejvíce. Jak vyplývá z práce Butlera et al. (12), skupina pacientů, u kterých došlo po implantaci LVAD (left ventricular assist device) ke zlepšení renálních funkci, měla nižší srdeční index, nižší body mass index (BMI) a menší výskyt diabetes mellitus (DM) než skupina pacientů, u kterých nedošlo po implantaci ke změně renálních funkci. Vysvětlení, které se nabízí pro lepší výsledky u skupiny s nižším srdečním indexem, je skutečnost, že těžce omezené renální funkce při relativně zachovaném srdečním výdeji předznamenávají vnitřní patologii ledvin a jsou špatným prognostickým znamením z hlediska reverzibility.
KAZUISTIKA
Muž, 62 let, s dilatační kardiomyopatií, od června 2004 v dispenzarizaci ambulance chronického srdečního selhání IKEM Praha. Během roku 2005 byl pacient v relativně stabilizovaném stavu. Začátkem roku 2006 došlo k postupnému zhoršování stavu ve smyslu snížené toleranci k zátěži (objektivně při spiroergometrii pacient toleroval v 03/2006 maximálně 75W s VO2 Max 17,2 l/kg/min). Kromě dysfunkční pravé a levé komory došlo také k rozvoji významné trikuspidální regurgitace a těžké plicní hypertenze. U pacienta také docházelo ke snížení perfuze koncových orgánů a klinicky manifestní renální insuficienci. V laboratoři byla zvýšena hladina sérového bilirubinu na 22 μmol/l a sérového kreatininu na 164 μmol/l. Na SONO břicha byla detekována difuzní hepatopatie, ledviny s maximální velikostí 9 cm s redukovaným parenchymem a nerovnými konturami. Byla stanovena diagnóza chronického onemocnění ledvin stadia CDK3 na podkladě vaskulární nefrosklerózy se spoluúčastí nízkého minutového výdeje.
Pacient byl zařazen jako kandidát na čekací listinu pro plánovanou kombinovanou transplantaci srdce a ledviny. V únoru pak došlo k prohloubení orgánové hypoperfuze se vzestupem hladiny sérového bilirubinu na 60 a sérového kreatininu na 263. Při měření pravostranných tlaků byly hodnoty tlaků v plicnici 54/29/41, tlak v zaklínění 30, a srdeční index 1,6 ml/kg/min. Dne 28. března 2007 došlo při komorové tachykardii k zástavě oběhu s nutností KPCR a krátkodobě umělé plicní ventilace. Navzdory kombinované inotropní podpoře (Noradrenalin, Dobutrex, Levosimendan) v maximálních dávkách, srdeční index dosahoval maximálně 1,4 ml/kg/min. Vzhledem k vyčerpání možností konzervativní léčby byl pacient 31. března 2007 indikován k implantaci biventrikulární pulzatilní mechanické srdeční podpory Thoratec IVAD (Thoratec Corp. USA) k přemostění ke kombinované transplantaci srdce a ledviny (obr. 1). Samotnou techniku implantace jsme publikovali v našem předchozím sdělení (13).
1. Biventrikulární mechanická srdeční podpora s pulzatilním průtokem Thoratec IVAD (Thoratec Corp. USA) 
Po znovuobnovení adekvátního srdečního výdeje generovaného mechanickou srdeční podporou stoupl srdeční výdej na 5,4 l/min. V průběhu několika málo dní došlo také k výraznému zlepšení renálních funkci s poklesem sérové hladiny kreatininu z původních 184 na 123 μmol/l 10 dní od implantace. Současně došlo k vzestupu glomerulární filtrace (výpočtem dle MDRD) z původních 33 na 59 ml/min/spt (graf 1, 2).
1. Dynamika renálních funkcí v prvních dnech po implantaci 
kreatin v séru (μmol/l) 2. Dynamika renálních funkcí v prvních dnech po implantaci 
MDRD (ml/s/spt) Vzhledem k pozitivnímu trendu reparace renálních funkcí byla revokována indikace ke kombinované transplantaci a pacient zůstal dále zařazen pouze k transplantaci srdce. Samotná transplantace se následně uskutečnila 9. května 2007. V době psaní textu je pacient ve velice dobrém klinickém stavu s uspokojivou hodnotou renálních funkcí (tab. 1).
1. Vývoj renálních funkcí 09/2006 až 08/2008 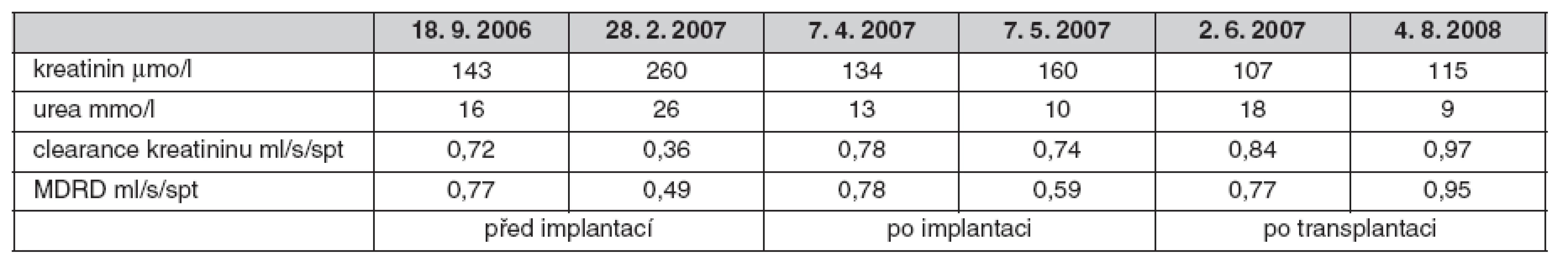
MDRD – modification on diet in renal disease DISKUZE
Naše zkušenosti s tímto případem potvrzují schopnost mechanické srdeční podpory zabezpečit adekvátní perfuzi koncových orgánů. Už za deset dní po implantaci došlo u našeho pacienta k normalizaci renálních funkcí. Tato rychlá restituce je v souladu s dosud publikovanými studiemi.
Z dostupné literatury je zřejmé, že výsledky kombinované transplantace srdce a ledviny dosahují mnohem nižší úspěšnosti než u samostatné transplantace srdce.
Neméně podstatná je i otázka vhodné alokace dárcovských orgánů. Námi zvolený postup umožnil eliminaci obou těchto negativních aspektů.
Díky znovuobnovení dostatečného srdečního výdeje generovaného mechanickou srdeční podporou vstupoval pacient do následné transplantace srdce v dobrém klinickém stavu s příznivou funkcí parenchymatózních orgánů, a tedy i výrazně nižším rizikem s ní spojené morbidity i mortality. Zároveň díky eliminaci transplantace ledviny došlo k ušetření nedostatkového dárcovského štěpu.
Naše dosavadní data sledování dokumentují příznivou funkci ledviny i v již poměrně dlouhodobém horizontu, a to i navzdory obecně nepříznivému vlivu dlouhodobého podávání imunosuprese.
Tato kazuistika je jedním z dalších příkladů přínosu mechanické srdeční podpory v rámci terapie pacientů v terminálním srdečním selhání. Demonstruje její zásadní vliv nejen na znovuobnovení dostatečných hemodynamických parametrů, ale dokumentuje i její působení na funkci jednotlivých koncových orgánů. Tím následně umožňuje exaktnější odlišení jednotlivých etiologických komponent ovlivňujících jejich selhávání.
Implantace mechanické srdeční podpory se stalo již rutinní součástí terapie srdečního selhání i v podmínkách České republiky. Naše dosavadní povzbudivé výsledky dokumentují i přínos u pacientů se selháváním více orgánových soustav. Považujeme proto za žádoucí širší a zejména časnější indikace k zahájení mechanické srdeční podpory. K dosažení tohoto cíle je zcela zásadní informovanost a spolupráce co nejširší odborné kardiologické veřejnosti.
Zkratky
- BMI – body mass index
- DM – diabetes mellitus
- GFR – glomerulal filtration rete
- CHARM – Candasertan in Heart Failure. Assesment of Reduction in Mortality and Morbidity
- CHSS – chronické srdeční selhání
- ISHLT – International Society For Heart and Lung Transplant
- KPCR – kardiopulmocerebrální resuscitace
- LVAD – left ventricular assist device
- MDRD – modification of diet in renal disease
Adresa pro korespondenci:
MUDr. Marián Urban
Klinika kardiovaskulární chirurgie IKEM
Vídeňská 1958/9
140 21 Praha 4
e-mail: maub@ikem.cz
Sources
1. Málek F. Má nová definice kardiorenálního syndromu význam pro klinickou praxi? Cor et Vasa 2009; 9 : 590–592.
2. Abassi Z, Gurbanov K, Rubinstein I, et al. Regulation of intrarenal blood flow in experimental heart failure: Role of Endothelin and Nitric Oxide. Am J Physiol 1998; 274: F766–F774.
3. Hillege HL, Nitsch D, Pheffer MA, et al. Renal function as a predictor of outcome in a broad spectrum of patiets with heart failure. Circulation 2006; 113 : 671–678.
4. Taylor DO, Edwards LB, Boucek MM, et al. International Society for Heart and Lung Transplantation. Registry of the International Society for Heart and Lung Transplantation: Twenty third official adult heart transplantation report – 2006. J Heart Lung Transplant 2006; 25 : 869–879.
5. Gill J, Shah T, Hristea I, et al. Outcomes of simultaneous heart-kidney transplant in the US: A Retrospective analysis using UPTN/UNOS data. Am J Transplant 2009; 9 : 844–852.
6. Narula J, Bennett LE, DiSalvo T, et al. Outcomes in recipients of combined heart-kidney transplantation: Multiorgan, same donor transplant study of International Society of Heart and Lung Transplantation. Transplantation 1997; 63 : 861–867.
7. Leeser DB, Valluvan J, Furukawa S, et al. Simultaneous heart and kidney transplantation in patients with end stage heart and renal failure. Am J Transplant 2001; 1 : 89–92.
8. Hsu RB, Tsai MK, Lee PH, et al. Simultaneous heart and kidney transplantation from a single donor. Eur J Cardio Thorac Surgery 2008; 34 : 1179–1184.
9. Netuka I, Szárszoi O, Malý J. Mechanické srdeční podpory v terapii terminálního srdečního selhání. Cor Vasa 2008; 50 : 207–214.
10. Bergler-Klein J, Pirich C, Laufer G, et al. The long-term effect of simultaneous heart and kidney transplantation on native renal function. Transplantation 2001; 71 : 1597–1600.
11. Sandner SE, Zimpfer D, Zrunek P, et al. Renal Function After Implantation of Continuous Versus Pulsatile Flow Left Ventricular Assist Devices. Ann Thorac Surg 2009; 87 : 1072–1078.
12. Butler J, Geisberg C, Houwser R, et al. Relationship between Renal Function and LVAD Use. Ann Thorac Surg 2006; 81 : 1745–1751.
13. Kettner J, Pirk J, Netuka I, et al. Mechanical cardiac support – the first use in Czech Republic. Čas Lék čes 2005; 144 : 38–42.
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental Hygienist
Article was published inJournal of Czech Physicians

-
All articles in this issue
- New options of influenza vaccination
- Urologic complications of HIV infection
- Adrenocortical insufficiency and diabetes mellitus type 1
- Impact of mechanical circulatory support on renal function in a patient with end stage heart failure
- Prediction of postoperative complications and optimization of surgical technique
- The Year of the Lung
- Practical instrument for pathological gamblers and other patients with heavy debts
- Journal of Czech Physicians
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Adrenocortical insufficiency and diabetes mellitus type 1
- New options of influenza vaccination
- Urologic complications of HIV infection
- Impact of mechanical circulatory support on renal function in a patient with end stage heart failure
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

