-
Medical journals
- Career
Mortalitní riziko pacientů hospitalizovaných mezi lety 2003 a 2019 pro ischemickou cévní mozkovou příhodu
Authors: Lenka Kielbergerová 1; Otto Mayer Jr. 1,2; Jan Bruthans 1,3
Authors‘ workplace: Neurochirurgická klinika, Fakultní nemocnice, Plzeň 1; II. interní klinika, Univerzita Karlova, Lékařská fakulta a Fakultní nemocnice, Plzeň 2; Biomedicínské centrum, Univerzita Karlova, Lékařská fakulta a Fakultní nemocnice, Plzeň 3; Centrum kardiovaskulární prevence, Thomayerova nemocnice a 1. lékařská fakulta Univerzity Karlovy, Praha 4
Published in: Vnitř Lék 2022; 68(E-3): 4-11
Category: Original Contributions
Overview
Východisko: Cévní mozkové příhody (CMP) jsou důležitou součástí zdravotně‑sociální zátěže představované kardiovaskulárními chorobami. Přestože specifická úmrtnost na cerebrovaskulární onemocnění v České republice od 80. let klesá, individuální prognóza a trend úmrtnosti u pacientů, kteří CMP prodělali, není zcela jasný. V souboru pacientů hospitalizovaných pro iCMP jsme analyzovali trendy mortality v posledních dvou desetiletích.
Metodika: Celkem bylo ve studii sledováno 9076 pacientů (průměrný věk 71,8 let, 51,9 % mužů) hospitalizovaných v letech 2003–2019 pro iCMP ve FN Plzeň. Vitální stav byl zjištěn na základě registrů ÚZIS k 31. 12. 2020, ostatní okolnosti z nemocničního informačního systému
Výsledky: Celkem v průběhu sledování zemřelo 5583 pacientů. Úmrtnost ještě během iniciální hospitalizace činila 9,1 %, třicetidenní 14,2 % a jednoroční mortalita 28,4 %. U pacientů hospitalizovaných v letech 2003 až 2015 bylo možno stanovit i pětiletou mortalitu, která činila 49,8 %. Když jsme porovnali riziko úmrtí ve 4 delších obdobích (tj. 2003–07, 2008–11, 2012–15 a 2016–19), žádné statisticky významné změny v nemocniční úmrtnosti, třicetidenní, jednoroční či pětileté mortalitě jsme nenalezli. Jak se dalo očekávat, každá dekáda věku pacientů byla spojena s asi dvakrát vyšším rizikem úmrtí. Indikace intravenózní trombolýzy jako součást počáteční léčby CMP se v průběhu sledovaného období výrazně zvýšila (z 2,4 % v letech 2003–07 na 48,1 % v letech 2016–19). Tento postup však příznivě ovlivnil pouze jednoroční riziko úmrtí, zatímco u pětileté mortality byl jeho efekt neutrální.
Závěry: Přes prokazatelně příznivé trendy cerebrovaskulárních příhod z populačního hlediska zůstává individuální prognóza pacientů po cévní mozkové příhodě velmi nepříznivá.
Klíčová slova:
prognóza – cerebrovaskulární příhody – hospitalizační fatalita
Úvod
Základním předpokladem, jak omezit dopady kardiovaskulárních chorob na zdraví celé populace a náležitě formulovat zdravotnickou politiku, je znát epidemiologickou situaci v oblasti dané choroby. V tomto směru je asi nejvíce objektivní sledovat mortalitu a morbiditu na konkrétní chorobu, respektive zejména její vývoj v delším časovém období. Tento přístup, u nás realizovaný především Ústavem zdravotnické informace a statistiky (ÚZIS), nám dává globální pohled na zdravotnické následky příslušné choroby, nakolik se dané onemocnění podílí na celkové mortalitě a invalidizaci, a zejména zdali její nižší incidence či smrtnost přispívá k prodloužení průměrné délky lidského života v dané oblasti.
Průměrná i očekávatelná délka života se v ČR po roce 1989 poměrně zásadně prodloužila a největší zásluhu na této skutečnosti má bezpochyby právě pokles mortality na kardiovaskulární choroby. Jakkoliv tato informace představuje možná nejobjektivnější obraz „celkového zdraví populace“, nelze jednoznačně určit, nakolik za tímto poklesem stojí snížení incidence kardiovaskulárních příhod (připsatelné převážně na vrub primární prevence a snížení dopadu kardiovaskulárních rizikových faktorů), či zda jde o efekt prodloužení přežívání pacientů díky rozvoji péče o pacienty s akutní manifestací příslušné kardiovaskulární choroby a jejich dlouhodobé léčby („kurativy“ a sekundární prevence). V případě ischemické choroby srdeční (ICHS) je v podstatě prokázané, že v praxi se oba jevy vzájemně kombinují a doplňují (resp. efekt prevence mírně převažuje) (1). U cerebrovaskulárních chorob, které jsou z hlediska dopadu na mortalitní riziko zřejmě hned za ICHS, může být situace poněkud odlišná, už jenom z důvodu, že léčebné možnosti jsou v případě jejich akutní manifestace daleko menší, než je tomu u ICHS. Co však víme je, že po roce 1989 deklarovaná mortalita (tj. příčina uvedená v úmrtním listě) na cerebrovaskulární choroby dle ÚZIS celkem setrvale klesá (2).
V naších předcházejících analýzách jsme se zabývali otázkou, nakolik důsledně jsou u stabilizovaných pacientů po první ischemické cévní mozkové příhodě (iCMP) do praxe implementovány obecné principy sekundární prevence vaskulárních chorob a jak se tyto vyvíjely v čase (jednalo se o tzv. „stroke specific module“ studie EUROASPIRE III z roku 2007 a tzv. „ESH stroke survey“ z roku 2012/13 (3–5)). Z těchto analýz na zvláště selektovaných a vyšetřených souborech pacientů po prodělané iCMP jsme jednak prokázali, že úroveň kontroly základních rizikových faktorů i důslednost, s jakou je předepisovaná rutinní farmakoterapie v sekundární prevenci, není zdaleka optimální (6). Hlavně z nich však vyplynulo, že pacienti po iCMP vykazují výrazné mortalitní riziko, a to přesto, že v rámci těchto studií byli záměrně vyšetřeni stabilizovaní a zřejmě i relativně méně postižení pacienti (6)
Základním cílem naší analýzy bylo stanovit, jaká je vlastně prognóza pacientů přijatých k hospitalizaci pro iCMP a nakolik se v posledních dvou dekádách vyvíjí.
Metoda
Všechny studijní procedury byly prováděny v souladu s principy Správné klinické praxe ve smyslu Helsinské deklarace z roku 1984 a pozdějších dodatků. Studijní protokol byl schválen lokální Etickou komisí Fakultní nemocnice (FN) Plzeň, pacienti podepsali v úvodu hospitalizace informovaný souhlas. Se všemi získanými daty je nakládáno v souladu se Zákonem na ochranu osobních údajů a směrnicí GDPR Evropské komise
Design a studovaná populace
Studie byla koncipovaná jako čistě epidemiologická prospektivní survey, nebyla tedy řešena žádná formálně položená hypotéza. Pacienti hospitalizovaní pro CMP byli identifikováni v nemocničním informačním systému FN Plzeň na základě formální deklarované primární příčiny hospitalizace v propouštěcí zprávě (či listu o prohlídce zemřelého) a dalších uložených informací, přičemž tato diagnóza musela být verifikována na základě neurologického vyšetření a zobrazovací metody (převážně CT). Ve vlastní definici CMP jsme se drželi klinického dojmu ošetřujícího lékaře (tj. pokud byla cerebrovaskulární příhoda například deklarována jako tranzitorní ischemická ataka, nebyl tento pacient do analýzy zařazen). Celkem ve FN Plzeň došlo mezi 1. 1. 2003 a 31. 12. 2019 k 14 729 hospitalizacím pro některý z typů mozkové příhody, kdy pacienti byli primárně přijati na Neurologickou kliniku či na jednu z 5 klinických jednotek FN Plzeň zaměřených na problematiku vnitřního lékařství (tj. I. interní klinika, II. interní klinika, Kardiologická klinika, Interní oddělení a Oddělení klinické farmakologie). Z tohoto počtu však bylo vyřazeno 4060 hospitalizací, kdy proběhlá mozková příhoda byla deklarována jako hemorrhagické etiologie. Po vyřazení duplicitních hospitalizací téhož jedince (tj. rekurentních CMP) jsme získali soubor 9320 pacientů, z něhož však bylo ještě vyřazeno dalších 244 osob, kde po zhodnocení dostupné dokumentace byla jako primární příčina hospitalizace seznána jiná diagnóza než CMP, ischemická etiologie dubiózní (neverifikována) či se jednalo o cizí státní příslušníky, kde nebylo možno ověřit jejich vitální status. Finální sledovaný soubor tak činil 9076 subjektů, u nichž v průběhu sedmnáctiletého sledovaného období došlo k iCMP.
Zpracování dat
Na základě údajů obsažených v nemocničním informačním systému FN Plzeň byla částečně automaticky a v nezbytných případech manuálně vytvořena databáze předmětných pacientů a pomocí jejich rodných čísel naše databáze agregována s údaji obsaženými v Centrálním registru obyvatelstva, spravovaném ÚZIS a získán tak údaj ohledně eventuálního data smrti a její deklarované primární příčiny (tak jak jsou ze zákona uváděny v Listu o prohlídce mrtvého); tento průzkum vitálního statusu byl realizován k 31. 12. 2020, takže máme k dispozici stanovení přinejmenším 1roční mortality, zatímco pro pacienty přijaté před 1. 1. 2015 i pětiletou mortalitu. Posledním krokem bylo odstranění všech údajů umožňujících konkrétní osobní identifikaci zařazených pacientů a další analýzy již byly realizovány jen na anonymizovaných datech.
Jako testovaný výstup „outcome“ bylo použito úmrtí z jakékoliv či jen kardiovaskulární příčiny, a to v průběhu 1 roku, nebo 5 let (u osob hospitalizovaných v letech 2003–15, n = 6930). Pro potřeby posouzení trendu mortality byl soubor v prvním kroku rozdělen podle roku hospitalizace (který byl zároveň jedinou formální „expozicí“) a v druhé kroku do 4 větších „sezon“ (čtyřletých, s výjimkou jedné pětileté sezony 2003–2007, která byla zároveň použita jako referenční). Statisticky byla data testována pomocí software STATA/ SE 8, přičemž použity byly jen konvenční deskriptivní/statistické metody a standardní regresní modely (detaily jsou uvedeny v příslušných sekcích).
Výsledky
Celkem bylo v této analýze sledováno 9076 subjektů (průměrný věk 71,8 (± SD 12,3), 51,9 % mužů), z čehož 7737 pacientů bylo iniciálně přijato na Neurologickou kliniku, zatímco 1340 na lůžko některého z interních oddělení. Pacientů ve věku ≤ 65 let bylo 2417 (26,6 %). Medián doby hospitalizace činil 5 dní (IQR: 3–10), přičemž hospitalizace byla delší než 10 dní u 22,1 % pacientů. Dohromady 53,8 % pacientů alespoň část hospitalizace strávilo na iktové jednotce, trombolýza byla realizována u 25 % pacientů a trombektomie u 2,3 %, zatímco u osob ve věku ≤ 65 let činily tyto údaje 57,3 %, 26,8 % a 2,7 %, resp.
V celém souboru v průběhu sledovaného období (dohromady ≈41 244 člověko‑let sledování) zemřelo 5 583 osob při střední době sledování 1249 (IQR: 212–2658) dní. Hospitalizační mortalita (fatalita) činila 9,1 %, třicetidenní mortalita 14,2 %, jednoroční mortalita 28,4 % a pětiletá mortalita (u části vzorku 2003–2015) 49,8 %. U pacientů ≤ 65 let činily tyto standardizované mortality 3,3 %, 5,1 %, 10,1 % a 20,2 %, resp. Pokud jsme z analýzy vyřadili pacienty, kteří zemřeli již během hospitalizace (a za celek jsme považovali pouze ty, co byli z hospitalizace propuštěni a akutní ataku CMP tedy přežili), činila 30denní mortalita 5,8 %, jednoroční 21,2 % a pětiletá 44,8 %, resp. 1,8 %, 7,0 a 17,4 % pro ty ve věku ≤ 65 let.
Změny standardizované mortality podle roku hospitalizace v průběhu celého sledovaného období udává graf 1. Hospitalizační, třicetidenní i jednoroční mortalita sice mezi lety do určité míry fluktuovaly, nicméně jednoznačný trend v nich vysledovat nelze a rozdíly ani nedosáhly statistické významnosti. Určitý pokles po roce 2007 lze diferencovat v pětileté mortalitě a tento trend byl i statisticky významný (bylo ale možno hodnotit pouze do roku 2015).
Graph 1. Změny standardizované celkové mortality v průběhu sledovaného období 2003–2019 
Abychom minimalizovali vliv fluktuace mortality mezi jednotlivými roky, mortalitní trendy byly v dalším kroku posuzovány v delších obdobích („sezonách“ 2003–07, 2008–11, 2012–15 a 2016–19). Kaplan‑Meierovy křivky přežívání podle doby hospitalizace v jedné ze 4 definovaných „sezon“ jsou uvedeny v grafu 2. Procento zemřelých standardizované na příslušné časové intervaly (hospitalizační, 30denní…) ve 4 sledovaných „sezonách“ udává tabulka 1 (včetně dalších korespondujících základních charakteristik). Výsledky jsou podobné, jako když byly trendy hodnoceny podle jednotlivých let, tj. statisticky významný rozdíl byl pozorován pouze pro pětiletou mortalitu. V posledním kroku jsme rozdíly v celkové mortalitě mezi „sezonami“ ještě adjustovali na věk a pohlaví (Tab. 2). „Sezona“ 2003–2007 byla v této analýze brána jako referenční (s rizikem rovným 1) a kalkulováno bylo relativní riziko úmrtí v dalších obdobích. Po této adjustaci zůstaly rozdíly mezi „sezonami“ fakticky jen marginální a navíc ještě vymizel doposud statisticky významný pokles v pětileté mortalitě. Stejná analýza byla provedena jen s pacienty ve věku ≤ 65 let fakticky se stejným výsledkem, tj. opět nelze najít žádný statisticky významný časově podmíněný trend mezi jednotlivými „sezonami“ (data nejsou v tabulce uvedena).
Graph 2. Kaplan-Meierovy křivky přežívání pacientů hospitalizovaných pro iCMP v období 2003–07, 2008–11, 2012–15 a 2016–19 
Table 1. Základní údaje souboru pacientů hospitalizovaných pro ischemickou cévní mozkovou příhodu v průběhu let 2003–2019 a jejich mortalita 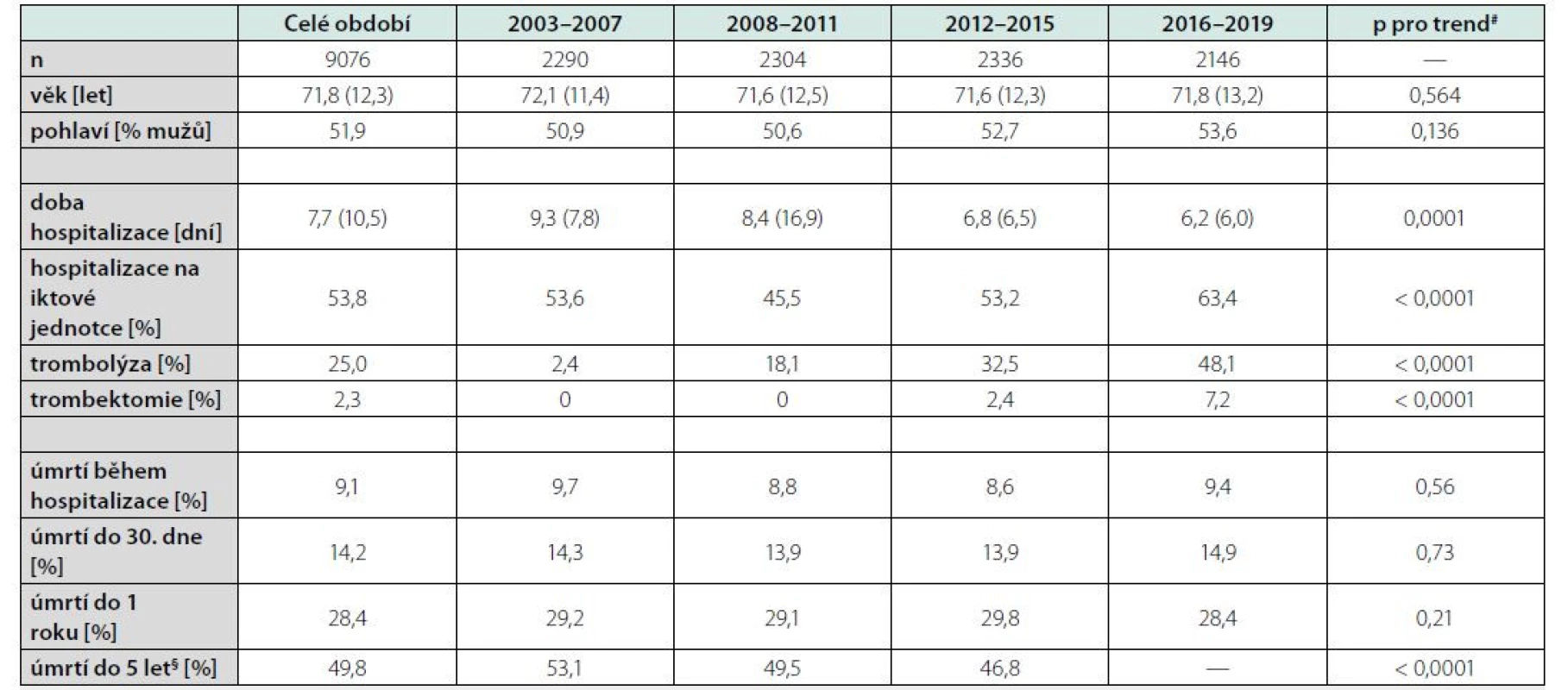
[průměr (standardní odchylka) či proporce], #Kruskal-Wallis ANOVA, §hodnoceno pouze pro pacienty hospitalizované do roku 2015 Table 2. Částečně adjustované riziko celkové a kardiovaskulární mortality v podle „sezony” hospitalizace 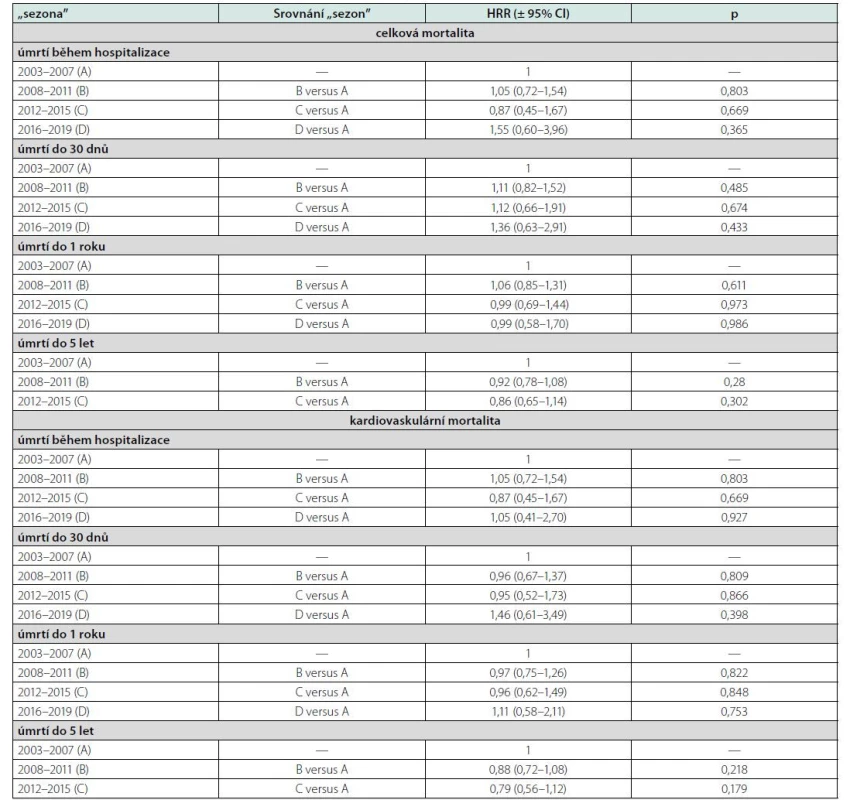
HRR (±95% CI), poměr rizik (95% intervaly spolehlivosti); adjustováno na věkovou dekádu, pohlaví a rok hospitalizace Závěrem byly v souboru provedeny ještě další dvě dílčí analýzy. Na základě údajů zvedených v Listu o prohlídce mrtvého byla vzata v úvahu deklarovaná hlavní příčina úmrtí. Takto 71,7 % úmrtí v našem souboru mělo deklarovánu kardiovaskulární příčinu, 9,5 % zhoubný novotvar a 18,7 % jinou příčinu. Vzájemný poměr těchto tří základních skupin příčin úmrtí se během let měnil spíše jen marginálně. Zopakovali jsme rovněž všechny výše zmíněné analýzy, pouze místo celkové jsme použili kardiovaskulární mortalitu. Hospitalizační kardiovaskulární mortalita činila 9,0 %, třicetidenní kardiovaskulární mortalita 11,3 %, jednoroční 20,5 %, zatímco pětiletá 32,4 %. Trend kardiovaskulární mortality také (jak se dalo čekat) v podstatě kopíroval trend mortality celkové a mezi 4 definovanými „sezonami“ jsme žádné statisticky významné rozdíly také nenalezli (Tab. 2, spodní panel).
Poslední provedenou analýzou bylo určit, nakolik některé známé základní charakteristiky ovlivnily riziko úmrtí jako závislé proměnné (použito bylo Coxova regresního modelu) (Tabulka 3). Významným faktorem byl očekávatelně věk pacientů. Konzistentně také ve všech v definovaných obdobích (tj. během hospitalizace, prvních 30 dnů atd.) paradoxně zvyšovalo relativní riziko úmrtí i alespoň přechodné umístění pacienta na iktové jednotce, a dále pak v případě úmrtí během hospitalizace i do 1 roku od přijetí také provedení trombektomie (jako součásti úvodního managementu). Hospitalizace delší 10 dnů byla spojena se sníženým rizikem úmrtí během hospitalizace a prvních 30 dnů, zatímco v případě jednoroční a pětileté mortality relativní riziko úmrtí naopak zvyšovala. Trombolýza signifikantně snižovala relativní riziko úmrtí do 1 roku, těsně za hranicí významnosti byla v případě hospitalizační mortality, naopak v případě pětileté mortality byl její efekt již neutrální. Pokud jsme použili jako závislou proměnnou kardiovaskulární mortalitu, vymizela statistická významnost benefitu podané trombolýzy i případě jednoroční mortality. Relativní riziko spojené s ostatními faktory zůstalo prakticky stejné (není uvedeno v tabulce)
Table 3. Relativní mortalitní riziko některých základních charakteristik pacientů 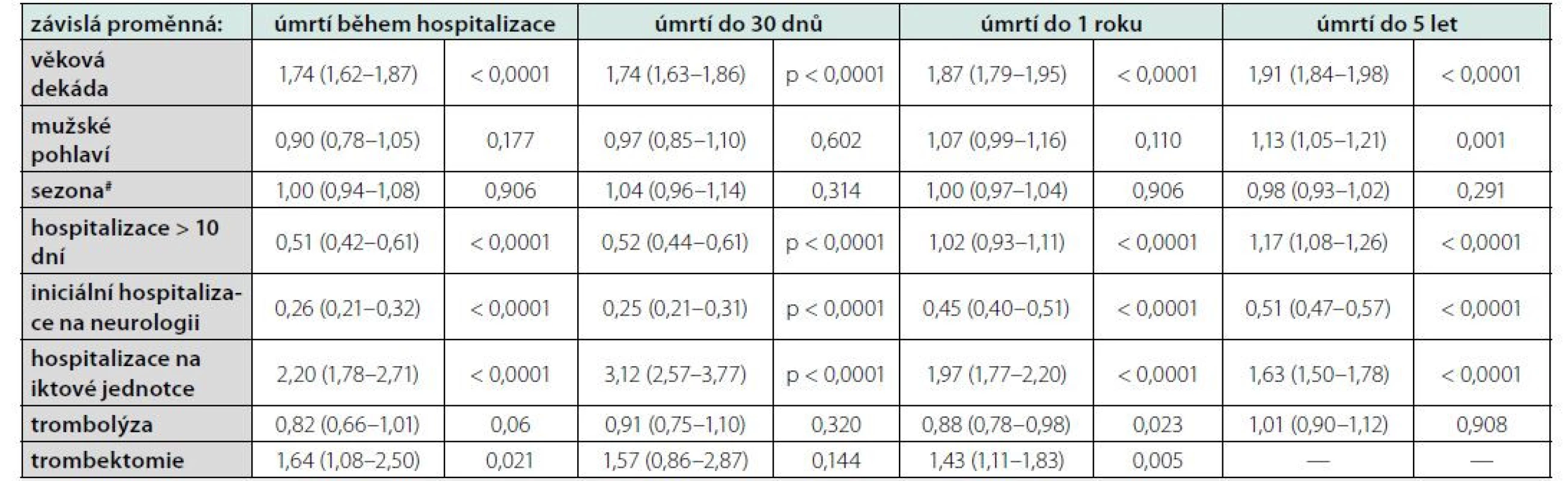
Coxův model proporcionálních rizik [poměr rizik (95% intervaly spolehlivosti); p]; #2003–07, 2008–11, 2012–15 a 2016–19 Diskuze
Základním poznatkem vyplývajícím z naší analýzy je, že mortalita pacientů, u nichž došlo k iCMP, zůstává enormně vysoká. V průměru ve sledovaném období 2003–2015 zemřelo do 5 let od manifestace 50 % postižených pacientů, více než 1/5 nepřežilo ani 1 rok po CMP (což dává prognózu horší než je tomu u mnohých malignit) a i krátkodobá mortalita (úmrtí do 30 dnů od přijetí) se po celé období pohybovala kolem 15 %. Navíc si je třeba uvědomit, že naše analýza nezahrnuje úmrtí před příjezdem do nemocnice, tudíž výše zmíněný dopad na životy postižených osob bude zřejmě ve skutečnosti ještě o něco horší. Lze předpokládat, že alespoň část pozorované vysoké mortality jde jistě na vrub poměrně vysokého věku postižených pacientů – ten v našem souboru činil v průměru ~72 let a asi 10 % sledovaných osob bylo dokonce starších 85 let. Pětiletá celková mortalita však zůstává podobně extrémní i po vyřazení těchto nejstarších osob z analýzy (a u osob ve věku ≤ 85 let tak činila 49,4 %). Dosti alarmující je nakonec i u osob nominálně středního věku (≤ 65 let), tj. 23,1 %.
Pozorovaný mortalitní impakt ischemických CMP je relativně vysoký v kontextu nejen podobných údajů z celé Evropy, ale v rámci ČR. Průměrná třicetidenní mortalita po manifestaci iCMP činila v roce 2017 v zemích OECD 7,7 %, zatímco v celé České republice 9,4 % (7). Námi pozorovaný výsledek krátkodobé mortality na cerebrovaskulární choroby (tj. 14,5 % do 30. dne od přijetí do nemocnice) by tedy Plzeňský region, ze kterého naprostá většina zařazených pacientů pochází, řadil zcela na konec pomyslného žebříčku (na úroveň zemí jako je Litva či Lotyšsko). Je fakt, že podobné znevýhodnění západočeského regionu z hlediska kardiovaskulárního rizika (a toho zprostředkovaného cerebrovaskulárními příhodami zvláště) jsme pozorovali ještě zhruba v polovině 90. let (8), nicméně doposud jsme se domnívali, že tento rozdíl již časem vymizel. Na druhé straně pokud vezmeme volně dostupná celostátní data z registrů ÚZIS (9), mortalita na všechny kardiovaskulární choroby je v Plzeňském kraji velmi blízko celostátnímu průměru (534,6 versus 537,5 úmrtí na 100 000 obyvatel). Mortalitní riziko pacientů po prodělané iCMP také velmi „vyčnívá“ v kontextu ostatních kardiovaskulárních chorob. Například v jiné naší studii jsme rovněž měli možnost posoudit pětiletou mortalitu u 5159 pacientů mladších 85 let, hospitalizovaných ve FN Plzeň pro akutní infarkt myokardu mezi lety 2006–15 (10). Pětiletá celková mortalita u těchto pacientů (včetně těch, co zemřeli během hospitalizace) činila 24,2 % (tj. asi polovinu počtu, který jsme nyní pozorovali u pacientů po iCMP).
Podobně znepokojující je fakt, že za celé poměrně dlouhé období, které naše analýza obsáhla, nelze u pacientů hospitalizovaných pro iCMP prakticky doložit žádný přesvědčivý trend k poklesu celkové či kardiovaskulární mortality. Jedinou výjimkou je snad pětiletá mortalita po roce 2007, kde jsme již určitý, statisticky významný trend pozorovali (na hrubých, neadjustovaných datech činil pokles asi cca 1,4 % za rok). V parciálně adjustovaném modelu (věk, pohlaví a iniciální hospitalizaci na neurologii) ještě vykazovali pacienti hospitalizovaní v letech 2012–15 asi o 14 % nižší riziko pětileté celkové mortality než ti hospitalizovaní v letech 2003–7, rozdíl však již nedosáhl statistické významnosti. Vývoj pětileté mortality mohl být ale analyzován pouze do roku 2015 a teprve další léta ukážou, zdali se jedná o reálný trend, či jenom výkyv. V tomto místě je nutno opět zmínit patrný nesoulad s celostátními údaji o mortalitě na cerebrovaskulární příhody z registrů ÚZIS (9), které ukazují po roce 1989 do současnosti jednoznačný pokles jak u mužů, tak u žen (doposud přinejmenším o 50 % oproti hodnotě z konce 80. let). Tento celostátní údaj je ale založen na příčině úmrtí deklarované v úmrtním listu a značí pouze jen, že ubylo úmrtí, kde dle názoru ohledávajícího lékaře byla hlavní příčinou cerebrovaskulární příhoda. Z největší pravděpodobností tedy především odráží sníženou incidenci cerebrovaskulárních chorob, a to nejspíše na vrub zlepšené kontroly hypertenze (11). Naopak naše data nyní ukazují, že fatalita těchto příhod a dlouhodobější přežívání v sekundární prevenci po iCMP se v průběhu takřka dvou dekád (přinejmenším v Plzeňském regionu) zásadněji nezlepšily. Bohužel nutno konstatovat, že se v tomto parametru lišíme od vyspělých zemí západní Evropy či USA, kde je zlepšené přežívání po prodělané iCMP již prokazatelné. Longitudinální studie založená na Erlagenském registru mozkových mrtvic (realizovaná tedy ve velmi blízkém a i historicky dosti provázaném regionu) prokázala v průběhu dvacetiletého sledování (1996–2015) signifikantní pokles mortality či rekurence CMP (každý rok sledování byl v průměru spojen s asi 2% poklesem relativního rizika), a jak se dalo celkem čekat, přežívání bylo významně ovlivněno subtypem mozkové mrtvice (12). Dánská studie založená na celonárodním registru a zahrnující takřka 220 000 pacientů zjistila, že pětiletá mortalita po prodělané CMP klesla z 56,4 % v letech 1994–1998 na 46,1 % v letech 2004–2008 (13). Jiná studie z USA založená na sledování 8561 pacientů po iCMP mezi lety 2004 a 2018 prokázala signifikantně nižší jednoroční mortalitu v období 2014–18 (tj. 14,8 %), oproti předchozím dvěma obdobím 2009–13 a 2004–2008 (tj. 17,3 % a 17,0 %, resp.); paradoxně rekurence ischemických CMP během sledovaného období naopak stoupala (14). Je třeba také zdůraznit, že hodnoty jednoroční mortality byly v této studii zhruba poloviční, než ty pozorované v naší studii (14), a to navíc ještě před 14 lety. Pro kontext je také opět nutno zmínit situaci u pacientů po prodělaném infarktu myokardu, kde v ČR mezi lety 1994 a 2016 hospitalizační fatalita klesla ze 17 % na 7,5 % a pětiletá celková mortalita ze 41,7 na 34 % (15). Fakt, že mortalita pacientů po prodělané iCMP hospitalizovaných ve FN Plzeň neklesá, je tedy fenomén, který by měl být dále analyzován (v první řadě asi verifikován i v některých jiných regionech ČR) a zejména hledány jeho příčiny.
Příznivější obraz jsme zaznamenali v oblasti akutního managementu pacientů s iCMP, jmenovitě v nárůstu realizovaných trombolýz. Zatímco na počátku hodnoceného období („sezoně“ 2003–07) byla trombolýza provedena jen u necelých 3 % pacientů, ke konci („sezona“ 2016–19) stoupla indikace tohoto opatření na ≈ 48 %. Podobně v průběhu času výrazně narostl počet pacientů hospitalizovaných alespoň po nějaký čas na dedikované iktové jednotce a významně se zkrátila i průměrná doba hospitalizace; toto obojí ukazuje na zlepšený institucionální rámec péče o pacienty s CMP v akutním stadiu a její žádoucí centralizaci. Počínaje rokem 2014 se již rovněž začala u hodnocených pacientů realizovat endovaskulární mechanická trombektomie (jakožto nejúčinnější kauzální léčba trombotického uzávěru velké mozkové tepny (16)) a v „sezoně“ 2016–19 byl tento zákrok proveden u ≈ 7 % sledovaných pacientů. Jakkoliv se tento počet může zdát relativně nízký, nebude asi příliš daleko od realistického potenciálu této metodiky (který je silně modifikován časovým oknem, prokázanou přítomností okluze velké tepny a dalším faktory). Relativně ještě nedávná analýza z Velké Británie odhadla potenciál této metody asi na 15 % (17), zatímco jiná tamtéž dokonce jen na asi 10 % (18). Také, s jedinou výjimkou, v 7 provedených intervenčních studiích nepřesáhla indikace této metody 20 % (16).
V naší studii jsme se pokusili určit některé alespoň základní determinanty mortalitního rizika. Jak se dalo čekat, významný faktor představoval zejména věk pacientů, kdy každá věková dekáda byla spojena s asi 74–91% zvýšením rizika úmrtí. Paradoxně s vyšším rizikem bylo spojeno i umístění pacienta na iktové jednotce, což je ale celkem vysvětlitelné tím, že lehčí případy mozkových mrtvic (které mají zároveň lepší prognózu) jsou umisťovány rovnou na standardní lůžko. Trombolýza byla spojena s významnou, asi 12% redukcí rizika úmrtí z jakékoliv příčiny do 1 roku, zatímco v případě pětileté mortality byl již její efekt neutrální. Tato diskrepance může být dána tím, že jakkoliv je u pacienta úspěšně provedena trombolýza (tj. s dobrým efektem z hlediska neurologické deficitu), již sám fakt, že k ní muselo být přistoupeno, značí excesivní riziko recidivy CMP v budoucnosti – zejména pokud příslušného pacienta srovnáme s jiným, u něhož byla závažnost CMP natolik nízká, že k trombolýze vůbec přistoupeno nebylo. Tento výsledek tedy nelze interpretovat tak, že by trombolýzy nemělo smysl provádět, neboť k tomu naše analýza (díky svému observačnímu designu) není stavěná. Naopak jak dostupné důkazy, tak současná guidelines použití trombolýzy silně podporují jako jedno z mála kauzálních opatření v akutním managementu CMP (19, 20). Podobně jsme paradoxně pozorovali, že trombektomie byla spojena s významným vzestupem úmrtí do 1 roku. Zde předpokládáme identický fenomén, tj. že trombektomie byla používána u relativně těžších případů, a naopak nevyužívaná u pacientů s minimální symptomatologií, kteří však mají již z podstaty věci primárně lepší prognózu. Výsledky z randomizovaných intervenčních studií opět dokazují, že trombektomie je spojena s významným benefitem ve smyslu následného funkčního statusu (16) a je opět vysoce doporučitelným opatřením v akutním managementu iCMP (21).
Limitace studie
Naše analýza má samozřejmě řadu limitací. Především nezahrnuje rekuretní nefatální CMP jako jistě velmi podstatný ukazatel dalšího osudu sledovaných pacientů. Podobně jsme neměli u všech pacientů k dispozici spolehlivý údaj ohledně předchozích iCMP. Z důvodu aplikace směrnice GDPR totiž nebylo možno tyto parametry z dostupných registrů získat, resp. údaje máme k dispozici pouze u pacientů hospitalizovaných do roku 2012. V tomto částečném souboru (kohortě 4259 pacientů) došlo v průběhu 5 let k rekurentní nefatální iCMP u 860 osob (20,2 % souboru). V této analýze jsme rovněž nebrali v úvahu nakolik okolnosti sekundární prevence a další komorbidity ovlivnily prognózu pacientů po CMP. Z dat, co máme k dispozici (a plně zkompletována je máme opět pouze pro pacienty hospitalizované do roku 2012), vyplývá zejména, že léčba antikoagulancii, clopidogrelem či statiny byla spojena s významným přínosem ve smyslu pětileté mortality či rekurence CMP, zatímco přítomnost fibrilace síní, špatně kontrolované glykemie či zvýšeného kreatinu naopak riziko pacientů významně zvyšovala (tyto výsledky plánujeme publikovat v jiné analýze). Podobně by pro lepší stratifikaci individuálního mortalitního rizika pacientů (a zejména posouzení efektu trombolýzy/trombektomie) jistě bylo přínosné znát neurologický a celkový funkční status pacientů bezprostředně po manifestaci iCMP, resp. po definitivní stabilizaci (v podobě například NIHSS skóre či modifikovaného Rankinova skóre). Tyto údaje však opět pro celý, poměrně rozsáhlý, soubor nemáme k dispozici.
Závěry
Mortalita pacientů po iCMP zůstává enormní a přinejmenším na základě našich dat zatím nelze vysledovat jakýkoliv přesvědčivější trend ke zlepšení. Jakkoliv v průběhu sledovaného období došlo k poměrně zásadnímu zlepšení v oblasti akutní péče (zejména nárůstu počtu trombolýz, vyšší stupeň centralizace péče a nově též i zavedení intervenčních trombektomií), zásadnější efekt ve smyslu globálního zlepšení prognózy pacientů po CMP zatím prokázat nelze. Nejvyšší potenciál ke snížení zdravotně‑sociálních dopadů cévních mozkových příhod na populaci si tedy stále udržuje primární prevence.
Předkládaná analýza byla realizována za grantové podpory fondu Specifického výzkumu Univerzity Karlovy (grant SVV 260 393). Chtěli bychom rovněž poděkovat všem pracovníkům Ústavu zdravotnické informace a statistiky a jmenovitě p. Adolfu Binderovi za laskavé stanovení vitálního statusu našich pacientů, bez čehož by tato analýza nebyla možná.
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Lenka Kielbergerová
Neurochirurgická klinika LF UK a FN Plzeň
Alej Svobody 923, 301 00 Plzeň
Cit. zkr: Vnitř Lék. 2022;68(3):E4-E11
Článek přijat redakcí: 23. 2. 2022
Článek přijat po recenzích: 1. 4. 2022
Sources
1. Bruthans J, Cifkova R, Lanska V, O‘Flaherty M, Critchley JA, Holub J et al. Explaining the decline in coronary heart disease mortality in the Czech Republic between 1985 and 2007. Eur J Prev Cardiol. 2014;21 : 829-39.
2. ÚZIS. Zdravotnická statistika. Zemřelí 2017. stav zdravotnických informací a statistiky ČR. 2018. Praha. dostupné z https://www.uzis.cz/sites/default/files/knihovna/demozem2017. pdf. 2018.
3. Heuschmann PU, Kircher J, Nowe T, Dittrich R, Reiner Z, Cifkova R et al. Control of main risk factors after ischaemic stroke across Europe: data from the stroke‑specific module of the EUROASPIRE III survey. Eur J Prev Cardiol. 2015;22 : 1354-62.
4. Cífková R, Wohlfahrt P, Krajčoviechová A, Jozífová M, Mayer O, Vaněk J et al. Blood pressure control and risk profile in poststroke survivors: a comparison with the general population. J Hypertens. 2015;33 : 2107-14.
5. Vanek J, Mayer O, Wohlfahrt P, Kielbergerova L, Krajcoviechova A, Bruthans J et al. The changes of secondary prevention practice in Czech post‑stroke patients between 2007 and 2012/13. Cor Et Vasa. 2016;58:E367-E73.
6. Vaněk J, Mayer O, Seidlerová J, Bruthans J, Kielbergerová L, Wohlfahrt P et al. A comparison of secondary prevention practice in poststroke and coronary heart disease patients. Public Health. 2016;137 : 64-72.
7. OECD. OECD (2019), „Mortality following ischaemic stroke“, in Health at a Glance 2019: OECD Indicators, OECD Publishing, Paris. StatLink https://doi.org/10.1787/888934016227.
8. Mayer O, Jr., Rosolová H, Sefrna F, Neumann M, Simon J. Analysis of mortality trends in the West Bohemian Region in comparison with the entire Czech Republic 1988-1995. Cas Lek Cesk. 1998;137 : 207-10.
9. ÚZIS. Regionální zpravodajství NZIS. Dostupné z https://reporting.uzis.cz/).
10. Mayer O, Jr., Seidlerová J, Bruthans J, Opatrný J, Hromádka M, Jirák J et al. The prognostic impact of renal function decline during hospitalization for myocardial infarction. J Comp Eff Res. 2021;10 : 219-28.
11. Cífková R, Bruthans J, Wohlfahrt P, Krajčoviechová A, Šulc P, Jozífová M et al. 30-year trends in major cardiovascular risk factors in the Czech population, Czech MONICA and Czech post‑MONICA, 1985 - 2016/17. PLoS One. 2020;15:e0232845.
12. Rücker V, Heuschmann PU, O‘Flaherty M, Weingärtner M, Hess M, Sedlak C et al. Twenty‑Year Time Trends in Long‑Term Case‑Fatality and Recurrence Rates After Ischemic Stroke Stratified by Etiology. Stroke. 2020;51 : 2778-85.
13. Schmidt M, Jacobsen JB, Johnsen SP, Bøtker HE, Sørensen HT. Eighteen‑year trends in stroke mortality and the prognostic influence of comorbidity. Neurology. 2014;82 : 340-50.
14. Chaudhary D, Khan A, Shahjouei S, Gupta M, Lambert C, Avula V, et al. Trends in ischemic stroke outcomes in a rural population in the United States. J Neurol Sci. 2021;422 : 117339.
15. Bruthans J, Mayer O, Jarkovsky J, Zvolsky M. Long ‑ term trends in the incidence, treatment, hospital fatality and subsequent mortality from acute myocardial infarction in the Czech Republic. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub. 2021;165 : 283-90.
16. Goyal M, Menon BK, van Zwam WH, Dippel DW, Mitchell PJ, Demchuk AM et al. Endovascular thrombectomy after large‑vessel ischaemic stroke: a meta‑analysis of individual patient data from five randomised trials. Lancet. 2016;387 : 1723-31.
17. Tawil SE, Cheripelli B, Huang X, Moreton F, Kalladka D, MacDougal NJ et al. How many stroke patients might be eligible for mechanical thrombectomy? Eur Stroke J. 2016;1 : 264-71.
18. McMeekin P, White P, James MA, Price CI, Flynn D, Ford GA. Estimating the number of UK stroke patients eligible for endovascular thrombectomy. Eur Stroke J. 2017;2 : 319-26.
19. Berge E, Whiteley W, Audebert H, De Marchis GM, Fonseca AC, Padiglioni C et al. European Stroke Organisation (ESO) guidelines on intravenous thrombolysis for acute ischaemic stroke. Eur Stroke J. 2021;6:I ‑ lxii.
20. Neumann J, Šaňák D, Tomek A, Bar M, Herzig R, Kovář M et al. Doporučení pro intravenózní trombolýzu v léčbě akutního mozkového infarktu – verze 2021. Cesk Slov Neurol N 2021;84/117(3):291-99.
21. Šaňák D, Mikulík R, Tomek A, Bar M, Herzig R, Neumann J et al. Doporučení pro mechanickou trombektomii akutního mozkového infarktu – verze 2019. Cesk Slov Neurol N. 2019;82(6):700-5.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2022 Issue E-3
Most read in this issue- Adrenal incidentaloma
- Acute infections in kidney transplant recipients
- Detection, examination and therapy of sexual dysfunctions in patients with diabetes
- The mortality risk of patients hospitalized for ischemic stroke between 2003 and 2019
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

