-
Medical journals
- Career
Pomer butyrylcholínesteráza/HDL-cholesterol a aterogénny index plazmy u pacientov so steatózou pečene
Authors: Ladislav Turecký 1; Viera Kupčová 2; Monika Urfinová 1; Marcel Repiský 1; Eva Uhlíková 1
Authors‘ workplace: Ústav lekárskej chémie, biochémie a klinickej biochémie Lekárskej fakulty Univerzity Komenského a 1; III. interná klinika Lekárskej fakulty Univerzity Komenského v Bratislave 2
Published in: Vnitř Lék 2021; 67(E-2): 4-8
Category: Original Contributions
Overview
Kardiovaskulárne choroby na aterosklerotickom podklade predstavujú závažný zdravotnícky problém. Medzi dobre známe, závažné rizikové faktory pri vzniku kardiovaskulárnych ochorení patrí zmena v spektre lipoproteínov. Ako ukazujú práce viacerých autorov, môže vyšetrenie pomeru niektorých lipoproteínov poskytnúť presnejšiu informáciu o kardiovaskulárnom riziku u daného jedinca ako samotné jednotlivé lipidové parametre. Nealkoholová tuková choroba pečene (NAFLD) predstavuje v súčasnosti najčastejšiu formu chronickej hepatopatie.
Cieľom našej práce bolo vyšetriť lipoproteínové indexy – aterogénny index plazmy (AIP) a pomer butyrylcholínesteráza/ HDL-cholesterol – u pacientov s NAFLD a zhodnotiť aj ich zmeny vo vzťahu ku závažnosti steatózy pečene. Vyšetrovaný súbor tvorilo 64 pacientov so steatózou pečene, 32 mužov a 32 žien. Z biochemických parametrov sme u pacientov vyšetrovali sérové koncentrácie celkového cholesterolu, HDL - a LDL-cholesterolu, triacylglycerolov a aktivitu butyrylcholínesterázy.
Ako ukázali výsledky našej štúdie, oba základné lipidové parametre – celkový cholesterol a triacylglyceroly boli u pacientov so steatózou pečene zvýšené v porovnaní s hodnotami v kontrolnom súbore (Chol: 3,59 ± 0,16 vs. 5,14 ± 0,14 mmol/l; TAG: 0,85 ± 0,06 vs. 1,86 ± 0,14 mmol/l). Oba vyšetrované lipoproteínové indexy – AIP aj pomer BChE/HDL-cholesterol boli u pacientov so steatózou pečene taktiež signifikantne zvýšené (AIP: -0,191 ± 0,04 vs. 0,157 ± 0,04; BChE/HDL-C: 3171 ± 123 vs. 4602 ± 291). Hodnota pomeru BChE/HDL-cholesterol dobre korelovala s indexom celkový cholesterol/HDL cholesterol (korel.koef. 0,802) aj s aterogénnym indexom plazmy (korel.koef. 0,702). Nálezy zvýšených hodnôt AIP a pomeru BChE/ HDL-C potvrdili predpoklady o zvýšenom riziku vzniku kardiovaskulárnych ochorení u pacientov postihnutých stukovatením pečene. Nález signifikantnej pozitívnej korelácie medzi hodnotami AIP a BChE/HDL-C na jednej strane a fatty liver index (FLI) na druhej strane svedčí o tom, že toto riziko sa zvyšuje so závažnosťou steatotického poškodenia pečene.
Klíčová slova:
steatóza pečene – kardiovaskulárne riziko – butyrylcholínesteráza – aterogénny index plazmy – pomer BChE/ HDL-cholesterol – pomer celkový cholesterol/HDL-cholesterol.
Úvod
Kardiovaskulárne choroby (KVCH), z ktorých hlavná časť pripadá na aterosklerotické kardiovaskulárne choroby, sú zodpovedné v Európe každoročne za viac ako 4 milióny úmrtí, a preto je dôležitá prevencia ich vzniku (1). Dôležitou súčasťou prevencie je zmena životného štýlu a zníženie hodnôt rizikových faktorov (napr. LDL-cholesterolu, hodnôt tlaku krvi) podieľajúcich sa na vzniku týchto chorobných zmien.
Ateroskleróza je multifaktoriálna patologická zmena s komplexnou patogenézou. Jej vznik a rozvoj je podmienený súborom viacerých rizikových faktorov. Rizikový faktor môžeme charakterizovať ako klinický, laboratórny alebo psychologický znak, ktorého prítomnosť je spojená so štatisticky signifikantne vyššou pravdepodobnosťou, že k ochoreniu v budúcnosti dôjde (2). Medzi dobre známe laboratórne rizikové faktory vzniku KVCH patrí zvýšená koncentrácia LDL-cholesterolu a na cholesterol bohatých apoB-obsahujúcich lipoproteínov, pokles HDL-cholesterolu a zvýšenie koncentrácie triacylglycerolov. Niektorí autori poukazujú na skutočnosť, že používanie lipoproteínových pomerov (tzv. „aterogénne ukazovatele“) môže poskytnúť presnejšiu informáciu o kardiovaskulárnom riziku u daného jedinca ako samotné jednotlivé lipidové parametre (3). Pomer medzi koncentráciou celkového cholesterolu a HDLcholesterolu (T-Chol/HDL-C), nazývaný aj ako Castelliho index a pomer LDL-cholesterol/HDL-cholesterol sú dva dobre známe dôležité indikátory kardiovaskulárneho rizika, ktorých prediktívna hodnota je vyššia ako hodnota jednotlivých samostatných lipidových parametrov (3).
V našej práci sme venovali pozornosť dvom novším lipoproteínovým indexom – aterogénnemu indexu plazmy (AIP) a pomeru butyrylcholínesteráza/ HDL-C (BChE/HDL-C) u pacientov s nealkoholovou tukovou chorobou pečene (NAFLD). AIP je logaritmicky transformovaný pomer TAG/HDL-C, ktorý koreluje s veľkosťou HDL a LDL častíc (4, 5). Index BChE/ HDL-C uvádzajú Kutty a spol. (6) ako doplnkový rizikový faktor (complementary risk factor) ku indexu T-Chol/HDL-C (established risk factor). NAFLD je charakteristické hromadením triacylglycerolov (TAG) v pečeni. Závažnosť tejto poruchy spočíva v tom, že 10–20 % jedincov s NAFLD progreduje do nealkoholovej steatohepatitídy (NASH) až cirhózy pečene, prípadne hepatocelulárneho karcinómu. Zatiaľ čo jednoduchá steatóza pečene má relatívne benignú prognózu, NASH sa vyznačuje vysokým rizikom progresie do cirhózy pečene a hepatocelulárneho karcinómu (7, 8). V súčasnosti je NAFLD najčastejšou príčinou chronických hepatopatií. Epidemiologické štúdie ukázali, že v poslednom období došlo ku výraznému nárastu prevalencie NAFLD v mnohých krajinách (9, 10). Viaceré epidemiologické štúdie u pacientov s tukovým ochorením pečene ukázali, že kardiovaskulárne ochorenia predstavovali najčastejšiu príčinu smrti u týchto pacientov (11, 12, 13). Dá sa predpokladať, že významným prvkom v patogenéze KVCH u tejto skupiny pacientov je dyslipidémia. Cieľom našej práce bolo vyšetriť lipoproteínové indexy – AIP a BChE/HDL-C – u pacientov s NAFLD a zhodnotiť aj ich zmeny vo vzťahu ku závažnosti steatózy pečene.
Súbor pacientov a použité metódy
Vyšetrovaný súbor tvorilo 64 pacientov so steatózou pečene, 32 mužov a 32 žien. Vek pacientov sa pohyboval u mužov medzi 23 a 66 rokov, u žien medzi 29 a 76 rokov, priemerný vek v súbore bol 55,2 rokov, u žien 58,3 rokov a u mužov 52,3 rokov. Pacienti zaradení do súboru spĺňali sonografické kritériá pre steatózu pečene a mali pozitívne hodnoty steatotického indexu pečene (fatty liver index, FLI). FLI sme vyšetrovali podľa originálnej metódy Bedogniho a kol. (14), pričom výsledný algoritmus bol modifikovaný na základe prác Fedchuka a kol.(15) a Motameda a kol. (16), a zohľadňuje BMI, obvod pásu, sérovú hladinu TAG a sérovú aktivitu GGT. Hodnoty FLI nad 60,0 signalizujú prítomnosť steatózy pričom pozitívna prediktívna hodnota tohto indexu pri hodnotách nad 60 je 99 % a negatívna prediktívna hodnota 15 %. Hodnota FLI pod 30,0 vylučuje steatózu pečene (14). Ani jeden pacient z nášho súboru nemal hodnotu FLI menej ako 30. 89 % členov súboru malo hodnoty FLI viac ako 60.
Čo sa týka etiológie, vo väčšine prípadov išlo o nealkoholovú steatózu pečene, pričom u niekoľkých pacientov nie je možné vylúčiť v minulosti konzumáciu alkoholu a podiel alkoholu v patogenéze steatotického poškodenia pečene. Vo väčšine prípadov zohrávala v mechanizme vzniku steatózy pečene úlohu obezita, hyperlipoproteinémia, metabolický syndróm a diabetes mellitus.
U pacientov bol vyšetrený BMI, pričom hodnota BMI v norme (hodnota 18,5–25) bola len u 10 % pacientov, 38 % pacientov podľa BMI trpelo nadváhou (hodnota BMI 25 až 30), 47 % malo hodnoty BMI zodpovedajúce obezite (hodnoty 30–40) a 5 % pacientov dokonca extrémnej obezite (hodnota BMI viac ako 40). U 58 % pacientov bol prítomný diabetes mellitus.
Kontrolný súbor tvorilo 26 jedincov (15 žien, 11 mužov) bez klinických známok ochorenia. Išlo o študentov medicíny, pracovníkov zdravotníckeho zariadenia a ich rodinných príslušníkov. Priemerný vek bol 35,6 rokov (od 22 do70 rokov). Ani jeden člen kontrolného súboru netrpel diabetom ani nemal zvýšené sérové aktivity hepatálnych enzýmov (ALT, AST a GGT).
Krv sme odoberali ráno, nalačno za štandardných podmienok (po 12 hodinovom lačnení). Odoberali sme krv bez pridania protizrážlivého činidla a jednotlivé biochemické parametre sme vyšetrovali v sére. Na stanovenie sérovej koncentrácie cholesterolu, HDL-cholesterolu a TAG sme použili komerčné diagnostické súpravy. Aktivitu butyrylcholínesterázy sme vyšetrovali kineticky pri 25 °C s použitím butyrylthiocholín jodidu ako substrátu.
Pri štatistickom vyhodnotení výsledkov sme na základe skutočnosti, že sme si nie istý tvarom distribučnej funkcie meranej veličiny (či ide o normálne rozdelenie alebo nie), použili neparametrické testy (17). Pri porovnaní výsledkov medzi dvoma súbormi sme použili Wilcoxonov test. Ako limit významnosti používame hodnotu P < 0,05. Údaje v jednotlivých skupinách udávame ako aritmetické priemery x ± stredná chyba priemeru (SEM). Pri sledovaní vzájomnej závislosti dvoch parametrov sme používali Spearmanov koeficient korelácie a lineárnu regresiu (17). Výpočty sme robili pomocou štatistického programu SPSS (Statistical Package for the Social Sciences, SPSS Inc., Chicago, IL, USA) verzia 19 pre Microsoft Windows.
Výsledky
V tabuľke 1 sú uvedené výsledky oboch vyšetrovaných lipoproteínových indexov – CHE/HDL-C a aterogénny index plazmy (AIP) – ako aj hodnoty základných lipidových parametrov potrebných na ich výpočet. Ako sa ukázalo, oba základné lipidové parametre – celkový cholesterol a TAG boli u pacientov so steatózou pečene zvýšené v porovnaní s hodnotami v kontrolnom súbore. Hladina celkového cholesterolu sa zvyšovala o niečo viac ako o 40 % a triacylglyceroly o 118 % v porovnaní s kontrolným súborom.
Table 1. Vyšetrované lipidové parametre v sére pacientov so steatózou pečene a kontrol 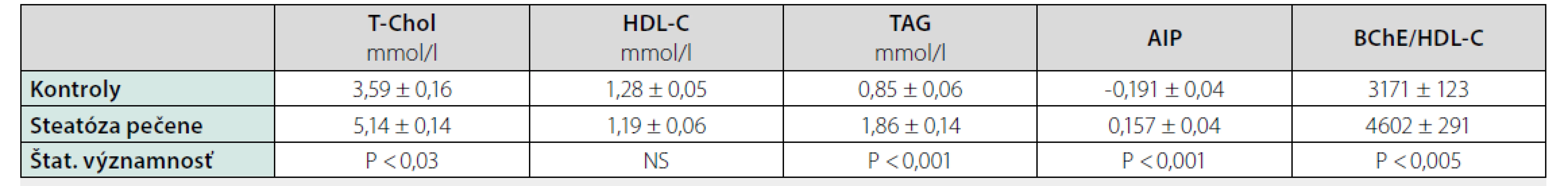
Výsledky udávame ako aritmetický priemer ± SEM, štatistická významnosť je oproti kontrolám Zvýšenie sérovej koncentrácie celkového cholesterolu aj TAG bolo štatisticky významné. Obe hodnoty, ako celkový cholesterol tak aj TAG boli v priemere vyššie ako doporučované hodnoty (cholesterol viac ako 5,0 mmol/l, triacylglyceroly viac ako 1,7 mmol/l) (18). Sérová koncentrácia HDL-cholesterolu bola u pacientov so steatózou pečene mierne znížená (zhruba o 10%) avšak táto zmena nebola štatisticky významná.
Hodnota aterogénneho indexu plazmy (AIP) bola u pacientov so steatózou pečene signifikantne vyššia ako u kontrol (0,157 ± 0,04 vs. -0,191 ± 0,04, P < 0,001). Rovnako aj pomer BChE/HDL-C bol u pacientov so steatózou pečene signifikantne zvýšený (4602 ± 291 vs. 3171 ± 123, P < 0,005).
Zaujímalo nás, do akej miery súvisí hodnota indexu BChE/HDL-C považovaného za doplnkový rizikový faktor so závažnosťou kardiovaskulárneho rizika vyjadreného pomerom T-Chol/HDL-C a aterogénnym indexom plazmy. Po rozdelení pacientov so steatózou pečene podľa hodnoty AIP na skupinu s nízkym rizikom KVCH (hodnota AIP menej ako 0,11), stredným rizikom KVCH (hodnota AIP 0,11–0,24) a vysokým rizikom KVCH (hodnota AIP viac ako 0,24) sa ukázalo, že hodnota indexu BChE/HDL-C sa s rastúcim rizikom KVCH signifikantne zvyšovala (Tab. 2).
Table 2. Hodnoty pomeru BChE/HDL-C u pacientov so steatózou pečene rozdelených podľa hodnoty aterogénneho indexu plazmy (AIP) 
Výsledky udávame ako aritmetický priemer ± SEM, štatistická významnosť je oproti kontrolám Pacienti s nízkym rizikom vzniku KVCH mali hodnotu pomeru BChE/HDL-C o niečo vyššiu ako v kontrolnom súbore (zhruba o 10 %), avšak tento rozdiel nebol štatisticky významný. Pacienti s hodnotami AIP, signalizujúcimi stredný stupeň rizika KVCH, mali hodnotu pomeru BChE/HDL-C signifikantne vyššiu v porovnaní s kontrolným súborom (zhruba o jednu tretinu). Pacienti s vysokým rizikom vzniku KVCH mali index BChE/HDL-C v porovnaní s kontrolami vyšší skoro o 100 % a táto hodnota bola štatisticky významne vyššia v porovnaní so skupinami s nízkym rizikom a stredným rizikom vzniku KVCH (P < 0,005). Regresná analýza závislosti hodnoty BChE/HDL-C na hodnote AIP ukázala šta - tisticky významnú lineárnu závislosť týchto dvoch veličín (korelačný koeficient = 0,702, P < 0,001) (Obr. 1).
Image 1. Korelácia medzi pomerom BChE/HDL-cholesterol a aterogénnym indexom plazmy u pacientov so steatózou pečene (P < 0,001) 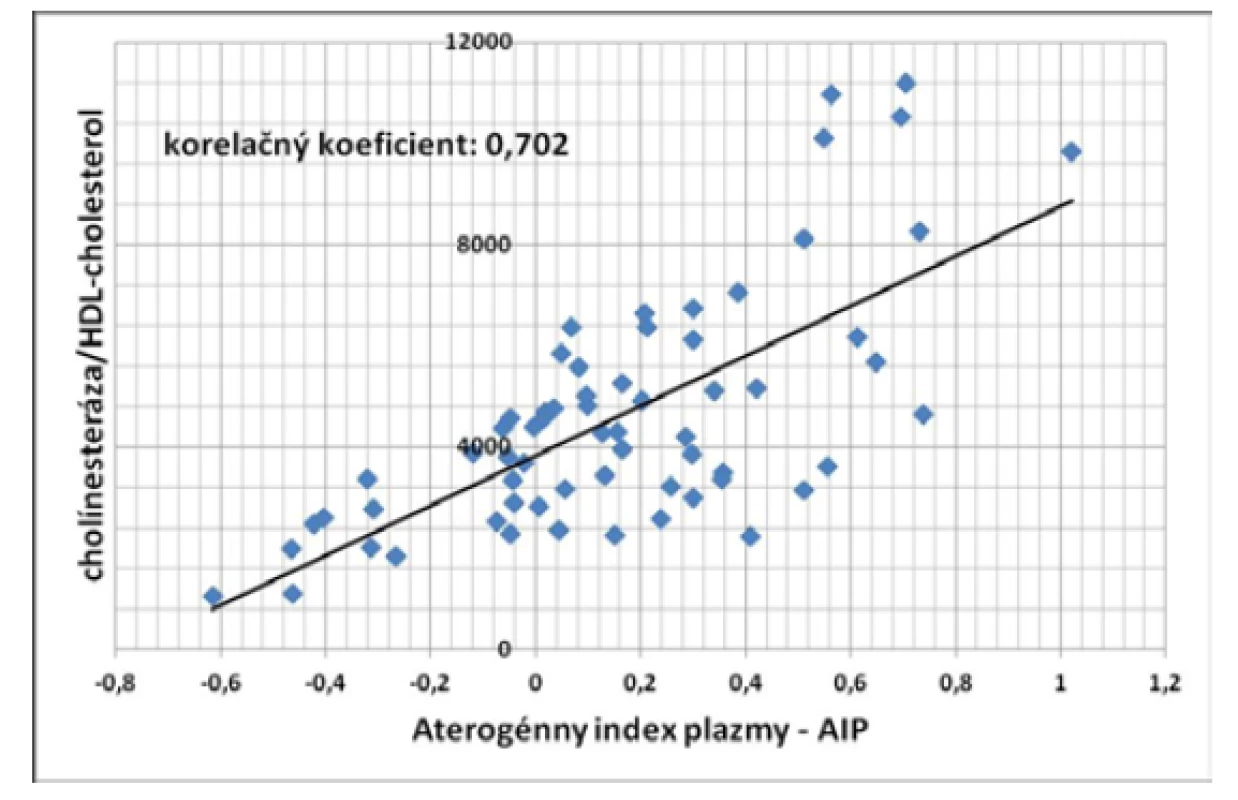
Podobné zmeny v hodnotách pomeru BChE/HDL-cholesterol sme zaznamenali aj po rozdelení pacientov so steatózou pečene do troch rizikových skupín na základe pomeru T-Chol/HDL-C (nízke riziko KVCH – hodnoty pomeru T-Chol/HDL-C menej ako 4,0, priemerné riziko KVCH – hodnoty pomeru 4,0–5,0 a zýšené riziko KVCH – hodnoty pomeru nad 5,0) (Tab. 3). Pacienti v nízko rizikovej skupine mali hodnoty indexu BChE/HDL-C v porovnaní s kontrolami prakticky nezmenené (zmena o 7 %). Pacienti v skupine s priemerným rizikom KVCH mali hodnoty v porovnaní s kontrolami o 23 % vyššie, pričom toto zvýšenie bolo štatisticky významné (P < 0,001). V skupine so zvýšeným rizikom KVCH boli hodnoty pomeru BChE/HDL-C vyššie o 117 %.
Table 3. Hodnoty pomeru BChE/HDL-C u pacientov so steatózou pečene rozdelených podľa hodnoty pomeru T-Chol/HDL-C 
Výsledky udávame ako aritmetický priemer ± SEM, štatistická významnosť je oproti kontrolám Podobne ako v prípade porovnania AIP a BChE/HDL-C ukázala regresná analýza veľmi dobrú štatisticky významnú pozitívnu koreláciu medzi T-Chol/ HDL-C a BChE/HDL-C (korelačný koeficient = 0,802, P < 0,001) (Obr. 2). Zaujímal nás aj vzťah hodnôt vyšetrovaných indexov ku závažnosti steatózy pečene vyjadrenej pomocou FLI (fatty liver index). V prípade vzťahu indexu BChE/HDL-C ku závažnosti steatózy pečene sa ukázala štatisticky významná pozitívna korelácia (korelačný koeficient = 0,572, P < 0,01) (Obr. 3). Dobrú koreláciu ukázala regresná analýza aj medzi hodnotami aterogénneho indexu plazmy a závažnosťou steatózy pečene (korelačný koeficient = 0,634, P < 0,005) (Obr. 4).
Image 2. Korelácia medzi pomerom BChE/HDL-cholesterol a pomerom T-Chol/HDL-cholesterol u pacientov so steatózou pečene (P < 0,001) 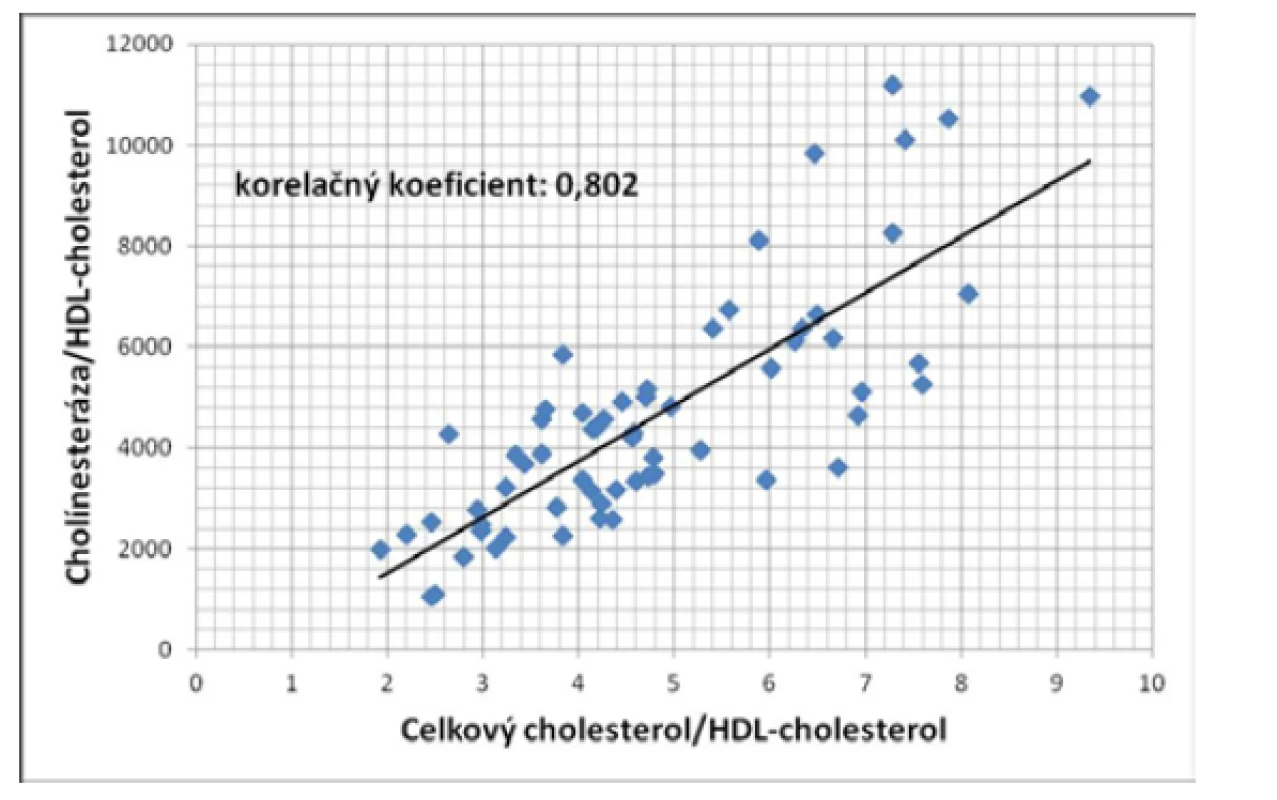
Image 3. Korelácia medzi pomerom BChE/HDL-cholesterol a tukovým indexom pečene (FLI) u pacientov so steatózou pečene (P < 0,01) 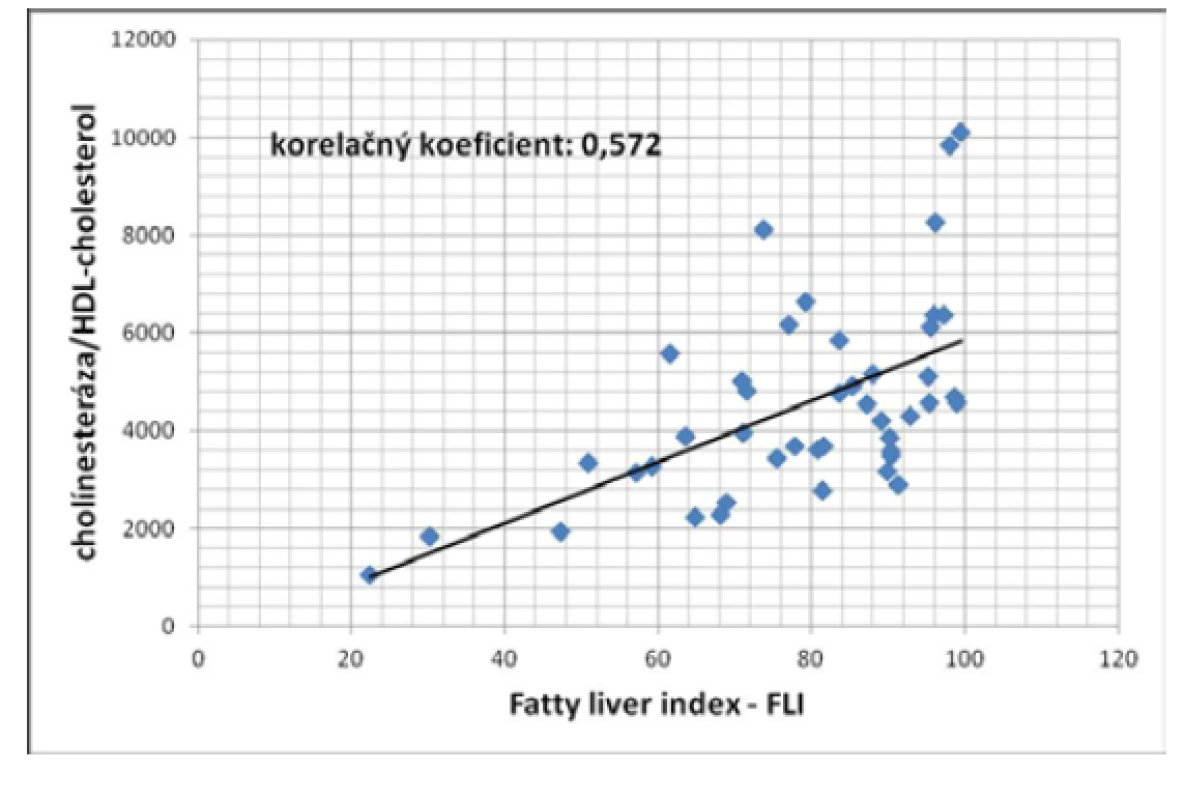
Image 4. Korelácia medzi aterogénnym indexom plazmy (AIP) a tukovým indexom pečene (FLI) u pacientov so steatózou pečene (P < 0,005) 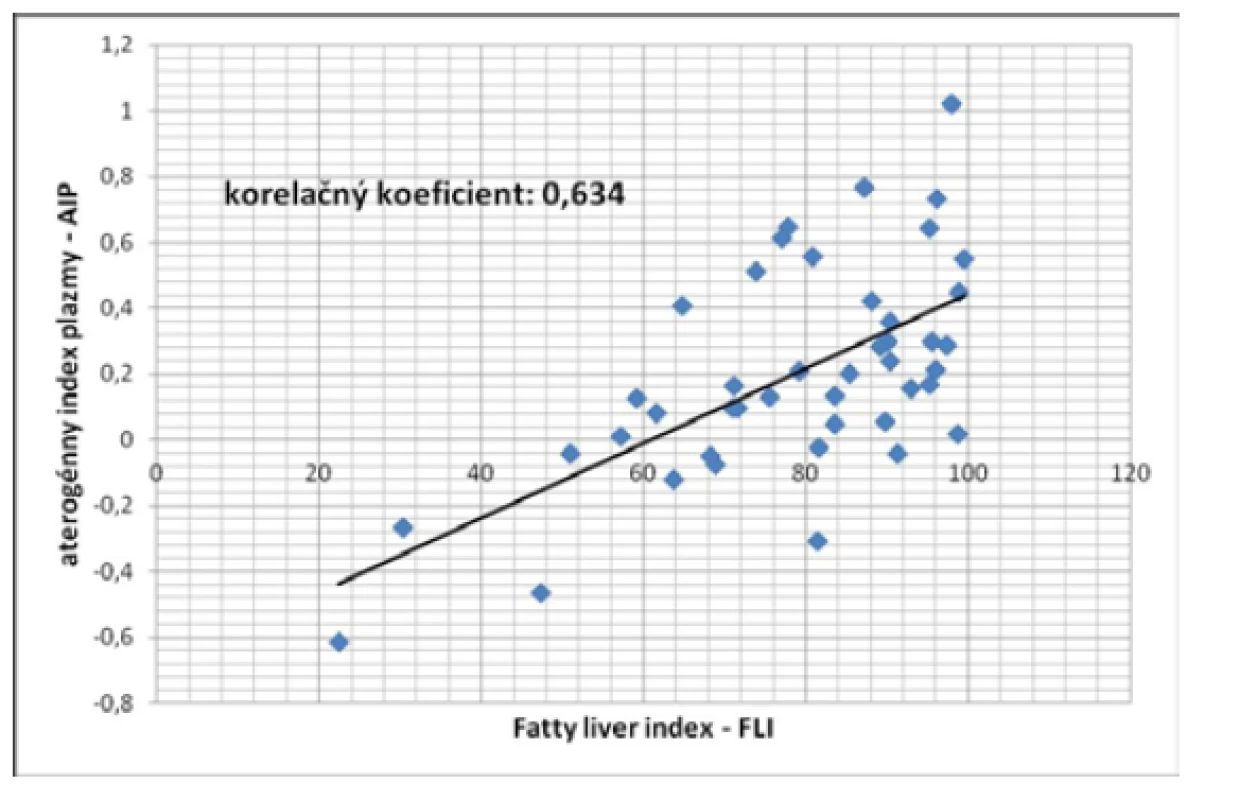
Diskusia
Ako ukázali výsledky našej štúdie, oba sledované lipoproteínové indexy, ktoré sa akceptujú ako rizikové faktory pri vzniku KVCH, boli v súbore pacientov so steatózou pečene signifikantne zvýšené.
Index AIP je logaritmicky transformovaný pomer sérových koncentrácií triacylglycerolov a HDL-cholesterolu a koreluje s veľkosťou HDL, LDL a VLDL častíc (5). Veľkosť lipoproteínových častíc predstavuje významný prvok pri hodnotení aterogénneho rizika a markery zohľadňujúce túto skutočnosť hodnotia aterogénny fenotyp plazmy presnejšie ako klasické biochemické parametre ako napr. celkový cholesterol, LDL-C, HDL-C a TAG. Z hľadiska rizikovosti sú dôležité veľkosti jednotlivých lipoproteínových častíc. Prevalencia veľkých HDL častíc má protektívny účinok, zatiaľ čo malé HDL častice zvyšujú aterogénne riziko. Podobne aj veľké LDL častice s menšou hustotou sú menej aterogénne ako malé denzné LDL častice. V prípade VLDL lipoproteínov je situácia opačná, rizikovejšie sú veľké, na TAG bohaté VLDL častice ako malé VLDL častice. Zvýšenie koncentrácie TAG a pokles koncentrácie HDL-cholesterolu majú za následok zvýšenie podielu rizikovejších malých HDL a LDL a veľkých VLDL častíc. Na základe týchto faktov vytvorili Dobiášová a spol. (4, 5, 19) index AIP, ktorý dobre koreluje s veľkosťou lipoproteínových častíc v sére pacientov a predstavuje tak dobrý ukazovateľ aterogénneho rizika. O tom, že pacienti so steatózou pečene sú vo zvýšenej miere ohrození vznikom KVCH svedčí nielen skutočnosť, že v súbore týchto pacientov bola hodnota AIP signifikantne vyššia ako u zdravých kontrol, ale aj skutočnosť, že až 44 % zo všetkých vyšetrovaných pacientov so steatózou pečene bolo vo vysoko rizikovej skupine s hodnotou AIP vyššou ako 0,24.
U pacientov so steatózou pečene sme zistili zvýšené hodnoty aj druhého sledovaného rizikového faktora – pomeru BChE/HDL-C. Enzým butyrylcholínesteráza (EC3.1.1.8., BChE), označovaný aj ako pseudocholínesteráza, je hydroláza syntetizovaná v hepatocytoch pečene a secernovaná do krvnej plazmy. BChE kóduje gén na chromozóme č.3 v polohe 3q26.1-26.2, ktorý má 4 exóny. Presná fyziologická funkcia BChE nie je dodnes jasná. BChE je schopná hydrolyticky štiepiť rôzne hydrofilné aj hydrofóbne estery cholínu a je známe, že sa podieľa aj na odbúravaní viacerých xenobiotík, ako sú napr. sukcinylcholín, mivacurium, lidokaín, prokaín, tetrakaín, niektoré analgetiká vrátane kyseliny acetylsalicylovej, kokaín a heroín (20). Ako ukazujú práce viacerých autorov, BChE je spojená aj s metabolizmom lipoproteínov (21, 22, 23). Sérová aktivita BChE korelovala so vzostupom sérovej koncentrácie TAG, LDL-C a poklesom koncentrácie HDL-C. Podávanie iso-OMPA, netoxického inhibítora sérovej BChE, vyvolávalo u experimentálnych zvierat zníženie koncentrácie TAG a VLDL v sére, čo naznačuje úlohu BChE v metabolizme VLDL. Koncentrácia HDL-cholesterolu má negatívny vzťah k riziku vzniku KVCH, čo súvisí s funkciou HDL v reverznom transporte cholesterolu z periférie do pečene. Dobrá korelácia pomeru BChE/HDL-C s aterogénnym indexom plazmy (AIP) a pomerom T-Chol/ HDL-C potvrdzujú vhodnosť použitia tohto indexu ako dobrého indikátora pri posudzovaní rizika vzniku kardiovaskulárnych chorôb.
Zvýšené hodnoty AIP a BChE/HDL-C potvrdzujú výsledky epidemiologických štúdií hovoriace o zvýšenom riziku vzniku KVCH u pacientov so steatózou pečene (12, 13, 24). Podstatnú úlohu pri zvýšení tohto rizika pravdepodobne zohrávajú poruchy metabolizmu lipoproteínov, charakterizované zvýšením aterogénneho charakteru profilu lipoproteínov plazmy u týchto pacientov.
Nález signifikantnej pozitívnej korelácie medzi hodnotami AIP a BChE/HDL-C na jednej strane a fatty liver index (FLI) na druhej strane svedčí o tom, že toto riziko sa zvyšuje so závažnosťou steatotického poškodenia pečene.
Závery
Nálezy zvýšených hodnôt AIP a pomeru BChE/HDL-C potvrdili predpoklady o zvýšenom riziku vzniku kardiovaskulárnych ochorení u pacientov postihnutých stukovatením pečene. Toto riziko sa zvyšovalo so závažnosťou steatotického poškodenia pečene. Z toho vyplýva, že v starostlivosti o týchto pacientov je potrebné venovať pozornosť nielen liečbe zabraňujúcej prechodu NAFLD do nealkoholovej steatohepatititídy resp. cirhózy pečene, ale aj prevencii vzniku kardiovaskulárnych chorôb, ktorými sú títo pacienti vo zvýšenej miere ohrození.
Poďakovanie. Štúdia bola finančne podporená grantom VEGA 1/0826/18
KORESPONDENČNÍ ADRESA AUTORA:
prof. MUDr. Ladislav Turecký, CSc.
ladislav.turecky@fmed.uniba.sk
Ústav lekárskej chémie, biochémie a klinickej biochémie LFUK,
Sasinkova 2, 811 08 Bratislava, Slovenská republika
Článek přijat redakcí: 6. 9. 2020
Článek přijat po recenzích k publikaci: 24. 2. 2021
Sources
1. Mach F, Baigent C, Catapano AL, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J 2020; 41(1): 111–188.
2. Žák A. Poruchy metabolismu lipidu a lipoproteinu. In: Zima T (ed): Laboratorní diagnostika.
3. vydanie. Galén: Praha 2013 : 169–207. ISBN 978-80-7492-062-2. 3. Millán J, Pintó X, Muňoz A, et al. Lipoprotein ratios: Physiological significance and clinical usefulness in cardiovascular prevention. Vascular Health and Risk Management 2009; 5 : 757–765.
4. Dobiášová M, Frohlich J. Nový aterogenní index plazmy (AIP) odpovídá poměru triglyceridů a HDL-cholesterolu, velikosti částic lipoproteinů a esterifikační rychlosti cholesterolu: změny po léčbě lipanorem. Vnitř Lék 2000; 46(3): 152–156.
5. Dobiášová M. AIP – Aterogenní index plazmy jako významný prediktor kardiovaskulárního rizika: od výskumu do praxe. Vnitř lék 2006; 52(1): 64–71.
6. Kutty KM, Jain R, Huang S, et al. Serum pseudocholinesterase: high density lipoprotein cholesterol ratio as an index of risk for cardiovascular disease. Clin Chim Acta 1981; 115(1): 55–61.
7. Wierzbicki AS, Oben J. Nonalcoholic fatty liver and lipids. Curr Opinion Lipidol 2012; 23(4): 345–352.
8. Maratos-Flier E. Fatty liver and FGF21 physiology. Experimental Cell Res 2017; 360(1): 2–5.
9. Chitturi S, Farrell GC, Hashimoto E, et al. Non-alcoholic fatty liver disease in the Asia - -Pacific region: definitions and overview of proposal guidelines. J Gastroenterol Hepatol 2007; 22(6): 778–787.
10. Fan JG, Farrell GC. Epidemiology of non-alcoholic fatty liver disease in China. J Hepatol 2009; 50(1): 204–210.
11. Söderberg C, Stal P, Askling J, et al. Decreased survival of subjects with elevated liver function tests during a 28-year follow-up. Hepatology 2010; 51(2): 595–602.
12. Brea A, Pintó X, Ascaso JF, et al. Nonalcoholic fatty liver disease, association with cardiovascular disease and treatment. (I) Nonalcoholic fatty liver disease and its association with cardiovascular disease. Clin Investig Arterioscler 2017; 29(3): 141–148.
13. Bedogni G, Gastaldelli A, Foschi FG. Fatty liver, cardiometabolic disease and mortality. Curr Opinion Lipidol 2020; 31(1): 27–31.
14. Bedogni G, Bellentani S, Miglioli L, et al. The fatty liver index: a simple and accurate predictor of hepatic steatosis in the general population. BMC Gastroenterol 2014; 6: doi: 10.1186/1471-230X-6-33.
15. Fedchuk L, Nascimbeni F, Pais R, et al. Performance and limitations of steatosis biomarkers in patients with nonalcokolic fatty liver disease. Aliment Pharmacol Therap 2014; 40(10): 1209–1222.
16. Motamed N, Sohrabi M, Ajdarkosh M, et al. Fatty liver index vs waist circumference for predicting non-alcoholic fatty liver disease. World J Gastroenterol 2016; 22(10): 3023–3030.
17. Havránek T. Statistika pro biologické a lékařské vědy. Academia Praha 1993, 478 s. ISBN 80-200-0080-1
18. von Eckardstein A, Thomas L. Lipoprotein-stoffwechsel. In: L.Thomas (ed): Labor und Diagnose, Vol.1, TH-Books Verlagsgesellschaft mbH Frankfurt/Main 2012; 8 : 254–281. ISBN 978-3-9805215-8-1
19. Dobiášová M. Atherogenic index of plasma [log(triglycerides/HDL-cholesterol)]: theoretical and practical implications. Clin Chem 2004; 50(7): 1113–1115.
20. Pohanka M. Diagnoses of pathological states based on acetylcholinesterase and butyrylcholinesterase. Curr Med Chem 2020; 27(18): 2994–3011.
21. Rustemeijer C, Schouten JA, Voerman HJ, et al. Is pseudocholinesterase activity related to markers of triacylglycerol synthesis in type II diabetes mellitus? Clin Sci (Lond) 2001; 101(1): 29–35.
22. Iwasaki T, Yoneda M, Nakajima A, et al. Serum butyrylcholinesterase is strongly associated with adiposity, the serum lipid profile and insulin resistance. Internal Med 2007; 46(19): 1633–1639.
23. Oda E. Associations between serum cholinesterase and incident hyper-LDL cholesterolemia, hypertriglyceridemia and hypo-HDL cholesterolemia as well as changes in lipid levels in a health screening population. Atherosclerosis 2015; 241(1): 1–5.
24. Mathews SE, Kumar RB, Shukla AP. Nonalcoholic steatohepatitis, obesity and cardiac dysfunction. Curr Opinion Endocrinol Diabetes Obesity 2018; 25(5): 315–320.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2021 Issue E-2-
All articles in this issue
- Pomer butyrylcholínesteráza/HDL-cholesterol a aterogénny index plazmy u pacientov so steatózou pečene
- Stanovenie LDL-cholesterolu novými rovnicami Martin a Sampson, porovnanie so starým Friedewaldom na reálnych dátach a na umelom súbore
- Reumatoidná artritída a poruchy metabolizmu
- Nefarmakologická liečba dny
- Použitie chirurgického rúška spolu s vysoko-prietokovou nazálnou kanylou (HFNC) vedie k zlepšeniu oxygenácie u pacientov s COVID-19: súbor kazuistík
- Primárna pneumokoková peritonitída s fulminantným priebehom
- Screening rizikového užívání alkoholu v ordinaci lékaře
- RECENZE MONOGRAFIE SRDEČNÍ SELHÁNÍ
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nefarmakologická liečba dny
- Pomer butyrylcholínesteráza/HDL-cholesterol a aterogénny index plazmy u pacientov so steatózou pečene
- Screening rizikového užívání alkoholu v ordinaci lékaře
- Reumatoidná artritída a poruchy metabolizmu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

