-
Medical journals
- Career
Prvé prípady geneticky potvrdenej kongenitálnej hnačky so stratou chloridov na Slovensku
Authors: Ľudmila Podracká; Mária Chocholová
Authors‘ workplace: Detská klinika LF UK a Národného ústavu detských chorôb Bratislava, Slovenská republika
Published in: Vnitř Lék 2020; 66(3): 186-189
Category: Case Report
Overview
Chloridové ióny sa podieľajú na regulácií objemu buniek, sekrécii telesných tekutín a udržaní acidobázickej rovnováhy. Hypo/hyperchlorémia u novorodencov a dojčiat je emergentná situácia vyžadujúca dôkladnú diferenciálnu diagnostiku na zistenie kauzálnej príčiny stavu. K vzácnym príčinám poruchy vylučovania chloridových iónov patrí kongenitálna chloridorea (CLD), ktorá je charakterizovaná torpídnymi objemnými hnačkami, vysokou koncentráciou chloridov v stolici a metabolickou alkalózou. CLD je zriedkavé autozómovo‑recesívne ochorenie zapríčinené mutáciou SLC26A3 génu lokalizovaného na chromózome 7q31, ktorý kóduje transmembránový proteín v intestinálnych bunkách. Genetický defekt spôsobuje poruchu črevnej absorpcie chloridov a sekrécie bikarbonátov. Profúzne hnačky zapríčiňujú významné straty vody a elektrolytov, čo vedie k volumovej deplécií, hyperreninémii, hyperaldosteronizmu, renálnym stratám kália a u niektorých aj k rozvoju chronickej nefropatie. Autori prezentujú vzácne kazuistiky 2 bratov s geneticky potvrdenou CLD. Obidve deti sa narodili s nižšou pôrodnou hmotnosťou a krátko po narodení vyžadovali hospitalizáciu pre distendované bruško a hnačky so závažnou dehydratáciou a elektrolytovou dysbalanciou. V laboratórnom obraze dominovala signifikantná hypochlorémia (76 mmol/l resp. 78 mmol/l) a extrémna metabolická alkalóza (pH 7,63; HCO3 46 mmol/l resp. pH 7,73; HCO3 40 mmol/l). Vylúčili sme renálne straty chloridov a cystickú fibrózu; vyšetrenie koncentrácie chloridov v stolici na našom pracovisku nebolo dostupné. Po substitučnej liečbe sa biochemické abnormality čiastočne upravili, vodnaté stolice pretrvávajú ďalej. V ďalšom vývoji pacienti slabšie prospievali a pre epizódy dehydratácie boli opakovane hospitalizovaní na podanie parenterálnej liečby. Renálne funkcie sú vo veku 6 resp. 2 roky primerané, ale starší chlapec má známky počínajúcej nefrokalcinózy. Priamym sekvenovaním kódujucej oblasti génu SLC26A3 sa u obidvoch súrodencov detegoval rovnaký genotyp – doteraz neopísaný variant c.629_63Ildel (p. Ile210del) a patogénny variant v géne SLC26A3 v heterozygótnom stave. Pri perzistujúcich vodnatých hnačkách, hypochlorémii, hypokaliémii a metabolickej alkalóze treba myslieť na konge ‑ nitálnu chloridorheu. Diagnóza sa opiera o charakteristický klinický obraz vodnatých hnačiek od novorodeneckého veku, dôkaz vysokej koncentrácie chloridov v stolici > 90 mmol/l a molekulovo‑genetické vyšetrenie. Pacienti s CLD vyžadujú pravidelné nefrologické sledovanie pre riziko rozvoja chronickej nefropatie a funkčné poškodenie tubulov.
Klíčová slova:
alkalóza – hypochlorémia – kongenitalne chloridové hnačky
Úvod
Torpídne hnačky s rozvratom vnútorného prostredia u novorodencov a dojčiat predstavujú emergentnú situáciu, ktorá vyžaduje širokú diferenciálnu diagnostiku a promptnú substitučnú liečbu. Neliečené stavy vedú k bezprostrednému ohrozeniu života a môžu končiť letálne už v prvých týždňoch po narodení. K raritným príčinám závažnej hypochlorémie a metabolickej alkalózy patria kongenitálne chloridové hnačky (CLD). V predkladanom článku uvádzame vzácne kazuistiky 2 súrodencov s excesívnou hypochlorémiou asociovanou s extrémnou metabolickou alkalózou, u ktorých sme geneticky potvrdili CLD.
Prvá zmienka o raritnom ochorení pochádza z roku 1945, kedy Darrow a Gamble nezávisle od seba opísali 2 simultánne prípady detí s novým, dovtedy nepoznaným syndrómom charakterizovaným vodnatou hnačkou, vysokou koncentráciou chloridov v stolici a metabolickou alkalózou a pomenovali ho kongenitálna alkalóza (1, 2). O 2 dekády neskôr familiárne zoskupenie viacerých prípadov vo Fínsku podnietilo záujem vedcov o hľadanie genetickej a klinickej charakteristiky tohto zriedkavého ochorenia (3). Úsilie bolo korunované objavením genetickej príčiny a objasnením poruchy transportu chloridov v distálnom ileu a hrubom čreve, čo viedlo k výstižnej zmene názvu ochorenia na kongenitálne chloridové hnačky (congenital chloride diarrhoe, OMIM # 214700, CLD) (3, 4). V 60. rokoch 20. storočia sa zaviedla do rutinnej liečby pravidelná substitúcia elektrolytov, ktorá je dodnes život zachraňujúcou terapiou detí s CLD.
CLD je zriedkavé autozómovo‑recesívne ochorenie zapríčinené mutáciou SLC26A3 génu lokalizovaného na chromózome 7q31, ktorý kóduje transmembránový proteín v intestinálnych bunkách. Genetický defekt spôsobuje poruchu črevnej absorpcie chloridov a sekrécie bikarbonátov (5). Profúzne hnačky zapríčiňujú významné straty vody a elektrolytov, čo vedie k volumovej deplécii, hyperreninémii, hyperaldosteronizmu, renálnym stratám kália a u niektorých aj k rozvoju chronickej nefropatie. Diagnóza kongenitálnej chloridovej hnačky sa v neonatálnom období opiera o typický klinický obraz a vysokú koncentráciu chloridov v stolici presahujúcu 90 mmol/l. Pri extrémnej dehydratácii a soľnej deplécii sa kompenzačne znižuje frekvencia a objem hnačiek, čo vyvoláva prechodne nízke koncentrácie chloridov v stolici. Ide však o tranzientný jav a preto pri podozrení na CLD treba vyšetrenie stolice opakovať. Vo väčšine prípadov je jednoduché meranie fekálnych chloridov spolu s vodnatou stolicou s pH v rozmedzí 4–6 dostatočné na potvrdenie diagnózy (5). Ak sa ochorenie nediagnostikuje v ranom detstve, protrahovaný chronický priebeh s hypovolémiou a hypoelektrolytémiou vedie k spomaleniu telesného rastu. Akútne zhoršenie klinického stavu môže nastať po bežných infekciách alebo vracaní. Nezriedka sa ochorenie môže diagnostikovať až po dlhej perióde chronickej hnačky neznámej etiológie. Chronické zníženie intravaskulárneho priestoru predisponuje k závažným komplikáciám ako je renálne poškodenie a dna (6).
V článku prezentujeme vzácne kazuistiky 2 súrodencov s torpídnou hypochlorémiou zapríčinenou kongenitálnou chloridovou hnačkou.
Kazuistiky
Obidvaja bratia non‑konsanguinných rodičov pochádzajú z gravidity po in vitro fertilizácii a embryo transfere pre oligoastenoteratozoospermiu otca. V širokom príbuzenstve sa ochorenie gastrointestinálneho traktu ani chronické hnačky nevyskytujú.
Starší proband je 1. dieťa rodičov, v súčasnosti má 6 rokov. Pre rizikovú graviditu bola matka pravidelne kontrolovaná a starostlivo podstúpila všetky odporúčané prenatálne diagnostické testy. Z pozoruhodných nálezov treba zmieniť obraz dilatácie črevných kľučiek pozorovaný na ultrazvuku plodu v 30. týždni gravidity. Chlapček sa narodil predčasne, v 33. týždni s nižšou pôrodnou hmotnosťou 2 160 g a dĺžkou 49 cm. Po narodení vyžadoval intenzívnu liečbu vrátane oxygenoterapie pre tachydyspnoe a cyanózu. Pre podozrenie na črevnú obštrukciu bola indikovaná natívna snímka brucha, ktorá preukázala subileózny stav, na 3. deň sa pasáž gastrointestinálnym traktom obnovila a od operácie sa upustilo. Dieťa vo veku 4 mesiacov bolo pre hypotóniu, neprospievanie a hnačky odoslané na našu kliniku. Už pri vstupnom vyšetrení sme v laboratórnom obraze zistili signifikantný rozvrat vnútorného prostredia, dominovala závažná hypochlorémia sprevádzaná extrémnou metabolickou alkalózou a hypokaliémia (Tab. 1). Po intenzívnej parenterálnej substitúcii elektrolytov sa celkový klinický stav a ionogram čiastočne upravili, ale naďalej pretrvávali početné stolice. Po širokej diferenciálnej diagnostike a vylúčení iných príčin sme suponovali vrodené chloridové hnačky. V súčasnosti je chlapček drobnejšieho vzrastu, bez mentálneho deficitu. Denne má 5–7 vodnatých stolíc, krvný tlak je v pásme 50. percentilu. Na dlhodobej perorálnej substitúcii (20 mmol NaCl/deň) si relatívne udržiava elektrolytovú rovnováhu, hodnoty plazmatickej renínovej aktivity a aldosterónu sú v norme. Z recentných nálezov sa pridružila hyperurikémia a na ultrasonografii incipientná nefrokalcinóza. Glomerulová filtrácia zodpovedá 90 ml/min/1,73 m2 .
Table 1. Laboratórne parametre u pacienta č. 1 v úvode ochorenie 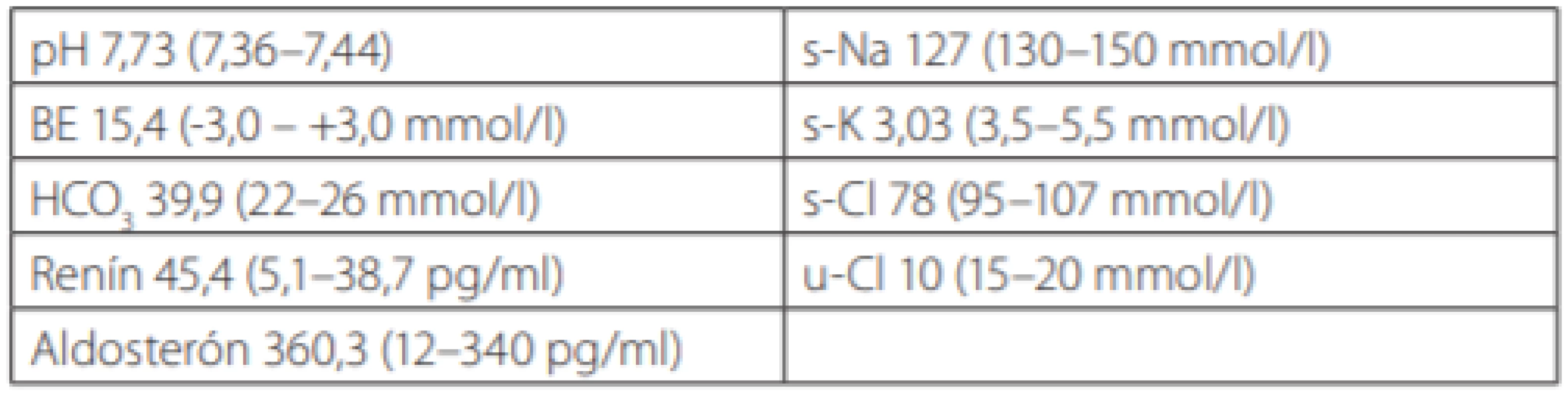
Table 2. Laboratórne parametre u pacienta č. 2 v úvode ochorenia 
2-ročný brat prvého pacienta je tiež z in vitro fertilizácie. Jeho postnatálny vývoj a priebeh boli takmer identické ako u staršieho súrodenca. Narodil sa predčasne v 32. gestačnom týždni s nižšou pôrodnou hmotnosťou 2380 g a dĺžkou 46 cm a Apgar skóre 6/8. Krátko po narodení sa manifestovala hypotónia, subcyanóza a novorodenecká žltačka s potrebou fototerapie. Pacient od začiatku neprospieval, intermitentne teplotoval a vracal, v popredí kliniky boli nápadné profúzne hnačky. Pre epizódy dehydratácie vyžadoval opakované hospitalizácie. V ionograme bola normonatriémia (140 mmol/l), priekazná hypokaliémia (2,76 mmol/l) a hypochlorémia (76 mmol/l) asociovaná s výraznou metabolickou alkalózou (pH 7,63; HCO3 46,2 mmol/l). Odpady chloridov močom boli znížené (menej ako 15 mmol/l), čo vylúčilo renálnu príčinu hypochlorémie. Dieťa je na pravidelnej perorálnej substitúcií chloridom sodným 15 mmol/deň a draselným, zvláda bežné nekomplikované infekcie, no aj u neho perzistujú časté vodnaté stolice. Pre nápadnú podobnosť fenotypických prejavov obidvoch súrodencov sme predpokladali genetickú príčinu chronických hnačiek a indikovali sme molekulovo‑genetické vyšetrenie. Priamym sekvenovaním kódujucej oblasti génu SLC26A3 sa u obidvoch súrodencov detegoval rovnaký genotyp – doteraz neopísaný variant c.629_63Ildel (p. Ile210del) a patogénny variant c.2024_2026dup(p. Ile675dup) v heterozygótnom stave. U rodičov sme segregačnou analýzou zistili, že matka je bezpríznakovou nosičkou patogénneho variantu SLC26A3 (c.629_63I1del (p. Ile210del)) v heterozygotnom stave a patogénny variant c.2024_2026dup(p. Ile675dup) identifikovaný u otca je zrejme príčinou oligoasthenoteratozoospermie.
Podľa našich dostupných vedomostí ide o prvé prípady geneticky potvrdenej kongenitálnej chloridovej hnačky na Slovensku aj v Čechách.
Diskusia
Kongenitálne chloridové hnačky patria k vzácnym príčinám hypochlorémie asociovanej s metabolickou alkalózou. V svetovej literatúre je doteraz opísaných iba 250 prípadov tohto zriedkavého ochorenia. Najvyššia incidencia je hlásená z Fínska (1 : 30 000–1 : 40 000), Poľska (1 : 20 0000) a arabských krajín v okolí Perzského zálivu, čo sa vysvetľuje vysokou mierou pokrvných manželstiev (7). Výskyt v iných geografických oblastiach či ďalších krajinách Európy nie je známy. V prezentovanom článku opisujeme prvé 2 prípady slovenských pacientov s geneticky potvrdenou CLD. CLD (OMIM # 214700) je zriedkavé dedičné autozómovo‑recesívne ochorenie, zapríčinené mutáciou génu SLC26A3 (solubile family 26protein A3) lokalizovaného na chromozóme 7q31 (8). SLC26A3 kóduje transmembránový proteín, ktorý reguluje transport Cl-⁄ HCO3 - aniónov v črevnom epiteli (9). Jeho kľúčový význam v chloridovej homeostáze sa potvrdil aj v experimentálnom modeli SLC26A3-deficitných myší (10).
Hoci je známych viac ako 50 rôznych mutácií SLC26A3 génu, napriek variabilite mutácií a ich širokej distribúcii v rozličných oblastiach SLC26A3 génu, neexistujú relevantné dôkazy o genotypovo fenotypových koreláciách (11). Dokonca aj identické genetické pozadie CLD môže prebiehať pod rôznym klinickým obrazom, ak sa ochorenie neskoro diagnostikuje a/alebo liečba nie je adekvátna (12). U našich 2 súrodencov sme detegovali 2 rôzne patogénne varianty v heterozygotnom stave. Mutácia identifikovaná u staršieho probanda nebola doteraz v literatúre opísaná. CLD sa dedí autozómovo‑recesívne. Familiárny výskyt je častý aj v nepríbuzenských rodinách. V nedávno publikovanej sérií 8 kórejských detí z nonkonsanguiných rodín až 4 probandi tvorili 2 súrodenecké páry, z toho jeden pár tvorili dvojvaječné dvojčatá (13). Je zaujímavé, že podobne ako v kórejskej kohorte aj naši dvaja súrodenci sú mužského pohlavia. Nové doteraz neopísané mutácie u nášho pacienta ako aj u kórejských detí potvrdzuje širokú genetickú variabilitu CLD.
Kauzálny genetický defekt intestinálneho Cl-/HCO3 -aniónoveho meniča spôsobuje poruchu aktívneho vstrebávania chloridov v epitelových bunkách ilea a hrubého čreva (14). Sekundárne je poškodený aj sodíkovo vodíkový transport cez Na+/H+ meniče (15). Klinickým dôsledkom je masívna strata NaCl a tekutín črevom prejavujúca sa objemnou na vodu a chloridy bohatou hnačkou. V neliečených prípadoch, hypochlorémia, hyponátriémia a dehydratácia aktivujú systém renín‑angiotenzín‑aldosterón, čo indukuje reabsorpciu sodíka a sekréciu draslíka v distálnom úseku hrubého čreva a distálnom tubule obličiek. Kompenzačnými hormonálnymi mechanizmami sa sodík v sére zvýši, avšak za cenu straty draslíka, čo vedie k signifikantnej hypokaliémii. Na metabolickej alkalóze sa čiastočne podieľa zvýšená exkrécia vodíkových iónov a chýbanie sekrécie bikarbonátov v ileu a kolone. Už intrauterínne sa pozoruje objemné vylučovanie tekutej stolice imitujúcej moč, čo má za následok rozšírenie črevných kľučiek a polyhydramnion (16). Pri starostlivom sonografickom vyšetrení sú tieto markantné znaky viditeľné už prenatálne, podobne ako to bolo u nášho prvého pacienta. Postihnutí jedinci sa zvyčajne rodia s nízkou pôrodnou hmotnosťou, majú nápadné distendované brucho a viditeľnú peristaltiku črevných kľučiek. Nie je zriedkavosťou, že tieto klinické príznaky sa chybne interpretujú ako črevná obštrukcia a môžu viesť k zbytočnej chirurgickej intervencii (13). Skoro po narodení sa objaví profúzna vodnatá hnačka, ktorá sa pre tekutú konzistenciu môže ľahko pomýliť s močom. Falošná „polyúria“ a dehydratácia s typickou poruchou elektrolytov môžu viesť k zámene s Bartterovým syndrómom, tubulopatiou zapríčinenou genetickým defektom Na‑K-Cl kotransportéra vedúceho k výrazným stratám chloridov močom. Pacient sa nezriedka môže diagnostikovať až po dlhej perióde chronickej hnačky neznámej etiológie. Protrahované chronické zníženie intravaskulárneho priestoru predisponuje k závažným komplikáciám ako je renálne poškodenie a dna (17). Hnačka a fekálna inkontinencia u chorých s CLD je celoživotná. Vo fínskej sérii pacientov varíroval počet stolíc od 2 do 7 hnačiek za deň, čo korešponduje aj s anamnestickými údajmi našich probandov (18). Obličkové poškodenie je najzávažnejšou komplikáciou nesprávnej terapie CLD v detstve. Chronická hypovolémia aktivuje renín a angiotenzín s vývojom sekundárneho hyperaldosteronizmu, ktorý indukuje podobné cievne zmeny v obličke, ako sa pozorujú pri hypertenzii, hoci pacienti majú normálny tlak krvi. Chronická hypokaliémia vedie k funkčnému poškodeniu renálnych tubulov a črevných absorpčných buniek. V odbornej literatúre sú opísané 2 prípady pacientov s CLD a chronickým zlyhaním obličiek, ktorí podstúpili úspešnú transplantáciu obličiek (18).
Až u 6 z 8 kórejských detí sa ochorenie diagnostikovalo oneskorene a mesiace až roky sa mylne viedlo ako chronické nešpecifické hnačky a/alebo Bartterov syndróm (13). U našich súrodencov sme Bartterov syndróm nepriamo vylúčili nízkymi hodnotami chloridov v moči, preto sme zvažovali chloridovú hnačku. Pri určení správnej diagnózy je nápomocné jednoduché meranie koncentrácie chloridov konvenčným analyzátorom krvných plynov vo vzorke stolice. Užitočné je aj stanovenie pH stolice, ktoré môže iniciálne včasne rozlíšiť kyslú chloridovú hnačku od ostatných dedičných sekretorických hnačiek, ktoré spôsobujú alkalické stolice. Na Slovensku meranie fekálnych chloridov nie je dostupné a technicky realizovať vyšetrenie na zahraničnom pracovisku je náročné. V krajinách so známym výskytom CLD je nález chloridov v stolici nad 90 mmol/l u detí s charakteristickou anamnézou a klinickým priebehom postačujúci pre diagnostiku CLD, ale v geografických oblastiach so sporadickými prípadmi sa odporúča molekulovo‑genetické vyšetrenie (19). Aj u našich probandov sme na definitívne potvrdenie ochorenia indikovali DNA analýzu.
Záver
V článku opisujeme kazuistiky prvých 2 slovenských pacientov s geneticky potvrdenou kongenitálnou chloridovou hnačkou. U staršieho súrodenca sme identifikovali novú doteraz neopísanú mutáciu SCL26A3 génu. Klinické podozrenie vzbudzujú profúzne vodnaté hnačky manifestujúce sa vo včasnom neonatálnom období, dehydratácia s hypochlorémiou a metabolickou alkalózou. Dôležitý podporný anamnestický údaj je polyhydramnion a prenatálna dilatácia črevných kľučiek. Diagnózu podporí vysoká fekálna koncentrácia chloridov a definitívne potvrdí mutačná analýza SCL26A3 génu. Pri kontinuálnej substitúcii NaCl a KCl je dlhodobá prognóza ochorenia priaznivá.
KORESPONDENČNÍ ADRESA AUTORA:
prof. MUDr. Ľudmila Podracká, CSc.,
Detská klinika LF UK a NÚDCH ,
Limbová 1,
833 40 Bratislava,
Slovenská republika
Cit. zkr: Vnitř Lék 2020; 66(3): 186–189
Článek přijat redakcí: 23. 9. 2018
Článek přijat k publikaci: 20. 12. 2018
Sources
1. Darrow DC Congenital alkalosis with diarrhoea. J Pediatr 1945; 426 : 519–532.
2. Gamble JL, Fahey KR, Appleton J et al. Congenital alkalosis with diarrhoea. J Pediatr 1945; 26 : 509–518.
3. Perheentupa J, Eklund J, Kojo N Familial chloride diarrhoea („congenital alkalosis with diarrhoea“). Acta Paediatr Scand 1965; 159: (Suppl.): 119–120.
4. Launiala K, Perheentupa J, Pasternack A et al. Familial chloride diarrhea-chloride malabsorption. Bibl Paediatr 1968; 87 : 137–149.
5. Li WC, Shih HH, Wu KL et al. Congenital chloride diarrhea in a child. J Formos Med Assoc 2003; 102 : 424–428.
6. Wedenoja S, Ormälä T, Berg UB et al. The impact of sodium chloride and volume depletion in the chronic kidney disease of congenital chloride diarrhea. Kidney Int. 2008; 74 : 1085–1093.
7. Höglund P, Auranen M, Socha J et al. Genetic background of congenital chloride diarrhea in high‑incidence populations: Finland, Poland, and Saudi Arabia and Kuwait. Am J Hum Genet 1998; 63 : 760–768.
8. Höglund P, Haila S, Socha J et al. Mutations of the down‑regulated in adenoma (DRA) gene cause congenital chloride diarrhoea. Nat Genet 1996; 14 : 316–319.
9. Moseley RH, Höglund P, Wu GD et al. Downregulated in adenoma gene encodes a chloride transporter defective in congenital chloride diarrhea. Am J Physiol 1999; 276: G 185–G192.
10. Schweinfest CW, Spyropoulos DD, Henderson KW et al. slc26a3(dra)-deficient mice display chloride‑losing diarrhea, enhanced colonic proliferation, and distinct up‑regulation of ion transporters in the colon. J Biol Chem 2006; 281 : 37962–37971.
11. Wedenoja S, Pekansaari E, Höglund P et al. Update on SLC26A3 mutations in congenital chloride diarrhea. Hum Mutat 2011; 32 : 715–722.
12. Höglund P, Holmberg C, Sherman P et al. Distinct outcomes of chloride diarrhoea in two siblings with identical genetic back‑ground of the disease: implications for early diagnosis and treatment. Gut 2001; 48 : 724–727.
13. Hong J, Seo JK, Ko JS et al. Congenital chloride diarrhea in Korean children: novel mutations and genetic characteristics. Eur J Pediatr 2013; 172 : 545–550.
14. Turnberg LA. Abnormalities in intestinal electrolyte transport in congenital chloridorrhoea. Gut 1971; 12 : 544–551
15. Hayashi H, Suruga K, Yamashita Y Regulation of intestinal Cl-/HCO3-exchanger SLC26A3 by intracellular pH. Am J Physiol Cell Physiol 2009; 296: C1279–C1290.
16. Holmberg C, Perheentupa J, Launiala K et al. Congenital chloride diarrhoea. Clinical analysis of 21 Finnish patients. Arch Dis Child 1977; 52 : 255–267.
17. Hihnala S, Kujala M, Toppari J et al. Expression of SLC26A3, CFTR and NHE3 in the human male reproductive tract: role in male subfertility caused by congenital chloride diarrhoea. Mol Hum Reprod 2006; 12 : 107–111.
18. Wedenoja S, Höglund P, Holmberg C Review article: the clinical management of congenital chloride diarrhoea. Aliment Pharmacol Ther 2010; 31 : 47–485.
19. Gils C, Eckhardt MC, Nielsen PE et al. Congenital chloride diarrhea: Diagnosis by easy accessible chloride measurement in feces. Case reports in Pediatrics 2016; 2519498 : 3 pages. http://dx.doi.org/10.1155/2016/2519498.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2020 Issue 3-
All articles in this issue
- „All‑in‑one“ koncept funkčně vedené revaskularizace myokardu v katetrizační laboratoři
- Prodlužování agresivní antitrombotické léčby po infarktu myokardu: proč, komu a jakou léčbu vybrat?
- Jsou inhibitory protonové pumpy účinným a bezpečným lékem nejen v profylaxi gastrointestinálního krvácení při antitrombotické léčbě?
- Psychické reakce nemocných na negativní informaci typu: „Máte maligní nemocnění“
- Čo sa skrýva za autoinflamáciou?
- Postižení srdce při hypereozinofilii
- Význam dechových testů k hodnocení jaterních funkcí u pacientů s chronickým onemocněním ledvin
- Adherence k principům kardiovaskulární prevence u osob s vysokým rizikem
- Prvé prípady geneticky potvrdenej kongenitálnej hnačky so stratou chloridov na Slovensku
- Stresová kardiomyopatia vyprovokovaná netypickou situáciou
- Hepatorenální syndrom – update 2020
- Lokální trombolýza v léčbě pacientů s hlubokou žilní trombózou: proč, komu a jak?
- Jaké jsou cílové hodnoty krevního tlaku u pacientů s chronickým onemocněním ledvin?
- Proteinurie z pohledu internisty
- Proteinurie z pohledu internisty
- Euvascor – časná intervence u hypertonika s dyslipidemií, resp. dyslipidemika s hypertenzí (fixní kombinace atorvastatinu a perindoprilu)
- Rivaroxaban ve studii COMPASS
- Arteriální hypertenze a infekce COVID-19: Stručný komentář
- Vnitřní lékařství v době koronavirové
- Vážení a milí čtenáři Vnitřního lékařství,
- Miroslav Souček, Petr Svačina a kolektiv. Vnitřní lékařství v kostce. Grada; Praha 2019; 462 stran; ISBN 978-80-271-2289-9 (print)
- Profesorka MUDr. Sylvie Opatrná, PhD. – in memoriam (1959–2020)
- Distanční léčba diabetu: Co mohou pacient, lékař a sestra zvládnout na dálku?
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Čo sa skrýva za autoinflamáciou?
- Lokální trombolýza v léčbě pacientů s hlubokou žilní trombózou: proč, komu a jak?
- Proteinurie z pohledu internisty
- Hepatorenální syndrom – update 2020
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

