-
Medical journals
- Career
„All‑in‑one“ koncept funkčně vedené revaskularizace myokardu v katetrizační laboratoři
Authors: Tomáš Kovárník 1; Petr Kala 2
Authors‘ workplace: II. interní klinika – kardiologie a angiologie, Všeobecná fakultní nemocnice a 1. LF Univerzity Karlovy, Praha 1; Fakultní nemocnice Brno a LF Masarykovy univerzity, Brno 2
Published in: Vnitř Lék 2020; 66(3): 152-159
Category: Main Topic
Overview
Revaskularizace myokardu na základě prokázané ischemie, tzn. koncept funkčně vedené revaskularizace, má v současných guidelines Evropské a České kardiologické společnosti velmi silné doporučení. Jeho přísnou aplikací je u pacientů s chronickými formami ICHS, ale, s určitými omezeními, i s akutním koronárním syndromem možné snížit počet koronárních intervencí při zachované klinické efektivitě. V invazivní kardiologii se dlouhodobě využívá měření tlakových gradientů vytvořených koronární stenózou/koronárním postižením, které dobře korelují s koronárním průtokem. Hodnoty jsou získávány v průběhu maximální hyperemie (FFR – frakční průtoková rezerva) nebo v klidu (např. iFR – instantaneous wave free ratio). Hodnoty FFRmyo ≤ 0,80 nebo iFR ≤ 0,89 značí funkčně významné koronární postižení, kdy revaskularizace je obecně indikována. V neinvazivní kardiologii se pak ke stanovení funkční významnosti koronárního postižení využívají zobrazovací zátěžové metody: perfuzní scintigrafie, magnetická rezonance či pozitronová emisní tomografie a také 3D koronární rekonstrukce z počítačové tomografie (FFRCT) nebo koronární angiografie (QFR – quantitative flow ratio). Oproti angiograficky vedené revaskularizaci a údajem o její kompletnosti se v praxi budeme stále častěji setkávat s klinicky příhodnějším termínem „funkčně kompletní revaskularizace“ a konceptem all‑in‑one v katetrizační laboratoři.
Klíčová slova:
funkční revaskularizace myokardu – ischemie – FFR – iFR – revaskularizace – koronární stenóza – katetrizace – hemodynamicky významný
Úvod
Zavedení konceptu funkčně vedené revaskularizace do stávající běžné praxe (1, 2) předcházel intenzivní výzkum na poli koronární cirkulace a často nacházeném nepoměru mezi angiografickým (anatomickým či morfologickým) posouzením koronárního postižení a funkční významností koronárních lézí (3). Vzhledem k patofyziologii koronární aterosklerózy se funkční posouzení začalo studovat nejdříve u pacientů s chronickými formami ischemické choroby srdce (ICHS). S větším časovým odstupem byla pozornost upřena i na pacienty s akutním koronárním syndromem (AKS) a nestabilním koronárním plátem, a to především při posuzování neinfarktových tepen/lézí. Do určité míry je přínosné i funkční hodnocení intervenované tepny po PCI, tzn. výsledné FFR nebo iFR (4–6).
K detekci ischemie myokardu je možné využít neinvazivní metody, v katetrizační laboratoři se však etablovalo posouzení invazivní, založené na měření tlakových gradientů tvořených koronárním postižením.
Mezi neinvazivní testy patří především zobrazovací metody (zátě ‑ žová scintigrafie myokardu – SPECT, zátěžová echokardiografie, magnetická rezonance srdce – CMR, pozitronová emisní tomografie – PET a nověji pak i matematické modely založené na 3D rekonstrukcích koronárních tepen – frakční průtoková rezerva získaná z počítačové tomografie – FFRCT a kvantitativní poměr průtoků – QFR z koronární angiografie). Od detekce ischemie pomocí zátěžového EKG se vzhledem k jeho relativně nízké senzitivitě a specificitě, která je ještě nižší u žen, spíše upouští. Tato jednoduchá metoda má však své praktické uplatnění při stanovení funkční kapacity a tolerance zátěže (2).
Invazivní posouzení funkční významnosti koronárního postižení je zaměřeno nejčastěji na konkrétní tepnu/tepny většinou s diametrem 2 a více mm a jednotlivé či tandemové léze, méně často se invazivně posuzuje mikrocirkulace či jejich kombinace. Nejdéle známým indexem je tzv. hyperemický index, frakční průtoková rezerva myokardu (FFR či FFRmyo), ke kterému se v doporučení vyrovnal index klidový, iFR (instantaneous wave‑free ratio) (2).
Posouzení globální koronární cirkulace zatím zůstává předmětem výzkumu (7).
Toto sdělení je zaměřeno na invazivní metody pro diagnostiku ischemie myokardu a jejich využití k indikaci a vedení koronárních intervencí – tzv. ALL‑IN‑ONE koncept. Pojmy „hemodynamicky“ a „funkčně“ významná stenóza se významově neliší a v textu jsou využity oba termíny.
Rozsah ischemie myokardu a prognóza
Větší rozsah ischemie myokardu nad 10 % negativně ovlivňuje prognózu a vyžaduje naši plnou pozornost. V praxi však přesné stanovení masy ischemického myokardu při zátěži není jednoduché a modely posouzení závisí na použitých diagnostických metodách (2).
Poslední evropská doporučení pro revaskularizaci myokardu z roku 2018 stanovují níže uvedená kritéria pro revaskularizaci, která u pacientů s chronickou ICHS nebo novějším termínem chronickými koronárními syndromy (CHKS) (2) zlepšují prognózu. V ostatních případech se jedná o revaskularizaci zlepšující symptomy.
„Prognostická revaskularizace“ (2)
- hemodynamicky významná stenóza kmene levé věnčité tepny,
- hemodynamicky významná stenóza proximální části ramus interventricularis anterior (RIA),
- hemodynamicky významná stenóza dvou nebo tří tepen v kombinaci se sníženou systolickou funkcí levé komory srdeční (ejekční frakce < 35 %),
- ischemie myokardu s rozsahem větším než 10 %, nebo abnormální nález při FFR
Hemodynamická významnost stenóz je definována hodnotou FFR ≤ 0,8, nebo iFR ≤ 0,89, nebo se jedná o stenózu > 90 % při angiografickém hodnocení. Stabilní pacienti naplňující minimálně jedno zmíněné kritérium tak mají významně horší prognózu v případě, že jsou léčeni konzervativně, tzn. optimálně vedenou a individualizovanou farmakoterapií (OMT) (8, 9). Naopak zlepšení prognózy je u nich spojené s revaskularizací, jejíž cílem je dosažení revaskularizace kompletní. Na rozdíl od revaskularizace vedené angiograficky se však stále více uplatňuje termín funkčně kompletní revaskularizace vycházející z výše uvedených rozdílů mezi anatomickou a funkční významností koronárního postižení.
Existují však i studie, kde tento vztah nebyl prokázán. Například ve studii STITCH (srovnávající chirurgickou či konzervativní terapii u pacientů s dysfunkcí levé komory srdeční definovanou jako ejekční frakce < 35 %) byla provedena podstudie zahrnující pacienty s prokázanou ischemií myokardu (pomocí SPECT, či dobutaminové echokardiografie). U celkem 399 pacientů nebyl prokázán rozdíl v prognóze nemocných léčených chirurgicky nebo konzervativně ve vztahu k ischemii myokardu (10).
V kardiologické obci hodně diskutovanou byla studie COURAGE porovnávající klinické výsledky koronární intervence (PCI) a konzervativní léčby, a především pak její zátěžová podstudie u pacientů, u kterých byl před a po revaskularizaci proveden SPECT myokardu. Jednalo se o nerandomizované srovnání s menším počtem 314 pacientů, z nichž pouze 1/3 měla rozsah ischemie větší než 10 %. Studie prokázala, že PCI vede k častější redukci ischemie myokardu alespoň o 5 %, které poukázalo na možnou hranici pro redukci mortality a výskytu infarktu myokardu (IM). V multivariační analýze, stejně jako v další analýze studie, však tento výsledek nebyl potvrzen (9). Podobně nebyl potvrzen ani v analýze následné, kde prediktorem výskytu úmrtí a IM byl rozsah koronárního postižení posouzený kvantitativně, který nicméně koreloval s rozsahem ischemie (11).
Dosud největší studií, kterou si zde dovolíme uvést, ačkoliv zatím nebyla publikována, byla randomizovaná studie ISCHEMIA prezentovaná v loňském roce (12). Tato multicentrická mezinárodní studie s poměrně komplikovaným designem byla zaměřena na posouzení vlivu revaskularizace (PCI nebo bypassová operace – CABG) u pacientů s prokázanou ischemií myokardu. Do studie bylo zařazeno 5179 pacientů se stabilní anginou pectoris, s ejekční frakcí > 35 % a s prokázanou ischemií myokardu pomocí SPECT, zátěžovou echokardiografií, CMR nebo bicyklovou ergometrií. U 50 % pacientů byla ischemie hodnocena jako těžká, střední u 33 % a lehká či žádná u 12 %. Vylučovacími kritérii byla stenóza kmene > 50 % na CT koronarografii, akutní koronární syndrom, PCI nebo CABG v předchozím roce. Pacienti byli randomizováni buď k invazivní strategii s event. následnou revaskularizací v kombinaci s OMT, nebo k OMT bez angiografie. Dominantním typem revaskularizace byla PCI s lékovými stenty (74 %, resp. 98 %) a CABG u 26 % (v 92 % byl použit arteriální štěp na RIA). Na základě CT koronarografie, která byla provedena u 73 % pacientů a výsledky byly řešitelům zaslepeny, byli ze studie vyřazeni pacienti se stenózou kmene levé věnčité tepny, nebo s nálezem „podobně významným“. Průměrná doba sledování pacientů byla 3,3 roky (2,2–4,4 roky). V invazivní skupině podstoupilo koronární revaskularizaci 80 % pacientů (tzn. že 20 % pacientů v této větvi bylo léčeno konzervativně), a naopak ve skupině konzervativní léčby bylo 25 % nemocných revaskularizováno. Pro pomalý nábor pacientů byla kritéria pro zařazení do studie snižována z rozsahu ischemie myokardu 10 % na 5 % a na EKG změny během zátěžového testu bez verifikace zobrazovací metodou. Primární kombinovaný cíl ve studii byl kombinovaný: kardiovaskulární mortalita, nebo IM, který byl koncem studie rozšířen o hospitalizaci pro srdeční selhání, hospitalizaci pro nestabilní anginu a resuscitaci pro srdeční zástavu. Výskyt primárního cíle se významně nelišil (Hazard ratio – HR 0,93). Z jednotlivých sledovaných parametrů byl zjištěn rozdíl pouze ve výskytu spontánního infarktu myokardu, který byl signifikantně nižší v intervenční skupině (HR 0,67, p < 0,01) a snížení anginózních obtíží. S napětím jsou očekávány další analýzy studie a z pohledu funkční revaskularizace budou velmi zajímavé výsledky vztahu mezi rozsahem ischemie myokardu a vznikem koronárních příhod či srdečního selhání, přestože nebylo provedeno kontrolní vyšetření rozsahu ischemie myokardu. Vzhledem k rozložení tíže ischemie v souboru pacientů je zřejmé, že revaskularizace u pacientů s CHKS byla z dnešního pohledu nadužívána.
Význam kompletní revaskularizace u pacientů s AKS
Význam kompletní revaskularizace u nemocných s AKS na prognózu pacientů v poslední době dobře zdokumentovala studie COMPLETE (13), ve které kompletní revaskularizace vedla v průběhu 3letého sledování k významnému snížení primárního kombinovaného cíle (kardiovaskulární mortalita a nový infarkt myokardu) i sekundárního kombinovaného cíle (kardiovaskulární mortalita, nový infarkt myokardu a ischemií indikovaná revaskularizace) ve srovnání s intervencí pouze infarktové tepny a s dalšími stenózami řešenými konzervativně (7,8 % vs. 10,5 %; p = 0,004, resp. 8,9 % vs. 16,7 %; p < 0,001). Efekt intervence neinfarktové tepny nebyl závislý na době provedení, které bylo jak v průběhu primárního ošetření AKS, tak odloženě do 45 dnů od primární intervence. Kritériem hemodymamicky významné léze ve studii COMPLETE byla více než 70% stenóza při angiografickém hodnocení, nebo stenóza v rozmezí 50–70 % při FFR ≤ 0,8 (těchto lézí bylo však ve studii méně než 1%). FFR vedená kompletní revaskularizace ve srovnání s intervencí jen infarktové tepny (ovšem se zaslepeným vyšetřením FFR ostatních tepen) vedla ve studii COMPARE ACUTE k signifikantní redukci MACCE (celková mortalita, nefatální IM, revaskularizace, či cerebrovaskulární příhoda). Hlavním rozdílem mezi oběma skupinami byla nutnost revaskularizace a nevýznamné snížení výskytu spontánního IM (1,7 % vs. 2,9 %; p = 0,29). Pozitivní FFR ve skupině pouze s ošetřením infarktové tepny bylo nalezeno u 47,8 % lézí (14).
I ve FFR podstudii DANAMI PRIMULTI byl nižší výskyt kombinovaného primárního cíle (celková mortalita, nefatální IM a revaskularizace indikovaná ischemií) ve skupině s FFR vedenou kompletní revaskularizací ve srovnání s léčbou pouze infarktové tepny. Nižší výskyt nového IM byl sice ještě výraznější než ve studii COMPARE ACUTE, ale opět nedosáhl statistické významnosti (4 % vs. 8 %; HR 0,39; p = 0,28) (15).
Invazivní měření tlakového gradientu na stenóze – FFR a iFR
Přesná technika měření tlaků v aortě a za stenózou je základní podmínkou správného posouzení funkční významnosti koronárního postižení. Fyziologicky je tlak v aortě a v koronární tepně stejný a k jeho poklesu dochází až v arteriolách. Každá tlaková změna v epikardiální části tepen tedy vypovídá o jejich postižení. K výpočtu tlakového gradientu se v koronárních tepnách používá poměr mezi distálním tlakem – Pd (distal pressure, tj. tlak za stenózou) měřeným mikrosenzorem umístěným na intrakoronárním vodiči a aortální tlakem – Pa (aortic pressure) měřeným standardně tlakovým převodníkem využívajícím změnu tlaku vodního sloupce. Index FFR značí poměr Pd/Pa středních tlaků za hyperemie (16) (Obr. 1, 2). V případě klidových indexů, jejichž hlavním reprezentantem je iFR, se využívá fyziologicky nízké a stabilní hodnoty mikrovaskulární rezistence v průběhu střední části diastoly, ve které je provedeno měření Pd/Pa (17) (FFR) (Obr. 3).
Image 1. Princip měření frakční průtokové rezervy (FFR) 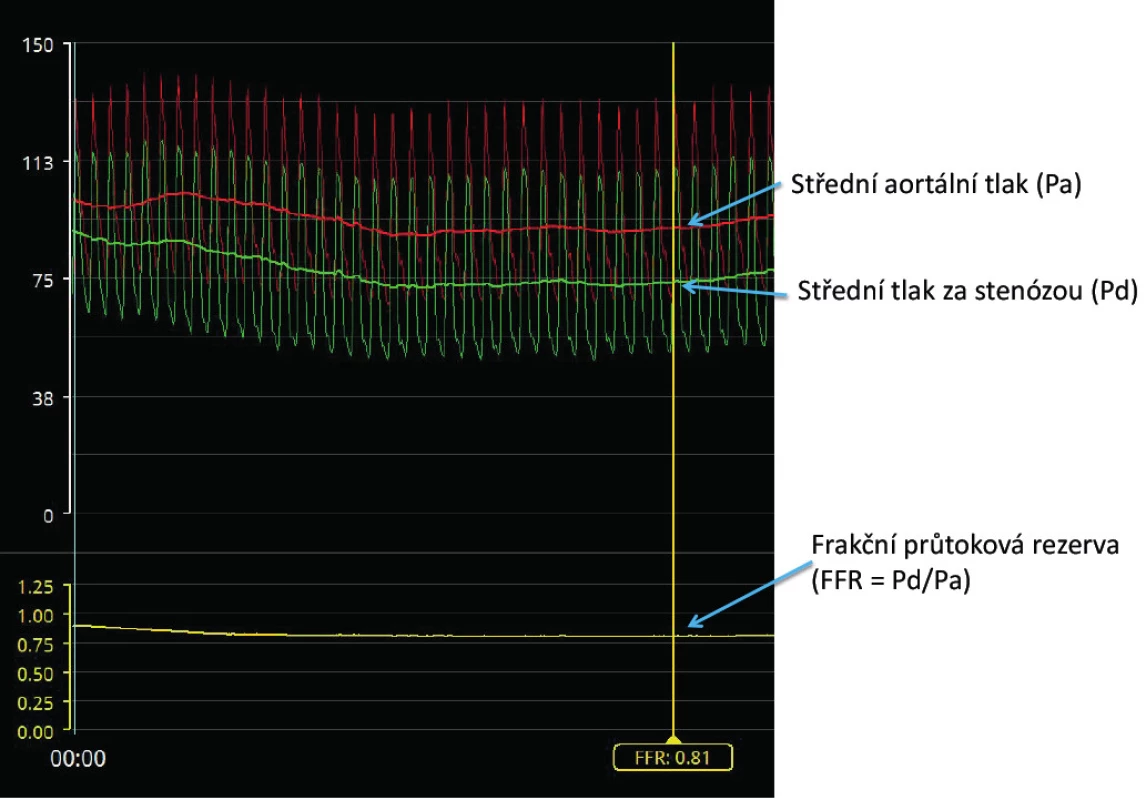
Image 2. FFR měření funkčně nevýznamné stenózy 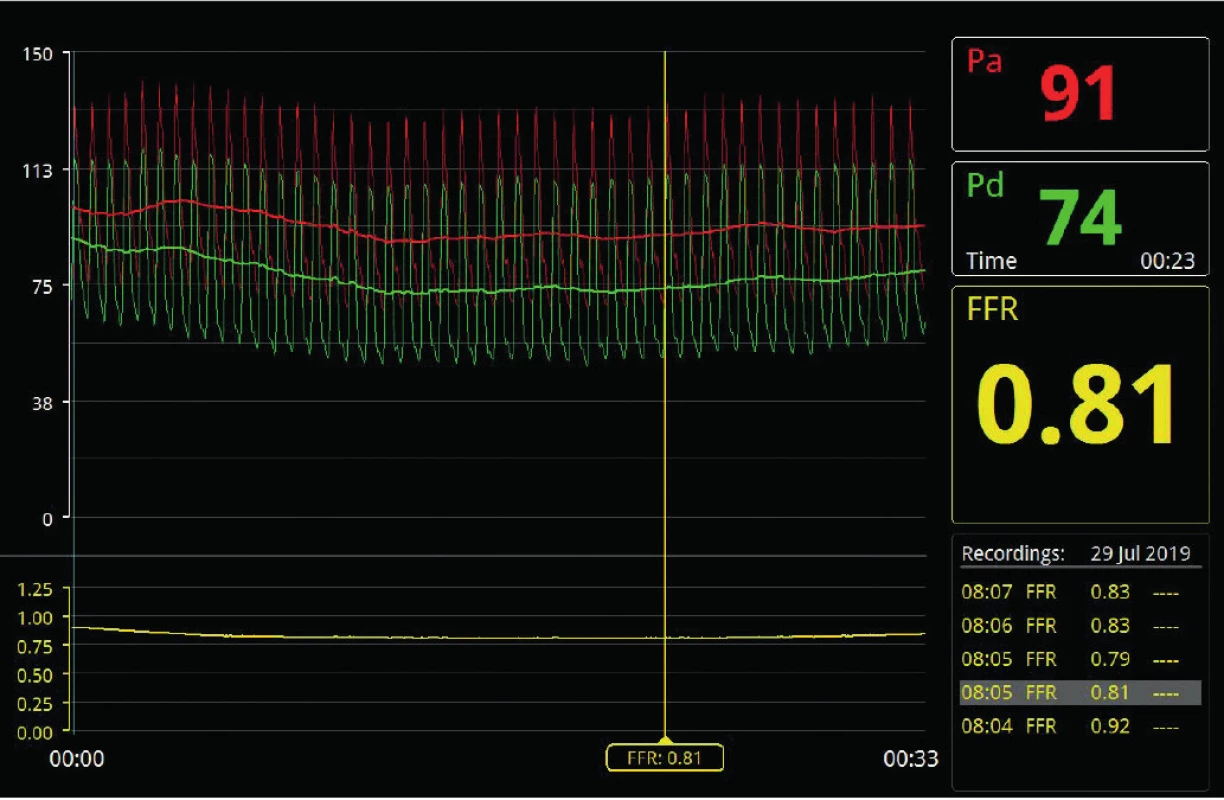
Pozn. Pa – střední aortální tlak; Pd – střední tlak za stenózou, FFR – frakční průtoková rezerva Image 3. iFR měření funkčně nevýznamné stenózy 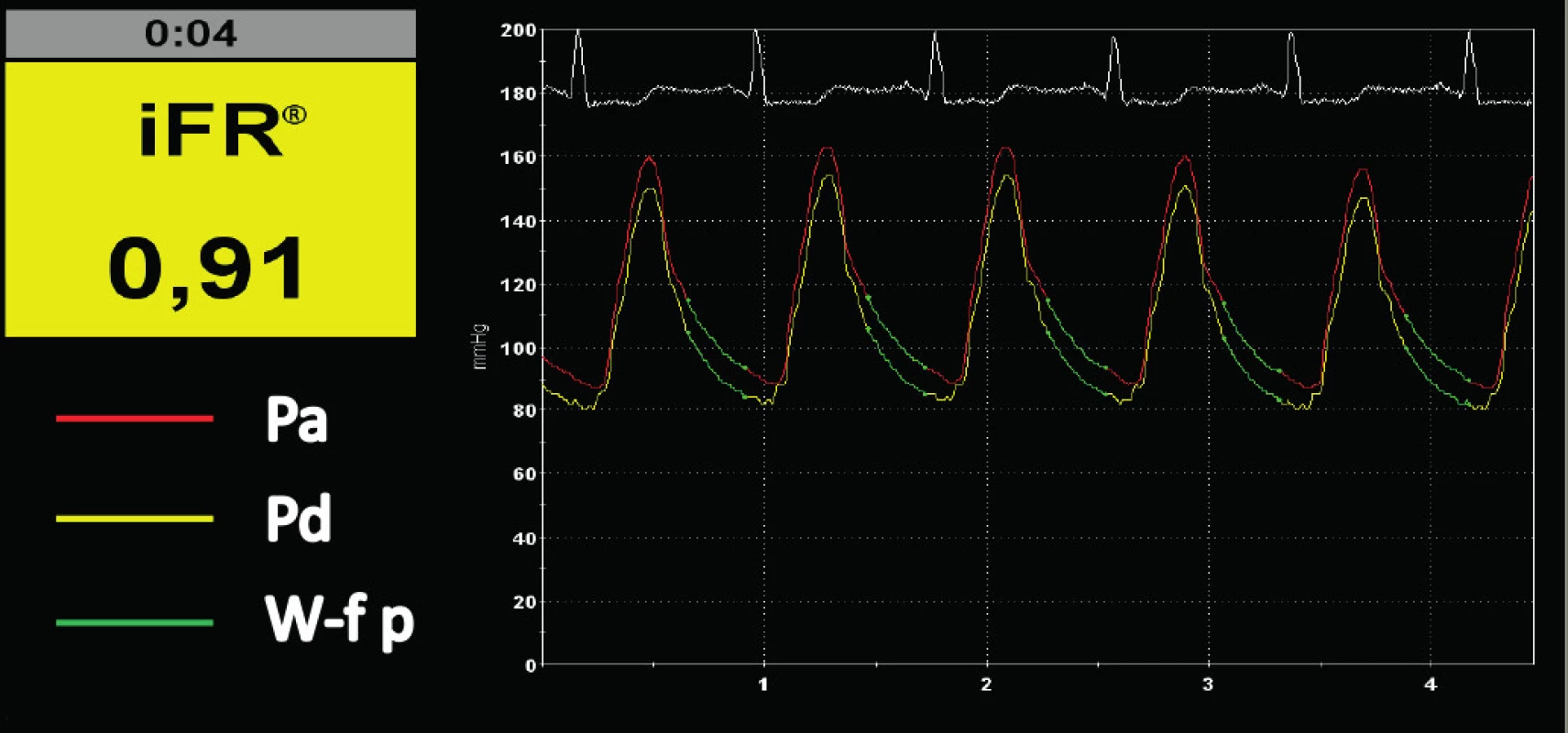
Pozn. Pa – aortální tlak; Pd – tlak za stenózou; W-f p – „Wave-free period“ ve střední části diastoly; iFR – instantaneous wave-free ratio Hodnoty tlakového gradientu, až na výjimky, odpovídají průtoku. Výjimkou tvoří stavy s vysokou mikrovaskulární rezistencí a vysokým tlakem v pravé síni, se kterými se běžně setkáváme u pacientů s akutním infarktem myokardu, resp. rozvinutým srdečním selháním. Obecně se na funkční významnosti podílejí tři faktory: 1) procentuální zúžení lumen, 2) délka stenotického úseku a 3) množství (masa) zásobovaného viabilního myokardu, kdy se se zvyšujícími hodnotami zvyšuje pravděpodobnost funkčně významného postižení. Cíleně je v bodě 3 zdůrazněno množství viabilního myokardu, neboť zcela odlišné nároky na průtok a krevní zásobení vykazuje oblast plně viabilní oproti oblasti s rozsáhlejší jizvou po IM (Obr. 4, 5).
Image 4. Funkčně nevýznamná stenóza pravé věnčité tepny s vyznačenou, angiograficky hraniční stenózou s velkým povodím za stenózou zásobující oblast po rozsáhlém infarktu myokardu dolní stěny v minulosti. 4a – angiografie s vyznačením hraničního postižení; 4b – měření FFR 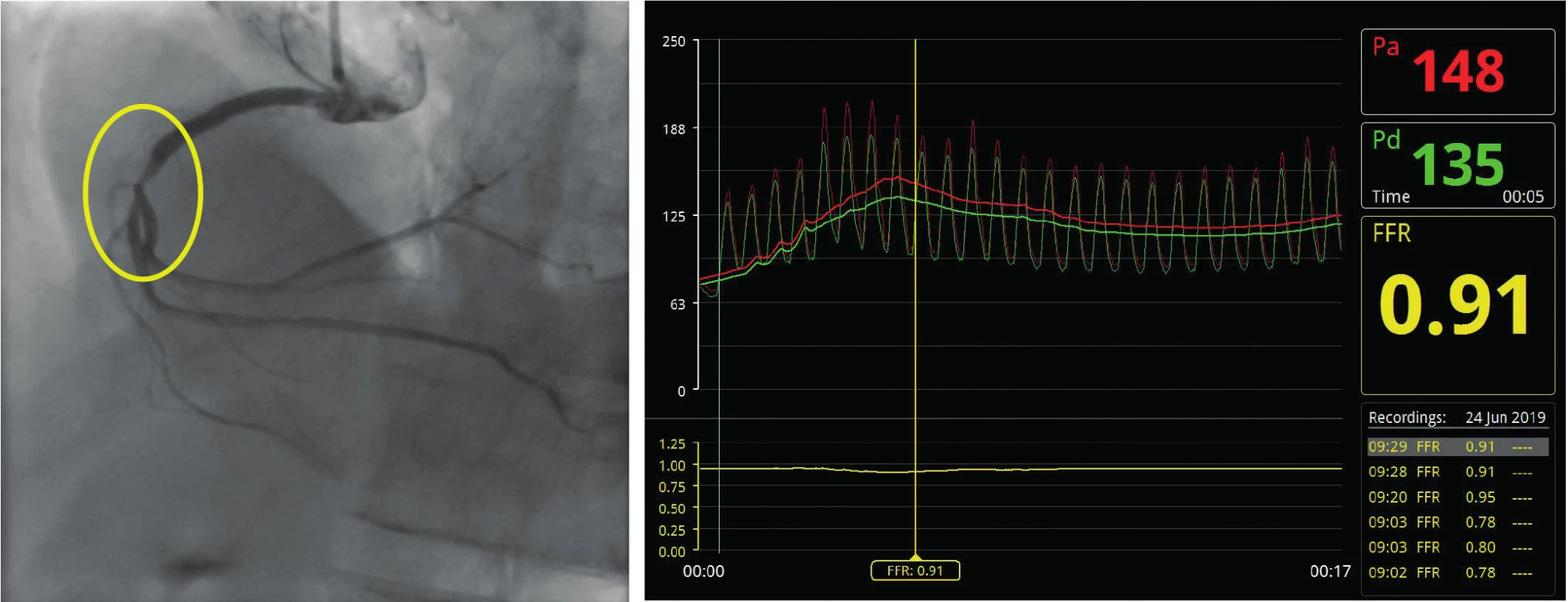
Pozn. Pa – střední aortální tlak; Pd – střední tlak za stenózou, FFR – frakční průtoková rezerva Image 5. Funkčně významná stenóza pravé věnčité tepny s vyznačenou, angiograficky hraniční stenózou a difuzním postižením periferie s velkým povodím za stenózou zásobujícím plně viabilní oblast myokardu. 5a – angiografie s vyznačeným hraničním postižením; 5b – měření FFR 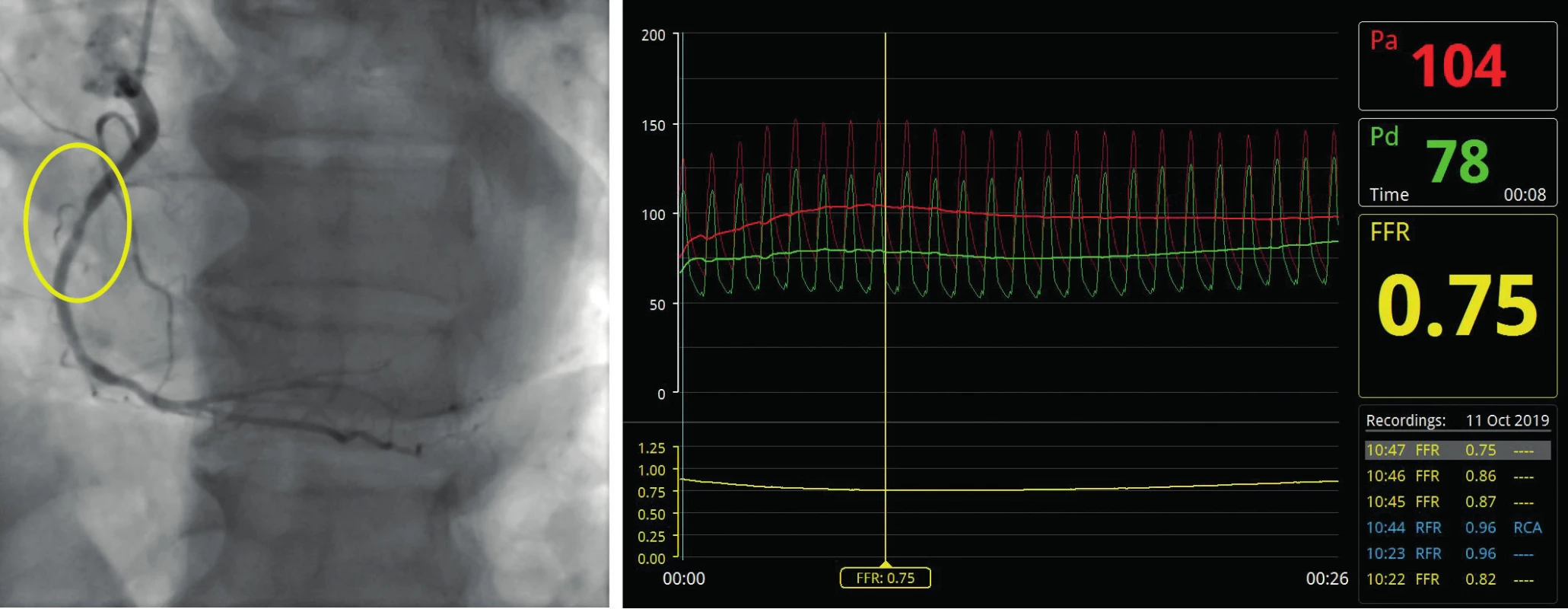
Pozn. Pa – střední aortální tlak; Pd – střední tlak za stenózou, FFR – frakční průtoková rezerva Hodnota FFR ≤ 0,8, nebo iFR ≤ 0,89 značí funkčně významnou stenózu, kde revaskularizace vede k významnému odstranění ischemického myokardu. Při jasně stanovené cut‑off hodnotě je zjevné, že vyšetření musí být provedeno velmi pečlivě a technicky správně. Ačkoliv by se mohlo zdát, že se jedná o jednoduché principy a postupy, koronární cirkulace a koronární fyziologie jsou velmi komplexní problematikou vyžadující nejen správnou indikaci a techniku měření, ale i zkušenost při interpretování výsledků a tvoření závěrů. Příkladů složitějších angiografických nálezů a interpretací je mnoho, pro představu např. tandemové či vícečetné stenózy, přítomnost kolaterál nebo „iatrogenních kolaterál“ (bypassů).
Přibližně ve 20 % měření je také možné se setkat s diskrepancí mezi měřeními FFR a iFR (18, 19). Tyto rozdíly nemají jednoduché vysvětlení a vyžadují od katetrizujících lékařů obezřetnost.
V praxi se ve většině případů posuzují angiograficky hraniční stenózy 40–70 % a záměrně je zde uveden interval s hodnotou od 40 %, neboť v praxi nejsou výjimkou překvapivé situace, kdy již 40% postižení může být funkčně významné (Obr. 6), ale naopak funkčně nevýznamnou může být 70% nebo dokonce i významnější stenóza (Obr. 7). Významnou roli v těchto případech hraje jedna z limitací koronární angiografie, kterou je potřeba zdravého referenčního úseku ke stanovení správné angiografické významnosti vyjádřené v procentech. Tato limitace je poměrně často nalézána u pacientů s déle trvajícím diabetem mellitem, kde koronární ateroskleróza bývá nezřídka difuzní (Obr. 8). Především u tepen zásobujících velkou oblast myokardu, většinou kmene levé věnčité tepny a RIA, není funkční podhodnocení výjimkou a naopak se jedná o oblasti, které jsou pro pacienty vitálně důležité (Obr. 9).
Image 6. Funkčně významná stenóza ramus interventricularis anterior s rozsáhlým viabilním povodím s vyznačenou, angiograficky maximálně hraniční (40 %) stenózou. 6a – angiografie; 6b – FFR; 6c – angiografie po implantaci lékového stentu 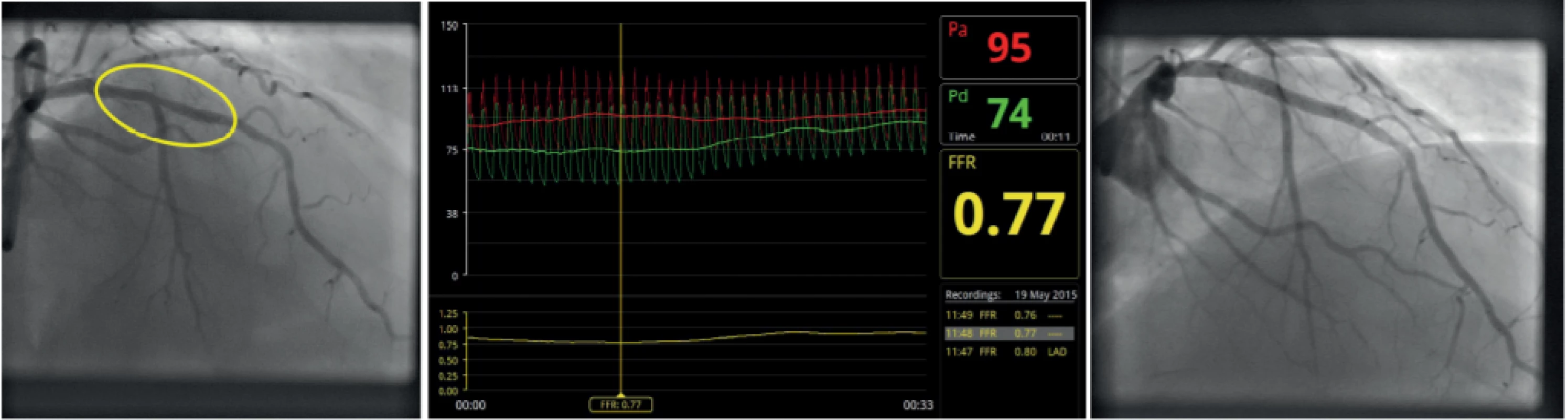
Pozn. Pa – střední aortální tlak; Pd – střední tlak za stenózou, FFR – frakční průtoková rezerva Table 1. Funkčně nevýznamná stenóza ramus marginalis s vyznačenou, angiograficky významnou segmentární stenózou. 7a – angiografie; 7b – FFR 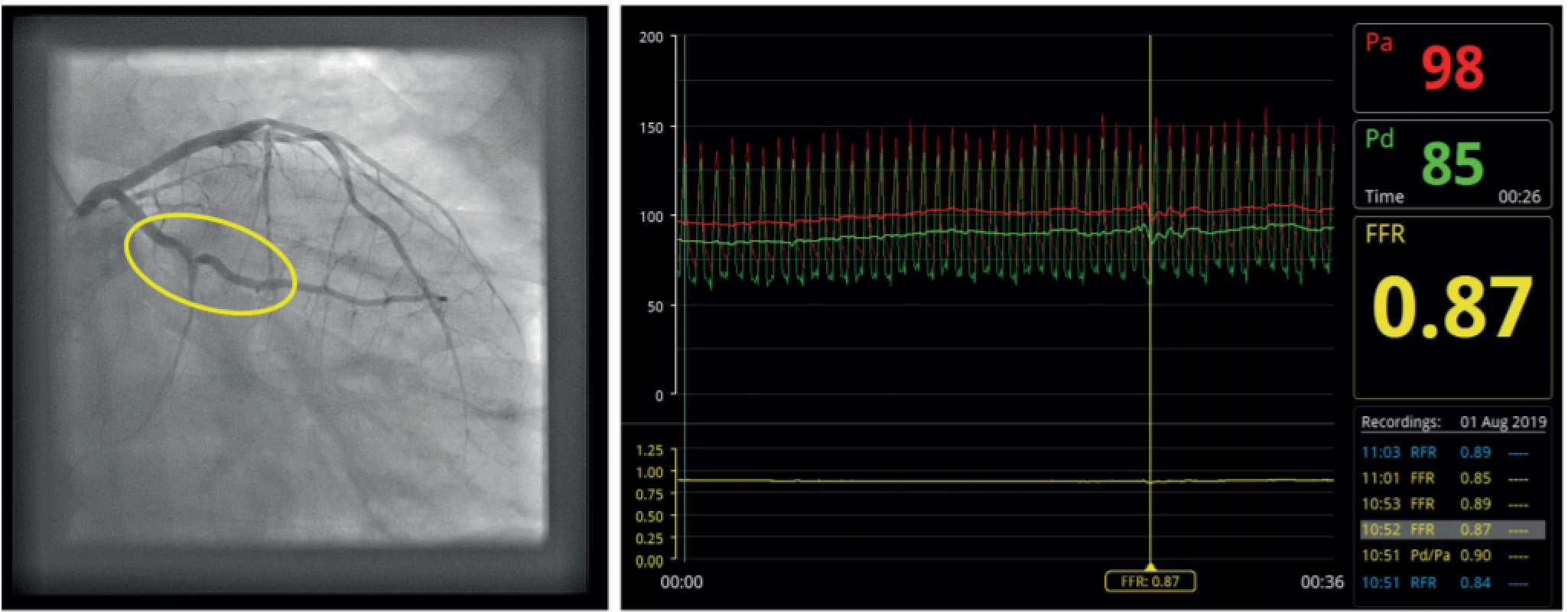
Pozn. Pa – střední aortální tlak; Pd – střední tlak za stenózou, FFR – frakční průtoková rezerva Image 7. Difuzní postižení ramus interventricularis anterior na hranici funkční významnosti. 8a – angiografie; 8F – FFR; 8c – intrakoronární optická koherentní tomografie s podélným obrazem a vybranými příčnými řezy 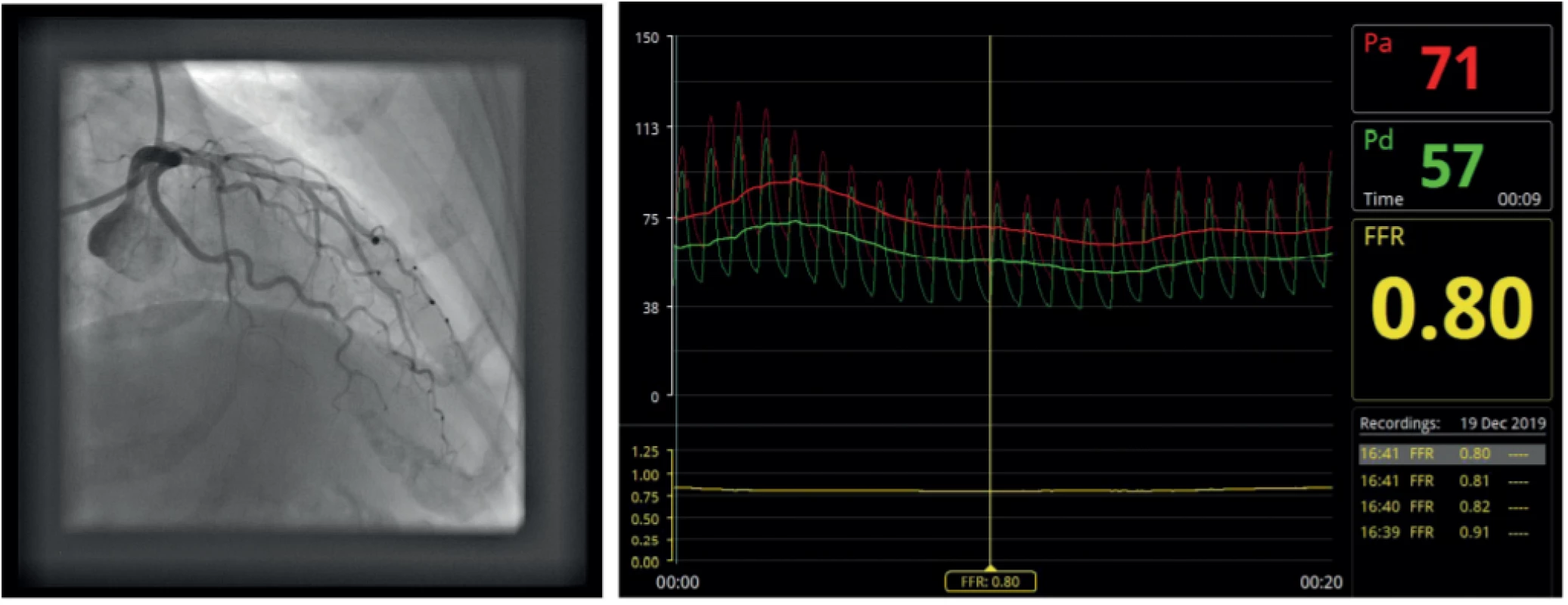
Pozn. Pa – střední aortální tlak; Pd – střední tlak za stenózou, FFR – frakční průtoková rezerva Obr. 8c. Funkčně významné postižení kmene levé věnčité tepny s vyznačenou, angiograficky maximálně hraničním postižením 40%. 8a – angiografie; 8b – FFR; 8c – optická koherentní tomografie se simultánním zobrazením angiografie v podélném a příčném řezu (znázorněná plocha lumen 4,4 mm2 značí funkčně významné postižení) 
Pozn. Pa – střední aortální tlak; Pd – střední tlak za stenózou, FFR – frakční průtoková rezerva Image 8. Měření koronární průtokové rezervy myokardu dopplerovskou metodou 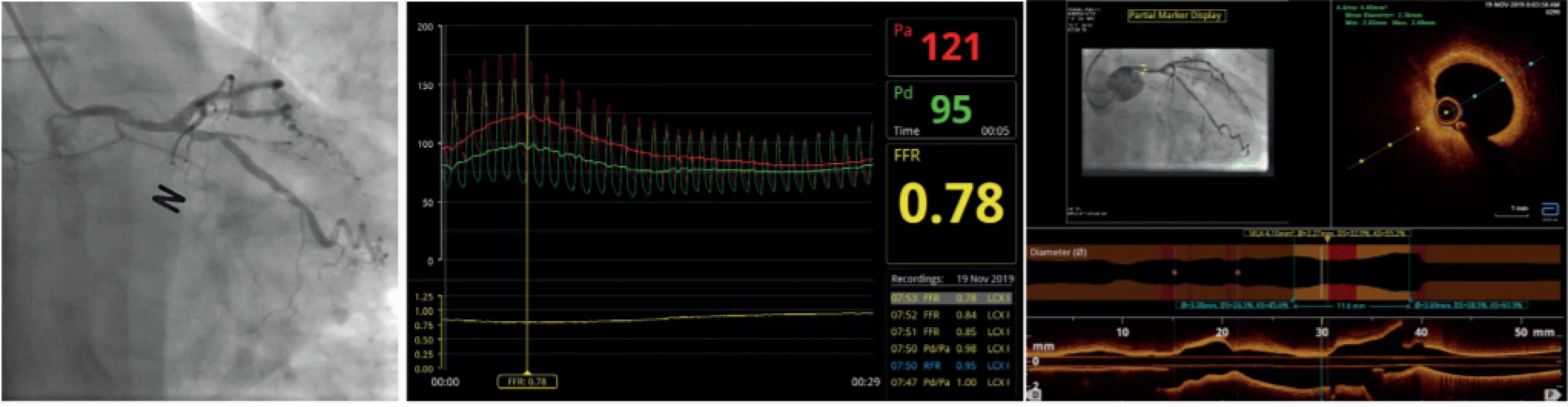
V případě hyperemických indexů se k minimalizaci intramyokardiální rezistence intrakoronárně či intravenózně aplikují silná vazodilatancia (adenozin, papaverin, regadenoson). V kombinaci s intrakoronárním podáním nitrátu působícím na epikardiální části tepen je možné dosáhnout maximální hyperemie, která je při intrakoronárním podání krátkodobá a v případě intravenózní aplikace trvá po dobu infuze a umožňuje provedení vyšetření delšího úseku tepny pomocí vytahování (tzv. pullback) vodiče směrem od periferie tepny k ostiu s kontinuálním záznamem tlaků.
Na základě provedených studií, které prokázaly stejné dlouhodobé výsledky při indikaci ke koronární revaskularizaci, mají nyní jak FFR tak iFR stejné doporučení pro indikaci provedení PCI, a to nejvyšší, tedy IA (1).
Vedle těchto doporučených indexů se využívá celá řada dalších klidových indexů, se kterými je možné se setkat v popisech z katetrizační laboratoře, jako jsou DPR (diastolic pressure ratio) a jeho varianta dPR, RFR (resting full cycle ratio), DFR (diastolic hyperemia free ratio). Cut‑off hodnota je pro všechny klidové indexy stejná, tzn. 0,89 (20).
Měření intrakoronárního průtoku – CFR
Na rozdíl od relativně jednoduchého měření intrakoronárních tlaků je měření koronární průtoku technicky složitější a tedy i méně často využívané. Zároveň se však jedná o cíl našeho hodnocení vypovídající o společné funkční významnosti epikardiálního a intramyokardiálního postižení. K nepřímému hodnocení průtoku se využívá metoda dopplerovská nebo přímé měření krevního průtoku termodilucí. V obou případech se k měření využívají speciální intrakoronární vodiče – s piezoelektrickým krystalem (Obr. 10), resp. s termistorem (Obr. 11).
Image 9. Měření patologické koronární průtokové rezervy myokardu (cut-off ≤ 2) termodiluční technikou 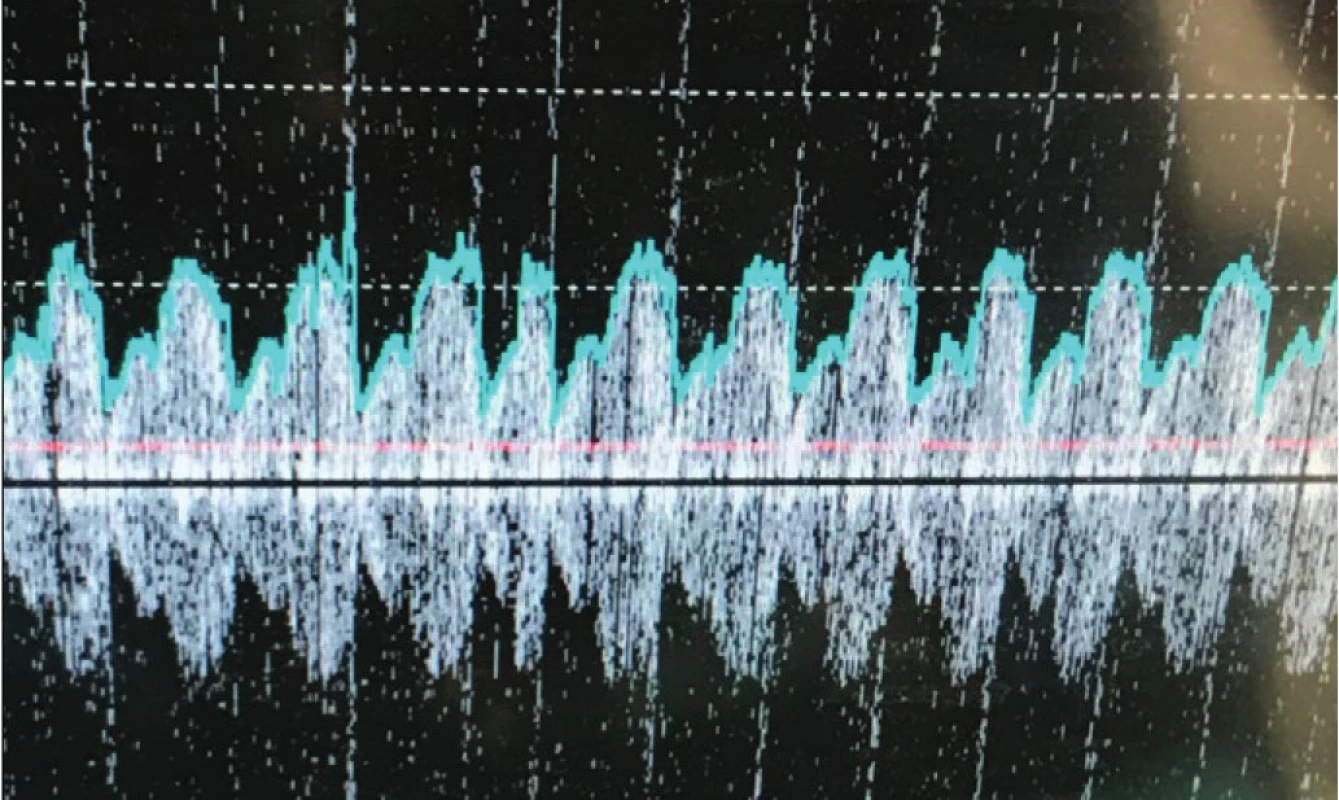
Pozn. Pa – střední aortální tlak; Pd – střední tlak za stenózou, CFR – koronární průtoková rezerva; FFR – frakční průtoková rezerva Image 10. Měření normální koronární průtokové rezervy myokardu (> 2) termodiluční technikou 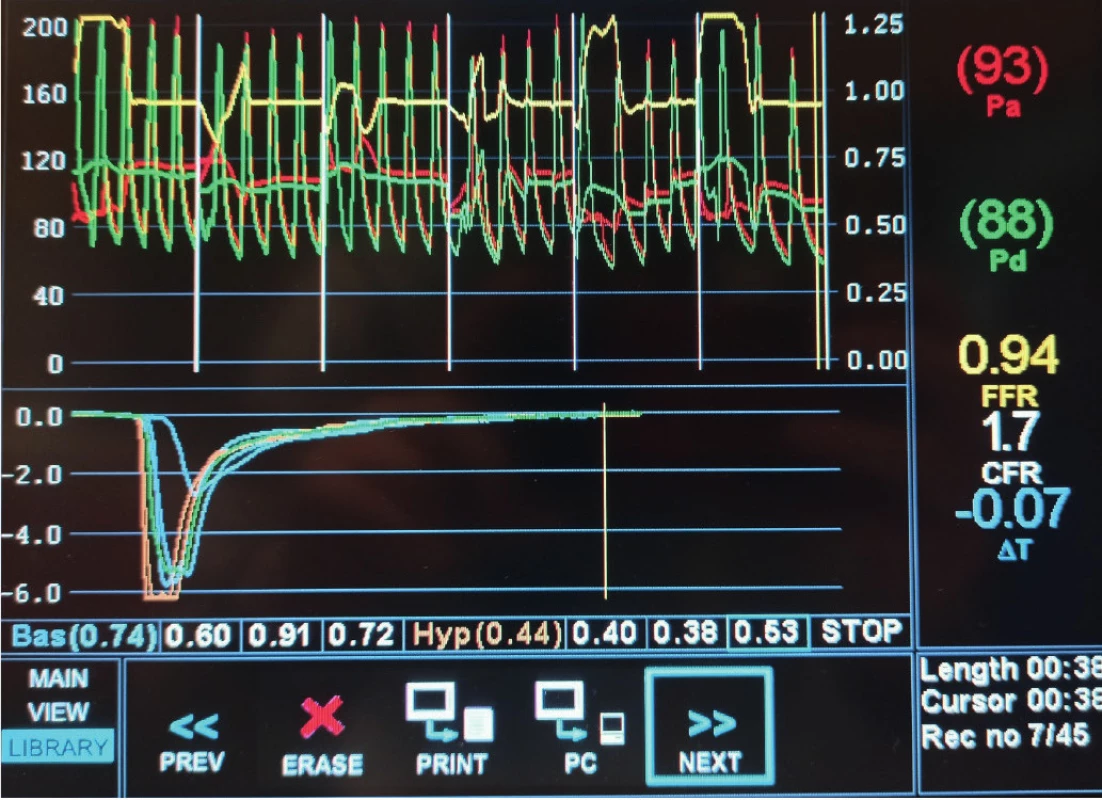
Pozn. Pa – střední aortální tlak; Pd – střední tlak za stenózou, CFR – koronární průtoková rezerva; FFR - frakční průtoková rezerva Obě techniky využíváme k měření koronární průtokové rezervy (CFR – coronary flow reserve), které je dáno poměrem mezi koronárním průtokem při maximální hyperemii a klidovým průtokem. Normální hodnota CFR je ≥ 2, tzn. že krevní průtok koronárním řečištěm se při námaze zvýší minimálně dvakrát (Obr. 12).
Image 11. Patologická hodnota indexu mikrovaskulární rezistence (IMR = 33) vypočítaná z hodnoty Pd a Tmn (Hyp) vyznačenými červeně, resp. žlutě 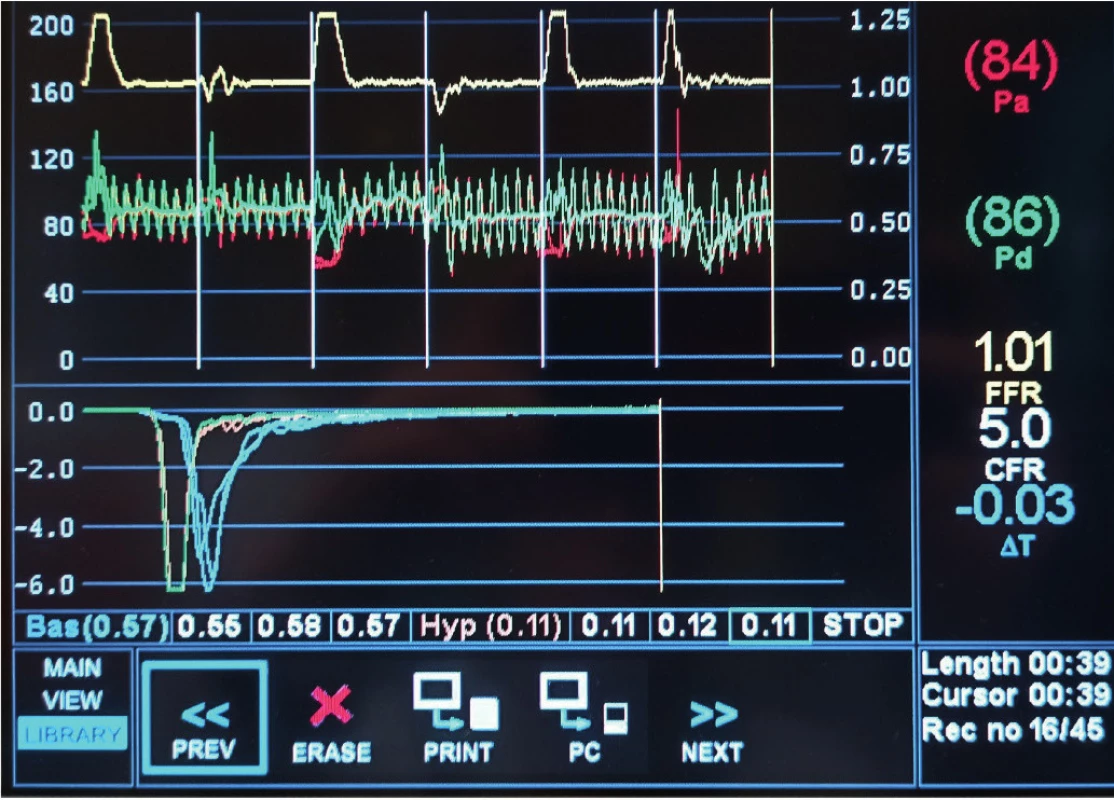
Pozn. Pa – střední aortální tlak; Pd – střední tlak za stenózou, CFR – koronární průtoková rezerva; FFR - frakční průtoková rezerva; Tmn – mean transit time Zjednodušeně se dá říci, že hodnoty FFR a iFR jsou dány zejména závažností epikardiálních stenóz, kdežto hodnota CFR je sumací epikardiální stenózy a postižení mikrocirkulace. V některých případech pak nalézáme rozdíly ve výsledcích jednotlivých indexů (21, 22).
Hodnocení mikrocirkulace – IMR
Výhradní index pro hodnocení mikrovaskulárního řečiště je IMR (index of microvascular resistence). Jeho normální hodnota se pohybuje v rozmezí 7–27 (23, 24) (Obr. 13).
Image 12. Patologická hodnota indexu mikrovaskulární rezistence (IMR = 33) vypočítaná z hodnoty Pd a Tmn (Hyp) vyznačenými červeně, resp. žlutě 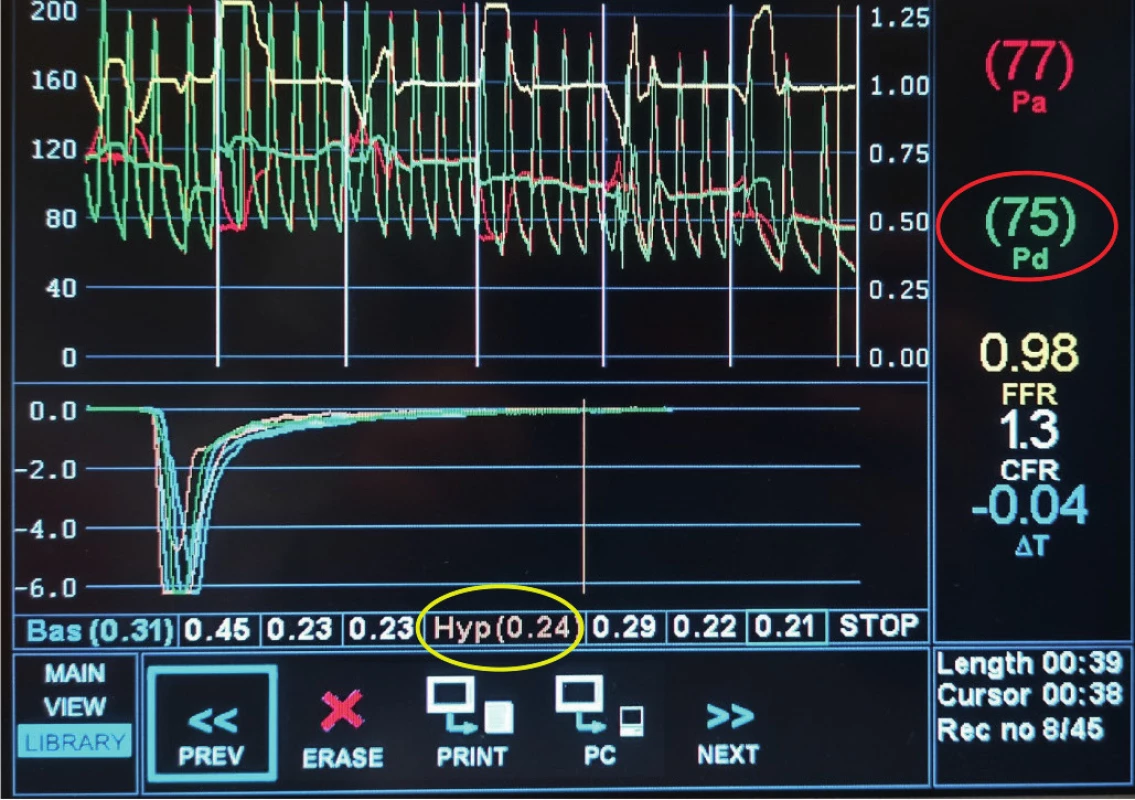
Důvody pro používání funkčně vedené revaskularizace
Pro prognózu pacienta s CHKS je výrazný rozdíl, zda je daná stenóza funkčně významná, tj. zda vede k rozvoji ischemie myokardu, či nikoliv. Vznik tlakového gradientu na stenóze potencuje proces koronární aterosklerózy a zvyšuje riziko vzniku AKS (25, 26). Naopak léze, které nevedou k ovlivnění koronárního průtoku, mají velmi dobrou prognózu a nízké riziko vzniku AKS, jak bylo doloženo v dlouhodobém sledování pacientů ve studii DEFER (27).
Revaskularizace funkčně nevýznamných lézí tedy nevede ke zlepšení prognózy, ale naopak zatěžuje pacienta rizikem periprocedurálních komplikací a komplikací spojených s implantací stentu a kombinované antitrombotické léčby.
U pacientů s AKS je, s výjimkou akutního vyšetření infarktové tepny u pacientů se STEMI, FFR měření možné bezpečně provést a získat přesná data o funkční významnosti (28). Data pro použití iFR u pacientů s AKS pocházejí ze studií DEFINE FLAIR, kde bylo nemocných s AKS 15 % (29, 30).
Studie podporující dosažení funkčně kompletní revaskularizace u pacientů se STEMI jsou zmíněny výše.
Závěr
Funkčně vedená revaskularizace myokardu je doporučeným způsobem léčby ICHS, který se zaměřuje na indikace k revaskularizaci jen těch lézí, které způsobují ischemii myokardu, a vede ke snížení počtu „zbytných“ PCI. Je určena také pro stanovení optimální léčebné strategie pacientů s AKS (především u neinfarktových tepen/lézí) a optimalizaci výsledků PCI. Takto vedená revaskularizace myokardu vede k výraznější redukci ischemie oproti konzervativní léčbě a umožňuje komplexní přístup all‑in‑one v katetrizační laboratoři.
Nedílnou součástí invazivní strategie je však optimálně vedená a individualizovaná farmakologická léčba, důsledná sekundární prevence a zdravý životní styl.
Tato práce byla podpořena grantem Agentury pro zdravotnický výzkum České republiky AZV 16-28525 A a MH CZ – DRO (FNBr, 65269705).
KORESPONDENČNÍ ADRESA AUTORA:
doc. MUDr. Petr Kala, Ph.D., FESC, FSCAI,
Interní kardiologická klinika FN Brno a LF MU,
Jihlavská 20,
625 00 Brno
Cit. zkr: Vnitř Lék 2020; 66(3): 152–159
Článek přijat redakcí: 27. 2. 2020
Článek přijat k publikaci: 12. 3. 2020
Sources
1. Neumann FJ, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur. Heart J. (2018) doi:10.1093/eurheartj/ehy394.
2. Knuuti J, et al. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur. Heart J. 41, 407–477 (2020).
3. Tonino PAL, et al. Angiographic versus functional severity of coronary artery stenoses in the FAME study fractional flow reserve versus angiography in multivessel evaluation. J. Am. Coll. Cardiol. 55, 2816–2821 (2010).
4. Kobayashi Y,. et al. The Prognostic Value of Residual Coronary Stenoses After Functionally Complete Revascularization. J. Am. Coll. Cardiol. 67, 1701–1711 (2016).
5. Pijls, N. H. J. et al. Coronary pressure measurement after stenting predicts adverse events at follow-up: a multicenter registry. Circulation 105, 2950–2954 (2002).
6. Piroth Z, et al. Prognostic Value of Fractional Flow Reserve Measured Immediately After Drug-Eluting Stent Implantation. Circ. Cardiovasc. Interv. 10, (2017).
7. Knott KD, et al. The Prognostic Significance of Quantitative Myocardial Perfusion: An Arti ‑ ficial Intelligence Based Approach Using Perfusion Mapping. Circulation (2020) doi:10.1161/ CIRCULATIONAHA.119.044666.
8. Farzaneh-Far A, et al. Ischemia change in stable coronary artery disease is an independent predictor of death and myocardial infarction. JACC Cardiovasc. Imaging 5, 715–724 (2012).
9. Shaw LJ, et al. Impact of left ventricular function and the extent of ischemia and scar by stress myocardial perfusion imaging on prognosis and therapeutic risk reduction in diabetic patients with coronary artery disease: results from the Bypass Angioplasty Revascularization Investigation 2 Diabetes (BARI 2D) trial. J. Nucl. Cardiol. Off. Publ. Am. Soc. Nucl. Cardiol. 19, 658–669 (2012).
10. Panza JA, et al. Inducible myocardial ischemia and outcomes in patients with coronary artery disease and left ventricular dysfunction. J. Am. Coll. Cardiol. 61, 1860–1870 (2013).
11. Mancini GBJ, et al. Predicting outcome in the COURAGE trial (Clinical Outcomes Utilizing Revascularization and Aggressive Drug Evaluation): coronary anatomy versus ischemia. JACC Cardiovasc. Interv. 7, 195–201 (2014).
12. Hochman J S, et al. Baseline Characteristics and Risk Profiles of Participants in the ISCHEMIA Randomized Clinical Trial. JAMA Cardiol. 4, 273–286 (2019).
13. Mehta SR, et al. Complete Revascularization with Multivessel PCI for Myocardial Infarction. N. Engl. J. Med. 381, 1411–1421 (2019).
14. Smits PC, et al. Fractional Flow Reserve-Guided Multivessel Angioplasty in Myocardial Infarction. N. Engl. J. Med. 376, 1234–1244 (2017).
15. Lønborg J, et al. Fractional Flow Reserve-Guided Complete Revascularization Improves the Prognosis in Patients With ST-Segment-Elevation Myocardial Infarction and Severe Nonculprit Disease: A DANAMI 3-PRIMULTI Substudy (Primary PCI in Patients With ST-Elevation Myocardial Infarction and Multivessel Disease: Treatment of Culprit Lesion Only or Complete Revascularization). Circ. Cardiovasc. Interv. 10, (2017).
16. Pijls N H, et al. Fractional flow reserve. A useful index to evaluate the influence of an epicardial coronary stenosis on myocardial blood flow. Circulation 92, 3183–3193 (1995).
17. Sen S, et al. Development and validation of a new adenosine-independent index of stenosis severity from coronary wave-intensity analysis: results of the ADVISE (ADenosine Vasodilator Independent Stenosis Evaluation) study. J. Am. Coll. Cardiol. 59, 1392–1402 (2012).
18. Lee JM, et al. Discrepancy between fractional flow reserve and instantaneous wave-free ratio: Clinical and angiographic characteristics. Int. J. Cardiol. 245, 63–68 (2017).
19. Berry C, et al. VERIFY (VERification of Instantaneous Wave-Free Ratio and Fractional Flow Reserve for the Assessment of Coronary Artery Stenosis Severity in EverydaY Practice): a multicenter study in consecutive patients. J. Am. Coll. Cardiol. 61, 1421–1427 (2013).
20. Ligthart J, et al. Validation of Resting Diastolic Pressure Ratio Calculated by a Novel Algorithm and Its Correlation With Distal Coronary Artery Pressure to Aortic Pressure, Instantaneous Wave-Free Ratio, and Fractional Flow Reserve. Circ. Cardiovasc. Interv. 11, e006911 (2018).
21. van de Hoef TP, et al. Physiological basis and long-term clinical outcome of discordance between fractional flow reserve and coronary flow velocity reserve in coronary stenoses of intermediate severity. Circ. Cardiovasc. Interv. 7, 301–311 (2014).
22. Petraco R, et al. Baseline instantaneous wave-free ratio as a pressure-only estimation of underlying coronary flow reserve: results of the JUSTIFY-CFR Study (Joined Coronary Pressure and Flow Analysis to Determine Diagnostic Characteristics of Basal and Hyperemic Indices of Functional Lesion Severity-Coronary Flow Reserve). Circ. Cardiovasc. Interv. 7, 492–502 (2014).
23. Fearon W F, et al. Novel index for invasively assessing the coronary microcirculation. Circulation 107, 3129–3132 (2003).
24. Solberg, O. G. et al. Reference interval for the index of coronary microvascular resistance. EuroIntervention J. Eur. Collab. Work. Group Interv. Cardiol. Eur. Soc. Cardiol. 9, 1069–1075 (2014).
25. Xaplanteris P, et al. Coronary lesion progression as assessed by fractional flow reserve (FFR) and angiography. EuroIntervention J. Eur. Collab. Work. Group Interv. Cardiol. Eur. Soc. Cardiol. 14, 907–914 (2018).
26. Ford TJ, et al. Physiological Predictors of Acute Coronary Syndromes: Emerging Insights From the Plaque to the Vulnerable Patient. JACC Cardiovasc. Interv. 10, 2539–2547 (2017).
27. Zimmermann F M, et al. Deferral vs. performance of percutaneous coronary intervention of functionally non-significant coronary stenosis: 15-year follow-up of the DEFER trial. Eur. Heart J. 36, 3182–3188 (2015).
28. Fearon WF, De Bruyne B, Pijls NHJ. Fractional Flow Reserve in Acute Coronary Syndromes. J. Am. Coll. Cardiol. 68, 1192–1194 (2016).
29. Davies J E, et al. Use of the Instantaneous Wave-free Ratio or Fractional Flow Reserve in PCI. N. Engl. J. Med. 376, 1824–1834 (2017).
30. Götberg M, et al. Instantaneous Wave-free Ratio versus Fractional Flow Reserve to Guide PCI. N. Engl. J. Med. 376, 1813–1823 (2017).
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2020 Issue 3-
All articles in this issue
- „All‑in‑one“ koncept funkčně vedené revaskularizace myokardu v katetrizační laboratoři
- Prodlužování agresivní antitrombotické léčby po infarktu myokardu: proč, komu a jakou léčbu vybrat?
- Jsou inhibitory protonové pumpy účinným a bezpečným lékem nejen v profylaxi gastrointestinálního krvácení při antitrombotické léčbě?
- Psychické reakce nemocných na negativní informaci typu: „Máte maligní nemocnění“
- Čo sa skrýva za autoinflamáciou?
- Postižení srdce při hypereozinofilii
- Význam dechových testů k hodnocení jaterních funkcí u pacientů s chronickým onemocněním ledvin
- Adherence k principům kardiovaskulární prevence u osob s vysokým rizikem
- Prvé prípady geneticky potvrdenej kongenitálnej hnačky so stratou chloridov na Slovensku
- Stresová kardiomyopatia vyprovokovaná netypickou situáciou
- Hepatorenální syndrom – update 2020
- Lokální trombolýza v léčbě pacientů s hlubokou žilní trombózou: proč, komu a jak?
- Jaké jsou cílové hodnoty krevního tlaku u pacientů s chronickým onemocněním ledvin?
- Proteinurie z pohledu internisty
- Proteinurie z pohledu internisty
- Euvascor – časná intervence u hypertonika s dyslipidemií, resp. dyslipidemika s hypertenzí (fixní kombinace atorvastatinu a perindoprilu)
- Rivaroxaban ve studii COMPASS
- Arteriální hypertenze a infekce COVID-19: Stručný komentář
- Vnitřní lékařství v době koronavirové
- Vážení a milí čtenáři Vnitřního lékařství,
- Miroslav Souček, Petr Svačina a kolektiv. Vnitřní lékařství v kostce. Grada; Praha 2019; 462 stran; ISBN 978-80-271-2289-9 (print)
- Profesorka MUDr. Sylvie Opatrná, PhD. – in memoriam (1959–2020)
- Distanční léčba diabetu: Co mohou pacient, lékař a sestra zvládnout na dálku?
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Čo sa skrýva za autoinflamáciou?
- Lokální trombolýza v léčbě pacientů s hlubokou žilní trombózou: proč, komu a jak?
- Proteinurie z pohledu internisty
- Hepatorenální syndrom – update 2020
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

