-
Medical journals
- Career
Hepatotoxicita indukovaná bodybuilding suplementami
Authors: Martina Jakabovičová; Zuzana Urkovičová; Tereza Hlavatá; Mária Szántová
Authors‘ workplace: III. interná klinika LF UK a UN, Nemocnica akademika Ladislava Dérera, Bratislava
Published in: Vnitř Lék 2020; 66(1): 28-33
Category:
Overview
Bodybuilding suplementy sú označované ako anabolicko‑androgénne steroidy (AAS) a tiež doplnky stravy s ich prímesou. Bez medicínskej indikácie sú ilegálne, zato ľahko dostupné a zdraviu škodlivé, schopné spôsobiť rozličné formy pečeňového poškodenia od prechodného zvýšenia sérových enzýmov cez akútny cholestatický syndróm až po rozvoj hepatálnych tumorov pri dlhodobom užívaní. Najsilnejšie hepatotoxické účinky sú spájané s alkylovanými formami, hoci tumory boli tiež asociované s nemodifikovaným alebo esterifikovaným testosterónom. Od 80. rokov 20. storočia sú rozšírené nielen v špičkovom športe, ale aj v bežnej populácii. Užívajú sa s cieľom zlepšenia športovej výkonnosti a formovania postavy. Podľa epidemiologických štúdií dochádza v posledných rokoch k nárastu ich užívania.
Klíčová slova:
anabolicko-androgénne steroidy – herbálne a výživové doplnky (HDS) – hepatocelulárny karcinóm – prolongovaný ikterus – testosterón
Úvod
Androgénne anabolické steroidy (AAS) označované ako bodybuilding suplementy patria do skupiny herbálnych a výživových doplnkov (HDS), ktoré podľa súčasných dát zodpovedajú za približne 20 % všetkých prípadov hepatotoxicity v USA (1). Prevažnú časť tejto skupiny tvoria AAS. Podľa údajov databázy DILIN (Drug Induced Liver Injury Network) v USA ich podiel stúpol z 2 % v rokoch 2004–2005 na 6 % v rokoch 2013–2014 (2). Produkty bodybuilding priemyslu (slangovo bobule, sypačka, zobanie, zrno) (3) zahŕňajú prohormóny, AAS a výživové doplnky s ich obsahom, ich užívanie je ilegálne. Hlavné dôvody pre ich medicínsky neindikované užívanie je cielené zväčšenie objemu svalov, snaha o zvýšenie športového výkonu alebo redukcia telesného tuku. Môžu byť monozložkové alebo vo forme zmesí, často bez deklarovaného zoznamu zloženia. Prímes AAS bola detegovaná i vo vitamínových produktoch (4). Ďalej môžu byť prípravky kontaminované ťažkými kovmi alebo inými medikamentami s cieľom zvýšenia účinku. Najčastejšie ich užívajú špičkoví i rekreační športovci, adolescenti, prevažne mladí muži, často s nadváhou, zväčša bielej rasy.
AAS sú syntetické deriváty testosterónu, ktorý stimuluje rast svalovej hmoty (anabolický efekt) a ovplyvňuje mužské pohlavné znaky (androgénny efekt) (5). Viac ako 95 % jeho tvorby prebieha v Leydigových bunkách testes u mužov, zvyšok má pôvod v nadobličkách oboch pohlaví. Produkciu a vylučovanie riadi hormón adenohypofýzy – luteinizačný hormón. Testosterón prvýkrát izoloval David a spolupracovníci v roku 1935 z býčích testes (6) a v rovnakom roku ho úspešne syntetizoval Butenandt v Göttingene (Nemecko) a Ruzicka v Bazileji (Švajčiarsko) (7). Po tomto kroku bol pripravený na komerčné účely. Neskôr boli vyvíjané ďalšie analógy AAS alebo designer steroidy s cieľom maximalizovať anabolický a minimalizovať androgénny efekt, hoci k úplnej disociácii neprišlo (6). V 80. rokoch 20. storočia sa rozšírilo užívanie zo závodných na amatérskych športovcov ako aj rekreačných vyznávačov cvičenia vo fitnescentrách (8). Od roku 1991 sa AAS zaradili do zoznamu kontrolovaných látok v USA (Drug Enforcement Administration – DEA) (6).
Epidemiológia
Od roku 2010 významne stúpol podiel HDS hepototoxity indukovanej zakázanými anabolickými steroidmi (9). Podľa údajov španielskeho registra v rokoch 1994–2000 sa nezaznamenal žiaden prípad, v rokoch 2001–2009 sa vyskytlo 5 prípadov, za ďalšie 4 roky (2010–2013) počet stúpol na 15 prípadov, t.j. vzostup z 1 % na 8 % všetkých prípadov DILI (Drug Induced Liver Injury). Do roku 2016 bol zaznamenaný ďalší vzostup na 20 prípadov (10) (obr. 1). Nieschlag et al udávajú výskyt zneužívania AAS v celosvetovej populácii u 6,4 % mužov a u 1,6 % žien (11). Vzhľadom na fakt, že ide o nelegálne látky, zdravotné riziká a nežiaduce účinky zostávajú podhodnotené a nehlásené. Podľa prieskumov prevalencia zneužívania AAS dospievajúcimi kolíše medzi 2,6–11 % a je dominantná u chlapcov (12). Podľa odhadov v roku 2007 3,9 % adolescentov (5,1 % chlapcov a 2,7 % dievčat) v USA užilo AAS bez predpisu lekára jeden alebo viackrát počas svojho života (13). V roku 2011 to bolo už 5,9 % dospievajúcich chlapcov (14). Medzinárodná štúdia ESPAD (Európsky prieskum školopovinných detí o alkohole a iných drogách) v roku 2007 u 16-ročnej mládeže v Českej republike preukázala užitie AAS u 4,3 % respondentov, 6,6 % chlapcov a 2,1 % dievčat, pričom v roku 2003 to bolo celkovo len 1,1 %. Uvedené fakty dokumentujú vzrastajúci trend spotreby AAS u mladistvých (15). Nepoznáme epidemiologické štúdie, ktoré by mapovali zneužívanie v Slovenskej republike, ale v prieskume vedomostí a skúseností študentov vysokých škôl s návykovými látkami 1,3 % respondentov priznalo aspoň jednu vlastnú skúsenosť s týmito látkami a 21,3 % respondentov poznalo niekoho, kto AAS užíva (3). Za predajom výživových doplnkov stojí biznis s ročným ziskom 19 miliárd dolárov len v USA (1).
Image 1. Dlhodobý trend výskytu AAS DILI v španielskom DILI registri (1994–2016) (10) 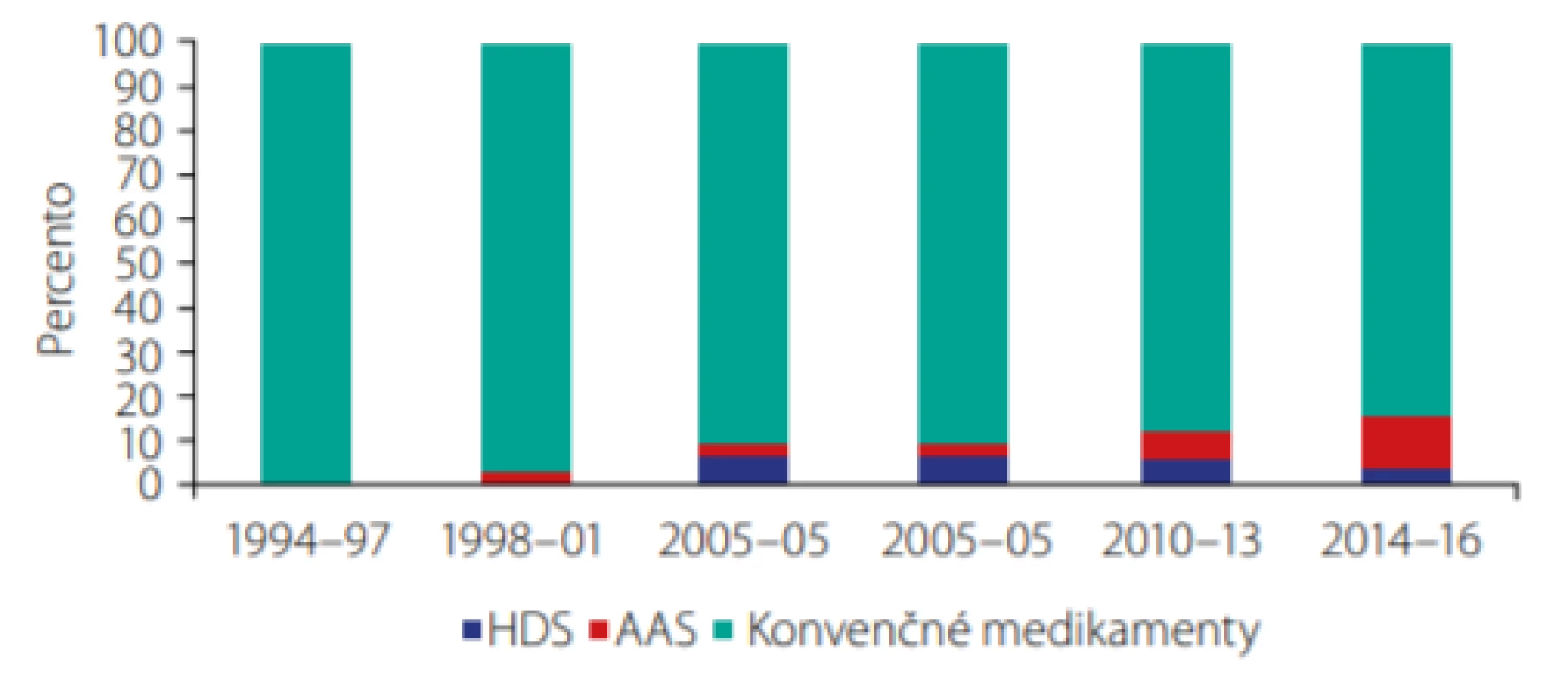
Španielsky DILI (Drug Induced Liver Injury) register z celkového počtu 856 prípadov hepatotoxicity v rokoch 1994–2016 zaznamenal AAS v 20 prípadoch DILI (2 %), herbálne a výživové doplnky (HDS) predstavovali 32 prípadov (4 %), zvyšok konvenčné medikamenty. Skupina s AAS predstavovala výlučne mužov od 20–49 rokov.
Victor J. Navarro et al v prospektívnej štúdii hepatotoxicity (HT) indukovanej HDS vychádzajúcej z DILIN registra (Drug Induced Liver Injury Network v USA) v rokoch 2004–2013 zaznamenal 839 prípadov hepatotoxicity, z čoho 85 % (709 prípadov) vyvolali lieky a 15,5 % (130 prípadov) HDS (2). Z poslednej podskupiny HDS -DILI podskupina bodybuilding HDS obsahovala 45 pacientov (35 % súboru), mužov prevažne mladšieho veku (medián 31 rokov) (2). V priebehu 10-ročného sledovania sa zaznamenal až 200 % vzostup výskytu DILI v dôsledku AAS, resp. BBS (bodybuilding suplementov) v americkom DILIN registri (obr. 2).
Image 2. Trend vývoja HDS a AAS (BBS) v americkom DILIN registri (2004–2014) (2) 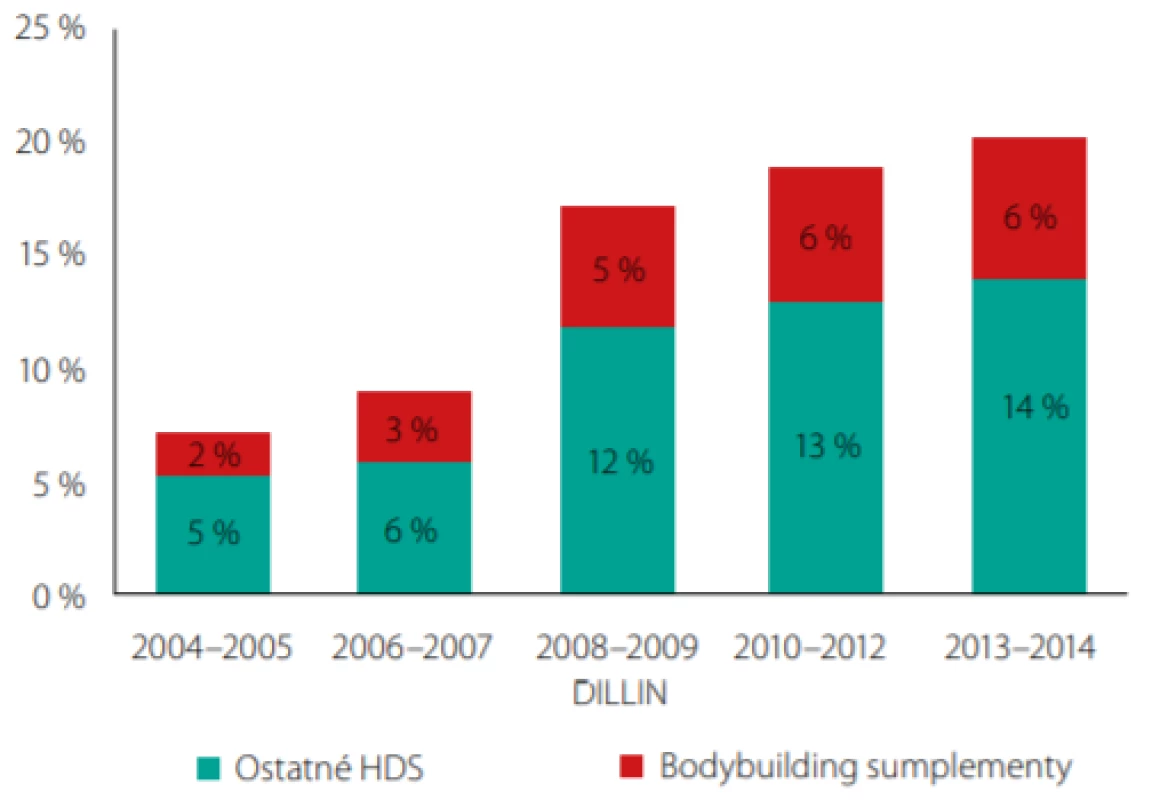
Spôsob užívania a mechanizmy účinku
Užívanie AAS mimo medicínskej preskripcie je ilegálne, prípravky sú komerčne distribuované na čiernom trhu, cez e -shopy, fitnescentrá, trénerov, nevhodnou preskripciou alebo krádežou. Prostredníctvom internetu sú dostupné informácie o očakávaných účinkoch spolu s návodmi na ich užívanie. Najčastejšie sú užívané v 4–12-týždňových cykloch opakujúcich sa niekoľkokrát ročne, často v kombinácii (tzv. skladačka) a v rôznych aplikačných formách (orálna, injekčná, transdermálna, bukálna alebo sublinguálna) (6). Primárne orálne formy sa podieľajú na pečeňovom poškodení. Pri úmyselnom zneužívaní dávkovanie často prekračuje 10–100-násobne dávky odporúčané v terapeutických indikáciách. S cieľom maximalizácie efektu a minimalizácie vedľajších účinkov užívatelia nasledujú rôzne schémy užívania: pyramídová, cyklická, skladačka. Neexistujú vedecké dôkazy o tom, že uvedené schémy zabránia vzniku nepriaznivých účinkov týchto substancií (6). Kombinácia viacerých AAS býva často spojená s užívaním ďalších farmák (tyreoidálne hormóny, diuretiká a psychostimulanciá).
Účinky AAS
AAS stimulujú proteosyntézu prostredníctvom génovej transkripcie po naviazaní sa na androgénne receptory, ktoré sú exprimované v kostiach, tukovom tkanive, kostrovom svalstve, mozgu, prostate, pečeni, obličkách, reprodukčných orgánoch. Počet receptorov a afinita k rôznym typom AAS vysvetľuje pestré účinky v organizme (16). Okrem toho sa naväzujú na glukokortikoidové receptory a tým antagonizujú ich účinok, čo vedie k zníženiu proteosyntézy. Predpokladá sa, že tiež psychicky motivujú užívateľov želajúcich si zvýšenie výkonu.
Etiopatogenetický mechanizmus AAS DILI
Presné mechanizmy AAS indukovanej hepatotoxicity nie sú celkom objasnené. Podľa animálnych modelov sa predpokladá imunoalergický mechanizmus navodený hypersenzitivitou. Oxidačný stres sa zdá byť možným etiologickým faktorom.
AAS
Syntetické AAS sú zlúčeniny derivované z prírodného testosterónu, líšia sa rôznymi modifikáciami, ktoré pozmenia anabolickú alebo androgénnu aktivitu, väzbovú afinitu na androgénový receptor a metabolický klírens (17). Hlavné chemické substitúcie testosterónu sú 17-β -esterifikácia a 17-α -alkylácia (17-αa) (tab. 1). Alkylácia na C-17 pozícii zahŕňa inhibíciu metabolickej deaktivácie oxidáciou 17-β -hydroxy skupiny v pečeni, takže umožňuje orálne podanie, spomaľuje pečeňový metabolizmus AAS, prevažuje anabolický účinok nad maskulinizačným efektom. 17-αa spôsobujú pečeňové poškodenie vrátane prolongovanej cholestázy, peliosis hepatis, nodulárnej regenerácie, hepatocelulárnych adenómov (HCA) a hepatocelulárneho karcinómu (HCC).
Table 1. Modifikované formy testosterónu (21) 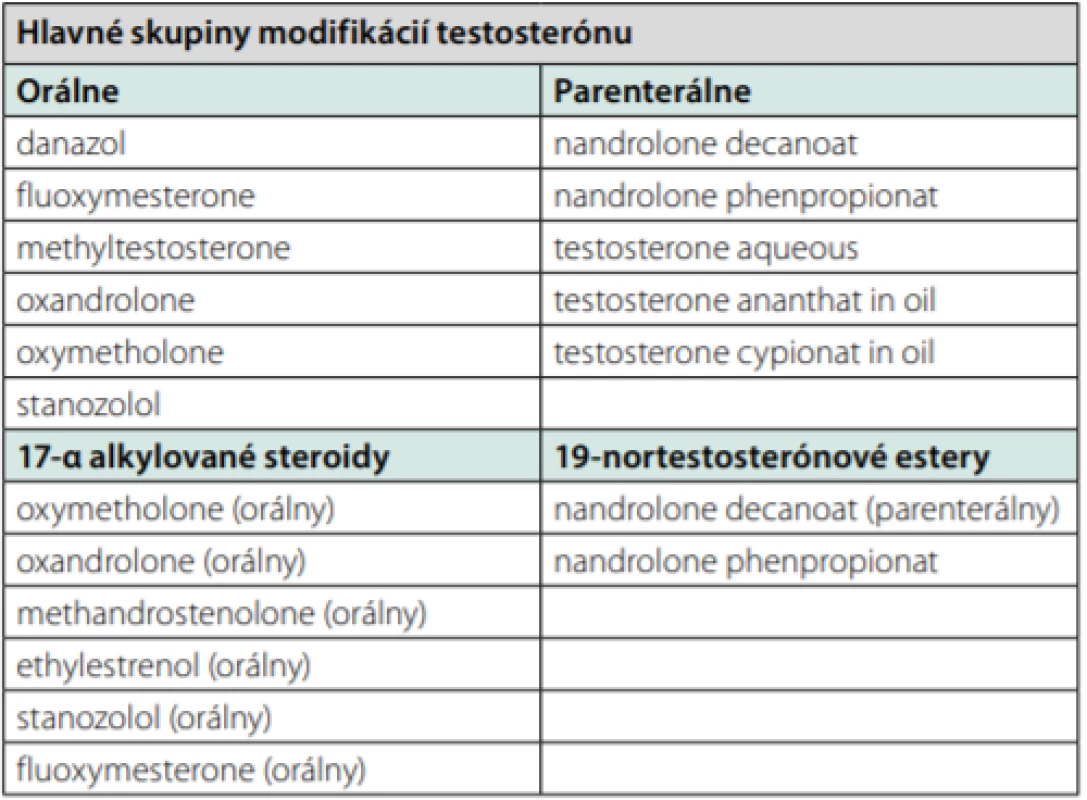
Esterifikáciou (testosterón cypionát, enantát a propionát) 17-β -hydroxylovej skupiny sa zvýšia hydrofóbne vlastnosti, čo predlžuje a zosiluje účinok AAS pri zachovaní virilizačného efektu. Len zriedka spôsobujú cholestázu aj keď dlhodobé používanie môže zvýšiť riziko hepatálnych tumorov a nodulárnej transformácie, zrejme ale v menšej miere ako 17-αa testosterón (11).
Skupina AAS zahŕňa tiež prekurzory čiže prohormóny (slabšie formy AAS) ako dehydroepiandrosterón (DHEA), dihydrotestosterón (DHT), 1-testosterón, 19-norandrostendión, prostazonol a androstendión. Tieto látky bývajú zvyčajne prítomné vo výživových doplnkoch (6). Podávajú sa viacerými spôsobmi, pričom najsilnejší hepatotoxický účinok majú primárne orálne formy.
Klinické prejavy a údaje z registrov
Klinická manifestácia môže imitovať akékoľvek iné pečeňové ochorenie. Varíruje od asymptomatického zvýšenia pečeňových testov (často náhodne zistené) až po fulminantné pečeňové zlyhanie. Spája sa s charakteristickou formou akútnej cholestázy. Úvodné prejavy sú často nešpecifické (nechutenstvo, nauzea, zvracanie, malátnosť), neskôr sa pridruží pruritus, ikterus, tmavý moč, hypocholická stolica, bolesť brucha pod pravým rebrovým oblúkom, hepatomegália a splenomegália. Môžu sa vyskytnúť imunoalergické prejavy – erytém, exantém, subfebrility, prípadne artralgie, myalgie a slzenie. Vzostup sérových enzýmov je typicky mierny. Zvýšenie ALT, ALP býva často menej ako 2–3-násobok hornej hranice normy, dokonca môžu byť v norme i pri ťažkom iktere. Sérové hodnoty ALT môžu byť vysoké na začiatku poškodenia, neskôr klesajú. I napriek vysadeniu môže u 5–10 % stav progredovať do pokročilej fibrózy či cirhózy (18). AAS nepriaznivo ovplyvňujú lipidový profil, znižujú hodnoty HDL -cholesterolu a zvyšujú hodnoty nízkodenzitných lipoproteínov. Zároveň vplyvom na trombocyty zvyšujú riziko trombózy.
Podľa priebehu rozlišujeme akútne (+ fulminantné) DILI – trvá dni až týždne, avšak vždy < 3 mesiace, subakútne DILI trvá týždne až mesiace a chronické DILI > 3 mesiace.
Podľa laboratórneho nálezu rozlišujeme 3 typy hepatotoxicity: hepatocelulárna, cholestatická a zmiešaná (tab. 2) (19).
Table 2. Klinické formy herbálnej hepatotoxicity (19) 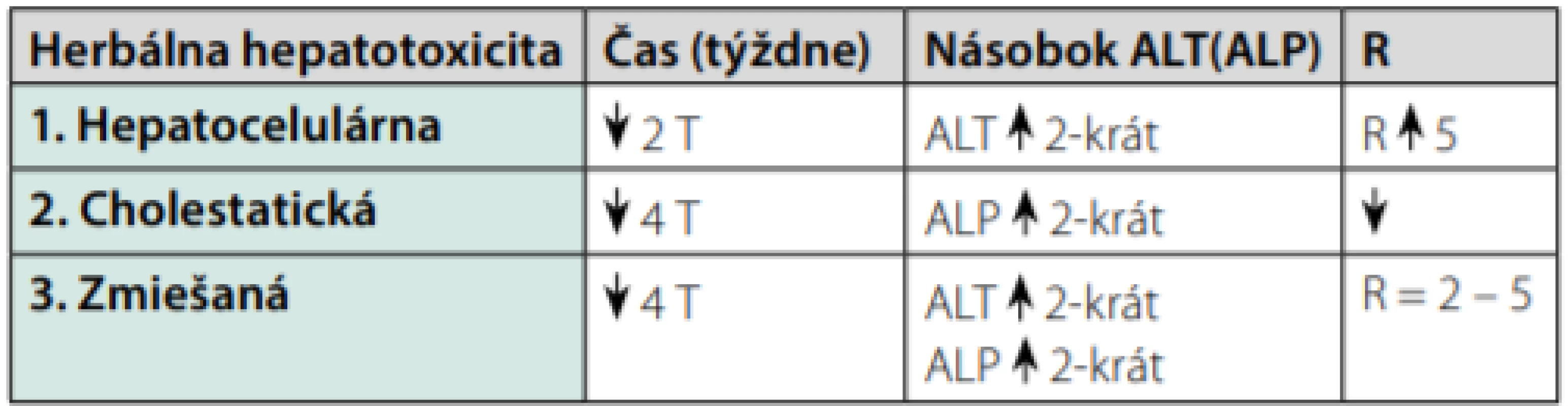
T – týždne
Čas – prejav DILI od začiatku podávania lieku
R – násobok ALT/násobok ALP
Cholestáza
Patrí medzi akútne pečeňové poškodenie. Mechanizmus vzniku pôsobením C-17 substituovaných androgénov nie je úplne objasnený. Predpokladá sa redukcia proteínov transportujúcich žlčové soli a disrupcia intrahepatálnych mikrofilamentov (21). Rozvoj cholestatického ikteru je predvídateľný a viazaný na dávku a trvanie užívania. Zväčša vzniká do 1–4 mesiacov od začiatku užívania, ale môže sa oneskoriť o 6–24 mesiacov. Po vysadení AAS je prechodný a plne reverzibilný (8). Má tendenciu pretrvávať dlho aj po vysadení lieku/suplementu a je spojený s vyšším rizikom prechodu do chronicity. Klinicky sa manifestuje únavou, pruritom, pri závažnom stupni obštrukčným ikterom. Laboratórne sú prítomné známky cholestázy, t.j. zvýšenie cholestatických enzýmov (ALP, GMT), bilirubínu zvyčajne na 5–8-násobok normy. Miera zvýšenia ALP, GMT je daná takto: > 1,5-násobok hornej hranice normy (HHN) ALP a > 3-násobok HHN GMT. Prítomnosť elevácie koncentrácie bilirubínu (viac ako 2-násobok HHN) v kombinácii so zvýšenou aktivitou aminotransferáz – predovšetkým ALT (viac ako 3-násobok HHN) je spojená s horšou prognózou než v prípade izolovanej elevácie aktivity ALT. Táto kombinácia predstavuje Hyovo pravidlo určenia DILI (Hy’s law, podľa Hansa Zimmermanna).
Peliosis hepatis
Patrí medzi chronické pečeňové poškodenie. Ide o vzácny syndróm, podľa publikovaných prípadov došlo k rozvoju po 2–27 mesiacoch liečby AAS. Nemusí byť plne reverzibilný po ukončení užívania. Je charakterizovaný prítomnosťou fokálnych alebo difúznych intrahepatálnych cýst vyplnených krvou (21). Lézie môžu byť asymptomatické alebo je subjektívne udávaný diskomfort v pravom hornom kvadrante brucha. Náhla abdominálna bolesť a vaskulárny kolaps je asociovaný s rizikom ruptúry pečene alebo hemoperitonea.
Hepatálne tumory
Patria medzi chronické pečeňové poškodenie. Pečeňové neoplázie sú asociované s nemodifikovaným alebo esterifikovaným testosterónom. Môžu ich indukovať parenterálne aj orálne preparáty zväčša po 5–15 rokoch užívania (22). Histopatologicky ide o hepatocelulárny adenóm (HCA), adenóm s okrskami malígnej transformácie alebo dobre diferencovaný hepatocelulárny karcinóm (HCC). Typ tumoru môže byť asociovaný s typom androgénu. Kým danazol je asociovaný s HCA, iné preparáty ako oxymetolón, metyltestosterón vedú k HCC (23). Po prerušení užívania môže dôjsť k spontánnej regresii tumoru (8). Dôležitá je skorá detekcia v prevencii rizika malígnej transformácie i náhlej ruptúry a krvácania s hemoperitoneom (21). Športovci zneužívajúci AAS by mali byť starostlivo monitorovaní, adekvátnym skríningom sa zdá byť sonografia brucha.
Takmer všetky prípady AAS zaznamenané v španielskom DILI registri sa klinicky prezentovali ikterom (95 %), prevažoval hepatocelulárny typ pečeňového poškodenia (60 %), bez progresie do akútneho pečeňového zlyhania či potreby transplantácie pečene, alebo fatálnych následkov (10).
V americkom DILIN registri sa hepatotoxicita prejavila prolongovaným ikterom (medián 91 dní), bez potreby transplantácie či bez úmrtia. Autori zistili, že herbálne a výživové doplnky spôsobujú častejšie hepatotoxicitu vyžadujúcu transplantáciu pečene než konvenčné medikamenty (13 % vs. 3 %, p < 0,001). Počas 10 rokov trvania štúdie podiel prípadov viažucich sa k HDS sa zvýšil signifikantne zo 7 % na 20 %.
Ďalšia štúdia analyzovala dáta AAS DILI v španielskom (20 prípadov) a v latinskoamerickom (5 prípadov) DILI registri v priebehu rokov 2001–2013 (20). Autori záverovali, že AAS DILI vedie k vážnemu hepatálnemu a renálnemu poškodeniu, je asociovaná so zreteľným fenotypom – značným zvýšením hodnôt bilirubínu nezávisle od typu poškodenia. Hoci dominantné je hepatocelulárne poškodenie, cholestatické prípady so zreteľným ikterom sú sprevádzané vývojom akútneho obličkového poškodenia.
Štúdia realizovaná v Brazílii v roku 2011 zahŕňala 180 nesúťažných kulturistov, 95 užívateľov, zvyšok neužívateľov AAS, bez pečeňového poškodenia (24). Autori upozornili na možnosť indukcie toxickej tukovej choroby pečene (toxin -associated fatty liver disease – TAFLD) vplyvom AAS, ktorá bola pozorovaná u 12,6 % z 95 užívateľov AAS. Garcia et al na súbore 182 asymptomatických mladých rekreačných kulturistov užívajúcich AAS po obdobie viac ako 6 mesiacov zaznamenali jeden prípad fokálnej nodulárnej hyperplázie, hepatocelulárneho adenómu, hepatitídy B a hepatitídy C (25).
Diagnostika
Diagnóza si vyžaduje podrobnú farmakologickú anamnézu s časovými vzťahmi užívania jednotlivých liekov/prípravkov a klinických ťažkostí. Ďalej koleráciu typu a charakteru pečeňovej lézie so známym charakterom suspektného lieku. Nevyhnutnou podmienkou je vylúčenie iných príčin ochorenia pečene (infekčné príčiny, alkoholová choroba pečene, autoimunitná hepatitída, vrodené metabolické choroby (tab. 5), zrealizovanie ultrasonografie abdomenu a dopplerovské vyšetrenie portálneho systému, vylúčenie inej možnej toxicity (potravinové doplnky, herbálne produkty). Diagnostické prekážky zahŕňajú neoznačené prímesi a prísady, kontaminácie prípravkov. Pre diagnózu DILI nie je zásadná pečeňová biopsia, môže byť však prínosom pri vylúčení inej etiológie (predovšetkým nádorovej infiltrácie). Histologický obraz nie je špecifický a prekrýva sa s inými ochoreniami pečene (vrátane autoimunitnej hepatitídy) (26). Biopsia pečene typicky preukazuje miernu kanalikulárnu cholestázu s minimálnou inflamáciou a hepatocelulárnou nekrózou. Poškodenie žlčovodov typicky nie je prítomné alebo je minimálne. Vzácne vzniká syndróm miznúcich žlčovodov. Podľa FDA sa biopsia odporúča, ak dôjde k vzostupu aminotransferáz napriek vysadeniu prípravku, alebo ak ALT neklesne o viac ako 50 % do 30–60 dní od jeho zistenia pri hepatocelulárnom liekovom poškodení, alebo ak ALP neklesne o viac ako 50 % do 180 dní pri cholestatickom type, a ak biochemické abnormality pretrvávajú viac ako 180 dní (19). Vo väčšine prípadov očakávame zlepšenie stavu po vysadení prípravku. Pre klinickú prax FDA navrhla klasifikáciu typov DILI (tab. 4) (19). Najrozšírenejšia metóda hodnotenia kauzality je „Roussel Uclaf Causality Method“ (RUCAM) z roku 1993, inovovaná v roku 2016 (19). Predstavuje štandardizovanú skórovaciu metódu, využiteľnú najmä v klinických štúdiách, ktorá je časovo náročnejšia na použitie v rutinnej praxi. Použitie on -line kakulátora uľahčuje výpočet skóre (http://farmacologiaclinica.info/scales/CIOMS -RUCAM/).
Table 3. Lieková hepatatotoxicita podľa FDA – Food and Drug Administration(19) 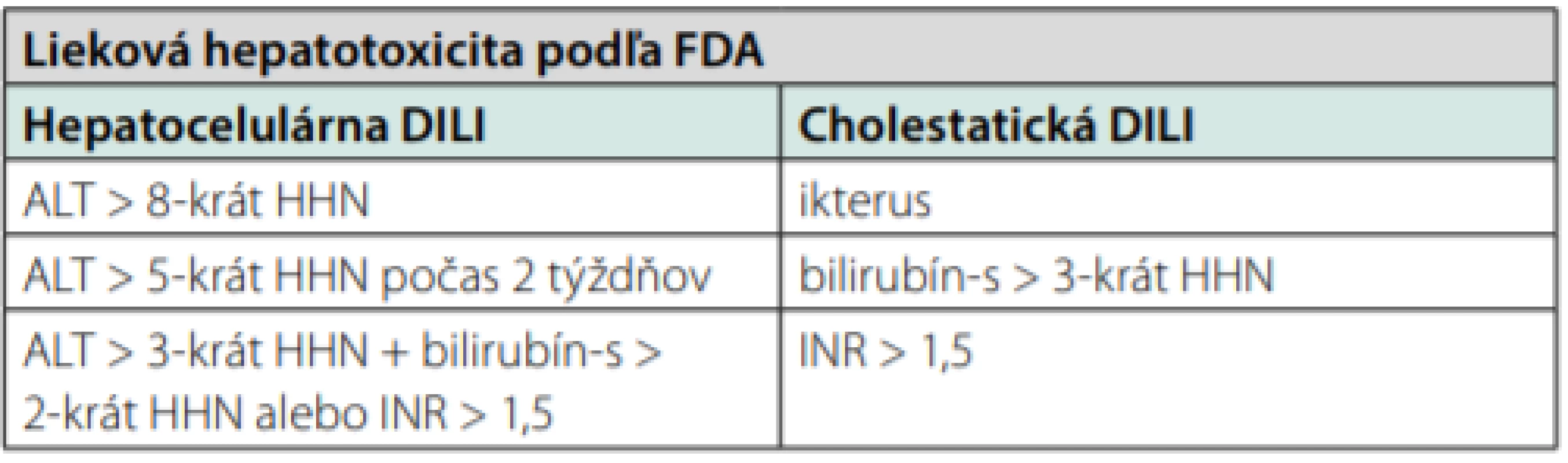
Table 4. Diferenciálna diagnostika hepatálneho poškodenia, upravené podľa (30) 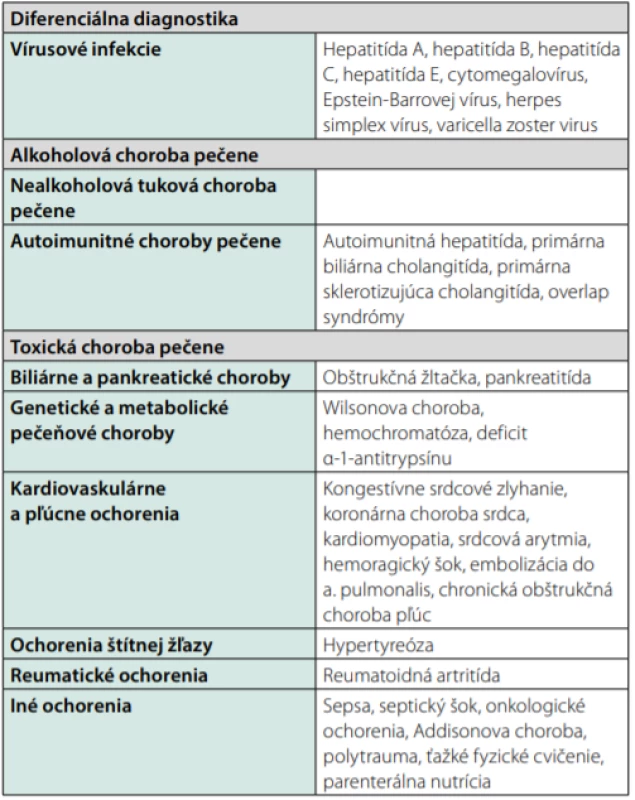
Terapia
Skoré rozpoznanie DILI a promptné vysadenie produktu/lieku je rozhodujúce pre minimalizáciu poškodenia a progresie stavu. Súčasná liečba DILI je podporná a symptomatická (napr. pruritus) (27). Doplnená všeobecnými podpornými opatreniami – diéta, hepatiká, pokoj na lôžku, pri ťažkom priebehu hospitalizácia s monitoringom klinického stavu a laboratórnych ukazovateľov. Zaužívané hepatiká (silymarín, kyselina ursodeoxycholová, fosfatidylcholín, S -adenozylmetionín a pod.) majú cytoprotektívne, antifibrotické, protizápalové, antioxidačné a anticholestatické účinky, avšak ich pôsobenie či priaznivý vplyv na prognózu nie je podporený súčasne dostupnými klinickými štúdiami. Z podávania kyseliny ursodeoxycholovej by mali profitovať pacienti s cholestatickou hepatitídou s eleváciou transamináz, u ktorých nedošlo k rýchlemu zlepšeniu biochemických ukazovateľov po vysadení preparátu. I keď ide o off -label indikáciu, EASL odporúčania pre cholestatické choroby pečene dokladujú zlepšenie u 2/3 pacientov s DILI po liečbe (29). Kontroverznou možnosťou liečby je podávanie kortikosteroidov. Ich prínos pri bežnom DILI sa nedokázal a ich podanie je spojené s rizikom výskytu nežiaducich účinkov (28). Pozitívny efekt môžu mať len v prípade DILI s klinickými symptómami hypersenzitivity (vrátane extrahepatálnych prejavov). Symptomatická liečba pruritu (cholestyramín, kyselina ursodeoxycholová, antihistaminiká) majú zväčša len mierny efekt. Fulminantné zlyhanie pečene sa lieči rovnako ako zlyhanie pečene inej etiológie. V najťažších prípadoch je indikovaná transplantácia pečene (Clichy kritériá alebo King’s College kritériá). Je tiež potrebné vyhnúť sa reexpozícii inkriminovaného prípravku.
Záver
Lekári prvého kontaktu by mali mať dostatočné informácie o možných prejavoch AAS toxicity. Dôležité je dokázať zavčasu rozpoznať prejavy užívania AAS, ako je enormný nárast svalovej hmoty, gynekomastia, ťažko liečiteľné akné na chrbte, strie, skoré známky maskulínnej alopécie, hypertenzia, zvýšenie hepatálnych enzýmov, bilirubínu, zmeny hladiny cholesterolu, narastajúca agresivita a emočná labilita. Morálnou povinnosťou každého zdravotníka je dôsledná prevencia užívania, zisťovanie, dokumentácia a hlásenie každého zisteného prípadu Štátnemu ústavu pre kontrolu liečiv. Bez kontroly týchto dostupných látok hrozí neobmedzený prístup k prípravkom. Nebezpečná je tzv. self -medikácia, prekračovanie dávok, zatajovanie užívania. Závislosť môže vzniknúť už po niekoľkých mesiacoch užívania. Mnoho abuzérov používajúcich injekčné formy AAS sa vystavuje riziku parenterálne prenášaných infekcií (HIV, hepatitída B a C). Chýba regulácia či kontrola zloženia a štandardizácia účinných látok. World Anti -Doping Agency (WADA) založená v roku 1999 ako medzinárodná nezávislá agentúra zakazuje akýkoľvek AAS alebo príbuznú zložku. DEA (Drug Enforcement Administration) nepretržite zahŕňa nové látky do zoznamu, avšak neustále sa vyvýjajú nové preparáty. Môžeme konštatovať, že žiadne „bezpečné užívanie“ anabolických steroidov neexistuje. V roku 1993 pristúpila Slovenská republika k Dohovoru proti dopingu Rady Európy, podľa ktorého sa medzi dopingové skupiny zaraďujú aj anabolické steroidy. V roku 1994 bolo podávanie anabolických látok mládeži na iný ako liečebný účel kvalifikované Trestným zákonom ako trestný čin. I keď v dostupnej literatúre sme nezaznamenali prípad transplantácie pečene v súvislosti s AAS DILI, AAS sú jednoznačne asociované s možnosťou vývoja TAFLD a iných život ohrozujúcich komplikácií (neoplázie, peliosis hepatis) s rizikom fatálnej ruptúry a hemoperitonea, ako i rizikom vzniku závislosti či renálneho zlyhania. Úlohou lekárov je zodpovedný prístup v prevencii, osvete, monitorovaní a hlásení všetkých zistených prípadov AAS–DILI. Zavedenie národného klinického registra hepatotoxicity by napomohlo k presnejšej evidencii všetkých prípadov AAS DILI, k zjednoteniu a optimalizácii postupov v liečbe i k implementácii ďalších preventívnych systémových opatrení.
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Martina Jakabovičová,
III. interná klinika LF UK a UNB, Nemocnica ak. L. Dérera,
Limbová 5,
833 05 Bratislava
Cit. zkr: Vnitř Lék 2020; 66(1): 28–33
Článek přijat redakcí: 2. 1. 2019
Článek přijat k publikaci: 29. 7. 2019
Sources
1. Navarro V, Khan I, Bjornsson E. Liver Injury from Herbal and Dietary Supplements. Hepatology 2017; 65 : 363–373.
2. Navarro VJ, Barnhart H, Bonkovsky H et al. Liver Injury from Herbal and Dietary Supplements in the US Drug Induced Liver Injury Network. Hepatology 2014; 60 : 1399–1408.
3. Kolibáš E Anabolické steroidy - psychiatrická problematika ich zneužívania. Alkohol Drog Záv (Protialkohol Obz) 2004; 4-5 : 217–235.
4. Rahnema CD, Crosnoe LE, Kimed H. Designer steroids over the counter supplements and their androgenic component: review of an increasing problem. Andrology 2015; 3 : 150–155.
5. Maravelias C, Dona A, Stefanidou M et al. Adverse effects of anabolic steroids in athletes. A constant threat. Toxicol Lett 2005; 158 : 167–175.
6. Barceloux DG, Palmer RB Anabolic -androgenic steroids. Dis Mon 2013; 59 : 226–248.
7. Kanayama G, Hudson JI, Pope jr. HG Illicit anabolic androgenic steroid use. Horm Behav 2010; 58 : 111–121.
8. Shahidi NT. A review of the chemistry, biological action, and clinical applications of anabolic -androgenic steroids. Clin Ther 2001; 23 : 1355–1390.
9. Szántová M Hepatotoxicita indukovaná herbálnou medicínou a dietetickými doplnkami. Interná med 2017; 17 : 473–479.
10. Caliz IM, Cortes MG, Jimenez AG. Herbal and Dietary Supplement -Induced Liver Injuries in the Spanish DILI Registry. Clinic Gastroent and Hep 2018; 16 : 1495–1502.
11. Nieschlag E, Vorona E. Doping with anabolic androgenic steroids (AAS): adverse effects on nonreproductive organs and functions. Rev Endocr Metab Disord 2015; 16 : 199–211.
12. Kabíček P. Zneužívaní anabolických steroidu u dospívajícich v medzinárodním kontextu. Vox pediatriae 2005; 5 : 14–15.
13. Eaton DK et al. Youth risk behavior surveillance - United States, 2007. Mortality and Morbidity Weekly Report. Surveillance Summaries 2008; 57 : 1–131.
14. Eisenberg ME, Wall M, Neumark -Sztainer D. Muscle -Enhancing Behaviors Among Adolescent Girls and Boys. Pediatrics 2012; 130 : 1019-1036.
15. Šimurka P, Zavrel M. Anabolické steroidy a mládež. Pediatr pro Praxi 2008; 9 : 294–297.
16. Snyder PJ. Androgens. In: Hardman JG, Limbird LE, Gilman AG (eds.). Goodman and Gilman’s The Pharmacological Basis of Therapeutics. New York: McGraw Hill 2001; 1635–1648.
17. Pope jr. HG, Wood RI, Rogol A et al. Adverse health consequences of performance-enhancing drugs: an endocrine society scientific statement. Endocr Rev 2014; 35 : 341–375.
18. Andrade RJ, Lucena MI, Fernandez MC et al. Drug -induced liver injury: an analysis of 461 incidences submitted to the Spanish registry over 10-years period. Gastroenterology 2005; 129 : 512–521.
19. Szántová M, Sedlačko J, Jakabovičová M. Lieková a herbálna hepatotoxicita: Prehľad klinických klasifikácií. Vnitr lek 2018; 64 : 384–393.
20. Robles DM, Gonzalez JA, Medina CI. Distinct phenotype of hepatotoxicity associated with illicit use of anabolic androgenic steroids. Aliment Pharmacol Ther 2015; 41 : 116–125.
21. Modlinski R, Fields KB. The effect of anabolic steroids on the gastrointestinal system, kidneys, and adrenal glands. Curr Sports Med Rep 2006; 5 : 104–109.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2020 Issue 1-
All articles in this issue
- Ve spojení a jednotě je síla
- Hlavní téma: Metabolický syndrom
- Léčba hypertenze u metabolického syndromu – update 2019
- Aterogenní dyslipidemie typické pro metabolický syndrom
- Diabetes mellitus 2. typu v praxi – balancování mezi rezistencí a sekrecí
- Hepatotoxicita indukovaná bodybuilding suplementami
- Chronický stres, psychická nepohoda a deprese zvyšují četnost infekčních, autoimunitních, ale i maligních nemocí
- Sarkopenická obezita – aktuální přehled problematiky
- Autoimunitní hepatitida
- Dvacet let cesty nefrologa do hlubin toxicity fosforu
- Monitorovanie a individualizácia liečby inhibítormi P2Y12 ADP receptorov
- Infarkt myokardu u pacienta s metabolickým syndromem a prokázaným syndromem obstrukční spánkové apnoe
- Úskalí v diagnostice srdeční amyloidózy a možnosti terapie
- Bolesti a deformace dolní čelisti – projev fibrózní dysplazie čelisti
- K čemu lze využít výsledek vyšetření koncentrace celkového cholesterolu?
- Několik poznámek ze čtení posledních doporučených postupů pro léčbu DLP verze 2019
- Založení profesního spolku SAI – sdružení ambulantních internistů, z. s.
- Odešel velký člověk a lékař prof. MUDr. Vítězslav Kolek, DrSc., FCCP
- Prevalence a rizikové faktory T buňkami zprostředkované rejekce u pacientů po transplantaci jater od zemřelého dárce – retrospektivní studie v desetiletém období
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Sarkopenická obezita – aktuální přehled problematiky
- Chronický stres, psychická nepohoda a deprese zvyšují četnost infekčních, autoimunitních, ale i maligních nemocí
- Odešel velký člověk a lékař prof. MUDr. Vítězslav Kolek, DrSc., FCCP
- Autoimunitní hepatitida
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

