-
Medical journals
- Career
Zamyšlení nad chlopenními vadami včera a dnes
Authors: Pavel Gregor; Hana Línková
Authors‘ workplace: Kardiocentrum – III. interní-kardiologická klinika 3. LF UK a FN Královské Vinohrady, Praha
Published in: Vnitř Lék 2017; 63(5): 322-327
Category: Reviews
Overview
Práce se zabývá problematikou získaných chlopenních vad. Zahrnuje především nové poznatky týkající se etiopatogeneze, diagnostiky, posuzování a léčby, zvláště katetrizační. Ve vyspělých zemích téměř vymizely porevmatické vady, jejich současná etiologie se podstatně změnila (mitrální stenóza). Naopak převažují vady degenerativní, dříve relativně vzácné, které postihují především starší nemocné (stenóza aorty). Podstatně se změnily i léčebné metody získaných vad – při jejich korekci se v současnosti častěji uplatňují katetrizační přístupy.
Klíčová slova:
aortální regurgitace – aortální stenóza – echokardiografie u chlopenních vad – magnetická rezonance u vad – mitrální regurgitace – mitrální stenóza – náhrada chlopněÚvod
Poznatky o chlopenních vadách se v uplynulých desítiletích velmi podstatně změnily. Došlo ke změnám v zastoupení jednotlivých vad v populaci, prohloubily se naše znalosti o etiopatogenezi vad, v důsledku dokonalejších vyšetřovacích metod se upřesnila i jejich diagnostika. Podstatně se změnila i léčba, a to především díky katetrizačním metodám. V tomto článku si dovolujeme na některé tyto změny poukázat, a to v kontextu dřívějších poznatků.
Posun názorů na etiologii chlopenních vad můžeme dobře ilustrovat na následujícím příkladu. V učebnici interny, z níž se učila naše generace [1], začíná kapitola o aortální regurgitaci takto: „Většina čistých aortálních insuficiencí nebo kombinovaných se stenózou je revmatického původu… Vzácnější příčiny jsou bakteriální endokarditida, vrozené anomálie, disekující aneuryzma v kořenu aorty, Marfanův syndrom a luetická aortitida“. Z ukázky vyplývá, jak zásadně se v průběhu necelého čtvrtstoletí situace změnila. Luetická mezaortitida ve vyspělých zemích neexistuje, tak jak vymizel terciální lues, mezi nejčastější naopak patří vrozené, zvláště bikuspidální aortální vady, ale především vady degenerativní, které nejsou ve výše uvedeném výňatku vůbec uvedeny.
Ve vyspělých zemích včetně ČR nevidíme již revmatickou horečku, tudíž vady, které jsou s touto etiologií spojeny, jsou tam velmi vzácné. To je případ především mitrální stenózy (MS), která v současnosti patří v uvedených zemích mezi vzácné vady. Podle evropských dat tvoří něco málo přes 10 % vad u dospělých [2], v praxi pracovišť v České republice je její výskyt ještě nižší. Při jednom z posledních termínů kardiologických atestací dokonce vyšlo najevo, že adept kardiologie, který dostal otázku MS, se s touto vadou během studia ani v dalších několika letech práce v jednom z předních českých kardiocenter dosud nesetkal. Lze si jistě pak snadno představit, že se v praxi na takovéto vady nemyslí a nemusí se řádně a včas diagnostikovat.
Chlopenní vady dnes
Otázka výskytu revmatické horečky a porevmatických srdečních vad však zaslouží podrobnější diskusi. Rozhodně nelze podlehnout dojmu, že těchto chorob zásadně ubylo v celém světě – v chudších a rozvojových zemích naopak stále patří k nejzávažnějším zdravotnickým problémům [2]. V roce 2010 přesáhl celkový počet nemocných s revmatickými srdečními vadami 34 milionů osob s více než 345 000 úmrtími a 10 miliony invalidity za rok [3]. V nejvyšším riziku akutní revmatické horečky jsou děti od 3 do 15 let, vrchol výskytu porevmatických vad je 25–45 let. Postiženy jsou převážně levostranné chlopně, ale existuje obrovská regionální heterogenita jak pokud jde o věk, tak i způsob prezentace chlopenního postižení. U osob mladších 10 let většinou dominuje mitrální regurgitace, od 3. dekády pak mitrální stenóza [3].
Mnoho pacientů s chlopenními vadami je dnes ve vyspělých zemích starších a polymorbidních. S tím, jak v některých zemích ubylo revmatické horečky, rozšířil se počet nerevmatických vad a celé spektrum chlopenních vad se v porovnání s dřívějším stavem změnilo. Extrémně přibyl počet nemocných po kardiochirurgických a v posledních letech i katetrizačních zákrocích.
Prevalence získaných chlopenních vad se pohybuje v obecné populaci v rozmezí 0,2–1 %, nejnovější data z USA však ukazují ještě podstatně vyšší čísla pohybující se kolem 2,5 % [4]. V celkovém počtu operovaných vad zaujímají v České republice prvá dvě místa stenóza aorty (> 50 %) a mitrální regurgitace (> 20 %). Aortální regurgitace je v počtu operovaných vad na 3. místě [5].
Situace se zásadně mění s věkem. Ve skupině 80 a víceletých je prevalence středně až více významných vad 17 % [6]. Převažuje stenóza aorty, i když v některých regionech může být pořadí vad jiné [7].
Velmi komplikovaně se může jevit v současné době etiologie některých chlopenních vad – lze to demonstrovat na mitrální stenóze (MS). Ještě nedávno byla situace jednoduchá – v drtivé většině šlo o postrevmatické vady s typickým srůstem cípů v komisurách, ztluštěním cípů, mitrálních šlašinek s následným ukládáním vápníku. Vrozený původ MS byl a stále je raritou. Lze se s ním setkat u Lutenbacherova syndromu (spojení MS a defektu septa síní typu secundum) a dále u padákovité (parachut) mitrální chlopně.
Zvláštní je vztah myxomů levé síně a MS. Tyto myxomy mají průměrnou velikost 5 cm a lze si snadno představit, že mohou vést k obstrukci mitrálního ústí. Kombinace myxomu a mitrální stenózy je však naproti tomu extrémně vzácná – mitrální stenóza může pak působit jako určitý ochranný mechanizmus proti embolizacím větších částí myxomu do velkého oběhu [8]. Vzácná je MS u jiných benigních srdečních nádorů, např. hemangiomu [9], MS byla popsána i u některých maligních nádorů srdce [10,11]. MS se může vyskytnout i u některých systémových chorob, nejnověji byla popsána u tuberózní sklerózy [12].
MS však může mít i degenerativní původ, což není – na rozdíl od našich dřívějších názorů – nijak vzácná situace. V minulosti byla tato etiologie MS zcela na okraji zájmu, dnes se jí věnuje výraznější pozornost jednak s ohledem na její vyšší výskyt, zejména u starších žen diabetiček a nemocných s renální insuficiencí [13], jednak s ohledem na prodlužování lidského věku ve vyspělých zemích. Degenerativní MS je charakterizována přítomností rozsáhlejší kalcifikace v mitrálním prstenci spojené s transmitrálním diastolickým gradientem ≥ 2 mm Hg. Jak vyplynulo z 5letého sledování více než 1 000členného souboru nemocných, prognóza této vady je špatná, především u starších osob, současné renální insuficience, fibrilace síní nebo dalších chlopenních vad [13]. Podávání inhibitorů ACE a statinů může vést ke zlepšení prognózy, zatímco užití digoxinu prognózu spíše zhoršuje a jeho podávání se v této indikaci spíše nedoporučuje [13]. Problematická může být u rozsáhlejších kalcifikací i kardiochirurgická terapie, velká část pacientů je léčena medikamentózně. Perkutánní intervence k řešení těchto vad dlouho neexistovaly [14], i když v posledních letech bylo i u nich dosaženo výraznějšího pokroku, jak zmíníme v dalším textu.
V současnosti je věnována podstatně větší pozornost než dříve také kalcifikacím v mitrálním prstenci, které byly pokládány spíše za banální sekundární, náhodně zjištěný nález. Jejich prevalence se v populaci pohybuje mezi 8 a 15 % [15–17]. Jsou spojeny s vyšší kardiovaskulární morbiditou i mortalitou, jak prokázala Framinghamská studie [18] i další práce [19,20]. Je u nich častější vývoj mitrální stenózy i regurgitace, vzácně i infekční endokarditidy. Někdy se spojují i s některými poruchami srdečního rytmu (atrioventrikulární a raménkové blokády, fibrilace síní), mohou významně ovlivňovat výskyt komplikací po kardiochirurgických, ale i katetrizačních výkonech, zejména po TAVI [21]. Tradiční diagnostickou metodou je echokardiografie, její specificita je však poměrně nízká, neboť odlišení kalcifikací od denzního kolagenu je často problematické [17]. V současnosti lze k jejich diagnostice a přesnému popisu využít CT [22]. Dříve se na ně nahlíželo jako na výsledek pasivního, spíše náhodně vzniklého nálezu spojeného s věkem, aterosklerózou a renální insuficiencí. Dnes je zřejmé, že jde o proces odrážející přítomnost kardiovaskulárních rizikových faktorů stejně jako aterosklerotické tepenné postižení – jde o různé projevy jedné a téže choroby. Nacházejí se častěji u aterosklerotických změn aorty, karotid, tepen dolních končetin, ICHS a dále u pacientů s mozkovými cévními příhodami [16]. Vznik kalcifikací prstence je akcelerován u stavů zvýšeného napětí mitrální chlopně, jak tomu bývá u hypertenze, hypertrofické kardiomyopatie, stenózy aorty a dále při vyšší tenzi mitrálního aparátu u prolapsu, více se nacházejí i po náhradě mitrální chlopně [16,23]. Častější jsou i u poruch metabolizmu kalcia a fosforu, především u chronické renální insuficience [16,23]. Častěji se nacházejí u žen, což může souviset s výskytem kalciových ektopických depozit při postmenopauzální osteoporóze [24]. Odstranění kalcifikací mitrálního prstence bývá při operacích často obtížné. V případech extrémně rozsáhlého postižení bylo referováno o nutnosti resekce celého prstence a jeho rekonstrukce s pomocí koňského perikardu [25].
Patogeneze chlopenních vad může být také podstatně složitější, než jsme si mohli v dřívějších letech představit, což také souvisí s nárůstem našich znalostí. Pravděpodobně nejvíce poznatků máme o degenerativních aortálních vadách, přesněji o „kalcifikační aortální chlopenní nemoci“ (Calcific Aortic Valve Disease – CAVD). Ta představuje především ve vyspělých zemích závažný zdravotnický problém a u starších osob lze hovořit až o epidemickém výskytu. Postihuje třetinu osob starších 65 let, při jejím vzniku může hrát roli kromě věku i pohlaví, hypercholesterolemie, kouření, hypertenze [15], ale i diabetes mellitus 2. typu [26], což jsou faktory, které jistě z dřívějších popisů chlopenních vad neznáme. Operace aortální stenózy je dnes po aortokoronárním bypassu 2. nejčastějším kardiochirurgickým výkonem [27].
Srdeční chlopně jsou tvořeny zevní vrstvou endoteliárních buněk obklopených 3 vrstvami extracelulární matrix proložené zvláštními intersticiálními buňkami. V úvodních fázích vzniku CAVD vzniká dysfunkce endoteliárních buněk s akumulací lipidů a subendoteliární matrix na komorové straně aortální chlopně [28]. V patogenezi CAVD se dále uplatňuje zánět a řada faktorů s ním spojených včetně tumor nekrotizujícícho faktoru, interleukinu 1-β a celé řady dalších procesů [29].
V posledních letech se objevila řada nových poznatků týkajících se genetických vlivů při vzniku chlopenních vad. Byly identifikovány geny podílející se na normálním vývoji a funkci všech 4 srdečních chlopní a současně i na různých jejich patologických stavech [30]. K nejčastějším vrozeným chlopenním abnormalitám patří bikuspidální aortální chlopeň a prolaps mitrální chlopně. Velmi zajímavá je z tohoto hlediska patogeneze mitrálního prolapsu, v níž zaujímá důležitou roli růstový faktor β (TGF β), který je nezbytný k utváření chlopně [30]. Patogeneze chlopenních vad se však účastní i dlouhá řada nejrůznějších biomarkerů, v těchto podrobnostech však odkazujeme na speciální literaturu [4].
Zcela odlišná je problematika sekundárních (funkčních) vad, které jsou způsobeny remodelací komory bez primárního postižení samotných chlopní – tuto problematiku však zde nelze rozebírat. Z nich je pravděpodobně pro praxi nejzajímavější a nejčastější mitrální regurgitace vznikající obvykle u selhávající levé komory – podrobný a recentní přehled této problematiky je čtenářům k dispozici z roku 2015 [31].
Pokud jde o neinvazívní zobrazovací metody u chlopenních vad, stále platí pořadí echokardiografie – kardiovaskulární magnetická rezonance – CT. Dostupnost a zkušenosti s echokardiografickou diagnostikou zůstávají stále nepřekonány, také v literatuře je k dispozici extrémní množství nejrůznějších prací prověřených časem. Echokardiografie může na jedné straně sloužit k velmi rychlé diagnostice, např. v podobě kapesních přístrojů využitelných kdekoli [32,33], na druhé straně se uplatňují některé novější echokardiografické mody [34–36]. Jako příklad může sloužit metoda tkáňového dopplerovského vyšetření a speckle-tracking [33,34], dále pak trojrozměrná echokardiografie vhodná k podrobnějšímu posouzení morfologie chlopní (obr. 1), měření chlopenních ústí i mitrálního prstence [39–41].
Image 1. 3D echo-zobrazení prolapsu zadního cípu mitrální chlopně. 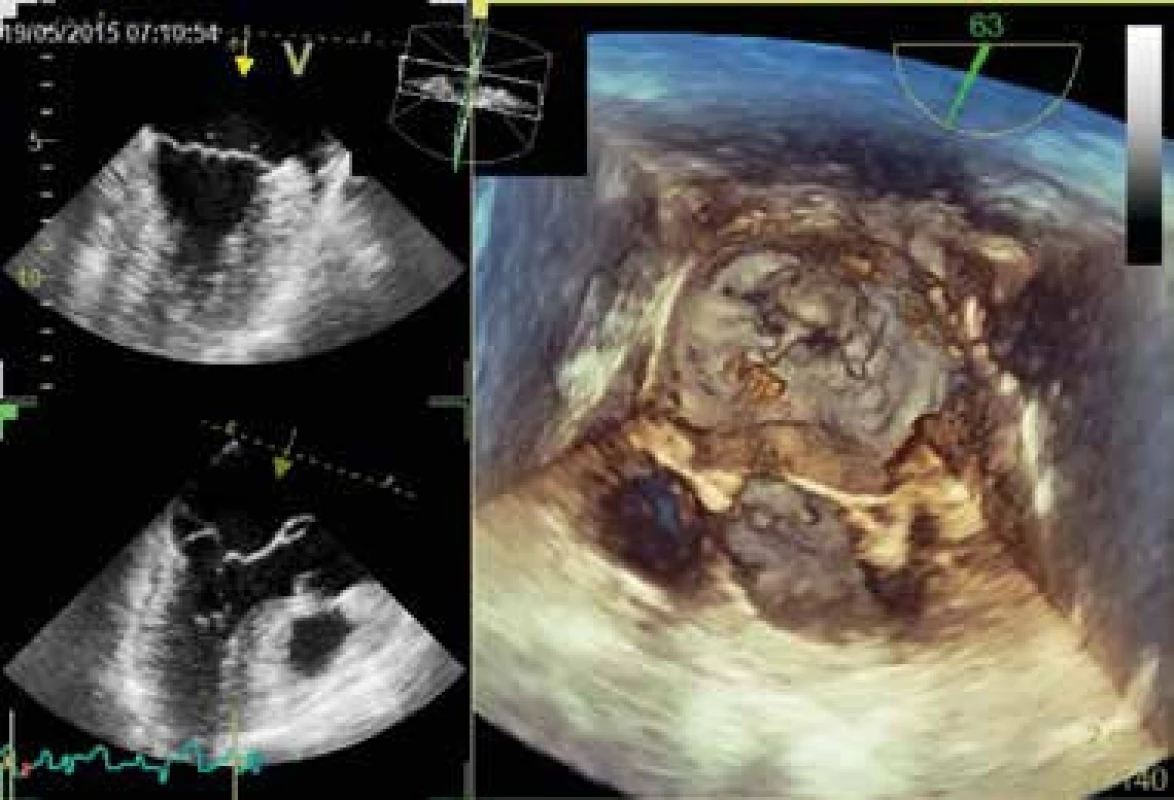
Prolaps scalopu P2 je ve 2D a 3D zobrazení označen šipkou Stále více se uplatňuje kardiovaskulární magnetická rezonance [42–44]. Určitý význam může mít i CT vyšetření, např. při kvantifikaci chlopenních ústí, rozměru a geometrie mitrálního anulu (často se používá např. před katetrizačními zákroky na chlopních typu TAVI, obr. 2) nebo k bližšímu posouzení odstupujících velkých tepen [44–46]. Velké naděje přináší 4rozměrné CT.
Image 2. CT vyšetření aortální chlopně a ascendentní aorty před plánovanou katetrizační náhradou aortální chlopně 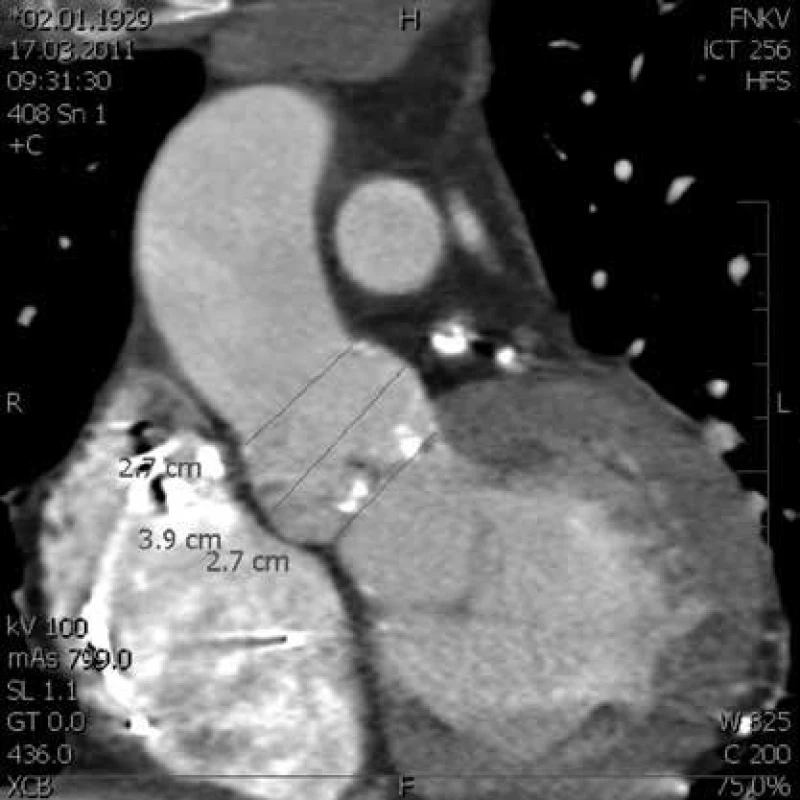
Vedle nárůstu našich znalostí týkajících se etiopatogeneze chlopenních vad je nejvíce fascinující rozšíření spektra léčebných zákroků – jednak spadajících pod působnost kardiochirurgie [47], jednak zákroků patřících mezi katetrizační intervence. Ty se staly velmi efektivním a bezpečným způsobem řešení řady chlopenních vad. Nejdéle je známa transkatétrová náhrada aortální chlopně (TAVI, TAVR), která se začala užívat jako alternativa chirurgické náhrady u pacientů s výrazně zvýšeným operačním rizikem. Podařilo se u ní v podstatné míře zvládnout různé překážky a problémy, které ji zpočátku provázely (mozkové cévní příhody, paravalvulární regurgitace). Nyní se hlavní pozornost soustřeďuje na vývoj dalších, trvanlivějších chlopní s postupným rozšiřováním tohoto výkonu i na jiné než pouze nejrizikovější nemocné, a dále na jiné chlopně a struktury, než je pouze aortální chlopeň [48]. Transkatétrové chlopenní intervence nejsou indikovány již pouze u trikuspidálních aortálních chlopní, ale i u stenóz bikuspidální aortální chlopně, implantací typu valve-in-valve nebo valve-in-ring, v některých případech i u aortálních regurgitací.
TAVI řeší pochopitelně situaci u aortální stenózy. Problém v těchto případech představují přidružená chlopenní postižení, především těžší mitrální regurgitace, která navíc zvyšuje i riziko samotného výkonu [49]. Po úspěšné TAVI však může dojít k jejímu zlepšení [50]. V některých případech docházelo k tomuto zlepšení až později bez dalšího symptomatického efektu, ale s trendem ke zlepšení prognózy [51]. Podle posledních výsledků sledování nemocných po TAVI se zdá, že prognóza je zřetelně zhoršena pouze u nemocných se současnou mitrální regurgitací a regurgitací aortální, která vznikne nově po TAVI [52]. Ze zkušeností po kardiochirurgické náhradě aortální chlopně u více než 400 nemocných s lehčí nebo středně významnou mitrální regurgitací vyplývá, že se tato regurgitace může po výkonu významně zlepšit s příznivým mortalitním trendem (na hranici statistické významnosti) při 5letém sledování [53], u pacientů bez ovlivnění mitrální regurgitace k tomuto trendu nedochází.
Velmi impozantní je rozšíření katetrizačních výkonů i na chlopně v mitrální nebo trikuspidální pozici. Bylo referováno o jejich užití u čisté mitrální, trikuspidální nebo pulmonální regurgitace [54]. Pro běžnou praxi asi nejzajímavější novinkou posledních několika let je uplatnění této metody u mitrálních vad s vysokým rizikem operačního výkonu. Ve srovnání s aortální chlopní je však problematika mitrální chlopně podstatně složitější především s ohledem na její komplexní strukturu zahrnující cípy, šlašinky, papilární svaly, anulus a stěnu levé komory. Detailní porozumění celé anatomii, ale i patologii mitrální chlopně spolu s jejich výraznější heterogenitou je podstatně větším problémem, než je situace u aortálního ústí [55]. Katetrizační způsoby řešení byly použity jak u mitrálních stenóz, tak regurgitací, jsou však zprávy o jejich využití i v modu valve-in-valve, především u rizikových nemocných se selhávající mitrální biologickou protézou [56–58]. Podobně byly použity i protézy trikuspidální [59], bylo popsáno dokonce jejich využití i u výrazných kalcifikací v mitrálním prstenci nebo v samotné mitrální chlopni, které jinak představují pro tyto výkony výraznou limitaci [60–62].
Metoda MitraClip
Nejvíce zkušeností je ovšem s metodou MitraClipu u primárních i sekundárních regurgitací [63,64]. Tato katetrizační intervence se využívá opět především u nemocných s vysokým operačním rizikem, např. u sekundárních mitrálních regurgitací při těžké dysfunkci levé komory. V budoucnu se plánuje započetí studií s cílem porovnání efektu MitraClipu oproti kardiochirurgické terapii u nemocných se středním operačním rizikem [63], v současnosti probíhají studie srovnávající nejrůznější parametry ve srovnání s medikamentózní terapií. Řada výsledků vyznívá pro metodu MitraClipu velmi dobře, především u sekundárních regurgitací, do podrobností zde však nelze zacházet. Pokud se jedná o problematiku katetrizačních zákroků u vrozených srdečních vad, pak odkazujeme na speciální literaturu [65].
prof. MUDr. Pavel Gregor, DrSc.
pavel.gregor@fnkv.cz
Kardiocentrum – III. interní-kardiologická klinika 3. LF UK a FN Královské Vinohrady,
Praha
www.fnkv.cz
Doručeno do redakce 21. 3. 2017
Přijato po recenzi 26. 4. 2017
Sources
1. Widimský J. Insuficience aorty. In: Kordač V et al (eds). Vnitřní lékařství I. Avicenum: Praha 1988 : 560–563. ISBN 80–201–0188–8.
2. Vahanian A, Alfieri O, Andreotti F et al. [Joint Task Force on the Management of Valvular Heart Disease of the European Society of Cardiology and the European Association for Cardio-Thoracic Surgery]. Guidelines on the management of valvular heart diseases (Version 2012). Eur Heart J 2012; 33:(19) 2451–2496. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehs109>.
3. Remenyi B, El Guindy A, Smith SC Jr et al. Valvular aspects of rheumatic heart disease. Lancet 2016; 387(10025): 1335–1346. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(16)00547-X>.
4. Zeng Y, Rongrong S, Xianchi L et al. Pathophysiology of valvular heart disease. Exp Ther Med 2016; 11(4): 1184–1188.
5. Čerbák R. Nejčastější chlopenní vady: aortální stenóza a mitrální insuficience. Galén: Praha 2007. ISBN 978–80–7262–523–9.
6. Rezzoug N, Vaes B, de Meester CH et al. The clinical impact of valvular heart disease in a population-based cohort of subjects aged 80 and older. BMC Cardiovac Disord 2016; 16 : 7. Dostupné z DOI: <http://dx.doi.org/10.1186/s12872–016–0184–8>.
7. Shu C, Chen S, Quin TT et al. Prevalence and correlates of valvular heart diseases in the elderly population in Hubei, China. Sci Rep 2016; 6 : 627253. Dostupné z DOI: <http://dx.doi.org/10.1038/srep27253>.
8. Demers P, Beaulieu N. Left atrial myxoma in association with life-saving mitral stenosis. J Thorac Cardiovasc Surg 2012; 143(2): e9-e10. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jtcvs.2011.10.084>.
9. Kirman M, Erdem K, Mercan H et al. Large mobile hemangioma arising from interatrial septum which mimics mitral stenosis. Turk J Thor Cardiovasc Surg 2013; 21 : 434–436.
10. Auer J, Berent R, Gurtner F. „Malignant“ mitral stenosis. J Cardiovasc Surg 2012; 7 : 19. Dostupné z DOI: <http://dx.doi.org/10.1186/1749–8090–7–19>.
11. Wilbring M, Kappert U, Daubner D et al. Metastazing primary arterial leiomyosarcoma causing a functional high-grade mitral stenosis. Heart Surg Forum 2012; 15(2): E108-E110. Dostupné z DOI: <http://dx.doi.org/10.1532/HSF98.20111147>.
12. Singla S, Bansal M, Agarwal A. Mitral stenosis in tuberous sclerosis: A case of dystrophic calcification. J Postgrad Med 2012; 58(2): 167–170. Dostupné z DOI: <http://doi: 10.4103/0022–3859.97192>.
13. Pasca I, Tyagi G, Patel R et al. Malignant natural history of patients with degenerative mitral stenosis: biological predictors of survival in a cohort of 1004 patients. J Am Coll Cardiol 2012; 59(Suppl 13): E1970. Dostupné z DOI: <http://10.1016/S0735–1097(12)61971–8>.
14. Sud K, Agarwal S, Parashar A et al. Degenerative mitral stenosis unmet need for percutaneous interventions. Circulation 2016; 133(16): 1594–1604. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.115.020185>.
15. Rajamannan NM, Evans FJ, Aikawa E et al. Calcific aortic valve disease: not simply a degenerative process: a review and agenda for research from the National Heart and Lung and Blood Institute Aortic Stenosis Working Group. Circulation 2011; 124(16): 1783–1791. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.110.006767>.
16. Abramowitz Y, Jilaihawi H, Chakravarty T et al. Mitral anulus calcification. J Am Coll Cardiol 2015; 66(17): 1934–1941. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2015.08.872>.
17. Kanjanauthai S, Nasir K, Katz R et al. Relationships of mitral annular calcification to cardiovascular risk factors: the Multi-Ethnic Study of Atherosclerosis (MESA). Atherosclerosis 2010; 213(2): 558–562. Dostupné z DOI: <http://dx.doi.org/10.1016/j.atherosclerosis.2010.08.072>.
18. Fox CS, Vasan RS, Parise H et al. Mitral annular calcification predicts cardiovascular morbidity and mortality: the Framingham Heart Study. Circulation 2003; 107(11): 1492–1496.
19. Pasca I, Dang P, Tyagi G et al. Survival in patients with degenerative mitral stenosis: results from a large retrospective cohort study. J Am Soc Echocardiogr 2016; 29(5): 461–469. Dostupné z DOI: <http://dx.doi.org/10.1016/j.echo.2015.12.012>.
20. Ramaraj R, Manrique C, Hashemzadeh H et al. Mitral annulus calcification is independently associated with all-cause mortality. Exp Clin Cardiol 2013; 18(1): e5-e7.
21. Okada Y. Surgical management of mitral annular calcification. Gen Thorac Cardiovasc Surg 2013; 61(11): 619–625. Dostupné z DOI: <http://dx.doi.org/10.1007/s11748–013–0207–7>.
22. Higgins J, Mayo J, Skarsgard P. Cardiac computed tomography facilitates operative planning in patients with mitral calcification. Ann Thorac Surg 2013; 95(1): e9-e11. Dostupné z DOI: <http://dx.doi.org/10.1016/j.athoracsur.2012.07.059>.
23. Silbiger JJ. Anatomy, mechanics, and pathophysiology of the mitral annulus. Am Heart J 2012; 16(2): 163–176. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ahj.2012.05.014>.
24. Elmariah S, Budoff MJ, Delaney JAC et al. Risk factors associated with the incidence and progression of mitral annulus calcification: the Multi-Ethnic Study of Atherosclerosis. Am Heart J 2013; 166(5): 904–912. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ahj.2013.08.015>.
25. Uchimuro T, Fukui T, Shimizu A et al. Mitral valve surgery in patients with severe mitral annular calcification. Ann Thorac Surg 2016; 101(3): 889–895. Dostupné z DOI: <http://dx.doi.org/10.1016/j.athoracsur.2015.08.071>.
26. Katz R, Wong ND, Kronmal R et al. Feature of the metabolic syndrome and diabetes mellitus as predictors of aortic valve calcification in the Multi-Ethnic Study of Atherosclerosis. Circulation 2013; 113(17): 2113–2119. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.105.598086>.
27. Beckmann E, Grau JB, Sainger R et al. Insights into the use of biomarkers in calcific aortic valve disease. J Heart Valve Dis 2010; 19(4): 441–452.
28. Balachandran K, Alfort PW, Wylie-Sears J et al. Cyclic strain induces dual-mode endothelial – mesenchymal transformation of the cardiac valve. Proc Natl Acad Sci USA 2011; 108(50): 19943–19948. Dostupné z DOI: <http://dx.doi.org/10.1073/pnas.1106954108>.
29. Towler DA. Molecular and cellular aspects of calcific aortic valve diabase. Circ Res 2013; 113(2): 198–208. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCRESAHA.113.300155>.
30. Lincoln J, Garg V. Etiology of valvular heart disease – genetic and developmental origins. Circ J 2014; 78(8): 1801–1807.
31. Asgar AW, Mack MJ, Stone GW. Secondary mitral regurgitation in heart failure. J Am Coll Cardiol 2015; 65(12): 1231–1248. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2015.02.009>. Erratum in J Am Coll Cardiol 2015; 65(20): 2265.
32. Gulic TG, Makuc J, Prosen G et al. Pocket-size imaging device as a screening tool for aortic stenosis. Wien Klin Wochenschr 2016; 128(9–10): 348–353. Dostupné z DOI: <http://dx.doi.org/10.1007/s00508–015–0904–6>.
33. Niederle P, Mandysová E. Transezofageální echokardiografie do kapsy. Triton: Praha 2000. ISBN 80–7254–104–8.
34. Gregor P, Línková H. Aortální stenóza. Vnitř Lék 2013; 59(4): 277–283.
35. Gregor P, Línková H. Aortální regurgitace. Vnitř Lék 2013; 59(2): 99–104.
36. Gregor P, Línková H. Mitrální stenóza. Vnitř Lék 2014; 60(4): 304–309.
37. Galli E, Fournet M, Chabbane C et al. Prognostic value of left atrial reservoir fiction in patients with severe aortic stenosis: a 2D speckle-tracking echocardiographic study. Eur Heart J Cardiovasc Imaging 2016; 17(5): 533–541. Dostupné z DOI: <http://dx.doi.org/10.1093/ehjci/jev230>.
38. Dahl JS, Gomes SB, Videbaek L et al. Early diastolic strain rate in relation to systolic and diastolic fiction and prognosis in aortic stenosis. JACC Cardiovasc Imaging 2016; 9(5): 519–528. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jcmg.2015.06.029>.
39. Lee AP, Fang F, Jin ChN et al. Quantification of mitral valve morfology with three-dimensional echocardiography. Circulation Journal 2014; 78(5): 1029–1037.
40. Ngernsritrakul T, Chandrachamnong S, Hul D et al. Novel automated three-dimensional mitral valve area measurement in rheumatic mitral stenosis. J Am Coll Cardiol 2015; 65(10; Suppl 17): A2021.
41. Jone PN, Bremen C, Di Maria M et al. Three-dimensional echocardiography enhances diagnostic accuracy of supramitral ring. Echocardiography 2015; 32(6): 1048–1050. Dostupné z DOI: <http://dx.doi.org/10.1111/echo.12867>.
42. Looi JL, Kerr AJ, Gabriel R. Morphology of congenital and aquired aortic valve disease by cardiovascular magnetic resonance imaging. Eur J Radiol 2015; 84(11): 2144–2154. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ejrad.2015.07.022>.
43. Debonnaire P, Delgado V, Bax JJ. Potential role of fibrosis paging in severe valvular heart disease. Heart 2015; 101(5): 397–407. Dostupné z DOI: <http://dx.doi.org/10.1136/heartjnl-2013–304679>.
44. Kim SS, Ko SM, Song MG et al. Quantification of stenotic mitral valve area and diagnostic accuracy of mitral stenosis by dual-source computed tomography in patients with atrial fibrillation: comparison with cardiovascular magnetic resonance and transthoracic echocardiography. Int J Cardiovasc Imaging 2015; 31(Suppl 1): 103–114. Dostupné z DOI: <http://dx.doi.org/10.1007/s10554–014–0488–7>.
45. Naoum Ch, Leipsic J, Cheung A et al. Mitral annular dimensions and geometry in patients with functional mitral regurgitation and mitral valve prolaps. JACC Cardiovasc Imaging 2016; 9(3): 269–280. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jcmg.2015.08.022>.
46. Aksu HU, Gorgulu S, Diker M et al. Cardiac computed tomography versus echocardiography in the assessment of stenotic rheumatic mitral valve. Echocardiography 2016; 33(3): 346–352. Dostupné z DOI: <http://dx.doi.org/10.1111/echo.13076>.
47. Vojáček J, Dominik J, Žáček P et al. Záchovné operace a plastiky aortální chlopně – od anatomie chlopně až k dlouhodobým výsledkům. Vnitř Lék 2009; 55(2): 117–122.
48. Vahl TP, Kodali SK, Leon MB. Transcatheter Aortic Valve Replacement 2016: A Modern-Day „Through the Looking-Glass“ Adventure. J Am Coll Cardiol 2016; 67(12): 1472–1487. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2015.12.059>.
49. Chakravarty T, Belle EV, Jilaihawi H et al. Meta-analysis of the impact of mitral regurgitation on outcomes after transcatheter aortic valve implantation. Am J Cardiol 2015; 115(7): 942–949. Dostupné z DOI: <http://dx.doi.org/10.1016/j.amjcard.2015.01.022>.
50. Sannino A, Losi MA, Schiattarella GG et al. Meta-analysis of mortality outcomes and mitral regurgitation evolution in 4,839 patients having transcatheter aortic valve implantation for severe aortic stenosis. Am J Cardiol 2014; 114(6): 875–882. Dostupné z DOI: <http://dx.dpo.org/10.1016/j.amjcard.2014.06.022>.
51. van Dijk KG, Wiegerinck EMA, Takama T et al. Mitral regurgitation prior to transcathetetr aortic valve implantation involuences survival but not symptoms. Int J Cardiol 2016; 204 : 95–100. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ijcard.2015.11.129>.
52. Szymanski P, Hryniewiecki T, Dabrowski M et al. Mitral and aortic regurgitation following transcatheter aortic valve replacement. Heart 2016; 102(9): 701–706. Dostupné z DOI: <http://dx.doi.org/10.1136/heartjnl-2015–308842>.
53. Schubert SA, Yarboro LT, Madala S et al. Natural history of coexistent mitral regurgitation after aortic valve replacement. J Thorac Cardiovasc Surg 2016; 151(4): 1032–1039, 1042.e1. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jtcvs.2015.12.006>.
54. Praz P, Windecker S, Huber Ch et al. Expanding indications of transcatheter heart valve interventions CME. JACC Cardiovasc Interv 2015; 8(14): 1777–1796. <http://dx.doi.org/10.1016/j.jcin.2015.08.015>.
55. Tang HGL, Hahn GI, Vinayak BV et al. Transcatheter mitral valve replacement design implications. Potential pitfalls and outcomes assessment. Cardiol Rev 2015; 23(6): 290–296. Dostupné z DOI: <http://dx.doi.org/10.1097/CRD.0000000000000086>.
56. Ahn HC, Baranowski J, Dahlin LG et al. Transvenous implantation of a stent valve in patients with degenerated mitral prostheses and native mitral stenosis. Ann Thorac Surg 2016; 101(6): 2279–2284. Dostupné z DOI: <http://dx.doi.org/10.1016/j.athoracsur.2015.11.019>.
57. Nachum ER, Raanani E, Segev A et al. Transapical transcatheter valve-in-valve implantation for failed mitral valve bioprosthesis. Isr Med Assoc J 2016; 18(1): 13–17.
58. Kliger C, Angulo R, Maranan L et al. Percutanous complete repair of failed mitral valve prosthesis: Simultaneous closure of mitral paravalvular leaks and transcatheter mitral valve implantation. Eurointervention 2015; 10(11): 1336–1345. Dostupné z DOI: <http://dx.doi.org/10.4244/EIJY14M05_01>.
59. Ranney DN, Williams JB, Wang A et al. Valve-in-valve transcatheter valve implantation in the nonaortic position. J Card Surg 2016; 31(5): 282–288. Dostupné z DOI: <http://dx.doi.org/10.1111/jocs.12745>.
60. Koeckert MS, Loulmet DF, Williams MR et al. Robotic transcatheter mitral valve replacement using the Sapien XT in the petting of severe mitral annular calcification. J Card Surg 2016; 31(5): 303–305. Dostupné z DOI: <http://dx.doi.org/10.1111/jocs.12737>.
61. Jain R, Algahim MF, Bajwa TK et al. Native mitral stenosis treated with transcatheter mitral valve replacement. Ann Thorac Surg 2016; 101(3): e75–77. Dostupné z DOI: <http://dx.doi.org/10.1016/j.athoracsur.2015.09.020>.
62. Puri R, Altisent OAJ, del Trigo M et al. Transcatheter mitral valve implantation ofr inoperable severely calcified native mitral valve disease: A systematic review. Catheter Cardiovasc Interv 2016; 87(3): 540–548. Dostupné z DOI: <http://dx.doi.org/10.1002/ccd.26262>.
63. Nishimura RA, Vahanian A, Eleid M et al. Mitral valve disease – current management and future challenges. Lancet. 2016; 387(10025): 1324–1334. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(16)00558–4>.
64. Želízko M, Pořízka V, Kočková R. Katetrizační metoda léčby chronické mitrální regurgitace pomocí mitrální svorky (MitraClip). Vnitř Lék 2014; 60(12): 1090–1094.
65. Sizarov A, Boudjemline Y. Novel materials and device in the transcatheter management of congenital heart disease – the future comes slowly. Arch Cardiovasc Dis. 2016; 109(4): 278–285. Dostupné z DOI: <http://dx.doi.org/10.1016/j.acvd.2015.12.002>.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2017 Issue 5-
All articles in this issue
- Současný pohled na ivabradin v léčbě kardiovaskulárních onemocnění
- Osteoprotektivní léčba bisfosfonáty nebo denosumabem u nemocných s mnohočetným myelomem: přínos a rizika
- Zamyšlení nad chlopenními vadami včera a dnes
- Čo nám hovorí klinická štúdia GLAGOV?
- Novinky v léčbě hypertenze a dyslipidemie
- Záchrana diabetické nohy komplexní individualizovanou léčbou diabetika 2. typu: kazuistika
- Akutní lymfoblastická leukemie dospělých – případ dlouhého došetřování bolestí kyčlí s překvapivým závěrem: kazuistika
- Cévní ektázie žaludečního antra a syndrom solitárního rektálního vředu – dvě vzácné diagnózy jako příčina anémie u téhož pacienta: kazuistika
- Je to znovu střevní tuberkulóza? Kazuistika
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Osteoprotektivní léčba bisfosfonáty nebo denosumabem u nemocných s mnohočetným myelomem: přínos a rizika
- Akutní lymfoblastická leukemie dospělých – případ dlouhého došetřování bolestí kyčlí s překvapivým závěrem: kazuistika
- Je to znovu střevní tuberkulóza? Kazuistika
- Zamyšlení nad chlopenními vadami včera a dnes
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

