-
Medical journals
- Career
Nepravidelnosti dýchání při spiroergometrickém vyšetření – od mírné nepravidelnosti dechového vzoru až po periodické dýchání typu oscilující ventilace
Authors: František Várnay; Leona Mífková; Pavel Homolka; Petr Dobšák
Authors‘ workplace: Klinika tělovýchovného lékařství a rehabilitace LF MU a FN u sv. Anny v Brně
Published in: Vnitř Lék 2017; 63(3): 175-182
Category: Reviews
Overview
Kolísavý průběh dechového objemu (VT), dechové frekvence (DF) a minutové ventilace (VE) při spiroergometrickém vyšetření rampovým protokolem se vyskytuje nejen u nemocných, ale relativně často i u zdravých osob. Může vysvětlit řadu nepravidelností průběhu křivek příjmu kyslíku (VO2), výdeje oxidu uhličitého (VCO2) a zejména křivek ventilačních ekvivalentů pro O2 a CO2 (EQO2, EQCO2) a též křivek parciálních tlaků O2 a CO2 na konci výdechu (PETO2, PETCO2), které se používají mimo jiné i ke stanovení ventilačních prahů. Přítomnost oscilujícího dýchání při zátěži (EOV) odráží závažnost srdečního selhání a je nezávislým prediktorem zvýšené morbidity, kardiální i celkové mortality a náhlé smrti z kardiálních příčin. V současné době ale není k dispozici všeobecně akceptovaná univerzální definice EOV, užívají se různá kritéria. Nenašli jsme porovnání, zda a jak se liší „síla“ prognostického kritéria pro EOV stanoveného dle různých metod. Je proto velmi důležité uvést, jakou metodou, respektive podle jakých kritérií byla EOV stanovena.
Klíčová slova:
dechový vzor – EOV – oscilující dýchání při zátěži – periodické dýcháníÚvod
V tab. 1 je uveden abecedně řazený seznam některých zkratek použitých v této práci.
Minutová ventilace (VE) je součinem dechového objemu (VT) a dechové frekvence (DF). Platí vztah VE = VT × DF. Klidová minutová ventilace bývá kolem 6–10 l/min a je závislá na antropometrických parametrech člověka, na DF a VT.
Předpokladem dokonalé výměny plynů je dobrá souhra mezi ventilací a perfuzí (průtokem krve kolem alveolů). Při asi 300–400 milionech alveolů však nelze dokonalý vzájemný poměr očekávat ani za normálních okolností. Vztah mezi ventilací a perfuzí se běžně uvádí jako ventilačně-perfuzní poměr a označuje se V/Q. Přesněji se jedná o poměr alveolární ventilace (VA) k plicní perfuzi. V plicích existuje autoregulace. Při nedostatečné perfuzi některé oblasti plic dochází k lokální bronchokonstrikci a odklonu ventilace do lépe perfundované oblasti. Analogicky při nedostatečné ventilaci dochází k lokální vazokonstrikci plicních cév a odklonu perfuze do dobře ventilovaných oblastí. Rovnováha mezi ventilací a perfuzí je udržována především lokálním autoregulačním mechanismem na úrovní bronchiol a prekapilár.
Při regulaci dýchání se na výsledné minutové ventilaci může dechová frekvence a dechový objem podílet různě. Stejná minutová ventilace VE (např. 30 l/min) může být dosažena málo zrychleným prohloubeným dýcháním (DF = 20 dechů/min a VT = 1,5 l) nebo velmi rychlým mělkým dýcháním (DF = 40 dechů/min a VT = 0,75 l) s odlišnou velikostí ventilace mrtvého prostoru. Při anatomickém mrtvém prostoru 250 ml a DF 20 dechů/min je ventilace tohoto prostoru 20krát 250 ml = 5 l/min, při DF 40 dechů/min je to 10 l/min z výše uvedené celkové VE = 30 l/min. Pro velikost dechové práce hraje významnou roli dechový vzor (jedinečná kombinace trvání inspiria a exspiria, objemů a průtoků, resp. DF a VT, ze kterých sestává ventilace) a velikost mrtvého prostoru. Z hlediska dechové práce (kontrakční síly dechových svalů) je optimální taková DF, při které se dané úrovně alveolární ventilace dosáhne s nejmenší prací.
Table 1. Vybrané užité zkratky 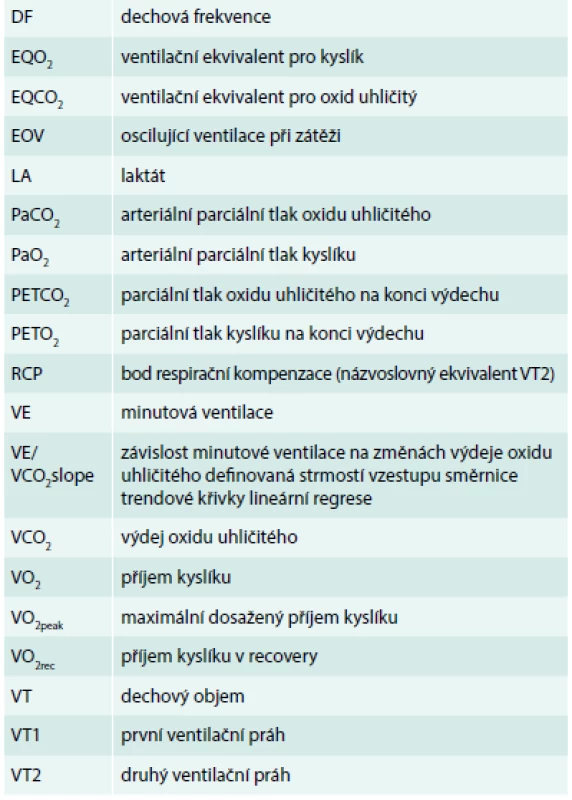
Regulace dýchání
Regulace dýchání má komplexní charakter. Při normální funkci ledvin je cílem udržet arteriální parciální tlak oxidu uhličitého (PaCO2) a/nebo pH na téměř konstantní úrovni a zajistit dostatečný příjem kyslíku. Základem je chemoreflex se zpětnou vazbou, jehož základní řídící veličinou je PaCO2, H+ ionty a případně též arteriální parciální tlak kyslíku (PaO2). Hodnoty PaO2, PaCO2 a pH jsou snímány periferními a centrálními chemoreceptory a signály jsou předávány respiračním centrům v prodloužené míše a pons Varoli. Na základě informací z chemoreceptorů je v respiračních centrech vytvářen základní dechový vzor, který je modulován zejména vlivem CNS, signály z ergoreceptorů ve svalech, receptorů v plicích a dalších oblastí. Tím je v respiračním centru vytvořen vzruch pro aktivaci dýchacích svalů definující délku a hloubku inspiria a exspiria a dechovou frekvenci. Výsledkem činnosti dýchacích svalů je vytvoření určitého dechového objemu při určité dechové frekvenci, tedy minutová ventilace. Na výsledných hodnotách PaO2 a PaCO2 se při momentální alveolární ventilaci podílí krevní oběh (perfuze) a difuze přes alveolokapilární membránu. Alveolární ventilací dosažené hodnoty PaO2, PaCO2, pH jsou potom znovu a permanentně kontrolovány receptory a probíhá nový cyklus řízení ventilace cestou chemoreflexu, a tak je zajištěna včasná reakce na měnící se situaci.
Při svalové práci se zvyšuje příjem kyslíku a produkce oxidu uhličitého. Zajištění výměny plynů je realizováno současným zvýšením plicní ventilace a průtoku krve v plicním oběhu a v pracujících svalech. Vzhledem k tomu, že k vzestupu plicní ventilace dochází bezprostředně po zahájení svalové práce, je zřejmé, že se na tom podílí vlivy z CNS. Také aktivace ergoreceptorů v pracujících svalech je současně impulzem pro stimulaci respiračního centra. Chemické podněty pak upřesňují regulaci dýchání. Vliv mozkové kůry na tato centra je v průběhu života modulován procesem učení.
Průběh dechového vzoru (dechového objemu, dechové frekvence a ventilace) při spiroergometrickém testu s kontinuálně se zvyšující zátěží (rampový protokol)
Při kontinuálně se zvyšující zátěži typu rampového protokolu je produkované množství CO2 zpočátku (při nízké zátěži) výsledkem aerobního metabolizmu. Nad prvním ventilačním prahem (VT1) postupně přibývá k aerobnímu metabolizmu i anaerobní (anaerobní glykolýza) s narůstající produkcí laktátu (LA), a tím i koncentrací vodíkových iontů. Vodíkové ionty (H+) jsou v nárazníkovém systému vychytávány za vzniku dalšího CO2, který se přidává k metabolicky vznikajícímu CO2. Při zvyšujícím VCO2 se úměrně lineárně zvyšuje VE až do bodu respirační kompenzace (RCP) jako projev řízení ventilace hodnotou CO2 v krvi. Až v místě RCP neboli druhého ventilačního prahu (VT2) je kapacita nárazníkového systému vyčerpaná. Při stále se zvyšující zátěži pokračuje vzestup produkce LA a v souvislosti s tím úměrně narůstá koncentrace H+, které už nemohou být nárazníkovým systémem odstraňovány. Při nadbytku H+ se snižuje pH a vzniká metabolická (laktátová) acidóza. Pokles pH při acidóze je detekován chemoreceptory (periferními) a stává se rozhodujícím parametrem regulace dýchání (převáží nad vlivem PaCO2). Od VT2 tedy řízení ventilace přebírají H+ ionty (acidóza), protože udržení pH v přijatelných mezích je pro správnou funkci enzymatických systémů již životně důležitou prioritou. Aktivují se respirační centra v mozkovém kmeni ke zvýšení alveolární ventilace a dochází k hyperventilaci, tedy respirační kompenzaci metabolické acidózy (zvětší se výdej oxidu uhličitého VCO2 a klesá PaCO2).
Ukázky různých dechových vzorů
Na grafu 1, který ukazuje normální průběh VE, DF a VT při spiroergometrii, je vidět, že při nízké zátěži je zvyšování VE dosaženo primárně zvětšujícím se dechovým objemem, zrychlení dechové frekvence je méně výrazné.
Graph 1. Normální průběh minutové ventilace, dechové frekvence a dechového objemu při kontinuálním vzestupu zátěže při spiroergometrickém vyšetření 
VE – minutová ventilace DF – dechová frekvence VT – dechový objem Až později, obvykle v poslední třetině zátěžové fáze, jsou možnosti dalšího zvýšení dechového objemu limitovány a minutová ventilace se zvyšuje spíše zrychlením dechové frekvence. DF na vrcholu zátěže obvykle dosahuje 34–46 dechů/min, málokdy překročí 55 dechů/min (s výjimkou sportovců nebo osob s restrikčním plicním onemocněním) [2]. Na grafu 1 je vidět, že při vyšší dechové frekvenci se dechový objem již snižuje, i když se celková minutová ventilace dále zvyšuje. Jedinou „abnormalitou“ na grafu 1 je krátké emoční tachypnoe na začátku vyšetření, tj. dechová frekvence kolem 40 dechů/min, ale další průběh je už normální.
Regulace dýchání je velmi složitý proces, proto se nelze divit, že i u zdravých lidí je zcela pravidelné dýchání při zátěži spíše výjimkou. Často se setkáváme s kolísáním VT a DF různého stupně. Toto kolísání se může vzájemně dobře a úplně korigovat, takže se na výsledné minutové ventilaci neprojeví žádné nebo jen mírné nepravidelnosti (graf 2).
Graph 2. Abnormální dechový vzor: při zřetelném kolísání dechové frekvence a dechového objemu jsou přítomny jen mírné nepravidelnosti minutové ventilace 
VE – minutová ventilace DF – dechová frekvence VT – dechový objem Graf 2 ukazuje abnormální dechový vzor s výrazným diskordantním kolísáním VT a DF s jen částečnou vzájemnou korekcí. Výsledná VE je primárně ovlivněna (řízena) směrem a velikostí výkyvu VT. V době mezi 420.–480. s je vzestup VT nedostatečně korigován poklesem DF, což vede k dočasné hyperventilaci, která ale nemá charakter klasické vzestupně-sestupné oscilace. V navazujícím úseku mezi 480.–540. s je naopak zřetelný výrazný pokles VT, který není dostatečně korigován velikostí zrychlení DF, což vede v uvedeném úseku k dočasné hypoventilaci. Nepravidelnosti výsledné VE jsou viditelné, ale nevelké. Nesplňují kritéria periodického dýchání, schází pravidelné oscilace VE s dostatečnou amplitudou. Dechový vzor s kolísáním VT ale vede k velmi výraznému kolísání křivek PETO2 i PETCO2 (graf 3). Na grafu 4 je pro porovnání zobrazen normální průběh křivek PETO2 a PETCO2 s vyznačením VT1 a VT2 u jiné (zdravé) osoby, kde nejsou žádné oscilace.
Graph 3. Kolísání křivek parciálního tlaku kyslíku a oxidu uhličitého na konci výdechu (PETO2 a PETCO2) 
PETO2 – parciální tlak kyslíku na konci výdechu PETCO2 – parciální tlak oxidu uhličitého na konci výdechu Graph 4. Vzorový průběh křivek parciálního tlaku kyslíku a oxidu uhličitého na konci výdechu (PETO2 a PETCO2) 
PETO2 – parciální tlak kyslíku na konci výdechu PETCO2 – parciální tlak oxidu uhličitého na konci výdechu Graf 5 ukazuje další příklad abnormálního průběhu DF, VT a VE v zátěžové fázi spiroergometrického vyšetření. Primárně kolísá DF (konkordantně s VE), která není korigovaná protichůdným kolísáním VT, což vede k periodickému kolísaní VE. Periodické kolísání DF, VT a VE se vyskytuje jen do úrovně druhého ventilačního prahu (VT2). Na konci zátěžové fáze již oscilace vymizely. Při popisu oscilační vlny jsou nejnižší lokální body oscilace obecně pojmenovány jako nadir (nejnižší bod na začátku oscilační vlny je označen jako nadir1, na konci jako nadir2). Černá silná svislá úsečka zobrazuje amplitudu oscilace (v době mezi 360.–420. s), přerušovaná křivka spojnici nadir bodů. Délka cyklu se měří jako vzdálenost obou nadir. Zobrazená křivka splňuje kritéria oscilatorní ventilace při zátěži (EOV) dle Společného odborného doporučení Evropské asociace pro kardiovaskulární prevenci a rehabilitaci (EACPR) a Americké kardiologické společnosti (AHA) – EACPR/AHA Joint Scientific Statement [3,4], avšak ne přísnější kritéria ostatních metod [5–7].
Graph 5. Abnormální dechový vzor s periodickým kolísáním dechového objemu, dechové frekvence a minutové ventilace 
VE – minutová ventilace DF – dechová frekvence VT – dechový objem VEneosc – spojnice nadir bodů Ampl – amplituda oscilační vlny Přehled abnormalit dýchání
U závažnějšího chronického srdečního selhání (CHSS) se při svalové námaze může vyskytovat relativní hyperventilace, kterou lze při spiroergometrickém vyšetření kvantifikovat určením ventilační třídy dle VE/VCO2 slope. Dalším projevem narušené regulace dýchání u CHSS mohou být různé formy abnormalit dechového vzoru od mírných změn až po oscilační typ dýchání. Obecně by se mělo rozlišovat mezi nepravidelným dýcháním a periodickým (cyklickým) dýcháním. Periodické dýchání je charakterizované pravidelně, cyklicky se opakujícími oscilacemi hodnot VE.
Tématem článku jsou abnormality dýchání při spiroergometrickém zátěžovém vyšetření, ale kvůli komplexnosti je uveden i stručný přehled abnormalit dýchání nesouvisejících se zátěžovým testem.
Periodické dýchání s apnoe
Klasickým příkladem je Cheyneovo-Stokesovo dýchání. Vyskytuje se u pacientů s pokročilým srdečním selháním. Objevuje se jak během bdění, tak ve spánku. Je charakterizováno typickými crescendo-decrescendo oscilacemi dýchání (tachypnoe a hyperpnoe), které jsou v pravidelných intervalech přerušovány apnoickými (event. hypopnoickými) pauzami. Bylo prokázáno, že je velmi silným negativním prognostickým faktorem.
Periodické dýchání s apnoe ve spánku (tzv. sleep apnoe) je charakterizováno absencí průtoku vzduchu trvající nejméně 10 s. Podle přítomnosti nebo absence pohybu hrudníku se rozlišuje typ s obstrukcí (obstructive sleep apnea – OSA) způsobený obstrukcí dýchacích cest (tedy mechanickou překážkou, způsobenou kolapsem až uzávěrem dýchacích cest) a typ bez obstrukce (central sleep apnea – CSA).
Periodické (oscilující) dýchání bez apnoe
Periodické dýchání bez apnoe vyskytující se v klidovém stavu, tedy bez zátěže (tzv. awake PB), není u pacientů s mírnou až střední tíží srdečního selhání nepříznivým ukazatelem prognózy [8].
Periodické (oscilující) dýchání při zátěži
Hlavním cílem práce je popis periodického dýchání objevujícího se během fyzické zátěže. Je označováno různými výrazy a zkratkami: exercise-related periodic breathing (EPB) [5], exercise oscillatory breathing (EOB), nověji jako exercise oscillatory ventilation (EOV). Je bez apnoických pauz, není to Cheyneovo-Stokesovo dýchání.
Do skupiny EOV nepatří oscilace dýchání zjištěné pouze v klidu, ve spánku a při kontinuální zátěži v rovnovážném stavu (steady-state exercise).
Pro potvrzení přítomnosti EOV musí být splněna určená definiční kritéria, která jsou uvedena níže. Dosud není dostupné spolehlivé automatické vyhodnocení přítomnosti EOV během spiroergometrického vyšetření, proto se analýza provádí obvykle vizuálně a manuálně, což může být časově náročné a vést k nepřesnostem.
Přehled základních variant kritérií definujících oscilující dýchání při zátěži
Cornelis et al [9] v přehledné práci na základě analýzy 75 studií uvádějí 4 původní metody definující EOV podle Kremser et al (1987) [10], Leite et al (2003) [5], Ben-Dov et al (1992) [6] a Sun et al (2010) [7] a jejich modifikace. Navíc v písemnictví byly použity i jejich kombinace. Podrobný rozbor a porovnání uvedených metod již přesahuje možnosti a cíl tohoto článku; zájemce odkazujeme na níže uvedené literární zdroje.
V současné době není k dispozici všeobecně akceptovaná univerzální definice EOV. Z celé řady kritérií v různých studiích byla pro definici EOV ve Společném odborném doporučení Evropské asociace pro kardiovaskulární prevenci a rehabilitaci (EACPR) a Americké kardiologické společnosti (AHA) – EACPR/AHA Joint Scientific Statement [3,4,11] – vybrána tato kritéria: EOV je definována jako oscilační vzor dýchání, který může být již v klidové fázi a trvá ≥ 60 % zátěžového testu s amplitudou ≥ 15 % průměrné klidové hodnoty VE. Doporučuje se 10sekundové zprůměrování dat pro grafické zobrazení. EOV reflektuje závažnost onemocnění a špatnou prognózu pacientů. Za žádných okolností se nejedná o normální ventilační reakci na zátěž.
Je však nutno upozornit, že kritéria pro stanovení EOV se podle jednotlivých metod významně liší hlavně ve velikosti požadované (minimální) amplitudy. Liší se ale i v druhém klíčovém kritériu, zda se amplituda porovnává s klidovou VE [3,4] nebo s průměrnou VE v rámci analyzované oscilace [6,7], případně je definovaná absolutní hodnotou 5 l/min [5]. Nejméně přísná kritéria pro velikost amplitudy jsou uvedena v EACPR/AHA Joint Scientific Statement (amplituda oscilace VE ≥ 15 % průměrné klidové hodnoty VE, což by při klidové hodnotě VE 10 l/min odpovídalo limitní amplitudě 1,5 l/min) [3,4]. Nejpřísnější kritéria pro velikost amplitudy oscilace má Leite (≥ 5 l/min) [5]. Limitní kritérium zvolené pro EOV dle EACPR/AHA Joint Scientific Statement [3,4] je tedy výrazně nižší (kolem 1,5 l/min), což je méně než třetina z požadovaného limitu 5 l/min, který uvádí Leite [5]. Podle kritérií uvedených v EACPR/AHA Joint Scientific Statement bude EOV stanovena i u pacientů s významně menší velikostí oscilační amplitudy, tedy častěji.
Je prokázáno, že EOV odráží závažnost srdečního selhání a nepříznivou prognózu, ale nenašli jsme porovnání, zda a jak se liší „síla“ prognostického kritéria pro EOV stanovené dle různých metod.
Graf 6 ukazuje extrémní oscilace VT, DF a VE splňující kritéria periodického (oscilujícího) dýchání při zátěži (EOV) dle všech metod.
Graph 6. Oscilující dýchání při zátěži (EOV) 
VE – minutová ventilace DF – dechová frekvence VT – dechový objem spojnice nadir – spojnice všech lokálních nadir bodů Ampl – amplituda oscilační vlny V zátěžové fázi jsou 4 oscilace VE; největší oscilace VE jsou od 10. až do 150. s a od 150. až do 260. s. Primárně jsou vyvolány velkými oscilacemi VT nekorigovanými poklesem DF (v té době je DF 11, resp. 14 dechů/min, takže významné snížení DF je málo reálné). Klidová VE je 10,5 l/min. Amplituda první oscilace v zátěžové fázi je zobrazena černou silnou vertikální úsečkou spojující peakVE oscilační vlny a časově příslušný bod spojnice nadir1 a nadir2. Amplituda oscilace je zde 20 l/min. Spojnice všech lokálních minimálních hodnot oscilací (nadir bodů) je zobrazena přerušovanou čarou. Na obrázku je zobrazena jen analýza první oscilační vlny, ale pro komplexní posouzení EOV je nutná analýza 2–3 oscilací (dle zvolené metody).
Prognostický význam EOV u CHSS
U CHSS s redukovanou i zachovalou ejekční frakcí je přítomnost abnormality ventilace charakteru periodického dýchání při zátěži (EOV) nezávislým prediktorem zvýšené morbidity, kardiální i celkové mortality a náhlé smrti z kardiálních příčin [12–17]. Je nezávislý na dalších prognostických ukazatelích získaných při spiroergometrickém vyšetření, jako je nízká hodnota VO2peak, zvýšené VE/VCO2 slope a výrazně zpomalená kinetika VO2 v recovery (pokles příjmu kyslíku z VO2peak během 2 min recovery menší než o 30 %). Přítomnost EOV znamená zařazení do horší, nejméně III. ventilační třídy, přestože by dle VE/VCO2 slope a VO2peak bylo možné zařazení do lepší ventilační třídy. Pro posouzení prognózy podle EOV, VE/VCO2 slope a VO2 v recovery (VO2rec) stačí spiroergometrické vyšetření ukončené při submaximální zátěži na rozdíl od stanovení VO2peak, kde je žádoucí plné metabolické vytížení, což u pokročilých forem CHSS není vždy možné. EOV představuje 3krát vyšší riziko při porovnání s pacienty bez EOV. Prognózu výrazně zhoršuje koincidence EOV se zvýšeným VE/VCO2 slope, nízkým VO2peak a významně prodlouženou kinetikou VO2rec. Ukazuje se, že výskyt EOV je za určitých okolnosti reverzibilní – např. po srdečních operacích, po transplantaci srdce, po 3měsíčním tréninku v rámci kardiovaskulární rehabilitace [18,19] a některých medikamentech.
Závěr
Různé typy kolísavého průběhu VT, DF a VE se vyskytují nejen u nemocných, ale relativně často i u zdravých osob, a dokonce i u sportovců. Pokud graf dechového vzoru není konstantní součástí 9panelového zobrazení grafů poskytovaných softwarem výrobce, je možným východiskem export dat do softwarové aplikace (např. MS Excelu) umožňující vytvořit tento graf a jeho analýzu. Podle našeho názoru by ale graf dechového vzoru měl patřit do základní sady grafů vytvářených softwarem výrobců spiroergometrie. Může vysvětlit řadu nepravidelností průběhu křivek VO2, VCO2 a zejména křivek ventilačních ekvivalentů pro O2 a CO2 (EQO2, EQCO2) a též křivek parciálních tlaků O2 a CO2 na konci výdechu (PETO2, PETCO2). Bez znalosti případných abnormalit dechového vzoru by mohlo docházet k nesprávné interpretaci uvedených křivek a tím, mimo jiné, k nesprávné lokalizaci ventilačních prahů. V současné době není k dispozici všeobecně akceptovaná univerzální definice EOV, užívají se různá kritéria. Je prokázáno, že EOV odráží závažnost srdečního selhání. Přítomnost EOV je nezávislým prediktorem zvýšené morbidity, kardiální i celkové mortality a náhlé smrti z kardiálních příčin. Nenašli jsme ale porovnání, zda a jak se liší „síla“ prognostického kritéria pro EOV stanoveného dle různých metod. Je proto velmi důležité uvést, jakou metodou, respektive podle jakých kritérií byla EOV stanovena.
prim. MUDr. František Várnay, CSc.
varnay@seznam.cz
Klinika tělovýchovného lékařství a rehabilitace LF MU a FN u sv. Anny v Brně
www.fnusa.cz
Doručeno do redakce 7. 12. 2016
Přijato po recenzi 20. 1. 2017
Sources
1. Paleček F. Patofyziologie dýchání. 2.ed. Academia: Praha 1999. ISBN 80–200–0723–7.
2. Wasserman K, Hansen JE, James E et al. Principles of Exercise Testing and Interpretation. Including Pathophysiology and Clinical Applications. 5th ed. Lippincott Williams and Wilkins: Philadelphia 2012. ISBN 978–1609138998.
3. Guazzi M, Adams V, Conraads V et al. EACPR/AHA Scientific Statement. Clinical Recommendations for Cardiopulmonary Exercise Testing Data Assessment in Specific Patient Populations. Eur Heart J 2012; 33(23): 2917–2927. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehs221>.
4. Guazzi M, Ross A, Halle M et al. EACPR/AHA Scientific Statement. 2016 Focused Update: Clinical Recommendations for Cardiopulmonary Exercise Testing Data Assessment in Specific Patient Populations. Circulation 2016; 133(24): e694-e711. Dostupné z DOI: <http://dx.doi.org/10.1161/CIR.0000000000000406>.
5. Leite JJ, Mansur AJ, de Freitas HFG et al. Periodic Breathing During Incremental Exercise Predicts Mortality in Patients With Chronic Heart Failure Evaluated for Cardiac Transplantation. J Am Coll Cardiol 2003; 41(12): 2175–2188.
6. Ben-Dov I, Sietsema KE, Casaburi R et al. Evidence that circulatory oscillations accompany ventilatory oscillations during exercise in patients with heart failure. Am Rev Respir Dis 1992; 145(4 Pt 1): 776–781.
7. Sun XG, Hansen JE, Beshai JF et al. Oscillatory Breathing and Exercise Gas Exchange Abnormalities Prognosticate Early Mortality and Morbidity in Heart Failure. J Am Coll Cardiol 2010; 55(17): 1814–1823. Dostupné z DOI:<http://dx.doi.org/10.1016/j.jacc.2009.10.075>.
8. Koike A, Shimizu N, Tajima A et al. Relation between oscillatory ventilation at rest before cardiopulmonary exercise testing and prognosis in patients with left ventricular dysfunction. Chest 2003; 123(2): 372–379.
9. Cornelis J, Beckers P, Vanroy CH et al. An overview of the applied definitions and diagnostic methods to assess exercise oscillatory ventilation – A systematic review. Int J Cardiol 2015; 190 : 161–169. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ijcard.2015.04.111>.
10. Kremser CB, O´Toole MF, Leff AR. Oscillatory hyperventilation in severe congestive heart failure secondary to idiopathic dilated cardiomyopathy or to ischemic cardiomyopathy. Am J Cardiol 1987; 59(8): 900–905.
11. Corra U. Exercise oscillatory ventilation in heart failure. Int J Cardiol 2016; 206(Suppl): S13-S15. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ijcard.2016.02.122>.
12. Dhakal BP, Lewis GD. Exercise oscillatory ventilation: Mechanisms and prognostic significance. World J Cardiol 2016; 8(3): 258–266. Dostupné z DOI: <http://dx.doi.org/10.4330/wjc.v8.i3.258>.
13. Corra U, Giordano A, Bosimini E et al. Oscillatory Ventilation During Exercise in Patients With Chronic Heart Failure. Clinical Correlates and Prognostic Implications. Chest 2002; 121(5): 1572–1580.
14. Guazzi M, Arena R, Ascione A et al. Exercise oscillatory breathing and increased ventilation to carbon dioxide production slope in heart failure: An unfavorable combination with high prognostic value. Am Heart J 2007; 153(5): 859–867.
15. Guazzi M, Raimondo R, Vicenzi M et al. Exercise Oscillatory Ventilation May Predict Sudden Cardiac Death in Heart Failure Patients. J Am Coll Cardiol 2007; 50(4): 299–308.
16. Kroidl RF, Swarz S, Lehnigk B. Kursbuch Spiroergometrie. Technik und Befundung verständlich gemacht. 3rd ed. Georg Thieme Verlag: Stuttgart 2014. ISBN (print) 9783131434432. ISBN (on-line) 9783131952035.
17. Murphy RM, Shah RV, Malhotra R et al. Exercise Oscillatory Ventilation in Systolic Heart Failure. An Indicator of Impaired Hemodynamic Response to Exercise. Circulation 2011; 124(13): 1442–1451. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.111.024141>.
18. Zurek M, Corra U, Piepoli MF et al. Exercise training reverses exertional oscilatory ventilation in heart failure patients. Eur Respir J 2012; 40(5): 1238–1244. Dostupné z DOI: <http://dx.doi.org/10.1183/09031936.00167011>.
19. Mífková L, Várnay, P, Homolka et al. Vyhodnocení kinetiky VO2 v zotavovací fázi spiroergometrického vyšetření u kardiologicky nemocných – význam a klasifikace. Vnitř Lék 2017; 63(2): 107–113.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2017 Issue 3-
All articles in this issue
- Možnosti efektivní edukace v diabetologii – návod pro edukátory
- Nepravidelnosti dýchání při spiroergometrickém vyšetření – od mírné nepravidelnosti dechového vzoru až po periodické dýchání typu oscilující ventilace
- Přínos CT kolografie v klinické praxi
- Diabetes mellitus 2. typu a chronická obličková choroba
-
Význam zobrazení srdce pomocí magnetické rezonance v diagnostice hypertrofické kardiomyopatie
Část I - Kardiovaskulární komplikace nádorů a jejich léčby
- Komentár k aktuálnym odporúčaniam v liečbe diabetu 2. typu
- Radiofrekvenční katétrová ablace pro fibrilaci síní prováděná v celkové anestezii: výsledky unicentrické randomizované studie
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Přínos CT kolografie v klinické praxi
- Možnosti efektivní edukace v diabetologii – návod pro edukátory
- Radiofrekvenční katétrová ablace pro fibrilaci síní prováděná v celkové anestezii: výsledky unicentrické randomizované studie
- Nepravidelnosti dýchání při spiroergometrickém vyšetření – od mírné nepravidelnosti dechového vzoru až po periodické dýchání typu oscilující ventilace
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

