-
Medical journals
- Career
Dlouhodobá léčba tromboembolické nemoci u pacientů se zhoubným nádorem
Authors: Jan Šmrha 1,2; Petr Kessler 3; Hynek Poul 3; Michaela Harudová 3
Authors‘ workplace: Interní oddělení Nemocnice Pelhřimov, p. o. 1; Kardiologické oddělení Nemocnice Jihlava, p. o. 2; Oddělení hematologie a transfuziologie Nemocnice Pelhřimov p. o. 3
Published in: Vnitř Lék 2016; 62(6): 449-452
Category: Original Contributions
Overview
Úvod:
U pacientů léčených pro tromboembolickou nemoc asociovanou s nádorem (TENAN) je doporučena léčba nízkomolekulárním heparinem (LMWH) po dobu prvních 6 měsíců; iniciální terapeutická dávka může být po uplynutí 1 měsíce redukována na 60–75 %. Po 6 měsících by měla být terapie přehodnocena a následná léčba LMWH nebo warfarinem by měla být podávána nejméně do doby vyléčení nádoru nebo vzniku závažné kontraindikace. Cíle: Zjistit použití léčebných modalit po uplynutí 6 měsíců od diagnózy TENAN ve vztahu k průběhu nádorového onemocnění.Sledovaná skupina:
87 pacientů (49 mužů a 38 žen) ve věku 27–87 let (průměrný věk 64 let) s léčených pro TENAN.Metodika:
Pacienti byli prospektivně sledováni během léčby TENAN. Bylo analyzováno zastoupení pacientů, u nichž byl LMWH nahrazen warfarinem během prvních 6 měsíců a během celého sledování ve vztahu k průběhu nádorového onemocnění. Ke statistickému zhodnocení byly použity testy χ2 a χ2 s Yatesovou korekcí.Výsledky:
Medián doby sledování od vzniku trombózy byl 445 dnů, průměrná doba sledování 743 dnů. 6 měsíců po diagnóze trombózy 9/30 (30 %) pacientů v kompletní remisi (CR) bylo léčeno warfarinem, zatímco pouze 3 z 12 (25 %) v parciální remisi (PR); 0 z 9 se stabilním onemocněním (SD) a 1 ze 13 s progresí onemocnění (7,7 %) byl léčen warfarinem. Pacienti v kompletní remisi a v parciální remisi byli léčeni warfarinem častěji než pacienti se stabilním či progredujícím nádorovým onemocněním (P = 0,02). Během celého sledování 25/30 (83,3 %) pacientů, jejichž nádor byl v 6 měsících od diagnózy trombózy v CR, bylo převedeno na warfarin, zatímco jenom 5/12 (41,7 %), 1/9 (11,1 %) a 1/13 (7,7 %) pacientů v PR, SD a progresi bylo převedeno na warfarin. Podíl pacientů v CR, převedených na warfarin, byl vyšší než podíl pacientů v PR (P = 0,007), v SD (P = 0,0003) a s progresí nádoru (P < 0,0001). Medián času od diagnózy trombózy do převodu z LMWH na warfarin byl u pacientů, kteří byli v 6 měsících v CR, 219 dnů a nebyl dosažen u pacientů, kteří v 6 měsících nebyli v CR.Závěr:
Průběh maligního onemocnění je důležitým faktorem ve výběru léčebné strategie TENAN po 6 měsících i v následném období. Pacienti v kompletní remisi jsou častěji převedeni na léčbu warfarinem.Klíčová slova:
nízkomolekulární heparin – tromboembolická nemoc – warfarin – zhoubný nádorÚvod
Riziko žilního tromboembolizmu je u pacientů s maligním onemocněním 4krát větší než u zdravé populace [1], s paraneoplastickou žilní trombózou/plicní embolií se tedy v běžné praxi setkáváme často, přesto dostupných dat o optimální léčebné strategii je relativně málo.
Na nutnost hledání vhodnější antikoagulační léčby u pacientů s tromboembolickou nemocí asociovanou s nádorem (TENAN) upozornila v roce 2000 studie Palaretiho et al, která u pacientů se zhoubným nádorem léčených warfarinem prokázala významně vyšší výskyt krvácivých komplikací a statisticky nevýznamný trend k většímu výskytu trombotických komplikací oproti pacientům bez malignity [2].
Dle aktuálních evropských guidelines pro léčbu plicní embolie z roku 2014 se v úvodních 3–6 měsících podává nízkomolekulární heparin (LMWH) [3]. Tato léčebná strategie vede k signifikantnímu poklesu rekurence tromboembolické nemoci oproti skupině pacientů léčených warfarinem bez současného zvýšení rizika krvácivých komplikací [4,5].
O optimální léčbě po prvních 6 měsících léčby je v této době k dispozici poměrně malé množství dat, doporučení Evropské kardiologické společnosti (ESC guidelines) udávají následné léčebné možnosti: pokračování v léčbě LMWH, převedení pacienta na terapii warfarinem nebo ukončení antikoagulační léčby. Výběr konkrétní léčebné strategie má být učiněn individuálně v závislosti na úspěšnosti dosud podávané léčby, odhadu rizika rekurence, rizika krvácivých komplikací a preferenci pacienta.
Cíle
Cílem naší práce bylo analyzovat zastoupení různých léčebných strategií TENAN po uplynutí prvních 6 měsíců léčby nízkomolekulárním heparinem.
Sledovaná skupina
Sledovanou skupinou bylo 87 pacientů (49 mužů a 38 žen) ve věku 27–87 let (průměrný věk 64 let) s TENAN. Zastoupení jednotlivých druhů nádorových onemocnění je uvedeno v tab. 1. Ačkoliv je s nejvyšším relativním rizikem vzniku TEN asociován mnohočetný myelom, tumory mozku a pankreatu [6], v námi sledované skupině byly nejčastějšími nádory kolorektální karcinom, karcinom prsu a bronchogenní karcinom, což odpovídá jejich vysokému výskytu v české populaci.
Table 1. Zastoupení jednotlivých nádorových onemocnění v souboru 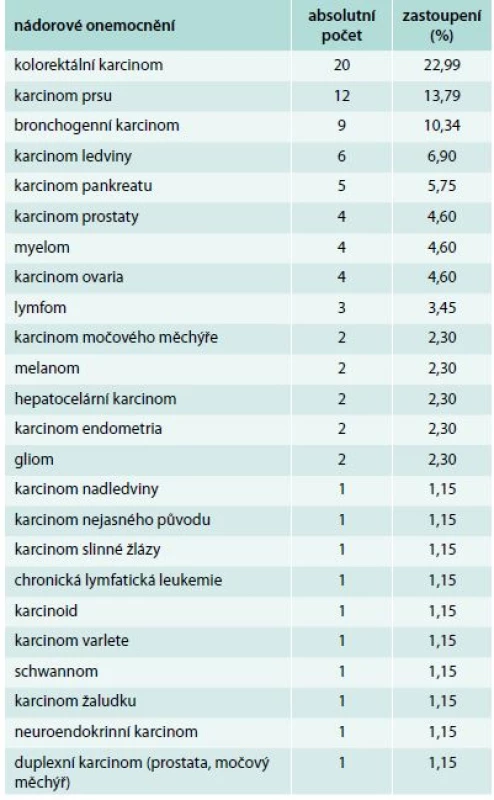
Tab. 2 udává, ve kterém období nádorového onemocnění byla trombóza diagnostikována; v tab. 3 je uvedeno procentuální zastoupení pacientů s plicní embolií, hlubokou žilní trombózou, kombinací hluboké žilní trombózy s plicní embolií a trombózou v jiné lokalizaci.
Table 2. Diagnóza TENAN v časovém vztahu k nádorovému onemocnění 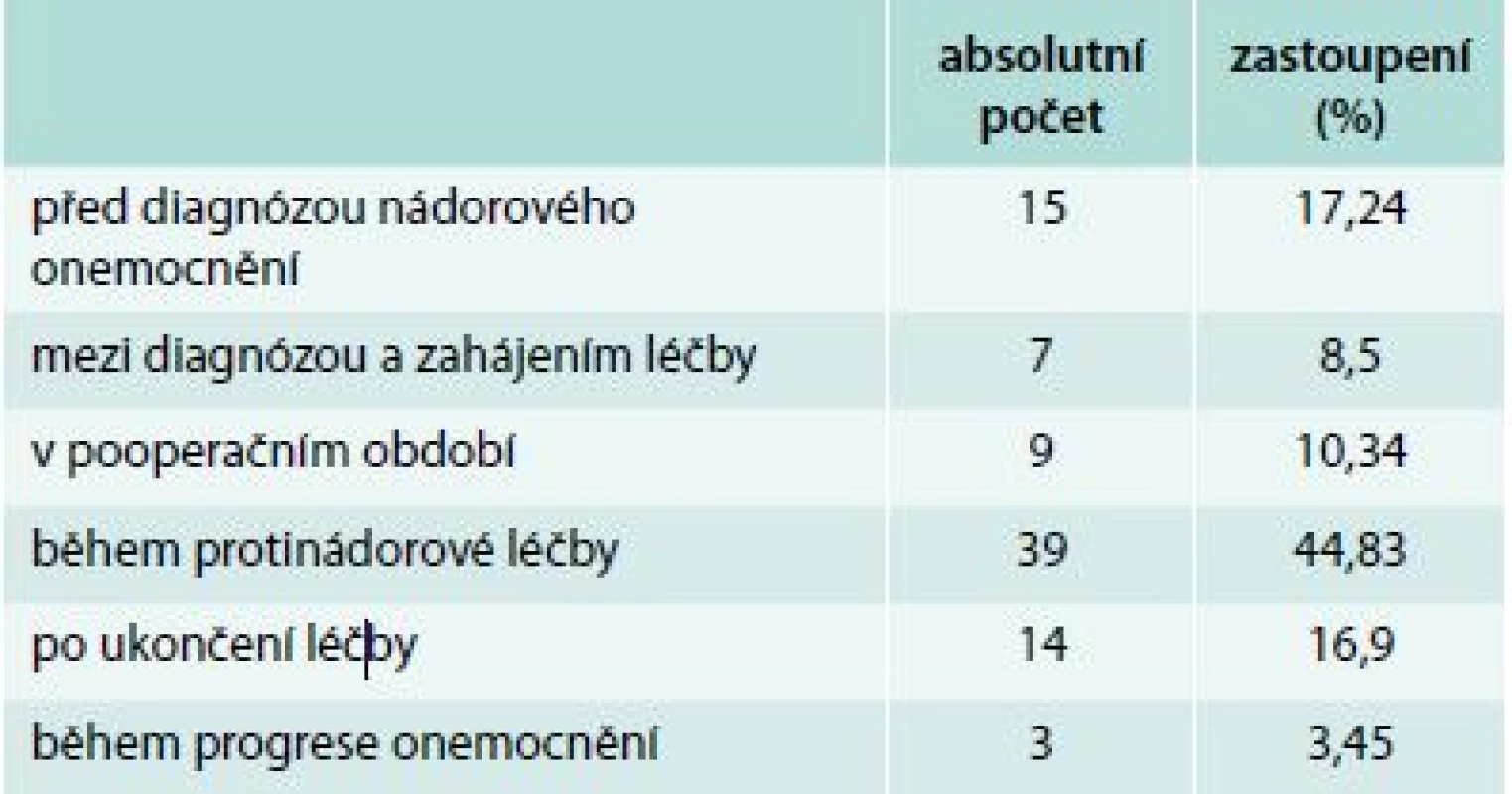
Table 3. Zastoupení jednotlivých forem TEN 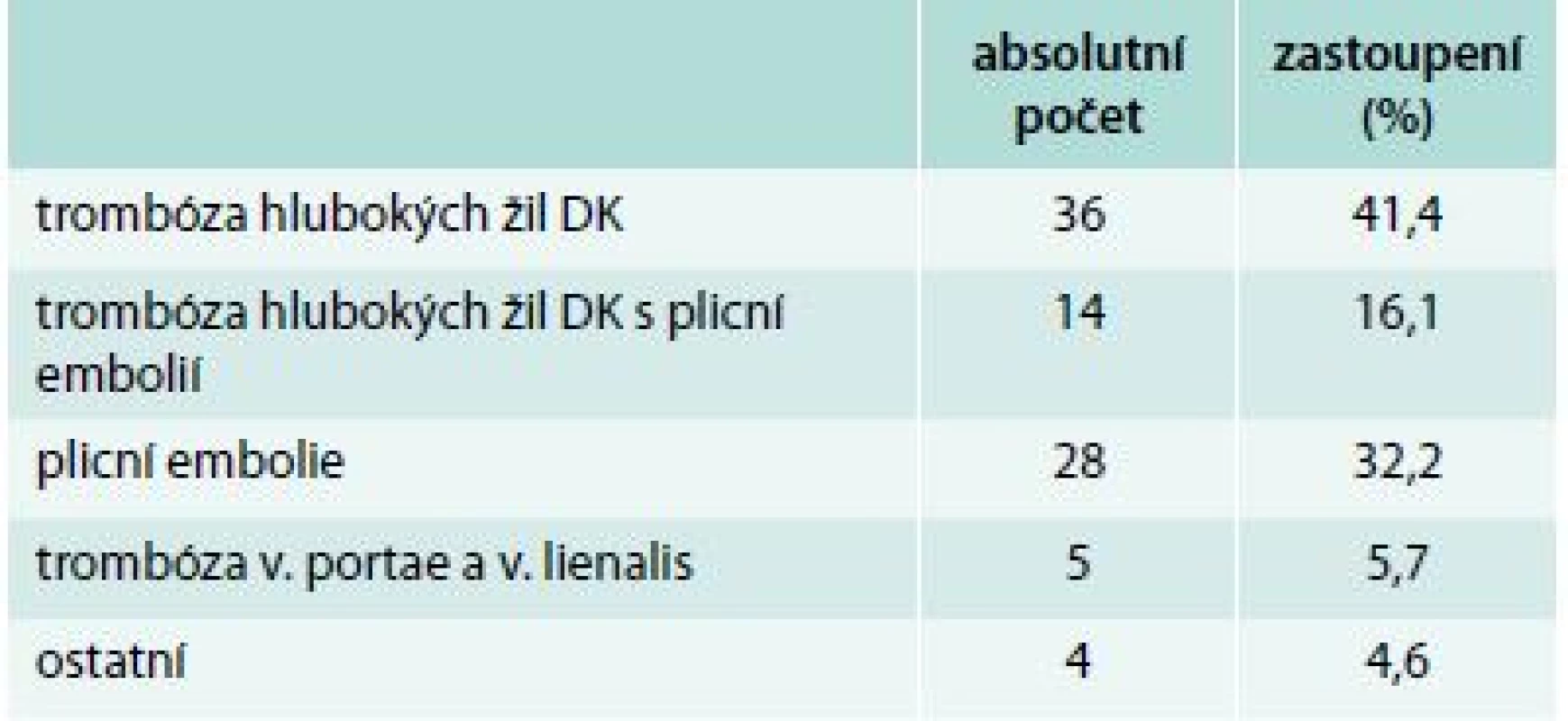
Metodika
Pacienti byli prospektivně sledováni během léčby TENAN. Kontrolní vyšetření zobrazovacími metodami bylo prováděno jen cíleně při podezření na rekurenci trombózy nebo před plánovaným vysazením antikoagulační léčby, nebylo prováděno systematicky před převodem z LMWH na warfarin. Bylo analyzováno zastoupení pacientů, u nichž byl LMWH nahrazen warfarinem během prvních 6 měsíců a během celého sledování ve vztahu k průběhu nádorového onemocnění. Ke statistickému zhodnocení byly použity testy χ2 a χ2 s Yatesovou korekcí.
Výsledky a zhodnocení
Medián doby sledování od vzniku trombózy byl 445 dnů, průměrná doba sledování 743 dnů. Typ a lokalizace nádoru ani forma TEN neovlivnily rozhodování o načasování převodu z LMWH na warfarin. Nádorové onemocnění bylo po 6 měsících od vzniku trombózy v kompletní remisi (CR) u 30 pacientů (34 %), v parciální remisi (PR) u 12 (14 %), stabilní (SD) u 9 (10 %), progredující (PG) u 13 (14 %). 13 (15 %) pacientů zemřelo, 8 pacientů bylo sledováno méně než 6 měsíců a u 2 nebyla k dispozici data o stavu nádorového onemocnění.
6 měsíců po diagnóze trombózy 9 z 30 (30 %) pacientů v CR bylo léčeno warfarinem, zatímco ve skupině v PR pouze 3 ze 12 (25 %). Ve skupině pacientů se SD nebyl warfarinem léčen žádný z 9 a u nemocných s progresí pouze 1 ze 13 (7,7 %). Pacienti v CR nebo PR byli léčeni warfarinem častěji než pacienti se stabilním či progredujícím nádorovým onemocněním (P = 0,02). Během celé doby sledování 25 ze 30 (83,3 %) pacientů, jejichž nádor byl v 6 měsících od diagnózy trombózy v CR, bylo převedeno na warfarin, zatímco jenom 5 ze 12 (41,7 %), 1 z 9 (11,1 %) a 1 ze 13 (7,7 %) pacientů v PR, SD a progresi bylo převedeno na warfarin. Podíl pacientů v CR převedených na warfarin byl vyšší než podíl pacientů v PR (P = 0,007), v SD (P = 0,0003) a s progresí nádoru (P < 0,0001).
Medián času od diagnózy trombózy do převodu z LMWH na warfarin byl u pacientů, kteří byli v 6 měsících v CR, 219 dnů a nebyl dosažen u pacientů, kteří v 6 měsících nebyli v CR.
Během prvních 6 měsíců od diagnózy TENAN nebyla pozorována žádná symptomatická rekurence trombózy, byla pozorována 4 velká krvácení, a to 3krát při léčbě LMWH a 1krát při léčbě warfarinem; tento pacient byl poté znovu převeden na LMWH.
Diskuse
Přes rozšiřující se poznatky zůstává léčba TENAN pro klinického lékaře výzvou i s ohledem na mnoho jejích specifik – pacienti s onkologickým onemocněním častěji podstupují invazivní zákroky, jsou více ohroženi malnutricí, infekčními nemocemi, zhoršením renálních a jaterních funkcí či trombocytopenií indukovanou protinádorovou léčbou. Výhodou LMWH v těchto situacích je oproti warfarinu významně kratší doba účinku, jednodušší nastavení optimální dávky, menší ovlivnění účinku event. malnutricí či interkurentní infekcí, absence lékových interakcí. Významným pozitivem LMWH je i vliv na dlouhodobé přežití u pacientů, kteří v době diagnózy trombózy neměli metastázy [7]. Naproti tomu těžká renální insuficience nebo významné kolísání renálních funkcí favorizují užití warfarinu [8]. LMWH také není možno podávat pacientům s heparinem indukovanou trombocytopenií nebo s polyvalentní alergií na LMWH.
Současná doporučení pro léčbu paraneoplastické TEN vycházejí především z randomizované studie CLOT [4] a metaanalýzy Akleho et al [9], které prokázaly nižší rekurenci TEN při léčbě LMWH oproti léčbě warfarinem v iniciálních 6 měsících. Další studie včetně studie CATCH [5,10,11] sice nepřinesly zásadní statisticky významné výsledky, což bylo vesměs dáno tím, že neměly dostatečný počet pacientů, nicméně vždy potvrdily stejné trendy jako studie CLOT. Podávání LMWH v období 6–12 měsíců od vzniku trombózy podporují i výsledky recentně publikované studie DALTECAN [12], která prokázala, že výskyt velkého krvácení i rekurence trombózy je nejvyšší během 1. měsíce od stanovení diagnózy a po uplynutí 6 měsíců je výskyt krvácivých komplikací malý. Hlavním faktorem ovlivňujícím strategii léčby TENAN po iniciální terapii LMWH je následný stav a průběh maligního onemocnění, což potvrzuje i naše práce. Při léčbě vždy zohledňujeme i pacientovy preference, nicméně nedávný průzkum [13] ukázal, že obavy mnohých kliniků z odmítání subkutánní aplikace léků pacienty mohou být přehnané – 39 % léčených považovalo za nejdůležitější vlastnost antikoagulancia co nejmenší interferenci s podávanou protinádorovou léčbou, pro 24 % nemocných bylo zásadní nízké riziko rekurence TENAN a pro 19 % pacientů nízké riziko krvácivých komplikací. Forma aplikace byla nejdůležitější vlastností preparátu pro pouhých 13 % nemocných [13].
Významný počet plicních embolií u onkologicky nemocných je diagnostikován náhodně při CT vyšetřeních z jiné indikace. Odhaduje se, že 3,1 % všech onkologicky nemocných má takto zjištěnou TENAN. Práce van der Hulleho et al, zabývající se léčbou náhodně zjištěné TENAN při CT, srovnávala 3 terapeutické postupy: nepodávání antikoagulační léčby, terapii LMWH a terapii warfarinem. Rekurence tromboembolie byla nejvyšší u neléčených pacientů (12 %) a nelišila se mezi pacienty léčenými LMWH a warfarinem (6,2 vs 6,4 %), ale skupina léčená LMWH měla významně nižší riziko velkých krvácivých komplikací (3,9 % vs 13 %). Riziko rekurence bylo stejné u subsegmentální náhodně zjištěné plicní embolie ve srovnání s proximálněji lokalizovanou embolií. Výše uvedené výsledky podporují léčbu náhodně zjištěné TENAN nízkomolekulárním heparinem a stejný terapeutický přístup k subsegmentální plicní embolii jako k embolii lokalizované proximálně [14]. Tento přístup dlouhodobě používáme i na našem pracovišti.
Je možné, že management léčby pacientů s TENAN v budoucnu zásadním způsobem změní nová antikoagulancia. Pro jejich užití v indikaci léčby trombózy asociované s nádorem nemáme zatím dostatek důkazů, nicméně první studie naznačují dobrou účinnost i bezpečnost užití nových antikoagulancií v této indikaci [15,16]. Více odpovědí by měla přinést probíhající studie SELECT-D, která bude první randomizovanou kontrolovanou studií srovnávající head-to-head LMWH a nové antikoagulans v léčbě TENAN – konkrétně dalteparin a rivaroxaban.
Nezodpovězenou otázkou zůstává optimální léčebná strategie u onkologických pacientů majících vyjma TENAN ještě jinou indikaci k chronické antikoagulaci, např. fibrilaci síní nebo umělou chlopenní náhradu.
MUDr. Jan Šmrha
jansmrha@centrum.cz
Interní oddělení Nemocnice Pelhřimov, a.s.
www.hospital-pe.cz
Doručeno do redakce 25. 2. 2016
Přijato po recenzi 26. 4. 2016
Sources
1. Heit JA, Silverstein MD, Mohr DN et al. Risk factors for deep vein thrombosis and pulmonary embolism: a population-based case-control study. Arch Intern Med 2000; 160(6): 809–815.
2. Palareti G, Legnani C, Lee AY et al. A comparison of the safety and efficacy of oral anticoagulation for the treatment of venous thromboembolic disease in patients with or without malignancy. Thromb Haemost 2000; 84(5): 805–810.
3. Konstantinides S, Torbicki A, Agnelli G et al. [Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the European Society of Cardiology (ESC)]. 2014 ESC Guidelines on the diagnosis and management of acute pulmonary embolism Eur Heart J 2014; 35(43): 3033–69, 3069a-3069. Dostupné z WWW: http://eurheartj.oxfordjournals.org/content/ehj/35/43/3033.full.pdf. Erratum in Corrigendum to: 2014 ESC Guidelines on the diagnosis and management of acute pulmonary embolism. [Eur Heart J 2015]. Corrigendum to: 2014 ESC Guidelines on the diagnosis and management of acute pulmonary embolism. [Eur Heart J 2015]
4. Lee AY, Levine MN, Baker RI et al. Randomized Comparison of Low-Molecular-Weight Heparin versus Oral Anticoagulant Therapy for the Prevention of Recurrent Venous Thromboembolism in Patients with Cancer (CLOT) Investigators: Low-molecular-weight heparin versus a coumarin for the prevention of recurrent venous thromboembolism in patients with cancer. N Engl J Med 2003; 349(2): 146–153.
5. Lee AY, Bauersachs R, Janas MS et al. CATCH: a randomised clinical trial comparing long-term tinzaparin versus warfarin for treatment of acute venous thromboembolism in cancer patients. BMC Cancer 2013; 13 : 284. Dostupné z DOI: <http://dx.doi.org/10.1186/1471–2407–13–284>.
6. Cronin-Fenton DP, Søndergaard F, Pedersen LA et al. Hospitalisation for venous thromboembolism in cancer patients and the general population: a population-based cohort study in Denmark, 1997–2006. Br J Cancer 2010; 103(7): 947–953.
7. Lee AY, Rickles FR, Julian JA et al. Randomized comparison of low molecular weight heparin and coumarin derivatives on the survival of patients with cancer and venous thromboembolism. J Clin Oncol 2005; 23(10): 2123–2129.
8. Prandoni P. The treatment of cancer-associated venous thromboembolism in the era of the novel oral anticoagulants. Expert Opin Pharmacother 2015; 16(16):2391–2394.
9. Akl EA, Barba M, Rohilla S et al. Anticoagulation for the long term treatment of venous thromboembolism in patients with cancer. Cochrane Database Syst Rev 2008; 16(2): CD006650. Dostupné z DOI: http://dx.doi.org/10.1002/14651858.CD006650.pub2.
10. Meyer G, Marjanovic Z, Valcke J et al. Comparison of low-molecular-weight heparin and warfarin for the secondary prevention of venous thromboembolism in patients with cancer: a randomized controlled study. Arch Intern Med 2002; 162(15): 1729–1735.
11. Hull RD, Pineo GF, Brant RF et al. [LITE Trial Investigators]. Long-term low-molecular-weight heparin versus usual care in proximal-vein thrombosis patients with cancer. Am J Med 2006; 119(12): 1062–1072.
12. Francis CW, Kessler CM, Goldhaber SZ et al. Treatment of venous thromboembolism in cancer patients with dalteparin for up to 12 months: the DALTECAN Study. J Thromb Haemost 2015; 13(6): 1028–1035.
13. Noble S, Matzdorff A, Maraveyas A et al. Assessing patients‘ anticoagulation preferences for the treatment of cancer-associated thrombosis using conjoint methodology. Haematologica 2015; 100(11): 1486–1492.
14. van der Hulle T, den Exter PL, Planquette B et al. Risk of recurrent venous thromboembolism and major hemorrhage in incidental pulmonary embolism among treated and untreated patients: a pooled analysis of 926 patients. J Thromb Haemost 2016; 14(1): 105–113.
15. Vedovati MC, Germini F, Agnelli G et al. Direct oral anticoagulants in patients with VTE and cancer: a systematic review and meta-analysis. Chest 2015; 147(2): 475–483.
16. van Es N, Coppens M, Schulman S. Direct oral anticoagulants compared with vitamin K antagonists for acute venous thromboembolism: evidence from phase 3 trials. Blood 2014; 124(12): 1968–1975.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2016 Issue 6-
All articles in this issue
- Perkutánní endoskopická gastrostomie: analýza praxe v endoskopickém centru terciární lékařské péče
- Diabetic Kidney Disease 3rd stage – laboratory markers of mineral bone disorder
- Dlouhodobá léčba tromboembolické nemoci u pacientů se zhoubným nádorem
- Roční sledování vedlejších účinků podávání sitagliptinu u pacientů s diabetes mellitus 2. typu
- Akútne príčiny náhlych úmrtí u pacientov so závažnou hypoglykémiou
- Kardiomyopatie v MR obraze
- Studie HOPE-3: statiny snižují kardiovaskulární příhody u pacientů s intermediárním rizikem ICHS
- mikroRNA a vnitřní lékařství: od patofyziologie k novým diagnostickým a terapeutickým postupům
- Aplikační technika inzulinu u dospělých pacientů s diabetem
- Sinusová histiocytóza s masivní lymfadenopatií: FDG-PET/CT dokumentovaná parciální remise po léčbě 2-chlorodeoxyadenozinem
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Sinusová histiocytóza s masivní lymfadenopatií: FDG-PET/CT dokumentovaná parciální remise po léčbě 2-chlorodeoxyadenozinem
- Aplikační technika inzulinu u dospělých pacientů s diabetem
- Kardiomyopatie v MR obraze
- Perkutánní endoskopická gastrostomie: analýza praxe v endoskopickém centru terciární lékařské péče
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

