-
Medical journals
- Career
Antagonisté receptorů pro angiotenzin II (AT1-blokátory) v léčbě hypertenze
: Jiří Widimský Jr
: III. interní klinika 1. LF UK a VFN, Praha
: Vnitř Lék 2016; 62(2): 107-113
: Reviews
Blokátory angiotenzinových receptorů typu 1 (AT1-blokátory, sartany) patří mezi základní antihypertenzní látky vhodné pro monoterapii i kombinační léčbu hypertenze. AT1-blokátory mají srovnatelné účinky s dalšími hlavními třídami antihypertenziv včetně ACE-inhibitorů. Dle současných doporučení České společnosti pro hypertenzi jsou sartany spolu s ACE-inhibitory a blokátory kalciových kanálů považovány za tzv. univerzální antihypertenziva. Mají ze všech antihypertenziv nejméně nežádoucích účinků a nemocní léčení sartany vykazují nejlepší dlouhodobou perzistenci k léčbě. V článku jsou diskutovány mechanizmy antihypertenzního účinku jakož i srovnání antihypertenzních účinků sartanů s dalšími antihypertenzními látkami. Jsou uvedeny výsledky větších klinických studií se sartany a indikace u arteriální hypertenze.
Klíčová slova:
AT1-blokátory – hypertenze – léčbaÚvod
Systém renin-angiotenzin-aldosteron hraje spolu se sympatickým nervovým systémem významnou roli v regulaci sodíkové, volumové a tlakové homeostázy. Angiotenzin II je silnou vazokonstrikční látkou s natrium-retenčním a proliferativním (remodelace cévní, hypertrofie levé komory srdeční) působením. Za většinu známých nežádoucích účinků je zodpovědná aktivace specifických receptorů pro angiotenzin II typu 1 (AT1) [1]. Význam dalších typů receptorů pro angiotenzin II (zejména typu AT2) není do detailů objasněn. Zdá se, že stimulace AT2-receptorů vede k vazodilataci a má natriuretický a antiproliferativní účinek. Úloha dalších podtypů AT-receptorů (AT3 a AT4) není zcela jasná.
Antagonisté receptorů pro angiotenzin II (AT1-blokátory, sartany) byly zavedeny do klinické praxe v polovině 90. let minulého století. Prvým registrovaným zástupcem této skupiny byl losartan, ke kterému v průběhu let přibyla řada dalších. Mezi jednotlivými látkami jsou určité rozdíly v chemické struktuře, které mohou spolupodmiňovat určité rozdíly ve farmakokinetických a farmakodynamických vlastnostech [2].
Farmakologické vlastnosti
Antihypertenzní účinek AT1-blokátorů je způsoben selektivní vazbou na AT1-receptory s následnou blokádou biologických účinků angiotenzinu II. Blokáda receptorů může být buď kompetitivní (např. valsartan, irbesartan), nebo nekompetitivní (např. aktivní metabolit losartanu Exp3174, candesartan). Biologické účinky některých AT1-blokátorů závisí na konverzi na aktivní metabolit (např. losartan, candesartan, olmesartan). Zdá se, že neexistují klinicky významné rozdíly mezi AT1-blokátory s vlastní účinností výchozí molekuly a látkami ve formě proléku. Blokáda AT1-receptorů vede k vazodilataci s následným poklesem periferní cévní rezistence, na kterém se kromě blokády účinků angiotenzinu II podílí i snížení produkce aldosteronu a částečně i inhibice periferní sympatické nervové aktivity. Na rozdíl od ACE-inhibitorů AT1-blokátory neovlivňují metabolizmus bradykininu.
Základní farmakologická charakteristika nejčastěji používaných AT1-blokátorů je uvedena v tab. 1.
1. Charakteristika a dávkování nejčastěji používaných AT<sub>1</sub>-blokátorů 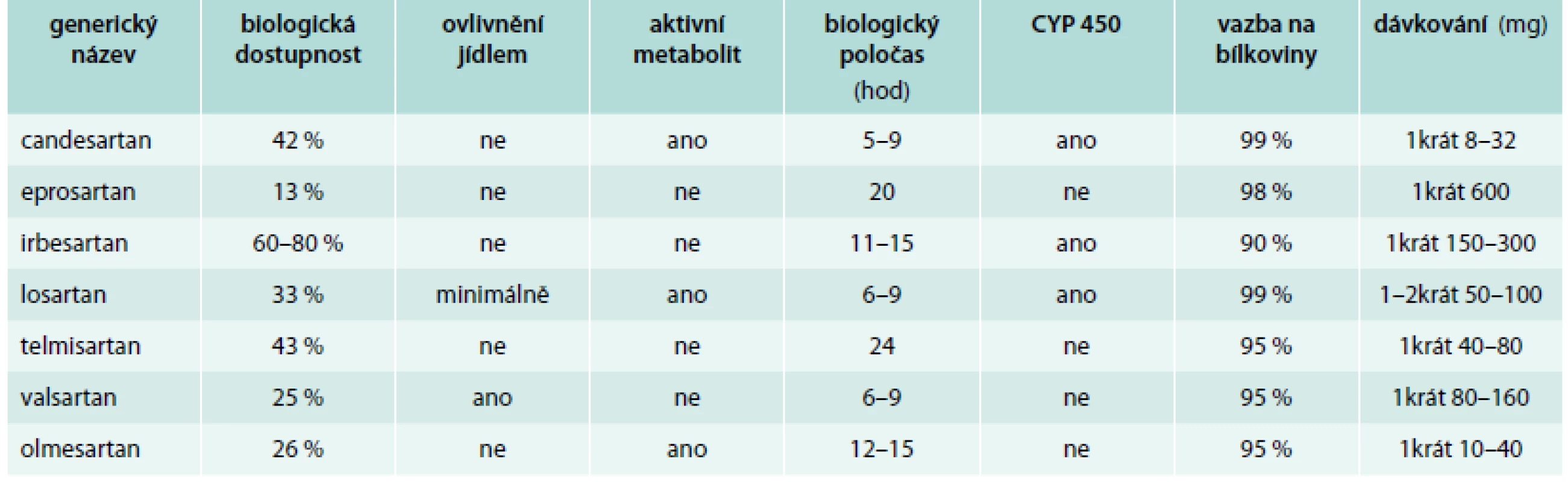
Kromě výše uvedených molekul je v ČR registrován i azilsartan. Další molekuly jsou vyvíjeny (např. embusartan, fonsartan, pratosartan nebo milfasartan) [2].
Nejvyšší vazebnou afinitu k AT1-receptorům má molekula azilsartanu, vysoká afinita je popisována rovněž u telmisartanu, olmesartanu a candesartanu, nejnižší je u losartanu [2,3]. V preklinických studiích působily některé AT1-blokátory (zejména telmisartan, v menší míře irbesartan) rovněž jako parciální agonista receptorů PPARγ, analogicky jako např. glitazony, a snižovaly tak hodnotu glykemie či triglyceridů. Nakolik jsou tyto metabolické účinky klinicky významné, není však zatím zcela jasné.
Důležitý při volbě konkrétního preparátu je rovněž údaj o způsobu eliminace, který se obvykle uvádí jako poměr vylučování játry/ledvinami. Nejvyšší poměr je detekován u telmisartanu a eprosartanu [2], a proto není třeba snižovat dávky těchto AT1-blokátorů u lehké a středně těžké renální insuficience. Losartan má jako jediný z celé třídy urikosurický efekt.
Antihypertenzní účinky
AT1-blokátory mají srovnatelné účinky s dalšími hlavními třídami antihypertenziv včetně ACE-inhibitorů [4]. Telmisartan ve srovnání s ramiprilem se jevil dokonce jako účinnější v ovlivnění 24hodinového TK, zejména v časných ranních hodinách [5]. Antihypertenzní účinnost AT1-blokátorů je nezávislá na věku pacientů a pohlaví [4].
Metaanalýza randomizovaných kontrolovaných studií sledujících antihypertenzní účinky různých AT1-blokátorů (losartan, valsartan, irbesartan a candesartan) nezjistila signifikantní rozdíly v ovlivnění krevního tlaku při použití obvyklých doporučených dávek (losartan 50–100 mg, valsartan 80–160 mg, irbesartan 150–300 mg, candesartan 8–16 mg) [6]. Určitou slabinou této metaanalýzy byla skutečnost, že antihypertenzní účinek byl vyhodnocován jen na základě jednorázových měření krevního tlaku. Proto jsou v této souvislosti velmi zajímavé výsledky rozsáhlé metaanalýzy antihypertenzního účinku AT1-blokátorů založené na analýze studií využívající 24hodinové monitorování krevního tlaku [7]. Studie zahrnuté do této metaanalýzy musely kromě skupiny AT1-blokátorů splňovat i následující přísná kritéria: publikování v recenzovaném renomovaném časopise a uvedení vstupních i finálních hodnoty krevního tlaku včetně 24hodinového průměrného TK. Velkou výhodou této metaanalýzy oproti Conlinově práci [6] byla navíc skutečnost, že použité AT1-blokátory zahrnovaly téměř všechny registrované látky podávané v obvyklých terapeutických dávkách: losartan (50–100 mg), valsartan (80–160 mg), irbesartan (150–300 mg), candesartan (8–16 mg), telmisartan (40–80 mg), eprosartan (600–900 mg) a olmesartan (20–40 mg) [7]. Podle výsledků této analýzy se zdá, že antihypertenzní účinek AT1-blokátorů nezávisí na počátečních hodnotách krevního tlaku (TK). Výsledky této metaanalýzy ukazují, že mohou existovat určité rozdíly v antihypertenzním účinku mezi jednotlivými AT1-blokátory a že tyto rozdíly se týkají zejména ovlivnění systolického krevního tlaku. Podle výsledků se zdá, že trend k nejvýraznějšímu poklesu TK, byl pozorován u olmesartanu, a naopak eprosartan se jevil jako nejméně účinný [7].
Přesnější porovnání antihypertenzního účinku jednotlivých AT1-blokátorů mezi sebou je však velmi obtížné s ohledem na retrospektivní charakter a rozdíly v designu jednotlivých studií. Ve většině použitých studií zmíněné metaanalýzy [7] nebyl navíc porovnávanou látkou jiný AT1-blokátor, ale placebo nebo jiné antihypertenzivum. Proto jsou zajímavé výsledky studií srovnávajících přímo antihypertenzní efekt dvou AT1-blokátorů pomocí 24hodinového monitorování krevního tlaku. Například v Bakrisově studii ovlivňoval azilsartan v porovnání s olmesartanem 24hodinový TK účinněji [8].
AT1-blokátory a kombinační léčba hypertenze
Nejvhodnější kombinací je kombinace s diuretiky a blokátory kalciových kanálů, která má velký aditivní antihypertenzní účinek. Například ve studii TEAMSTA-10 byla zkoumána účinnost fixní kombinace telmisartan 80 mg/amlodipin 10 mg u pacientů nedostatečně reagujících na amlodipin 10 mg [9]. Uvedená kombinace zlepšila antihypertenzní účinnost ve srovnání s maximální dávkou amlodipinu (10 mg) v monoterapii. Incidence vedlejších účinků (otoky) byla díky přítomnosti telmisartanu nízká.
Zajímavá byla i další studie zabývající se účinkem fixní kombinace candesartan/amlodipin [10]. Jednalo se o multicentrickou, randomizovanou, dvojitě zaslepenou a placebem kontrolovanou studii srovnávající antihypertenzní účinky candesartanu ve fixní kombinaci s amlodipinem (8/5 mg) oproti příslušným monoterapiím. Fixní kombinace vedla k velkému antihypertenznímu účinku, který byl statisticky významnější oproti monoterapii 8 mg candesartanu, resp. 5 mg amlodipinu [10].
Kombinace s betablokátory je u komplikované hypertenze pro menší ovlivnění TK méně vhodná. Kombinace AT1-blokátorů s ACE-inhibitory není na základě výsledků studie ONTARGET [11] a současných guidelines [12,13] doporučována vzhledem k velmi malému aditivnímu antihypertenznímu účinku, a naopak zvýšené incidenci vedlejších účinků. Podle nedávné klinické studie u diabetické nefropatie podávání AT1-blokátorů v kombinaci s ACE-inhibitory významně zvýšilo riziko hyperkalemie a renálního poškození [14]. Větší aditivní účinek než použití dvou blokátorů RAS má kombinace jednoho blokátoru RAS s malou dávkou spironolaktonu za podmínky častějšího monitorování mineralogramu a ledvinných funkcí. Pro kombinaci AT1-blokátorů s dalšími třídami antihypertenziv (alfa-blokátory, centrálně působící antihypertenziva) máme málo dokladů.
Velké studie s AT1-blokátory v léčbě hypertenze anebo nefropatie
Výsledky velkých klinických studií s užíváním AT1-blokátorů prokázaly významný renoprotektivní efekt těchto léků ve srovnání s placebem – studie RENAAL [15] a studie IRMA [16] a ve srovnání s amlodipinem – studie IDNT [17]. Do těchto studií byli zařazováni především diabetici 2. typu s přítomnou nebo nepřítomnou hypertenzí. Tyto výsledky vedly Americkou diabetologickou společnost k zavedení nové indikace pro AT1-blokátory – hypertenzní i nehypertenzní nemocní s diabetes mellitus 2. typu a mikroalbuminurií či klinickou albuminurií.
V roce 2002 a 2003 byly prezentovány výsledky dalších velkých studií s AT1-blokátory u hypertoniků – LIFE – Losartan Intervention For Endpoints a studie – SCOPE – the Study on Cognition and Prognosis in Elderly hypertensives.
Studie LIFE [18] sledovala 9 193 nemocných ve věku 55–80 let s hodnotou krevního tlaku při randomizaci 160–200/95–115 mm Hg a s prokázanou hypertrofií levé komory. Polovina nemocných byla léčena losartanem v dávce titrované od 50 do 100 mg, druhá polovina atenololem se stejnou titrací. Podle tlaku mohl být přidán hydrochlorothiazid. Průměrná doba sledování byla 4 roky. Hlavní výsledky ukazuje tab. 2.
2. Hlavní výsledky studie LIFE 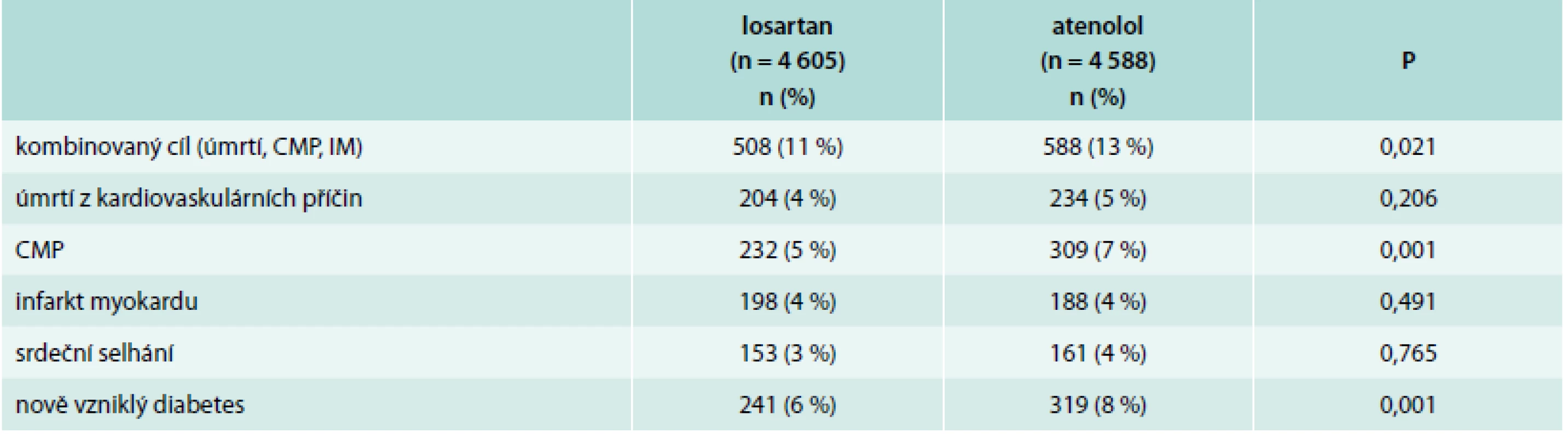
Studie LIFE byla jednou z prvních studií prokazující, že efekt některé lékové skupiny je ovlivněn nejen mírou poklesu krevního tlaku, ale i dalšími specifickými vlastnostmi.
Ve studii SCOPE [19] bylo porovnáváno podávání candesartanu s jinou antihypertenzní léčbou (vyjma ACEI a AT1-blokátory) u 4 937 hypertoniků starších 70 let. Pokud měli nemocní již zavedenou antihypertenzní léčbu, museli být převedeni na hydrochlorothiazid 12,5 mg a splnit vstupní kritéria. Poté byli nemocní randomizováni k léčbě candesartanem 8–16 mg nebo placebem, a pokud byl po 3 měsících STK > 160 mm Hg a/nebo DTK > 90 mm Hg, mohla být přidána libovolná antihypertenzní medikace vyjma ACEI a AT1-blokátoru, tak aby bylo dosaženo uspokojivé kontroly krevního tlaku. Nemocní byli sledování 3–5 let. Na konci studie byly hodnoty krevního tlaku ve skupině užívající candesartan 145/80 mm Hg, což znamená pokles o 21,7/10,8 mm Hg. V placebové větvi byl na konci studie krevní tlak 149/82 mm Hg, což znamená pokles o 18,5/9,2 mm Hg. Rozdíl v poklesu tlaku mezi oběma skupinami byl 3,2/1,6 mm Hg (p < 0,001).
Nebyly statisticky signifikantní rozdíly ve výskytu primárního cíle (úmrtí, IM, CMP) mezi candesartanovou větví a placebem. Statisticky významný byl pokles cévních mozkových příhod a na hranici statistické významnosti byl pokles výskytu nového diabetes mellitus. Signifikantní rozdíly ve výskytu primárního cíle byly pozorovány u nemocných, kteří neměli během studie přidánu další antihypertenzní medikaci. U těchto pacientů vedlo podávání candesartanu ke snížení rizika kardiovaskulárních příhod (úmrtí, IM, CMP) o 32,19 % (p = 0,012) [19].
V další rozsáhlé studii VALUE [20] byla u vysoce rizikových hypertoniků srovnávána antihypertenzní léčba založená na valsartanu a amlodipinu. Design této studie byl kritizován, neboť mohl vést k významnějšímu antihypertenznímu účinku v amlodipinové větvi na začátku studie. Když však byla obě léčebná ramena porovnána podle hodnot TK, byl počet kardiovaskulárních komplikací a mortalita z kardiovaskulárních příčin v obou ramenech studie podobná. Ve valsartanové větvi byl pozorován naopak nižší výskyt srdečního selhání a nově vzniklého diabetes mellitus [20].
V roce 2005 byly publikovány výsledky studie MOSES [21] (Morbidity and mortality after stroke, eprosartan compared with nitrendipine for secondary prevention), která srovnávala nitrendipin s eprosartanem u osob po CMP. Studie randomizovala 1 405 nemocných a pokles krevního tlaku byl v obou skupinách naprosto stejný, takže na konci studie byly hodnoty krevního tlaku 137/81 mm Hg ve větvi léčené eprosartanem a 136/81 mm Hg ve větvi léčené nitrendipinem. Přestože pokles krevního tlaku byl srovnatelný, primární celkový cíl – mortalita, nefatální kardiovaskulární příhody a nefatální cerebrovaskulární příhody – byl eprosartanem výrazně více snížen než nitrendipinem. Určitým problémem interpretace výsledků této studie může být skutečnost, že nitrendipin nebyl podáván v maximální dávce.
Studie PRoFESS [22] – Telmisartan to prevent recurrent stroke and cardiovascular events – měla za cíl potvrdit, že dlouhodobé snižování krevního tlaku telmisartanem po cévní mozkové příhodě povede ke snížení rizika opakování CMP. Jednalo se o mezinárodní multicentrickou klinickou studii, do které bylo zařazeno 20 332 nemocných starších 55 let s proběhlou cévní mozkovou příhodou. Ve studii byl 10 146 nemocných podáván telmisartan v dávce 80 mg 1krát denně a 10 186 užívalo placebo. Studie PRoFESS prokázala trend (statisticky nevýznamný) k poklesu CMP, kardiovaskulárních příhod i nového diabetes mellitus u nemocných po cévní mozkové příhodě léčených telmisartanem oproti placebu. Na absenci významnějších rozdílů se mohlo podílet krátké trvání studie – 2,5 roku.
Studie OSCAR [23] byla otevřená studie, jejímž cílem bylo vyhodnotit dopad léčby založené na eprosartanu na kognitivní funkce. Léčba krevního tlaku byla zahájena eprosartanem 600 mg/den s plánem nasadit další léky po 1 měsíci u pacientů s nedostatečnou reakcí krevního tlaku. Použití eprosartanu, buď jako monoterapie, nebo v kombinovaném režimu, bylo spojeno s výrazným snížením krevního tlaku a současně i významným poklesem celkového průměrného skóre zkoušky MMSE. Je však otázkou, nakolik přispělo k pozorovaným výsledkům vlastní snížení krevního tlaku. Zpomalení progrese deteriorace kognitivních funkcí bylo popsáno i u blokátorů kalciových kanálů (studie SYST-EUR).
Studie srovnávající účinky AT1-blokátorů a ACE-inhibitorů
Studie ONTARGET [11] sledovala 25 577 nemocných s ischemickou chorobou srdeční nebo ischemickou chorobou dolních končetin nebo mozku nebo s diabetes mellitus a orgánovým poškozením, z nichž přibližně polovina trpěla hypertenzí. Vstupní TK činil v průměru 142/82 mm Hg. Nemocní pak byli randomizováni k léčbě ramiprilem 10 mg nebo telmisartanem 80 mg denně nebo kombinací obou. Počet nemocných, kteří ukončili studii pro nežádoucí účinky při léčbě, byl v ramiprilové větvi 2 099 (24,5 %), telmisartanové větvi 1 962 (23,0 %) a ve větvi s kombinací obou 2 495 (29,3 %), p < 0,001. Hlavní rozdíl byl ve vyšším výskytu hypotenze (p < 0,001), průjmu (p < 0,001) a renální insuficience (p < 0,001) při léčbě kombinací.
Hlavní výsledky studie ONTARGET ukazuje tab. 3.
3. Hlavní výsledky studie ONTARGET 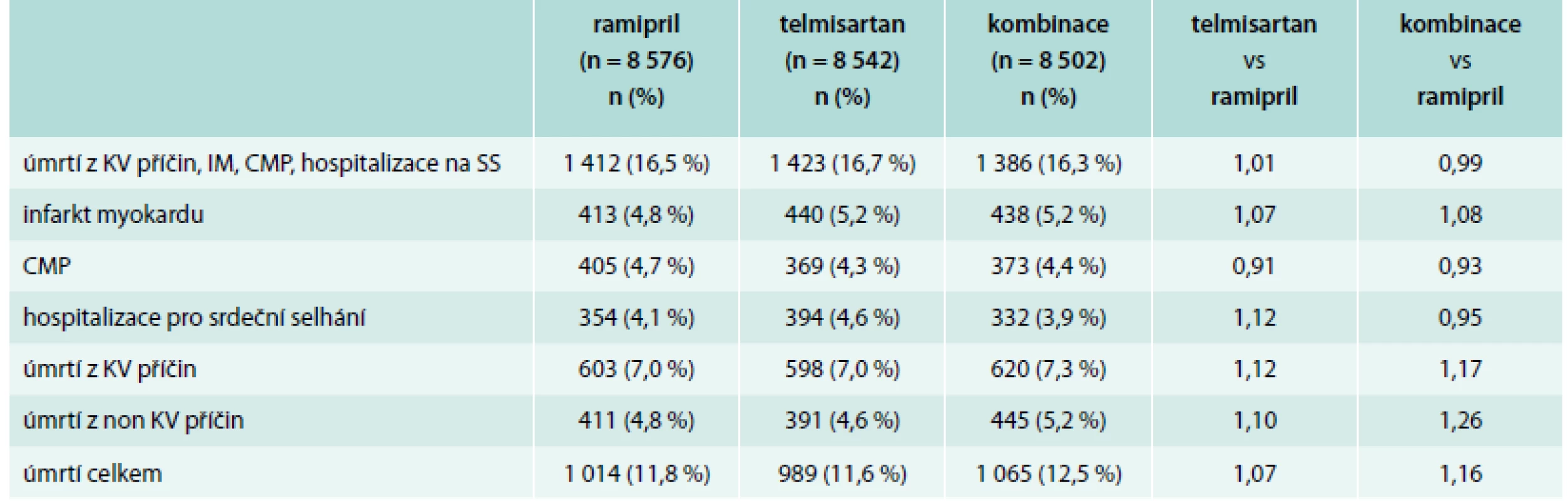
Z tab. 3 je patrné, že ani jeden parametr nedosáhl statistické významnosti a z pohledů hlavních cílů je léčba ramiprilem, telmisartanem i kombinací srovnatelná. Studie ONTARGET tak potvrdila rovnocennost AT1-blokátoru telmisartanu a ACE-inhibitoru ramiprilu v sekundární prevenci ischemické choroby srdeční a zároveň zřetelně upozornila na nebezpečí zhoršení renálních funkcí při léčbě kombinací obou preparátů [11].
V menší 5leté studii DETAIL byly srovnávány renoprotektivní účinky 80 mg telmisartanu a 20 mg enalaprilu [24] u osob s diabetes mellitus 2. typu a počínající nefropatií. Primárním cílem byly změny glomerulární filtrace (GFR) po 5 letech ve srovnání s výchozími hodnotami. Mezi oběma léčebnými rameny nebyly shledány významné rozdíly ve výskytu primárního i sekundárního (změny GFR, albuminurie, TK, KV příhody a celková mortalita) cíle.
V České republice probíhaly studie CORD A a CORD B [25]. Studie CORD A randomizovala 4 016 nemocných s TK < 160/100 mm Hg, kteří byli léčení ACE-inhibitorem déle než 3 měsíce, a tito nemocní byli během 1 dne převedeni na léčbu losartanem. Převod na losartan byl bezpečný a nedošlo k vzestupu krevního tlaku. Studie CORD B srovnala ramipril a losartan u 3 813 hypertoniků a neprokázala rozdíl v účinku na krevní tlak mezi losartanem a ramiprilem. Jediný rozdíl mezi oběma skupinami byl ve výskytu kašle, který byl 8krát častěji přítomen u nemocných léčených ramiprilem než losartanem.
V nedávné rozsáhlé observační asijské studii byly srovnávány účinky ACE-inhibitorů (u téměř 16 000 pacientů) a AT1-blokátorů (u téměř 24 000 pacientů) u hypertoniků s diabetes mellitus po proběhlé ischemické cévní mozkové příhodě (CMP) [26]. Do studie byli zařazeni pacienti, u kterých byla zahájena léčba blokátory RAS do 90 dní od vzniku CMP. Primárním cílem byl výskyt závažných KV příhod (infarkty myokardu, recidivy CMP a mortalita z KV příčin). Sekundárními cíli byla hospitalizace pro akutní ledvinné poškození a hyperkalemie. Podobně jako v předešlých studiích i v této kohortě pacientů nebyly shledány významné rozdíly ve výskytu primárních či sekundárních cílů mezi ACE-inhibitory a AT1-blokátory [26].
Indikace a kontraindikace AT1-blokátorů u hypertenze
Na základě výše uvedených studií uvádějí doporučení Evropské společnosti pro hypertenzi/Evropské kardiologické společnosti z roku 2013 [13] a ČSH z roku 2012 [12] následující indikace a kontraindikace pro podávání AT1-blokátorů (tab. 4).
4. Indikace a kontraindikace AT1-blokátorů u hypertenze 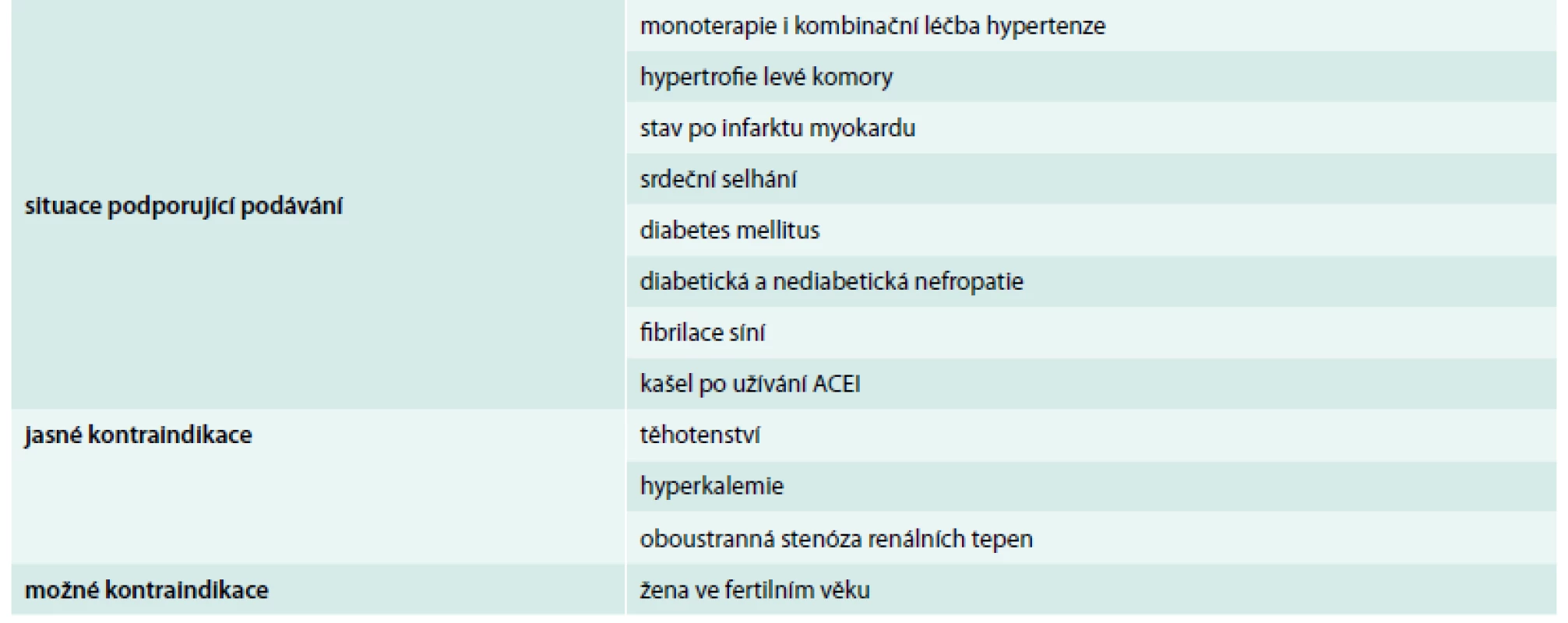
Nežádoucí účinky a adherence
Výskyt nežádoucích účinků je velmi nízký a v mnoha pracích srovnatelný s placebem. Výskyt kašle je ve srovnání s ACE-inhibitory nízký a srovnatelný s placebem. Výskyt angioedému je rovněž zřetelně nižší oproti ACE-inhibitorům. Podle některých názorů nelze tento nežádoucí vedlejší účinek ojediněle vyloučit ani při léčbě AT1-blokátory [27]. AT1-blokátory jsou však všeobecně považovány za látky s nejnižším výskytem vedlejších účinků, a tedy s velmi dobrou tolerancí. Výskyt vedlejších účinků není závislý na dávce [28,29]. Ojediněle se můžeme setkat se symptomatickou či asymptomatickou hypotenzí, hyperkalemií nebo se zhoršením renálních funkcí. Častější je výskyt hyperkalemie a renálního poškození při kombinaci s ACE-inhibitory, a proto není kombinace ACEI a AT1-blokátorů dle současných názorů doporučována. Kontraindikací je zatím pouze gravidita, hyperkalemie a známá alergie/intolerance.
Velmi dobrá tolerance s nízkým výskytem vedlejších účinků má za následek velmi dobrou dlouhodobou adherenci k léčbě, která je dle velmi rozsáhlé italské studie zahrnující 445 000 (!) osob nejvyšší ze všech tříd antihypertenziv [28]. Nejnižší adherence byla popisována u betablokátorů a diuretik [28]. Tyto závěry byly podpořeny i další studií, která analyzovala výsledky 8 studií srovnávajících perzistenci na léčbě různými antihypertenzními látkami [29]. Signifikantně vyšší perzistence byla pozorována při terapii AT1-blokátory ve srovnání s ACE-inhibitory, blokátory kalciových kanálů, betablokátory a diuretiky [29] (graf 1). Dobrá adherence k dlouhodobé, mnohdy celoživotní antihypertenzní léčbě má velký praktický význam, neboť nonadherentní hypertonici mají vyšší riziko celkové mortality [30].
1. Antihypertenzní léčba a perzistence na terapii. Upraveno podle [28] ![Antihypertenzní léčba a perzistence na terapii.
Upraveno podle [28]](https://pl-master.mdcdn.cz/media/image/69e51fe246c2188a57ad89ff5dc74f54.png?version=1537794432)
Interakce
Současné podávání AT1-blokátorů s látkami potenciálně zvyšujícími kalemii (suplementace kalia, amilorid, spironolakton, eplerenon, ACE-inhibitory) může zvyšovat riziko hyperkalemie. Vhodná je kombinace s kalium nešetřícími diuretiky.
Všechny následující substance zvyšující krevní tlak mohou snižovat antihypertenzní účinky AT1-blokátorů: sympatomimetika, látky s mineralokortikoidními účinky, kortikosteroidy, nesteroidní antiflogistika, hormonální antikoncepce, erytropoetin aj.
Při terapii AT1-blokátory může dojít ke sníženému vylučování lithia díky potenciálnímu poklesu glomerulární filtrace, a je proto vhodné v indikovaných případech monitorování jeho hladin.
Závěry
AT1-blokátory patří mezi základní (univerzální) antihypertenziva, vhodná jak pro monoterapii, tak pro kombinační léčbu. AT1-blokátory mají srovnatelné antihypertenzní účinky se všemi dalšími třídami antihypertenziv a dostatek evidence o příznivém ovlivnění prognózy osob s hypertenzí. Několik srovnávacích studií neprokázalo rozdíly v ovlivnění KV rizika a/nebo subklinického orgánového poškození u hypertenze mezi AT1-blokátory a ACE-inhibitory.
Hlavní výhodou AT1-blokátorů je především jejich velmi dobrá tolerance, považovaná za nejvyšší mezi všemi třídami antihypertenziv. Nepřekvapí proto zjištění, že rovněž adherence k dlouhodobé terapii AT1-blokátory je nejvyšší v celé velké skupině antihypertenzních látek.
Doručeno do redakce 14. 1. 2016
Přijato po recenzi 25. 1. 2016
prof. MUDr. Jiří Widimský jr, CSc.
jwidi@lf1.cuni.cz
III. interní klinika 1. LF UK a VFN, Praha
www.vfn.cz
Sources
1. Kaplan N. Victor RG. Kaplan’s Clinical Hypertension. 11th ed. Lippincott Williams and Wilkins: 2014. ISBN 978–1451190137.
2. Slíva J. Sartany v léčbě hypertenze. Acta medicinae 2015; 8 : 2–7.
3. Kakuta H, Sudoh K, Sasamata M et al. Telmisartan has the strongest binding affinity to angiotensin II type 1 receptor: comparison with other angiotensin II type 1 receptor blockers. Int J Clin Pharmacol Res 2005; 25(1): 41–46.
4. Weber MA. Angiotensin receptor blockers. In Izzo JL, Sica DA, Black R et al. Hypertension Primer: The Essentials of High Blood Pressure, Basic Science, Population Science, And Clinical Management. 4th ed. Lippincott Williams and Wilkins: 2007 : 461–464. ISBN 978–0781782050.
5. Williams B, Lacourcière Y, Schumacher H et al. Antihypertensive efficacy of telmisartan vs ramipril over the 24-h dosing period, including the critical early morning hours: a pooled analysis of the PRISMA I and II randomized trials. J Hum Hypertens 2009; 23(9): 610–619.
6. Conlin PR, Spence JD, Wiliams B et al. Angiotensin II antagonists for hypertension: are there differences in efficacy? Am J Hypertens 2000; 13(4 Pt 1): 418–426.
7. 7.Fabia MJ, Abdilla N, Oltra R et al. Antihypertensive activity of angiotensin II AT1 receptor antagonists: a systematic review of studies with 24 h ambulatory blood pressure monitoring. J Hypertens 2007; 25(7): 1327–1336.
8. Bakris GL, Sica D, Weber M et al. The comparative effects of azilsartan medoxomil and olmesartan on ambulatory and clinic blood pressure. J Clin Hypertens (Greenwich) 2011; 13(2): 81–88.
9. Neldam S, Edwards C, Jones R. TEAMSTA-10 Investigators.Switching patiens with uncotnrolled hypertension on amlodipin 10 mg to single –pill combinations of telmisartan and amlodipine: results of the TEAMSTA-10 study. Curr Med Res Opin 2011; 27(11): 1–9.
10. Rakugi H, Ogihara T, Miyata Y et al. Evaluation of the efficacy and tolerability of combination therapy with candesartan cilexetil and amlodipine besilate compared with candesartan cilexetil monotherapy and amlodipine besilate monotherapy in Japanese patients with mild-to-moderate essential hypertension: a multicenter, 12-week, randomized, double-blind, placebo-controlled, parallel-group study. Clin Ther 2012; 34(4): 838–848.
11. The ONTARGET Investigators. Telmisartan, ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008; 358(15): 1547–1559.
12. Filipovský J, Widimský J jr, Ceral J et al. Diagnostické a léčebné postupy u arteriální hypertenze-verze 2012. Doporučení České společnosti pro hypertenzi. Vnitř Lék 2012; 58(10): 785–801.
13. Mancia G, Fagard R, Narkiewicz K et al. 2013 ESH/ESC Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J Hypertens 2013; 31(7): 1281–1357.
14. Fried LF, Emanuele N, Zhang JH et al (VA NEPHRON-D Investigators). Combined angiotensin inhibition for the treatment of diabetic nephropathy. N Engl J Med 2013; 369(20): 1892–1903.
15. Brenner BM, Cooper ME, de Zeeuw D et al (RENAAL Study Investigators). Effects of losartan on renal and cardiovascular outcomes in patients with type-2 diabetes and nephropathy. N Engl J Med 2001; 345(12): 861–869.
16. Parving HH, Lehnert H, Bröchner-Mortensen J et al. Irbesartan in Patients with Type-2 Diabetes and Microalbuminuria Study Group. The effect of irbesartan on the development of diabetic nephropathy in patients with type-2 diabetes. N Engl J Med 2001; 345(12): 870–878.
17. Lewis EJ, Hunsicker LG, Clarke WR et al (Collaborative Study Group). Renoprotective effect of the angiotensin-receptor antagonist irbesartan in patients with nephropathy due to type 2 diabetes. N Engl J Med 2001; 345(12): 851–860.
18. Dahlöf B, Devereux RB, Kjeldsen SE et al (LIFE Study Group). Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoint reduction in hypertension study (LIFE): a randomized trial against atenolol. Lancet 2002; 359(9311): 995–1003.
19. Lithell H, Hansson L, Skoog I et al (SCOPE Study Group). The Study on Cognition and Prognosis in the Elderly (SCOPE): principal results of a randomized double-blind intervention trial. J Hypertens 2003; 21(5): 875–886.
20. Julius S, Kjeldsen SE, Weber M et al (VALUE Trial Group). Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipine: the VALUE randomised trial. Lancet 2004; 363(9426): 2022–2031.
21. Schrader J, Luders S, Kulschewski A et al (MOSES Study Group). Morbidity and Mortality After Stroke. Eprosartan Compared with Nitrendipine for Secondary Prevention: principal results of a prospective randomized controlled study (MOSES). Stroke 2005; 36(6): 1218–2126.
22. Yusuf S, Diener HC, Sacco RL et al. Telmisartan to prevent recurrent stroke and cardiovascular events, Profess study. N Engl J Med 2008; 359(12):1225–1237.
23. Petrella RJ , Shlyakhto E , Konradi AO et al. Blood pressure responses to hypertension treatment and trends in cognitive function in patients with initially difficult-to-treat hypertension: a retrospective subgroup analysis of the Observational Study on Cognitive Function and SBP Reduction (OSCAR) study. J Clin Hypertens 2012; 14(2): 78–84.
24. Barnett AH, Bain SC, Bouter P et al.:Angiotensin-receptor blockade versus converting-enzyme inhibition in type 2 diabetes and nephropathy. N Engl J Med 2004; 351(19):1952–1961.
25. Špinar J, Vítovec J, Souček M et al. CORD: COmparsion of Recommended Doses of ACE inhibitors and angiotensin II receptor blockers. Vnitř Lék 2009; 55(5): 481–488.
26. Shih CJ1, Chen HT, Chao PW et al. Angiotensin-converting enzyme inhibitors, angiotensin II receptor blockers and the risk of major adverse cardiac events in patients with diabetes and prior stroke: a nationwide study.. J Hypertens 2015. Dostupné z DOI: http://dx.doi.org/10.1097/HJH.0000000000000804.
27. Mancia G, Seravalle G, Grassi G. Tolerability and treatment compliance with angiotensin II receptor antagonists. Am J Hypertens 2003; 16(12): 1066–1073.
28. Corrao G, Zambon A, Parodi A et al. Discontinuation of and changes in drug therapy for hypertension among newly-treated patients: a population-based study in Italy. J Hypertens, 2008 : 26(4) :819–824.
29. Bramlage P, Hasford J. Blood pressure reduction, persistence and costs in the evaluation of antihypertensive drug treatment: a review. Cardiovasc Diabetol 2009; 8 : 18. Dostupné z DOI: http://dx.doi.org/10.1186/1475–2840–8-18.
30. Gosmanova EO, Lu JL, Streja E et al. Association of medical treatment nonadherence with all-cause mortality in newly treated hypertensive US veterans. Hypertension 2014; 64(5): 951–957.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2016 Issue 2-
All articles in this issue
- Use of systemic glucocorticoids in therapy of infectious diseases
- Proton pump inhibitors and their effect on the bone
- Fecal microbiota transplantation
- Severe osteoporosis – the story of chronic medication-related hyponatremia
- Lead poisoning. A surprising cause of constipation, abdominal pain and anemia
- Chronic pancreatitis diagnosed after the first attack of acute pancreatitis
- AT1-blockers in the treatment of hypertension: summary
- The patient complains of spinal pain or fatigue and weakness. How do I recognize whether their cause is spondylarthrosis, the patient’s age or multiple myeloma?
- The rational diagnostic of cholangiocarcinoma
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- The patient complains of spinal pain or fatigue and weakness. How do I recognize whether their cause is spondylarthrosis, the patient’s age or multiple myeloma?
- Lead poisoning. A surprising cause of constipation, abdominal pain and anemia
- AT1-blockers in the treatment of hypertension: summary
- Proton pump inhibitors and their effect on the bone
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

