-
Medical journals
- Career
Včasná diagnostika familiární hypercholesterolemie v České republice v rámci projektu MedPed
Authors: Tomáš Freiberger 1; Michal Vrablík 2
Authors‘ workplace: Genetická laboratoř, Centrum kardiovaskulární a transplantační chirurgie, Brno, ředitel doc. MUDr. Petr Němec, CSc., MBA, FETCS 1; III. interní klinika1. LF UK a VFN Praha, přednosta prof. MUDr. Štěpán Svačina, DrSc., MBA 2
Published in: Vnitř Lék 2015; 61(11): 942-945
Category: Reviews
Overview
Nedávné studie ukázaly, že prevalence familiární hypercholesterolemie (FH) je přibližně dvojnásobná oproti dřívějším předpokladům a onemocnění tak postihuje přibližně jednoho z 250 jedinců obecné populace. Jedná se tedy o nejčastější vrozené metabolické onemocnění vůbec. V důsledku geneticky podmíněné poruchy v metabolizmu LDL-cholesterolu dochází k jeho hromadění v cirkulaci a ve tkáních, což vede předčasnému rozvoji aterosklerózy. Neléčení jedinci mohou mít infarkt myokardu ve 3. nebo 4. dekádě života, až v jedné třetině případů s fatálním koncem. Onemocnění je celosvětově nedostatečně diagnostikováno a léčeno. V České republice běží již od roku 1998 projekt MedPed, který se soustředí na včasnou diagnostiku FH s cílem zahájit léčbu co nejdříve, a snížit tak u postižených jedinců riziko předčasné klinické manifestace ischemické choroby srdeční a předčasného úmrtí. Důležitým bodem projektu je kaskádovitý screening mezi příbuznými pacientů s FH. V celonárodní databázi evidujeme již více než 6 350 pacientů s FH, což představuje asi 16 % z očekávaného počtu pacientů v České republice. Takový záchyt nás řadí mezi nejúspěšnější země na světě, ale i s ohledem na příchod nových terapeutických možností zůstává detekce a včasné zahájení léčby nemocných s FH v centru naší pozornosti.
Klíčová slova:
familiární hypercholesterolemie – kardiovaskulární riziko – kaskádovitý screening – MedPedÚvod
Riziko předčasné klinické manifestace aterosklerózy a úmrtí v mladém věku je u pacientů s familiární hypercholesterolemií (FH) velmi významně zvýšeno [1]. Dnes již není pochyb o tom, že zvýšené sérové koncentrace LDL-cholesterolu jsou klíčovým rizikovým faktorem rozvoje aterosklerózy [2]. U pacientů s FH dochází v důsledku genetické poruchy k hromadění LDL-cholesterolu v cirkulaci a jeho ukládání do stěny cév i dalších tkání, a to již od narození, což je důležitý rozdíl oproti polygenně podmíněným případům hypercholesterolemie a významný činitel podmiňující vysoké riziko vzniku kardiovaskulárního onemocnění. Klinicky se FH projevuje vznikem šlachových xantomů a časnými projevy ischemické choroby srdeční (ICHS) [3].
Epidemiologie FH
Nedávné studie založené na stanovení diagnózy FH podle modifikovaných široce užívaných kritérií (Dutch Lipid Network Criteria) u rozsáhlého vzorku více než 69 000 osob dánské populace [4], resp. na molekulárně genetické analýze více než 104 000 jedinců nizozemské populace [5] ukázaly, že prevalence FH je vyšší než 1 : 500, jak se dlouho uvádělo na základě práce J. L. Goldsteina et al ze 70. let minulého století [6]. Podle zmíněných recentních studií trpí familiární hypercholesterolemií přibližně 1 osoba z 250. Homozygotní FH je vzácná a výrazně závažnější forma onemocnění, postihující 1 ze 160 000 až 300 000 osob [5]. Klinická manifestace aterosklerózy se může u ní objevit v adolescentním věku nebo dokonce dříve, přítomny jsou kožní nebo šlachové xantomy. Hodnoty LDL-cholesterolu jsou u homozygotní formy přibližně dvojnásobné oproti heterozygotní FH [1].
Přestože FH je velmi dobře definované onemocnění a přestože existuje účinná hypolipidemická léčba, většina pacientů s FH zůstává nediagnostikována nebo není adekvátně léčena [7]. Podle zmíněné dánské studie mají neléčení pacienti ve srovnání s obecnou populací 13krát vyšší riziko vzniku ICHS. Pozoruhodné je, že pacienti s FH, kteří léčeni jsou, mají pořád riziko vzniku ICHS 10krát zvýšené [4]. To svědčí o tom, že používaná léčba nevede u pacientů s FH k dostatečnému snížení hladin LDL-cholesterolu, respektive léčba zahájená v pozdějším věku není schopna zabránit manifestaci klinických komplikací aterosklerózy.
Fenotyp FH a diagnostika
Kromě předčasného výskytu kardiovaskulárních příhod v rodinné a osobní anamnéze (do 55 let u mužů a 60 let u žen) je potřeba věnovat pozornost přítomnosti šlachových xantomů, které jsou pro FH patognomické. Vyšetření Achillovy šlachy a šlach dalších extenzorů by nemělo být opomenuto, i když je potřeba říci, že absence šlachových xantomů FH zdaleka nevylučuje. Xantelazmata víček a arcus lipoides na rohovce patří sice k nespecifickým projevům choroby, ovšem jejich výskyt v nižších věkových skupinách může diagnózu FH podpořit. Klinické projevy obvykle chybějí u dětí a mladých dospělých. U pacientů s homozygotní formou FH se objevují i kožní xantomy a typická je akcelerovaná ateroskleróza v oblasti kořene aorty, při podezření na homozygotní FH je tedy potřeba pátrat po aortální stenóze nebo regurgitaci. U asymptomatických jedinců je nezbytný pravidelný screening subklinické aterosklerózy [8,9].
Důležitým diagnostickým pomocníkem jsou koncentrace celkového a především LDL-cholesterolu, přičemž by se mělo vycházet alespoň ze 2 měření. Nejpřesnější je použití hodnot specifických pro danou populaci, věk a pohlaví. Diagnóza FH je zvažována při překročení hranice 95. percentilu za předpokladu, že byla vyloučena sekundární hypercholesterolemie. Orientačně by diagnóza FH měla být zvažována při hodnotách celkového cholesterolu > 8 mmol/l a LDL-cholesterolu > 5 mmol/l. Koncentrace triglyceridů jsou typicky v normálních mezích, často jsou zvýšené hodnoty lipoproteinu (a). Samotná biochemická kritéria ovšem nejsou pro potvrzení diagnózy FH dostačující, a to vzhledem k překryvu s hodnotami nacházenými u části zdravé populace, resp. u osob s jinými formami hypercholesterolemie. Kritéria vytvořená v rámci mezinárodního projektu MedPed zohledňují skutečnost, že příbuzní pacienta s již diagnostikovanou FH mají ve srovnání s jedinci obecné populace vyšší pravděpodobnost, že jsou rovněž postiženi, a proto pro ně byly vypočteny odlišné hraniční hodnoty rozhodné pro diagnózu, a to v závislosti na stupni příbuznosti (tab. 1) [10].
Table 1. Koncentrace celkového a LDL-cholesterolu (v závorkách) rozhodné pro stanovení diagnózy FH - MedPed kritéria. 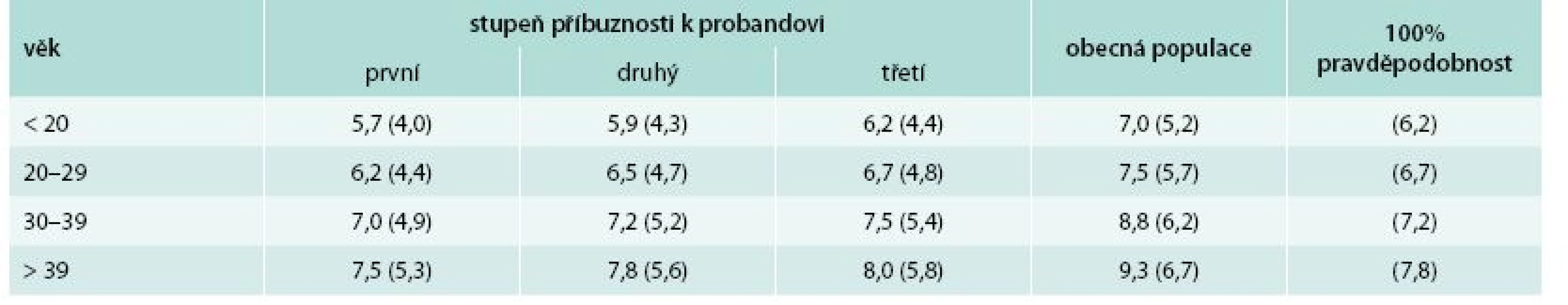
Předpokladem jsou normální koncentrace triglyceridů a vyloučení sekundární hypercholesterolemie. Koncentrace celkového a LDL-cholesterolu jsou vyjádřeny v mmol/l Zřejmě nejpřesnější je použití komplexních diagnostických kritérií. Využívána jsou britská kritéria založená na datech z registru Simona Brooma nebo nejvíce rozšířený nizozemský skórovací systém (Dutch Lipid Network Criteria) [11]. Tento systém je poměrně sofistikovaný, body jsou přidělovány za výskyt ICHS (do 55 let u mužů nebo 65 let u žen) nebo hypercholesterolemie v rodině, ICHS v osobní anamnéze (do 55 let u mužů nebo 65 let u žen), přítomnost šlachových xantomů nebo arcus lipoides do 45 let věku, za zvýšenou koncentraci LDL-cholesterolu (diferencovaně podle míry zvýšení) a nakonec za nález kauzální mutace v genu pro LDL receptor, pro apolipoprotein B nebo v genu PCSK9 (tab. 2) [11].
Table 2. Dutch Lipid Network Criteria (DLNC) pro diagnózu familiární hypercholesterolemie 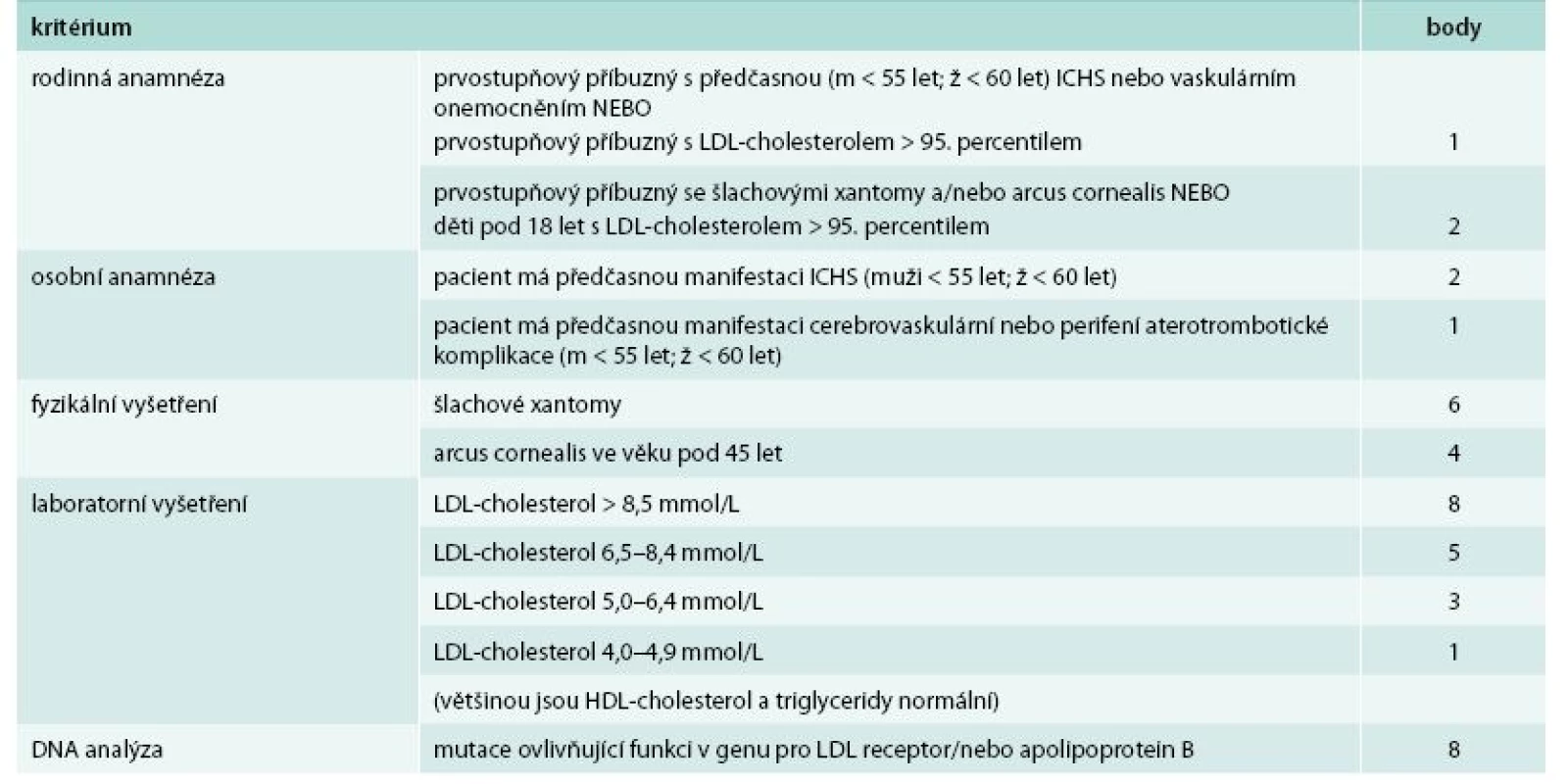
V každé z kategorií (rodinná anamnéza, osobní anamnéza, fyzikální vyšetření, laboratorní vyšetření, DNA analýza) je zvolena jen jedna (ta nejvyšší platná) bodová hodnota. Diagnóza FH je jistá při DLNC skóre ≥ 8, pravděpodobná při DLNC skóre 6–8, možná při DLNC skóre 3–5. Genetika FH
FH se vyznačuje autozomálně dominantním typem dědičnosti, což znamená přítomnost onemocnění u jednoho z rodičů, jednoho z prarodičů, poloviny sourozenců a poloviny potomků postiženého probanda. V případě, že jeden z rodičů má heterozygotní FH, existuje tedy 50% pravděpodobnost, že i potomek bude mít FH. V každé rodině pacienta s FH je tak obvykle několik, někdy to mohou být i desítky, postižených příbuzných. Pečlivý odběr rodinné anamnézy a vyšetření dostupných rodinných příslušníků již diagnostikovaného pacienta je proto zcela zásadní. Většina těchto příbuzných totiž o svém onemocnění neví, přitom jsou ve velmi vysokém riziku předčasné manifestace závažné kardiovaskulární příhody, jíž lze včasným zahájením hypolipidemické léčby předejít nebo ji přinejmenším významně oddálit.
Fenotyp autozomálně dominantní hypercholesterolemie (ADH) může být způsoben defektem různých genů. Stále více je tedy v původním významu familiární hypercholesterolemie používán pojem ADH, který zahrnuje:
- klasickou FH podmíněnou mutacemi v genu pro LDL receptor (LDLR)
- familiární defekt apolipoproteinu (apo) B-100 (FDB) podmíněný defektem genu pro apoB (APOB)
- tzv. non-FH/non-FDB ADH, případně non-LDLR/non-APOB ADH, FH3 či ADH3, která je podmíněna defektem genu PCSK9 nebo mutacemi jiného, dosud neznámého genu [12]
U homozygotní FH je defekt přítomen na obou alelách zmíněných genů, oba rodiče jsou heterozygoti FH a je u nich 25% riziko, že potomek bude trpět homozygotní formou choroby.
S homozygotní FH je spojen i defekt genu LDLRAP1 (LDL receptor adaptor protein 1), označovaný také jako ARH, jehož defekt je příčinou autozomálně recesivní formy onemocnění (ARH – autozomálně recesivní hypercholesterolemie), která klinicky odpovídá homozygotní formě ADH. Adaptorový protein interaguje s cytoplazmatickým koncem LDL receptoru a s klatrinem (clathrin) a je spoluzodpovědný za endocytózu LDL receptorů cestou vezikul obdaných klatrinem. Jeho defekt vede k poruše internalizace LDL receptoru s navázaným LDL-cholesterolem, což je důvodem zvýšených koncentrací LDL-cholesterolu v cirkulaci. Postižený jedinec má defektní obě alely, zatímco jeho rodiče jsou zdraví přenašeči choroby. V rodinné anamnéze tak není patrný vertikální přenos onemocnění, což je výrazná odlišnost oproti FH, resp. ADH. Rodiče nesoucí poškozený gen mají 25% pravděpodobnost narození potomka s ARH [13]. Onemocnění je vzácné, více se vyskytuje u příbuzenských sňatků, které jsou ovšem v podmínkách České republiky nečetné.
Molekulárně genetické vyšetření přináší potvrzení diagnózy FH, a tím monogenní povahy onemocnění, což je cenné pro individuální posouzení kardiovaskulárního rizika pacientů, zejména u klinicky a laboratorně nejasných případů. Je to také důležité pro provádění kaskádovitého screeningu v rodinách pacientů. Pokud je v rodině známa mutace, je velmi rychle možno diagnózu potvrdit či vyloučit u všech rodinných příslušníků. I jedinci s hodnotami cholesterolu, které nesplňují diagnostická kritéria FH, pokud jsou nositeli kauzální mutace FH, jsou totiž ve vysokém riziku předčasné klinické manifestace aterosklerózy.
Projekt MedPed
Skutečnost, že přes existenci účinné terapie zůstává většina pacientů s FH nediagnostikována a neléčena, nebo je léčena neadekvátně, vyvolala mezinárodní úsilí tuto situaci zvrátit. V roce 1994 vznikl projekt MedPed (Make early diagnosis to Prevent early deaths), do něhož se postupně zapojilo více než 30 zemí a jehož hlavním cílem je významně snížit riziko předčasného úmrtí u pacientů s FH [14]. Hlavními prostředky jsou včasné stanovení diagnózy a včasná a dlouhodobá léčba postižených osob, přičemž důraz je kladen zejména na vyhledávání ohrožených jedinců mezi příbuznými již diagnostikovaných pacientů, a také na molekulárně genetickou diagnostiku. Bylo opakovaně vykalkulováno, že kaskádovitý screening pacientů s FH uplatňovaný v rámci projektu je vysoce efektivní i z hlediska vynaložených nákladů. Česká republika se k projektu připojila v roce 1998 [15].
Síť projektu MedPed v ČR je nyní tvořena 63 aktivními centry a spolupracovníky. Sestává ze 2 párů národních center v Praze a v Brně, 15 regionálních center pro dospělé a 10 pro děti, 18 specializovaných pracovišť pro dospělé a 7 pro děti a dalších 9 spolupracujících lékařů. Síť je dynamická a stále se zapojují nová centra, některá naopak končí. Organizace projektu probíhá tak, že lékaři různých odborností, kteří přicházejí do styku s pacienty s FH, mají možnost přímého zapojení do projektu, nebo mohou své pacienty odeslat do některého ze sítě center, které zároveň slouží jako konziliární pracoviště nejen pro těžké či atypické případy FH, ale pro všechny závažné dyslipidemie.
V současné době máme v databázi evidováno 6 354 pacientů z 4 755 rodin. Počet pacientů s FH/FDB zařazených do databáze tak činí 15,9 % z očekávaného počtu asi 40 000 pacientů v ČR (při uvažované prevalenci 1 : 250). U 599 pacientů byla diagnóza stanovena do 19 let věku. Vzorek DNA je k dispozici od 4 049 nepříbuzných pacientů a mutace v genu pro LDL receptor nebo apoB byla zatím prokázána u 1 223 z nich. Kauzální mutace v genu PCSK9 nebyla v české populaci doposud detekována. V ČR evidujeme také 12 pacientů s homozygotní formou FH, resp. FDB.
Závěr
FH je závažná dědičná porucha lipidového metabolizmu, která vede k předčasným úmrtím v důsledku klinické manifestace aterosklerózy. Vzhledem k tomu, že existuje účinná terapie, je včasné stanovení diagnózy a včasné zahájení léčby kriticky důležité. Projekt MedPed v České republice významně přispívá k vyhledání nových pacientů s FH, jejich léčbě a dlouhodobému sledování.
Tato práce byla podpořena projektem IGA MZd ČR č. NT14186. Poděkování patří všem spolupracujícím lékařům (jejich seznam je uveden na http://athero.cz/cze/projekt-medped.html), koordinátorce Editě Firoňové, pracovníkům zajišťujícím molekulární diagnostiku, zejména doc. RNDr. Lence Fajkusové, CSc., Mgr. Lukáši Tichému, Ph.D., Marii Plotěné a Mgr. Petře Zapletalové, společnosti Galén Symposion a Mgr. Haně Středové za pomoc s logistikou projektu a sponzorujícím společnostem Amgen, AOP Orphan, Krka, MSD, Pfizer a Sanofi.
MUDr. Tomáš Freiberger, Ph.D.
tomas.freiberger@cktch.cz
Genetická laboratoř, Centrum kardiovaskulární a transplantační chirurgie, Brno
www.cktch.cz
Doručeno do redakce 25. 11. 2015
Přijato po recenzi 29. 11. 2015
Sources
1. Goldstein, JL, Hobbs, HH, Brown, MS. Familial hypercholesterolemia. In: Scriver CR et al. The metabolic and molecular bases of inherited disease. 8th ed. New York, McGraw-Hill 2001 : 2863–2914.
2. Baigent C, Blackwell L, Emberson J et al. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet 2010; 376(9753): 1670–81.
3. Marks D, Thorogood M, Neil SM et al. A review on the diagnosis, natural history, and treatment of familial hypercholesterolaemia. Atherosclerosis 2003; 168(1): 1–14.
4. Benn M, Watts GF, Tybjaerg-Hansen A et al. Familial hypercholesterolemia in the danish general population: prevalence, coronary artery disease, and cholesterol-lowering medication. J Clin Endocrinol Metab 2012; 97(11): 3956–3964.
5. Sjouke B, Kusters DM, Kindt I et al. Homozygous autosomal dominant hypercholesterolaemia in the Netherlands: prevalence, genotype-phenotype relationship, and clinical outcome. Eur Heart J 2015; 36(9): 560–565.
6. Goldstein JL, Brown MS. Familial hypercholesterolemia: identification of a defect in the regulation of 3-hydroxy-3-methylglutaryl coenzyme A reductase activity associated with overproduction of cholesterol. Proc Natl Acad Sci USA 1973; 70(10):2804–2808.
7. Nordestgaard BG, Chapman MJ, Humphries SE et al. For the European Atherosclerosis Society Consensus Panel. Familial hypercholesterolaemia is underdiagnosed and undertreated in the general population: guidance for clinicians to prevent coronary heart disease: Consensus Statement of the European Atherosclerosis Society. Eur Heart J 2013; 34(45): 3478–3490a.
8. Descamps OS, Tenoutasse S, Stephenne X et al. Management of familial hypercholesterolemia in children and young adults: consensus paper developed by a panel of lipidologists, cardiologists, paediatricians, nutritionists, gastroenterologists, general practitioners and a patient organization. Atherosclerosis 2011; 218(2): 272–280.
9. Vrablík M, Češka R, Freiberger T et al. Souhrn konsenzu panelu expertů European Atherosclerosis Society k otázce diagnostiky a klinickému vedení nemocných s homozygotní formou familiární hypercholesterolemie. Hypertenze a KV prevence 2015, 4 : 59–61.
10. Williams RR, Hunt SC, Schumacher MC et al. Diagnosing heterozygous familial hypercholesterolemia using new practical criteria validated by molecular genetics. Am J Cardiol 1993, 72(2): 171–176.
11. van Aalst-Cohen ES, Jansen AC, Tanck MW, Defesche JC, Trip MD, Lansberg PJ et al. Diagnosing familial hypercholesterolaemia: the relevance of genetic testing. Eur Heart J 2006; 27(18): 2240–2246.
12. Varret M, Abifadel M, Rabès JP et al. Genetic heterogeneity of autosomal dominant hypercholesterolemia. Clin Genet 2008; 73(1): 1–13.
13. Rader DJ, Cohen J, Hobbs HH. Monogenic hypercholesterolemia: new insights in pathogenesis and treatment. J Clin Invest 2003; 111(12): 1795–803.
14. World Health Organization: Familial hypercholesterolemia – report of a second WHO Consultation. Geneva, Switzerland: World Health Organization 1999 (WHO publication No. WHO/HGN/FH/CONS/99.2). Dostupné z WWW: <http://apps.who.int/iris/bitstream/10665/66346/1/WHO_HGN_FH_CONS_99.2.pdf>.
15. Freiberger T, Vrablík M. 15 let projektu MedPed v České republice. Hypertenze a KV prevence 2013, 2 : 58–60.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2015 Issue 11-
All articles in this issue
- Ateroskleróza: od etiologie po možnosti ovlivnění
- Praktický přístup ke statinové intoleranci
- Včasná diagnostika familiární hypercholesterolemie v České republice v rámci projektu MedPed
- Inhibice PCSK9 jako nová naděje pro nemocné s familiární hypercholesterolemií, statinovou intolerancí a posléze pro všechny pacienty v nejvyšším kardiovaskulárním riziku? Zaměřeno na alirokumab – Praluent®
- Evolokumab a projekt PROFICIO: první výsledky
- Postavení lipoproteinové aferézy v současnosti
- Vliv kombinace simvastatinu s ezetimibem na krevní lipidy a na kardiovaskulární příhody u diabetiků (komentář k výsledkům subanalýzy studie IMPROVE-IT)
-
Co přináší přehledný článek o důkazech redukce makrovaskulárního rizika u pacientů s aterogenní dyslipidemií?
Zpráva o konsenzu expertů o významu kombinované terapie fenofibrátem a statinem Hana Rosolová - Studie TECOS, EXAMINE a SAVOR – čím se liší a co přinášejí?
- Klinický význam nových bazálních inzulinů a inzulin Toujeo® 300 U/ml
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Klinický význam nových bazálních inzulinů a inzulin Toujeo® 300 U/ml
- Ateroskleróza: od etiologie po možnosti ovlivnění
- Postavení lipoproteinové aferézy v současnosti
- Praktický přístup ke statinové intoleranci
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

