-
Medical journals
- Career
Mají natriuretické peptidy novou šanci v léčbě srdečního selhání?
Authors: Lenka Špinarová 1; Jindřich Špinar 2; Jiří Vítovec 1
Authors‘ workplace: I. interní kardio-angiologická klinika LF MU a FN u sv. Anny Brno, přednostka prof. MUDr. Lenka Špinarová, Ph. D., FESC 1; Interní kardiologická klinika LF MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Jindřich Špinar, CSc., FESC 2
Published in: Vnitř Lék 2014; 60(12): 1076-1080
Category: 70. birthday prof. MUDr. Michael Aschermann, DrSc., FESC, FACC
Overview
Vliv natriuretických peptidů na kardiovaskulární a renální systém představuje potenciální možnosti využít tyto působky v léčbě hypertenze a srdečního selhání, i když současné výsledky klinických studií nejsou povzbudivé. Syntetický B-natriuretický peptid sice prokázal krátkodobé hemodynamické zlepšení pacientů, nicméně z pohledu renálních funkcí a dlouhodobé prognózy pacientů byl účinek sporný. Naopak novou nadějí je ularitid a duální inhibitor neprilyzinu a ARB: LCZ 696, u nejž probíhají klinické studie a předchozí data z pilotních studií se jeví slibná.
Klíčová slova:
inhibitory vazopeptidáz – natriuretické peptidy – srdeční selháníÚvod
Léky, které používají účinky natriuretických peptidů lze rozdělit na:
- natriuretické peptidy – ANP, BNP – nesiritid, CNP, DNP, ularitid, cenderidid
- zábrana degradace natriuretických peptidů – inhibitory neutrálních endopeptidáz (neprilyzin)
Natriuretické peptidy
Historie natriuretických peptidů sahá do roku 1981, kdy byl popsán extrakt ze srdečních síní, který způsobuje natriurézu a vazodilataci. V roce 1984 byla popsána chemická struktura síňového natriuretického peptidu ANP, v roce 1988 byl izolovaný z mozku prasete brain natriuretic peptid – BNP a v roce 1990 C-natriuretic peptid.
Atriální natriuretický peptid (ANP)
Při zvýšení tlaku v pravé síni při hypervolemii je secernován ze srdečních síní natriuretický peptid. ANP je C-reziduální peptid, který je odvozený ze 126 aminokyselinového prekurzoru pro-ANP, který je skladován v sekrečních granulích. Jako N-terminální fragment ANP (N-ANP) se označuje zbytek proANP po odštěpení vlastního ANP. N-ANP je odstraňován mnohem pomaleji a tak cirkuluje v oběhu ve vyšší koncentraci než vlastní ANP.
Mozkový natriuretický peptid (BNP)
Byl objeven v mozku prasete – odtud jeho jméno – ale u člověka je téměř výhradně vylučovaný ze srdce, především z komor. BNP vzniká z prepro-BNP, přes proBNP, který je závěrečně rozštěpen na vlastní BNP a N-terminál proBNP (NT-proBNP), obr 1. Má podobné účinky jako ANP, proto tyto dva peptidy fungují jako duální kardiální natriuretický peptidový systém. Oba peptidy potlačují uvolňování endotelinu , inhibují sympatoadrenální systém, stimulují vagová vlákna, inhibují renin-angiotenzin-aldosteronový systém, způsobují natriurézu a vazodilataci a snižují proliferaci svalových buněk.
Image 1. B-natriuretický peptid 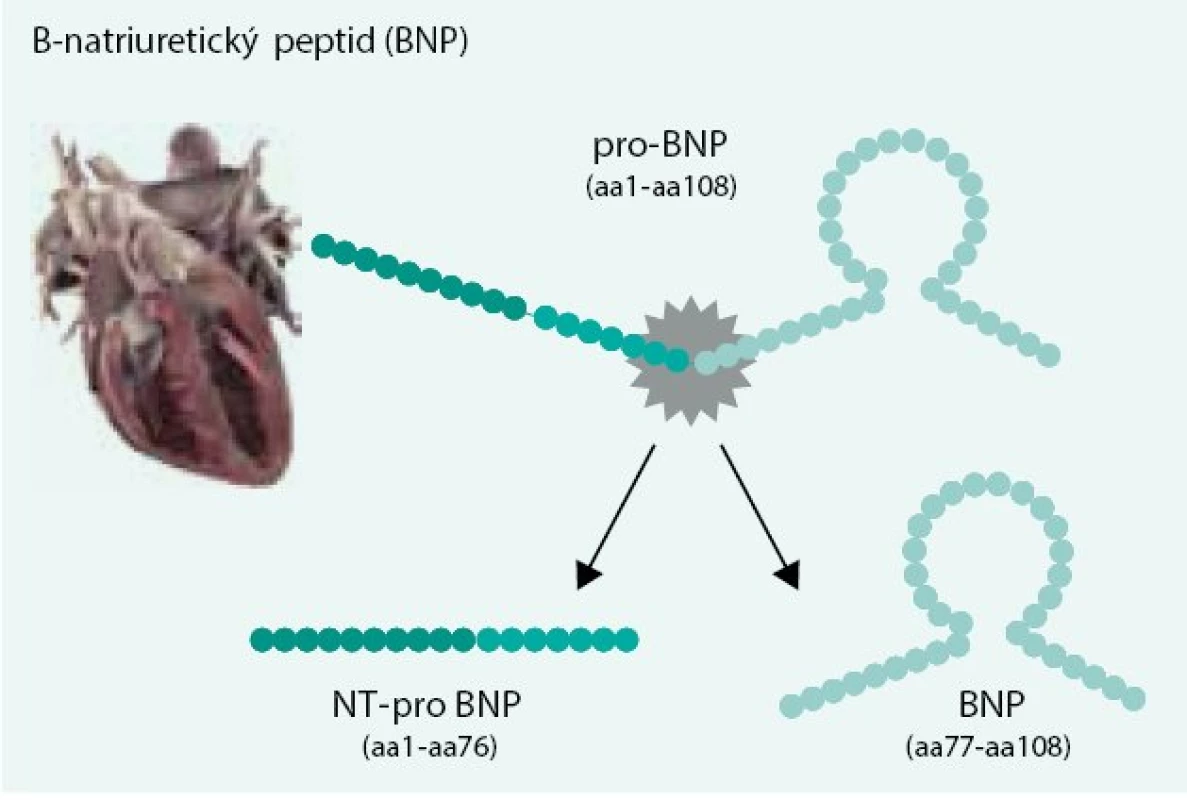
Natriuretické peptidy jsou odbourávány štěpením neutrálními endopeptidázami nebo vazbou na clearensový receptor. Několik menších studií s podáváním nesiritidu prokázalo jeho příznivé účinky na hemodynamiku: NATRECOR či NESIRITIDE [1,2]. Větší studie VMAC (Vasodilatation in the Management of Acute Congestive Heart Failure) srovnávala u 489 nemocných s dekompenzovaným srdečním selháním nesiritid, nitrožilní nitroglycerin nebo placebo. Při podání nesiritidu došlo k výraznějšímu poklesu středního tlaku v zaklínění ve srovnání s nitroglycerinem ve 3. a 24. hod. Zmírnění dušnosti bylo obdobné po nesiritidu i nitroglycerinu, ale nebylo pozorováno po placebu. Vzhledem k tomu, že ve studii VMAC byla užita nižší dávka nesiritidu, byla symptomatická hypotenze pouze v 5 % obdobně jako po nitroglycerinu (tab. 1) [3].
Table 1. Zhoršení ledvinných funkcí ve studiích s nesiritidem 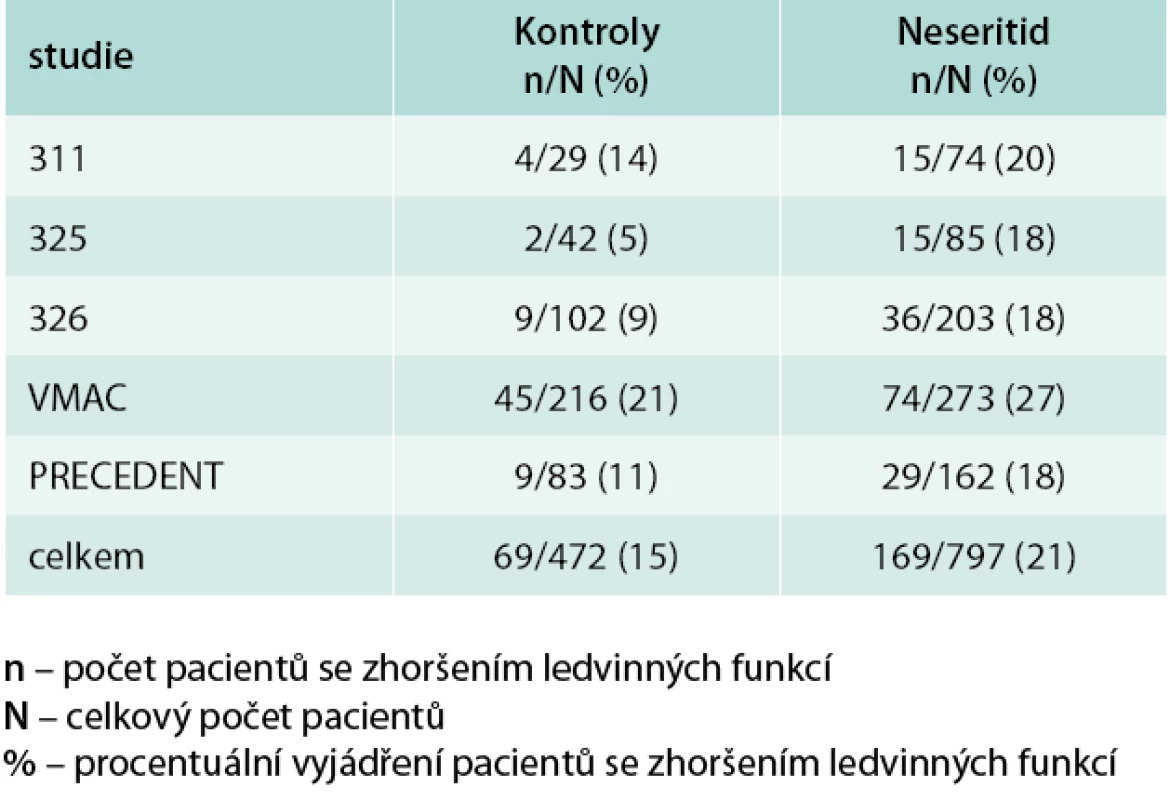
Syntetický BNP – nesiritid – byl na základě těchto výsledků povolen k užívání v USA a v minulých letech byl i často předepisován nemocným (statisíce preskripce/rok). V roce 2013 však jeho preskripce klesla na minimum. Nesiritid nemá schválení ve většině evropských zemí, ani v České republice.
Při provedení metaanalýzy studií sledujících podávání nesiritidu u pacientů s dekompenzací srdečního selhání bylo dokonce zjištěno zhoršení renálních funkcí ve skupině léčených nesiritidem, ať již v porovnání s placebem či léčbou pozitivně inotropními látkami (tab. 1) [4].
Studie ASCEND-HF (Acute Study of Clinical Effectivness of Nesiritide in Decompensated Heart Failure) zařadila 7 007 nemocných s akutním srdečním selháním, kteří museli být randomizováni do 24 hod od vzniku příznaků a ke standardní léčbě byl přidán nesiritid nebo placebo na dobu 24–168 hod (studii neschválil SÚKL, proto v ČR neprobíhala). Primárním cílem bylo posouzení dušnosti na 7stupňové škále za 6 a 24 hod a 30denní mortalita a rehospitalizace pro srdeční selhání [5].
Z pohledu primárního cíle – změny dušnosti – bylo dosaženo pozitivního výsledku. Nebyl potvrzen negativní vliv nesiritidu na renální funkce. Na druhé straně výskyt hypotenze, a to jak symptomatické, tak asymptomatické, byl po nesiritidu téměř dvojnásobný.
Druhý primární cíl – 30denní rehospitalizace a mortalita – ukazuje tab. 2. 30denní mortalita a rehospitalizace ukazují trend ve prospěch nesiritidu, který však nedosáhl statistické významnosti. Z tab. 2 je patrné, že nesiritid mortalitu ani morbiditu neovlivnil.
Table 2. 30denní mortalita a rehospitalizace ve studii ASCEND-HF 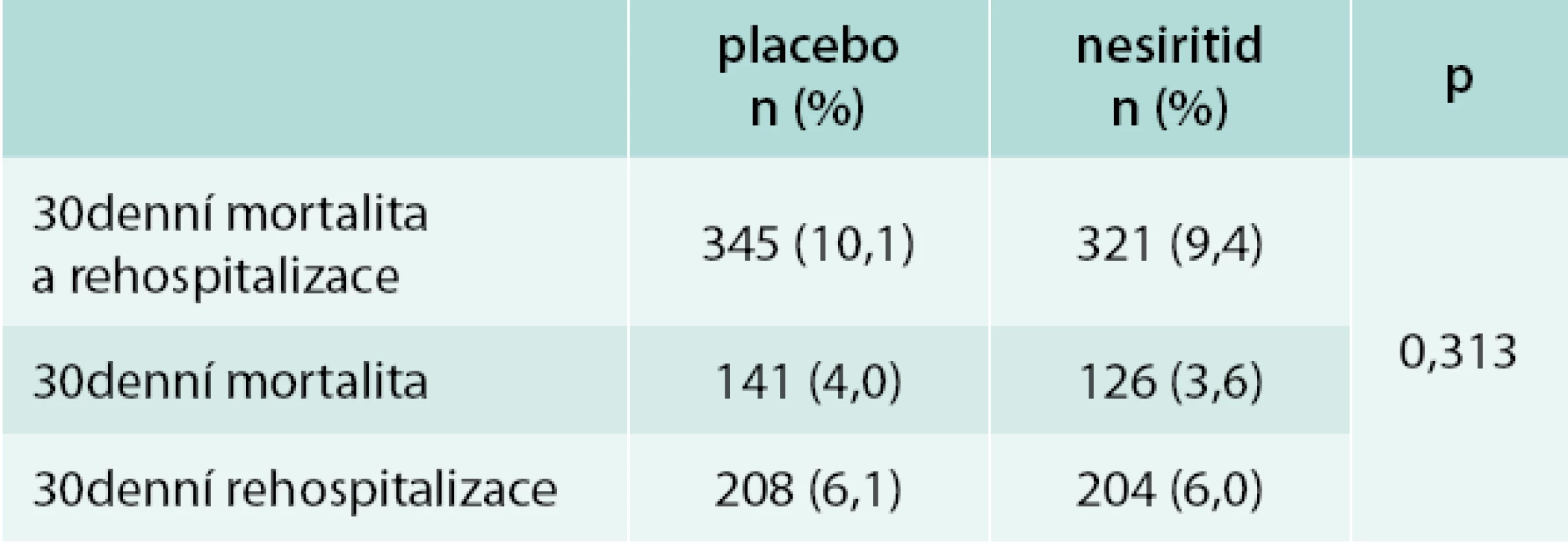
Velká pozornost byla věnována bezpečnosti podávání nesiritidu, především výskytu zhoršení renálních funkcí a hypotenze (tab. 3). Z tab. 3 je patrné, že nebyl potvrzen negativní vliv nesiritidu na renální funkce a že z tohoto pohledu byl nesiritid bezpečný a to dokonce i u nemocných s úvodně sníženou glomerulární filtrací. Na druhé straně výskyt hypotenze, a to jak symptomatické, tak asymptomatické, byl po nesiritidu téměř dvojnásobný.
Table 3. Zhoršení renálních funkcí a hypotenze ve studii ASCEND-HF 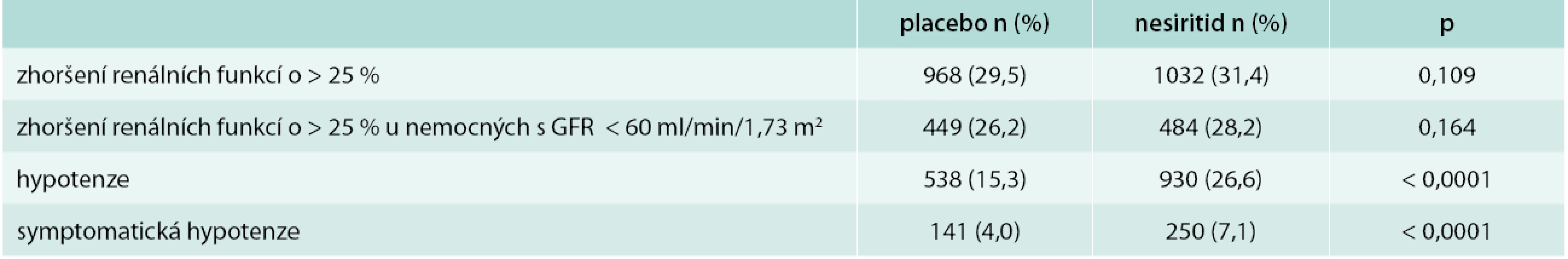
Z dalších vedlejších závažných příhod je třeba zmínit dvojnásobný výskyt reinfarktu při léčbě nesiritidem (14 vs 6), který ale nedosáhl statistické významnosti.
Steering committee pak navrhla tyto závěry:
- nesiritid nesnižuje 30denní rehospitalizace
- nesiritid nesnižuje 30denní mortalitu
- nesiritid zlepšuje dušnost po 6 a 24 hod
- nesiritid nezhoršuje renální funkce do 30 dní [5]
Zcela recentní studie ROSE-AHF měla za cíl prokázat hypotézu, že nízké dávky nesiritidu přidané k diuretikům u pacientů s akutní dekompenzací srdečního selhání a sníženými renálními funkcemi mohou působit pozitivně. Bohužel, ani tato studie neprokázala, že by podání nesiritidu zlepšilo dekongesci – hodnocenou jak objemem moči za 72 hod, tak ledvinné funkce – hodnocené poklesem cystatinu [6].
Central nervous system natriuretický peptid (CNP)
Současná doba je ve znamení objevování dalších natriuretických peptidů, které jsou označovány CNP, DNP atd, a je zkoumán nejen jejich prediktivní význam, ale i jejich možné terapeutické využití.
CNP byl původně izolován z mozku v roce 1990, má však mnohem větší distribuci a částečně se sám a jeho receptory nacházejí v periferních krevních cévách.
Kombinací CNP a DNP je syntetický peptid cenderidid, který nyní rovněž probíhá začátkem klinických studií u akutního srdečního selhání.
Ularitid
Je to syntetická forma urodilatinu, hormonu, který je produkován v buňkách distálního ledvinného tubulu. Patří mezi natriuretické peptidy. Reguluje vaskulární a renální homeostázu, zvyšuje vazodilataci a exkreci sodíku, chloridu a snižuje neurohumorální vazokonstrikční aktivaci.
Data z metaanalýz používání nesiritidu poukázala na zvýšené riziko zhoršení renálních funkcí. Proto je snaha najít látku, která by zlepšila hemodynamické parametry a zachovala ledvinné funkce.
Ve studii SIRIUS I, která podávala ularitid u akutní dekompenzace srdečního selhání, došlo po podání 24hodinové infuze ke snížení tlaku v zaklínění.
Studie SIRIUS II sledovala hemodynamické a klinické efekty ularitidu podaného pacientům s dekompenzací srdečního selhání. Po 6 hodinách podávání došlo ve všech skupinách aktivní léčby ke statisticky významnému poklesu tlaku v zaklínění a zlepšení dušnosti oproti placebu.
Ularitid v dávce 15 a 30 ng/kg/min snížil systémovou vaskulární rezistenci a zvýšil srdeční index.
Nežádoucí účinky (tab. 4) byly mírné nebo střední: nejčastěji šlo o pokles krevního tlaku (5,4 %), pocení (4,2 %) a slabost (3,0 %). Pacienti léčeni ularitidem měli méně závažných komplikací (SAE) a úmrtí než pacienti na placebu.
Table 4. Nežádoucí účinky a úmrtí ve studii SIRIUS II 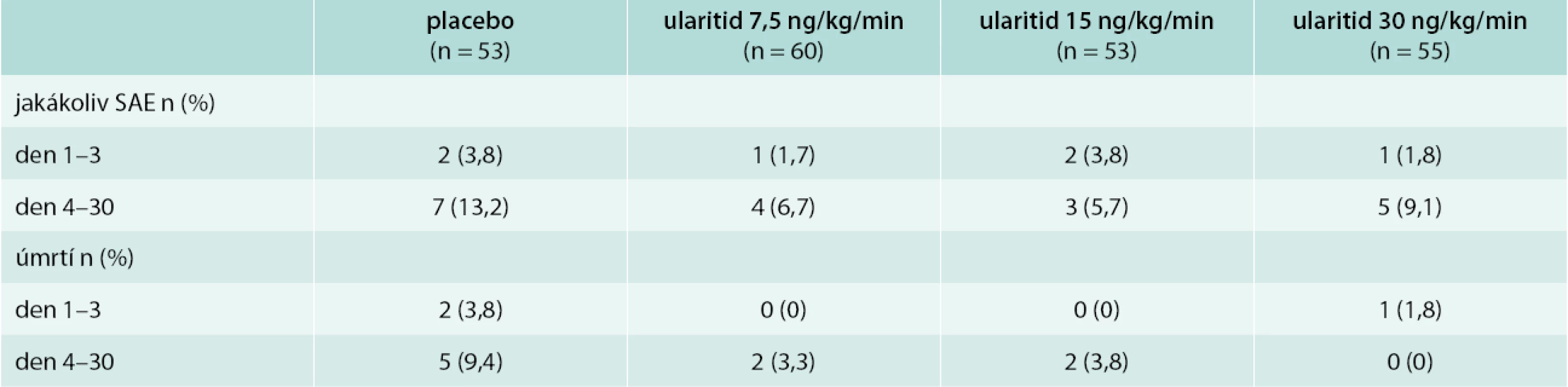
Ve skupině pacientů užívajících ularitid v dávce 15 ng/kg/min a 30 ng/kg/min byla kratší doba hospitalizace (122 a 158 hod) ve srovnání s 201 a 192 hod u placeba a dávky 7,5 ng/kg/min. Tento rozdíl však nedosáhl statistické významnosti [7].
Na potvrzení účinku ularitidu na mortalitu je však třeba další randomizované studie, která nyní probíhá. Studie TRUE-AHF sleduje účinek 48hodinové kontinuální infuze ularitidu (15 ng/kg/min) vs placebo na klinický stav pacientů s akutně dekompenzovaným srdečním selháním. Vstupní kritéria jsou: pacienti přijati k neplánované hospitalizaci pro akutní dekompenzaci srdečního selhání, které je definované jako klidová dušnost, která se zhoršovala v průběhu minulých týdnů, RTG známky srdečního selhání, brain natriuretic peptide (BNP) > 500 pg/ml nebo N-terminal pro-brain natriuretic peptide (NT-pro BNP) > 2 000 pg/ml. V době randomizace je požadovaný systolický krevní tlak ≥ 116 mm Hg a ≤ 180 mm Hg. Klidová dušnost musí přetrvávat navzdory terapii srdečního selhání, která musí obsahovat intravenózní dávku furosemidu ≥ 40 mg.
Primární cíle (společné):
- zlepšení klinického stavu sestávající z těchto složek: hodnocení klinického stavu pacientem na 7stupňové škále, perzistující zhoršení srdečního selhání vyžadující intervenci (zahájení nebo intenzifikace intravenózní terapie, mechanická ventilační nebo oběhová podpora, chirurgická intervence, ultrafiltrace, hemofiltrace nebo dialýza); hodnocení klinického složeného cíle bude probíhat v 6., 24. a 48. hodině po začátku infuze
- celková mortalita, která bude sledována po celou dobu trvání sledování, je 90 dnů
Sekundární cíle:
- změna N-terminal pro-brain natriuretického peptidu (NT-pro BNP) 48 hod od počátku léčby ve srovnání se začátkem studie
- celková mortalita a kardiovaskulární rehospitalizace za 90 dnů
- kardiovaskulární rehospitalizace za 90 dnů [8]
- Na začátku července roku 2014 měla studie randomizováno 1 400 nemocných z plánovaných 2 116, tedy nadpoloviční většinu, a ukončení náboru se očekává ještě v letošním roce.
Zábrana degradace natriuretických peptidů
První duální inhibitor endopeptidáz omapatrilat v sobě zahrnoval inhibici angiotenzin-konvertujicího enzymu a současně neutrálních endopeptidáz – NEP (neprilyzin). Bránil tedy přeměně angiotenzinu I na angiotenzin II a současně i rozpadu natriuretických peptidů. Experimentální farmakologické pokusy a pilotní studie vedly k optimistickým předpokladům, že omapatrilat bude účinnější než ACE inhibitory samotné v léčbě hypertenze a srdečního selhání.
První velká dvojitě slepá, randomizovaná studie srovnávající omapatrilat a enalapril u nemocných s hypertenzí – OCTAVE sice prokázala účinnější hypotenzní vliv omapatrilatu, ale s vyšším výskytem angioedému [9].
Další multicentrická srovnávací studie u srdečního selhání OVERTURE neprokázala rozdíl ve výskytu primárního cíle (úmrtí či hospitalizace pro srdeční selhání) mezi omapatrilatem a enalaprilem. Zde byl výskyt angioedému sice nižší než ve studii OCTAVE, ale přesto omapatrilat nebyl FDA doporučen pro léčbu hypertenze a srdečního selhání, právě pro vyšší výskyt angioedému [10].
Novou možností duálního inhibitoru neutrálních endopeptidáz (NEP) a současně receptoru 1 pro angiotenzin II je látka LCZ 696 (angiotensin receptor neprilysin inhibitor – ARNI). Její výhodou je eliminace zvýšených hladin bradykininu přímým působením na receptor pro angiotenzin.
Po perorálnim podání se LCZ 696 rychle metabolizuje na AHU 377, což je specifický NEP inhibitor a valsartan. Podání LCZ 696 je spojeno s na dávce závislým zvýšením plazmatického cGMP, reninové aktivity a angiotenzinu II, což je v souladu s duálním účinkem. Dávka 200–400 mg LCZ 696 dosáhne přibližně 90% maximální NEP inhibice [11].
Na kongresu Evropské kardiologické společnosti (ESC) v Mnichově v roce 2013 byla prezentována a současně publikována v časopise Lancet studie PARAMOUNT u nemocných se srdečním selháním NYHA II-IV a zachovalou ejekční frakcí nad 45 % (HF NEF – heart failure with normal ejection fraction). Jednalo se o studii fáze 2, která byla randomizovaná, dvojitě zaslepená a multicentrická, v níž musela být koncentrace NT-proBNP > 400 pg/ml. Nemocní byli randomizováni buď do větve s LCZ696 s titrací do 2krát 200 mg nebo do větve s valsartanem 2krát 160 mg. Léčba trvala 36 týdnů. Primárním cílem byly změny koncentrace NT-proBNP po 12 týdnech léčby. Celkem bylo zařazeno 301 nemocných a studii dokončilo 266 nemocných (134 na LCZ 696 a 132 na valsartanu). NT-proBNP poklesl významně ve skupině LCZ z 783 pg/ml na 605 pg/ml (p < 0,005) a po valsartanu z 862 pg/ml na 835 pg/ml (ns), obr. 2.
Image 2. Studie PAPAMOUNT, výsledky NT-proBNP 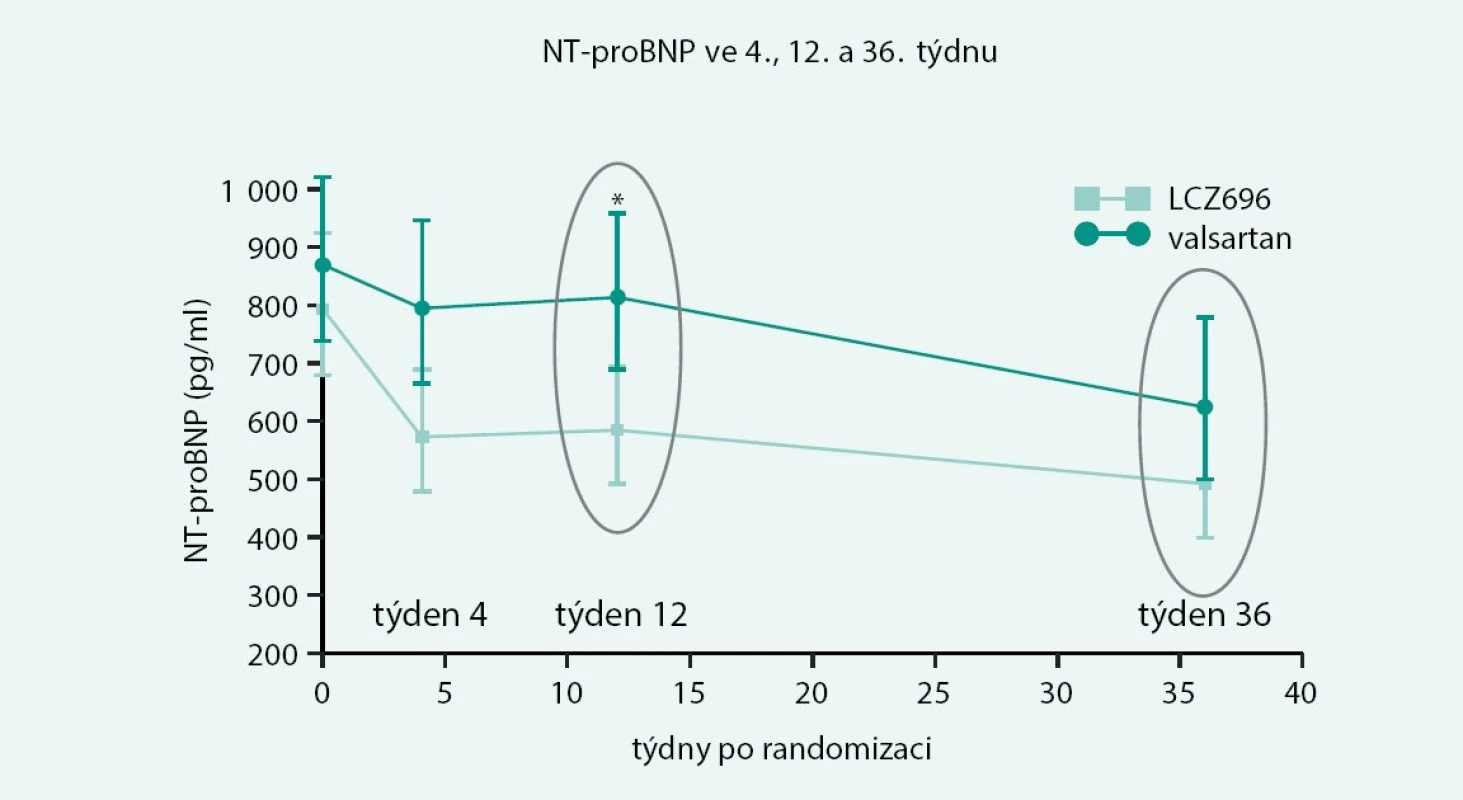
Po LCZ 696 došlo také po 36 týdnech ke zmenšení objemu levé síně o 4,6 ml (p < 0,003). Látka byla velmi dobře tolerovaná a opět nebyl hlášen jediný výskyt angioedému [12].
Zda-li bude tento příznivý účinek prokázán i v další klinické studii PARADIGM-HF, která sleduje nemocné s chronickým srdečním selháním NYHA II-IV, se zvýšenou hladinou natriuretických peptidů a EF pod 40 %, se dozvíme již tento rok. Studie srovnává látku LCZ696 v dávce 200 mg 2krát denně oproti enalaprilu v dávce 2krát 10 mg v oddálení prvého výskytu srdečního selhání či kardiovaskulární mortality. Bylo zahrnuto celkem 8 436 pacientů v poměru 1 : 1 do každé léčebné větve a studie je nyní ve stavu zpracování výsledků [13].
Závěr
Nesiritid v léčbě akutního srdečního selhání spíše neprokázal pozitivní účinky a jeho další zkoušení se nejeví perspektivní.
Naopak novou nadějí je ularitid a duální inhibitor neprilyzinu a ARB: LCZ 696, u nichž probíhají klinické studie a předchozí data z pilotních studií se jeví slibná.
V oblasti experimentu jsou zatím chimerické natriuretické peptidy, jako je cenderitid.
Článek je věnovaný životnímu jubileu prof. MUDr. Michaela Aschermanna, DrSc., významného kardiologa, našeho dlouholetého spolupracovníka ve výboru České kardiologické společnosti a kamaráda. Milý Michale, všechno nejlepší, hodně zdraví a hodně elánu do dalších plánů a cílů!
Tvoji Brňáci
prof. MUDr. Lenka Špinarová, Ph.D., FESC
lenka.spinarova@fnusa.cz
I. interní kardio-angiologická klinika LF MU a FN u sv. Anny, Brno
www.fnusa.cz
Doručeno do redakce 17. 7. 2014
Přijato po recenzi 15. 8. 2014
Sources
1. Mills RM, LeJemtel TH, Horton DP et al. Sustained hemodynamic effects of an infusion of nesiritide (human B-type natriuretic peptide) in heart failure. A randomized, double-blind, placebo-controlled clinical trial. NATRECOR Study Group. J Am Coll Cardiol 1999; 34(1): 155–162.
2. Colluci WS, Elkayem U, Horton DP et al. Intravenous nesiritide, a natriuretic peptide, in the treatment of decompensated congestive heart failure. NESIRITIDE Study Group. N Engl J Med 2000; 343(4): 246–253. Errata in N Engl J Med 2000 Nov 16; 343(20): 1504 et N Engl J Med 2000; 343(12): 896.
3. The VMAC Investigators. Intravenous neseritide vs nitroglycerin for treatment of decompesated congestive heart failure. JAMA 2002; 287(12): 1531–1540. Erratum in JAMA 2002; 288(5): 577.
4. Sackner-Bernstein JD, Skopicki HA, Aaronson KD. Risk of worsening renal function with nesiritide in patients with acutely decompensated heart failure. Circulation 2005; 111(12): 1487–1491. Erratum in Circulation 2005; 111(17): 2274.
5. O´Connor CM, Starling RC, Hernandez AF et al. Effect of nesiritide in patients with acute decompensated heart failure. N Engl J Med 2011; 365(1): 32–43. Erratum in N Engl J Med. 2011; 365(8): 773.
6. Chen HH, Anstrom KJ, Givertz MM et al. Low-Dose Dopamine or Low-Dose Nesiritide in Acute Heart Failure With Renal Dysfunction. The ROSE Acute Heart Failure Randomized Trial. JAMA 2013; 310(23): 2533–2543.
7. Mitrovic V, Seferovic PM, Simeunovic D et al. Haemodynamic and clinical effects of ularitide in decompensated heart failure. Eur Heart J 2006; 27(23): 2823–2832.
8. Clinicaltrials.gov. Dostupné z WWW: <http://www.clinicaltrials.gov/ct2/show/NCT01035255>.
9. Kostis JB, Packer M, Black HR et al. Omapatrilat and enalapril in patients with hypertension: the Omapatrilat Cardiovascular Treatment vs. Enalapril (OCTAVE) trial. Am J Hypertens 2004; 17(2): 103–111.
10. Packer M, Califf RM, Konstam MA et al. Comparison of omapatrilat and enalapril in patients with chronic heart failure: the Omapatrilat versus Enalapril Randomized Trial of Utility in Reducing Events (OVERTURE). Circulation 2002; 106(8): 920–926.
11. Gu J, Noe A, Chandra P et al. Pharmacokinetics and pharmacodynamics of LCZ696, a novel dual acting angiotensin receptor – neprilysin inhibitor (ARNi). J Clin Pharmacol 2010; 50(4): 401–414.
12. Salomon SD, Zile M, Pieske B et al. The angiotensin receptor neprilysin inhibitor LCZ696 in heart failure with preserved ejection fraction: a phase 2 double-blind randomised controlled trial. Lancet 2012; 308(9851): 1387–1395.
13. McMurray JJ, Packer M, Desai AS et al. PARADIGM-HF Committees and Investigators. Dual angiotensin receptor and neprilysin inhibition as an alternative to angiotensin-converting enzyme inhibition in patients with chronic systolic heart failure: rationale for and design of the Prospective comparison of ARNI with ACEI to Determine Impact on Global Mortality and morbidity in Heart Failure trial (PARADIGM-HF). Eur J Heart Fail 2013; 15(9): 1062–1073.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2014 Issue 12-
All articles in this issue
-
Orientační běh od intervence k prevenci.
Prof. MUDr. Michael Aschermann slaví významné životní jubileum - Životní jubileum prof. MUDr. Michaela Aschermanna, DrSc., FESC, FACC
- Antikoagulační léčba v sekundární prevenci koronárních příhod
-
Anémie a nedostatek železa v interní praxi:
od gastroenterologie ke kardiologii a ještě dál - Embolizační ischemické cévní mozkové příhody
- Pomůže nám nový SGLT2 inhibitor empagliflozin snížit riziko hypoglykemie?
- Minulost a současnost problematiky plicní cirkulace ve Všeobecné fakultní nemocnici v Praze
- Katetrizační ablace fokálně spouštěné fibrilace komor u pacientů se strukturálním postižením srdce
- Současné postavení intravaskulární ultrasonografie v intervenční kardiologii
- Obezita a srdce
- Karotický stenting – vývoj, trendy a inovace
- Mají natriuretické peptidy novou šanci v léčbě srdečního selhání?
-
Renální denervace u pacientů s rezistentní hypertenzí:
je možné ji ještě resuscitovat? - Moderní léčba akutních iktů: příklad multidisciplinární spolupráce
- Katetrizační metoda léčby chronické mitrální regurgitace pomocí mitrální svorky (MitraClip)
- IMProved Reduction of Outcomes: Vytorin Efficacy International Trial (studie IMPROVE-IT)
-
Orientační běh od intervence k prevenci.
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Katetrizační metoda léčby chronické mitrální regurgitace pomocí mitrální svorky (MitraClip)
-
Anémie a nedostatek železa v interní praxi:
od gastroenterologie ke kardiologii a ještě dál - Embolizační ischemické cévní mozkové příhody
- Obezita a srdce
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

