-
Medical journals
- Career
Imunosupresivní terapie a její úskalí
Authors: M. Kuman
Authors‘ workplace: Centrum kardiovaskulární a transplantační chirurgie Brno, ředitel doc. MUDr. Petr Němec, CSc.
Published in: Vnitř Lék 2011; 57(7&8): 655-658
Category: 136th internal medicine day, XXIV. Vanýskův den, Brno 2011
Overview
Imunosupresivní terapie je nezbytnou podmínkou úspěšné transplantace ledviny. Tři základní typy imunosupresivní terapie jsou: úvodní – indukční, antirejekční a udržovací. Základ udržovací imunosupresivní terapie tvoří kombinace ve složení kortikoidy + tacrolimus + mykofenolát mofetil. Nežádoucí účinky imunosupresivní terapie jsou krátkodobé a dlouhodobé. Závažné jsou lékové interakce, hlavně s antimykotiky a makrolidy. Spolupráce transplantologa s lékaři podílejícími se na péči o transplantovaného je zásadní pro nastavení hladiny imunosupresivní terapie, adekvátní aktuálnímu stavu. Nedostatek spolupráce a komunikace může vést k nenávratnému poškození funkce transplantovaného orgánu.
Klíčová slova:
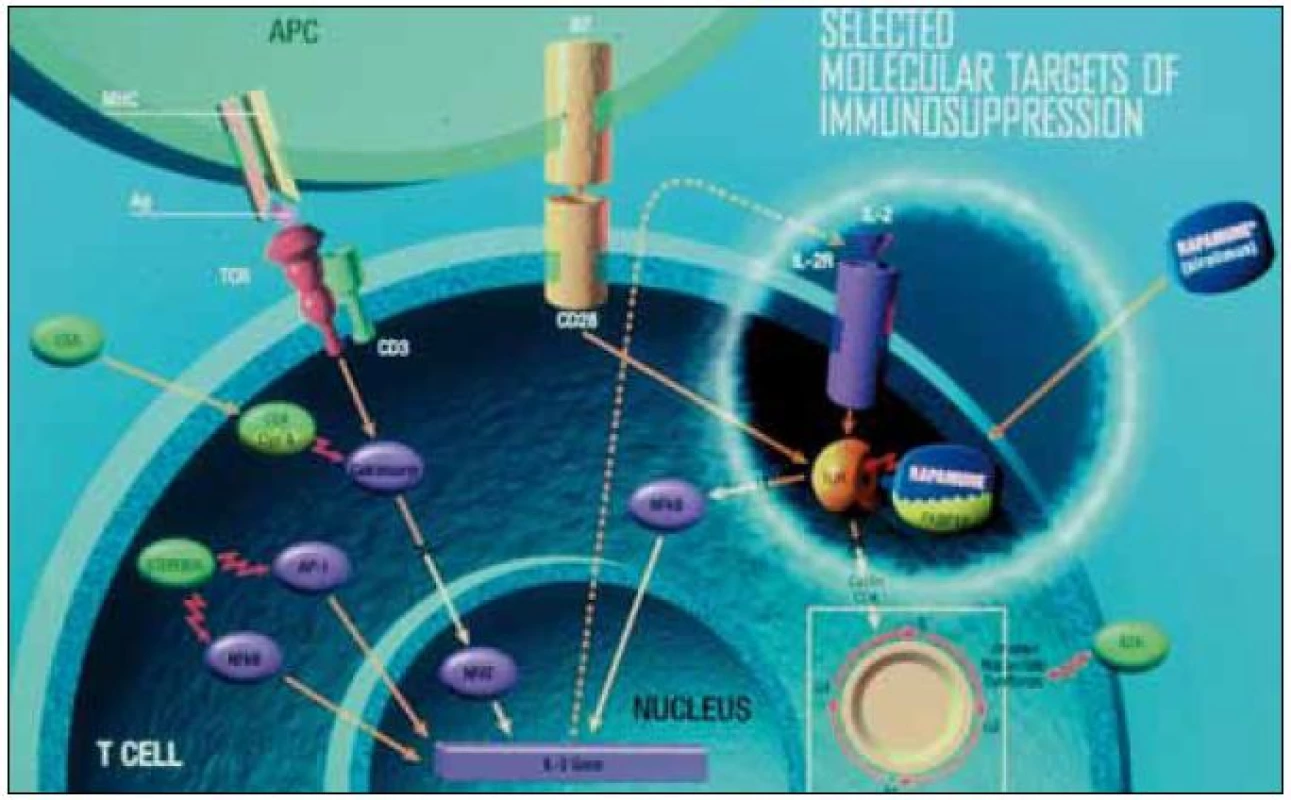
imunosupresivní terapie – imunosupresiva – nežádoucí účinky – interakce – spolupráceImunosupresivní terapie (IT) je nezbytnou podmínkou úspěšné transplantace ledviny (TL). Cílem je zabránit odhojení transplantovaného orgánu – rejekci. Základním mechanizmem je znemožnit rozpoznání komplexu antigen-antigen-prezentující buňka imunitním systémem příjemce a zahájit rejekční kaskádu [1,2] (obr. 1 a 2).
Image 1. Mechanizmus akce I. Podle [1,2]. ![Mechanizmus akce I. Podle [1,2].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/ab056616042d260334ef68c1bb032a83.jpeg)
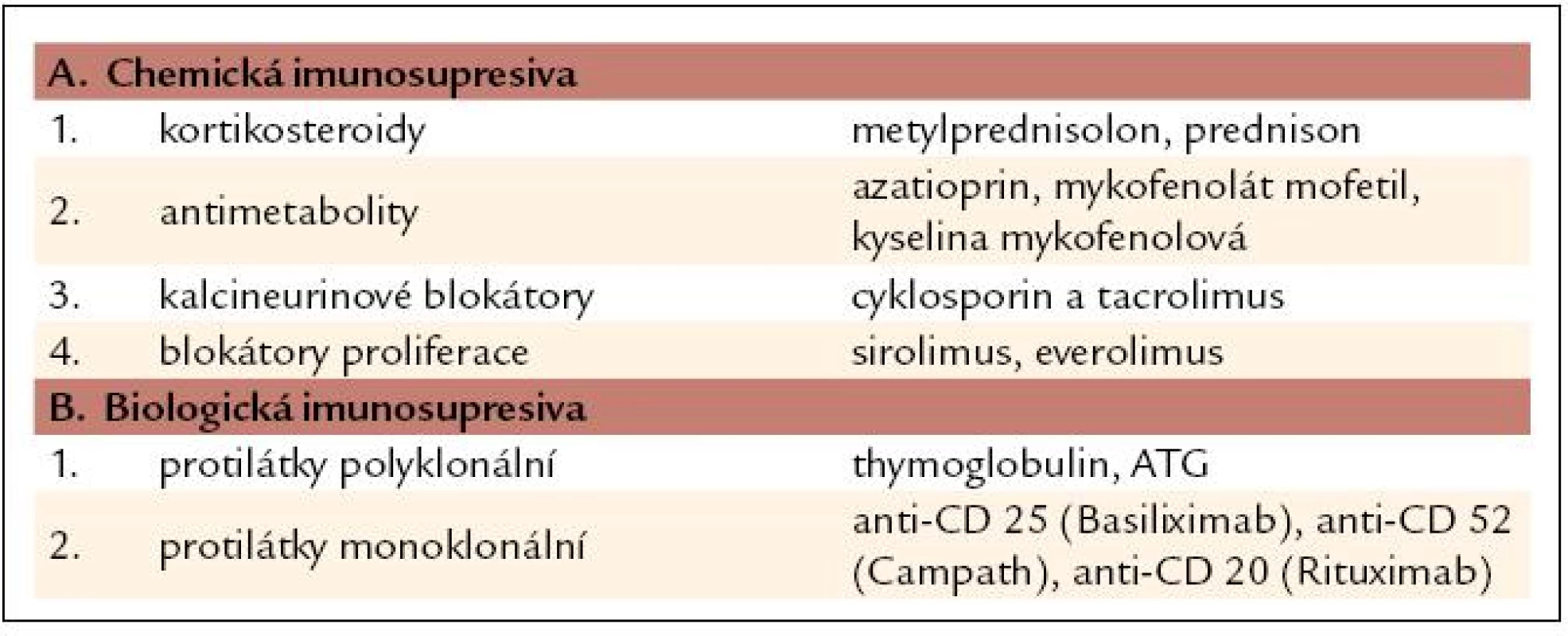
Imunosupresiva (IS) dělíme dle jejich povahy na chemická – kortikosteroidy, antimetabolity, kalcineurinové blokátory a blokátory proliferace – m-tor inhibitory; a na biologická (tab. 1).
Tři základní typy IT jsou: úvodní – indukční (basiliximab, thymoglobulin), antirejekční (obojí v kompetenci transplantačních oddělení) a udržovací, chronická, se kterou se setkávají při péči o transplantované praktičtí lékaři, specialisté i lůžková oddělení. Transplantovaný pacient je dnes již běžným klientem společným pro transplantology, praktické lékaře i specialisty. Mezi bazální udržovací imunosupresiva patří kortikosteroidy, antimetabolity, blokátory kalcineurinu a blokátory proliferace (tab. 2).
Table 2. Imunosuprese – udržovací. 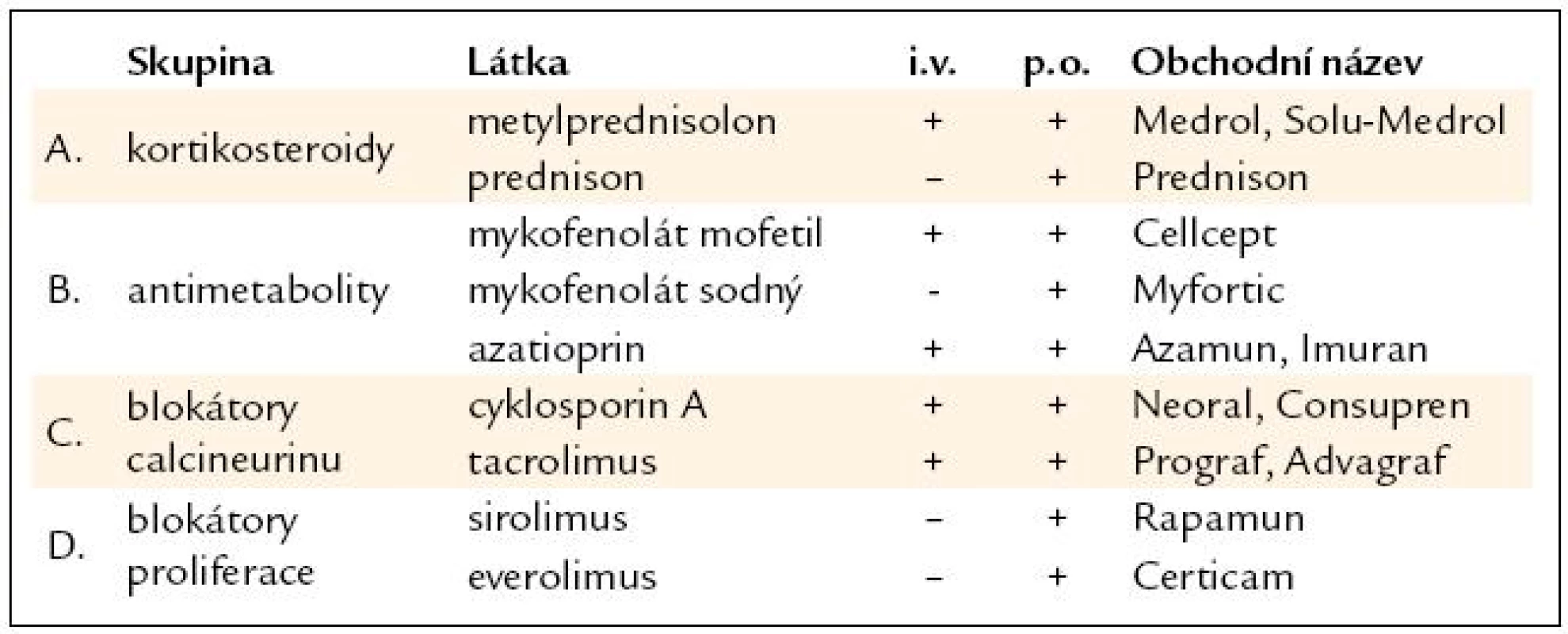
Pilíř udržovací IT tvoří kombinace ve složení kortikoidy + tacrolimus (alternativně cyklosporin nebo sirolimus, everolimus ve speciálních indikacích) + mykofenolát mofetil (mykofenolát sodný) (obr. 3). IT u transplantací ledvin je v časné fázi držena na vyšší hladině s důrazem na časné dosažení efektivních hodnot mezi 3. a 5. dnem po transplantaci, zpoždění mívá za následek častější rejekce. S postupem času je IT při příznivém průběhu snižována na nejnižší možnou úroveň zajišťující dobrou funkci transplantovaného orgánu a zároveň eliminující nežádoucí projevy – infekce, toxicitu. Důležité je pravidelné monitorování úrovně IT – jednak pomocí sledování hladin v séru (u tacrolimu, cyklosporinu, sirolimu, everolimu a kyseliny mykofenolové), dále pak hematologickými a imunologickými parametry. Významným vodítkem je výskyt nežádoucích účinků IT.
Image 3. Imunosuprese u transplantace ledviny. 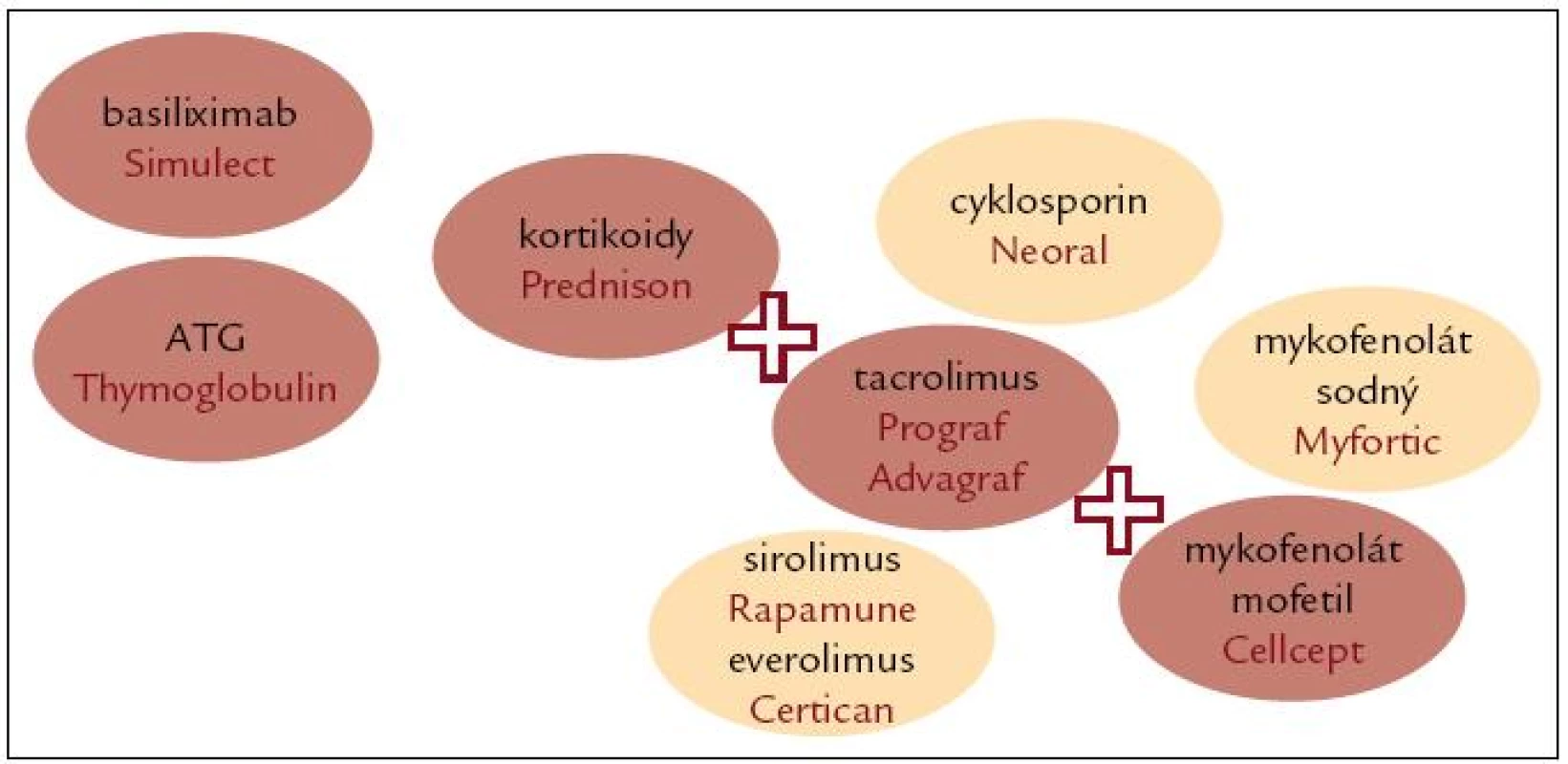
Nežádoucí účinky IT jsou krátkodobé (infekce vs rejekce) a dlouhodobé (recidivující infekce, diabetes mellitus, hypertenze, ateroskleróza, tumory a další). Jsou nespecifické i specifické pro jednotlivá imunosupresiva. Zároveň s výhodami jednotlivých IS je nutno počítat také s jejími nevýhodami. Jejich znalost umožňuje zvolit optimální kombinaci individuálně uzpůsobenou pro daného pacienta. Pozitiva a negativa nejčastěji užívaných IS (kortikoidy, mykofenolát mofetil, cyklosporin A, tacrolimus, sirolimus) je nutno vždy dobře zvážit (tab. 3–8).
Table 3. Kortikoidy – Prednison. 
Table 4. Mykofenolát mofetil – Cellcept generika: Mykofenolát mofetil Teva, Sandoz, Myfenax Teva. 
Table 5. Cyklosporin A – Sandimmun Neoral Equoral Teva, Sigmasporin Helvetia Pharma ČR. 
Table 6. Tacrolimus – Prograf. 
Table 7. Tacrolimus – Advagraf. 
Table 8. Sirolimus – Rapamune. 
Terapeuticky významná je elementární znalost lékových interakcí zvyšujících hladiny IS. Dochází k několikanásobnému navýšení hladin v séru až do toxických hodnot. Objevují se toxické projevy – poškození funkce štěpu (reverzibilní vs ireverzibilní), hepatopatie, neuropatie, postižení gastrointestinálního traktu (průjmy) nebo závažné infekce (multirezistentní bakterie, viry – CMV, EBV, herpes a další, plísně). Nejvýznamnější je interakce s antimykotiky (ketokonazol, flukonazol, itrakonazol, clotrimazol) a makrolidy (claritromycin, erytromycin, telitromycin), v menší míře způsobuje zvýšení diltiazem, doxycyklin a metoclopropamid. Stejný efekt (inhibice degradačního cytochromu CYP3A4) má grapefruit a pomelo. Tyto druhy ovoce a šťávy z nich jsou pro transplantované zakázány (tab. 9). Naopak snížení účinku IS (snížení hladin v séru) působí induktory CYP3A4 – antibiotika rifampicin, rifabutin, antikonvulziva karbamazepin, fenobarbital, fenytoin; z drog pak třezalka tečkovaná (hypericum perforatum) (tab. 10).
Table 9. Tacrolimus – Prograf, cyklosporin A – Sandimmun Neoral, sirolimus – Rapamune. 
Table 10. Tacrolimus – Prograf, cyklosporin A – Sandimmun Neoral, sirolimus – Rapamune. 
Těsná spolupráce mezi transplantology, klinickými pracovníky, specialisty a praktickými lékaři při péči o transplantované je velmi důležitá a mnohdy zcela zásadní pro zajištění dobrých a dlouhodobých výsledků transplantací. Nedostatek spolupráce a komunikace může vést k nenávratnému poškození funkce transplantovaného orgánu. Je nutné dát pozor na lékové interakce a zajištění kontinuity adekvátní imunosuprese. Včas informovat ošetřujícího transplantologa a konzultovat s ním je žádoucí ve všech závažnějších situacích (tab. 11).
Table 11. Imunosuprimovaný pacient v ambulanci nebo na oddělení. 
MUDr. Milan Kuman
www.cktch.cz
e-mail: milan.kuman@cktch.czDoručeno do redakce: 20. 6. 2011
Sources
1. Kahan BD, Koch SM. Current immunosuppressant regiment: considerations for critical care. Curr Opin Crit Care 2001; 7 : 242–250.
2. Masri MA. The mosaic of immunosuppressive drugs. Mol Immunol 2003; 39 : 1073–1077.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2011 Issue 7&8-
All articles in this issue
- Biologická léčba po transplantaci ledviny
- Imunosupresivní terapie a její úskalí
- Minulost, současnost a budoucnost náhrady funkce ledvin
- Etiologie a klinický obraz chronického selhání ledvin
- Hypertenze a kardiovaskulární komplikace chronického selhání ledvin
- Kostní choroba u chronického selhání ledvin a její moderní terapie
- Infekce močového traktu a chronické selhání ledvin
- Anémie u chronického selhání ledvin
- Peritoneální dialýza a její modifikace v léčbě chronického selhání ledvin
- Hemodialýza – současná praxe
- Přehled výsledků transplantací ledvin v České republice
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Hemodialýza – současná praxe
- Anémie u chronického selhání ledvin
- Imunosupresivní terapie a její úskalí
- Etiologie a klinický obraz chronického selhání ledvin
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career