-
Medical journals
- Career
Maligní arytmie u pacienta s variantní (Prinzmetalovou) anginou pectoris
Authors: T. Skála; M. Hutyra; J. Galuszka; M. Fedorco; R. Husár; M. Richter; J. Lukl
Authors‘ workplace: I. interní klinika Lékařské fakulty UP a FN Olomouc, přednosta prof. MUDr. Jan Lukl, CSc.
Published in: Vnitř Lék 2007; 53(6): 724-728
Category: Case Reports
Overview
Maligní arytmie jsou častou komplikací ischemie myokardu během rozvoje spazmu koronární cévy. Popisujeme pacienta s variantní anginou pectoris, opakovaně resuscitovaného pro zástavu oběhu při maligní arytmii, kterému byl naimplantován ICD. Během stenokardií se na EKG objevuje obraz elevací ST segmentů v oblasti přední stěny, se vznikem setrvalé polymorfní komorové tachykardie. Pro recidivy tachyarytmie byla nutná zevní defibrilace. Při koronarografii dochází na RIA k rozvoji spazmu s počátkem v periferii tepny, postupujícím až do oblasti bifurkace s RD s přechodným uzávěrem tepny a vznikem komorové tachykardie. Po přidání blokátoru kalciového kanálu a depotního nitrátu a vysazení betablokátoru je pacient již nadále zcela bez potíží.
Klíčová slova:
variantní angina pectoris - koronární spazmus - maligní arytmie - koronarografie - provokační testy - hyperventilační echokardiografieKazuistika
59letý muž, který se doposud léčil pouze pro vysoký krevní tlak a deprese, nekuřák, byl v terénu resuscitován pro zástavu oběhu. Při příjezdu zjistila RZP fibrilaci komor, defibrilací obnovila srdeční akci. Vstupně natočené EKG nevykazovalo žádné známky ischemie, QRS komplexy byly štíhlé, QT interval nebyl prodloužen. Na EKG nadále nedošlo k vývoji, žádné známky ischemie se neobjevily. Po resuscitaci odebraný Hladina troponinu T odebraná po resuscitaci měla hodnotu 0,5 µg/l (norma laboratoře do 0,1 µg/l). Selektivní koronarografií nebylo zobrazeno postižení věnčitých tepen. Stejně normální obraz nám poskytla i echokardiografie, zobrazená LK měla normální velikost i kinetiku s EF 65 %, beze známek strukturálního postižení srdce. K zajištění před náhlou smrtí tak pacient podle platných guidelines podstoupil implantaci kardioverter-defibrilátoru (Biotronik Belos VR 4085).
O 12 měsíců později byl tentýž pacient opět resuscitován pro zástavu oběhu, na vstupním EKG RZP zachytila setrvalou monomorfní komorovou tachykardii o frekvenci kolem 200/min. Po vyčerpání 6 naprogramovaných výbojů ICD byla nutná zevní defibrilace. Následně byl pacient hospitalizován ve spádové okresní nemocnici. Vstupní laboratorní odběry ukázaly mírně zvýšenou hladinu troponinu I 0,163 µg/l (norma laboratoře do 0,1 µg/l), která s odstupem 2 dnů poklesla na 0,013 µg/l. Kalemie byla v normě - 4,5 mmol/l, z patologických hodnot byla zachycena jen mírná hypomagnezemie 0,75 mmol/l. Po substituci magnezia (Mg) již další laboratorní hodnoty hladiny Mg neklesly pod normu.
Pacient doposud denně užíval 20 mg betaxololu, 1,25 mg cilazaprilu, 3 tbl Mg-laktátu po 0,5 g, fluoxetin a alprazolam. V úvodu hospitalizace bylo z důvodu vstupní komorové tachykardie započato sycení amiodaronem. I přes tuto léčbu opětovně docházelo k epizodám setrvalé polymorfní komorové tachykardie, a to klinicky vždy současně se stenokardiemi a presynkopálním stavem. Nutno podotknout, že pacientovi byl stále podáván betablokátor. Po domluvě byl pacient přeložen k došetření do naší nemocnice.
Krátce po přijetí na oddělení došlo v klidu na lůžku za kontinuální monitorace EKG k vzniku typických stenokardií. Současně se na EKG objevily de novo obrovské elevace ST úseků I, aVL, V2-6 (obr. 1). Po několika desítkách vteřin se na monitoru objevily opakované běhy nesetrvalé komorové tachykardie (obr. 2a 3) a následně došlo i ke vzniku setrvalé monomorfní komorové tachykardie. Po aplikaci NTG s.l. vymizely bolesti na hrudi, ustoupil EKG obraz elevací ST a došlo k terminaci komorové tachykardie (obr. 4). QTc interval byl 473 ms během stenokardií a 413 ms v klidu. Při následném kontinuálním i.v. podávání nitrátu se potíže již neopakovaly. Sérová hladina troponinu byla opakovaně negativní, stejně tak byl zcela v normě mineralogram. Dle výpisu z ICD (obr. 5) jsme zjistili proběhlé recidivující setrvalé monomorfní i polymorfní komorové tachykardie s opakovanou adekvátní terapií over-drivingem a výboji. Funkce ICD byla dle kontroly správná.
Image 1. Elevace ST úseků I, aVL, V<sub>2–6</sub> na vstupním EKG. 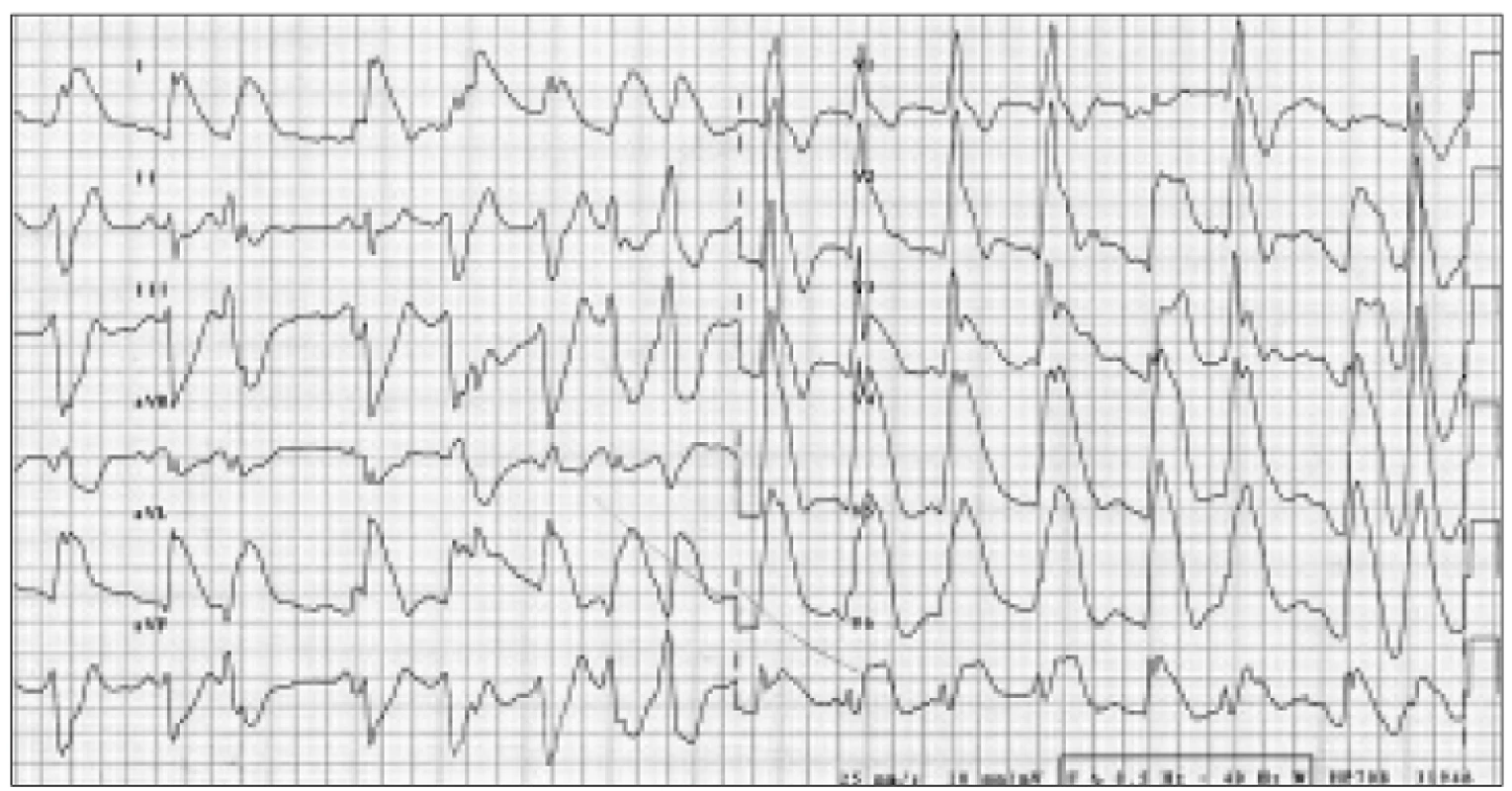
Obr. 2 a 3. Komorové tachykardie při spazmu koronární tepny. 
Image 2. Po aplikaci NTG s.l. ustupuje EKG obraz elevací ST i komorová tachykardie. 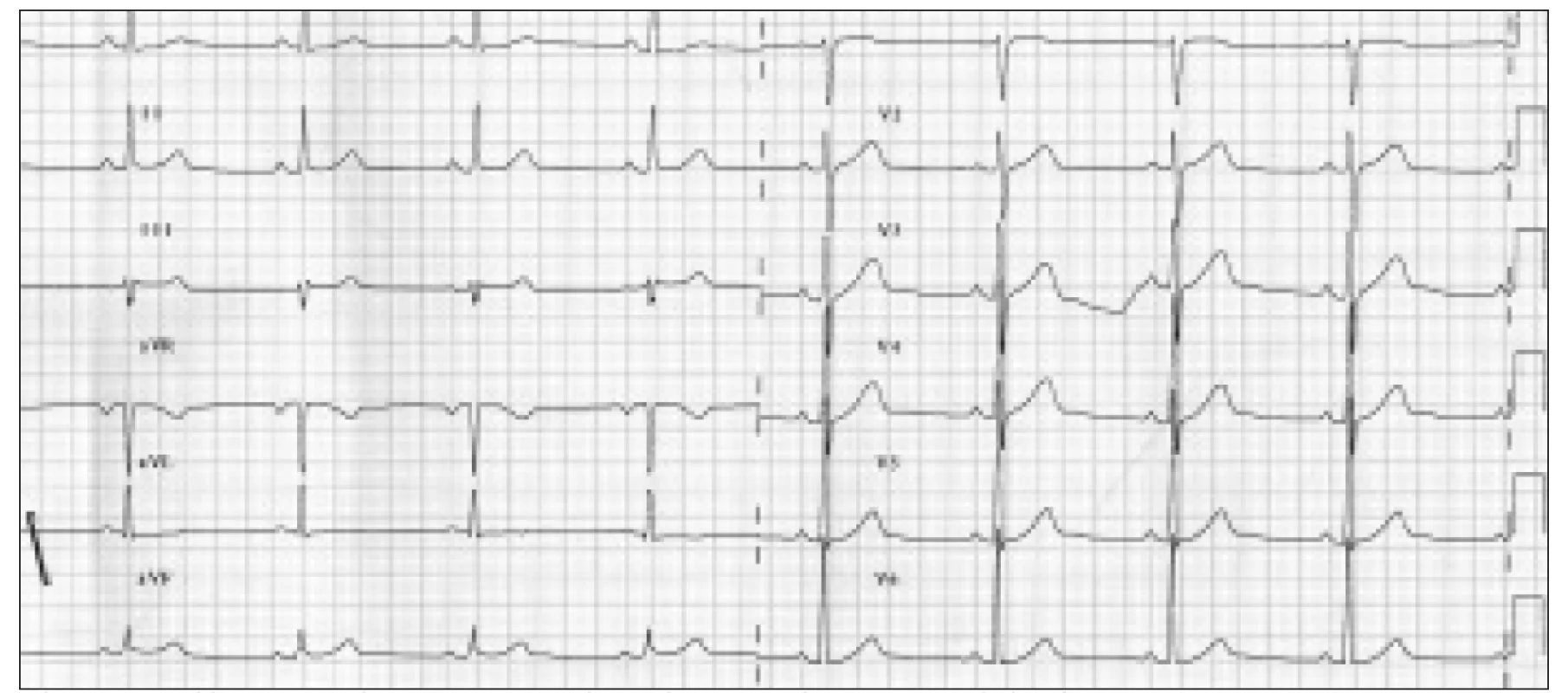
Image 3. Výpis z paměti ICD – v úvodu sinusový rytmus, následující komorová tachyarytmie detekována přístrojem v zóně VF – po nabití přístroje vydán defibrilační výboj s terminací tachykardie. 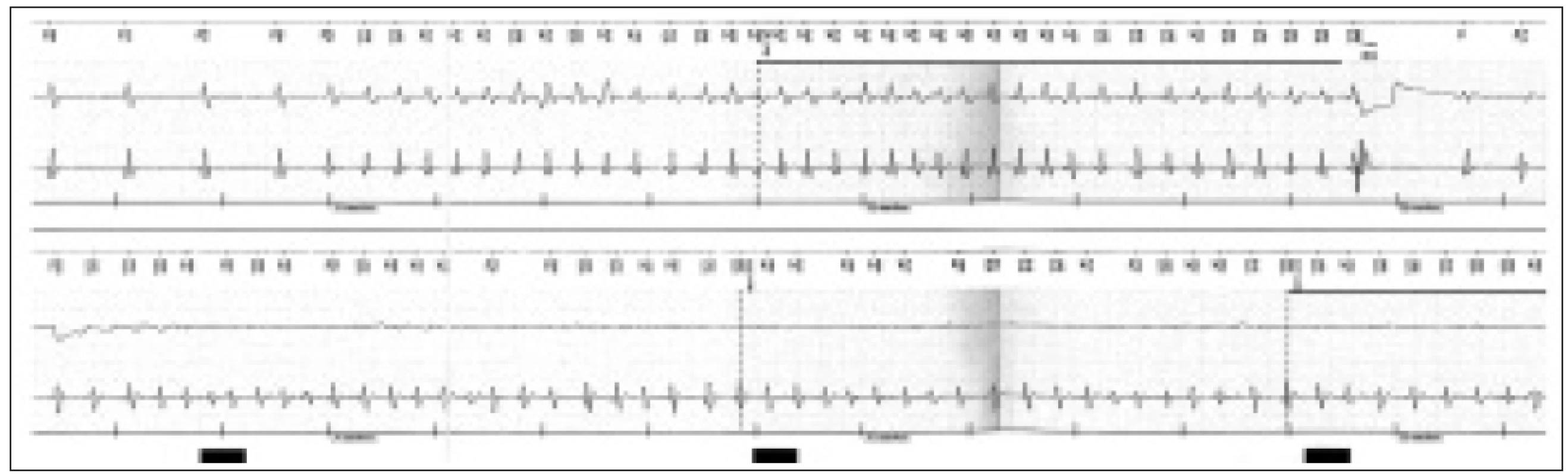
Při ještě vstupně ponechaném betablokátoru jsme provedli echokardiografické vyšetření s hyperventilací, během kterého se nepodařilo vyvolat EKG změny, stenokardie, či poruchu kinetiky LK. Echokardiograficky nedošlo ke změně stavu, LK nevykazovala poruchy kinetiky, systolická funkce byla stále normální.
Při rekoronarografii se spontánně na RIA rozvinul spazmus (obr. 6), s počátkem v periferii tepny, postupujícím až do oblasti bifurkace s RD, s přechodným uzávěrem tepny, což vyústilo ve vznik stenokardií a následně i komorové tachykardie. Po intrakoronární aplikaci Isoketu pak spolu s obnovením průtoku do periferie RIA promptně ustoupily subjektivní potíže i komorová tachykardie. Na ACD jsme rovněž pozorovali krátký, přechodný spazmus, nasedající na ústí diagnostického katétru v odstupu tepny. Ostatní tepny byly zcela hladké, bez stenóz. Plánovaný provokační test s ergonovinem tak nemusel být proveden.
Image 4. Selektivní koronarografie, při které byl dokumentován spontánně vzniklý difuzní spazmus RIA (počátek spazmu označený šipkou), s počátkem v periferii tepny, postupujícím až do oblasti bifurkace s RD. 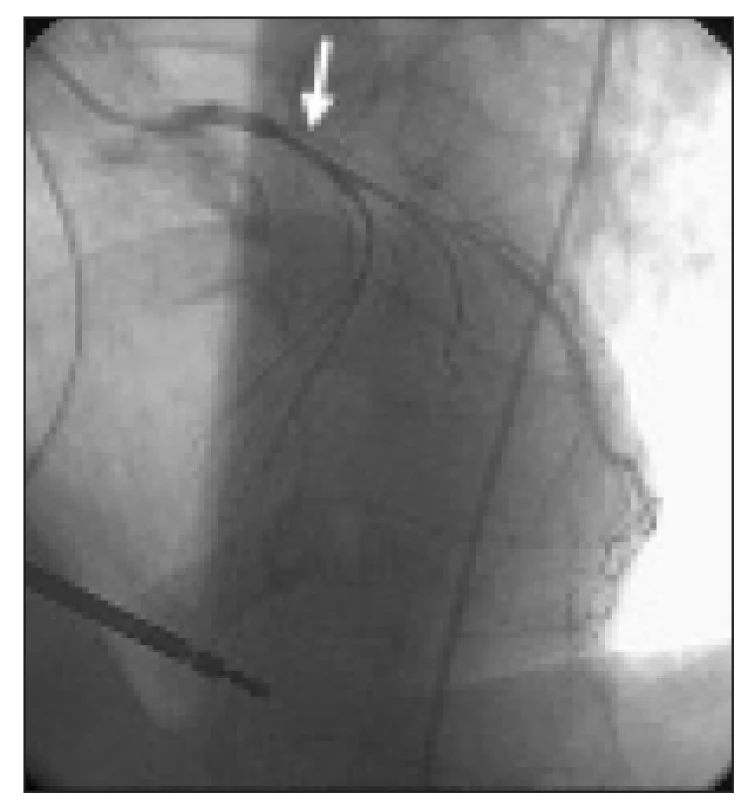
V rámci úpravy terapie jsme vysadili betablokátor a do medikace přidali depotní nitrát (100 mg izosorbid-mononitrátu denně) a BKK (10 mg amlodipinu denně). V dalším podávání amiodaronu jsme již nepokračovali.
Během následujícího 1 roku již nedošlo k dalšímu výskytu stenokardií či synkopy, nebyla dokumentována žádná významnější arytmie, stejně jako žádné další terapie ICD. Vzhledem k průběhu onemocnění a rizikovosti pacienta byla výše uvedená terapie i nadále ponechána.
Diskuse
Variantní (Prinzmetalova) angina se řadí mezi nestabilní anginy pectoris, obvykle se objevuje spontánně a je charakterizována přechodnou elevací ST segmentů, přičemž ve většině případů nevede k infarktu myokardu [1]. Definice koronárního spazmu je arbitrární, ale panuje všeobecná shoda, že koronární spazmus je závažná, abnormální vazokonstrikce velké epikardiální arterie, která často vede k transmurální ischemii myokardu. Není přesně stanoveno, jaká je nutná redukce lumen tepny k označení za spazmus, ale u pacientů s anginou a normálním koronarografickým nálezem, u kterých dojde k ischemiím myokardu, bývá průsvit cévy snížený o více než 70 %. Spazmus je povětšinou fokální, ale může se vyskytovat na více než jednom místě [2].
Koronární spazmus je dle současných poznatků zřejmě způsoben odpovědí nespecifické lokální hyperreaktivity koronárních cév na konstrikční podněty. Pacienti s variantní anginou mají zvýšenou koronární reaktivitu na celou řadu vazokonstrikčních stimulů a koronární spazmus u fokální hyperreaktivity je často důsledkem působení všeobecně vazokonstrikčního stimulu [3]. Koronární spazmus má množství možných spouštěcích faktorů, což naznačuje nespecifičnost koronární hyperreaktivity. Může být vyvolán řadou agens, jako jsou např. ergonovine, noradrenalin, serotonin, acetylcholin, histamin [4]. Dokonce i vzestupem pH krve při hyperventilačním testu [5]. Vzhledem k tomu, že spazmy koronárních cév byly pozorovány i u transplantovaných srdcí, je primárně nervová příčina nepravděpodobná. Opravdová prevalence variantní anginy není známa. Obě pohlaví jsou ale zřejmě postižena stejnou měrou. V porovnání s pacienty s chronickou stabilní anginou pectoris jsou pacienti s variantní anginou mladší a s výjimkou kouření cigaret mají obecně méně rizikových faktorů ICHS [6]. Kuřáctví je naopak s koronárními spazmy asociováno [7].
Obvykle spazmus trvá jen několik málo minut, než spontánně odezní, ale prolongované spazmy nejsou výjimečné a mohou vyústit až v infarkt myokardu, arytmie či náhlou smrt. Infarkt myokardu je u pacientů s normálním či téměř normálním koronarografickým obrazem velmi vzácnou komplikací přetrvávajícího koronárního spazmu. Nicméně v případě, že spazmus komplikuje vážnější postižení věnčitých tepen, je infarkt myokardu daleko běžnější [8].
Jako manifestace variantní anginy pectoris bylo popsáno různé spektrum arytmií - kompletní AV blokáda [8], asystolie, komorové tachykardie, torsade de pointes i fibrilace komor [9]. Mnohdy tak, stejně jako v popisovaném případě, může být první známkou manifestace variantní anginy oběhová zástava na podkladě maligní arytmie s nutností elektrické kardioverze. Na možnost variantní anginy pectoris by se tak mělo myslet při maligních arytmiích jinak neobjasněné etiologie. Pacienti s život ohrožujícími arytmiemi mívají širší klidový QT interval, odrážející heterogenitu repolarizace, přítomnou i mimo ischemii. Disperze QT intervalu se ukazuje být známkou zvýšeného rizika náhlé smrti během záchvatu variantní anginy [10].
Diagnóza variantní anginy je stanovena na základě elevací ST segmentu během epizody bolesti na hrudi, vznikající obvykle v klidu, které mizí s ústupem potíží. Ačkoli je ST elevace charakteristickou známkou variantní anginy, koronární spazmy mohou být spojeny i s depresí ST úseku, inverzí či pseudonormalizací vlny T. Deprese ST úseku se často vyskytuje u spazmu téměř plně obturujícího lumen cévy, či u okluze plné v přítomnosti kolaterální cirkulace. Během spazmu byly popsány i pseudonormalizace T vlny.
Pokud je koronarografické vyšetření normální a elevace ST segmentů jsou zachyceny během bolesti na hrudi, pak lze předpokládat diagnózu variantní anginy pectoris a další testy nejsou třeba. Nejdůležitější je tak získat EKG záznam během bolestí na hrudi, pokud se potíže vyskytují častěji, může být prospěšné 24hodinové holterovské EKG monitorování. Bolest na hrudi povětšinou vzniká bez předcházejícího nárůstu požadavku myokardu na kyslík, většina pacientů tak má normální pracovní toleranci a zátěžové testy mohou být negativní. Nicméně variantní anginu lze mnohdy vyprovokovat cvičením, hyperventilací a chladem. Řada provokačních testů (acetylcholine, methacholine a methylergonovine) může i při vstupním chybění elevací ST segmentů při bolesti na hrudi předpovědět koronární spazmus, který může být viditelný angiograficky a následně elevacemi doprovázený. Před provedením provokačních testů mají být vysazeny nitráty a BKK. Hyperventilace prováděná po 6 min samostatně či po zátěžovém testu je dalším testem k provokaci arteriálního spazmu. Hyperventilační test s 5 min rázné ventilace má udávanou senzitivitu 62 % a specificitu až 100 %. Pacienti s pozitivním hyperventilačním testem inklinují k větší frekvenci spazmů, postižení více tepen a častějšímu výskytu komplikující AV blokády či komorové tachykardie než pacienti s negativním hyperventilačním testem [11]. Největší senzitivitu i specificitu ze všech provokačních testů má provokační test s ergonovinem [12].
Cílem dlouhodobé terapie je prevence vzniku koronárních spazmů a přidružené ischemie myokardu. Koronární spazmy povětšinou velmi dobře reagují na NTG, dlouhodobě působící nitráty a blokátory kalciových kanálů [13]. V terapii se má začít blokátorem kalciových kanálů ve vyšší dávce. Pokud nedojde k plné eliminaci epizod, přidává se dlouhodobě působící nitrát či BKK z jiné skupiny. Dobrý efekt zvláště u pacientů nezcela plně odpovídajících na terapii BKK mohou mít blokátory α-receptorů [14]. Podávání betablokátorů může zvýšit četnost a tíži koronárních spazmů, především pak u pacientů s normálními koronárními tepnami. Nicméně betablokátory mohou být přínosem u pacientů s významnou koronární aterosklerózou a námahovou anginou nezpůsobenou koronárním spazmem. Ale i zde je kontraindikována terapie betablokátory samotnými, obzvláště pak neselektivními. Pokud dojde ke vzniku koronárního spazmu v průběhu koronarografie, měl by se nitrát aplikovat intrakoronárně. Nezbytný je zákaz kouření.
Během prvních 3-6 měsíců dochází k nejvážnějším epizodám variantní anginy, a terapie by tudíž alespoň během této doby měla být maximalizovaná. U pacientů, kteří neměli závažné arytmie či synkopy během záchvatů variantní anginy, lze terapii pozvolna vysadit během 1-1,5 roku. U pacientů se spazmy komplikovanými či opakovanými je terapie chronická. Před vysazením terapie jsou ale nezbytné holterovské EKG monitorování a provokační test. Je nutno se vyvarovat spouštěcích faktorů, které mohou mít vliv na opakování spazmů, jako jsou kouření, alkoholizmus, abúzus kokainu, hypomagnezemie, používání SSRI, hyperventilace, vystavování chladu a emoční stres.
Prognóza je obvykle výborná u pacientů, kteří dostanou adekvátní farmakologickou terapii. Ve skupině pacientů publikované Yasue et al bylo celkové 5leté přežití 89 – 97 %. Během 7letého sledování asi 300 pacientů byla incidence náhlé smrti 3,6 % a incidence infarktu myokardu 6,5 % [15]. Bory et al. u 277 pacientů sledovaných v průměru 7,5 roku zjistili opakovanou anginu pectoris u 39 %, nicméně infarkt myokardu u 3,5 % a smrt z kardiální příčiny u 6,5 % [16]. Prognóza je obzvláště dobrá u pacientů s normální či téměř normální koronarografií. Pacienti s koronárním spazmem již nasedajícím na zúženou tepnu mají prognózu horší. Ve studii 162 pacientů s variantní anginou pectoris, publikované Rovai et al, měli pacienti s normální koronarografií a chorobou jedné tepny 5leté přežití 95 % ve srovnání s 85 % u pacientů s postižením více tepen [17]. Prakticky ke stejným výsledkům o něco dříve došel i Walling et al [18]. Ukazuje se, že variantní angina může perzistovat i navzdory terapii nitráty a blokátory kalciových kanálů. Dlouhodobé potíže bývají spojeny s pokračováním v kouření, nedostatečnou dávkou antianginózní medikace a trvalým vystavením faktorům spouštějících spazmus koronárních cév. U pacientů rezistentních na farmakoterapii by mohlo být eventuálně přínosné zavedení intrakoronárního stentu. Bylo popsáno několik úspěšných implantací stentu bez další rekurence variantní anginy pectoris [19]. U pacientů refrakterních na farmakologickou terapii i stenting byla popsána úspěšná sympatektomie [20]. Nicméně u takto léčených pacientů zatím není k dispozici dostatek dat z dlouhodobého sledování k ověření přínosu této léčebné strategie.
Závěr
První manifestací variantní anginy pectoris může být oběhová zástava na podkladě maligní arytmie. Na možnost variantní anginy pectoris by se mělo myslet při maligních arytmiích jinak neobjasněné etiologie a to i u recidivujících maligních arytmiích u pacientů s již naimplantovaným ICD.
MUDr. Tomáš Skála
www.fnol.cz
e-mail: tomasskala@gmail.com
Doručeno do redakce: 22. 11. 2006
Přijato po recenzi: 25. 1. 2007
Sources
1. Sovová E, Lukl P, Číhalík Č. Vasospastická angína. Vnitř Lék 2005; 51 : 548-554.
2. Ozaki Y, Keane D, Serruys PW. Fluctuation of spastic location in patients with vasospastic angina: a quantitative angiographic study. J Am Coll Cardiol 1995; 26 : 1606-1614.
3. Kaski JC, Maseri A, Vejar M et al. Spontaneous coronary artery spasm in variant angina results from a local hyperreactivity to a generalized constrictor stimulus. J Am Coll Cardiol. 1989; 14 : 1456-1463.
4. Kaski JC, Crea F, Meran D et al. Local coronary supersensitivity to diverse vasoconstrictive stimuli in patients with variant angina. Circulation 1986; 74 : 1255-1265.
5. Sovová E, Marek D, Škvařilová M et al. Echokardiografický hyperventilační test u pacientů s negativní koronarografií. Vnitř Lék 2001; 47 : 156-160.
6. Nobuyoshi M, Abe M, Nosaka H et al. Statistical analysis of clinical risk factors for coronary artery spasm: identification of the most important determinant. Am Heart J 1992; 124 : 32-38.
7. Sugiishi M, Takatsu F. Cigarette smoking is a major risk factor for coronary spasm. Circulation 1993; 87 : 76-79.
8. Ujhelyi E, Bohm A, Toth C et al. Prinzmetal angina pectoris associated with 3rd degree atrioventricular block. Orv Hetil 2001; 142 : 1809-1811.
9. Kreuzer J, von Hodenberg E, Jahn L et al. Recurrent ventricular fibrillation in a patient with angiographically normal coronary arteries and intermittent ST segment elevation. Z Kardiol 1990; 79 : 592-598.
10. Parchure A, Batchvarov V, Malik M et al. Increased QT dispersion in patients with Prinzmetal's variant angina and cardiac arrest. Cardiovasc Res 2001; 50 : 379-385.
11. Nakao K, Ohgushi M, Zoshimura M et al. Hyperventilation as a specific test for diagnosis of coronary artery spasm. Am J Cardiol 1997; 80 : 545-549.
12. Hamilton KK, Pepine CJ. A renaissance of provocative testing for coronary spasm? J Am Coll Cardiol 2000; 35 : 1857-1859.
13. Chahine RA, Feldman RL, Giles TD et al. Randomized placebo-controlled trial of amlodipine in vasospastic angina. Amlodipine Study 160 Group. J Am Coll Cardiol 1993; 21 : 1365-1370.
14. Yasue H, Touyama M, Kato H et al. Prinzmetal’s variant form of angina as a manifestation of alpha-adrenergic receptor-mediated coronary artery spasm: documentation by coronary arteriography. Am Heart J 1976; 91 : 148-155.
15. Yasue H, Takizawa A, Nagao M. Long-term prognosis for patients with variant angina and influential factors. Circulation 1988; 78 : 19.
16. Bory M, Pierron F, Panagides D et al. Coronary artery spasm in patients with normal or near normal coronary arteries. Long-term follow-up of 277 patients. Eur Heart J 1996; 17 : 1015-1021.
17. Rovai D, Bianchi M, Baratto M et al. Organic coronary stenosis in Prinzmetal’s variant angina. J Cardiol 1997; 30 : 299-305.
18. Walling A, Waters DD, Miller DD et al. Long-term prognosis of patients with variant angina. Circulation 1987; 76 : 990-997.
19. Gupta S et al. Coronary stent for variant angina: atypical presentation. Cathet Cardiovasc Diagn 1998; 45 : 439-441.
20. Shin DL et al. Therapy options for Prinzmetal angina induced ventricular vulnerability. Z Kardiol 2003; 92 : 332-338.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2007 Issue 6-
All articles in this issue
- Klinické zkušenosti s léčbou dlouhodobým inzulinovým analogem glargin v diabetologickém centru
- Vliv dlouhodobé terapie inzulinovou pumpou (CSII) u pacientů s diabetes mellitus 1. typu na metabolickou kompenzaci a výskyt hypoglykemií. Porovnání s intenzifikovanou konvenční inzulinovou terapií (MDI)
- Subpopulace CD34+buněk a jejich význam pro přihojení štěpu u příbuzenských alogenních transplantací periferních kmenových buněk
- Esenciální trombocytemie a další myeloproliferace s trombocytemií v údajích registru pacientů léčených Thromboreductinem® do konce roku 2006
- Optimální délka antikoagulační léčby po žilní tromboembolické příhodě: obecný či individualizovaný přístup?
- Kardiotoxicita antracyklínovej liečby vo svetle nových biochemických diagnostických možností
- Genetické faktory a riziko kardiovaskulárnych ochorení
-
Nové poznatky v genetice autoimunitního diabetu
(1): Monogenně podmíněné typy autoimunitního diabetu - Je familiární hypercholesterolemie v České republice pod kontrolou?
- Hypogonadizmus - závažná komplikace chronické nedostatečnosti ledvin
- Postavení neoadjuvantní chemoterapie v léčbě nemalobuněčného plicního karcinomu
- Maligní arytmie u pacienta s variantní (Prinzmetalovou) anginou pectoris
- Ojedinělá komplikace při pokusu o zavedení dočasné kardiostimulace
- Zlepšování výsledků léčby vybraných krevních chorob a změny nákladů na tuto léčbu. Otázky pro ekonomy a další odborníky
- Jsou nezbytná kvalifikovaná rozhodnutí vycházející z věrohodných dat
- Náklady na léky v České republice - příčiny růstu a návrhy řešení
- Príspevok nefrológie vo Fakultnej nemocnici L. Pasteura a Lekárskej fakulty Univerzity P. J. Šafárika v Košiciach ku histórii českej nefrológie
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Náklady na léky v České republice - příčiny růstu a návrhy řešení
- Hypogonadizmus - závažná komplikace chronické nedostatečnosti ledvin
- Maligní arytmie u pacienta s variantní (Prinzmetalovou) anginou pectoris
- Genetické faktory a riziko kardiovaskulárnych ochorení
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

