-
Medical journals
- Career
Aortální stenóza, skleróza a ateroskleróza
: K. Linhartová 1; R. Čerbák 2; H. Rosolová 3
: I. interní klinika Lékařské fakulty UK a FN Plzeň, přednosta prof. MUDr. K. Opatrný, jr. DrSc. 1; Centrum kardiovaskulární a transplantační chirurgie Brno, ředitel prof. MUDr. J. Černý, DrSc. 2; II. interní klinika Lékařské fakulty UK a FN Plzeň, přednosta doc. MUDr. J. Filipovský, CSc. 3
: Vnitř Lék 2005; 51(4): 458-461
: Reviews
V posledních 10 letech bylo prokázáno, že do rodiny aterosklerózy patří kalcifikační nemoc aortální chlopně zahrnující širokou škálu postižení od kalcifikace bez obstrukce průtoku, aortální sklerózy, po významnou aortální stenózu. Pro příbuznost s aterosklerózou svědčí histologické studie, uplatnění stejných základních rizikových faktorů i častá koincidence s koronární nemocí. Předmětem výzkumu je vztah k alteraci metabolizmu kalcia, dysfunkci endotelu, zánětlivé, infekční etiologii i genetickým faktorům. Nový pohled na patologii aortální chlopně mohou přinést studie hledající nové rizikové faktory a rozdíly mezi koronární nemocí a nemocí aortální chlopně. Otázku kauzálního vztahu rizikových faktorů a kalcifikované, aterosklerotické, či dokonce „ateroskleritické“ nemoci aortální chlopně pak mohou vyřešit prospektivní randomizované intervenční studie.
Klíčová slova:
kalcifikace aortální chlopně – aortální skleróza–aortální stenóza – koronární nemoc – aterosklerózaÚvod
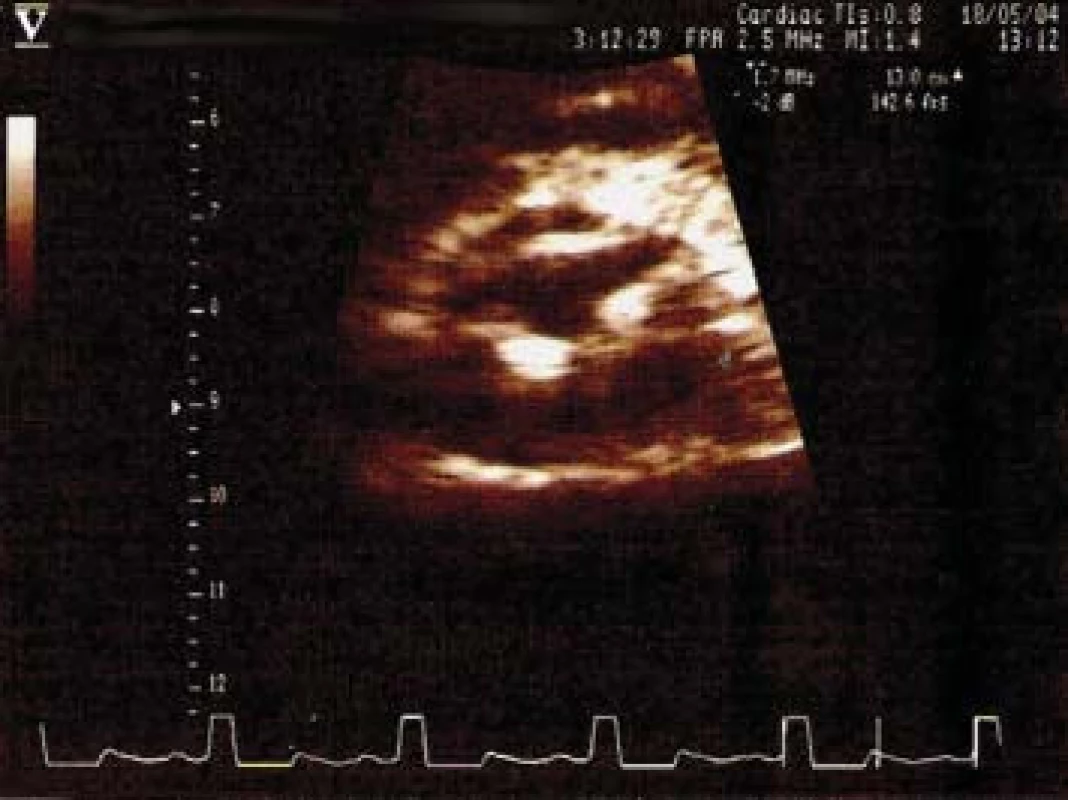
Kardiovaskulární nemoci jsou ve vyspělých zemích příčinou více než poloviny úmrtí. Teprve v posledních 10 letech bylo prokázáno, že do rodiny aterosklerózy patří i kalcifikační nemoc aortální chlopně (calcific aortic valve disease). Zahrnuje širokou škálu postižení od kalcifikace aortální chlopně bez obstrukce průtoku, označované aortální skleróza (obr. 1), po hemodynamicky významnou aortální stenózu.
Aortální stenóza je dnes ve vyspělých zemích nejčastěji operovanou chlopenní vadou. Její prevalence stoupá s věkem, v populaci osob starších 65 let se udává 2–3 % [1,2].
Aortální skleróza se nachází u 21 až 26 % osob starších 65 let. Je spojena s asi 50% zvýšením rizika kardiovaskulární mortality i morbidity [1,3].
Histologie kalcifikované aortální chlopně
Aortální chlopeň se skládá ze 3 jasně definovaných vrstev: centrálně uložené fibrózy obsahující kolagen, ventricularis – vrstvy bohaté na elastin na komorové straně cípu – a spongiozy, vrstvy řídké pojivové tkáně v bazální třetině cípu. Strukturální změny se koncentrují na aortální straně cípů. Společným rysem aortální sklerózy a lehké aortální stenózy je takzvaná „časná léze“ [4,5,6]. Charakterizuje ji porušení bazální membrány a ztluštění subendoteliální vrstvy dané infiltrací lipidů a buněčných elementů, zejména T-lymfocytů a monocytů, z nichž se stávají makrofágy a posléze pěnové buňky. Změny pokračují i do fibrózy. V pokročilém stadiu jsou cípy stenotických chlopní difuzně ztluštělé s degenerací komponent struktury. Dominantním rysem významné aortální stenózy je kalcifikace, nezřídka se nachází i zralá trámčitá kost s krvetvornými elementy a aktivní remodelací [7]. Kalcifikace u dvojcípé aortální chlopně jsou spíše nodulární a u trojcípé více difuzní, avšak histologické rysy se významně neliší [1].
Patogeneze aortální sklerózy a stenózy
Experimentální práce na zvířatech ukazují, že v patogenezi aortální vady se uplatňuje proces buněčné proliferace i apoptózy [8,9]. Společným rysem aortální sklerózy a stenózy je makroskopické ztluštění cípů chlopně, dané akumulací buněk, lipidů a extracelulární matrix. Ústřední roli hrají lipoproteiny, které pronikají přes poškozený endotel na aortální straně cípů, jsou modifikovány a pohlcovány makrofágy, z nichž vznikají pěnové buňky. Pro plazmatický původ lipidů svědčí společná lokalizace extracelulárních lipidů a aterogenních apolipoproteinů apo-B, (a) a E. Předpokládá se, že pod toxickým vlivem oxidovaného LDL uvolňují fibroblasty měchýřky matrix, které jsou jádrem následné kalcifikace. Subendoteliálně a ve fibróze se nachází velké množství aktivovaných T-lymfocytů uvolňujících cytokiny včetně TGF, který aktivuje tvorbu extracelulární matrix. Dále byla popsána přítomnost kalcifikačních buněk nejasného původu, které se transformují v buňky podobné osteoblastům a spontánně tvoří kalcifikované uzlíky. Po stimulaci růstovými faktory tvoří tyto buňky proteiny podílející se na osifikaci, jako například osteopontin. Kalcifikace aortální chlopně je tedy komplexní, vysoce regulovaný a potenciálně modifikovatelný proces, který má mnoho společných rysů s aterosklerózou. Na rozdíl od tepenné aterosklerózy se ve chlopních neuplatňují buňky hladké svaloviny [4,11].
Klinické faktory spojené s kalcifikacemi aortální chlopně
Řada klinických studií prokázala asociaci aortální stenózy i sklerózy s klasickými rizikovými faktory aterosklerózy, jako je věk, mužské pohlaví, hladina celkového cholesterolu, LDL - cholesterolu, LP(a), diabetes mellitus, hypertenze a kouření [1,10]. Ústřední roli z rizikových faktorů má patrně hladina lipidů [11].
Aortální skleróza byla v Cardiovascular Health Study [3] spojena s asi 50% zvýšením kardiovaskulární morbidity a mortality osob nad 65 let, a to i po kontrole na základní rizikové faktory a přítomnost aterosklerózy. Asociace s nepříznivým klinickým průběhem byla zjištěna i u kalcifikací mitrálního anulu [12]. Jeon et al zjistili, že kalciová depozita v aortální chlopni, mitrálním anulu a ascendentní aortě jsou významným prediktorem abnormálních SPECT-nálezů u osob pod 65 let [13]. Kalcifikace v chlopních korelují se stupněm kalcifikací v koronárních tepnách [14]. Méně je známo o korelaci extrakoronárních kalcifikací s koronarografickými nálezy. Nečetné studie svědčí pro asociaci aortální sklerózy s významnou koronární nemocí [14,19]. Naopak stupeň kalcifikace 187 excidovaných stenotických aortálních chlopní stanovený atomovou absorpční spektroskopií nekoreloval se závažností koronární nemoci v době operace [15].
Kalcifikace aortální chlopně a nepříznivá prognóza
Vztah mezi hemodynamicky významnou aortální stenózou a mortalitou byl podrobně popsán a je podkladem indikace náhrady aortální chlopně [16]. Stenóza dvojcípé aortální chlopně obvykle progreduje rychleji, takže pacienti s významnou bikuspidální stenózou jsou v průměru o 10 let mladší než s trojcípou [1]. Mechanizmus vyšší kardiovaskulární mortality amorbidity u aortální sklerózy není zatím jasný. Prospektivní sledování pacientů se sklerózou aortální chlopně ukázalo, že během 4 let vznikne aortální stenóza u třetiny pacientů. Rychlost progrese je však individuálně velmi rozdílná a progrese k aortální stenóze zřejmě horší prognózu aortální sklerózy nevysvětluje [17,18]. Další hypotézou je, že aortální skleróza je pouze markerem pokročilejší koronární nemoci [14,19]. Koronární nemoc i aortální skleróza mohou být také důsledkem společného patofyziologického mechanizmu, například zánětu [20] nebo jiných dosud nedefinovaných faktorů.
Aortální stenóza a skleróza versus ateroskleróza
Většina prací se zatím zaměřovala na průkaz společných rysů aortální stenózy, sklerózy i aterosklerózy. Mezi těmito procesy však existuje i řada odlišností. Zatímco asi polovina osob s aortální stenózou má také koronární nemoc, pouze menšina pacientů s koronární nemocí má aortální stenózu [21]. Dvojcípá chlopeň akceleruje rozvoj aortální stenózy, avšak u řady pacientů s bikuspidální chlopní stenóza nikdy nevznikne. Progrese od aortální sklerózy ke stenóze je nekonstantní a nemá patrně zásadní význam. U pacientů s koronární nemocí je důležitým faktorem nestabilita plátu, ruptura a nasedající trombóza, na chlopních tyto procesy nebyly prokázány. Rozdílná odpověď na noxu (nebo noxy) endotelu a endokardu může být dána i rozdílností obou výstelek.
Dominantním rysem aterosklerotického procesu v aortální chlopni je kalcifikace. Nabízí se proto otázka, zda horší prognóza pacientů s kalcifikovanými chlopněmi nesouvisí například s abnormální tkáňovou kalcifikací či obecně s alterací metabolizmu kalcia. Stupeň kardiálních i vaskulárních kalcifikací je vyšší u pacientů s renální insuficiencí, a to již v predialyzačním stadiu [22]. Mortalita pacientů v terminální fázi selhání ledvin je navíc 20násobná oproti věkem a pohlavím odpovídajícím kontrolám. U pacientů v renální insuficienci byl nalezen vztah mezi kalcifikacemi a hladinou kalcia, fosforu, vyššími hladinami parathormonu, léčbou analogy vitaminu D, hladinou homocysteinu a stupněm renální insuficience či délkou dialýzy [22,23,24]. Vztah metabolizmu kalcia a kalcifikací v srdci u pacientů s normální funkcí ledvin zatím nebyl podrobně zkoumán. První nedávno publikovaná studie na toto téma zjistila asociaci vyšších hladin fosforu a kalcium-fosfátového součinu se stupněm aortální stenózy u 107 pacientů s normální funkcí ledvin [25], jiní nalezli vztah mezi genetickými polymorfizmy receptoru pro vitamin D a vznikem aortální stenózy [26].
Dysfunkce endotelu má zásadní význam v patofyziologii koronární nemoci i dalších kardiovaskulárních onemocnění. Byla nalezena asociace systémové endoteliální dysfunkce s aortální sklerózou [27]. Ghaisas et al [28] zjistili u aortální stenózy zvýšenou hladinu V-CAM-1, I-CAM-1 a E-selektinu v periferní krvi, která korelovala s endoteliální expresí na chlopni a klesala až po 18 měsících po náhradě chlopně. Cytoadhezivní molekuly mají klíčový význam v nasměrování leukocytů do místa zánětu a jejich přítomnost na stenotických chlopních naznačuje možnou roli zánětu v patogenezi aortální stenózy. Hypotézu zánětlivé etiologie podporují i studie prokazující možný podíl Chlamydia pneumoniae u koronární nemoci i aortální stenózy [29,30].
Zcela nový úhel pohledu na souvislost mezi aortálními vadami, dysfunkcí endotelu a genetickými faktory přináší experimentální studie, v níž byla zkoumána aortální chlopeň u myší s deficitem endoteliální NO-syntházy (eNOS): 5 z 12 eNOS deficientních myší mělo dvojcípou aortální chlopeň, zatímco umyší bez deficitu se dvojcípá chlopeň vůbec nevyskytla [31].
Aterosklerotický proces v cévách a v aortální chlopni má řadu společných rysů histologicky i na molekulární úrovni, často se vyskytují společně, u obou se uplatňují klasické rizikové faktory aterosklerózy, naopak odlišností je dominantní význam kalcifikace a neúčast hladké svaloviny při postižení chlopně. Dalším krokem k pochopení obou procesů by mělo být zkoumání rozdílů v uplatnění rizikových faktorů mezi koronární a aortální nemocí i hledání nových metabolických souvislostí. Otázku kauzálního vztahu rizikových faktorů a kalcifikované, aterosklerotické či dokonce „ateroskleritické“ nemoci aortální chlopně mohou vyřešit prospektivní randomizované intervenční studie.
Práce byla podpořena grantem IGA MZ NR/8306-5.
MUDr. Kateřina Linhartová
www.fnplzen.cz
e-mail: linhartova@fnplzen.cz
Doručeno do redakce: 25. 5. 2004
Přijato po recenzi: 13. 7. 2004
Sources
1. Davies MJ, Treasure T, Parker DJ et al. Demographic characteristics of patients undergoing aortic valve replacement for stenosis: relation to valve morphology. Heart 1996; 75 : 174–178.
2. Stewart BF, Siscovick D, Lind BK et al. Clinical factors associated with calcific aortic valve disease. J Am Coll Cardiol 1997; 29 : 630–634.
3. Otto C, Lind BK, Kitzman DW et al. Association of aortic valve sclerosis with cardiovascular mortality and morbidity in the elderly. N Engl J Med 1999; 341 : 142–147.
4. Otto CM, Kuusisto J, Reichenbach DD et al. Characterization of the early lesion of „degenerative“ valvular aortic stenosis: histologic and immunohistochemical studies. Circulation 1994; 90 : 844–853.
5. O’Brien KD, Reichenbach DD, Marcovina SM et al. Apolipoproteins B, (a) and E accumulate in the morphologically early lesion of „degenerative“ valvular aortic stenosis. Arterioscler Tromb Vasc Biol 1996; 16 : 523–532.
6. Olsson M, Thyberg J, Nilsson J. Presence of oxidized low density lipoprotein in nonrheumatic stenotic aortic valves. Arterioscler Tromb Vasc Biol 1999; 19 : 1218–1222.
7. Mohler ER III, Gannon F, Reynolds C et al. Bone formation and inflammation in cardiac valves. Circulation 2001; 103 : 1522–1528.
8. Drolet MC, Arsenault M, Dojet J. Experimental aortic valve stenosis in rabbits. J Am Coll Cardiol 2003; 41 : 1211–1217.
9. Rajamannan NM, Subramanian M, Springett M et al. Atorvastatin inhibits hypercholesterolemia-induced cellular proliferation and bone matrix production in the rabbit aortic valve. Circulation 2002; 105 : 2660 – 665.
10. Agmon Y, Khandheria BK, Meissner I et al. Aortic valve sclerosis and „aortic atherosclerosis“ different manifestations of the same disease? Insights from a population-based study. J Am Coll Cardiol 2001; 38 : 827–834
11. Chan KL. Is aortic stenosis a preventable disease? J Am Coll Cardiol 2003; 42 : 593–599.
12. Adler Y, Fink D, Spector D et al. Mitral annular calcification – a window to diffuse atherosclerosis of the vascular system. Atherosclerosis 2001; 155 : 1–8.
13. Jeon DS, Atar S, Brach AV et al. Association of mitral annulus calcification, aortic valve sclerosis and aortic root calcification with abnormal myocardial perfusion single proton emission tomography in subjects age ≤ 65 years old. J Am Coll Cardiol 2001; 38 : 1988–1993.
14. Yamamoto H, Shavelle D, Tarasu J et al. Valvular and thoracic calcium as a marker of the extent and severity of angiographic coronary artery disease. Am Heart J 2003; 146(1): 153–159.
15. Ortlepp JR, Schmitz F, Mevissen V et al. Lack of association between severity of coronary artery disease and aortic valve calcification determined by atomic absorption spectroscopy in 187 patients with aortic valve replacement. J Am Coll Cardiol 2004; 43 : 434A.
16. Ross J jr, Braunwald E. Aortic stenosis. Circulation 1968; 38 : 61–67.
17. Faggiano P, Antonini-Canterin F, Ehrlicher A et al. Progression of aortic valve sclerosis to aortic stenosis. Am J Cardiol 2003; 91 : 99–101.
18. Cosmi JE, Kort S, Tunick P A. et al. The risk of the development of aortic stenosis in patients with „benign“ aortic valve thickening. Arch Intern Med 2002; 162 : 2345–2347.
19. Adler Y, Vatuji M, Herz I et al. Nonobstructive aortic valve calcification: a window to significant coronary artery disease. Atherosclerosis 2002; 161 : 193–197.
20. Chandra HR, Goldstein JA, Choudhary N et al. Adverse outcome in aortic sclerosis is associated with coronary artery disease and inflammation. J Am Coll Cardiol 2004; 43 : 169–175.
21. Otto C, O’Brien KD. Why is there discordance between calcific aortic stenosis and coronary artery disease? Heart 2001; 85 : 601–602.
22. Qunibi WY, Nolan CA, Ayus JC. Cardiovascular calcification in patients with end-stage renal disease: a century old phenomenon. Kidney International 2002; 62(Suppl 82): S73–S80.
23. Merjanian R, Budoff M, Adler S et al. Coronary artery, aortic wall, and valvular calcification in nondialyzed individuals with type 2 diabetes and renal disease. Kidney International 2003; 64 : 263–271.
24. Raggi P, Boulay A, Chasan-Taber S et al. Cardiac calcification in adult hemodialysis patients. A link between end-stage renal disease and cardiovascular disease? J Am Coll Cardiol 2002; 39 : 695–701.
25. Mills WR, Einstadter D, Finkelhor RS et al. Calcium-phosphorus product is associated with severity of aortic stenosis in patients with normal renal function. J Am Coll Cardiol 2004; 43 : 434A.
26. Ortlepp JR, Hoffmann R, Ohme F et al. The vitamin D receptor genotype predisposes to the development of calcific aortic stenosis. Heart 2001; 85 : 635–638.
27. Poggianti E, Venneri L, Chubuchny V et al. Aortic valve sclerosis is associated with systemic endotelial dysfunction. J Am Coll Cardiol 2003; 41 : 136–141.
28. Ghaisas NK, Foley JB, O’Briain DS et al. Adhesion molecules in nonrheumatic aortic valve disease: endothelial expression, serum levels and effects of valve replacement. J Am Coll Cardiol 2000; 36 : 2257–2262.
29. Cassone A. Chlamydia pneumoniae and lipoprotein (a): the right combination for atherosclerosis? Eur Heart J 2000; 21 : 559–560.
30. Glader CA, Birgander LS, Soederberg S et al. Lipoprotein (a), Chlamydia pneumoniae, leptin and tissue plasminogen activator as risk markers for valvular aortic stenosis. Eur Heart J 2003; 24 : 198–208.
31. Lee TC, Zhao YD, Clourtman DW et al. Abnormal aortic valve development in mice lacking endothelial nitric oxid synthase. Circulation 2000; 101 : 2345–2348.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2005 Issue 4-
All articles in this issue
- The influence of the combined aerobic training to the changes of autonomous modulation at the ill patients after the acute myocardial infarction
- The pleural effusion in general internal practice
- Molecular pathophysiology of late diabetic complications – genetic predisposition to the development of diabetic complications
- The transplantation of the stem cells in cardiology
- Aortic stenosis, sclerosis, and atherosclerosis
- Hyperhomocysteinemia – is it still the only interesting but diagnostically unsignificant finding?
- What are the risk factors of ischaemic cardiac disease (ICD) knowledge at our physicians? The comparison with the condition in 1991
- The epidemiological analysis of patients with permanent cardiostimulation at the Department of Cardiology in Faculty Hospital Brno-Bohunice
- Klinický význam mírně zvýšených hodnot α−fetoproteinu v séru u pacientů s chronickou hepatitidou C a B
- Rehabilitace po infarktu myokardu a revaskularizaci u starších nemocných
- The uncommon way of noninvasive demonstration of myocardial ischaemia via cold exposure
- Courses on ethics in the faculty of medicine: A route from descriptive ethics to moral norms
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Klinický význam mírně zvýšených hodnot α−fetoproteinu v séru u pacientů s chronickou hepatitidou C a B
- The pleural effusion in general internal practice
- Aortic stenosis, sclerosis, and atherosclerosis
- Hyperhomocysteinemia – is it still the only interesting but diagnostically unsignificant finding?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career