-
Medical journals
- Career
Vliv kombinovaného aerobního a silového tréninku na funkci levé komory srdeční u nemocných po akutním infarktu myokardu
Authors: L. Elbl 1; V. Chaloupka 1; I. Tomášková 1; F. Jedlička 1; S. Nehyba 1; P. Kala 2; J. Schildberger 2; M. Poloczek 2; O. Boček 2
Authors‘ workplace: Oddělení funkčního vyšetřování, FN Brno, pracoviště Bohunice, přednosta doc. MUDr. Václav Chaloupka, CSc. 1; Interní kardiologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Jindřich Špinar, CSc., FESC 2
Published in: Vnitř Lék 2005; 51(2): 190-197
Category: Original Contributions
Overview
Cíl práce:
Předložená práce se zaměřila na posouzení vlivu kombinovaného aerobního tréninku se silovým cvičením prováděného v rámci časné řízené ambulantní rehabilitace na funkci levé komory srdeční u nemocných po prvním akutním infarktu myokardu.Pacienti a metody:
Autoři zařadili do sledování 109 nemocných (18 žen, 91 mužů) ve věku 58 ± 9 let. 34 nemocných mělo sníženou ejekční frakci (EF) < 50 % (38 ± 6 %). Doba od vzniku infarktu myokardu do zahájení rehabilitace byla 31 ± 7 dní, u nemocných po aortokoronárním bypassu 45 ± 19 dní. Nemocní byli před a po rehabilitaci vyšetřeni pomocí klidové a dynamické zátěžové echokardiografie a spiroergometrie. Byla vyhodnocena klidová a zátěžová ejekční frakce, objemy levé komory (LK), index hybnosti stěny LK (IHSLK) a vrcholový příjem kyslíku (pVO2). Rehabilitační program probíhal po dobu 8 týdnů. Aerobní cvičení bylo provedeno na úrovni 60 % pVO2 a po 14 dnech doplněno o silová cvičení.Výsledky:
V obou podskupinách nemocných došlo po rehabilitaci k významnému zvýšení pVO2 a zátěžové tolerance. V podskupině se sníženou EF došlo k mírnému zlepšení klidových (38 ± 6 % vs 45 ± 6 %; p < 0,007) i zátěžových (50 ± 7 % vs 55 ± 6 %; p < 0,001) hodnot EF. Ke stejnému zlepšení došlo i při hodnocení IHSLK. Hodnoty enddiastolického objemu LK (EDV) byly v podskupině se sníženou EF signifikantně vyšší (p < 0,001), v žádné podskupině nedošlo po rehabilitaci k výšení klidových ani zátěžových hodnot EDV. Byl nalezen významný vztah mezi změnou klidové a zátěžové EF a změnou pVO2 u nemocných se sníženou EF (r = 0,36; p < 0,01; respektive r = 0,43; p < 0,001). Závěr: Kombinované aerobní a silové cvičení v rámci časné rehabilitace je bezpečné a nevede ke zhoršení procesu remodelace LK. Tyto závěry platí i pro nemocné s mírnou až středně těžkou systolickou dysfunkcí LK. Význam zjištěných nálezů je nutno zhodnotit dlouhodobým prospektivním sledováním.Klíčová slova:
akutní infarkt myokardu – časná rehabilitace – silové cvičení – remodelace levé komory srdečníÚvod
Kardiovaskulární rehabilitační program zahrnující aerobní cvičení je nedílnou součástí další léčby nemocných po akutním srdečním infarktu. Jeho přínos v rámci sekundární prevence ischemické choroby srdeční (ICHS) zahrnuje zlepšení tolerance zátěže, kvality života, snížení mortality a pravděpodobně i počtu hospitalizací. Významně přispívá k pozitivnímu ovlivnění řady rizikových faktorů ICHS [18,22].
V posledních deseti letech se věnuje problematice rehabilitace po akutním srdečním infarktu velká pozornost. Vedle zjištěných pozitiv zůstává nedořešena otázka možného nežádoucího účinku aerobního cvičení o střední a vyšší intenzitě na proces remodelace levé komory (LK). Tento problém nastínili ve své práci Jugdutt et al, kteří popsali zhoršení procesu remodelace LK u nemocných s rozsáhlým předním srdečním infarktem [15]. V dalším období byly zveřejněny studie, které tento negativní vliv nepotvrdily. Nicméně v některých studiích rehabilitační program probíhal v poměrně delším období po vzniku IM, nebyli zařazeni pacienti s významně sníženou ejekční frakcí (EF) nebo pacienti nerehabilitovali pod odborným vedením [2,5,8]. Navíc je v poslední době zařazováno k aerobnímu tréninku cvičení se silovými prvky, o jehož vlivu na remodelaci LK máme minimum informací [13,14].
Cílem předložené práce bylo posouzení vlivu kombinovaného aerobního tréninku se silovým cvičením na funkci levé komory srdeční po absolvování časného ambulantního řízeného rehabilitačního programu u nemocných po prvním akutním srdečním infarktu se zaměřením na nemocné se systolickou dysfunkcí LK.
Soubor nemocných
Do rehabilitačního programu jsme zařadili 109 nemocných, 18 žen a 91 mužů, po přestálém prvním IM ve věku (58 ± 9 let, medián 58 let, 26–80). Nemocné jsme rozdělili do 2 skupin podle vstupních hodnot EF. 34 nemocných (32 %) mělo sníženou EF LK pod 50 % a 75 (68 %) mělo normální hodnoty EF. Charakteristika obou podskupin je uvedena v tab. 1 a 2.
Table 1. Charakteristika podskupin. 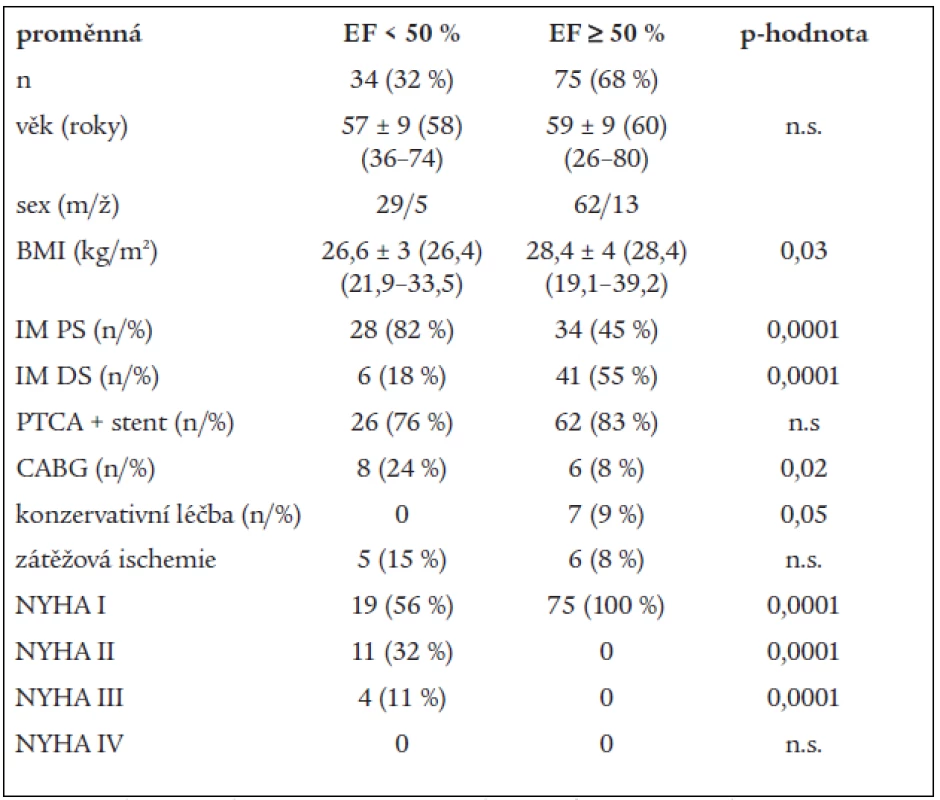
BMI – body mass index, IM PS – infarkt přední stěny levé komory srdeční, IM DS – infarkt dolní stěny levé komory srdeční, PTCA – perkutánní transluminální koronární angioplastika, CABG – aortokoronární bypass Table 2. Farmakoterapie v podskupinách. 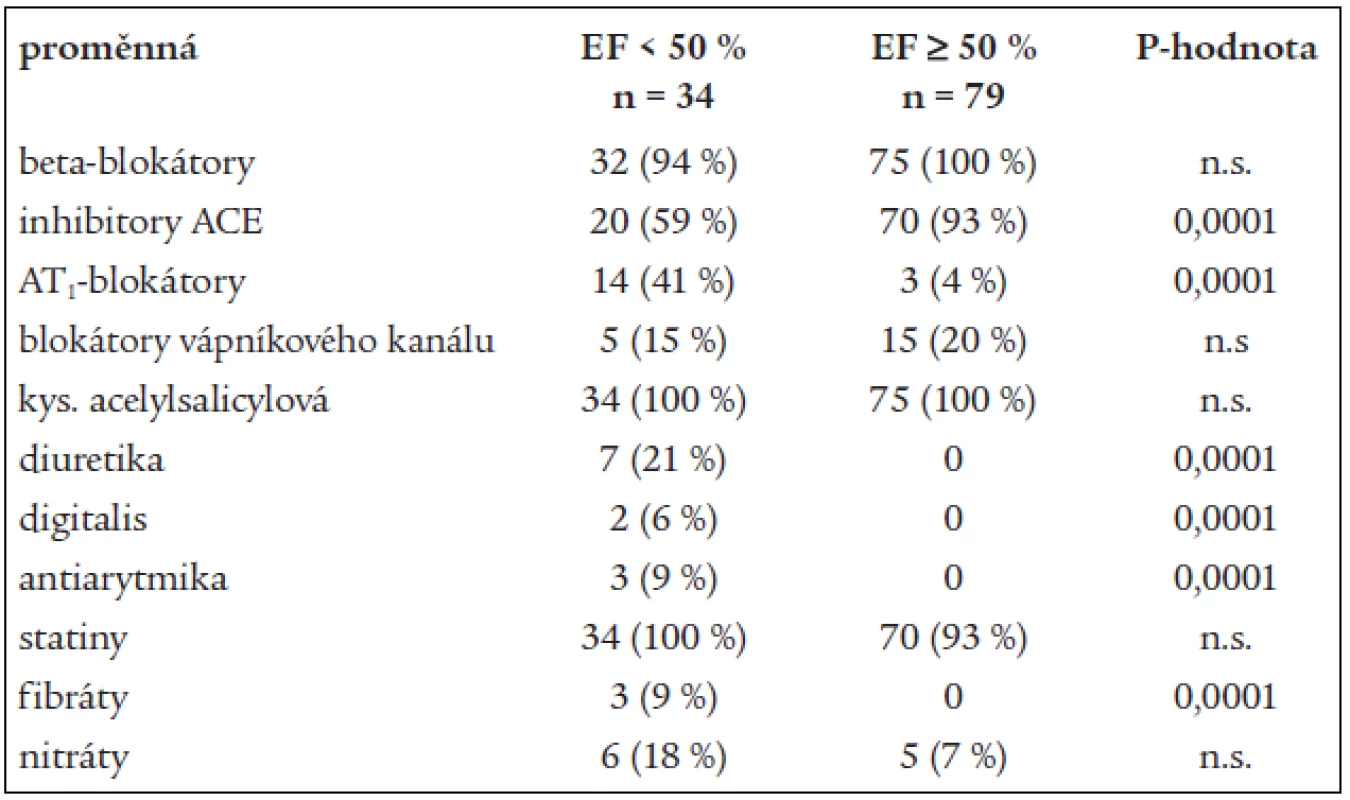
Nemocní byli zařazeni do rehabilitačního programu 31 ± 7 dní (medián 29 dní, 13–44) od vzniku akutního infarktu. U pacientů po kardiochirurgickému zákroku byla doba nástupu 45 ± 19 dní (medián 33 dní, 23–68).
Metodika
Rehabilitační program
Základem rehabilitačního programu je aerobní cvičení probíhající na ergometrech při tepové frekvenci (TF) odpovídající 60 % vrcholového příjmu kyslíku (pVO2). Trénink probíhá 3krát týdně po dobu 8 týdnů. Silové cviky zařazujeme po 2 týdnech od zahájení programu a provádíme je na posilovacím zařízení BASIC Kettler. Stanovíme pro každý cvik maximální zátěž, kterou je pacient schopen 1krát bez pomoci překonat (1-RM). Nemocní s normální EF cvičí na hodnotě 50 % 1-RM, u nemocných se sníženou EF začínáme na hodnotě 30 % 1-RM a cílem je dosáhnout 50 % 1-RM. U těchto nemocných je během silového cvičení trvale sledován EKG záznam na monitoru. Pro silové cvičení používáme sestavu tří cviků: A – vzpírání zátěže dopředu, B – posilování nohou sounož a C – stahování zátěže. Zátěž, se kterou pacient cvičí, je vyjádřena v kg a součtem jednotlivých cviků získáme celkovou sílu [12,13].
Echokardiografické vyšetření
Pacienti byli vyšetřeni před a po absolvování rehabilitačního programu klidovou a dynamickou zátěžovou echokardiografií (ATL UM 7). Zátěž byla provedena kontinuálním zatížením s přírůstkem 25 W/2 min. V klidu a bezprostředně po ukončení zátěže byla stanovena pomocí Simpsnovy metody EF LK. Na základě 16segmentového modelu jsme vypočetli index hybnosti stěny LK (IHSLK) opět pro klidový a pozátěžový záznam. Kinetiku segmentů stěny LK jsme subjektivně hodnotili následovně: normokineza – 1, hypokineza – 2, akineza – 3, dyskineza – 4. Index je výsledkem součtu hodnot přiřazených jednotlivým segmentům děleným počtem segmentů. Hodnoty 1,0 jsou fyziologické, vyšší než 1,0 patologické [11,19].
Spiroergometrie
Spiroergometrické vyšetření (Oxycon Delta, Jaeger) bylo provedeno před a po rehabilitačním programu. Provedli jsme rampový test 20 W/1 min do subjektivního maxima či vzniku symptomů. Stanovili jsme hodnotu vrcholového příjmu kyslíku (pVO2) pro vyhodnocení tréninkového efektu, hodnotu tepového kyslíku (TF-O2) a hodnotu anaerobního prahu (ventilační anaerobní práh) pro určení tréninkové TF.
Statistická analýza dat
Předložené výsledky jsou uvedeny jako průměr ± 1 SD, relativní četnost, interval a medián. Naměřené ukazatele před a po rehabilitačním programu byly srovnány párovým a nepárovým Studentovým t-testem. Vztahy mezi proměnnými jsme vyhodnotili lineární regresní analýzou. Neparametrické hodnoty byly testovány χ2 testem. Hodnoty p < 0,05 byly považovány za statisticky významné. Použili jsme statistický program NCSS 6.0 (Number Cruncher Statistical Systems, USA).
Výsledky
Spiroergometrické ukazatele
Tolerance zátěže (TZ) byla v podskupině se sníženou EF před rehabilitací významně snížena oproti skupině s normální funkcí LK. V obou podskupinách došlo po programu k významnému zvýšení TZ (p < 0,0001), přičemž nebyl nalezen statisticky významný rozdíl mezi podskupinami. Hodnoty vrcholového příjmu kyslíku na vrcholu testu (stejně tak i vztaženého k tělesné hmotnosti) byly nižší před rehabilitací u nemocných s dysfunkcí LK, ale po rehabilitaci rozdíl nalezen nebyl. Nárůst byl v obou podskupinách významný (p < 0,0001), u nemocných se sníženou EF dokonce vyšší (p < 0,05). V obou podskupinách se významně zvýšily hodnoty tepového kyslíku (p < 0,001). Zvýšila se významně hodnota pVO2 vyjádřena v procentu referenční hodnoty pro jedince (tab. 3).
Table 3. Změny zátěžových ukazatelů (spiroergometrie). 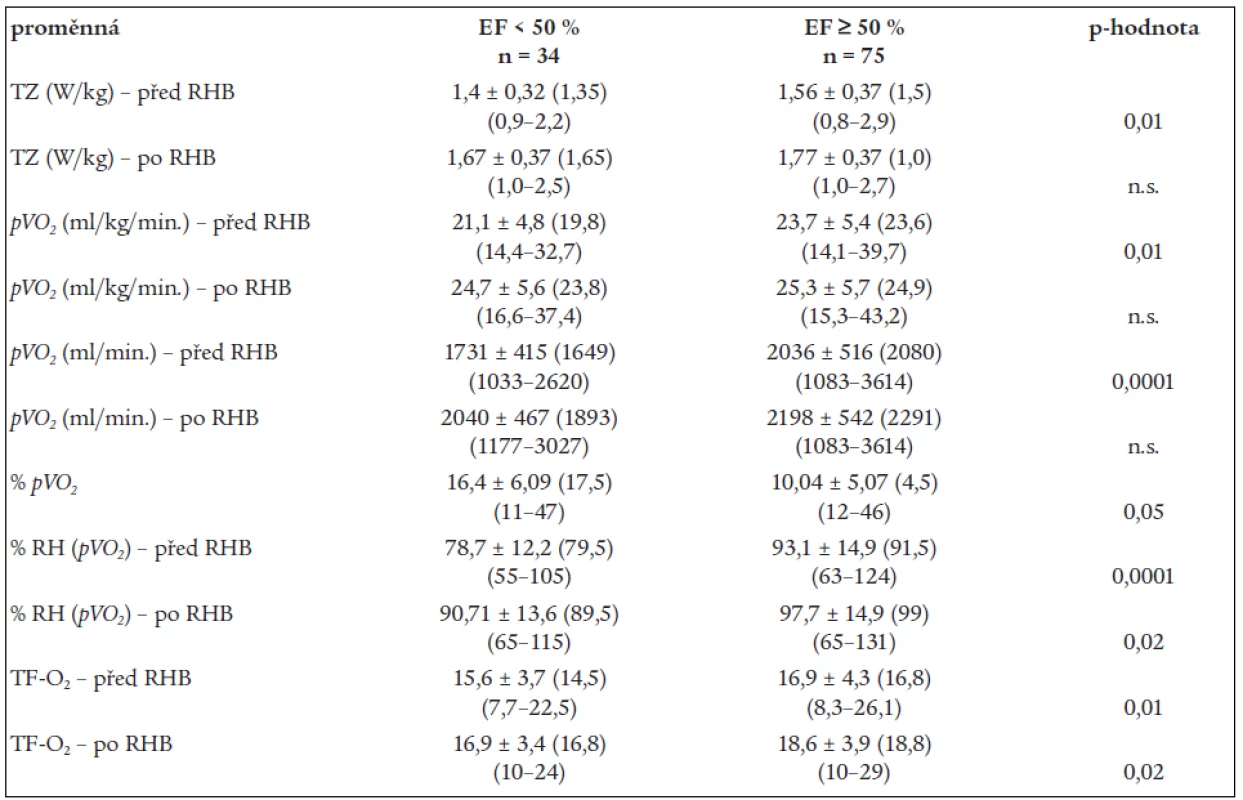
Hemodynamické ukazatele
Rehabilitační program neovlivnil hodnoty klidové TF v podskupinách. Nebyly též statisticky významně změněny hodnoty při maximální zátěži. Pacienti tedy reagovali na vyšší zátěž po rehabilitaci stejnou TF jako na nižší zátěž před zahájením programu. Stejný nález byl zjištěn i u hodnot TK. U nemocných se sníženou EF byly zátěžové hodnoty systolického TK před a po rehabilitaci signifikantně nižší (tab. 4).
Table 4. Změny oběhových ukazatelů. 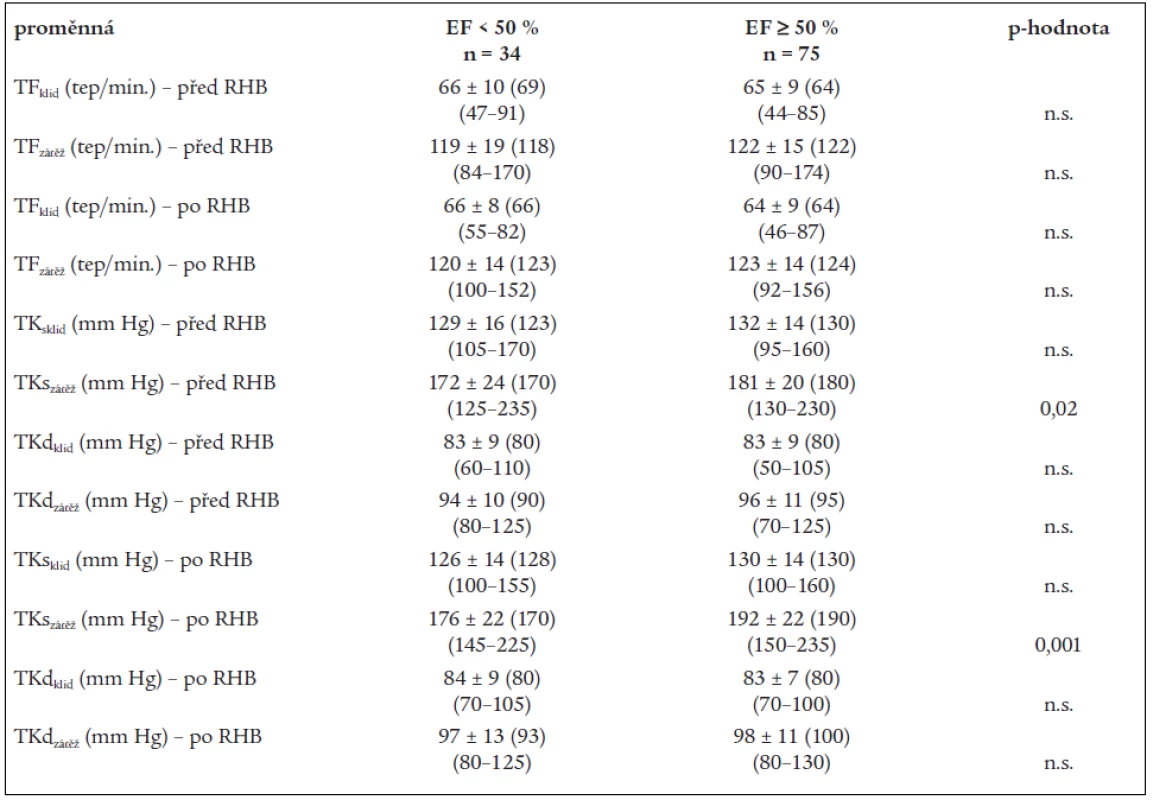
Echokardiografické ukazatele
Ve skupině s normálními hodnotami EF nedošlo ke statisticky významným změnám klidové i zátěžové hodnoty EF, stejně tak i IHSLK. U nemocných se sníženou vstupní EF (38 ± 6 %, medián 41 %, 28–47) došlo ke zvýšení klidové (45 ± 6 %, medián 47 %, 36–56, p < 0,007) i zátěžové hodnoty EF (50 ± 7 %, medián 52 %, 33–60 versus 55 ± 6 %, medián 55 %, 38–58, p < 0,001). Klidové i zátěžové hodnoty IHSLK v podskupině se sníženou EF byly významně horší před i po rehabilitaci ve srovnání s druhou skupinou (p < 0,0001). Po rehabilitaci jsme nalezli v této skupině významné zlepšení klidové (p < 0,01) i zátěžové hodnoty (p < 0,01) IHSLK, nicméně jsou nadále významně horší oproti druhé skupině (p < 0,0001). Ve skupině s normální EF nebyly hodnoty IHSLK významně změněny (tab. 5).
Table 5. Změny ukazatelů funkce levé komory srdeční. 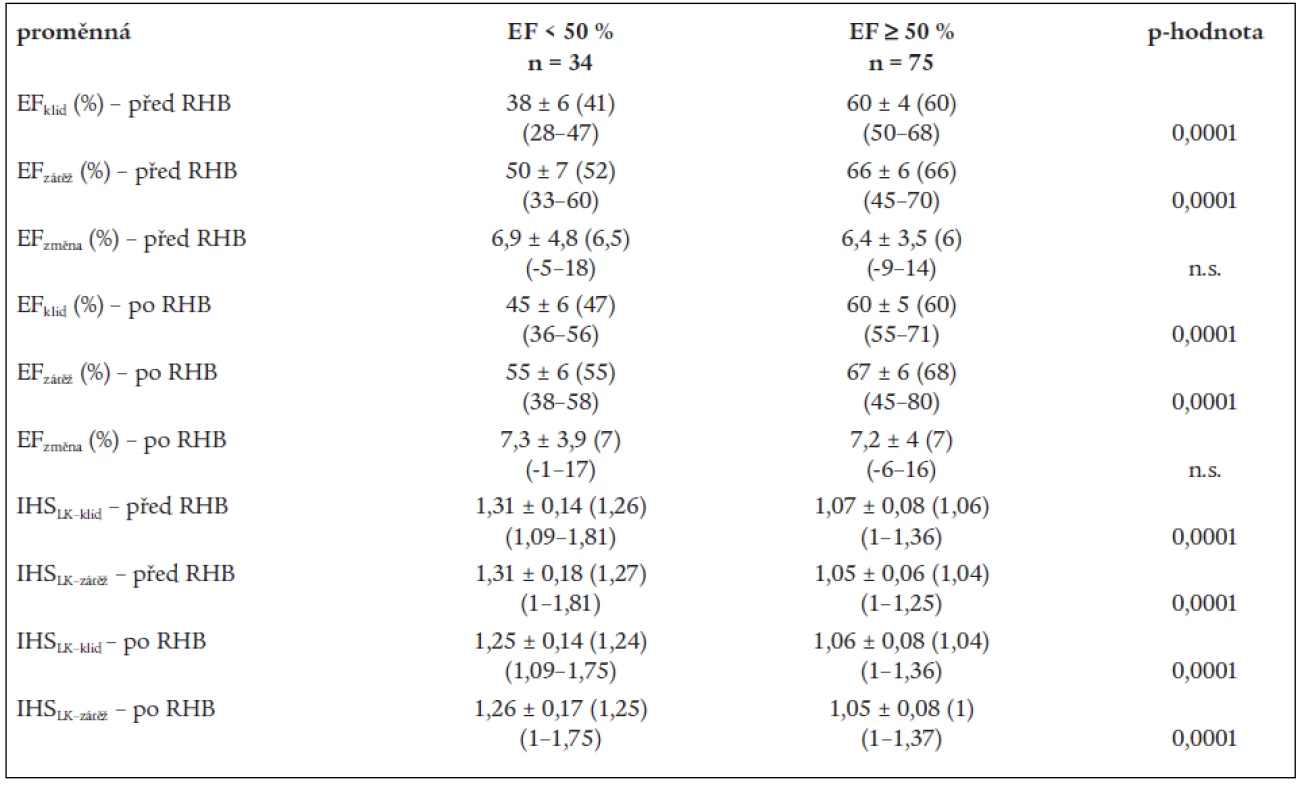
Vyhodnotili jsme změny enddiastolického objemu LK (EDV). Ve skupině se sníženou EF byly vstupní klidové hodnoty EDV významně vyšší ve srovnání s druhou skupinou (145 ± 34 ml, medián 140 ml, 92–231 vs 118 ± 30 ml, medián 119 ml, 49–195, p < 0,001), stejný nález byl zjištěn i u zátěžových hodnot (139 ± 35 ml, medián 133 ml, 75–227 versus 111 ± 28 ml, medián 113 ml, 42–192, p < 0,001). Rehabilitační program neovlivnil klidové ani zátěžové hodnoty EDV v obou skupinách nemocných v porovnání se vstupními hodnotami a rozdíly mezi podskupinami zůstávají nadále významné (graf). Když jsme posuzovali reakci EDV na zátěž, nalezli jsme v obou podskupinách významné snížení zátěžových hodnot v porovnání s klidovými hodnotami (p < 0,001 pro skupinu s EF < 50 %, p < 0,0001 pro skupinu s EF ≥ 50 %).
Graf. Změny enddiastolického objemu levé komory srdeční. Data vyjadřují medián hodnot EDV v klidu a při zátěžové echokardiografii v podskupinách dle hodnot ejekční frakce před rehabilitací a po jejím absolvování. 
EDV – enddiastolický objem levé komory srdeční, EF – ejekční frakce levé komory srdeční Regresní analýza
Nenalezli jsme významný vztah mezi klidovou a zátěžovou EF před RHB a po RHB k pVO2 pro celý soubor i podskupinu se sníženou EF. Nalezli jsme ovšem statisticky významný vztah mezi změnou klidové EF a změnou pVO2 (r = 0,36; p < 0,01), stejně tak mezi změnou zátěžové EF a změnou pVO2 (r = 0,43; p < 0,001) v podskupině se sníženou EF.
Výskyt nežádoucích účinků
Během rehabilitačního programu jsme nezaznamenali výskyt závažných kardiálních komplikací, které by vedly ke změně programu nebo doprovodné medikace. Všichni nemocní absolvovali předepsaná cvičení po celou dobu rehabilitačního programu, silové cvičení bylo ukončeno na úrovni 50 % 1-RM.
Diskuse
Jedním z faktorů určujících prognózu nemocných po akutním srdečním infarktu je funkce LK. Strukturální a funkční změny vedoucí k dilataci, a tedy k procesu remodelace komory mají úzký vztah k morbiditě a mortalitě pacientů [3].
Remodelace LK je proces vedoucí k vývoji dysfunkce LK a následnému rozvoji chronického srdečního selhání. Objemy LK jsou významným prediktorem přežívání nemocných po akutním srdečním infarktu. Endsystolický a enddiastolický objem je v nepřímém vztahu k přežívání, přičemž tento vztah je těsnější pro endsystolický objem [23].
Dilatace LK je lepším prediktorem 6měsíční mortality po IM než ejekční frakce či Killipova klasifikace [3]. Proces remodelace je komplexní zahrnující změny celulární, extracelulární matrix a intersticia. Ztráta viabilního myokardu nebo expanze infarktové oblasti v kombinaci s dilatací viabilního myokardu vede k dilataci komory. U nemocných s Q-infarkty probíhá tento proces již v období 3 dnů až 2 týdnů od vzniku infarktu [10].
Dilatace LK, daná expanzí infarktového ložiska v období 10 až 21 dnů od vzniku infarktu, obvykle vede v dalším období 6–30 měsíců k vývoji a progresi srdečního selhání [6,10].
Veškerá léčebná opatření ovlivňující rozsah ischemického poškození myokardu mohou zmírnit proces remodelace. Jedná se především o rychlé zprůchodnění infarktové tepny. Počet nemocných ošetřených intervenčně je i v naší studii vysoký. Navazující farmakoterapie zaměřená na ovlivnění dilatace komory a prevenci apoptózy zahrnuje podávání inhibitorů ACE, popřípadě AT1-blokátorů a podání beta-blokátorů u velkého procenta nemocných.
Rehabilitační program fáze 2 by měl co nejdříve navazovat na nemocniční fázi rehabilitace. Jeho základem je aerobní cvičení o střední intenzitě zatížení odpovídající 60 % pVO2 . Přínos cvičení v sekundární prevenci ICHS je znám. Rehabilitace snižuje i počet hospitalizací a pravděpodobně i morbiditu a mortalitu [18].
Problém, zda může zasáhnout do procesu remodelace, nastolila práce autorů Jugdutta et al, kteří prokázali u nemocných po předním Q-infarktu negativní vliv tréninku na remodelaci LK [15]. Některé experimentální studie tyto klinické závěry též potvrdily [7,17].
Na druhé straně ve studii EAMI Giannuzzi et al zařadili do 6měsíčního aerobního tréninkového programu nemocné po předním Q-infarktu za 4–8 týdnů po akutní příhodě. Ve srovnání s kontrolní skupinou trénink významně zvýšil zátěžovou toleranci. U nemocných s EF pod 40 % došlo v tomto období k remodelaci LK, ale nebyla negativně ovlivněna cvičením [8]. V další studii ELVD stejní autoři sledovali jen nemocné se sníženou EF < 40 % a zjistili, že dlouhodobé aerobní cvičení nejen zmírnilo proces remodelace, ale na rozdíl od kontrolního souboru došlo i ke zlepšení hodnot EF [9].
K obdobným výsledků dospěl i Dubach et al u nemocných po IM s EF < 40 % [5]. Otsuka et al provedli aerobní trénink na 50–60 % pVO2 i u nemocných po IM s EF < 35 % (30 ± 3 %). Nemocné zařadili velmi časně již 10. až 14. den po vzniku infarktu. I v této podskupině vedl trénink ke srovnatelnému zlepšení zátěžové tolerance ve srovnání s nemocnými s mírně sníženou nebo normální EF a nevedl ke zhoršení procesu remodelace [20].
Aerobní trénink na ergometrech je doplňován jinými typy cvičení. Cannistrová et al kombinovali aerobní cvičení se strečinkem. Echokardiograficky vyhodnotili proces remodelace po rehabilitaci. Autoři nezjistili negativní vliv cvičení na remodelaci při vyhodnocení celé skupiny nemocných, ale k individuálním změnám přesto docházelo a proces remodelace závisel na velikosti původního infarktového ložiska [2].
Dalším typem cvičení, které je v poslední době kombinováno s aerobním tréninkem, je cvičení se silovými prvky. Rezistenční cvičení významně posiluje efekt aerobního tréninku [22]. Bezpečnost silového cvičení byla prokázána u nemocných po IM, u nemocných se sníženou EF, u žen a nemocných starších 65 let a u nemocných s chronickým srdečním selháváním [1,13,14,21]. Nemáme doposud dostatek informací o vlivu tréninku obsahujícím silové prvky na proces remodelace. DeLagardelle et al použili silový trénink u nemocných po IM se srdečním selháním. Po absolvování 40 tréninkových jednotek došlo ve srovnání s kontrolním souborem cvičících bez silových prvků k významnému zvýšení pVO2 , ejekční frakce, frakčního zkrácení a snížení enddiastolického objemu LK [4]. Silové cvičení na úrovni 60 až 70 % 1-RM kombinované s aerobním tréninkem na úrovni 90 % anaerobního prahu nevedlo k progresi dilatace a snížení EF levé komory u nemocných se stabilizovaným srdečním selháváním po srdečním infarktu [16]. Naše práce prokázala, že časná rehabilitace obsahující silové cvičení na úrovni 50 % 1-RM u nemocných po akutním srdečním infarktu nevede v tomto období ke zhoršení procesu remodelace LK. Tento nález se týká též nemocných s lehkou až středně těžkou systolickou dysfunkcí LK. Tento fakt je důležitý pro posouzení, kdy s intenzivním tréninkem začít. Většina prací zařazovala nemocné v období 5 až 16 týdnů od vzniku infarktu. V práci Otsuky et al byli nemocní sice zařazeni ještě dříve než v naší studii a autoři sledovali i podskupinu 17 pacientů s EF < 35 %, ale nepoužili silový trénink [20].
Jedním z faktorů ovlivňujících proces remodelace LK je hodnota napětí stěny LK. Změny preloadu a afterloadu při aerobním cvičení mohou vést ke zvyšování systolického i diastolického napětí stěny komory a zhoršit proces remodelace u nemocných s předním infarktem. Silové cvičení představující izometrickou zátěž a vedoucí k náhlým změnám krevního tlaku může významně zvýšit endsystolické napětí stěny LK [7,17,22]. Hodnota dvojproduktu je u silového cvičení nižší než u aerobního. Navíc je zde snížen venózní návrat, je nižší enddiastolické napětí stěny LK, v důsledku vyššího diastolického tlaku i lepší subendokardiální perfuze. Hodnoty zatížení mezi 40–60 % 1-RM jsou pro pacienty po IM bezpečné a pravděpodobně neovlivní proces remodelace [22]. Proč aerobní trénink v některých studiích vedl ke zhoršení remodelace a v některých ne, je obtížné vysvětlit. Velkou roli v negativním vlivu na remodelaci hraje velikost infarktového ložiska a stav koronárního řečiště [10]. Řada pacientů v publikovaných studiích byla léčena konzervativně, tedy trombolýzou. Ne všechny studie mají k dispozici i koronarografické nálezy. Jak ukázala studie EAMI, remodelace LK se vyvíjí u všech pacientů nezávisle na tréninku, ale trénink její průběh nezhoršuje, což poukazuje i na volný vztah změn napětí stěny komory k vývoji remodelace [8].
Významnou roli hraje i stupeň zatížení. Naše výsledky poukazují na skutečnost, že při maximálním testu prováděném před a po rehabilitaci nedošlo ke zvýšení enddiastolického objemu LK. Pacienti rehabilitují na úrovni střední intenzity zátěže odpovídající 60 % pVO2 . Tento stupeň zatížení je bezpečný a pravděpodobně nepředstavuje riziko pro remodelaci LK.
Limitace studie
Předložená práce je prospektivním sledováním nemocných po srdečním infarktu. Prozatím řeší jen vývoj remodelace ve velmi krátkém poinfarktovém období, ale z časového hlediska nesmírně důležitém s ohledem na průběh reparačních procesů v myokardu po proběhlém akutním infarktu myokardu a s ohledem na nutnost rychlého zařazení pacienta do běžného denního života.
Jak ovlivní časná rehabilitace dlouhodobý proces remodelace, je úkolem dalšího prospektivního sledování, které provádíme.
Ve studii je poměrně málo nemocných s těžkou systolickou dysfunkcí LK. Pacientů s EF ≤ 35 % bylo zařazeno 7 a vzhledem k tak malému počtu jsme je prozatím nehodnotili jako samostatnou skupinu.
Jsme si vědomi absence kontrolního souboru. Vzhledem k tomu, že rehabilitace II. fáze po IM je léčebným standardem, nelze vytvořit adekvátní kontrolní soubor, či provést randomizaci. Do ambulantního řízeného programu nezařadíme kolem 20–30 % nemocných z důvodů přidružených onemocnění, nespolupráce pacienta, ale i ze sociálních a ekonomických důvodů. Tato skupina nemůže též představovat kontrolní soubor.
Závěr
Závěrem lze říci, že kombinovaný aerobní trénink se silovými prvky u nemocných po akutním infarktu je bezpečný a v rámci časné rehabilitace nevede ke zhoršení procesu remodelace LK. Tyto nálezy platí i pro nemocné s mírnou až středně těžkou systolickou dysfunkcí levé komory. Jejich význam je nutno zhodnotit na základě dlouhodobého prospektivního sledování.
Práce vznikla za podpory výzkumného záměru MZ ČR 00065269705.
doc. MUDr. Lubomír Elbl, CSc.
www.fnbrno.cz
e-mail: lelbl@fnbrno.cz
Doručeno do redakce: 18. 3. 2004
Přijato po recenzi: 28. 4. 2004
Sources
1. Adams KJ, Barnard KL, Swank AM et al. Combined High-Intensity Strength and Aerobic Training in Diverse Phase II Cardiac Rehabilitation Patients. J Cardiopulmonary Rehabil 1999; 19 : 209–215.
2. Cannistra LB, Davidoff R, Picard MH et al. Moderate-High Intensity Exercise Training after Myocardial infarction: Effect on Left Ventricular Remodeling. J Cardiopulmonary Rehabil 1999; 19 : 373–380.
3. deKam PJ, Nicolosi GL, Voors AA et al. Prediction of 6 months left ventricular dilatation after myocardial infarction in relation to cardiac morbidity and mortality. Eur Heart J 2002; 23 : 536–542.
4. DeLagardelle C, Feireisen P, Autier P et al. Strength/endurance training versus endurance training in congestive heart failure. Med Sci Sports Exerc 2002; 34(12): 1868–1872.
5. Dubach P, Myers J, Dziekan G et al. Effect of exercise training on myocardial remodeling in patients with reduced left ventricular function after myocardial infarction: application of magnetic resonance imaging. Circulation 1997; 95 : 2060–2067.
6. Erlebacher JA, Weiss JL, Eaton LW et al. Late effects of acute infarct dilation on heart size: a two dimensional echocardiographic study. Am J Cardiol 1982; 49 : 1120–1126.
7. Gaudron P, Hu K, Schamberger R et al. Effect of endurance training early or late after coronary artery occlusion on left ventricular remodeling, hemodynamics, and survival in rats with chronic transmural myocardial infarction. Circulation 1994; 89 : 402–412.
8. Giannuzzi P, Tavazzi L, Temporelli PL et al. Long–Term Physical Training and Left Ventricular Remodeling After Anterior Myocardial Infarction: Results of the Exercise in Anterior Myocardial Infarction (EAMI) Trial. J Am Coll Cardiol 1993; 22 : 1821–1829.
9. Giannuzzi P, Temporelli PL, Corra U et al. Attenuation of Unfavorable Remodeling by Exercise Training in Postinfarction Patients With Left Ventricular Dysfunction. Results of the Exercise in Left Ventricular Dysfunction (ELVD) Trial. Circulation 1997; 96 : 1790–1797.
10. Goldstein S, Abbas SA, Sabbah H. Ventricular remodeling. Cardiology Clinics 1998; 16(4): 623–631.
11. Chaloupka V, Elbl L. Zátěžová echokardiografie. Praha: Maxdorf Jesenius 1997.
12. Chaloupka V, Vaněk P, Juráň F et al. Nemocniční, posthospitalizační a lázeňská rehabilitace u nemocných s ICHS. Cor Vasa 1998; 40: K243–K251.
13. Chaloupka V, Elbl L, Nehyba S. Silový trénink u nemocných po infarktu myokardu. Vnitř Lék 2000; 46(12): 829–834.
14. Jančík J, Svačinová H, Dobšák P et al. Kombinovaný trénink u nemocných se systolickou dysfunkcí levé komory srdeční. Vnitř Lék 2003; 49(4): 280–284.
15. Jugdutt BI, Michorowski BL, Kappagoda CT et al. Exercise training after Q wave myocardial infarction: Importance of regional ventricular function and topography. J Am Coll Cardiol 1988; 12 : 362–372.
16. Karlsdottir AE, Foster C, Porcari JP et al. Hemodynamic Responses During Aerobic and Resistance Exercise. J Cardiopulmonary Rehabil 2002; 22 : 170–177.
17. Oh BH, Ono S, Gilpin E et al. Altered left ventricular remodeling with betaadrenergic blockade and exercise after coronary reperfusion in rats. Circulation 1993; 87 : 608–616.
18. Oldridge NB, Guyatt GH, Fischer ME et al. Cardiac rehabilitation after myocardial infarction: combined experience of randomised clinical trials. JAMA 1988; 260 : 954–950.
19. Otto MC. The Practice of Clinical Echocardiography. Philadelphia: WB Saunders 1997.
20. Otsuka Y, Takaki H, Okano Y et al. Exercise training without ventricular remodeling in patients with moderate to severe left ventricular dysfunction early after acute myocardial infarction. Int J Cardiol 2003; 87 : 237–244.
21. Parker DN, Hubter GR, Treuth MS et al. Effects of Strength Training on Cardiovascular Responses During a Submaximal Walk and a Weight-Loaded Walking Test in Older Females. J Cardiopulmonary Rehabil 1996; 16 : 56–62.
22. Pollock ML, Franklin BA, Balady GJ et al. Resistance Exercise in Individuals With and Without Cardiovascular Disease. Benefits, Rationale, Safety, and Prescription. An Advisory From the Committee on Exercise, Rehabilitation, and Prevention, Council on Clinical Cardiology, American Heart Association. Circulation 2000; 101 : 828–833.
23. White HD, Norris RM, Brown MA et al. Left ventricular end-systolic volume as the major determinant of survival after recovery from myocardial infarction. Circulation 1987; 76 : 44–5.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2005 Issue 2-
All articles in this issue
- Geriatrics as an inter-disciplinary science on the threshold of the 21st century
- Kmenové buňky: nový příslib v medicíně
- Syndróm z rozpadu nádoru – tumor lysis syndrome
- Adiponektin – nový adipocytární hormon se vztahem k obezitě a inzulinové rezistenci
- Kongenitální adrenální hyperplazie, defekt 17α−hydroxylázy jako vzácná příčina hypertenze a hypokalemie
- Heparinem indukovaná trombocytopenie u pacientky se stenózou kmene levé věnčité tepny
- Léčba chronické infekce virem hepatitidy C pegylovaným interferonem a ribavirinem u pacienta se smíšenou kryoglobulinemií
- Pedální bypass v léčbě ischemie diabetické nohy – střednědobé výsledky
- Pulzní tlak v mladé populaci stanovený 24hodinovým ambulantním monitorováním krevního tlaku a jeho vztah k metabolickým a antropometrickým parametrům
- Hodnocení apoptózy buněk akutní myeloidní leukemie a B−lymfocytární chronické lymfatické leukemie po kultivaci s cytostatiky a její vztah k mnohočetné rezistenci
- Vlastní zkušenosti se vznikem a trváním spontánní remise u dospělých diabetiků typu 1
- Vliv kombinovaného aerobního a silového tréninku na funkci levé komory srdeční u nemocných po akutním infarktu myokardu
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Pulzní tlak v mladé populaci stanovený 24hodinovým ambulantním monitorováním krevního tlaku a jeho vztah k metabolickým a antropometrickým parametrům
- Kongenitální adrenální hyperplazie, defekt 17α−hydroxylázy jako vzácná příčina hypertenze a hypokalemie
- Syndróm z rozpadu nádoru – tumor lysis syndrome
- Vlastní zkušenosti se vznikem a trváním spontánní remise u dospělých diabetiků typu 1
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

