-
Medical journals
- Career
Vztah refluxní choroby jícnu k astmatu bronchiale a horním cestám dýchacím
: Z. Matyášová 1; B. Novotná 2; M. Matulová 3; Jiří Dolina 1; R. Kroupa 1; Z. Láníková 4; V. Znojil 5; A. Hep 1; Petr Dítě 1
: Interní gastroenterologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Petr Dítě, DrSc. 1; Alergologické oddělení Interní gastroenterologické kliniky Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Petr Dítě, DrSc. 2; ORL oddělení FN Brno, pracoviště Bohunice, přednosta prim. MUDr. Aleš Trnka 3; Viameda, s. r. o., ambulance alergologie a klinické imunologie, Brno, ředitelka RNDr. Veronika Vlčková 4; Ústav patologické fyziologie Lékařské fakulty MU, Brno, přednosta prof. MUDr. Anna Vašků, CSc. 5
: Vnitř Lék 2005; 51(12): 1341-1350
: Original Contributions
Refluxní choroba jícnu (RCHJ) představuje jednu z nejčastějších chorob postihujících horní gastrointestinální trakt. Jedná se o jedno z nejrozšířenějších chronických onemocnění zejména v západním světě, jehož incidence i prevalence vykazuje během posledních 30 let stabilní nárůst. RCHJ je onemocnění způsobené patologickým gastroezofageálním refluxem, bez ohledu na přítomnost či nepřítomnost ezofagitidy. Termín RCHJ zahrnuje nejen refluxní chorobu endoskopicky pozitivní, ale i endoskopicky negativní a extraezofageální. Právě mimojícnové projevy refluxní choroby na sebe v posledních letech upoutávají stále častěji pozornost lékařů. Nejčastěji je diskutován vztah patologického gastroezofageálního refluxu (GER) k astmatu bronchiale, chronickému dráždivému kašli, symptomatologii z horních cest dýchacích, nekardiální bolesti na hrudi a mnoha dalším projevům.
Cíl:
Na naší klinice jsme provedli 5letou studii, jejímž cílem bylo monitorovat přítomnost RCHJ u pacientů s bronchiálním astmatem, chronickým dráždivým kašlem a afekcemi v horních cestách dýchacích. Dále jsme zjišťovali, zda lze vlivem 3měsíční antirefluxní terapie zlepšit plicní funkce, subjektivní potíže (kašel) a kontrolu RCHJ u pacientů s astmatem bronchiale; zda lze vlivem této terapie snížit antiastmatickou medikaci; zda lze zlepšit objektivní a subjektivní hodnocení u pacientů s chronickým dráždivým kašlem a u pacientů s postižením horních cest dýchacích. Stran RCHJ jsme hodnotili zlepšení objektivních (pH) a subjektivních (pyróza) parametrů.Metodika:
Celkem jsme vyšetřili 86 pacientů s různou tíží astmatu, 54 pacientů s chronickým dráždivým kašlem a 31 pacientů s afekcemi z oblasti horních cest dýchacích. Pacienti podstoupili vstupní 24hodinovou pH-metrii hodnotící přítomnost patologického GER, vyšetření plicních funkcí a vstupní ORL vyšetření flexibilní laryngoskopií. Při zjištění patologického GER byli pacienti přeléčeni 3měsíční plnou antirefluxní terapií zahrnující prokinetika a inhibitory protonové pumpy (PPI). Po této léčbě byla provedena kontrolní 24hodinová pH-metrie, kontrolní vyšetření plicních funkcí a kontrolní objektivní zhodnocení ORL nálezu. Pacienti měli také zaznamenávat, zda došlo ke změně subjektivních potíží.Výsledky:
Zjistili jsme, že prevalence GER u pacientů s výše uvedenou respirační symptomatikou byla značná. Po 3měsíční antireluxní terapii došlo u pacientů s astmatem bronchiale ke zlepšení jak plicních funkcí (FEV1) (p = 0,0319), tak i ke kontrole RCHJ (p = 0,0009) se statistickou významností. Došlo také ke zlepšení subjektivních potíží (kašle). Antirefluxní terapie podávaná 3 měsíce neumožnila zredukovat dlouhodobou preventivní antiastmatickou terapii, vedenou v souladu s doporučeními GINA, ale umožnila zredukovat tzv. nárazovou medikaci u 50 % pacientů. U pacientů s chronickým dráždivým kašlem došlo rovněž k výrazné redukci subjektivní symptomatologie (kašel se zlepšil u 75,8 %).Závěr:
U pacientů s afekcemi v horních cestách dýchacích došlo k ústupu jak objektivních patologických ORL nálezů, tak k redukci subjektivních potíží, a to v obou případech až u 75 % pacientů. Kontrola GER (objektivní parametry - DeMeesterovo skóre, i subjektivní potíže - pyróza) se zlepšila statisticky významně ve všech hodnocených skupinách pacientů. Závažným zjištěním bylo, že u pacientů s respirační symptomatologií RCHJ byla zjištěna vysoká přítomnost tzv. nočního kyselého průlomu (nocturnal acid breakthrough - NAB): u pacientů s astmatem bronchiale ve 30,3 %, u pacientů s chronickým dráždivým kašlem v 63,6 % a u pacientů s ORL afekcemi ve 45 %.Klíčová slova:
gastroezofageální reflux - astma bronchiale - kašel - horní cesty dýchací - inhibitory protonové pumpy - prokinetika - pH-metrie - noční kyselý průlomÚvod
Refluxní choroba jícnu (RCHJ) je onemocnění způsobené patologickým gastroezofageálním refluxem (GER) (37] bez ohledu na přítomnost či nepřítomnost ezofagitidy [25].
RCHJ je považována za primární poruchu motility. Jedná se o nozologickou jednotku, která v sobě zahrnuje spektrum chorob plynoucích z expozice jícnu kyselému žaludečnímu obsahu [22,33,34,37]. RCHJ zahrnuje endoskopicky pozitivní, endoskopicky negativní a extraezofageální refluxní chorobu [28].
Z hlediska klinického projevu může být GER zcela asymptomatický nebo se může projevit celou řadou příznaků. Nejčastějším příznakem GER je pyróza, dále překyselení v ústech, nadměrné slinění, regurgitace, dysfagie, odynofagie. V novorozeneckém a kojeneckém věku může být GER i život ohrožující, dojde-li k aspiraci většího množství žaludečního obsahu, a tudíž k reflexní zástavě oběhu [48,51].
Obecně dělíme symptomatologii RCHJ na jícnovou a mimojícnovou [36]. Oblast mimojícnová zahrnuje následující projevy: chronický kašel, laryngitidu, laryngotracheitidu, faryngitidu, subglotickou stenózu, chrapot, globus pharyngeus, noduly na hlasivkách, granulomy a symptomatologii z oblasti dýchacích cest, zejména astma bronchiale a chronický kašel [36,48].
Prevalence RCHJ v České republice není známa, avšak pyrózou trpí asi 10-20 % obyvatel [37]. V USA se přítomnost RCHJ odhaduje dokonce až na 1/3 dospělé populace [48].
Astma bronchiale je definováno jako chronické zánětlivé onemocnění dýchacích cest, u kterého je zvýšena reaktivita průdušek na různé stimuly vedoucí k variabilní bronchiální obstrukci, která je reverzibilní buď spontánně nebo vlivem terapie [52]. Definice podle Globální iniciativy pro astma (GINA) definuje astma jako chronické zánětlivé onemocnění dýchacích cest, v němž se účastní mnoho buněk a buněčných působků. Chronický zánět způsobuje průvodní zvýšení průduškové reaktivity, které vede k opakovaným epizodám pískotů při dýchání, dušnosti, tlaku na hrudi a kašle, převážně v noci a časně nad ránem. Tyto stavy jsou obvykle provázeny rozsáhlou, ale proměnlivou bronchiální obstrukcí, která je často reverzibilní, ať již spontánně či po léčbě [5,12]. Prevalence astmatu bronchiale v České republice je 5-10 %, ve světě 2,8-9,4 % [12].
Chronický dráždivý (neproduktivní) kašel je definován jako kašel trvající déle než 3 týdny, přičemž pacient má negativní skiagram hrudníku a je nekuřák [10]. Mnoho lékařů však akceptuje delší hranici, a to 6 až 8 týdnů s kritickým hodnocením dlouhodobějšího nachlazení, chřipky nebo jiné respirační infekce [31]. Podle mnoha autorů je nejčastější příčinou chronického neproduktivního kašle ve více než 90 % syndrom zadní rýmy, bronchiální astma nebo GER [4,11,22,23,45]. Ještě častěji se vyskytují tyto příčiny současně v různých kombinacích. Dalšími častými příčinami je léčba ACE inhibitory a postinfekční etiologie. GER je považován za příčinu chronického kašle u 10-40 % pacientů s chronickým kašlem [22,23,39,41,44]. Chronický kašel může být jediným příznakem jinak asymptomatického GER [14,21,23,24,45].
První zmínky o možné souvislosti RCHJ s postižením v oblasti laryngu zmiňuje v roce 1903 L. A. Coffin [55]. Aktuální prevalence ORL afekcí spojených s RCHJ není přesně známa, ale předpokládá se, že kolem 4-10 % pacientů ošetřených na ORL ambulancích mají symptomy a/nebo nálezy spojené s RCHJ [14,36,42,49,52,55]. Pro tuto skupinu pacientů je charakteristická variabilita jak subjektivních potíží (nejčastěji kašel, chrapot, globus, chronické odkašlávání, dysfonie, hlasová únava, dysfagie), tak ORL objektivních nálezů (chronická laryngitida, faryngitida, karcinom laryngu, kontaktní vředy, granulomy, laryngomalacie, stenóza laryngu, polypoidní degenerace aj) [32].
Jaké jsou patofyziologické vztahy mezi RCHJ a ostatními zmíněnými zdánlivě vzdálenými nozologickými jednotkami, se snaží postulovat několik teorií [2,9,16,20,39,46,48]:
- teorie vagového reflexu
- teorie mikroaspirační
- porušená rovnováha cholinergního a adrenergního systému
- abnormální autonomní regulace bronchiálního tonu
- a celá řada dalších, zahrnující zvýšený rozdíl tlaku mezi hrudníkem a břišní dutinou, alterace bránice při hyperinflaci plic, bronchodilatační léky (teofyliny, p.o. β2-agonisté) [18], výskyt hiátové hernie
- u ORL lézí se uvažuje o možném poškození tonu horního jícnového svěrače, ev. o nutnosti koexistence dalších rizikových faktorů ke vzniku laryngeální léze, jako např. nadměrné namáhání hlasu, chronické odkašlávání, těžký kašel anebo zvracení [1,9,50].
U pacientů se symptomatologií z oblasti dýchacích cest je za zlatý standard v diagnostice přítomnosti RCHJ považována 24hodinová ambulantní pH-metrie, a to buď s jednou [3] nebo dvěma elektrodami [1,7,9,47,53]. Pokud byla prováděna gastroskopie u pacientů s dýchacími potížemi, pak byly zjištěny většinou jen velmi lehké záněty jícnu maximálně I.-II. stupně dle Savary-Millera [55]. Kromě anamnézy a fyzikálního vyšetření je nutno především vyloučit základní patologii v oblasti dýchacích cest (spirometrie, RTG srdce a plic, laryngoskopie a další dle symptomatologie).
Na interní gastroenterologické klinice v Brně-Bohunicích proběhla ve spolupráci s alergologickým oddělením a s oddělením ORL 5letá studie s cílem zjistit: a) jaká je prevalence RCHJ u pacientů s astmatem bronchiale, chronickým kašlem a s afekcemi v horních cestách dýchacích; b) zda lze vlivem 3měsíční antirefluxní terapie zlepšit plicní funkce, symptomy a kontrolu RCHJ u pacientů s astmatem bronchiale; c) zda lze vlivem této terapie snížit antiastmatickou medikaci; d) zda lze zlepšit objektivní a subjektivní hodnocení u pacientů s chronickým dráždivým kašlem a u pacientů s afekcemi v horních cestách dýchacích.
Soubor nemocných
Celkem bylo vyšetřeno 130 pacientů z ambulance alergologie a 31 pacientů odeslaných z ambulance ORL pro nejrůznější afekce z oblasti horních cest dýchacích. Soubor pacientů byl rozdělen do tří skupin:
- a) pacienti s astmatem bronchiale (AB)
- b) pacienti se syndromem dráždivého kašle (kašel)
- c) pacienti s afekcemi v horních cestách dýchacích (ORL).
První skupinu tvořilo 83 pacientů s AB, z nichž u 9 jsme neprokázali přítomnost patologického kyselého GER a 18 pacientů se nedostavilo na další kontrolu. Výsledně jsme hodnotili 56 pacientů s astmatem bronchiale, 16 mužů a 40 žen. Průměrný věk v této skupině byl 43,4 (od 17 do 75 let); podle tíže astmatu jsme pacienty rozdělili do 4 skupin: 4 pacienti měli astma I. stupně (intermitentní), 8 pacientů II. stupně (lehké perzistující), 33 pacientů III. stupně (středně těžké perzistující) a 11 pacientů mělo astma IV. stupně (těžké perzistující).
Druhá skupina pacientů s chronickým dráždivým kašlem čítala původně 54 pacientů, kompletní data byla nakonec dostupná jen pro 33 pacientů, z nichž bylo 13 mužů a 20 žen. Průměrný věk skupiny byl 42,6 (od 19 do 68 let). Všichni pacienti byli odesláni z alergologické ambulance po vyloučení ostatních příčin kašle.
Třetí skupinu tvořilo původně 31 pacientů, nakonec jsme ale mohli hodnotit jen 20 pacientů, z toho 12 mužů a 8 žen. Průměrný věk celé skupiny byl 49,9 (od 27 do 70 let). Pro tuto skupinu byla příznačná značná heterogenita objektivních nálezů (chronická laryngitida, chronická faryngitida, chronická tonzilofaryngitida, v jednom případě laryngospazmus a Reinkeho edém hlasivek) i subjektivních potíží (kašel, chrapot, pocit pálení v krku, globus pharyngeus . V úvodu článku je uváděna řada nálezů, které mohou být spojovány s GER, kdy se reflux na jejich vzniku pravděpodobně podílí , ale nebude jedinou příčinou. Některé afekce uváděné v literatuře (např. stenóza laryngu a průdušnice, granulomy) jsme u pacientů uvedených v souboru nezachytili a jejich možnosti ovlivnění během 3 měsíční léčby GER jsou jistě diskutabilní, léčba je však nedílnou součástí komplexního přístupu k uvedené problematice.
Pacienti ze všech tří skupin byli nekuřáci. Minimální doba trvání obtíží (kašel, chrapot) u pacientů ve všech skupinách byla 3 měsíce, mnohdy však měsíce i roky.
Metodika
Všichni pacienti podstoupili na začátku studie 24hodinovou pH-metrii. U všech byly vyloučeny jiné afekce, které by mohly rovněž způsobovat danou patologii. Pacienti alergologie podstoupili spirometrii (k získání vstupních parametrů FEV1 a FEV1 % a vyloučení astmatu jako etiologického faktoru kašle u pacientů se syndromem dráždivého kašle). Byly provedeny bronchodilatační testy k diagnostice astmatu, testy k vyloučení alergie jako vyvolávajícího faktoru kašle a všichni pacienti měli proveden RTG plic. Na ORL ambulanci byla provedena vyšetření k vyloučení jiné příčiny pacientových obtíží než RCHJ (nepřímá laryngoskopie flexibilní nebo pevnou optikou, kultivace z krku a nosu a RTG paranazálních dutin).
Do dalšího sledování byli zařazeni pouze pacienti, u kterých byla zjištěna přítomnost patologického kyselého GER. Byli léčeni omeprazolem 20 mg 2krát denně a cisapridem 10 mg 4krát denně (v době, kdy studie začínala, byl cisaprid běžně používán, později byli před jeho nasazením pacienti řádně vyšetření na kardiologii a EKG - QT interval kontrolován při každé návštěvě pacienta, k vyloučení nežádoucích účinků). Kardiologické vyšetření zahrnovalo podrobnou anamnézu, fyzikální vyšetření, RTG srdce a plic a hodnocení EKG, zejména QT intervalu. Později byl místo cisapridu u některých pacientů používán itoprid 3krát 50 mg denně. Dávkování prokinetik nebylo voleno s ohledem ke srovnatelnému ekvivalentu, ale s cílem podat maximální účinnou a doporučovanou dávku prokinetik. U pacientů s nálezem nočního kyselého průlomu - nocturnal acid breakthrough (NAB) byla na noc přidána k léčbě PPI malá dávka H2-blokátoru (např. Famosan 40 mg). Přítomnost NAB stanovujeme při 24hodinové pH-metrii a je definován jako pokles pH v žaludku pod 4 během nočních hodin přes maximální terapii PPI 2krát denně, a to na delší dobu než 1 hodinu.
Po třech měsících léčby byla provedena kontrolní pH-metrie, kontrolní vyšetření na ambulanci alergologie (s provedením kontrolní spirometrie u astmatiků) a/nebo ORL a kontrola objektivního nálezu po terapii. U všech pacientů jsme zjišťovali subjektivní potíže, jak GER charakteru (pyróza), tak respirační (kašel), ev. dušnost. U pacientů ORL přítomnost specifických ORL potíží (chrapot, kašel, pocit pálení v krku) v korelaci s objektivním nálezem. U astmatiků byla zjišťována změna antiastmatické medikace a spotřeba úlevové léčby, podle doporučení GINA. Všichni pacienti zapisovali subjektivní potíže do dotazníků. Pacienti měli hodnotit intenzitu obtíží, to znamená přítomnost kašle (jeho častosti, záchvatovosti, noční obtíže, probouzení v důsledku kašle, denní obtíže, pokašlávání, ústup příznaků), přítomnosti pískotů na hrudi, dušnosti, pocitu tíže na hrudníku, nutnosti omezení běžné denní nebo fyzické aktivity. Pacienti s astmatem si vedli denní záznamy o měření vrcholové výdechové rychlosti (PEF) a spotřebě úlevových antiastmatických léků.
Při hodnocení nálezů ORL byly hodnoceny změny pozorované při běžném ORL vyšetření včetně laryngoskopie flexibilní či pevnou optikou. Kvantifikovat změny v uvedených oblastech před a po léčbě je obtížné, proto byly hodnoceny lokální nálezy jednou vyšetřující osobou a záznamy laryngoskopie přenášené do databáze počítačového archivu. Byly hodnoceny změny překrvení sliznic mezofaryngu, hrtanu, zejména sliznice interarytenoidní oblasti, překrvení a otok hlasivek, tvar a velikost polypoidních lézí. Jedná se jistě o hodnocení do jisté míry subjektivní, avšak hodnocením jednotlivých obrazových záznamů jsme se pokusili dosáhnout maximální přesnosti. Současně byly hodnoceny subjektivní potíže nemocných, zejména ovlivnění dysfonie, hlasové únavnosti a pocitů nepohody v krku označované jako „globus pharyngeus“. Všichni pacienti souboru již byli v předchozím období léčeni na ORL ambulanci konzervativně včetně hlasové terapie bez možnosti dalšího zlepšení stavu.
K pH-metrickému vyšetření byl používán přístroj MK III nebo MK IV Microdigitrapper firmy Medtronic-Synectics Medical. Vlastní měření pak zajišťuje sonda (elektroda) s jedním nebo dvěma senzory vzdálenými od sebe 15 cm. Na našem pracovišti jsme používali elektrody antimonové. Vyhodnocení bylo provedeno softwarem stejného výrobce.
24hodinové pH-metrické vyšetření probíhalo v ambulantních podmínkách, přičemž pacienti vysadili minimálně 3 dny před vyšetřením léky ovlivňující pH: prokinetika, antacida, H2-blokátory a inhibitory protonové pumpy. Nakalibrovaná sonda byla zaváděna intranazálně, po předchozím poučení pacienta s jeho souhlasem. Jednosenzorovou elektrodu jsme umístili 5 cm nad dolní jícnový svěrač, duální elektroda měla jeden senzor umístěn v žaludku a druhý 5 cm nad dolním jícnovým svěračem. Sonda byla propojena s pH-metrem. Analýza dat je prováděna pomocí příslušného hodnotícího PC softwaru po zadání časových hodnot korelujících s časy jídla, dobou strávenou ve vodorovné poloze a potíží pacienta. K hodnocení 24hodinové pH-metrie bylo použito multikompozitní tzv. DeMeesterovo-Johnsonovo skóre, kdy analýzou parametrů byla stanovena hranice normy 14,72 (vyšší hodnoty jsou patologické). Dále jsme hodnotili tzv. refluxní index a tzv. symptomový index. Refluxní index (též nazývaný fraction time) je podíl doby, kdy je patologické pH v jícnu v procentech. Na našem pracovišti používáme normu 3,4 %, hodnoty vyšší jsou patologické. Symptomový index je definován jako poměr počtu symptomů udaných pacientem během měření k celkově objektivně zjištěným refluxním epizodám v zadaném čase krát 100 % (pozitivní výsledek, tedy přítomnost patologického GER, je 50 % a více).
Spirometrie byla hodnocena pomocí pneumotachografu (Jaeger, Německo). Byla hodnocena křivka průtok/objem se základními plicními objemy včetně dynamických ukazatelů, měřených během usilovného výdechu. Měření byla prováděna jen za standardních podmínek, tzn. jen u pacientů bez akutních projevů zánětu dýchacích cest a při stabilizovaném astmatu.
Statistické vyhodnocení
Ke statistickému hodnocení rozdílů před a po terapii byly užity neparametrické statistické testy: Wilcoxonův párový test a Mann-Whitneyův U test, vzhledem k tomu, že se nejednalo o soubory s normálním rozložením dat dle Gaussovy křivky. K provedení statistických výpočtů byl použit software CSS STATISTICA (Statsoft, Tulsa, OK, USA).
Výsledky
Pacienti s AB
3měsíční antirefluxní terapie zlepšila kontrolu astmatu. Plicní funkce charakterizované parametrem FEV1 se zlepšily u 34 (60,7 %) pacientů, se statistickou významností (p = 0,0319) v celkovém počtu pacientů, významněji u žen (p = 0,003) a bez prokazatelných rozdílů u mužů (p = 0,6) podle Wilcoxonova párového testu. Větší významnost u žen si vysvětlujeme jednak tím, že počet žen ve skupině byl větší než počet mužů, a dále zvažujeme možnost vazby úspěšnosti léčby na pohlaví. Zlepšení plicních funkcí bylo spíše vázáno na pohlaví než na tíži astmatu, kde jsme hodnotili 3 skupiny - 4. stupeň (p = 0,35), 3. stupeň (p = 0,25) a pro malý počet pacientů v ostatních dvou skupinách dohromady 2. a 1. stupeň astmatu (p = 0,16) (graf 1).
1. Vliv antirefluxní terapie na plicní funkce FEV1 podle tíže astmatu. 
Legenda: Osa x - ukazuje vliv GERD terapie na plicní funkce ve smyslu zlepšení, zhoršení nebo stejného stavu v jednotlivých skupinách astmatiků: I - I. stupeň AB, II - II. stupeň AB, III - III. stupeň AB a IV - IV. stupeň AB. Osa y odpovídá počtu pacientů dle tíže astmatu v absolutních číslech Antirefluxní terapie vedla ke zlepšení kontroly RCHJ, u 42 (74 %) pacientů došlo ke zlepšení nálezu (dle DeMeesterova skóre) na hladině statistické významnosti (p = 0,0009) a symptomy RCHJ (pyróza) se zlepšily u 40 (71 %) pacientů, také statisticky signifikantně (p < 0,001) podle Wilcoxonova testu a Mann-Whitney U testu (tab. 1). S DeMeesterovým skóre korelovaly v podstatě i hodnoty refluxního indexu, kdy ke zlepšení došlo u 41 pacientů (73 %) a ke zhoršení došlo u 15 pacientů (27 %).
1. Vliv antirefluxní terapie na subjektivní hodnocení pacientů s AB (kašel a pyróza). 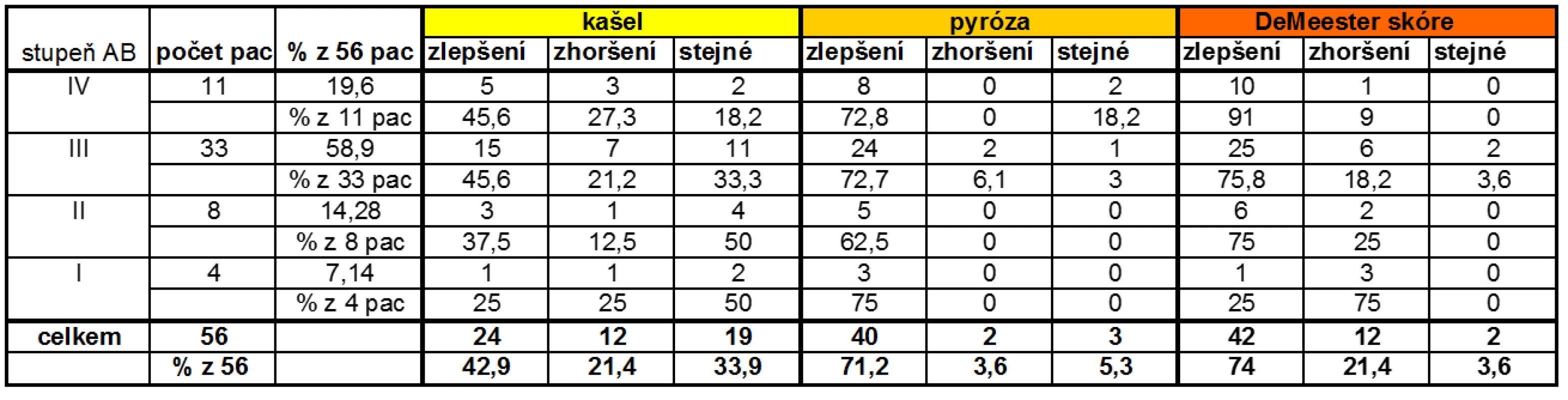
Pokud bychom hodnotili zlepšení DeMeesterova skóre zvlášť u mužů a zvlášť u žen, pak na rozdíl od plicních funkcí došlo k významnějšímu zlepšení pH u mužů (p = 0,01) než u žen (p = 0,1). Z hlediska tíže astmatu došlo k největšímu zlepšení hodnot DeMeesterova skóre u pacientů se 4. stupněm astmatu (p = 0,02) na rozdíl od skupiny pacientů s 1.-2. stupněm astmatu (p = 0,38). Tento výsledek odráží skutečnost, že ve skupině pacientů s 1. stupněm astmatu se DeMeesterovo skóre u 3 pacientů ze 4 zhoršilo.
NAB byl přítomen u 30,3 % pacientů, a proto je třeba aktivně pátrat po jeho přítomnosti u pacientů s respiračními potížemi, a to zejména u pacientů s nočním kašlem.
Pouze 6 (10,7 %) pacientů mohlo snížit dlouhodobou preventivní antiastmatickou léčbu, ale 12 (21,42 %) pacientů muselo léčbu navýšit. Používání tzv. záchranné medikace bylo častější nebo zůstalo beze změny u 29 (50 %) pacientů, a stejný počet pacientů - 28 (50 %) mohl snížit užívání záchranné medikace.
Zdá se, že tíže astmatu s odpovídající léčbou nemá vliv na ovlivnění kontroly astmatu antirefluxní terapií.
Jedním z nejdůležitějších závěrů je, že přesto, že došlo ke zlepšení astmatických symptomů (kašle) jen asi u 50 % pacientů, nemuseli ostatní pacienti zbytečně navyšovat antiastmatickou medikaci.
Pacienti se syndromem dráždivého kašle
Jedná se o skupinu pacientů, u kterých nebylo prokázáno jako příčina kašle astma bronchiale, CHOPN a postnasal drip. V této skupině bylo 33 pacientů; 13 mužů a 20 žen. Ve skupině mužů se průměrné DeMeesterovo skóre a refluxního indexu objektivně zlepšilo o 21,3 % (p = 0,3). Ze 13 mužů jich 11 (84,7 %) trpělo pyrózou, kašel byl přítomen u všech pacientů. Přítomnost nočního kyselého průlomu (NAB) jsme zjistili u 8 mužů (61,6 %). V této skupině došlo ke zlepšení DeMeesterova skóre u 8 mužů (61,6 %) a ke zhoršení u 5 mužů (38,5 %). Refluxní index se zlepšil u 9 mužů (69,2 %) a zhoršil u 4 mužů (30,8 %).
Stran subjektivních potíží pyrózou vůbec netrpěli 2 muži (15,4 % , po terapii byl beze změn 1 muž (7,7 %) a zlepšení pyrózy udávalo 10 mužů (77 %). Kašel se zlepšil u 9 mužů (69,3 %), ke zhoršení došlo v jednom případě (7,7 %) a beze změn byli 3 muži (23,1 %).
O něco lepší výsledky měly ženy, kterých bylo 20, a jejich průměrné DeMeesterovo skóre se zlepšilo o 56,8 % (p = 0,0002). Zajímavé přitom je, že objektivní nález ve smyslu hodnoceného vstupního DeMeesterova skóre byl u žen horší a průměrné zlepšení výraznější. Hodnoty refluxního indexu se rovněž zlepšily v korelaci s hodnotami DeMeesterova skóre (p = 0,0001). Pyrózou trpělo celkem 10 žen (50 %), kašlem trpěly všechny ženy. Přítomnost NAB jsme zjistili u 13 žen (65 %), podobně jako u mužů. Objektivně došlo ke zlepšení DeMeesterova skóre celkem u 18 žen (90 %), beze změny bylo DeMeesterovo skóre u 1 ženy (5 %) a ke zhoršení došlo rovněž u 1 ženy (5 %). Refluxní index se zlepšil celkem u 19 žen (95 %) a zhoršil u 1 ženy (5 %).
Pyróza nebyla vůbec přítomna u 10 žen (50 %), u 9 (45 %) žen došlo ke zlepšení, u 1 ženy (5 %) byly potíže stejné a ke zhoršení nedošlo u nikoho. Ženy trpěly pyrózou jen málo, na rozdíl od mužů. Kašel, který byl před zahájením antirefluxní terapie přítomen u všech žen, se zlepšil u 16 žen (80 %), u 3 (15 %) byly potíže beze změn a u 1 došlo ke zhoršení (5 %).
V celkovém hodnocení tedy bylo hodnoceno 33 pacientů, z nichž u 21 byla přítomna pyróza (63,6 %) a ve stejném počtu tedy 21 (63,6 %) byl přítomen noční průlom NAB.
Objektivně došlo ke zlepšení dle DeMeesterova skóre celkem u 26 pacientů, tedy v 78,8 % (p = 0,0008), beze změn bylo hodnocení před a po terapii u 1 pacienta (3,03 %) a ke zhoršení refluxu došlo u 6 pacientů (18,2 %). Refluxní index se celkově zlepšil u 28 pacientů (84,8 % ) s p = 0,002 a u 5 pacientů (15,2 %) došlo k jeho zhoršení.
Kašel, který byl na počátku přítomen u všech vyšetřených osob, se po třech měsících antirefluxní terapie zlepšil u 25 pacientů (75,8 %), beze změn byl u 6 pacientů (18,2 %) a zhoršil se u 2 pacientů (6,1 %) (tab. 2). Vzhledem k tomu, že v souboru pacientů měli všichni pacienti kašel, nelze se vyjádřit ke statistické významnosti změny kašle, a tuto změnu lze vyjádřit pouze procentuálně. Pyróza byla přítomna u 21 pacientů (63,6 %), nebyla přítomna u 12 (15,4 % , subjektivně se zlepšila u 19 (57,6 %) pacientů a potíže zůstaly stejné u 2 pacientů (6,1 %), ke zhoršení pyrózy na antirefluxní terapii nedošlo (tab. 2). Opět zde můžeme pozorovat rozdíly mezi muži a ženami, kdy ženy trpěly pyrózou podstatně méně než muži. Rozdíly ve výsledcích mezi muži a ženami si opět vysvětlujeme jako jevy vázané na pohlaví, přičemž roli může hrát i poměr počtu žen vůči mužům a fakt, že se jedná o soubor s malým počtem pacientů.
2. Subjektivní hodnocení kašle a GER po terapii u pacientů s kašlem. 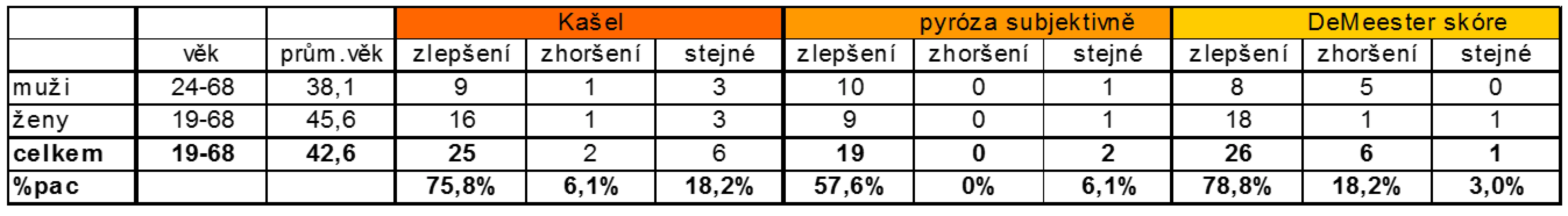
Pacienti s afekcemi v horních cestách dýchacích (ORL)
V této skupině bylo 20 pacientů; 12 mužů a 8 žen.
Ve skupině mužů se DeMeesterova skóre zlepšilo v průměru o 63,9 % (p = 0,009). U 11 pacientů (91,3 %) došlo ke zlepšení a u jednoho pacienta (8,3 %) ke zhoršení DeMeesterova skóre. Hodnoty refluxního indexu se zlepšily u 11 mužů (91,3 %) s p = 0,01 a zhoršily u 1 muže (8,3 %). Dále jsme hodnotili změnu objektivního nálezu při ORL vyšetření a zjistili jsme, že u 8 pacientů (66,4 %) došlo ke zlepšení, u 2 pacientů (16,6 %) byl nález stejný a u 2 pacientů (16,6 %) byl nález zhoršen. Subjektivně si pacienti nejvíce stěžovali na chrapot, pokašlávání, dysfonii nebo zahlenění, u některých bylo více stesků najednou. Po antirefluxní terapii se cítilo 8 pacientů (66,4 %) lépe, 4 pacienti (33,2 %) stejně a nezhoršil se nikdo. Z této skupiny 12 mužů mělo celkem 6 pacientů NAB (49,8 %). Před zahájením antirefluxní terapie trpěli 4 pacienti (33,2 %) pyrózou, po terapii pyrózu neudával nikdo.
Ve skupině žen došlo ke zlepšení DeMeesterova skóre v průměru o 62,3 % (p = 0,01). U 7 pacientek (87,5 %) došlo ke zlepšení, u 1 pacientky (12,5 %) bylo DeMeesterovo skóre i po terapii stejné a ke zhoršení nedošlo u nikoho. Ke zlepšení refluxního indexu došlo u všech pacientek, tedy ve 100 % (p = 0,01). Objektivní ORL nález se zlepšil u 7 pacientek (87,5 %), zůstal identický u 1 pacientky (12,5 %) a nezhoršil se u nikoho. Obdobně dopadlo i subjektivní hodnocení ORL potíží. Pyrózou trpěly před zahájením antirefluxní terapie celkem 3 pacientky (37,5 %), po terapii žádná a NAB bylo prokázáno rovněž u 3 pacientek (37,5 %).
V hodnocení celého souboru 20 pacientů došlo u 18 (90 %) ke zlepšení DeMeesterova skóre, stejné byly hodnoty v 1 případě (5 %) a ke zhoršení došlo rovněž u 1 pacienta (5 %). Došlo ke statisticky významnému zlepšení DeMeesterova skóre (p = 0,0003) po antirefluxní terapii. Zlepšení refluxního indexu koreluje se zlepšením DeMeesterova skóre s velkou statistickou významností v celém souboru pacientů (p = 0,0003). Objektivní ORL nález se po terapii zlepšil u 15 pacientů (75 %), zůstal beze změn celkem u 3 pacientů (15 %) a zhoršil se u 2 pacientů (10 %). Vzhledem k tomu, že v souboru pacientů měli všichni pacienti ORL potíže, nelze se vyjádřit ke statistické významnosti ORL změn a tyto změny lze vyjádřit pouze procentuálně. Subjektivně hodnotilo 15 pacientů (75 %) své potíže jako lepší, 5 pacientů (25 %) jako stejné a nikdo neudával zhoršení potíží. Pyróza byla udávána před terapií celkem 7 pacienty (35 %) a po terapii již nikým (tab. 3). NAB bylo zjištěno celkem u 9 pacientů (45 %).
3. Korelace subjektivních a objektivních ORL nálezů s pH (změnou DeMeesterova skóre). 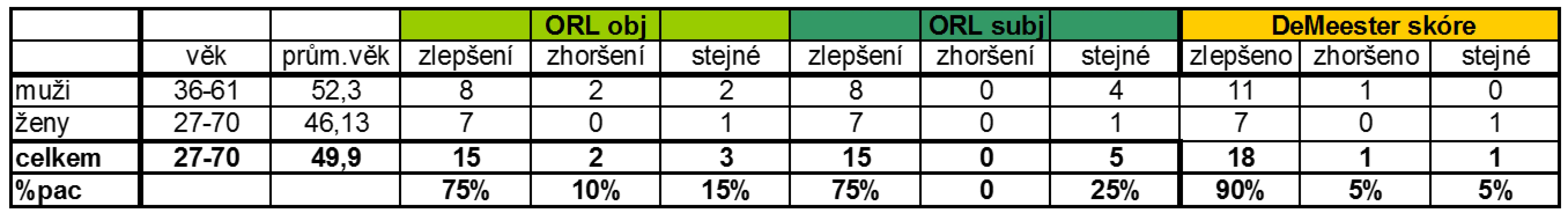
Diskuse
Problematika mimojícnových (respiračních) projevů RCHJ je v literatuře opředena mnoha nejasnostmi a kontroverzemi, které začínají již u epidemiologie a pokračují dále přes patogenezi, diagnostiku až k samotné léčbě.
Dosud nebyly provedeny žádné větší epidemiologické studie, které by ukázaly aktuální incidenci refluxem indukovaných mimojícnových afekcí, a to jak u pacientů s ezofagitidou, tak v celkové populaci. Avšak dle klinické zkušenosti je pravděpodobně prevalence tohoto typu komplikací relativně nízká ve srovnání s prevalencí jícnových afekcí. Na druhé straně může častá absence klasických jícnových příznaků vést k tomu, že je prevalence RCHJ v této skupině pacientů spíše podhodnocena.
Nejasnosti se objevují již v samotné patogenezi RCHJ indukovaných mimojícnových potíží. Nejčastěji se v literatuře objevují dvě teorie, které popisují vztah mezi RCHJ a respirační symptomatologií. Je to jednak teorie vagem mediovaného reflexního oblouku s následným vznikem bronchokonstrikce [14,15,30,38,39,48,56] a jednak teorie mikroaspirační, kdy se předpokládá, že během refluxních epizod dochází k mikroaspiraci žaludečního obsahu [8,14,15,30,38,46,48].
Někteří autoři ukazují na predominantní vznik mimojícnových komplikací během nočních refluxních epizod, jiní autoři uvádějí, že ke vzniku mimojícnových - zejména ORL afekcí dochází spíše ve vzpřímené poloze [7,24,33,40].
V naší studii jsme prokázali, že prevalence nočního kyselého refluxu (NAB) v celém souboru pacientů, tedy jak u pacientů s AB, tak u pacientů s chronickým dráždivým kašlem a ORL afekcemi, byla vysoká. U astmatiků byla přítomnost NAB při zavedené antirefluxní terapii 30,3 %, u pacientů s chronickým dráždivým kašlem dokonce 63,6 % a u pacientů s ORL afekcemi byl NAB přítomen u 45 % pacientů. Naše data spíše podporují významnost nočního refluxu u pacientů s respiračními komplikacemi RCHJ.
Diagnostika mimojícnových komplikací RCHJ je další kontroverzí. Existuje jednoznačný konsenzus, že je třeba v první linii vyloučit všechny možné jiné etiologie pacientových potíží, než je potíž dána do souvislosti s RCHJ, zejména je třeba pamatovat na chronické záněty a diagnózy onkologické. Při podezření na RCHJ doporučuje mnoho autorů jako metodu první volby provedení terapeutického testu [4,11]. Dle jiných autorů je zlatým standardem v diagnostice 24hodinová ambulantní pH-metrie [33,41].
Na našem pracovišti se přikláníme nejdříve k provedení 24hodinové pH-metrie před provedením terapeutického pokusu. Důvodem je zejména snaha o přesnou diagnostiku pacientových obtíží před nasazením léčby, navíc pacienti s AB již často užívají řadu léků. Pacienti s chronickým kašlem a ORL afekcemi již vyzkoušeli celou řadu jiných podpůrných léků, které jim byly nabídnuty jako léčba první volby, což může zhoršovat jejich komplianci a v neposlední řadě je důvodem i cena léčby verzus cena jednorázového vyšetření 24hodinovou pH-metrií. Terapeutický pokus používáme, pouze pokud pacient vyšetření 24hodinovou pH-metrií netoleruje nebo pokud přetrvávají jeho potíže i přes negativní výsledek vyšetření.
V léčbě mimojícnových afekcí je doporučen omeprazol v dávce 2krát 20 mg. Léčba by měla pokračovat alespoň 3 měsíce, a pokud je to možné, tak i 6 měsíců. Tato léčba je doporučována jak u astmatiků, tak u pacientů s chronickým kašlem nejasné etiologie a rovněž u pacientů s ORL afekcemi. Tato data korelují s výsledky naší studie, neboť často došlo k subjektivnímu zlepšení u pacientů (zejména s ORL afekcemi) až po delší době užívání antirefluxní medikace, řádově několik týdnů až 2-3 měsíců [1,3,6,9,14,17,19,20,33,54,55].
Kratší nebo nedostatečně efektivní terapie vede často k navyšování specifické léčby, např. u astmatiků (podle GINA doporučení), namísto vytrvání v dlouhodobém podávání PPI, které by umožnilo nezatěžovat pacienta vysokými dávkami jiných léků s malým účinkem, vzhledem k tomu, že nebyl odstraněn hlavní spouštěcí faktor. To jsme potvrdili i v naší studii, kdy ke zlepšení symptomů astmatu (kašle) došlo jen u 50 % astmatiků, ale ostatní nemuseli díky zavedení antirefluxní medikace zvyšovat dávky úlevové antiastmatické léčby.
U všech sledovaných skupin pacientů došlo k výraznějšímu zlepšení v subjektivním hodnocení (kašle, chrapotu) než při srovnání objektivních parametrů, které jsou v hodnocení směrodatnější. Tyto rozdíly budou spíše na vrub použití nových léčebných postupů (zavedení antirefluxní medikace) v terapii pacienta, s jistým stupněm placebo efektu na respirační potíže u pacientů s multifaktoriálním onemocněním, jakým astma beze sporu je. Z etických důvodů jsme však kontrolní skupinu pacientů a podávání placeba nezaváděli, což srovnání komplikuje. Na druhé straně je třeba říci, že při dalším sledování pacientů docházelo při vysazení léčby ke zhoršení pyrózy a kašle a podávání antirefluxní medikace je tedy zcela namístě, přesto, že ev. zlepšení plicních funkcí nebylo přítomné u všech pacientů.
Rozdíly výsledků mezi muži a ženami byly jednak dány rozdílnými počty mužů a žen, kdy v hodnocených skupinách byly ženy v mnohdy i významné početní převaze, jednak tím, že existují dnes již známé geneticky vázané rozdíly v projevech nemoci, ale např. i v reakcích na léčbu mezi oběma pohlavími [29].
Statistické srovnávání efektu antirefluxní terapie na možnost snížení či vysazení antiastmatické medikace (preventivní i záchranné) nebylo možné, vzhledem k velké diverzitě zavedené medikace, kdy detailní statistické rozlišení mezi velkým počtem skupin o malé četnosti je v podstatě nemožné a citlivost metod velmi nízká.
V důsledku značné kontroverznosti předkládaného problému bude v budoucnu potřeba iniciovat ještě více studií i placebem kontrolovaných, s lepším technickým vybavením pro měření kvantity kyselého refluxu (např. měření jícnové impedance, použití BRAVO kapsle nebo vícekanálové pH-metrické sondy), abychom mohli jednoznačně odpovědět na otázku, u kterého z pacientů s mimojícnovými symptomy je RCHJ hlavním etiologickým faktorem. Lékařská veřejnost by měla být uvědomována o možnosti spojitosti mezi RCHJ a mimojícnovými komplikacemi, aby tito pacienti mohli být včas odhaleni a efektivně léčeni [20].
Závěr
Prevalence RCHJ u pacientů s astmatem bronchiale a syndromem dráždivého kašle je vysoká a v našem souboru se pohybovala kolem 84,7 % a u pacientů s onemocněními z oblasti horních cest dýchacích byla prevalence v našem souboru 79,4%.
Účinná léčba RCHJ:
- vede ke zlepšení plicních funkcí se statistickou významností a vede statisticky významně ke kontrole RCHJ (pyróza i objektivní zlepšení DeMeesterova skóre),
- vede k redukci subjektivních potíží pacientů (kašle, chrapotu) přestože toto zlepšení vždy nemusí korelovat u všech pacientů se zlepšením spirometrického nálezu,
- neumožňuje zredukovat antiastmatickou preventivní dlouhodobou léčbu, ale u 50 % pacientů bylo možno snížit tzv. nárazovou/úlevovou medikaci,
- vede ke zlepšení ORL objektivního nálezu i subjektivní symptomatologie z oblasti horních cest dýchacích.
Je nezbytně nutné pomýšlet na možnou přítomnost NAB u pacientů s respiračními symptomy (nejen u astmatiků, ale i u pacientů s chronickým dráždivým kašlem a ORL afekcemi), zejména u těch pacientů, kteří mají noční kašel, neboť přítomnost NAB u pacientů s respiračními onemocněními je vysoká (v naší práci byl zjištěn NAB u 30,3 % astmatiků, 63,6 % pacientů s chronickým kašlem a 45 % pacientů s ORL afekcemi).
Je potřeba aktivněji pátrat po přítomnosti RCHJ u pacientů nejen s bronchiálním astmatem, ale také s chronickým dráždivým kašlem a afekcemi ORL, a to zejména u pacientů s kašlem, špatnou odpovědí na specifickou antiastmatickou léčbu (podle doporučení GINA), manifestací určitých vedoucích symptomů jako např. noční kašel, pacientů s těžkými a jinak nevysvětlitelnými exacerbacemi symptomů. Na možnou přítomnost GER můžeme usuzovat i v případě tzv. „silent - tichého“ GER, kdy zcela chybí příznaky GER z oblasti GIT ev. i respirační a pacient má patologický nález na pH-metrii.
V diagnostice GER je, po vyloučení ostatních možných etiologických faktorů, jak u klasické tak i u mimojícnové symptomatologie, zatím nejlepší metodou 24hodinová pH-metrie s jedním nebo lépe dvěma senzory. Pokud je pH-metrie negativní a pacient má dále přetrvávající potíže, lze po přezkoumání ostatních možných příčin provést terapeutický test.
V léčbě je důležité zachovat minimálně 3měsíční intenzivní antirefluxní terapii. Doporučujeme léčbu inhibitory protonové pumpy ve dvou denních dávkách (např.omeprazol 2krát 20 mg denně) a prokinetika v plné dávce (např. itoprid 3krát 50 mg). Pokud po 3měsíční léčbě potíže neustoupily, doporučujeme provedení kontrolní 24hodinové pH-metrie na terapii ke zjištění kontroly RCHJ. Je-li přítomen noční reflux (NAB), je možné na noc zvážit přidání H2-blokátorů k stávající léčbě PPI, alespoň na další 2 měsíce. Pokud se po krátkodobém vysazení antisekretorických léků, např. před prováděnou kontrolní 24hodinovou pH-metrií, pacient cítí dobře a k recidivě symptomů nedochází, je vhodné postupné snižování léčby (tzv. step-down princip léčby), kdy podávání maximálních dávek PPI postupně snižujeme (např. z denního dávkování omeprazolu 2krát 20 mg nejdříve na omeprazol 1krát 20 mg denně a postupně na 20 mg omeprazolu 2-3krát týdně, nebo pacient užívá 20 mg omeprazolu obden a postupně dospěje k tzv. terapii „on demand“, tedy jen při exacerbaci potíží).
Chirurgická intervence může být individuálně zvážena v případě recidivy patologického refluxu po vysazení antisekretorik. Nejlepších výsledků je při chirurgické intervenci dosahováno u pacientů s předcházející dobrou odpovědí na antirefluxní medikaci.
V problematice RCHJ a mimojícnových komplikací existuje sice celá řada nejasností, ale vzhledem k dobré odezvě těchto pacientů na antirefluxní medikaci (i když ne u 100 % pacientů) a i když není vždy dosaženo zlepšení všech objektivních parametrů, je potřeba po této diagnóze v souvislostech s mimojícnovými potížemi aktivně pátrat a v diferenciální diagnostice dané léze o možnosti RCHJ jako hlavního etiologického momentu uvažovat.
MUDr. Matyášová Zuzana, Ph.D.
www.fnbrno.cz
e-mail: danazuzka@quick.cz
Doručeno do redakce: 14. 4. 2005
Přijato po recenzi: 23. 6. 2005
Sources
1. Al-Sabbagh G, Wo JM. Supraesophageal Manifestations of Gastroesophageal reflux Disease. Seminars in Gastrointestinal disease 1999; 10 : 113-119.
2. Bauman NM, Sandler AD, Schmidt C et al. Reflex laryngospasm induced by stimulation of distal esophageal afferents. Laryngoscope 1994; 104 : 209-214.
3. Beauvillain de Montreuil C. Pharyngitis, laryngitis in the adult and gastroesophageal reflux. In: Giuli R, Galmiche JP, Jamieson Glynn G et al (Eds). O.E.S.O. - The esophagogastric junction. Paris: John Libbey Eurotext 1998 : 583-584.
4. Benini L, Ferrari M, Sembenini C et al. Cough threshold in reflux oesophagitis: influence of acid and of laryngeal and oesophageal damage. Gut 2000; 46 : 762-767.
5. Bohadana AB, Hannhart B, Teculescu DB. Nocturnal Worsening of asthma and sleep-disordered breathing. Journal of Asthma 2002; 39 : 85-100.
6. Borkowski G, Sommer P, Stark T et al. Recurrent respiratory papillomatosis associated with gastroesophageal reflux disease in children. Eur Arch Otorhinolaryngol 1999; 256 : 370-372.
7. Bove M, Ruth M, Cange L et al. 24-H Pharyngeal pH Monitoring in Healthy Volunteers: A Normative Study. Scand J Gastroenterol 2000; 3 : 234-241.
8. Bretza J, Novey HS. GE reflux and asthma. West J Med 1979; 131 : 320.
9. Close LG. Laryngopharyngeal manifestations of reflux: diagnosis and therapy. European Journal of Gastroenterology and Hepatology 2002; 14(Suppl): S23-S27.
10. Čáp P, Vondra V. Definice a výskyt kašle. In: Čáp P, Vondra V. Kašel: Obranný mechanismus, příznak, terapie. Praha: Galerie Vltavín 2000 : 7.
11. Čáp P, Vondra V. Chronický kašel (etiologie, diagnostika, terapie). In: Čáp P, Vondra V. Kašel: Obranný mechanismus, příznak, terapie. Praha: Galerie Vltavín 2000 : 11-21.
12. Špičák V, Kašák V, Pohunek P. Definice. In: Špičák V, Kašák V, Pohunek P. Globální strategie péče o astma a jeho prevenci. Praha: Česká iniciativa pro astma, Jalna 2003 : 1-28.
13. Špičák V, Kašák V, Pohunek P. Diagnóza a klasifikace. In: Špičák V, Kašák V, Pohunek P. Globální strategie péče o astma a jeho prevenci. Praha: Česká iniciativa pro astma, Jalna 2003 : 73-86.
14. Fennerty MB. Extraesopgaheal Gastroesophageal Reflux Disease. Presentations and Approach to Treatment. Gastroesophageal Reflux Disease. Gastroenterology Clinics of North America 1999; 28 : 861-873.
15. Gislason T, Janson Ch, Vermeire P et al. Respiratory Symptoms and Nocturnal Gastroesophageal Reflux. A Population-Based Study of Young Adults in Three European Countries. Chest 2002; 121 : 158-163.
16. Halstead LA. Role of gastroesophageal reflux in pediatric upper airway disorders. Otolaryngology-Head and Neck Surgery 1999; 120 : 208-214.
17. Hanson DG, Jiang JJ. Diagnosis and Management of Chronic Laryngitis Associated with Reflux. Am J Med 2000;108 : 112S-119S.
18. Harding SM. Acid reflux and Asthma. Current opinion in pulmonary Medicine 2003; 9 : 42-45.
19. Havas TE, Priestley J, Lowinger DSG A Management Strategy for Vocal Process Granulomas. Laryngoscope 1999; 109 : 301 - 305.
20. Hogan WJ, Shaker R. Supraesophageal Complications of Gastroesophageal Reflux. Disease-a-Month 2000; 46 : 195-232.
21. Ing AJ, Ngu MC, Breslin ABX. Chronic persistent cough and gastro-oesophageal reflux. Thorax 1991; 46 : 479-483.
22. Irwin RS, Corrao WM, Pratter MR. Chronic persistent cough in adult: the spectrum and frequency of causes and successful outcome of specific therapy. Am Rev Respir Dis 1981; 123 : 413-417.
23. Irwin RS, Curley FJ, French CL. Chronic cough: the spectrum and frequency of causes, key components of the diagnostic evaluation, and outcome of specific therapy. Am Rev Respir Dis 1990; 141 : 640-647.
24. Irwin RS, French CL, Curley FJ et al. Chronic cough due to gastroesophageal reflux: clinical, diagnostic, and pathogenetic aspects. Chest 1993; 104 : 1511-1517.
25. Isolauri J, Luostarinen M, Isolauri E et al. Natural Course of Gastroesophageal Reflux Disease: 17-22 Year Follow-Up of 60 Patients. Amer J Gastroenterol 1997; 92 : 37-41.
26. Jirásek V, Procházka V, Dostalík Z et al. Helicid (omeprazol, Léčiva, a.s.) v léčbě refluxní ezofagitidy. Čes Slov Gastroenet 2000; 54 : 43-46.
27. Johnston N, Bulmer D, Gill GA et al. Cell Biology of laryngeal epithelial defenses in health and disease: further studies. Ann Otol Rhinol Laryngol 2003; 112 : 481-491.
28. Kahrilas PJ. Gastroesophageal reflux disease. JAMA 1996; 276 : 983-998.
29. Kastelik JA, Thompson RH, Aziz I et al. Sex-related Differences in Cough Reflex Sensitivity in Patients with Chronic Cough . Am J Respiratory and Critical Care Medicine 2002; 16 : 961-964.
30. Kiljander TO, Salomaa ERM, Hietanen EK et al. Gastroesophageal reflux and Bronchial Responsivness: Correlation and the Effect of Fundoplication. Respiration 2002; 69 : 434-439.
31. Kolek V. Formy kašle. In: Kolek V. Chronický kašel - příčiny, diagnostika, léčba. Praha: Vltavín 2000 : 7-8.
32. Koufman JA, Aviv JE, Casiano RR et al. Laryngopharyngeal reflux: Position statement of the Comittee on Speech, Voice, and Swallowing Disorders of the American Academy of Otolaryngology-Head and Neck Surgery. Otolaryngol Head Neck Surg 2002; 127 : 32-35.
33. Locke GR III. What is the prevalence of gastroesophageal reflux disease in a population-based study? In: Giuli R, Galmiche JP, Jamieson Glynn G et al (Eds.). O.E.S.O. - The esophagogastric junction. Paris: John Libbey Eurotext 1998 : 493-496.
34. Lukáš K et al. Definice. In: Lukáš K et al. Refluxní choroba jícnu. Karolinum: Praha 2003 : 7-8.
35. Lukáš K et al. Diagnóza. In: Lukáš K et al. Refluxní choroba jícnu. Praha: Karolinum 2003 : 78-111.
36. Lukáš K et al. Klinický obraz. In: Lukáš K et al. Refluxní choroba jícnu. Praha: Karolinum 2003 : 42-56
37. Lukáš K. Současné názory na patofyziologii refluxní choroby jícnu. Čes Slov Gastroent 1995; 49 : 27-29.
38. Mansfield LE, Stein MR. Gastroesophageal reflux and asthma: a possible reflex mechanism. Ann Allergy 1978; 41 : 224-226.
39. Matuška J. Asthma bronchiale a refluxní nemoc jícnu. Alergie 2001; 3 : 234-241.
40. Postma GN. Ambulatory pH monitoring methodology. Ann Otol Rhinol Laryngol 2000; 109 (Suppl 184): 10-14.
41. Postma GN, Belafsky PC, Aviv JE et al. Laryngopharyngeal reflux testing. ENT 2002; 81 : 14-18.
42. Richter JE. Typical and atypical presentation of gastroesophageal reflux disease. Gastroenterol Clin A Am 1996; 25 : 75-102.
43. Shaker R, Dodds WJ, Hogan WJ et al. Mechanisms of esophago-pharyngeal acid regurgitation. Gastroenterology 1991; 100: A494.
44. Smout AJPM, Akkermans LMA. Gastro-oesophageal reflux disease. In: Smout AJPM, Akkermans LMA. Normal and disturbed motility of the gastrointestinal tract. s.. Petersfield (UK): Wrightson Biomedical Publishing 1992 : 67-86
45. Smyrnios NA, Irwin RS, Curley FJ. Chronic cough with history of excessive sputum production: the spectrum and frequency of causes, key components of the diagnostic evaluation, and outcome of specific therapy. Chest 1995; 108 : 991-997.
46. Sontag SJ. What are the potential mechanisms for esophageal acid-induced bronchoconstrition? In: Giuli R, Galmiche JP, Jamieson Glynn G et al (Eds). O.E.S.O. - The esophagogastric junction. Paris: John Libbey Eurotext 1998 : 592-598.
47. Stendal C. Reflux disorders. Pulmonary manifestations of gastroesophageal reflux. In: Stendal C. Pratical guide to gastrointestinal functional testing. Oxford: Blackwell Science Ltd 1998. 64-68.
48. Theodoropoulos DS, Lockey RF, Boyce HW Jr et al. Gastroesophageal reflux and asthma: a review of pathogenesis, diagnosis, and therapy. Allergy 1999; 54 : 651-661.
49. Toohill RJ, Kuhn JC. Role of refluxed acid in pathogenesis of laryngeal disorders. Am J Med 1997; 103 : 100S-106S.
50. Ulualp SO, Toohill RJ. Laryngopharyngeal reflux: state of the art diagnosis and treatment. Otolaryngol Clin North Am 2000; 33 : 785-801.
51. Vadenplas Y, Goyvaerts H, Helven R et al. Gastroesophageal reflux, as measured by 24 hour pH monitoring, in 509 healthy infants screened for risk of sudden infant death syndrome. Pediatrics 1991; 88 : 834-840.
52. Vaezi MF. Gastroesophageal Reflux Disease and the Larynx. J Clin Gastroenterol 2003; 36 : 198-203.
53. Williams RBH, Ali GN, Wallace KL et al. Esophagopharyngeal Acid regurgitation: Dual pH Monitoring Criteria for Its Detection and Insights Into Mechanisms. Gastroenterology 1999; 117 : 1051-1061.
54. Wo JM, Hunter JG, Waring JP. Dual-channel ambulatory pH monitoring - a useful diagnostic tool? Dig Dis Sci 1997; 42 : 2222-2226.
55. Wong RHK, Hanson DG, Waring PJ et al. ENT Manifestations of Gastroesophageal Reflux. Am J Gastroent 2000; 95: S15-S22.
56. Zerbib F, Guisset O, Lamouliatte H et al. Effects of Bronchial Obstruction on Lower Esophageal Sphincter Motility and Gastroesophageal Reflux in Patients with Asthma. Am J Respir Crit Care Med 2002; 166 : 1206-1211.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2005 Issue 12-
All articles in this issue
- The relation of GERD, bronchial asthma and symptomatology from ear, nose and throught regions
- The influence of long-term growth hormone replacement therapy on body composition, bone tissue and some metabolic parameters in adults with growth hormone deficiency
- Influence of recombinant human procalcitonin on phagocytic and candidacidal ability of polymorphonuclear leukocytes and on killing mechanisms of serum and blood against bacteria Staphylococcus aureus and Escherichia coli
- Possibilities of ultrasonographic differentiation of neck and axillary lymphadenopathy
- Idiopathic pulmonary fibrosis
- The idiopathic hypereosinophilic syndrome and chronic eosinophilic leukemia
- Prevention of cardiovascular events by the antihypertensive treatment using amlodipine and perindopril in comparison with the use of atenolol and bendroflumethiazide. The ASCOT (Anglo-Scandinavian Outcomes Trial: blood pressure lowe ring arm) study results – multicentre, randomised, controlled trial. Landmark in the development of opinions on combination therapy in hypertension? (comment)
- Atypical localisation of pyoderma gangraenosum in patient with ulcerative colitis
- Diagnostics and treatment of hepatocellular carcinoma
- Food intolerance – a cause or a consequence of digestive disorders?
-
Dopis redakci
Přínos pioglitazonu u pacientů s diabetes mellitus 2. typu a kardiovaskulárními komplikacemi - Evaluation of labeling and content of probiotics available in the Czech Republic
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- The idiopathic hypereosinophilic syndrome and chronic eosinophilic leukemia
- Possibilities of ultrasonographic differentiation of neck and axillary lymphadenopathy
- The relation of GERD, bronchial asthma and symptomatology from ear, nose and throught regions
- Idiopathic pulmonary fibrosis
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

